Изобретение относится к способам очистки сточных вод от цинка и может быть использовано в металлургической, химической и горно-рудной промышленности.
Известен способ очистки сточных вод от ионов цинка, состоящий в том, что сточные воды, содержащие цинк, смешивают со сточными водами, содержащими ионы никеля, и при pH 8-8,5 обрабатывают смесь полиоксихлоридом алюминия со степенью основности 2,5-2,67 [1]
Недостатком данного способа является то, что процесс осаждения цинка осуществляют в щелочной среде, и то, что цинксодержащие сточные воды необходимо смешивать с никельсодержащими сточными водами. Оксихлорид алюминия Aln(OH)3n-1Cl весьма дорогой реагент (16000 руб. за 1 кг).
Наиболее близким к предлагаемому изобретению относится способ очистки сточных вод от ионов цинка [2]
По указанному способу сточные воды, содержащие цинк (743 мг/дм3), серную кислоту (1020 мг/дм3), обрабатывают раствором аммофоса до достижения соотношения Zn2+:PO
Недостатками данного процесса являются:
1. Карбонат натрия (сода) как нейтрализатор дорогой реагент. Он дороже многих простых нейтрализаторов.
2. Большая длительность процесса осаждения цинка аммофосом (3,5-5,5 ч). В опыте N 5 время осаждения составляет 19 ч.
3. Аммофос хорошо растворяется в воде и, взятый в избытке (1:2,4-3,6), загрязняет сточные воды.
4. Карбонат натрия при нейтрализации серной кислоты образует сульфат натрия (Na2SO4), который остается в сточной воде и загрязняет ее.
Задачей данного изобретения является снижение стоимости, продолжительности и исключение загрязнения сточных вод осаждающими цинк реагентами.
Поставленная задача достигается тем, что для очистки сточных вод от цинка используется малорастворимое вещество гидроксид железа (II) Fe(OH)2. Для этого вначале проводится предварительная нейтрализация исходной серной кислоты до pH 3,6-4,8, а затем в точную воду вводится Fe(OH)2 в виде водной пульпы.
Очистка сточной воды от цинка протекает по реакции:
ZnSO4+Fe(OH)2 Zn(OH)2+FeSO4.
Гидроксид цинка Zn(OH)2 нерастворим в воде и при очистке увлекается избытком Fe(OH)2 в осадок.
Сульфат железа FeSO4, полученный по реакции (1), в нейтральной среде при аэрации (продувке воздухом) окисляется до Fe2(SO4)3 и переходит в осадок:
Fe2(SO4)3+6H2O=2Fe(OH)3+ 3H2SO4.
Выделяющуюся серную кислоту, как и исходную, нейтрализуем известняком CaCO3 или карбонатом бария BaCO3.
Нейтрализация кислоты осуществляется по реакции:
H2SO4+CaCO3=CaSO4+H2O+CO2.
Полученный CaSO4 практически нерастворим в воде. Аналогично при нейтрализации H2SO4 с помощью BaCO3 полученный BaSO4 также нерастворим в воде, вследствие этого сточная вода не загрязняется нейтрализатором.
Для осуществления очистки сточной воды от цинка необходимо поддерживать отношение Zn2+:Fe(OH)3=1:(3-3,6). После очистки от цинка пульпа, содержащая остаток Fe(OH)2 и осажденный Zn(OH)2, направляется на сгущение или фильтрацию для отделения указанных гидроксидов.
Во всех примерах, приведенных ниже, для очистки от цинка в сточную воду вводили водную пульпу Fe(OH)2 при pH 3,5-4,8. При данном значении pH получаются более плотные осадки.
Повышение pH до 6,2-6,6 позволяет свести до минимума содержание гидролизной серной кислоты.
Поскольку стоимость Fe(OH)2 и CaCO (или BaCO3) меньше суммарной стоимости аммофоса и соды, то затраты на очистку по предложенному способу ниже, чем по прототипу.
Пример 1.
Сточную воду (0,25 дм3), содержащую 11 мг/дм3 цинка, 530 мг/дм3 H2SO4 (pH 2), залили в химический стакан (0,5 дм3) и при перемешивании начали нейтрализацию до pH 4 при 25oC. Всего на нейтрализацию загрузили 0,25 г CaCO3 (мел). Для осаждения цинка загрузили в сточную воду 10 мг Fe(OH)2. Через 10 мин отделили осадок Zn(OH)2 с остатком Fe(OH)2, а раствор подвергли аэрации. Выпавший желтый осадок Fe(OH)3 отфильтровали, а раствор направили на химический анализ. Анализ показал, что содержание цинка в очищенной воде снизилось до 0,10 кг/дм3. Следовательно, степень очистки сточной воды составляет 99,10% Величина pH очищенной воды 6,2.
Пример 2.
Сточную воду с содержанием 200 мг/дм3 цинка и 5 мг/дм3 серной кислоты (pH 4) подвергли очистке от цинка при 35oC путем загрузки 150 мг/дм3 гидроксида Fe(OH)2. Полученную пульпу перемешивали в течение 10 мин. После этого отделили осадок Zn(OH)2 с остатками Fe(OH)2.
Последующим химическим анализом определено, что содержание цинка в очищенной сточной воде равняется 0,10 мг/дм3. Для удаления железа, перешедшего в сточную воду при очистке провели аэрацию (с нейтрализацией). На нейтрализацию гидролизной серной кислоты загрузили 0,20 г CaCO3. Степень очистки от цинка равна 99,9% Значение pH очищенной сточной воды повысилось до 6,3.
Пример 3.
В данном примере на очистку направили сточную воду, содержащую 2700 мг/дм3 Zn, 65 мг/дм3 серной кислоты (pH=3,5). Нейтрализацию этой сточной воды не проводили, а сразу при температуре 35oC начали осаждать цинк с помощью Fe(OH)2, количество которого составляло на 0,25 дм3 2,40 г. По окончании перемешивания (через 15 мин) сточной воды с Fe(OH)2 отделили осадок (Zn(OH)2 c Fe(OH)2), а фильтрат направили на анализ и на аэрацию для осаждения железа (и одновременную с ней нейтрализацию гидролизной серной кислоты). На нейтрализацию кислоты затратили 2,6 г CaCO3. Содержание цинка в очищенной воде снизилось до 0,15 мг/дм3, а железа до 0,9 мг/л. Степень очистки от цинка достигла 99,9% Величина pH очищенной воды 6,5.
Пример 4.
Сточную воду с повышенным содержанием серной кислоты (8,0 г/дм3 H2SO4) и цинка (5,9 г/дм3 Zn) подвергли нейтрализации известняком (мелом) до pH 4,8 и при перемешивании загрузили в сточную воду 5,31 г Fe(OH)2 в виде водной пульпы. Температура воды 40oC. Через 20 мин отделили цинк-железистый осадок от сточной воды путем фильтрации. Небольшую часть фильтрата (5 мл) использовали для анализа, а большую часть (245 мл) направили на аэрацию и одновременную с ней нейтрализацию гидролизной кислоты известняком. Всего на нейтрализацию исходной и гидролизной серной кислоты израсходовано 5,5 г CaCO3. Значение pH очищенной воды 6,2.
Содержание цинка в очищенной сточной воде составило 0,19 мг/дм. Содержание железа 0,8 мг/дм3. Степень извлечения цинка в цинкжелезистый осадок достигла 99,9%
Пример 5.
Цинкжелезистая сточная вода, содержащая 8,3 г/дм3 Zn, 3,1 г/дм3 железа (II) (pH=3,8) была подвергнута очистке от цинка гидроксидом железа.
При температуре 45oC в сточную воду (0,25 л) загрузили 7,2 г Fe(OH2) в виде пульпы. Через 20 мин осадок (Zn(OH)2 и Fe(OH)2) отделили фильтрацией; фильтрат направили на очистку от железа (аэрирование с нейтрализацией гидролизной кислоты). Часть фильтрата была использована для анализа на цинк. Содержание цинка в фильтрате не превышало 0,83 мг/дм3, а железа после аэрации с нейтрализацией равнялось 1,1 мг/дм3. Степень извлечения цинка из сточной воды составила 99,9% и 99,8% железа. Значение pH очищенной воды достигло 6,4. На нейтрализацию гидролизной кислоты затратили 5,5 г CaCO3.
Пример 6.
Раствор, полученный при выщелачивании твердых отходов цветной металлургии, содержащий 6,8 г/дм3 цинка и 15 г/дм3 H2SO4, направили на нейтрализацию исходной серной кислоты, для чего в раствор полунепрерывно загружали карбонат бария. За 10 мин загрузили 4,4 г BaCO3. Величина pH после нейтрализации равнялась 4,8. Температура сточной воды 45oC.
В нейтрализованный раствор ввели 5,9 г (Fe(OH)2. Через 10 мин мешалку отключали и отфильтровали цинк-железистый осадок. Фильтрат использовали для очистки от железа. Для нейтрализации гидролизной серной кислоты применили карбонат бария (5,2 г). Химический анализ показал, что содержание цинка в фильтрате равно 0,15 мг/дм3. Извлечение цинка достигло 99,98% Величина pH очищенной воды 6,2.
Пример 7.
В нейтральный раствор, содержащий 18 мг/дм3 цинка и 26 мг/дм3 H2SO4 (pH= 4,5), загрузили в стакан и начали осаждать цинк гидрооксидом железа (20 мг) путем перемешивания Fe(OH)2 со сточной водой. Через 10 мин отключили мешалку, отделили цинк-железистый осадок фильтрацией. Небольшую часть фильтрата использовали для химического анализа на цинк, а основную массу направили на очистку от железа аэрацией при одновременной подаче карбоната бария. Очищенный раствор содержал 0,08 мг/дм3 цинка и 0,35 мг/дм3 железа. Извлечение цинка составило 99,8% Величина pH воды 6,2.
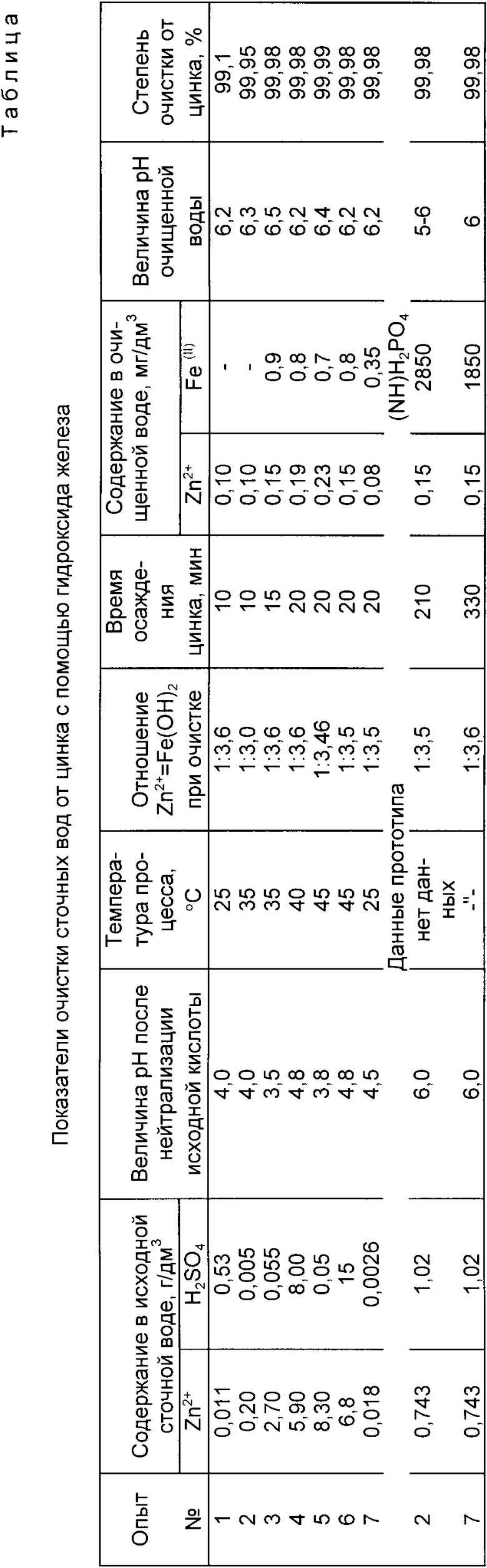
Таким образом, приведенные примеры показывают возможность полного удаления цинка из сточной воды до норма ПДК (1 мг/дм3). Основные показатели очистки приведены в таблице.
Из приведенных данных видно, что предложенной технологии извлечение цинка достигает 99,98% при остаточном содержании 0,10-0,23 мг/дм3, т.е. не выше, чем по способу-прототипу.
Продолжительность очистки от цинка колеблется в пределах 10-20 мин. Это значительно лучшие показатели, чем по прототипу (210-330 мин).
Количество осадителя (железа) в сточной воде находится в пределах 0,35-0,9 мг/дм3, а по прототипу содержание аммофоса достигает 1850-2850 мг/дм3. Это без учета сульфата натрия, который образуется при нейтрализации серной кислоты. Следовательно, сточные воды по предложенному способу получаются намного чище, чем по прототипу.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ очистки растворов от железа | 1990 |
|
SU1740464A1 |
| Способ очистки цинковых растворов от железа ( @ ) | 1987 |
|
SU1514814A1 |
| СПОСОБ ОЧИСТКИ СУЛЬФАТНЫХ РАСТВОРОВ, СОДЕРЖАЩИХ ТЯЖЕЛЫЕ ЦВЕТНЫЕ МЕТАЛЛЫ, ОТ ЖЕЛЕЗА | 1993 |
|
RU2068007C1 |
| Способ очистки сульфатных цинковых растворов от железа | 1983 |
|
SU1118705A1 |
| СПОСОБ НЕЙТРАЛИЗАЦИИ И ОЧИСТКИ СТОЧНЫХ ВОД | 2024 |
|
RU2838819C1 |
| СПОСОБ ПОВЫШЕНИЯ ИЗВЛЕЧЕНИЯ ЦЕННЫХ КОМПОНЕНТОВ ИЗ СУЛЬФИДНОГО СЫРЬЯ ЭЛЕКТРОИМПУЛЬСНОЙ ОБРАБОТКОЙ | 2014 |
|
RU2559599C1 |
| СПОСОБ ОЧИСТКИ МНОГОКОМПОНЕНТНЫХ ПРОМЫШЛЕННЫХ СТОЧНЫХ ВОД, СОДЕРЖАЩИХ ЦИНК И ХРОМ | 2022 |
|
RU2792510C1 |
| СПОСОБ ГЛУБОКОЙ ОЧИСТКИ СТОЧНЫХ ВОД ОТ ХРОМА /Ш/ | 1991 |
|
RU2068396C1 |
| Способ очистки кислых сточных вод от мышьяка и цветных металлов | 1990 |
|
SU1717548A1 |
| ОЧИСТКА РАСТВОРОВ, СОДЕРЖАЩИХ МЕТАЛЛ | 1996 |
|
RU2153026C2 |
Использование: очистка сточных вод от цинка. Сущность изобретения: сточные воды подвергают нейтрализации до pH 3,5 - 4,8 и осаждению гидроксидом железа (II). В качестве нейтрализаторов используют карбонаты кальция или бария. 1 з.п.ф-лы, 1 табл.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Способ очистки сточных вод от ионов никеля и цинка | 1983 |
|
SU1219529A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Способ очистки сточных вод от ионов цинка | 1985 |
|
SU1330079A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
1998-02-27—Публикация
1994-05-10—Подача