Изобретение относится к биотехнологии получения гибридом-продуцентов моноклональных антител (МКА) заданной специфичности. Штамм-продуцент моноклональных антител к антигену 200 kDa назван Bpm Vd-9 (5C2/F10/C9). Штамм депонирован в Государственную коллекцию патогенных микроорганизмов и клеточных культур «ГКПМ-ОБОЛЕНСК» под номером Н-31.
Изобретение может быть использовано в научно-исследовательской работе, а также при создании наборов реагентов для иммуноферментного выявления антигена 200 kDa Burkholderia pseudomallei. Согласно принятой в нашей стране классификации, возбудитель мелиоидоза является микроорганизмом II группы патогенности для человека [6]. Все этапы работы с живыми культурами этого микроорганизма выполняют в специализированных боксах согласно «СП 1.3.1285-03 ″Безопасность работы с микроорганизмами I-II групп патогенности (опасности)» [7].
С 2007 года мелиоидоз внесен в перечень международных медико-санитарных правил (ММСП) в качестве инфекции, требующей постоянного надзора в связи с расширением зон эндемичного распространения возбудителя данной инфекции, отсутствием зарегистрированных средств диагностики и специфической профилактики, а также эффективных схем лечения этого заболевания.
Принципы организации исследований материала, подозрительного на зараженность возбудителем мелиоидоза и его антигенами, схемы индикации и идентификации В. pseudomallei изложены в ряде документов [3, 4]. Согласно этим руководствам одним из способов обнаружения возбудителя мелиоидоза и его антигенов на этапе экспресс-анализа является ТИФМ.
В настоящее время экспериментально доказаны преимущества использования моноклональных антител (МКА) для изготовления компонентов иммуноферментных тест-систем [3, 8]. Переход на моноклональное сырье позволяет повысить чувствительность и специфичность тест-систем за счет наличия постоянного источника гомогенных по составу и свойствам антител, являющихся сырьем для их изготовления.
По данным литературы, зарубежными исследователями получены и апробированы в различных целях экспериментальные образцы моноклональных иммуноглобулинов к антигену 200 kDa возбудителя мелиоидоза [12, 13].
Цель изобретения - получение штамма гибридомы-продуцента высокоспецифичных МКА, пригодных к применению в качестве детектирующих антител, меченных пероксидазой хрена, в составе тест-системы иммуноферментной для обнаружения гликопротеина 200 kDa В. pseudomallei в различных пробах.
Получение гибридомы достигается гибридизацией двух типов клеток: спленоцитов инбредной мыши линии BALB/c, иммунизированной антигеном 200 kDa возбудителя мелиоидоза, и клеток мышиной миеломы.
Гибридома-продуцент МКА 5C2/F10/C9 получена слиянием спленоцитов иммунной мыши линии BALB/c с клетками мышиной миеломы Р3-X63.Ag8.653 в присутствии конъюгирующего агента - полиэтиленгликоля (ПЭГ-4000), последующего рассева взвеси клеток в лунки 96-луночных культуральных пластин, выращивания в селективных средах в течение трех недель с постепенным переходом на полную среду культивирования гибридных клеток, отбора первичного клона по показателю продукции специфических антител, узнающих антиген 200 kDa возбудителя мелиоидоза, его клонирования и реклонирования методом лимитирующих разведении. Штамм назван Bpm Vd-9 (5C2/F10/C9), депонирован в Государственную коллекцию патогенных микроорганизмов и клеточных культур «ГКПМ-ОБОЛЕНСК» под номером Н-31, характеризуется следующими признаками.
Культуральные признаки. Клетки культивируют in vitro при 37°C в атмосфере 5-7% CO2 и влажности 70-80%. Для культивирования гибридомы используют среду RPMI-1640 с 15% эмбриональной телячьей сыворотки (ЭТС), 2 mM L-глютамина, 10 mM Hepes, 4 mM пирувата натрия. Характер роста культуры полусуспензионный. Пересевы делают каждые 3-4 сут, интенсивность роста популяции клеток контролируют ежедневно при просмотре лунок пластин в инвертированном микроскопе. Кратность рассева 1:4-1:8.
Культивирование в организме сингенного животного. Для накопления асцита in vivo клетки гибридомы вводят внутрибрюшинно предварительно праймированным мышам линии BALB/c, по 2·106 - 4·106 клеток на мышь. Прививаемость гибридных клеток в брюшной полости достигает 88%. Асцит образуется через 2-4 недели.
Продуктивность штамма. Продукция МКА в среде культивирования составляет 0,61 мкг/мл, в асцитической жидкости - 26-27 мг/мл. Объемы асцитической жидкости в среднем равны 3-4 мл.
Характеристика получаемого продукта. Антитела относятся к классу IgM. Они специфически взаимодействуют с антигеном 200 kDa возбудителя мелиоидоза. Специфичность взаимодействия определяют с помощью твердофазного иммуноферментного метода (ТИФМ).
Криоконсервирование. Вне периода экспериментов по накоплению препаративных количеств МКА 5C2/F10/C9 клетки гибридомы сохраняют в криоконсервированном состоянии. Для перевода их в такое состояние взвесь клеток гибридомы в количестве 4·106 клеток в 1 мл защитной среды, состоящей из среды RPMI-1640 с 20% ЭТС и 7% диметилсульфоксида, переносят в пластиковые ампулы. Ампулы помещают в аппарат для криоконсервирования биологического материала. Используют режим постепенного программируемого понижения температуры: в течение 20 минут - снижение температуры образца до 0°C, далее со скоростью 1°C в минуту до температуры минус 40°C и со скоростью 5°C в минуту от минус 40°C до минус 70°C. Затем ампулы погружают в биохранилище с жидким азотом и хранят до момента использования. Размораживание производят при 37°C на водяной бане в течение 2-3 минут. Жизнеспособность клеток после размораживания составляет 80% и более.
Пример 1. Получение антигена.
Источником выделения гликопротеина возбудителя мелиоидоза являются обеззараженные ацетоном и высушенные клетки штамма В. pseudomallei 100.
Экстракцию гликопротеина из клеток В. pseudomallei 100 осуществляют формамидом по методу Фуллера в модификации Пивня Н.Н., заключающейся в изменении температурного режима экстрагирования биополимера: этап необходимо проводить при более мягких температурных условиях (экстракция при 20°C, вместо 150°C, рекомендованных Фуллером) [5]. В антигенном препарате определяют содержание белка (спектрофотометрически), полисахаридов [14].
Пример 2. Получение штамма гибридомы-продуцента. Все манипуляции выполняют в ламинарном потоковом шкафу I класса защиты с горизонтальным потоком воздуха (тип ″защита продукта″).
Клетками-партнерами при соматической гибридизации клеточных линий с целью получения гибридом-продуцентов МКА являются В-лимфоциты мыши линии BALB/c, иммунизированной антигеном 200 kDa, и клетки мышиной миеломы P3-X63.Ag8.653.
1. Подготовка спленоцитов. Иммунизацию В-лимфоцитов мыши-донора, стимулированных антигеном 200 kDa В. pseudomallei, выполняют по схеме дробного введения минимальных доз антигена (суммарно не более 100-105 мкг) в течение относительно короткого промежутка времени (1,5 месяца), описанной в Патенте на изобретение №2371196 от 27.10.2009.
2. Подготовка миеломных клеток. В качестве злокачественного партнера в опытах по гибридизации клеточных линий используют клетки одной из наиболее распространенных мышиных миеломных линий Р3-Х63-Ag 8.653.
Клетки миеломы начинают готовить за 4 недели до опыта по гибридизации, соблюдая общепринятые требования: культивирование в среде с 8-азагуанином в течение 2 недель и последующих 2 недель в основной среде культивирования с 10% эмбриональной телячьей сыворотки. Смену сред и рассев клеток осуществляют каждые 3-4 сут. К моменту начала опыта клетки должны достичь экспоненциальной фазы роста.
3. Гибридизация спленоцитов и клеток мышиной миеломы. Процедуру соматической гибридизации спленоцитов и клеток миеломы выполняют в присутствии конъюгирующего агента - полиэтиленгликоля (ПЭГ) с м.м 1500-4000.
Взвесь иммунных спленоцитов (1·108 клеток) и миеломных клеток (1·107) вносят в стеклянный круглодонный стакан диаметром 3-5 см. Смесь клеток центрифугируют при 800-1000 об/мин в течение 10 мин. Надосадочную среду декантируют. Осадок осторожно размешивают запаянным концом пастеровской пипетки.
К осадку клеток очень медленно, в течение 2 мин, добавляют 1 мл 50% раствора ПЭГ, постоянно вращая при этом центрифужный стакан. Затем каждые последующие 2 мин, не прекращая вращения, вносят 1, 2, 4 и 8 мл бессывороточной среды. После завершения данной манипуляции клеточную суспензию центрифугируют, надосадочную жидкость декантируют, осадок клеток ресуспендируют в 20 мл селективной НАТ-среды с 15% эмбриональной телячьей сыворотки. По 2 капли суспензии разносят по лункам двух 96-луночных пластин с предварительно подготовленным слоем фидерных клеток.
Все этапы последующего культивирования гибридных клеток, отбора растущих клонов, секретирующих специфические иммуноглобулины, клонирования, тиражирования культур и накопления МКА in vivo выполняют согласно традиционного протокола [12].
Пример 3. Накопление МКА в препаративных количествах in vivo.
Тиражирование клеток гибридомы in vivo осуществляют в брюшной полости сингенного животного. Животным предварительно внутрибрюшинно вводят по 0,4 мл стерильного минерального масла, пристана - 2,6,10,14-тетраметил-пентадекана. Через 5-7 суток мышам внутрибрюшинно вводят по 2·106 - 4·106 клеток гибридомы. После накопления асцитической жидкости ее собирают, клетки осаждают центрифугированием, надосадочную жидкость отделяют и используют для выделения антител методом сульфатного трехкратного переосаждения белка при 50% насыщении сульфата аммония. Концентрацию белка в растворе МКА определяют спектрофотометрически при длине волны 280 нм. Полученный раствор моноклональных иммуноглобулинов стерилизуют методом мембранной фильтрации, ампулируют и хранят при минус 20°C до момента использования.
Специфическую активность МКА определяют с помощью ТИФМ. Постановка реакции проводится по общепринятой методике [1].
МКА 5C2/F10/C9, выделяемые из асцитической жидкости, активны в разведениях 1:105 - 3:105.
Средний объем асцитической жидкости, получаемый от одной мыши при культивировании гибридомы Bpm Vd-9 (5C2/F10/C9) in vivo, - 3-4 мл, концентрация МКА - 26-27 мг/мл.
Пример 4. Получение экспериментальных образцов МКА, меченных пероксидазой хрена (ПХ).
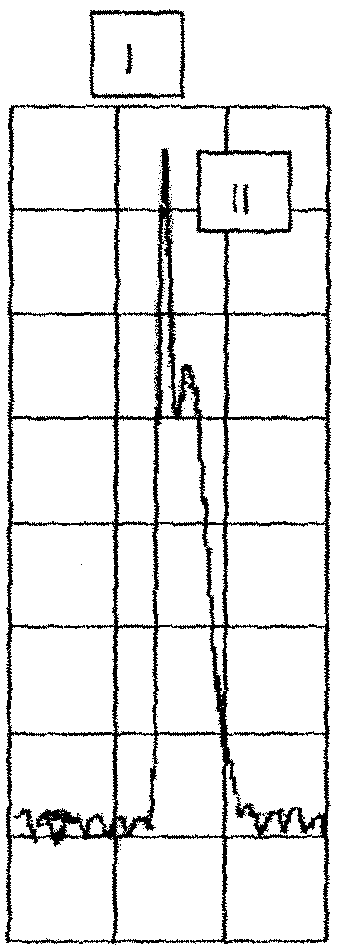
Метку МКА ферментом проводят по методу Nakane [13], используя ПХ с RZ не менее 3,0. Очистку ИПК от несвязавшихся компонентов выполняют с помощью метода гель-хроматографии на колонке с сефадексом G-100 0,1М фосфатным буфером, pH 7,5. Фракции со спектрофотометрическими показателями ОП403/ОП280, равными 0,4-0,6, объединяют. Объединенный образец смешивают с глицерином 1:1 по объему и хранят при минус 8-10°C. Рабочее разведение ИПК определяют методом шахматного титрования в двухкомпонентной реакции: гомологичный AT+МКА, меченные ферментом. График очистки конъюгата представлен на чертеже.
Фракции I пика используют для приготовления иммунопероксидазного конъюгата. После объединения фракций первого пика определяют рабочее разведение готового ИПК по методике шахматного титрования в ТИФМ. Параметры качества трех различных ИПК, полученных на основе индивидуальных образцов МКА, представлены в таблице 1.
Пример 5. Подбор компонентов для экспериментальной тест-системы.
Экспериментальная тест-система представляет собой сэндвич-вариант ТИФМ в следующей схеме: АТ(1)+АГ+ИПК.
В качестве антител первого порядка АТ(1), сорбируемых на твердой фазе, наиболее эффективной является смесь МКА 3C6+5C2+2A6, выполняющая функцию «захвата» антигена 200 kDa возбудителя мелиоидоза. Индексы аддитивности пар МКА 3C6 и 5C2, 3C6 и 2A6, 5C2 и 2A6 имеют значения 100%, 72% и 100% соответственно [11]. Константы аффинности МКА 3C6, 5C2, 2A6 составляют 9-10, 2-10, 8-10 М-1 соответственно [10]. Белковая нагрузка смеси МКА на пластины составляет 20 мкг/мл.
Второй компонент тест-системы - АГ - это стандартный образец антигена 200 kDa. Он содержит 1,68 мг/мл (по спектрофотометру) и 37,5 мг/мл ПС [14].
ИПК 5C2/F10/C9, используемый для детекции иммуноферментной реакции, был отобран после оценки специфической активности ИПК, приготовленных на основе индивидуальных образцов МКА.
Сравнительный анализ чувствительности тест-системы при выявлении контрольного антигена в зависимости от выбора ИПК представлен в таблице 2. Наиболее активным ИПК является конъюгат на основе 5C2/F10/C9.
Краткое описание чертежа.
На чертеже представлен график очистки конъюгата. Фракции I пика - квоты иммуноглобулинов, конъюгированные с ПХ, контролируемые по показателю RZ=ОП403/ОП280, II пик - свободная ПХ.
Представленные выше свойства гибридомы-продуцента МКА 5C2/F10/C9 позволили сделать заключение о том, что штамм культивируемых гибридных клеток животного Mus musculus (авторское название клеточной линии Bpm Vd-9) предназначен для получения моноклонального антитела 5C2/F10/C9, используемого в качестве детектирующих антител, меченных пероксидазой хрена, в составе тест-системы иммуноферментной для обнаружения гликопротеина 200 kDa В. pseudomallei в различных пробах.
Источники информации
1. Антитела. Методы. Пер. с англ./Под ред. Д. Кэтти. - М.: Мир, 1991. - 384 с.
2. Лабораторная диагностика мелиоидоза (МУ 4.2.2787-10.4.2) / Демина Ю.В., Пакскина Н.Д., Илюхин В.И., Алексеев В.В., Храпова Н.П. и др. // Изданы ФЦГиЭ. - 2011.
3. Лабораторная диагностика опасных инфекционных болезней: Практическое руководство / Под редакцией академика РАМН Г.Г. Онищенко, академика РАМН В.В. Кутырева. Изд. 2-е, переработанное и дополненное. - М.: ЗАО «Шико», 2013. - 560 с.
4. Пивень Н.Н., Смирнова В.И. Выделение, очистка и химический состав поверхностного полисахаридного антигенного комплекса возбудителя мелиоидоза// Особо опасные инфекционные заболевания: диагностика, профилактика и биологические свойства возбудителей. Вып.4 / Волгоградский научно-исследовательский противочумный институт, 1990. - С.111-117.
5. Санитарные правила «Санитарная охрана территорий государств - участников Содружества Независимых Государств» (утверждены Решением Совета по сотрудничеству в области здравоохранения СНГ от 3 июня 2005 г.).
6. Санитарные правила 1.3.1285-03 ″Безопасность работы с микроорганизмами 1-11 групп патогенности (опасности)″ (утверждены Главным государственным санитарным врачом РФ 12 марта 2003 г.).
7. Храпова Н.П., Пивень Н.Н., Корсакова И.И. и др. Перспективы создания диагностических средств индикации и идентификации вирулентных штаммов возбудителя мелиоидоза// Матер, науч.-практич. конф. «Соврем. аспекты эпидемиологического надзора за особо опасными инфекционными заболеваниями на юге России» (21-22.03.07). - Ставрополь, 2007. - 4.2. - С.155-156.
8. Beatty J.D., Beatty B.C., Vlahos W.G. Measurement of monoclonal antibody affinity by non-competitive enzyme immunoassay // J. Immunol. Methods. - 1987. - V.100. - P.173-179.
9. Friguet В., Djavadi-Ohaniance L., Pages J. et al. A convenient enzyme-linked immunosorbent assay for testing whether monoclonal antibodies recognize the same antigenic site. Application to hybridomas specific for the 2 subunit of Esche-richia coli tryptophan synthase // J. Immunol. Methods. - 1983. - V.60. - P.351-358.
10. Goding J.W. Monoclonal Antibodies: Principles and Practice // Academic Press Inc.: London, 315 p.
11. Nakane P.K., Kawaoi A. Peroxidase-labeled antibody. A new method of conjugation//J. Histochem. Cytochem. - 1974. - V.22, №12. - P.1084 - 1091.
12. Shields R., Bumett W. Determination of protein bound carbohydrate in serum by modified anthrone method // Analyt. Chem.- 1960. - V.32. P.885-886.
13. Recent developments in laboratory diagnosis of melioidosis / Sirisinha S., Anuntagool N., Dharakul T. et al. // Acta Tropica. - 2000. - №74. - P.235-245.
14. Relationship between antigenicity and pathogenicity for Burkholderia pseudo-mallei and Burkholderia mallei revealed by a large panel of mouse MAbs / Zou N., Tsai S., Feng S.H. et al. // Hybridoma (Larchmt). - 2008. - №27 (4). - P.231-240.
| название | год | авторы | номер документа |
|---|---|---|---|
| ШТАММ КУЛЬТИВИРУЕМЫХ ГИБРИДНЫХ КЛЕТОК ЖИВОТНОГО MUS musculus Вpm Vd-8 - ПРОДУЦЕНТ МОНОКЛОНАЛЬНОГО АНТИТЕЛА 3C/A К АНТИГЕНУ 200 kDa ВОЗБУДИТЕЛЯ МЕЛИОИДОЗА | 2014 |
|
RU2555544C1 |
| ШТАММ КУЛЬТИВИРУЕМЫХ ГИБРИДНЫХ КЛЕТОК ЖИВОТНОГО MUS MUSCULUS L. BPM VD-11 - ПРОДУЦЕНТ МОНОКЛОНАЛЬНОГО АНТИТЕЛА 6A/G К АНТИГЕНУ 200 kDA ВОЗБУДИТЕЛЯ МЕЛИОИДОЗА | 2014 |
|
RU2570634C1 |
| ШТАММ КУЛЬТИВИРУЕМЫХ ГИБРИДНЫХ КЛЕТОК ЖИВОТНОГО MUS MUSCULUS L. BPM VD-10 - ПРОДУЦЕНТ МОНОКЛОНАЛЬНОГО АНТИТЕЛА 5H/E К АНТИГЕНУ 200 KDA ВОЗБУДИТЕЛЯ МЕЛИОИДОЗА | 2014 |
|
RU2570638C1 |
| ШТАММ КУЛЬТИВИРУЕМЫХ ГИБРИДНЫХ КЛЕТОК ЖИВОТНОГО MUS MUSCULUS - ПРОДУЦЕНТ МОНОКЛОНАЛЬНОГО АНТИТЕЛА К ТЕРМОСТАБИЛЬНОМУ КОМПОНЕНТУ КАПСУЛОПОДОБНОЙ СУБСТАНЦИИ ВОЗБУДИТЕЛЯ МЕЛИОИДОЗА | 1997 |
|
RU2117042C1 |
| ШТАММ КУЛЬТИВИРУЕМЫХ ГИБРИДНЫХ КЛЕТОК ЖИВОТНОГО MUS MUSCULUS - ПРОДУЦЕНТ МОНОКЛОНАЛЬНОГО АНТИТЕЛА К ТЕРМОСТАБИЛЬНОМУ АНТИГЕНУ, ОБЩЕМУ ДЛЯ ВОЗБУДИТЕЛЕЙ САПА И МЕЛИОИДОЗА | 1997 |
|
RU2117043C1 |
| ШТАММ КУЛЬТИВИРУЕМЫХ ГИБРИДНЫХ КЛЕТОК ЖИВОТНОГО MUS. MUSCULUS - ПРОДУЦЕНТ МОНОКЛОНАЛЬНОГО АНТИТЕЛА К ТЕРМОСТАБИЛЬНОМУ ПОВЕРХНОСТНОМУ АНТИГЕНУ ВОЗБУДИТЕЛЯ МЕЛИОИДОЗА | 1997 |
|
RU2116344C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПРЕДЕЛЬНО ДОПУСТИМОЙ АНТИГЕННОЙ НАГРУЗКИ, СТИМУЛИРУЮЩЕЙ ПРОДУКЦИЮ ГУМОРАЛЬНЫХ АНТИТЕЛ | 2008 |
|
RU2371196C1 |
| ШТАММ КУЛЬТИВИРУЕМЫХ ГИБРИДНЫХ КЛЕТОК ЖИВОТНОГО MUS MUSCULUS L. CCHFV Vd-2-ПРОДУЦЕНТ МОНОКЛОНАЛЬНОГО АНТИТЕЛА 1E2/E5 К ВИРУСУ КРЫМ-КОНГО ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКИ | 2013 |
|
RU2528868C1 |
| ШТАММ КУЛЬТИВИРУЕМЫХ ГИБРИДНЫХ КЛЕТОК ЖИВОТНОГО MUS MUSCULUS L. CCHFV VD-1-ПРОДУЦЕНТ МОНОКЛОНАЛЬНОГО АНТИТЕЛА 4G/B К ВИРУСУ КРЫМ-КОНГО ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКИ | 2013 |
|
RU2535982C1 |
| ШТАММ КУЛЬТИВИРУЕМЫХ ГИБРИДНЫХ КЛЕТОК ЖИВОТНОГО MUS MUSCULUS L. CCHFV Vd-3-ПРОДУЦЕНТ МОНОКЛОНАЛЬНОГО АНТИТЕЛА 3H6/F2 К ВИРУСУ КРЫМ-КОНГО ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКИ | 2013 |
|
RU2528869C1 |
Изобретение относится к биотехнологии. Предложен штамм культивируемых гибридных клеток животного Mus musculus Bpm Vd-9, депонированный в Государственную коллекцию патогенных микроорганизмов и клеточных культур «ГКПМ-ОБОЛЕНСК» под номером Н-31. Данный штамм является продуцентом моноклонального антитела 5C2/F10/C9 к гликопротеину 200 kDa возбудителя мелиоидоза. Антитело, продуцируемое клетками штамма по настоящему изобретению, может найти применение в качестве антитела второго порядка («детектирующего антитела»), меченного пероксидазой хрена в составе тест-системы для обнаружения гликопротеина 200 kDa В. pseudomallei в исследуемых пробах. 1 ил., 2 табл., 5 пр.
Штамм культивируемых гибридных клеток животного Mus musculus Bpm Vd-9, депонированный в Государственную коллекцию патогенных микроорганизмов и клеточных культур «ГКПМ-ОБОЛЕНСК» под номером Н-31, являющийся продуцентом моноклонального антитела 5C2/F10/C9 к антигену 200 kDa возбудителя мелиоидоза, пригодного к применению в качестве антитела второго порядка («детектирующего антитела»), меченного пероксидазой хрена в составе тест-системы иммуноферментной для обнаружения гликопротеина 200 kDa В.pseudomallei в исследуемых пробах.
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| Штамм гибридных культивируемых клеток животных MUS мUSсULUS L. - продуцент моноклональных антител к антигену РSеUDомоNаS рSеUDомаLLеI, не реагирующих с близкородственным возбудителем сапа | 1990 |
|
SU1740415A1 |
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ БАКТЕРИОСТАТИЧЕСКИХ СВОЙСТВ АНТИТЕЛ К ФАКТОРАМ ВИРУЛЕНТНОСТИ BURKHOLDERIA PSEUDOMALLEI | 2007 |
|
RU2337360C1 |
| FENG S.H | |||
| et al., "Development of mouse hybridomas for production of monoclonal antibodies specific to Burkholderia mallei and Burkholderia pseudomallei." Hybridoma (2006), 25(4), 193-201 | |||
| RUGDECH P | |||
| et al., "Monoclonal antibodies to | |||
Авторы
Даты
2015-07-20—Публикация
2014-04-16—Подача