Изобретение относится к области фторорганической химии, в частности к способу получения 2-метил-5-[ди(трифторметил)оксиметил] фурана, обладающего фунгицидными и вирулицидными свойствами.
Известен способ получения 2-метил-5-[ди(трифторметил)оксиметил] фурана (авт. св. СССР N 1016285, кл. C 07 D 307/42, 1983) взаимодействием 2-метилфурана с гексафторацетоном при 20oC, атмосферном давлении в течение 2 ч в присутствии катализатора КУ-2 с выходом 65%.
Недостатком способа является относительно низкий выход целевого продукта и необходимость регенерации катализатора.
Описан также способ получения 2-метил-5-[ди(трифторметил)оксиметил] фурана (авт. св. СССР N 1051087, кл. C 07 D 307/42, 1983) взаимодействием 2-метилфурана с гексафторацетоном при 30 - 60oC, атмосферном давлении в течение 1,5 ч в присутствии хлорной кислоты в качестве катализатора. Реакционную смесь обрабатывают содой, промывают водой, высушивают и перегоняют. Получают целевой продукт с выходом 80 - 90%.
Недостатком способа является необходимость проведения дополнительных операций по выделению целевого продукта из реакционной смеси, что существенно усложняет процесс. К числу недостатков относится также применение токсичного, сильного окислителя хлорной кислоты.
Известен способ получения 2-метил-5-[ди(трифторметил)оксиметил) фурана (Никишин Г. И. и др. Синтез фторсодержащих фурановых спиртов, Изв. Ан СССР, сер. "Химия", 1981, N 2, 479) взаимодействием 2-метилфурана с гексафторацетоном при 20oC, атмосферном давлении в течение 8 ч с выходом 40%.
Недостатком способа является низкий выход целевого продукта и длительность процесса.
Наиболее близким к заявленному техническому решению является способ получения метил-5-[ди(трифторметил)оксиметил] фурана (патент SU N 1833382 A8, кл. C 07 D 307/42, 1993) взаимодействием 2-метилфурана с гексафторацетоном при (+10) - (-35)oC с выходом 95 - 98%.
Недостатком способа является наличие в целевом продукте до 5% примесей гидратов гексафторацетона, образующихся в результате взаимодействия гексафторацетона с влагой из воздуха, которые очень сложно удалить химическим путем. Как выяснилось, наличие гидратов гексафторацетона в готовом продукте существенно снижает противомикробную активность, ухудшая бактерицидные свойства.
Задачей создания изобретения является упрощение процесса, уменьшение содержания примесей и стабилизация бактерицидных свойств.
Поставленная задача достигается использованием окиси гексафторпропилена в качестве исходного сырья, которая предконденсацией с 2-метилфураном проходит через колонку, заполненную оксидом алюминия при 100 - 120oC, и вступает в реакцию конденсации с 2-метилфураном.
Использование окиси гексафторпропилена в качестве исходного сырья позволяет получать целевой продукт с выходом не менее 98% и практически полностью избежать образование примесей, присутствие которых снижает бактерицидную активность.
Отличительным признаком предлагаемого способа является проведение процесса получения 2-метил-5-[ди(трифторметил)оксиметил] фурана с использованием в качестве исходного сырья окиси гексафторпропилена, которую предварительно пропускают через колонку, заполненную оксидом алюминия при 90 - 100oC. Выходящие из колонки газы вступают в реакцию конденсации с 2-метилфураном при (-5) - (+25)oC.
При соотношении исходных компонентов 1,0:1,5, предпочтительно 1,0:1,2 избыток 2-метилфурана позволяет снизить содержание побочных продуктов, влияющих на противомикробную активность.
Использование окиси гексафторпропилена в качестве исходного сырья и небольшого избытка 2-метилфурана позволяет существенно упростить процесс, снизить энерго-и трудозатраты, связанные с очисткой от примесей, которые неизбежно образуются в процессе конденсации и влияют на бактерицидные свойства гогового продукта. Избыток 2 метилфурана после перегонки используется вновь.
Снижение энерго- и трудозатрат уменьшает себестоимость готового продукта.
Это отличие является существенным, так как технических решений, обладающих сходными признаками в патентной и научно-технической литературе, не обнаружено.
Пример 1. В реактор из нержавеющей стали вместимостью 500 см3, снабженный перемешивающим устройством, сифонной трубкой для подачи окиси гексафторпропилена, соединенной с обогреваемой трубкой, заполненной оксидом алюминия, загружают 82,0 г (1,0 моль) 2-метилфурана и подают 166,0 г (1,0 моль) окиси гексафторпропилена через обогреваемую до 90 - 110oC трубку, заполненную оксидом алюминия. Скорость подачи окиси гексафторпропилена регулируется температурой в реакторе, которая не должна превышать - 5oC и по проскоку газообразных сдувок из реактора. После подачи расчетного количества окиси гексафторпропилена реакционную смесь перемешивают в течение 0,5 - 1,0 ч и перегоняют в вакууме при 59 - 60oC при 18 мм рт.ст.
Получают 244,2 г 2-метил-5-[ди(трифторметил)оксиметил]фурана, выход которого составляет 98,5%.
Пример 2. В условиях примера в реактор помещают 41,0 г (0,5 моль) 2-метилфурана и при температуре реакционной смеси +5oC подают 83,0 г (0,5 моль) окиси гексафторпропилена, предварительно пропустив ее через оксид алюминия.
Реакционную смесь перегоняют в вакууме, получают 122,6 г 2-метил-5-[ди(трифторметил)оксиметил]фурана, что составляет 98,9% от теории.
Пример 3. В условиях примера 1 в реактор загружают 45,1 г (0,55 моль) 2-метилфурана и при +5oC конденсируют 83,0 г (0,5 моль) обработанную аналогичным образом окись гексафторпропилена.
Реакционную смесь перегоняют в вакууме, получают 122,8 г 2-метил-5-[ди(трифторметил)оксиметил] фурана, что составляет 99,03% от теории.
Пример 4. В условиях примера 1 в реактор помещают 49,2 (0,6 моль) 2-метилфурана и при +5oC конденсируют 83,0 г (0,5 моль) обработанную аналогичным образом окись гексафторпропилена.
Реакционную смесь перегоняют в вакууме, получают 123,0 г 2-метил-5-[ди(трифторметил)оксиметил] фурана, что составляет 99,2% от теории.
Пример 5. В условиях примера 1 в реактор помещают 82,0 г (1,0 моль) 2-метилфурана и 166,0 г (1,0 моль) окиси гексафторпропилена, при +10oC, обработанную аналогичным образом. Далее температуру реакционной смеси повышают до комнатной, перегоняют в вакууме и получают 246,5 г 2-метил-5-[ди(трифторметил)оксиметил] фурана, что составляет 99,1% от теории.
Пример 6. В условиях примера 1 в реактор помещают 82,0 г (1,0 моль) 2-метилфурана и 166,0 г (1,0 моль) окиси гексафторпропилена, при +25oC, обработанную аналогичным образом. Далее температуру реакционной смеси повышают до комнатной, перегоняют в вакууме и получают 246,5 г 2-метил-5-[ди(трифторметил)оксиметил)фурана, что составляет 99,1% от теории.
Как видно из примеров 1 - 6, предлагаемый способ получения 2-метил-5-[ди(трифторметил)оксиметил] фурана позволяет значительно упростить процесс и получить целевой продукт с достаточно высоким стабильным выходом, а также избежать образование примесей, снижающих противомикробную активность.
Полученный таким образом 2-метил-5-[ди(трифторметил)оксиметил] фурана проявляет фунгицидные и вирулицидные свойства. Нижеследующие примеры подтверждают вышеуказанные свойства.
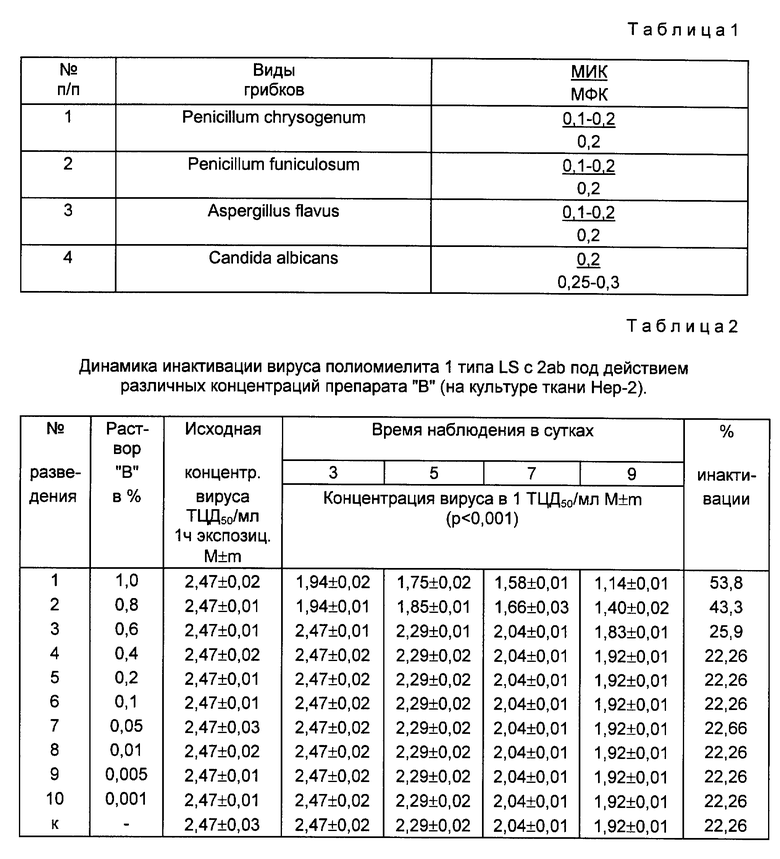
Пример 7. Фунгистатическую и фунгицидную активность 2-метил-5-[ди(трифторметил)оксиметил] фурана исследовали на жидкой питательной среде Сабуро (Милованова С.Н., 1974) готовили исходное разведение препарата в среде, затем из него производили ряд последовательно вдвое убывающих разведений в объеме 3 мл. Для заражения среды, содержащей различные концентрации препарата, использовали 2-недельные культуры грибков (Penicillum chrysogenum ВГИК 245; Penicillum funiculosum; Aspergillus flavus ВКМГ - 25; Candida albicans), приготовленную по оптическому стандарту одномиллиардную взвесь по 0,2 мл добавляли в разведения препарата. Контрольные и опытные пробирки термостатировали при t = 26oC в течение 7 дней, после чего проводили регистрацию результатов. Фунгицидную активность изучали в специальных опытах с тестами в пробирки с препаратом вносили батистовые тесты, зараженные грибками. После заданной экспозиции тесты обмывали в трех сменах стерильного физиологического раствора и помещали в пробирки со средой, не содержащей препарата. Засеянные пробирки выдерживали в термостате при t = 24 - 27oC в течение 8 - 10 дней и затем при комнатной температуре 1,5 - 2 месяца.
Результаты проведенных испытаний приведены в табл. 1.
Из табл. 1 следует заключить, что препарат оказывает на грибки пенициллум и аспергиллус фунгицидный эффект в концентрации 0,2 %, а гибель грибка кандида установлена при воздействии 0,3% 2-метил-5-[ди(трифторметил)оксиметил] фурана.
Пример 8. Вирулицидное действие вещества исследовали в соответствии с приказом М3 СССР N 250 от 13.03.75. Первый этап включал изучение токсического действия соединения на линии культур тканей Нер-2 и М-19. Для каждой линии получено 22 млн. клеток путем рассадки маточной культуры. После слива поддерживающей среды из пробирок с культурой ткани внесли по 0,2 мл концентрации исследуемого препарата. Время контакта с препаратом - 30 мин при 37oC в термостате. Затем слив, жидкость, отмыли 3-кратно культуру ткани поддерживающей и ростовой средой (Среда 199 и Игла МЭМ). Результаты контроля влияния разведений раствора препарата "Вилагин" (далее "B") не показали развитие неспецифического цитопатического или токсического действия препарата в данных разведениях на линии клеток Нер-2- в течение 9 суток наблюдения, линии М-19 - в течение 12 суток наблюдения.
Далее в качестве модели был использован аттенцированный штамм вируса полиомиелита типа LS с 2 ab. Определение вируса проводили методом титрования на 2 перевиваемых линиях пробирочных культур Нер-2 и М-19.
Титр вируса определяли методом конечных десятичных разведений в ТЦД50/мл по Риду и Менчу. Исходный титр вируса составлял 3,47 lg ТЦД50/мл. Готовили исходные разведения исследуемого вещества, в каждую концентрацию вносили вирус полиомиелита 1 типа в объеме 1 мл в концентрации 3,47 lg ТЦД50/мл, т. е. общая концентрация вируса в модельной емкости составила 2,47 lg ТЦД50/мл.
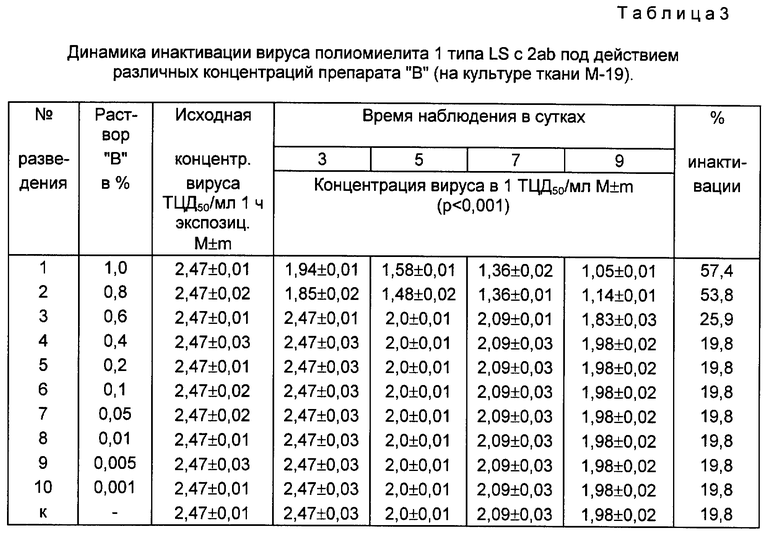
После часовой экспозиции провели 1-й отбор проб и заражение приготовленных пробирочных культур Нер-1 и М-19 из расчета по 4 пробирки каждой линии на каждую концентрацию раствора "B" и по 4 пробирки на контроль. Далее отбор проб для контроля динамики инактивации вирусов производили на 3, 5, 7 и 9 сутки наблюдения. Результаты определения содержания вируса и снижения его содержания под действием различных концентраций препарата "B" представлены в табл. 2 и 3.
Результаты свидетельствуют, что наблюдается статически достоверное (p<0,01) снижение содержания вируса в опыте по сравнению с контролем при концентрации препарата "B" 1,0% и 0,8%.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 2-МЕТИЛ-5-[ДИ(ТРИФТОРМЕТИЛ)ОКСИМЕТИЛ]ФУРАНА | 2002 |
|
RU2196771C1 |
| ДЕЗИНФИЦИРУЮЩЕЕ СРЕДСТВО | 2007 |
|
RU2354405C2 |
| АЭРОЗОЛЬНОЕ ДЕЗИНФИЦИРУЮЩЕЕ СРЕДСТВО "ВИЛАГ-2" | 1996 |
|
RU2119519C1 |
| Способ получения гексафторацетона | 1978 |
|
SU740741A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕРФТОРИРОВАННЫХ ПРОСТЫХ ЭФИРОВ С КОНЦЕВЫМИ ФУНКЦИОНАЛЬНЫМИ ГРУППАМИ | 2000 |
|
RU2179548C2 |
| СОПОЛИМЕРЫ ДИАЛЛИЛАМИНОФОСФОНИЕВЫХ СОЛЕЙ С ДИОКСИДОМ СЕРЫ, ПРОЯВЛЯЮЩИЕ АНТИМИКРОБНУЮ АКТИВНОСТЬ | 2008 |
|
RU2365596C1 |
| Способ получения перфторированных кетонов | 1975 |
|
SU569554A1 |
| Способ получения десфлурана | 2024 |
|
RU2833270C1 |
| ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ-МЕТИЛ 7-АРИЛ-4,9-ДИАРОИЛ-3-ГИДРОКСИ-1-(2-ГИДРОКСИФЕНИЛ)-2,6-ДИОКСО-1,7-ДИАЗАСПИРО[4.4]НОНА-3,8-ДИЕН-8-КАРБОКСИЛАТЫ; МЕТИЛ 6,9-ДИАРИЛ-11-АРОИЛ-2-(О-ГИДРОКСИФЕНИЛ)-3,4,10-ТРИОКСО-7-ОКСА-2,9-ДИАЗАТРИЦИКЛО[6.2.1.0]УНДЕЦ-5-ЕН-8-КАРБОКСИЛАТЫ; СПОСОБ ПОЛУЧЕНИЯ МЕТИЛ 6, 9-ДИАРИЛ-11-АРОИЛ-2-(О-ГИДРОКСИФЕНИЛ)-3,4,10-ТРИОКСО-7-ОКСА-2,9-ДИАЗАТРИЦИКЛО[6.2.1.0]УНДЕЦ-5-ЕН-8-КАРБОКСИЛАТОВ; МЕТИЛ 11-БЕНЗОИЛ-2-О-ГИДРОКСИФЕНИЛ-3,4,10-ТРИОКСО-9-П-ТОЛИЛ-6-ФЕНИЛ-7-ОКСА-2, 9-ДИАЗАТРИЦИКЛО[6.2.1.0]УНДЕЦ-5-ЕН-8-КАРБОКСИЛАТ, ОБЛАДАЮЩИЙ ПРОТИВОМИКРОБНОЙ АКТИВНОСТЬЮ | 2008 |
|
RU2383550C1 |
| Способ получения 2-алкил (арил) тиофенов | 1989 |
|
SU1685938A1 |
Изобретение относится к области фторорганической химии, в частности к способу получения 2-5-/ди(трифторметил)оксиметил/фурана, обладающего фунгицидными и вирулицидными свойствами. Этот способ позволяет достичь упрощения процесса, уменьшения содержания примесей и стабилизацию бактерицидных свойств. Способ заключается в проведении процесса получения 2-метил-5-/ди-(трифторметил)оксиметил/фурана с использованием в качестве исходного сырья окиси гексафторпропилена, которую предварительно пропускают через колонку, заполненную оксидом алюминия при 90-100oC. Выходящие из колонки газы вступают в реакцию конденсации с 2-метилфураном при (-5)-(+25)oC. При соотношении исходных компонентов 1,0:1,5, предпочтительно 1,0:1,2 избыток 2-метилфурана позволяет снизить содержание побочных продуктов, влияющих на противомикробную активность. 3 табл.
Способ получения 2-метил-5-/ди(трифторметил)оксиметил/ фурана взаимодействием 2-метилфурана с фторкислородсодержащим соединением, отличающийся тем, что в качестве фторкислородсодержащего соединения используют окись гексафторпропилена, которую предварительно пропускают через оксид алюминия и подвергают взаимодействию с 2-метилфураном при (-5) - (+25)oC, и процесс ведут при соотношении исходных компонентов фторкислородсодержащего соединения и 2-метилфурана 1,0 : 1,5, предпочтительно 1,0 : 1,2.
| SU, 1016285, A, 1983 | |||
| SU, 1051087, A, 1983 | |||
| SU, 1833382, A3, 1993. |
Авторы
Даты
1998-11-10—Публикация
1997-10-07—Подача