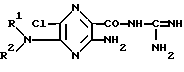
Изобретение относится к новым химическим веществам с ценными фармакологическими свойствами, в частности к производным пиразина общей формулы (I)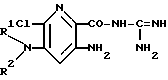
где
R1 - водород или алкил с 1 - 8 атомами углерода;
R2 - неразветвленная или разветвленная алкильная группа с 1 - 8 атомами углерода, незамещенная или замещенная независимыми остатками, выбранными из группы, включающей алкоксил с 1 - 4 атомами углерода, гидроксил, феноксигруппу, которая в свою очередь одно- или многократно замещена алкилом с 1 - 4 атомами углерода, алкоксилом с 1 - 4 атомами углерода, алкоксиалкилом с 1 - 4 атомами углерода в каждой алкильной части или цианогруппой, аминогруппу формулы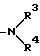
где
R3 - водород или алкил с 1 - 4 атомами углерода;
R4 - фенил, многократно замещенный алкилом с 1 - 4 атомами углерода, замещенный аминогруппой дихлорфенилсульфонил, неразветвленная или разветвленная алкильная группа с 1 - 8 атомами углерода, незамещенная или замещенная независимыми остатками, выбранными из группы, включающей гидроксил, феноксигруппу, которая в свою очередь многократно замещена галоидом или алкоксиалкилом с 1 - 4 атомами углерода в каждой алкильной части, карбонилрадикал формулы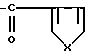
где
X - кислород или группу - NH-;
пиперидилрадикал, N-замещенный алкилом с 1 - 8 атомами углерода, незамещенным или замещенным независимыми остатками, выбранными из группы, включающей гидроксил, феноксигруппу, которая в свою очередь замещена алкоксилом с 1 - 4 атомами углерода или алкоксиалкилом с 1 - 4 атомами углерода в каждой алкильной части, и фенил, незамещенный или одно- или многократно замещенный алкоксилом с 1 - 4 атомами углерода, амидиногруппа формулы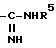
где
R5 - фенил, одно или многократно замещенный галоидом или алкилом с 1 - 4 атомами углерода,
а также группа формулы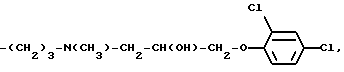
если
R1 означает водород, или R1 и R2 вместе с атомом азота, с которым они связаны, образуют пиперазиновое кольцо, незамещенное или замещенное в положении 4 группой формулы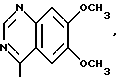
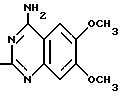
или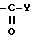
где
Y означает группы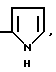
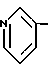
или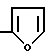
или алкилом с 1 - 8 атомами углерода, незамещенными или замещенными независимыми остатками, выбранными из группы, включающей гидроксил, феноксигруппу, замещенную алкоксилом с 1 - 4 атомами углерода или алкоксиалкилом с 1 - 4 атомами углерода в каждой алкильной группе, и α- нафтоксигруппу,
причем, если R1 означает водород, то R2 не означает алкил, бензил, метил-, фтор- или хлорбензил, фенилэтил, гидроксиэтил, или группу HOCH2-(CHOH)4-CH2, или если R1 означает алкил с 1 - 3 атомами углерода, то R2 не означает алкил с 1 - 4 атомами углерода,
и их кислотно-аддитивным солям.
Производные пиразина формулы (I) можно получать известными методами. В качестве примеров описываются два возможных способа.
1) Сложный алкиловый эфир 3-амино-5,6-дихлолорпиразин-2-карбоновой кислоты подвергают взамодействию с амином формулы (II)
HNR1R2
где
R1 и R2 имеют вышеуказанные значения, в безводных условиях и получаемое при этом соединение формулы (III)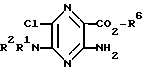
где
R6 - означает алкил с 1 - 4 атомами углерода,
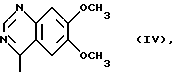
подвергают взаимодействию с гуанидином формулы (IV)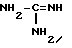
с последующим выделением целевого продукта.
Взаимодействие сложного алкилового эфира 3-амино-5,6-дихлорпиразин-2-карбоновой кислоты с амином (II) до промежуточного соединения общей формулы (III) осуществляют известными из литературы приемами в среде инертного растворителя при повышенной температуре в присутствии акцептора кислоты. При этом амин обычно используют в эквимолярном количестве. Однако возможно применять амин и в качестве акцептора кислоты и растворителя. Но в качестве растворителя предпочтительно используют диметилформамид и диметилсульфоид или их смеси. Температура реакции не является критической. Как правило, в зависимости от реакционноспособности используемого амина реакцию проводят при температурах от 80 до 100oC. В этих условиях реакция закончена по истечении примерно 1 - 2 часов. В качестве акцептора кислоты используют органическое и неорганические основания. Предпочтительно используют третичные амины, такие, как, например, пиридин, N-метилпиперидин, диметиланилин или триэтиламин.
Получаемые таким образом сложные эфиры 3,5-диаминопиразинкарбоновой кислоты формулы (III) в случае необходимости можно подвергать дополнительной обработке, как, например, ацилированию или алкилированию. Ацилирование проводят известными приемами, например, путем взаимодействия диамина формулы (III) с реакционноспособным производным карбоновой кислоты.
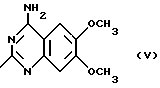
Алкилирование проводят, например, при получении соответствующих производных феноксипропаноламина. Для этой цели диаминосоединение формулы (V)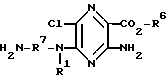
где
R7 - алкилен с 1 - 8 атомами углерода, R6 имеет вышеуказанное значение,
подвергают взаимодействию, например, с феноксипропиленоксидом общей формулы (VI)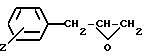
где
Z = алкоксил с 1 - 4 атомами углерода, алкоксиалкил с 1 - 4 атомами углерода в каждой алкильной группе, в среде пригодного растворителя, при комнатной температуре или при слегка повышенной температуре. Реакция обычно завершена примерно через 0,5 - 1 час.
Однако предпочитается вышеупомянутый непосредственный синтез.
Для получения целевых продуктов формулы (I) сложные эфиры 3,5-диаминопиразинкарбоновой кислоты формулы (III) подвергают взаимодействию с гуанидином формулы (IV) в среде пригодного растворителя при нагревании. В качестве растворителей особенно пригодны простые спирты. Реакцию предпочтительно проводят в метаноле при температуре кипения реакционной смеси. В таких условиях реакция, как правило, завершена через примерно 30 - 90 минут.
2) Взаимодействие производного пиразина формулы (VII)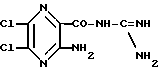
с амином формулы (II)
NHR1R2
где
R1 и R2 имеют вышеуказанные значения.
Взаимодействие проводят предпочтительно при повышенной температуре в полярном, по возможности безводном растворителе, как, например, диметилформамиде или диметилсульфоксиде.
Исходные соединения формулы (VII) получают известными способами. Их можно получать, например, согласно вышеприведенному способу 1), если используют сложные эфиры пиразинкарбоновой кислоты со структурой, аналогичной структуре эфиров формулы (III), содержащих, однако, в положении 5 вместо группы NR1R2 атом хлора.
Соединения формулы (I) можно использовать в качестве активных веществ в лекарственных средствах или в качестве промежуточных продуктов для получения таких активных веществ. Новые соединения тормозят обмены Na+/H- и Na+/Li+. Предлагаемые вещества можно использовать в качестве антигипертензивного муколитического, мочегонного и противораковых средств. Кроме того, их можно также применять для лечения связанных с ишемией болезней, таких, как, например, кардиальная, церебральная, желудочно-кишечная, легочная, ренальная ишемия, ишемия печени или скелетной мускулатуры. В качестве соответствующих болезней следует назвать, такие, как, например: коронарные заболевания сердца, стенокардия, эмболия в малом круге кровообращения, острая или хроническая почечная недостаточность, хроническая почечная недостаточность, инфаркт мозга и хронические нарушения кровообращений мозга. При повторной перфузии ишемического сердца, например, после стенокардии или инфаркта сердца, могут возникать необратимые повреждения кардиомиоцитов соответствующей области. В данном случае предлагаемые соединения можно использовать в качестве кардиозащитного средства.
Предлагаемые соединения можно также использовать для предотвращения повреждений, которые могут возникать вследствие недостаточного кровоснабжения при трансплантациях.
Для использования активных веществ пригодны обычные виды препаратов, такие, как, например, таблетки, драже, капсулы, гранулы, инъекционные растворы, в случае необходимости, апплицируемые через нос препараты, причем отдельная доза активного вещества обычно составляет 1 - 200 мг, предпочтительно 20 - 100 мг. Лекарственные средства получают известными приемами.
Нижеследующие примеры иллюстрируют получение производных пиразина формулы I.
Пример 1.
а) Сложный метиловый эфир 3-амино-6-хлор-5-(2-[1-(2,6-диметил-фенокси)] -пропиламино)-пиразин-2-карбоновой кислоты
4,44 г (20 ммоль) сложного метилового эфира 3-амино-5,6-дихлорпиразин-2-карбоновой кислоты, 3,6 г (20 ммоль) 2-амино-1-(2,6-диметилфенокси)пропана и 2,2 г (22 ммоль) триэтиламина нагревают в 40 мл безводного диметилформамида до температуры 95 - 100oC в течение 1,5 ч. После отгонки растворителя в вакууме остаток очищают на силикагеле (в качестве элюента используют смесь сложного этилового эфира уксусной кислоты, изопропанола и аммиака в соотношении 70 : 30 : 1).
Выход: 7,3 г.
б) Гидрохлорид N-амидино-3-амино-6-хлор-5-(2-[1-(2,6- диметилфенокси)] пропиламино)пиразин-2-карбоксамида
7,3 г (0,02 ммоль) сложного метилового эфира пиразинкарбоновой кислоты стадии а), растворенного в 50 мл метанола, и 80 мл 1-молярного метанольного раствора гуанидина нагревают на кипящей бане в течение 45 минут. Растворитель отгоняют в вакууме, остаток очищают на силикагеле (в качестве элюента используют смесь сложного этилового эфира уксусной кислоты, изопропанола и аммиака в соотношении 70 : 30 : 5) и получают гидрохлорид целевого продукта.
Выход: 4,9 г; т.пл.: 267 - 270oC.
Пример 2.
а) Сложный метиловый эфир 3-амино-6-хлор-5-[N'-(5-фтор-2-метил) фенил] -гуанидино-пиразин-2-карбоновой кислоты
13,3 г (60 ммоль) сложного метилового эфира 3-амино-5,6-дихлорпиразин-2-карбоновой кислоты, 15 г (90 ммоль) (5-фтор-2-метил)-фенилгуанидина и 6 г триэтиламина перемешивают в 100 мл диметилсульфоксида при температуре 90oC в течение двух часов. После охлаждения смешивают с 100 мл хлористого метилена. При охлаждении добавляют каплями 100 мл воды, отделяют метиленхлоридную фазу и водную фазу экстрагируют 150 мл хлористого метилена. Собранные метиленхлоридые фазы промывают небольшим количеством воды, сушат над сульфатом магния и сгущают. Остаток очищают на силикагеле (в качестве элюента используют смесь сложного этилового эфира уксусной кислоты и изопропанола в соотношении 95 : 5).
Выход: 12,6 г
б) N-амидино-3-амино-6-хлор-5-[N'-(5-фтор-2-метил)-фенил] -гуанидинопиразин-2-карбоксамид
5,5 г сложного метилового эфира пиразинкарбоновой кислоты стадии а) растворяют в 25 мл безводного диметилформамида, смешивают с 50 мл 1,2 молярного метанольного раствора гуанидина и кипятят с обратным холодильником в течение 30 минут. Затем метанол отгоняют и остаток очищают на силикагеле (в качестве элюента используют смесь сложного этилового эфира уксусной кислоты, изопропанола и аммиака в соотношении 70 : 30 : 5) и продукт реакции переводят в гидрохлорид.
Выход: 8,7 г; т.пл.: 242oC.
Пример 3.
Дигидробромид N-амидино-3-амино-6-хлор-5-(4-]2-(3-метокси- фенокси)этил] -1-пиперазинил)-пиразин-2-карбоксамида
858 мг (3 ммоль) N-амидино-3-амино-5,6-дихлорпиразин-2- карбоксамида, 924 мг (3 ммоль) N-[2-(3-метоксифенокси)-этил]пиперазина и 1,2 г (12 ммоль) триэтиламина нагревают до температуры 95 - 100oC в течение 75 минут. Растворитель отгоняют в вакууме, остаток очищают на силикагеле (в качестве элюента используют смесь сложного этилового эфира уксусной кислоты, изопропанола и аммиака в соотношении 7 : 3 : 1) и получаемый продукт переводят в дигидробромид.
Выход: 1,13 г; т.пл.: 159 - 162oC.
Пример 4.
Дигидрохлорид N-амидино-3-амино-6-хлор-5-[(4-амино-6,7-диметокси)-2-хиназолинил]-1- пиперазинил]-пиразин-2-карбоксамида
13,1 г (45,3 ммоль) N-[(4-амино-6,7-диметокси)-2-хиназолинил]- пиперазина подвергают взаимодействию с 10 г (45,3 ммоль) сложного метилового эфира 3-амино-5,6-дихлорпиразин-2-карбоновой кислоты и 7 мл триэтиламина в 60 мл диметилсульфоксида при температуре 80oC в течение двух часов. После охлаждения продукт реакции осаждают путем добавления 100 мл воды, отсасывают, сушат и без дальнейшей очистки переводят в целевой продукт аналогично примеру 1б путем взаимодействия с гуанидином.
Выход: 10,5 г; т.пл.: > 290oC.
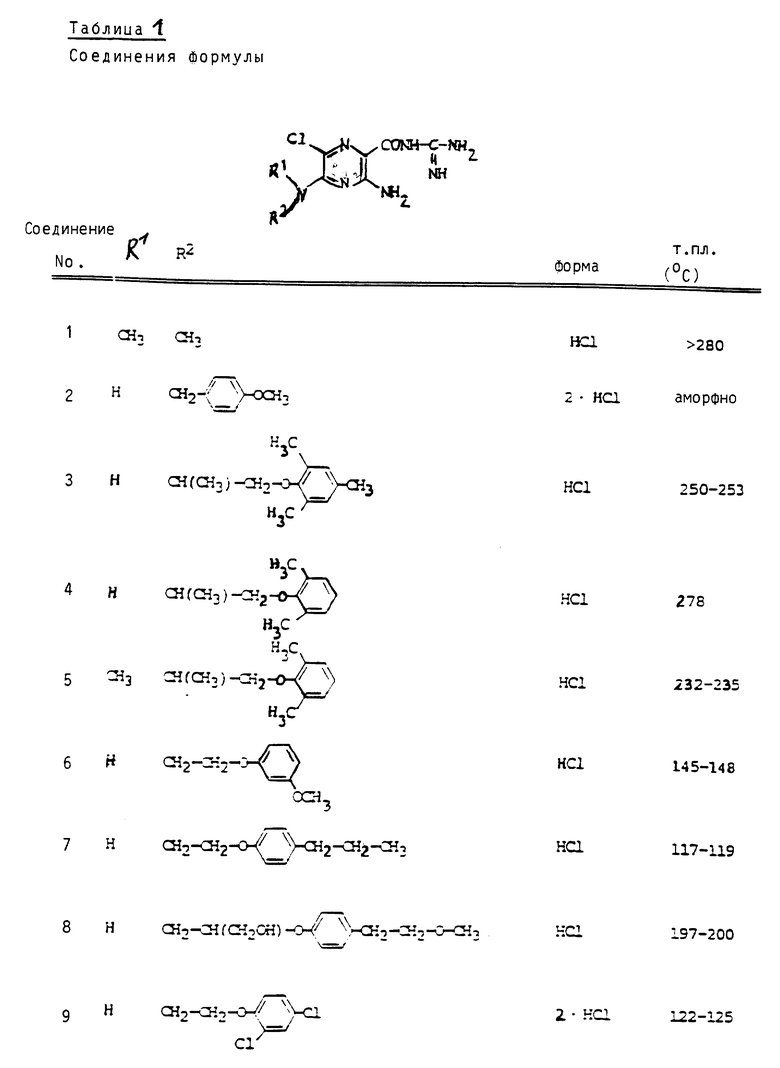
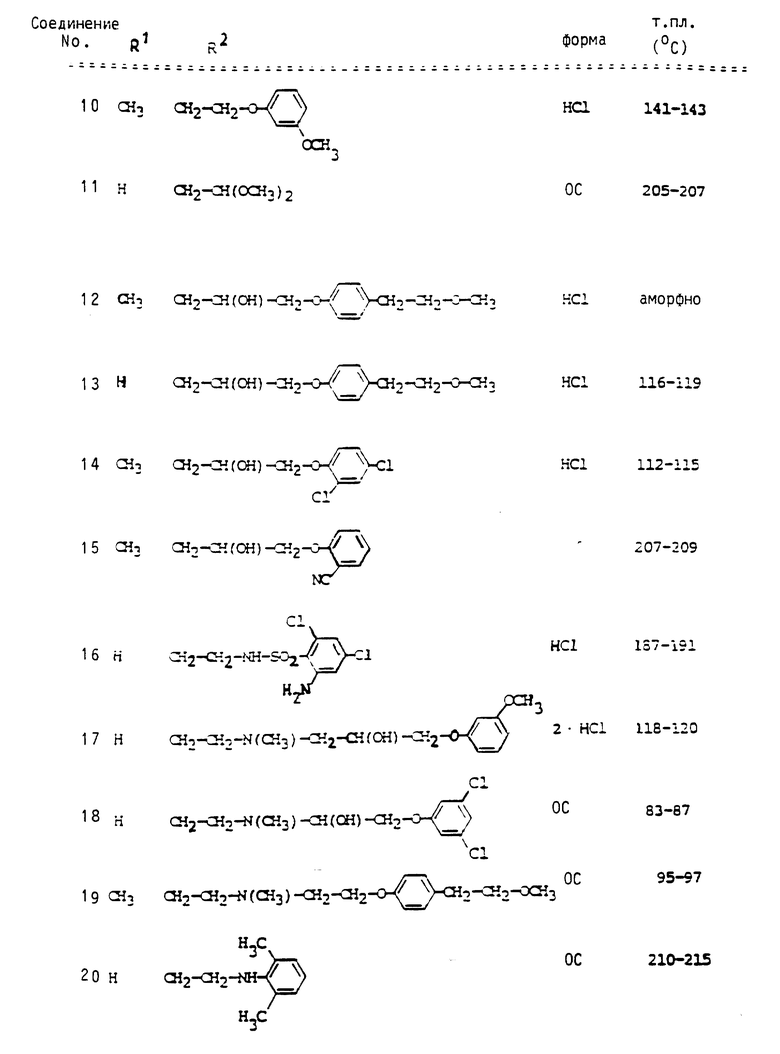
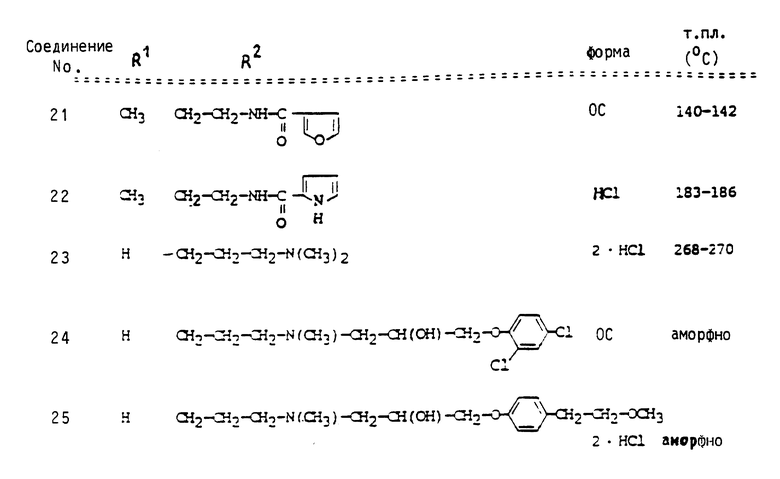
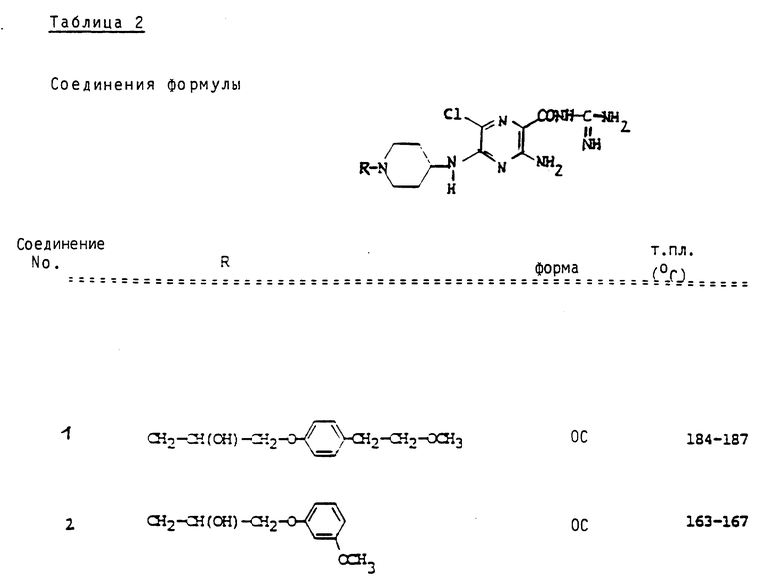
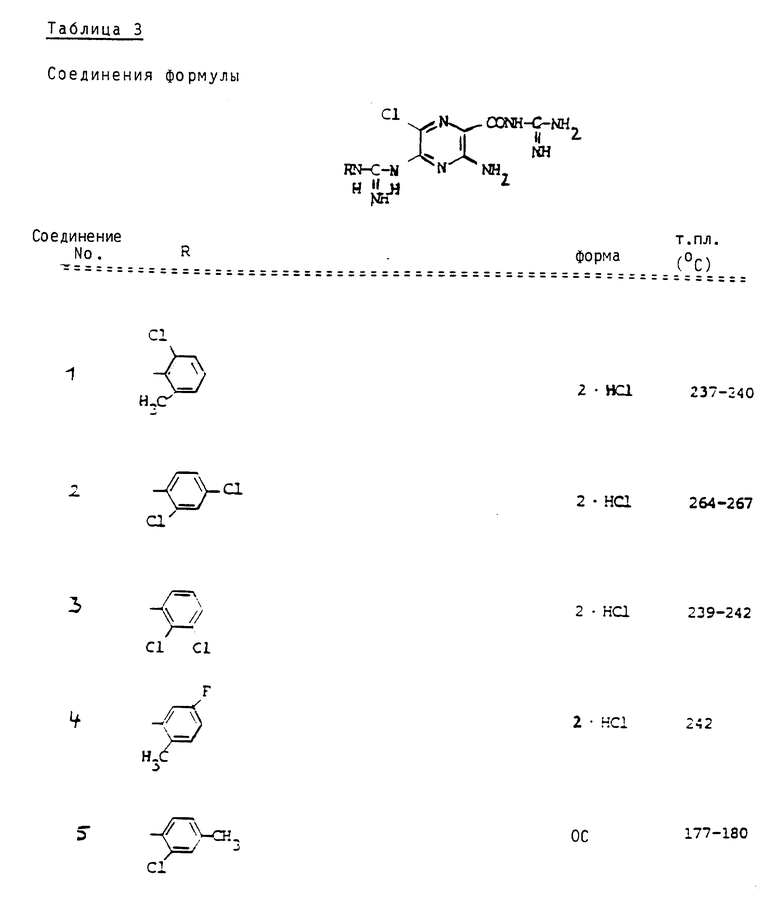
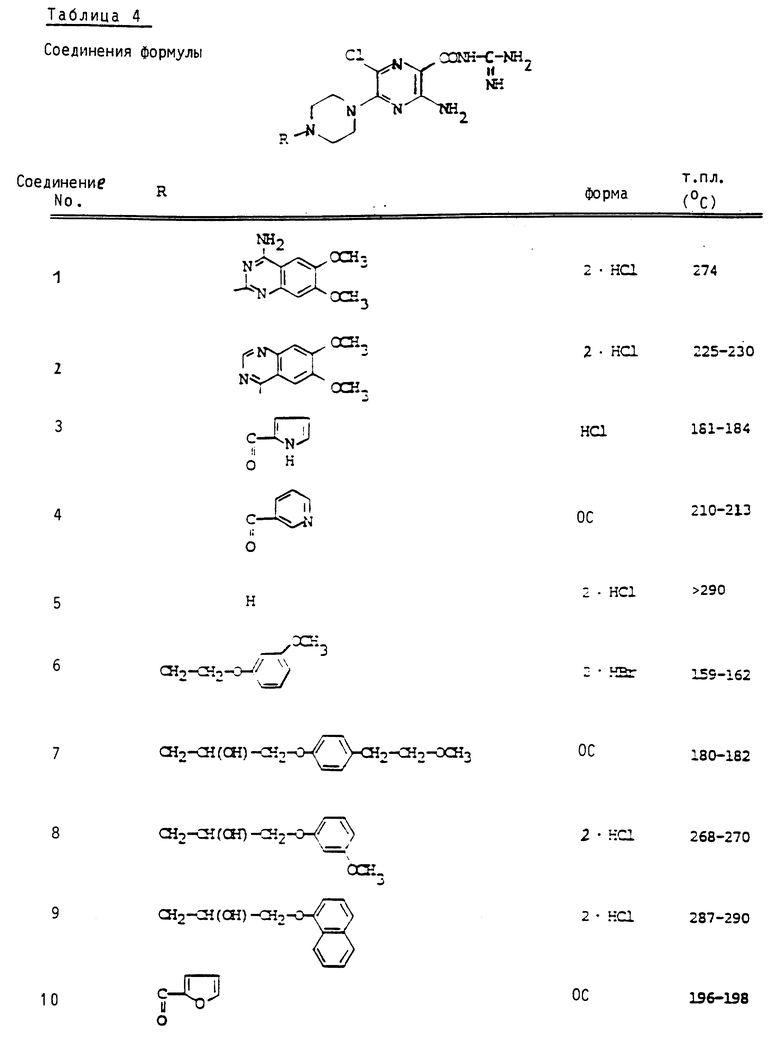
Сведенные в табл. 1 - 4 соединения можно получать аналогично вышеприведенным примерам и вышеприведенным общим данным. Если соединения получаются в виде оснований, то под понятием "форма" приводится условное сокращение OC, а в случае получения соли указывается используемая для солеобразования кислота. 2-HCl означает дигидрохлорид.
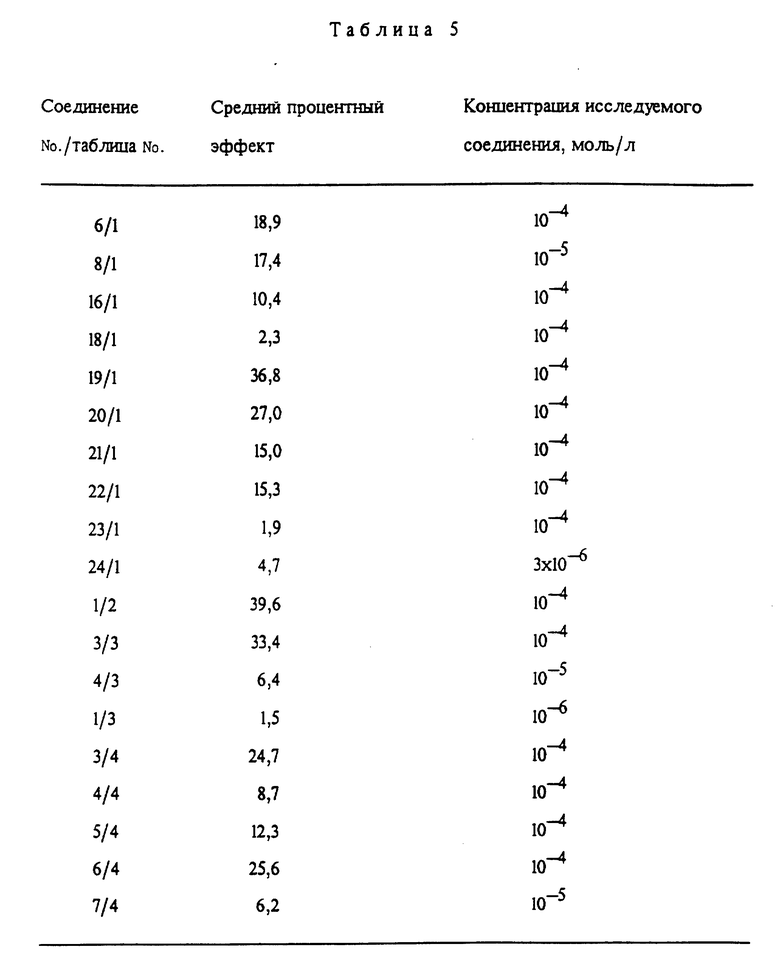
Производные пиразина формулы (I) представляют собой высокоактивные средства для торможения обмена натриевых и водородных ионов, а также обмена натриевых и литиевых ионов. При этом обмен натриевых и водородных ионов рассматривается как разница между водородсодержащими вытекающими потоками в натрийсодержащей и безнатриевой средах, которую определяли на эритроцитах кролика. Измеряли протонсодержащий вышеуказанный поток с помощью титрования pH при постоянной величине pH. При этом определяли так называемый "средний процентный эффект". Чем ниже этот эффект, тем лучше действие исследуемого соединения.
Результаты данного опыта сведены в следующей табл. 5.
Обмен натриевых и литиевых ионов рассматривается как разницу между литийсодержащими вытекающими потоками в натрийсодержащей и безнатриевой средах, которую определяли на эритроцитах человека. Измеряли литийсодержащий вытекающий поток с помощью атомной абсорбции. При этом определяли так называемый "средний процентный эффект". Чем ниже этот эффект, тем лучше действие исследуемого соединения. Результаты данного опыта сведены в следующей табл. 6.
Предлагаемые соединения относятся к категории малотоксичных веществ.

Изобретение относится к производным пиразина формулы I, где R1 - H или C1-8-алкил, R2 - C1-8-алкил, незамещенный или замещенный C1-4-алкоксилом, гидроксилом, феноксигруппой, которая в свою очередь одно- или многократно замещена C1-4-алкилом, C1-4-алкоксилом, алкоксиалкилом или цианогруппой, аминогруппа 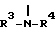 , где R3 - H или C1-4-алкил, R4-фенил, многократно замещенный C1-4-алкилом, замещенный аминогруппой дихлорфенилсульфонил, C1-4-алкил, незамещенный или замещенный остатками, выбранными из группы: гидроксил, феноксигруппа, в свою очередь многократно замещенная галоидом или алкоксиалкилом, карбонилрадикал формулы II, где X - кислород или -NH-, пиперидилрадикал, N-замещенный C1-8-алкилом, и фенил незамещенный или замещенный C1-4-алкоксилом, амидиногруппа формулы
, где R3 - H или C1-4-алкил, R4-фенил, многократно замещенный C1-4-алкилом, замещенный аминогруппой дихлорфенилсульфонил, C1-4-алкил, незамещенный или замещенный остатками, выбранными из группы: гидроксил, феноксигруппа, в свою очередь многократно замещенная галоидом или алкоксиалкилом, карбонилрадикал формулы II, где X - кислород или -NH-, пиперидилрадикал, N-замещенный C1-8-алкилом, и фенил незамещенный или замещенный C1-4-алкоксилом, амидиногруппа формулы 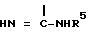 , где R5 - фенил, замещенный галоидом или C1-4-алкилом, а также группа формулы III, если R1 - H, или R1 и R2 вместе с атомом азота, с которым они связаны, образуют пиперазиновое кольцо, незамещенное или замещенное в положении 4 группой IV, V, или
, где R5 - фенил, замещенный галоидом или C1-4-алкилом, а также группа формулы III, если R1 - H, или R1 и R2 вместе с атомом азота, с которым они связаны, образуют пиперазиновое кольцо, незамещенное или замещенное в положении 4 группой IV, V, или 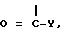 где Y-2-пирролил, 3-пиридил или 2-фурил, или C1-8-алкил, или алкоксиалкил, и α -нафтоксигруппа, причем если R1 - H, то R2 не означает алкил, бензил, фтор- или хлорбензил, фенэтил, гидроксиэтил или HOCH2 - (CHOH)4 - CH2, или если R1 - C1-3-алкил, то R2 не означает C1-4-алкил, и их кислотно-аддитивные соли. Соединения формулы I тормозят обмены Na+/H- и Na+/Li+ и можно использовать в качестве антигипертеизивного муколитического, мочегонного и противораковых средств. 1 з.п. ф-лы, 6 табл.
где Y-2-пирролил, 3-пиридил или 2-фурил, или C1-8-алкил, или алкоксиалкил, и α -нафтоксигруппа, причем если R1 - H, то R2 не означает алкил, бензил, фтор- или хлорбензил, фенэтил, гидроксиэтил или HOCH2 - (CHOH)4 - CH2, или если R1 - C1-3-алкил, то R2 не означает C1-4-алкил, и их кислотно-аддитивные соли. Соединения формулы I тормозят обмены Na+/H- и Na+/Li+ и можно использовать в качестве антигипертеизивного муколитического, мочегонного и противораковых средств. 1 з.п. ф-лы, 6 табл.
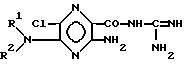 (I)
(I)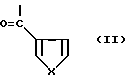
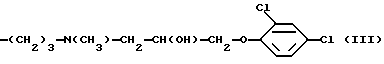
 \
\
где R1 - водород или алкил с 1 - 8 атомами углерода;
R2 - неразветвленная или разветвленная алкильная группа с 1 - 8 атомами углерода, незамещенная или замещенная независимыми остатками, выбранными из группы, включающей алкоксил с 1 - 4 атомами углерода, гидроксил, феноксигруппу, которая в свою очередь одно- или многократно замещена алкилом с 1 - 4 атомами углерода, алкоксилом с 1 - 4 атомами углерода, алкоксиалкилом с 1 - 4 атомами углерода в каждой алкильной части или цианогруппой, аминогруппу формулы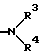
где R3 - водород или алкил с 1 - 4 атомами углерода;
R4 - фенил, многократно замещенный алкилом с 1 - 4 атомами углерода, замещенный аминогруппой дихлорфенилсульфонил, неразветвленная или разветвленная алкильная группа с 1 - 4 атомами углерода, незамещенная или замещенная независимыми остатками, выбранными из группы, включающей гидроксил, феноксигруппу, которая в свою очередь многократно замещена галоидом или алкоксиалкилом с 1 - 4 атомами углерода в каждой алкильной части, карбонилрадикал формулы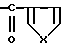
где Х - кислород или группа -NH-, пиперидилрадикал, N-замещенный алкилом с 1 - 8 атомами углерода, незамещенным или замещенным независимыми остатками, выбранными из группы, включающей гидроксил, феноксигруппу, которая в свою очередь замещена алкоксилом с 1 - 4 атомами углерода или алкоксиалкилом с 1 - 4 атомами углерода в каждой алкильной части, и фенил, незамещенный или одно- или многократно замещенный алкоксилом с 1 - 4 атомами углерода, амидиногруппа формулы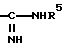
где R5 - фенил, одно- или многократно замещенный галоидом или алкилом с 1 - 4 атомами углерода,
а также группа формулы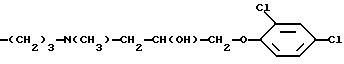
если R1 означает водород,
или R1 и R2 вместе с атомом азота, с которым они связаны, образуют пиперазиновое кольцо, незамещенное или замещенное в положении 4 группой формулы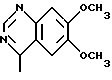
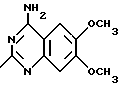
или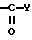
где Y означает группы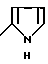
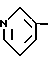
или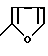
или алкилом с 1 - 8 атомами углерода, незамезенным или замещенным независимыми остатками, выбранными из группы, включающей гидроксил, феноксигруппу, замещенную алкоксилом с 1 - 4 атомами углерода или алкоксиалкилом с 1 - 4 атомами углерода в каждой алкильной группе, и α-нафтоксигруппу,
причем если R1 означает водород, то R2 не означает алкил, бензил, метил-, фтор- или хлорбензил, фенилэтил, гидроксиэтил, или группу HOCH2-(CHOH)4-CH2, или если R1 означает алкил с 1 - 3 атомами углерода, то R2 не означает алкил с 1 - 4 атомами углерода,
и их кислотно-аддитивные соли.
N-амидино-3-амино-6-хлор-5-[4-[(4-амино-6,7-диметокси)-2-хиназолинил] -1-пиперазинил]-пиразин-2-карбоксамид,
N-амидино-3-амино-6-хлор-5-[N'-(5-фтор-2-метил)-фенил] -гуанидинопиразин-2-карбоксамид и
N-амидино-3-амино-6-хлор-5-[2[1-(2,6-диметил)-фенокси)-пропиламино]пиразин-2-карбоксамид,
а также их кислотно-аддитивные соли.
| SU, 343447, 1972 | |||
| SU, 1627084, 1990 | |||
| US, 3539569, 1976. |
Авторы
Даты
1998-12-27—Публикация
1992-07-31—Подача