Изобретение относится к новым сложным эфирам карбоновой кислоты с ценными свойствами, в частности к сложным эфирам тиенилкарбоновой кислоты и аминоспиртов общей формулы (I)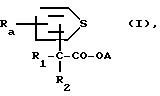
где А группа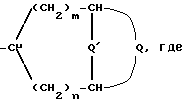
где m и n независимы друг от друга и означают 1 или 2,
Q группа формул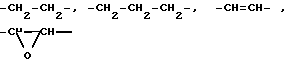
Q' группаNR, где R означает водород или алкил с 1 4 атомами углерода, незамещенный или замещенный галогеном или гидроксилом, или группа NRR', где R' алкил с 1 4 атомами углерода, или R и R' вместе образуют алкилен с 4 6 атомами углерода, причем в случае четвертого соединения к положительному заряду атома азота относится эквивалент аниона (X⊖ ),,
R1 тиенил, фенил, фурил, циклопентил и циклогексил, незамещенные или замещенные метилом, причем тиенил и фенил могут быть также замещены фтором или хлором,
R2 водород, алкоксил 1 4 атомами углерода или алкил с 1 4 атомами углерода,
Ra водород, фтор, хлор или метил, при условии, что если А означает 3-тропанил, R1 гидроксил и R2-2-или 3-тиенил, то Ra не означает водород, их продуктам кватернизации и кислотно-аддитивным солям, еслиNR означает вторичную или третичную аминогруппу, к содержащему упомянутые соединения лекарственному средству, а также к способу получения их соединений.
В соединениях формулы I R1 предпочтительно означает тиенил, а R2 гидроксил. Группа ОА предпочтительно имеет α-конфигурацию и является производным, например, скопина, тропина, гранатолина и 6,7-дигидротропина или соответствующих нор-соединений. Но группа ОА может также иметь b-конфигурацию, как, например, в псевдотропине и псевдоскопине.
В качестве соответствующих радикалов можно, например, назвать: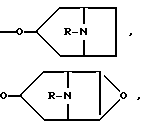 ,
,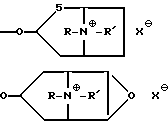
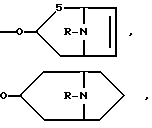 ,
,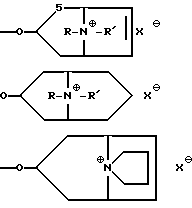
Радикал R предпочтительно является низшим алкильным радикалом, как, например, метилом, этилом, н-пропилом, изо-пропилом, предпочтительно метилом. R и R' вместе означают, например, пентилен. В качестве галоидного заместителя для R в первую очередь применяют фтор. Второстепенным заместителем является хлор. Если R означает галогензамещенный или гидроксилзамещенный алкильный радикал, то он предпочтительно означает фторэтил или оксиэтил. В соответствии с этим группа А означает, например, радикалы скопина, N-этилнорскопина, N-изопропилнорскопина, тропина, N-изопропилнортропина, 6,7-дегидротропина, N-β-фторэтилнортропина, N-изопропил-6,7-дегидронортропина, N-метилгранатолина четвертичные соединения, причем анион предпочтительно означает бром или метансульфонат.
В качестве кислотного остатка
прежде всего следует назвать:
Сложные эфиры тиенилкарбоновой кислоты и аминоспиртов вышеприведенной формулы (I), их продукты кватернизации и кислотно-аддитивные соли имеют, в частности, фармакологическую активность.
Для терапевтического применения особенно пригодны четвертичные соединения, в то время как третичные соединения можно применять не только в качестве активных веществ, но и в качестве промежуточных продуктов.
Предлагаемые соединения представляет собой сильно и долгодействующие антихолинергические агенты. При ингаляции соединений в микрограммовых дозах период активности составляет по меньшей мере 24 часов. Кроме того, их токсичность находится на том же уровне, что и торговый продукт ипратропиумбромид. Но терапевтическое действие является более сильным.
Новые соединения пригодны, например, для лечения хронического обструктивного бронхита и (легкой до среднетяжелой) астмы, а также для лечения вагально обусловленных синусовых бракардий. В то время как при заболеваниях дыхательных путей рекомендуется ингаляция (в частности четвертичных соединений), чем почти полностью исключаются побочные действия, то для лечения синусных брадикардий новые соединения предпочтительно используют внутривенно или орально. При этом оказался выгодным тот факт, что новые соединения практически не оказывают влияния на моторику желудка и кишечника.
Для аппликации предлагаемые соединения перерабатывают вместе с известными вспомогательными веществами и/или носителями в обычные галенические препараты, например, в растворы для ингаляции, суспензии в разжиженных рабочих газах, в содержащие липозомы или пролипозомы препараты, растворы для инъекции, таблетки, драже, капсулы, ингаляционные порошки, предназначенные для применения в стандартных ингаляционных приборах.
Примеры возможных препаратов (данные в вес.):
1. Аэрозоль
активное вещество согласно изобретению 0,005
сорбитантpиолеат 0,1
монофтортрихлорметан и дифтордихлорметан в соотношении 2:3 до 100.
Суспензию наполняют в стандартную емкость с дозировочным клапаном, позволяющим осуществить отдачу аэрозоля в предпочтительном количестве по 50 мкл. По желанию аэрозоль может иметь и более высокую концентрацию активного вещества (например, 0,02 вес.).
2. Таблетки
активное вещество согласно изобретению 0,05
коллоидальная кремниевая кислота 0,95
молочный сахар 65,00
картофельный крахмал 28,00
поливинилпирролидон 3,00
натриевая соль карбоксиметилцеллюлозы 2,00
стеарат магния 1,00.
Компоненты перерабатывают известными приемами в таблетки весом 200 мг.
Полезные свойства новых соединений проявляются, например, при торможении бронхолина у кролика (вызываемого внутривенной дачей ацетилхолина спазма). После внутривенной дачи новых соединений (доза 3 мкг/г внутривенно) максимальное действие достигается по истечении 10 400 минут. По истечении 5 часов тормозящее действие еще не снизилось до 50% то есть период полудействия составляет больше 5 часов, отчасти гораздо больше 5 часов, о чем свидетельствуют нижеприведенные данные по остаточному действию по истечении 5 часов:
Соединение N остаточное действие, в
А 76
Б 76
В 81
Г 61
Д 68
Е 73
Ж 69
Соединения А Ж имеют следующую формулу (см. чертеж)
Примечания:
1. Соединения, где R1 не означает 2-тиенил, представляет собой рацематы.
2. Речь идет о 3α-соединениях.
Для получения новых соединений служат известные способы.
Сложный эфир формулы (IV)
где R1, R2 и Ra имеют вышеуказанные значения, а R'' означает алкил с 1 4 атомами углерода, предпочтительно метил или этил, предпочтительно подвергают переэтерификации аминоспиртом формулы (V).

где m, n и Q имеют вышеуказанные значения,
Q означают группу -NR илиNH, а гидроксильная группа находится в α- или b-положении, в присутствии обычного катализатора переэтерификации и полученное соединение в случае необходимости подвергают кватернизации
a) реакционноспособным монопроизводным формулы Z-(1 - C4-алкил) соответствующего алкана (Z удаляемая группа), если Q'' означает группуNR (R≠H),
или
б) без промежуточного выделения дизамещенным на конце алканом формулы Z-C4 C6-алкилен)-Z, где Z имеет вышеуказанное значение, если "Q" означает группуNH.
Переэтерификацию проводят при нагревании в среде органического растворителя, как, например, толуола, ксилола, гептана, или в расплаве, причем сильные основания, как, метилат натрия, этилат натрия, гидрид натрия, металлический натрий, служат в качестве катализатора. Для удаления выделившегося низшего спирта из равновесия работают при пониженном давлении, в случае необходимости спирт отгоняют в виде азеотропа. Реакцию обычно проводят при температуре, не превышающей 95oС. Часто переэтерификация протекает более выгодно в расплаве. В случае необходимости с использованием основных соединений кислотно-аддитивные соли третичных аминов можно известными приемами переводить в свободные основания. Кватернизацию проводят в среде пригодных растворителей, как, например, ацетонитриле или смеси ацетонитрила и метиленхлорида, предпочтительно при комнатной температуре; при этом в качестве агента кватернизации предпочтительно используют соответствующий алкилгалогенид, например, алкилбромид. Продукты переэтерификации, у которых Q' означает группу NH, служат в качестве исходных веществ для таких соединений, где R и R' вместе означают алкилен с 4 6 атомами углерода. Переведение в третичное и затем в четвертичное соединение проводят при помощи пригодных 1,4-, 1,5- или 1,6-дигалогеналканов без промежуточного выделения.
Исходные вещества, если они не описаны, можно получать известными приемами.
Нижеследующие примеры иллюстрируют получение новых соединений общей формулы (I).
Пример 1. Сложный скопиновый эфир ди-(2-тиенил)гликолевой кислоты.
50,87 г (0,2 моль) сложного метилового эфира ди-(2-тиенил)гликолевой кислоты и 31,04 г (0,2 моль) скопиона растворяют в 100 мл абсолютного толуола и, добавляя 1,65 г (0,071 грамм-атома) натрия несколькими порциями, нагревают до температуры 90oС. При температуре 78 90oC реакционной смеси при давлении 500 мбар отгоняют образовавшийся метанол. Примерно через 5 часов реакции реакционную смесь вмешивают в смесь льда и соляной кислоты. Отделяют кислую фазу, подщелачивают карбонатом натрия и свободное основание экстрагируют метиленхлоридом. После сушки над сульфатом натрия метиленхлорид отгоняют при пониженном давлении и остаток перекристаллизовывают из ацетонитрила; получают бежевые кристаллы (из ацетонитрила) с точкой плавления 149 50oC.
Выход 33,79 г (44,7% теории).
Пример 2. Сложный скопиновый эфир ди-(2-тиенил)гликолевой кислоты.
12,72 г (0,05 моль) сложного метилового спирта ди-(2-тиенил)гликолевой кислоты и 7,76 г (0,05 моль) скопира расплавляют на нагревательной бане с температурой 70oC в вакууме, получаемой с помощью водоструйного насоса. К этому расплаву добавляют 2,70 г (0,05 моль) метилата натрия и реакционную смесь нагревают на нагревательной бане с температурой 70oC в течение часа в вакууме, получаемом с помощью водоструйного насоса, и для завершения реакции нагревают в нагревательной бане с температурой 90oС. Затвердевший расплав поглощают в смеси 100 мл воды и 100 мл метиленхлорида при контроле температуры и метиленхлоридную фазу экстрагируют несколько раз водой. Метиленхлоридную фазу экстрагируют соответствующим количеством разбавленной соляной кислоты. После добавления соответствующего количества карбоната натрия из собранных водных фаз экстрагируют метиленхлоридом сложный скопиновый эфир ди-(2-тиенил)гликолевой кислоты, который сушат над сульфатом натрия. Из высушенного метиленхлоридного раствора обычными примерами получают гидрохлорид. Кристаллы отсасывают, промывают ацетоном и сушат при температуре 35oC и пониженном давлении. Получают желтоватые кристаллы (из метанола), точка плавления: 238 41oC (разложение).
Выход: 10,99 г (53,1% теории).
Гидрохлорид можно проводить в основание обычными приемами.
Пример 3. Сложный скопиновый эфир ди-(2-тиенил)гликолевой кислоты.
38,15 г (0,15 моль) сложного метилового эфира ди-(2-тиенил)гликолевой кислоты смешивают с 23,28 г (0,15 моль) скопина, добавляют 0,34 г (0,015 грамм-атома) натрия и расплавляют на нагревательной бане с температурой 90oC в вакууме, получаемом с помощью водоструйного насоса. Время реакции составляет 2,5 часа. Затем добавляют 100 мл абсолютного толуола и перемешивают при указанной температуре до получения раствора. Реакционный расход охлаждают до комнатной температуры и вмешивают в охлажденную льдом смесь льда и соляной кислоты. Выкристаллизовавшийся гидрохлорид основного сложного эфира отсасывают, последовательно промывают водой, взятой в небольшом количестве, и простым диэтиловым эфиром, взятым в большом количестве. Фазы фильтрата отгоняют и водную фазу экстрагируют простым диэтиловым эфиром. Отсасываемый гидрохлорид суспендируют в (кислой) водной фазе и при контроле температуры и добавлении соответствующего количества карбоната натрия переводят в основание, которое экстрагируют метиленхлоридом. Собранные метиленхлоридные фазы сушат над сульфатом натрия. После отгонки метиленхлорида остается продукт кристаллизации, который очищают активным углем и перекристаллизовывают из ацетонитрила. Получают желтоватые кристаллы (из ацетонитрила) с точкой плавления: 148 149oC. Выход: 39,71 г (70,1% теории).
Аналогично получают сведенные в таблице 1 соединения.
Пример 4. Метобромид сложного скопинового эфира ди-(2-тиенил)гликолевой кислоты.
10,0 г (0,0265 моль) сложного скопинового эфира ди-(2-тиенил)гликолевой кислоты растворяют в смеси, состоящей из 20 мл безводного метиленхлорида и 30 мл безводного ацетонитрила, и смещают с 12,8 г (0,1325 моль) метилбромида (в виде 50% -ного раствора в безводном ацетонитриле) и реакционную смесь оставляют стоять в герметично закрытом реакторе при комнатной температуре в течение 24 часов. В течение этого времени выпадают кристаллы. Их отсасывают, промывают метиленхлоридом и сушат при температуре 35oC и пониженном давлении.
Получают белые кристаллы (из смеси метанола и ацетона) с точкой плавления 217 8oC (разложение) после сушки при температуре 111oC и пониженном давлении.
Аналогично получают сведенные в таблице 2 5 соединения.




Использование: в фармакологии в качестве лекарственных средств. Заявленные соединения получают путем переэтерификации метилового эфира ди-(2-диенил)гликолевой кислоты соответствующим спиртом. Продукт: сложный скопиновый эфир ди-(2-тиенил)гликолевой кислоты, т. пл. 238 - 241oC (разложение) 2 с. и 2 з.п. ф-лы, 5 табл., 1 ил.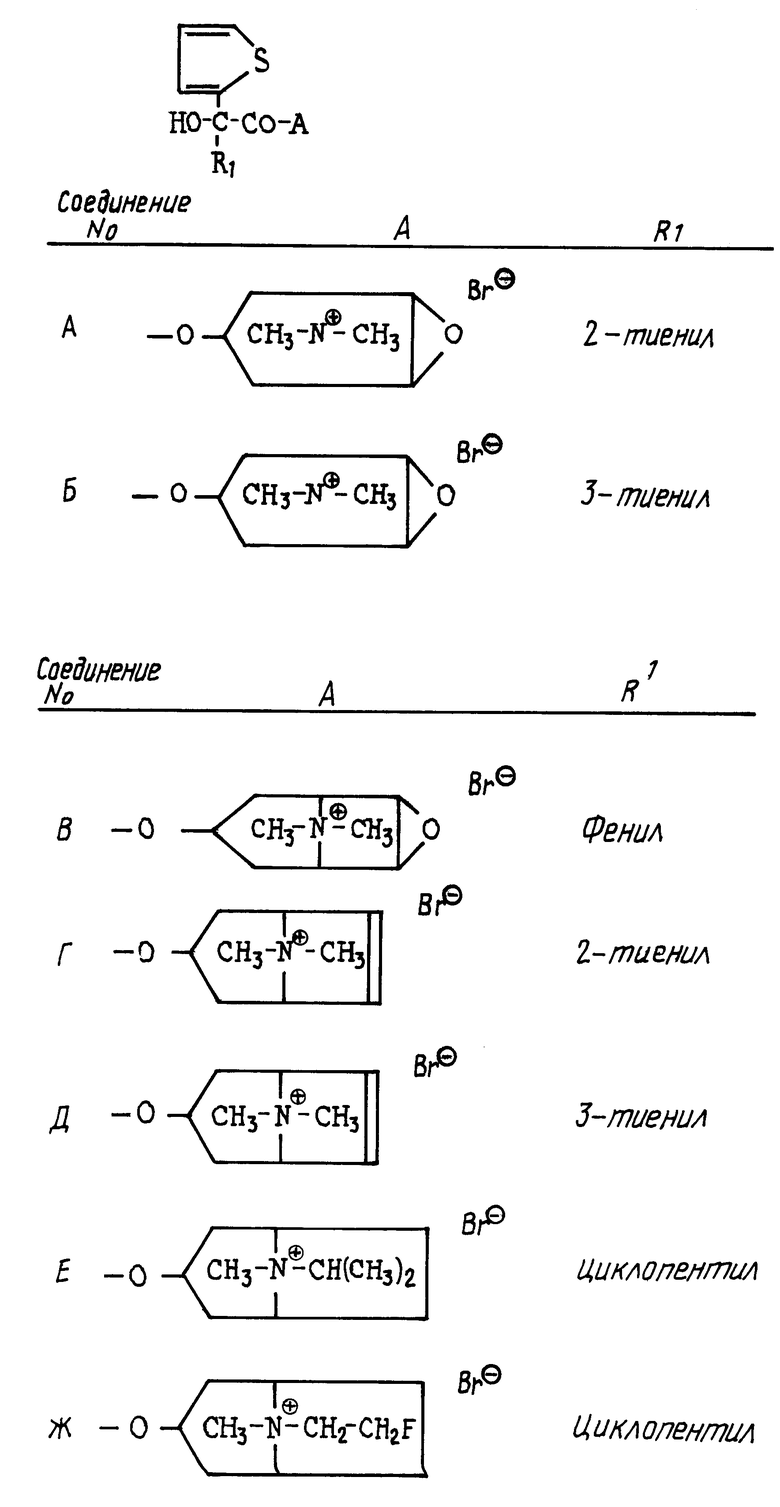
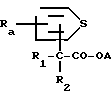
где A группа формулы
где Q группа формул -CH2-CH2, -CH2-CH2-CH2-, -CH=CH- или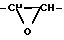
Q' группа NR, где R водород или C1 C4-алкил, незамещенный или замещенный галогеном или гидроксилом, или группа NRR', где R имеет указанное значение, R'- C1 C4-алкил или R и R' вместе образуют C4-C6- алкилен, причем в случае четвертичного соединения к положительному заряду атома азота относится эквивалент аниона,
R1 тиенил, фенил, циклопентил и циклогексил, незамещенные или замещенные метилом, причем тиенил и фенил могут быть также замещены фтором или хлором;
R2 водород, гидроксил, C1 C4-алкоксил или C1 C4-алкил;
R3 водород или метил, при условии, что если A 3-тропанил, R2 гидроксил и R1 2- или 3-тиенил, то Ra- метил,
их продукты кватернизации и кислотно-аддитивные соли, если NR - вторичная или третичная аминогруппа.
где R1, R2 и R3 имеют указанные значения; R'' - C1 C4-алкил,
подвергают взаимодействию с соединением общей формулы III
где Q имеет указанное значение;
O'' группа -NR илиNH,
в присутствии катализатора переэтерификации с последующей, в случае необходимости, кватернизацией реакционноспособным монопроизводным Z(C1-C4-алкил) соответствующего алкана, где Z удаляемая группа, если O'' группаNR, где R≠H,
и выделением целевого продукта в свободном виде, в виде продукта кватернизации или кислотно-аддитивной соли, если R вторичная или третичная аминогруппа.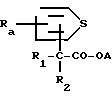
где A группа формулы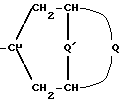
где Q группа формул -CH2-CH2, -CH2-CH2-CH2-, -CH=CH- или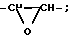
Q группаNR, где R водород или C1 C4-алкил, незамещенный или замещенный галогеном или гидроксилом, или группа NRR', где R имеет указанное значение, R' C1 C4-алкил или R и R' вместе образуют С4-C6-алкилен, причем в случае четвертичного соединения к положительному заряду атома азота относится эквивалент аниона;
R1 тиенил, фенил, циклопентил и циклогексил, незамещенные или замещенные метилом, причем тиенил и фенил могут быть также замещены фтором или хлором;
R2 водород, гидроксил, C1 C4-алкоксил или C1 C4-алкил;
Rа водород или метил при условии, что если A 3-тропанил, R2 гидроксил и R1 2- или 3-тиенил, то Ra метил или его продукт кватернизации или кислотно-аддитивную соль, если NR вторичная или третичная аминогруппа в эффективном количестве.
| Acta Chem | |||
| Scand., 24, N 5, 1590-96, 1970 | |||
| СВЕТОВОД | 1965 |
|
SU215545A1 |
| Устройство для сортировки каменного угля | 1921 |
|
SU61A1 |
| Патент США N 3808263, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1997-02-20—Публикация
1990-09-08—Подача