Соединения группы авермектинов являются потенциальными антигельминтиками и противопаразитарными агентами против внутренних и наружных паразитов. Авермектины природного происхождения описаны в пат. США 4310519 AIbers - Shonberg et al., 22, 23 - дигидроаверкмектины описаны Chabala et al., в пат. США 4199569. Авермектины вводят орально, парентерально или местным способом.
Однако обычные препаративные формы для местного применения не обеспечивают приемлемой эффективности против эктопаразитов, особенно против Chorioptes, блох и клещей. Часто такие препаративные формы неудачны вследствие потери эффективности. Животные после обработки вышеописанными препаративными формами быстро повторно заражались блохами, клещами и подобными паразитами просто при возвращении в среду, зараженную блохами. Кроме того, препаративные формы для местного применения применяемых в настоящее время медицинских препаратов не проявляют эффективность против эндопаразитов, таких как сердечные гельминт и нематоды.
В ветеринарии известно, что длительное высвобождение инсектицида получают при введении инсектицида в полимерную систему. Однако обычные полимерные препаративные формы основаны на испарении активного вещества, но этот тип системы не может быть использован для неиспаряющихся препаратов, см. пат. США NN 38525416 и 4172904. Кроме того, обычные препаративные формы существующих медицинских препаратов требуют периода выведения в несколько недель после применения активного вещества перед тем, как молоко молочных животных может быть использовано человеком.
Краткое описание изобретения.
Это изобретение касается препаративных форм авермектина в виде раствора для местного применения, которые эффективно уничтожают как эктопаразитов, особенно Chorioptes, блох и клещей, так и эндопаразитов, особенно сердечных гельминтов и нематод, у животных, таких как крупный рогатый скот, свиньи и т. д., в течение продолжительного периода вплоть до полных четырех недель, в частности, у домашних животных, таких как кошки и собаки. Заявленные препаративные формы также неожиданно обеспечивают нулевое время задержки отбора молока для использования в случае местного применения противопаразитарных агентов на молочных животных. Препаративные формы получают при использовании в качестве носителя растворителей, таких как вода, спирты, такие как этанол, метанол, изопропанол и другие, эфиры пропиленгликоля, глицериды или их производные.
Кроме активного авермектинового ингредиента и растворителя препаративные формы могут содержать полимер, такой как поливинилпирролидон. Препарат наносится на кожу с помощью полимера, который удерживает его на поверхности кожи после испарения растворителя после применения. Таким образом, объектом этого изобретения является описание такой эктопаразитарной и эндопаразитарной эффективности. Другим объектом изобретения является описание соединений авермектина, которые могут использоваться в препаративной форме. Дополнительным объектом изобретения является описание пути сохранения концентрации активного соединения в молоке молочных животных ниже безопасного уровня концентрации для потребления молока человеком.
Еще одним дополнительным объектом изобретения является описание пути получения длительной эффективности против блох, клещей и сердечных гельминт. Дополнительные объекты будут очевидны после ознакомления со следующим описанием.
Описание изобретения.
Это изобретение состоит из препаративной формы в виде раствора для местного применения на основе глицерида, гликоля или их производных в качестве носителя и авермектинового соединения, которое найдено эффективным для уничтожения как эктопаразитов, так и эндопаразитов. Кроме глицерида, гликоля или их производных и авермектина препаративная форма необязательно может содержать антиоксидант, такой как бутилированный гидроксианизол (ВНА), бутилированный гидрокситолуол (ВНТ) и другие добавки, такие как Crodamol/CAP, глицерин обычный, Tween 80 и другие, смесь воды и/или растворителей с относительно высоким давлением паров, таких как этанол, метанол, изопропанол и другие подобные, и полимерный материал, такой как поливинилпирролидон, поливиниловый спирт и другие подобные.
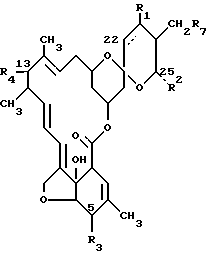
Соединения авермектина, используемые в данных препаративных формах, имеют следующую общую структуру: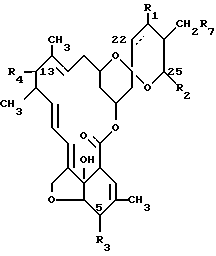
где прерывистая линия показывает простую или двойную связь у 22, 23 - положениях;
R1 является водородом или гидрокси при условии, что R1 присутствует только, когда прерывистая линия показывает простую связь;
R2 является алкилом с от одного до шести атомами углерода или алкенилом с от 3 до 6 атомами углерода, или циклоалкилом с от 3 до 8 атомами углерода;
R3 представляет собой гидрокси, метокси или =NOR5, где R5 означает водород или низший алкил;
R7 описывает водород, гидрокси или низший алкил;
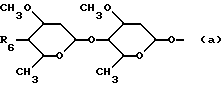
R4 представляет собой водород, гидрокси, полис C1 - C6-алкокси или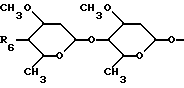
где
R6 означает гидрокси, амино, моно- или ди-C1-C6 алкиламино или C1-C6 алканоиламино.
Термин "низший алкил", используемый в настоящей заявке, отражает алкильные группы с прямой или разветвленной цепью, которые содержат 1 - 5 атомов углерода. Примерами таких алкильных групп являются метил, этил, пропил, изопропил, бутил, втор-бутил, пентил и другие подобные.
Термин "низший алканоил" включает алканоил группы, содержащей от одного до пяти атомов углерода в прямой или в разветвленной цепи. Примерами таких алканоилгрупп являются формил, ацетил, пропенил, бутирил, валерил и другие подобные.
Термин "галоген" включает атомы галогена: фтор, хлор, бром и иод.
Термин "полиалкокси" включает метоксиметокси, 2-метоксиэтокси, (2-метоксиэтокси) - метокси, [2-(2-метоксиэтокси)этокси]метокси; и другие подобные.
Используемое в настоящем изобретении родственное семейство природных продуктов известно как мильбемицины. Мильбемицины имеют ту же макроциклическую кольцевую структуру, что и авермектины, но они не содержат заместителя в положении 13 (R4 = водороду), а содержат метил или этилгруппу в положении 25 (R2 = метил или этил предпочтительнее, чем изопропил или втор-бутил, как в авермектинах). Мильбемицины в условиях ферментации, используемые при их получении, описаны в пат. США N 3950360. Близко родственные 13 - деоксиавермектин агликоны получают химической модификацией природных авермектинов, они описаны в пат. США N 4173571.
Одно предпочтительное воплощение (EI) этого изобретения содержит препаративную форму для местного применения в виде раствора при использовании глицерида, гликоля или их производных в качестве носителя и авермектинового соединения, которое найдено эффективным для уничтожения как эктопаразитов, особенно Chorioptes, так и эндопаразитов, при этом концентрация активного соединения в молоке молочных животных остается ниже адекватной концентрации, пригодной для потребления человеком, т.е. обеспечивается нулевое время задержки для потребления молока при местном применении эндектоцидов (концентрация в молоке 4-"ацетоламина-4" - деоксиавермектина BI (L-653648) при нулевом задерживании в молоке составляет (48 нг/мл).
Носителями являются олеоиловый спирт, пропиленгликоль и его эфиры, такие как пропилен дикаприлат/дикапринат, лаурат пропиленгликоля и другие подобные, гликолевые эфиры, такие как моноэтиловый эфир этиленгликоля, монобутиловый эфир диэтиленгликоля, диэтиловый эфир этиленгликоля и другие подобные, и глицериды, такие как PEG-6 триглицерид каприловой/капроновой кислот, диглицерилсукцинат каприловой/каприновой кислот, полигликолизированные глицериды и другие подобные, предпочтительно пропилен каприлат/каприлат или каприлат/капринат глицерид, доступные под такими торговыми названиями, как Miglyol 810 (триглицериды каприловой/каприновой кислот), Miglyol 812 (триглицериды каприловой/каприновой кислот), Miglyol 818 (триглицериды каприловой/каприновой/линолевой кислот), Miglyol 829 (триглицериды каприловой/каприновой/диянтарной кислот) и Miglyol 840 (дикаприлат/дикапраты пропиленгликоля), Sofrigen (PEG-6 диглицерид каприловой/каприновой кислот) и Labrasol ® (PEG-8 каприлат/капринат глицерид). Знак (/) в пропилен дикаприлате/дикапрате и PEG-6 в триглицериде каприловой/каприновой кислот означает смесь двух компонентов в соотношении 65-80/15-30.
Вышеприведенные носители придают препаративной форме хорошую проникающую способность и намазывающую способность активного соединения даже при низких температурах.
Предпочтительные авермектиновые соединения E1 имеют предпочтительную структурную формулу: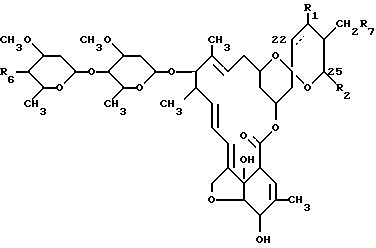
где пунктирная линия означает простую связь;
R1 представляет собой водород;
R2 является изопропилом или втор-бутилом;
R6 означает гидрокси, амино, моно- или ди-(C1-C6)алкиламино или С1-С6 алканоиламино;
Примерами предпочтительных соединений текущей EI препаративной формы являются:
4''-кетоавермектин B1;
4''-кетоавермектин P2;
4''-кето-22,23-дигидроавермектин B1;
4''-кето-22,23-дигидроавермектин B2;
4''-деокси-4''-аминоавермектин B1;
4''-деокси-4''-аминоавермектин B2;
4''-деокси-4''-амино-22,23-дигидроавермектин B1;
4''-деокси-4''-амино-22,23-дигидроавермектин B2;
4''-деокси-4''-ацетиламиноавермектин B1;
4''-деокси-4''-ацетиламиноавермектин B2;
4''-деокси-4''-ацетиламино-22,23-дигидроавермектин B1;
4''-деокси-4''-ацетиламино-22,23-дигидроавермектин B2;
4''-деокси-4''-диметиламиноавермектин B1;
4''-деокси-4''-диметиламиноавермектин B2;
4''-деокси-4''-диметиламино-22,23-дигидроавермектин B1;
4''-деокси-4''-диметиламино-22,23-дигидроавермектин B2;
4''-деокси-4''-п-хлорбензолсульфониламино-22,23- дигидроавермектин B1;
4''-деокси-4''-п-хлорбензолсульфониламино-22,23- дигидроавермектин B2;
4''-деокси-4''-(2-метилбензолсульфониламино)авермектин B1;
4''-деокси-4''-(2-метилбензолсульфониламино)авермектин B2.
Соединения "b",содержащие 25-изопропилгруппу, нет необходимости отделять от соответствующего "a" соединения с 25-вторбутилгруппой. Соединения обычно выделяются в виде смеси двух соединений, содержащих по крайней мере 80% вторбутильного соединения и не более 20% изопропильного соединения. Таким образом, ссылки в текущей заявке на "a" соединения, такие как B1a, A1a и другие подобные, истолковываются на самом деле как содержащие некоторую часть соответствующего "b" соединения. Или же иногда смесь представляется ссылкой на B1 или B2 соединения или разделением "a" соединения и "b" соединения чертой (/), например, так B1a/B1b; B2a/B2b и другие подобные. Кроме того, продуктами синтетических методик, таких как рецемизация или эпимеризация, методик, известных по предшествующим работами, могут быть смеси стереоизомеров. В частности, стереоизомеры по 13 и 23-положениям могут ориентироваться такими группами, представляющими или α-, или β-, которые располагаются, соответственно, ниже или выше основной плоскости молекулы. В каждом случае как α-, так и β- конфигурации и по другим положениям включаются в область этого изобретения.
В случае препаративной формы авермектина для местного применения невозможно обеспечить препаративную форму, которая бы обладала приемлемой эффективностью против эктопаразитов, особенно против Chorioptes. Кроме того, имеющиеся в настоящее время препаративные формы для местного применения не обеспечивают нулевого времени задерживания для потребления молока при применении эндектоцидов, что таким образом мешает использованию таких соединений на животных, продуцирующих молоко.
E1 текущего изобретения дает преимущества препаративных форм в виде растворов для местного применения, которые обеспечивают эффективную обработку животных и защиту их от эндопаразитов и эктопаразитов, особенно Chorioptes, и в то же самое время сохраняют концентрацию активного вещества в молоке молочных животных ниже безопасного для потребления человеком уровня. Дополнительные преимущества этого изобретения включают: препаративная форма не огнеопасна, не смывается быстро дождем, обладает хорошим размыванием, используются при низких температурах и хорошо совмещаются с применяемыми в настоящее время дозирующими устройствами.
E1 может содержать авермектиновое соединение и гликолевый или глицеридовый носитель в качестве единственных ингредиентов. Препаративные формы обычно получают введением безопасного и эффективного количества от 0,005 до 10 мас.% авермектинового компонента, более предпочтительно от 0,01 до 5 мас. %. Наиболее предпочтительно использовать препаративную форму, содержащую приблизительно 0,5% авермектива. При использовании предпочтительной величины дозы примерно 5 мл для обработки животного весом 50 кг препаративная форма содержит от примерно 1,0 до 50 мг авермектинового соединения на мл раствора. Гликолевый или глицеридный носитель добавляют к препаративной форме от примерно 40 до 100% q.s. об/об (q.s.=количество, необходимое для достижения общих 100% об/об).
Наиболее предпочтительная препаративная форма для E1 содержит в добавление к гликолю, глицериду или их производным и соединению авермектина, антиоксидант, такой как пропилгаллат ВНА (бутилированный гидроксианизол), ВНТ (бутилированный гидрокситолуол), монотиоглицерол и другие подобные, предпочтительно ВНТ. Антиоксиданты обычно добавляют к препаративной форме в количестве от 0,005 до 1,0% (мас/об). Также могут использоваться добавки, такие как Crodamol САР, глицерин обычный, Tween 80 пропиленгликоль и другие подобные, предпочтительно Crodamol САР. Обычно добавки добавляют к препаративной форме в количестве вплоть до 60% объема носителя, гликоля или глицерида, предпочтительно вплоть до 40% объема носителя.
E1 получают при растворении соединения авермектина в примерно 50 - 100% объема вышеприведенного носителя, затем доводят до объема 100% при добавлении конечного объема носителя или добавок. Антиоксидант и добавки могут смешиваться с вышеуказанными носителями до смешения с авермектином или до добавления в виде конечного объема растворителя.
Для того, чтобы можно было более полно понять E1 воплощение изобретения, приводится следующий пример. Он не ограничивает изобретения.
Пример изобретения.
Препаративные формы этого изобретения зависят от определенного авермектинового соединения и обработки. Авермектин растворяют в примерно 50% гликолевого или глицеридного носителя. После растворения необязательно добавляют антиоксидант и/или добавку, затем объем до 100% с конечным объемом гликолевого или глицеридного носителя. Раствор смешивают до получения гомогенного раствора. Обычно смешение достаточно проводить при комнатной температуре (15 - 25oC), однако, если необходимо, может быть полезным нагревание вплоть до 50oC. Следующие примеры, не ограничивая изобретение, предлагают композиции настоящего изобретения, которые обычно формулируются смешением компонентов, как показано выше.
Композиция I
4''-ацетиламино-4''-деоксиавермектин B1 - 0,5% мас/об
BHT - 0,01% мас./об
Crodamol CAP - 10,0% об/об
MigIyol 840 (q.s.) - 100,0% об/об
Композиция II
4''-ацетиламино-4''-деоксиавермектин B1 - 0,5% мас./об
BHT - 0,01% мас./об
Miglyol 840 (q.s.) - 100,0% об/об
Композиция III
4''-ацетиламино-4''-деоксиавермектин B1 - 0,5% мас./об
BHT - 0,01% мас./об
Изопропилмиристат - 10,0% об/об
Miglyol 840 (q.s.) - 100,0% об/об
Композиция IV
4''-ацетиламино-4''-деоксиавермектин B1 - 0,5% мас/об
Триацетин - 50,0% об/об
Miglyol 840 (q.s.) - 100,0% об/об
Композиция V
4''-ацетиламино-4''-деоксиавермектин B1 - 0,5% мас/об
Softigen 767 - 65,0% об/об
Miglyol 840 - 25,0% об/об
Этанол (q.s.) - 100,0% об/об
Композиция VI
4''-ацетиламино-4''-деоксиавермектин - 0,5% мас/об
Softigen 767 - 65,0% об/об
изопропанол (q.s.) - 100,0% об/об
Композиция VII
4''-ацетиламино-4''-деоксиавермектин B1 - 0,5% мас/об
ВНТ - 0,01% мас/об
Dowano1 DB (q.s.) - 100,0% об/об
Crodamol CAP является торговым названием смеси изопропилмиристата, цетилоктаноата и стерилоктаноата; Dowanol DB - торговое название бутилового эфира диэтиленгликоля.
E1 пример II.
Приведенные ниже данные показывают концентрацию авермектина (нг/мл) в молоке коров после местного применения некоторых из вышеприведенных препаративных форм, концентрация авермектина сохраняется ниже 48 нг/мл, что является концентрацией авермектина в молоке, требуемой для нулевого задерживания использования молока.
Концентрация 4''-ацетиламино-4''-деоксиавермектина B1 (нг/мл) в молоке коров после местного применения препарата. Обработка A: Miglyol 840/ВНТ/500 мкг/кг.
Обработка B: Триацетин/Miglyol 840 (50/50) /500 мкг/кг (см. табл. 1-7).
E1 пример III.
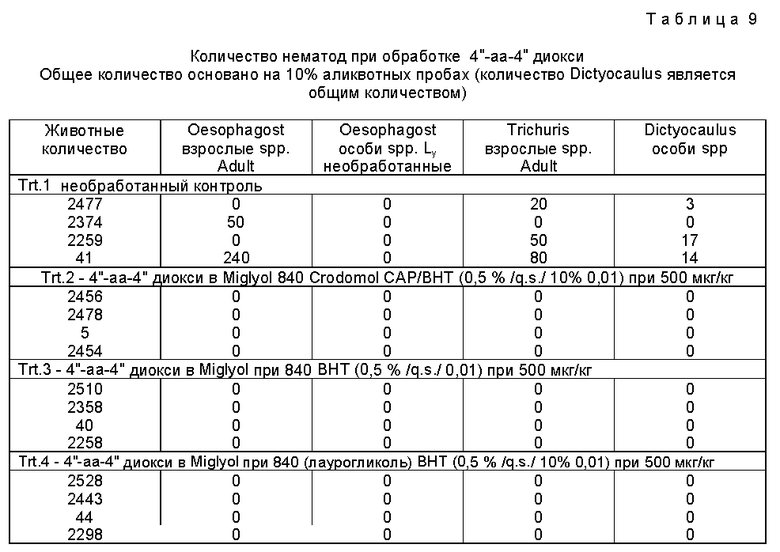
Для оценки некоторых из вышеприведенных препаративных форм проводят испытания их эффективности с Chorioptes и ключевыми эндопаразитами. В каждом опыте, оценивающем Chorioptes, четыре коровы заражают Chorioptes bovis на день - 1 и проводят обработку на день 0. В опытах, оценивающих эндопаразитов, животные заражаются Oelophagosfamum и Trichuris, Dictyocaulus в 17,7 и 7 день перед обработкой препаративной формой. Результаты приведены в табл. 8,9.
Другое предпочтительное воплощение (E2) текущей препаративной формы включает препаративную форму в растворе для местного применения на основе смеси растворителей из воды и/или растворителей с относительно высоким давлением паров, таких как этанол, метанол, изопропанол, ацетон и другие подобные, более предпочтительно этанол, полимерного материала, такого как поливинилпирролидон, поливиниловый спирт, производные целлюлозы, такие как метилцеллюлоза, этилцеллюлозы, карбоксиметилцеллюлоза и гидроксиэтилцеллюлоза и другие подобные, более предпочтительно поливинилпирролидон (молекулярная масса от примерно 20000 до 65000, предпочтительно 45000), замещенные производные протеинов кожи или волос, такие как гидролизованные протеины пшеницы, гидролизованные животные протеины, производные желатина, производные коллагена и другие подобные, спиртовые растворимые сополимеры, такие как акрилаты/трет-октилпропенамидный сополимер и другие подобные, и катионные четвертичные аминные соли и другие подобные. Форма обладает эффективностью, которая продлевается вплоть до полных четырех недель. Полимерный материал помогает сохранить препарат на поверхности кожи более длительный период при помощи того, что препарат остается на поверхности кожи после того, как растворители упариваются после применения. Оставшийся авермектин и полимер не изменяют внешнего вида волосяного покрова животных и авермектин высвобождается диффузией и/или эрозией полимера.
Предпочтительные соединения авермектина E2 имеют следующую структурную формулу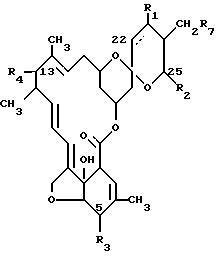
где
R1, R2 и R3 описаны выше;
R4 является водородом, гидрокси или полиалкокси;
штриховая линия показывает простую или двойную связь при 22, 23-положении, при условии, что R2 является гидрокси, только когда штриховая линия показывает простую связь.
Примерами предпочтительных соединений настоящего изобретения являются:
4'' - кетоавермектин B1;
4'' - кетоаеврмектин B2;
4'' - кето- 22, 23 - дигидроавермектин B1;
4'' - кето- 22, 23 - дигидроавермектин B2;
4'' - деокси-4'' - аминоавермектин B1;
4'' - деокси-4'' - аминоавермектин B2;
4'' - деокси-4'' - амино-22,23 - дигидроавермектин B1;
4'' - деокси-4'' - ацетиламиноавермектин B1;
4'' - деокси-4'' - ацетиламино авермектин B2;
4'' - деокси-4'' - ацетиламино- 22,23 - дигидроавермектин B1;
4'' - деокси-4'' - ацетиламино- 22,23 - дигидроавермектин B2;
4'' - деокси-4'' - диметиламиноавермектин B1;
4'' - деокси-4'' - диметиламиноавермектин B2;
4'' - деокси-4'' - диметиламино- 22,23 - дигидроавермектин B1;
4'' - деокси-4'' - диметиламино- 22,23 - дигидроавермектин B2;
4'' - деокси-4'' - п-хлорбензолсульфониламино- 22,23 - дигидроавермектин B1;
4'' - деокси-4'' - п-хлорбензолсульфонил- 22,23 - дигидро-13 - О-[(2-метоксиэтил) метил] авермектин B1 агликон (далее упоминается как 13-О-MEM AVM);
4'' - деокси-4'' - (2 - метилбензолсульфониламино) авермектин B1;
4'' - деокси-4'' - (2 - метилбензолсульфониламино) авермектин B2;
13-эпи-О- (метоксиметил)-22,23 - дигидроавермектин B1 агликон (далее упоминается как 13-О-MOM AVM).
Наиболее предпочтительным соединением является 22,23-дигидро-13-О-[(2-метоксиэтокси)метил] авермектин B1 агликон (упоминается далее как 13-О-MEM AVM).
Препаративная форма авермектина в формах для местного применения не может обеспечить препаративную форму, которая обеспечивает превосходную длительную эффективность против эктопаразитов, особенно против блох и клещей. Кроме того, применяемые в настоящее время препаративные формы для местного применения не обеспечивают достаточной эффективности против эндопаразитов, особенно против сердечного гельминта и нематод.
E2 воплощение текущей препаративной формы дает преимущества препаративной формы в виде раствора для местного применения, которая обеспечивает обработку животных с длительным эффективным действием и защиту их от эндопаразитов и эктопаразитов, особенно блох, клещей, чесоточных клещей, анкилостомы, аскарид и сердечного гельминта. Дополнительным преимуществом этого изобретения является то, что препаративная форма вытесняется не быстро при общении с животными, она хорошо размазывается и используется даже при низких температурах.
E2 воплощение настоящей препаративной формы может содержать соединение авермектина, спирт, воду и полимер в качестве единственных ингредиентов. Препаративные формы обычно получают введением авермектина в количестве от примерно 0,005% мас. до примерно 30% от общего состава, предпочтительно от 0,1 до 10% мас. и более предпочтительно примерно 5% мас. активного ингредиента. При предпочтительной дозе примерно 0,5 - 50 мг/кг препаративную форму применяют в дозе 0,05 - 4,0 мг/кг веса тела. Полимер присутствует в составах настоящего изобретения в количествах, изменяющихся от примеров 0% до 20% мас./об., предпочтительно от примерно 0,5 до 10% мас./об. по весу общей композиции и вплоть до 95% объема спирта, q.s. до 100% воды.
Предпочтительное E2 воплощение содержит в дополнение к полимеру, спирту, воде и соединению авермектина дополнительные ингредиенты, такие как антиоксиданты и гликоль, глицериды, гликолевые эфиры и их производные, указанные выше. Антиоксиданты обычно добавляют к препаративной форме в количестве от 0,005 до 1,0% (мас./об.), они могут быть пропилгаллатом, BНА (бутилированным гидроксианизолом), BHT (бутилированным гидрокситолуолом), монотиоглицерин и другие подобные, предпочтительно BHT.
E2 препаративную форму получают растворением соединения авермектина в требуемом объеме спирта. Затем антиоксидант и один из полимерных материалов, перечисленных выше, растворяют в смеси спирт/авермектин, после чего объем доводят до 100% добавления оставшегося объема воды. Раствор перемешивают до гомогенного состояния. Или BHT , или полимер, или оба сразу могут добавляться до внесения соединения авермектина.
Следующие примеры приводятся для того, чтобы наиболее полно можно было бы понять E2 воплощение изобретения. Они не ограничивают изобретения.
Примеры E2 изобретения.
E2 препаративные формы этого изобретения, которые могут использоваться, зависят от отдельного соединения авермектина и обработки. Для испытания эффективности E2 препаративных форм против блох и клещей получены следующие композиции:
Композиция VIII
13-О- MEM AVM - 0,3% мас/об
Поливинилпирролидон - 0,5% мас/об
Cremophor RH-40 - 1,0% мас/об
Безводный (денатурированный) этанол - 40,0% об/об
Softigen 767 - 20,0% об/об
Вода (q.s.) - 100,0% об/об
Композиция IX
13-О-MEM AVM - 0,3% мас/об
Поливинилпирролидон - 5,0% мас/об
Вода (q.s.) - 100,0% об/об
BHT - 0,01% мас/об
Композиция X
13-О-MOM AVM - 5,0% мас/об
Поливинилпирролидон - 5,0% мас/об
Безводный этанол - 90,0 об/об
Вода (q.s.) - 100,0 об/об
BHT - 0,01; мас/об
Композиция XI
13-О-MEM AVM - 0,6% мас/об
Поливнилпирролидон - 5,0% мас/об
Безводный этанол - 75,0% об/об
Вода (q.s.) - 100,0% об/об
Витамин E - 0,02% об/об
Композиция XII
13-О-MEM AVM - 0,6% мас/об
Гидролизованный протеин пшеницы - 3,0 мас/об
Безводный этанол - 90,0% об/об
Вода (q.s.) - 100,0% об/об
Витамин E - 0,02% об/об
Композиция XIII
13-О-MEM AVM - 0,6% мас/об
Ethocel - 2,0% мас/об
Безводный этанол - 90,0% об/об
Вода (q.s.) - 100,0% об/об
Витамин E - 0,02% об/об
Композиция XIV
13-О-MEM AVM - 0,6% мас/об
Поливинилпирролидон - 5,0% мас/об
Безводный этанол - 80,0% об/об
Вода (q.s.) - 100,0% об/об
Витамин E - 0,002% об/об
Miglyol - 0,5% об/об
Композиция XV
13-О-MEM AVM - 0,6% мас/об
Акрилаты/трет-октилпропенамидный сополимер - 1,0% мас/об
Поливинилпирролидон - 2,0% мас/об
Безводный этанол - 80,0% об/об
Вода (q.s.) - 100,0% об/об
Витамин E - 0,02% об/об
Softigen 767 торговое название PEG-6 каприлат/капринат глицерида, Cremophor RH-40 - торговое название смеси полиэтиленглицерина и гликоль оксистеарата и Ethocel - торговое название этилцеллюлозы.
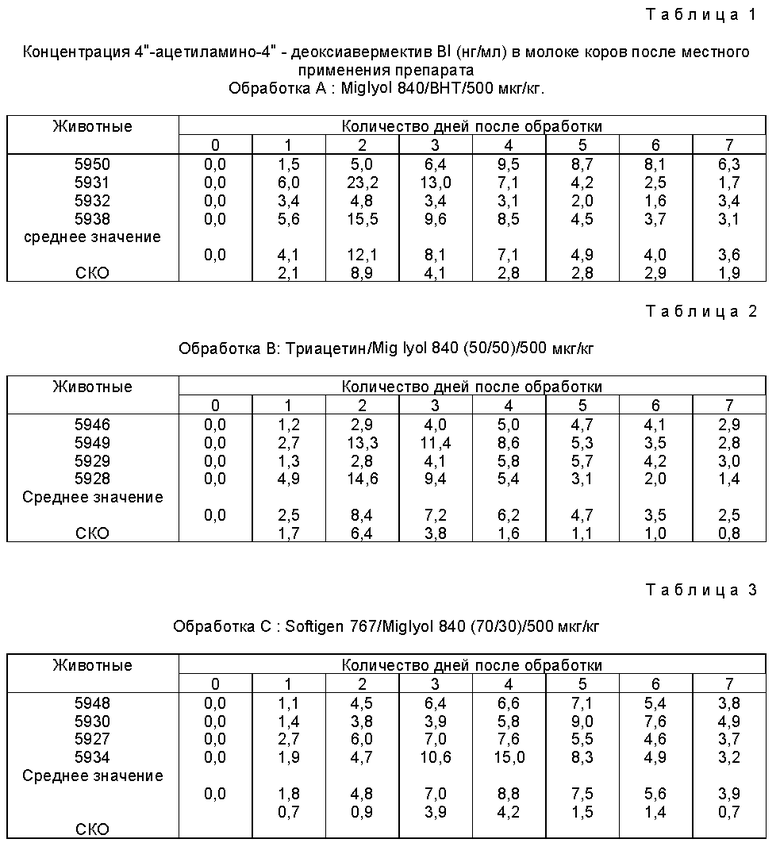
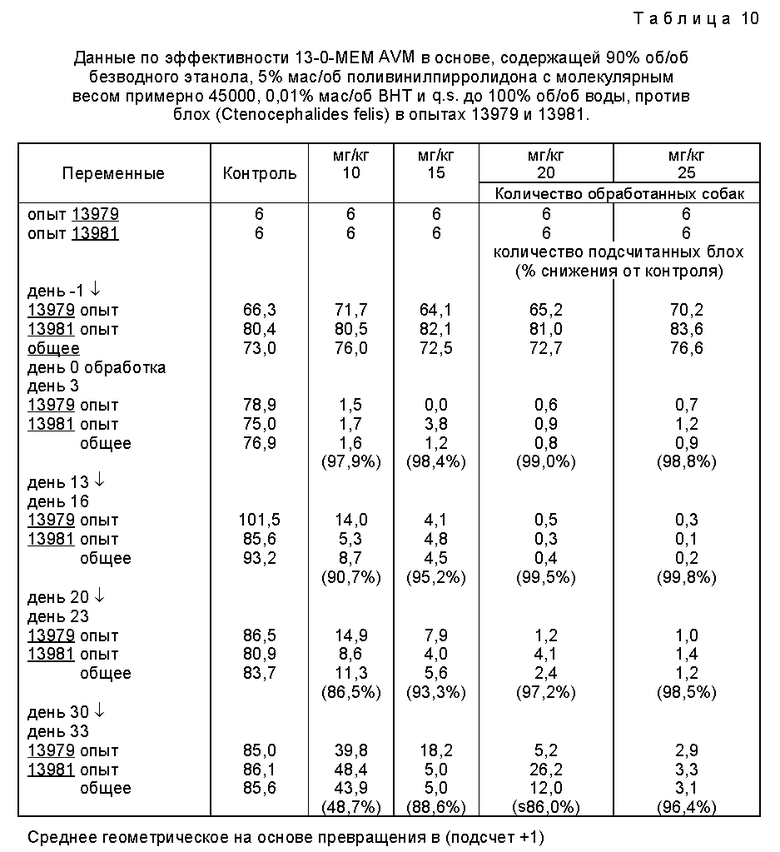
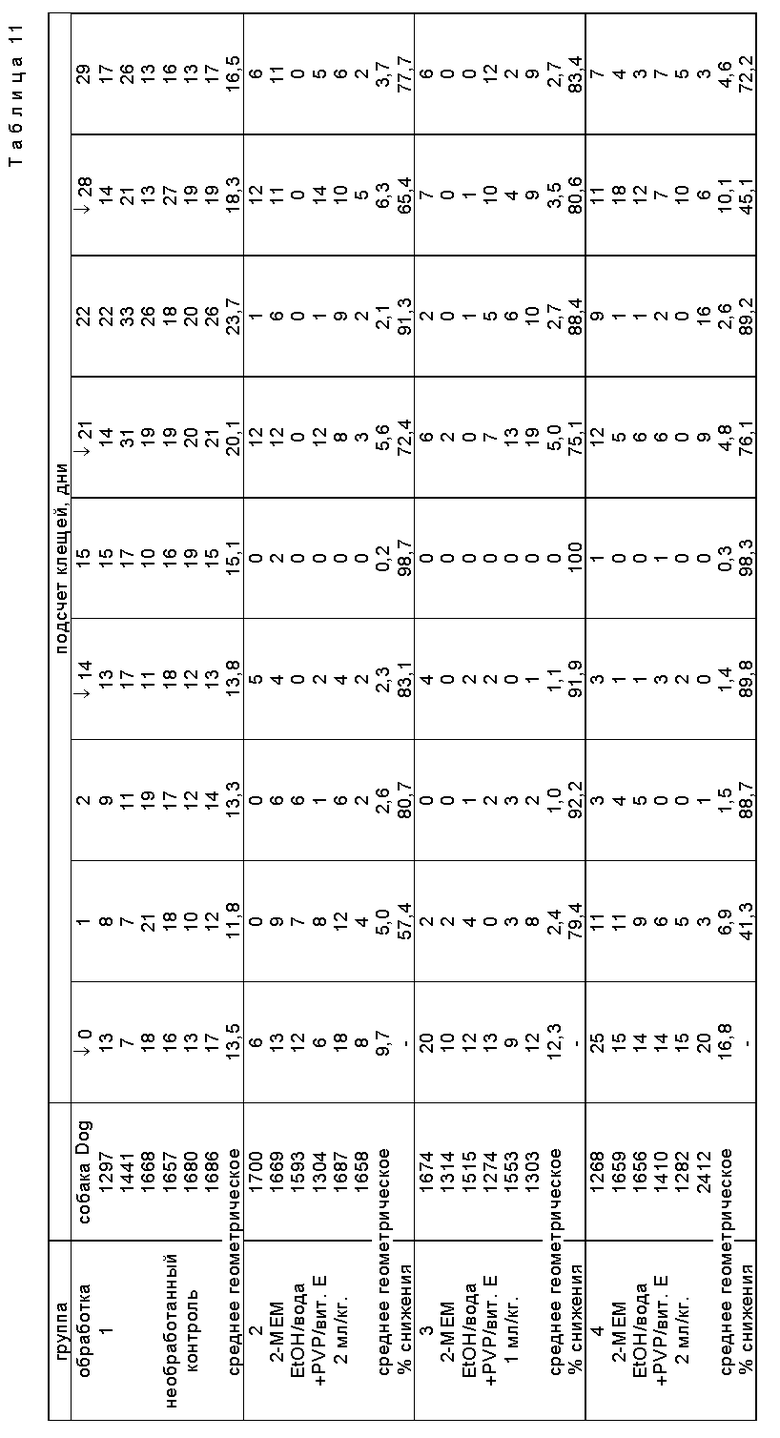
Вышеприведенную композицию X применяли местно во многих местах, обычно 2 - 6 точках, расположенных равностоящее между шеей и хвостом по спине зараженных блохами собак. Подсчет проводили расчесыванием волос, удалением и подсчетом живых паразитов на собаке в определенное время. Наблюдаемое уничтожение блох при разном количестве 13-О-MEM AVM приведено в табл. 10, где 60 собак подразделялись на четыре группы обработки. Собаки заражались 100 некормленными взрослыми блохами, обозначенными нижней стрелкой 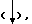 которая эквивалента трем дням перед проведением подсчета блок. Обработку проводили в день - 0. Табл. 11 суммирует результаты подобного теста, оценивающего эффективность композиции, содержащей 13-О-МЕМ AVE (названный 2-MEM) в различных формах, при обработке клещей.
которая эквивалента трем дням перед проведением подсчета блок. Обработку проводили в день - 0. Табл. 11 суммирует результаты подобного теста, оценивающего эффективность композиции, содержащей 13-О-МЕМ AVE (названный 2-MEM) в различных формах, при обработке клещей.
Настоящие препаративные формы могут использоваться для местного применения на теплокровных животных для обеспечения долгодействующих обработки и защиты против эндопаразитов и эктопаразитов или локально в месте заражения, или в многочисленных точках, обычно 2-6 точках, (многоточечное применение), вдоль спины домашних и комнатных животных, таких как крупный рогатый скот, овцы, кошки, собаки и другие подобные.
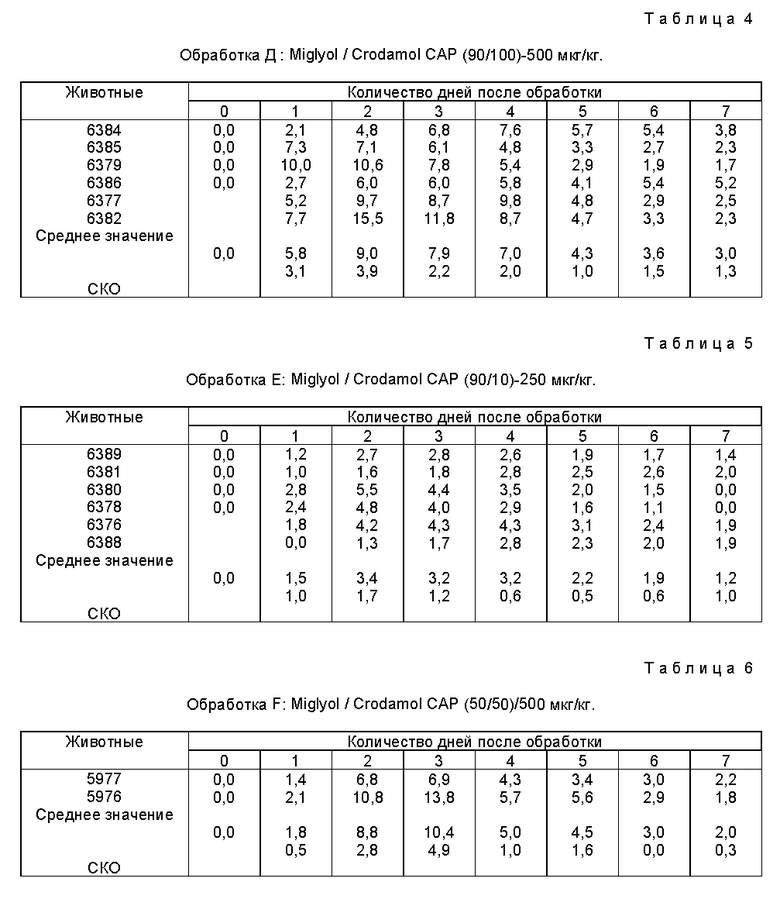
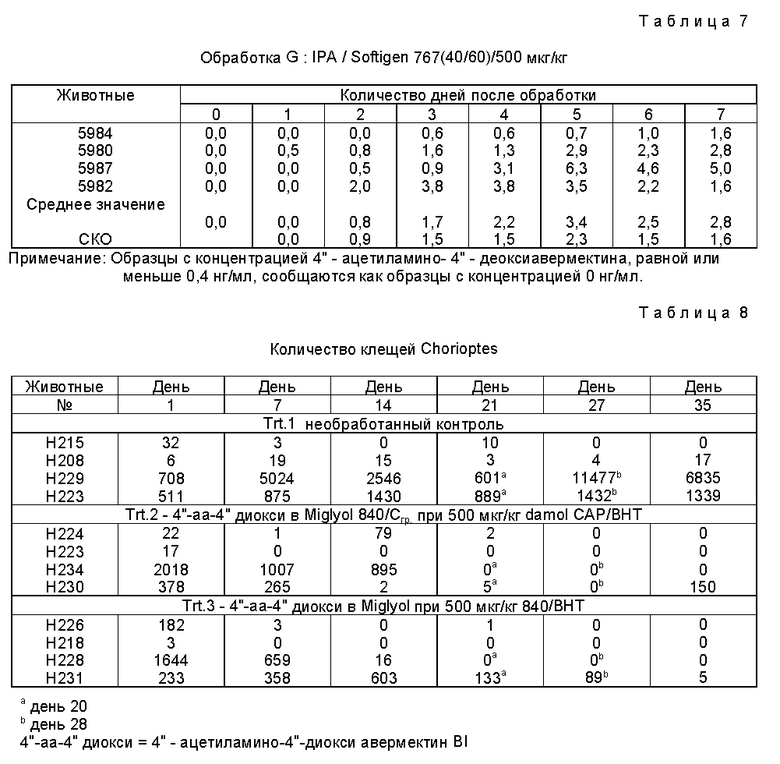
Препаративная форма в виде раствора для местного применения для обработки животных против эндо- и эктопаразитов включает аквермектины в качестве активного ингредиента и по крайней мере 50% гликоля, глицерида или полимерный материал. В качестве авермектина содержит соединение формулы I, где штриховая линия показывает простую или двойную связь в 22, 23 - положениях; R1 - водород или гидрокси; R2 - C1-C6-алкил или С3-C6-алкенил; R3 - гидрокси, метокси или =NOR5; R5 - водород или низший алкил; R7 - Н, гидрокси или низший алкил; R4 - Н, гидрокси, С1-C6-полиалкокси или остаток формулы (a), R6 -гидрокси, амино, моно- или ди(С1-C6)алкиламино или С1-C6-алканоиламино. Препаративная форма обеспечивает превосходную эффективность против эндопаразитов и эктопаразитов в сравнении с обычными препаративными формами и сохраняет концентрацию активного соединения в молоке молочных животных ниже безопасного для потребления человека уровня. 7 с. и 11 з.п. ф-лы, 11 табл. 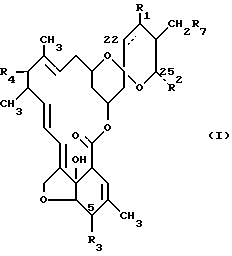
где штриховая линия показывает простую или двойную связь в 22,23-положениях;
R1 является водородом или гидрокси, при условии, что R1 присутствует только когда штриховая линия представляет собой простую связь;
R2 означает алкил от 1 до 6 атомов углерода, или алкенил от 3 до 6 атомов углерода, или циклоалкил от 3 до 6 атомов углерода;
R3 представляет собой гидрокси, метокси или =NOR5, где R5-водород или низший алкил;
R7 является водородом, гидрокси или низшим алкилом,
R4 означает водород, гидрокси, C1-C6-полиалкокси или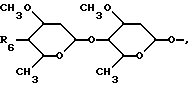
где R6 представляет собой гидрокси, амино, моно- или ди (C1-C6)-алкиламино или (C1 C6)-алканоиламино,
в количестве 0,005-10 мас.%/об, в качестве гликолевого или глицеридного эфира - пропилендикаприлат/дикапринат или триглицерид каприловой/ каприновой кислот - 40-99%q.s.об/об. и 0,005-1 мас.%/об. антиоксиданта.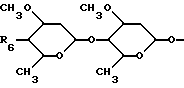
3. Форма по п.1, отличающаяся тем, что содержит от 0,01 до 5 мас.%об. авермектинового соединения.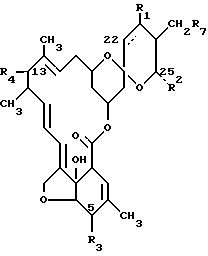
где штриховая линия показывает простую или двойную связь 22, 23 - положениях;
R1 является водородом или гидрокси, при условии, что R1 присутствует только, когда штриховая линия представляет собой простую связь;
R2 означает алкил от 1 до 6 атомов углерода, или алкенил от 3 до 6 атомов углерода, или циклоалкил от 3 до 6 атомов углерода;
R3 представляет собой гидрокси, метокси или =NOR5, где R5 водород или низший алкил,
R7 является водородом, гидрокси или низшим алкилом;
R4 означает водород, гидрокси, поли-C1-C6-алкокси или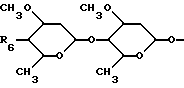
где R6 представляет собой гидрокси, амино, моно- или диC1-C6-алкиламино или C1-C5-алканоиламино.
16, Препаративная форма местного действия для прямого применения на коже животного для эффективной обработки заражения паразитами, содержащая соединение авермектина, антиоксидант и носитель, отличающаяся тем, что в качестве авермектина содержит 5,0 мас.%/об. 22,23-дигидро-13-0-[( 2-метоксиэтокси)метил] авермектина, В1 агликон, в качестве носителя содержит 90 об. %/об. этанола q.s. до 100% с водой, в качестве антиоксиданта содержит 0,01 мас.%/об. бутилированного гидрокситолуола (ВНТ) и дополнительно содержит 5,0 мас.%/об. поливинилпирролидона с мол.м. 45000.
| СПОСОБ И УСТРОЙСТВО ДЛЯ ПРЕДВАРИТЕЛЬНОГО СБРОСА ВОДЫ В СИСТЕМАХ СБОРА ПРОДУКЦИИ НЕФТЕДОБЫВАЮЩИХ СКВАЖИН | 1997 |
|
RU2135886C1 |
| МНОЖИТЕЛЬНО-ДЕЛИТЕЛЬНОЕ УСТРОЙСТВО | 1972 |
|
SU432494A1 |
| ВОДОНАГРЕВАТЕЛЬНАЯ ГЕЛИОУСТАНОВКА | 1991 |
|
RU2042893C1 |
| 0 |
|
SU301806A1 | |
| US 4897338, 1990 | |||
| Нефтяной конвертер | 1922 |
|
SU64A1 |
| US 4454113, 1984 | |||
| US 4939166, 1990 | |||
| Седых А.С | |||
| и др | |||
| Авермектины-новая группа инсектицидов и нематицидов: Обз.инф | |||
| - М.:НИИТЭХим, 1990, 34 с. | |||
Авторы
Даты
1999-01-10—Публикация
1994-04-28—Подача