Процесс свертывания крови и тромбообразование вызывается комплексным протеолитическим каскадом, ведущим к образованию тромбина. Тромбин протеолитически удаляет активационные пептиды из Aα- и Bβ-цепей фибриногена, который растворяется в плазме крови, инициируя образование нерастворимого фибрина.
Антикоагуляция обычно достигается путем введения гепаринов и кумаринов. Парентеральное фармакологическое регулирование коагуляции и тромбообразования основывается на ингибировании тромбина благодаря применению гепаринов. Гепарины косвенно воздействуют на тромбин, ускоряя ингибирующее действие эндогенного антитромбина III /основного физиологического ингибитора тромбина/. Поскольку уровень антитромбина III в плазме изменяется, и поскольку поверхностно-связанный тромбин оказывается устойчивым к таковому косвенному механизму воздействия, лечение гепаринами может быть неэффективным. Поскольку полагают, что некоторые испытания на свертывание являются эффективными и надежными, уровень гепарина обычно контролируют с помощью испытаний на свертывание /в частности, определяя время активированного неполного тромбопластина (the activated partial thromboplastin time /APTT/assay)/. Кумарины препятствуют генерации тромбина, блокируя посттрансляциональное гамма-карбоксилирование при синтезе протромбина и других протеинов этого типа. Вследствие механизма их воздействия, действие кумаринов может проявляться только медленно, через 6 - 24 часа после введения. Кроме того, они не являются селективными антикоагулянтами. Кумарины также требуют контроля с помощью испытаний на свертывание /в частности, определения протромбинового времени/.
Для лучшего понимания изобретения далее приводится краткое описание системы ферментной коагуляции. Систему коагуляции, иногда называемую также "каскадом", лучше всего рассматривать как цепную реакцию, включающую последовательную активацию зимогенов до активных сериновых протеаз, которая, в конечном счете, приводит к образованию фермента тромбина. Тромбин через ограниченный протеолиз превращает фибриноген плазмы в нерастворимый гель - фибрин. Двумя ключевыми моментами в коагуляционном каскаде являются конверсия фактора свертывания X и Xa посредством фактора свертывания IXa и конверсия протромбина в тромбин под действием фактора свертывания Xa.
Обе реакции происходят на поверхности клеток, наиболее заметно - на поверхности пластинчатых эндотелиальных клеток, и обе реакции требуют кофакторов. Основные кофакторы - факторы V и VIII - циркулируют как относительно неактивные предшественники, но когда образуются первые несколько молекул тромбина, тромбин путем ограниченного протеолиза активирует кофакторы. Активированные кофакторы - Va и VIIIa - ускоряют примерно на три порядка как конверсию протромбина в тромбин, так и конверсию фактора X в фактор Xa.
Активированный протеин C в большинстве случаев предпочитает два плазменных протеина-субстрата, которые он гидролизует и необратимо разрушает. Эти плазменные протеиновые субстраты представляют собой активированные формы кофакторов свертывания V и VIII /кофакторы Va и VIIIa, соответственно/. Активированный протеин C только минимально разрушает неактивные предшественники - факторы свертывания V и VIII. На собаках показано, что активированный протеин C резко увеличивает уровень циркуляции основного физиологического фибринолитического фермента - тканевого плазменного активатора.
Однако активация протеина C затрагивает тромбин, конечную сериновую протеазу в коагуляционном каскаде и связанный с мембранами эндотелиальных клеток гликопротеин - тромбомодулин. Тромбомодулин образует прочный стехиометрический - 1:1 - комплекс с тромбином. Тромбомодулин, когда образует комплекс с тромбином, существенно модифицирует свойства тромбина. Тромбин в каскаде коагуляции обычно свертывает фибриноген, активирует тромбоциты и превращает кофакторы свертывания V и VIII в их активные формы - Va и VIIIa. Тромбин, когда один, действует как активатор протеина C, но только очень медленно и неэффективно. В противоположность этому, тромбин в виде комплекса 1: 1 с тромбомодулином не способен свертывать фибриноген, не активирует тромбоциты и не превращает факторы свертывания V и VIII в их активные формы. Комплекс тромбина с тромбомодулином промотирует активацию протеина C, причем константа скорости активации протеина C в 20000 раз выше для комплекса тромбина C с тромбомодулином, чем для одного тромбина.
Следовательно, активированный протеин C является противотромботическим средством с более широким терапевтическим индексом, чем другие антикоагулянты, такие как гепарин и оральные антикоагулянты гидроксикумаринового типа, такие как варфарин. Ни протеин C, ни активированный протеин C не являются эффективными до тех пор, пока в каком-либо отдельном месте негенерируется тромбин. Активированный протеин C фактически неэффективен без тромбина, поскольку тромбин нужен для того, чтобы превратить факторы свертывания V в Va, а фактор свертывания VIII - в VIIIa. Как отмечалось, активированные формы двух кофакторов являются предпочтительным субстратом для активированного протеина C. При введении пациентам зимоген протеина C будет оставаться неактивным до тех пор, пока генерируется тромбин. Без комплекса тромбомодулина с тромбином зимоген протеина C превращается в активированный протеин C с очень небольшой скоростью. Настоящее изобретение направлено на раскрытие соединений, определение которым дается ниже, которые увеличивают экспрессию тромбомодулина, и биологически пригодны для перорального применения.
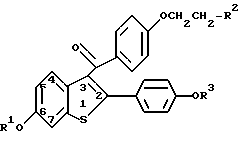
Настоящее изобретение предлагает способы увеличения экспрессии тромбомодулина, включающие введение людям, нуждающимся в таком лечении, эффективного количества соединения формулы I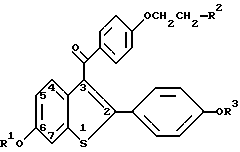
в которой R1 и R3 независимо представляют собой водород, -CH3,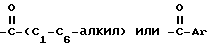
где Ar представляет собой необязательно замещенный фенил; R2 выбирают из группы, состоящей из пирролидино-, гексаметиленимино- и пиперидиногруппы, и его фармацевтически приемлемых солей и сольватов.
Изобретение также охватывает способ ингибирования тромботических осложнений или случаев, который включает введение нуждающемуся в этом человеку эффективного количества соединения формулы I.
Изобретение также охватывает способ увеличения скорости активации протеина C, который включает введение соединений формулы I.
Настоящее изобретение касается открытия, что 2-фенил-3-ароилбензотиофены /бензотиофены/ выбранной группы, имеющие формулу I, пригодны для увеличения экспрессии тромбомодулина. Способы применения, предлагаемые настоящим изобретением, на практике представляют собой введение человеку или млекопитающему, нуждающемуся в этом, дозы соединения формулы I или его фармацевтически приемлемой соли, или его сольвата, которая является эффективной для увеличения экспрессии тромбомодулина. Настоящий способ включает как консервативное лечение, так и/или профилактическую обработку, в зависимости от предназначения.
Термин "ингибирование" включает обычно значения, которые включают задержку, предупреждение, торможение, замедление или реверсию.
Ралоксифен - соединение настоящего изобретения - представляет собой гидрохлорид соединения формулы I, в которой R1 и R3 представляют собой водород, и R2 является пиперидинилом.
Обычно соединение формулируют с обычными эксципиентами, разбавителями или носителями и прессуют в таблетки, или формулируют в виде эликсиров или растворов для обычного перорального введения, или вводят внутримышечно или внутривенно. Соединения могут быть введены чрезкожно и могут быть сформулированы в виде дозировочных форм с длительным высвобождением и т.п.
Соединения, применяемые в способах настоящего изобретения, могут быть получены в соответствии с разработанными методиками, такими, какие подробно описаны в патентах США N 4133814, 4418068 и 4380635, которые все внесены в настоящее изобретение в качестве ссылок. Вообще, способ начинается с бензо[b] тиофена, содержащего 6-гидроксильную группу и 2-(4-гидроксифенильную) группу. В исходное соединение вводят защитную группу, алкилируют или ацилируют, и удаляют защитную группу, чтобы получить соединения формулы I. Примеры получения таких соединений приводятся в упомянутых выше патентах США. Необязательно замещенный фенил включает фенил и фенил, замещенный одной или двумя группами, из числа (C1-C6)-алкила, (C1-C4)-алкоксила, гидроксигруппы, нитрогруппы, хлора, фтора или три(хлор или фтор)метила.
Соединения, используемые в способах настоящего изобретения, образуют соли присоединения кислот и оснований с широким рядом органических кислот и неорганических кислот и оснований, которые часто применяются в фармацевтической химии. Такие соли также являются частью настоящего изобретения. Типичные неорганические кислоты, применяемые для образования таких солей, включают соляную кислоту, бромистоводородную, иодистоводородную, азотную, серную, фосфорную, гипофосфорную кислоту - и т.п. Также могут применяться соли, происходящие от органических кислот, таких как алифатические моно- и дикарбоновые кислоты, жирные одно- и двухосновные оксикислоты, ароматические кислоты, алифатические и ароматические сульфоновые кислоты. Таким образом, фармацевтически приемлемые соли включают ацетаты, фенилацетаты, трифторацетаты, акрилаты, аскорбаты, бензоаты, хлорбензоаты, динитробензоаты, гидроксибанзоаты, метоксибензоаты, метилбензоаты, о-ацетоксибензоаты, нафталин-2-бензоаты, бромиды, изобутираты, фениолбутираты, β-гидроксибутираты, бутил-1,4-диоаты, гексин-1,4-диоаты, капраты, каприлаты, хлориды, циннаматы, цитраты, формиаты, фумараты, гликоляты, гептаноаты, гиппураты, лактаты, малеаты, малаты, гидроксималеаты, малонаты, манделаты, мезилаты, никотинаты, изоникотинаты, нитраты, оксалаты, фталаты, терефталаты, фостфаты, моногидрофосфаты, дигидрофосфаты, метафосфаты, пирофосфаты, пропиолаты, пропионаты, фенилпропионаты, салицилаты, себацаты, сукцинаты, субераты, сульфаты, бисульфаты, пиросульфаты, сульфиты, бисульфиты сульфонаты, бензолсульфонаты, п-бромфенилсульфонаты, хлорбензолсульфонаты, этансульфонаты, 2-гидроксиэтансульфонаты, метансульфонаты, нафталин-2-сульфонаты, нафталин-2-сульфонаты, п-толуолсульфонаты, ксилолсульфонаты, тартраты и т.п. Предпочтительной солью является хлористоводородная соль.
Фармацевтически приемлемые соли присоединения кислот, как правило, получают взаимодействием соединения формулы I с эквимолярным или избыточным количеством кислоты. Реагенты обычно соединяют в совместном растворителе, таком как диэтиловый эфир или бензол. Соль обычно выпадает из раствора в течение одного часа и до 10 дней, и может быть отделена фильтрацией, или растворитель может быть удален обычным способами.
Основания, обычно применяемые для образования солей, включают гидроксид аммония и гидроксиды щелочных и щелочноземельных металлов, карбонаты, а также алифатические и первичные, вторичные и третичные амины, алифатические диамины. Основания, особенно пригодные для получения солей присоединения оснований, включают гидроксид аммония, карбонат калия, метиламин, диэтиламин, этилендиамин и циклогексиламин.
Фармацевтически приемлемые соли, как правило, имеют повышенную растворимость, по сравнению с соединением, из которого их получают, и, таким образом, часто более подходящие для формулировок в виде жидкостей или эмульсий.
Фармацевтические препараты могут быть получены приемами, известными в технике. Например, соединения могут быть введены в препараты с обычными наполнителями, разбавителями или носителями, и сформированы в таблетки, капсулы, суспензии, порошки и т.п. Примеры наполнителей, разбавителей и носителей, которые являются подходящими для таких препаратов, включают следующие материалы: наполнители и сухие разбавители, такие как крахмал, сахара, маннит и кремнийсодержащие производные; связующие агенты, такие как карбоксиметилцеллюлоза и другие производные целлюлозы, альгинаты, желатин и поливинилпирролидон; увлажняющие агенты, такие как глицерин; средства, препятствующие слеживанию, такие как карбонат кальция и бикарбонат натрия; агенты для замедления растворения, такие как парафин; ускорители ресорбции, такие как соединения четвертичного аммония; поверхностно-активные вещества, такие как цетиловый спирт, моностеарат глицерина; адсорбирующие носители, такие как каслин и бентонит; и смазывающие вещества, такие как тальк, стеарат кальция и магния и твердые полиэтиленгликоли. Соединения могут быть также сформулированы в виде эликсиров или растворов для обычного перорального введения, или в виде растворов, подходящих для парентерального введения, например внутримышечным, подкожным или внутривенным путем. Кроме того, соединения хорошо подходят для препаратов в виде дозировочных форм с замедленным высвобождением лекарственного средства и т.п. Препараты могут быть также составлены таким образом, что они могут высвобождать активный ингредиент только, или предпочтительно, в определенной части желудочно-кишечного тракта, возможно в течение некоторого времени. Покрытия, оболочки и защитные основы могут быть изготовлены, например, из полимерных веществ или восков.
Конкретная дозировка соединения формулы I, требуемая для увеличения экспрессии тромбомодулина, ингибирования тромботического осложнения или случая, или увеличения скорости активации протеина C, в соответствии с настоящим изобретением, будет зависеть от серьезности и природы состояния, способа введения и прочих факторов, которые будут определяться штатными врачами лечебного учреждения. Как правило, принятые и эффективные ежедневные дозы будут составлять от 0,1 до 1000 мг/день, и более типично - от 50 до 200 мг/день. Такие дозы будут вводиться субъекту, нуждающемуся в лечении, от одного до трех раз в день, или чаще, как это требуется, чтобы эффективно увеличить экспрессию тромбомодулина, увеличить активацию протеина C или ингибировать тромботические нарушения.
Обычно предпочтительно вводить соединения формулы I в форме соли присоединения кислоты, что является привычным при введении фармацевтических препаратов, несущих такую основную группу, как пиперидиновое кольцо. Также выгодно вводить такое соединение пероральным путем. Для таких целей подходит дозировочные формы для перорального введения, перечисленные далее.
Препараты
В препаратах, о которых идет речь далее, "активный ингредиент" означает соединение формулы I.
Препарат 1. Желатиновые капсулы
Готовят твердые желатиновые капсулы, используя перечисленные далее ингредиенты (см. табл.1).
Ингредиенты смешивают, пропускают через сито N 45 меш /США/, и заполняют твердые желатиновые капсулы.
Примеры конкретных капсульных формулировок с ралоксифеном, которые готовят, включают перечисленные ниже.
Препарат 2. Капсула с ралоксифеном (см. табл. 2).
Препарат 3. Капсулы с ралоксифеном (см. табл. 3).
Препарат 4. Капсула с ралоксифеном (см. табл. 4).
Препарат 5. Капсула с ралоксифеном (см. табл. 5).
Конкретные, приведенные выше, формулировки могут быть изменены в разумных пределах.
Формулировку в виде таблеток готовят, используя перечисленные ниже ингредиенты.
Препарат 6. Таблетки ( см. табл. 6 )
Компоненты смешивают и прессуют для получения таблеток.
С другой стороны, таблетки, каждая из которых содержит 0,1 - 1000 мг активного ингредиента, готовят следующим образом.
Препарат 7. Таблетки ( см. табл. 7).
Активный ингредиент, крахмал и целлюлозу пропускают через сито N 45 меш /США/ и тщательно смешивают. Раствор поливинилпирролидона смешивают с полученными в результате порошками, которые затем пропускают через сито N 14 меш /США/. Полученные таким образом гранулы сушат при 50o - 60oC, и пропускают через сито N 18 меш /США/. Затем к гранулам добавляют натрийкарбоксиметилкрахмал, стеарат магния и тальк, предварительно просеивают через сито N 60 меш /США/, и после перемешивания, прессуют на таблетировочной машине, и получают таблетки.
Суспензии, содержащие 0,1 - 1000 мг активного ингредиента в 5-мл дозе, готовят следующим образом.
Препарат 8. Суспензии ( см. табл. 8).
Активный ингредиент просеивают через сито N 45 меш /США/, и смешивают с натрийкарбоксиметилцеллюлозой и сиропом, получают однородную пасту. Раствор бензойной кислоты, отдушку и краситель разбавляют некоторым количеством воды и добавляют в пасту при перемешивании. Затем добавляют воду в количестве, достаточном для получения требуемого объема.
Другие варианты осуществления изобретения относятся к лечению, у человека или животного, состояния, когда требуется ингибирование тромботического нарушения. Тромботические нарушения или случаи, и тромбоэмболические заболевания, включают широкое разнообразие приобретенных болезненных состояний, в том числе внутрисосудистую коагуляцию, включая глубокий тромбофлебит, эмболию легких, сердечную ишемию, инфаркт миокарда, церебральный тромбоз, неспецифические состояния, состояния с местной гиперкоагуляцией и распространенные повреждения ткани, относящиеся к воспалительным процессам, капиллярный артериальный тромбоз, периферический артериальный тромбоз, эмболию, исходящую из сердечной или периферических артерий, острый инфаркт миокарда, тромботические удары и рассеянную внутрисосудистую коагуляцию. Рассеянная внутрисосудистая коагуляция имеет место, как осложнение, при многих болезненных состояниях, включая обширную травму, обширное оперативное вмешательство, тепловой удар, септицемию, острые и хронические заполнения печени, злокачественные заболевания, включая твердые опухоли, лейкозы и лимфомы, широкое разнообразие бактериальных, грибковых, паразитарных и вирусных инфекционных болезней, акушерские осложнения, гемолитические процессы, кардиогенный шок, любой случай сердечно-сосудистой недостаточности, тяжелые прогрессирующие удары, укусы змей, коллагенные васкулярные нарушения, молниеносную пурпуру, острый панкреатит, аллергический васкулит, polycythemia vera, тромбоцитемию и неспецифический язвенный колит, среди прочих. Хотя еще не раскрыто, врожденная недостаточность в экспрессии тромбомодулина может быть подемонстрирована у пациентов с тромбоэмболическими проблемами. Обострения у таких пациентов будут поддаваться лечению соединениями формулы I.
Полагают, что соединения формулы I также пригодны для лечения тромботических ударов. Уровень тромбомодулина в сосудах мозга является низким, таким образом повышение его будет важным при тромботическом ударе. На сегодняшний день удары, как правило, обычными антикоагулянтами не лечатся. Лечение ударов либо гепарином, либо пероральными антикоагулянтами хотя подчас успешно, однако несет высокий риск кровотечения в области поврежденного мозга, а также удар сопровождает ухудшение неврологического состояния.
Кроме того, полагают, что соединения настоящего изобретения пригодны для лечения острого инфаркта миокарда, поскольку очевидно, что основной предложенный механизм действия тромбомодулина и производных, т.е. антикоагуляция через активацию протеина C, составляет высокоэффективный способ достижения антитромботических эффектов на артериальной стороне циркуляции, так же, как и уменьшения реперфузионного повреждения. В ходе испытаний с тромболитическими средствами при остром инфаркте миокарда и из экспериментов на животных, станет ясно, что гепарин, как вспомогательное лечебное средство, является относительно неэффективным в качестве антитромботического средства на артериальной стороне циркуляции.
Также предполагается, что соединения настоящего изобретения пригодны для лечения рассеянной внутрисосудистой коагуляции /"DIC"/. Существуют экспериментальные данные, что посредники при воспалении, также как II - I, ИПF и I P-эндотоксин, резко снижают экспрессию тромбомодулина на эндотелиальных клетках, что в свою очередь ведет к недостаточной активации протеина C в антикоагулянтном каскаде. Гепарин и другие пероральные антикоагулянты давались пациентам с рассеянной внутрисосудистой коагуляцией в расширенных клинических испытаниях, но результаты этих испытаний разочаровывают. Характерно, что у пациента с рассеянной внутрисосудистой коагуляцией тромбы широко распространены, включая капиллярное кровообращение, с сопутствующими, зачастую серьезными проблемами кровотечения, которые являются результатом "расходования" важных факторов свертывания, которые сначала активируются, а затем инактивируются в ходе образования широко распространенных микроциркуляторных фибриновых тромбов.
Поскольку тромбомодулин падает с помощью различных посредников от воспаления, предпочтительное применение соединений состоит в регулировании воспалительных состояний, связанных с капиллярным тромбозом. В широком смысле это будет включать любое состояние, отмечаемое дисфункцией сосудистого эндотелия, как это происходит при сепсисе, повреждениях, включающих обширное повреждение ткани, и травмах, синдроме системного воспалительного отклика, синдроме сепсиса, септическом шоке и синдроме нарушения функций многих органов, включая DIC.
Существуют данные, что обычные антикоагулирующие лекарственные препараты, в частности варфарин, пригодны для лечения инвазивных злокачественных опухолей. Многие опухолевые клетки продуцируют вещества, которые вызывают активацию системы коагуляции, давая в результате локальные отложения фибрина. Эти фибринные отложения функционируют как "гнезда", в которых раковые клетки могут делиться, образуя метастатические повреждения. В одном клиническом исследовании показано, что пациенты, получающие варфарин в дополнение к противораковой химиотерапии при лечении мелкоклеточного рака легких, живут дольше и имеют менее обширные метастатические повреждения, чем пациенты, получающие одну химиотерапию. Однако раковая химиотерапия, использованная при этом исследовании, была менее интенсивной, чем та, которая на сегодняшний день считается оптимальной в клинической онкологии. Более интенсивные формы раковой химиотерапии почти всегда дают резкое ухудшение количества тромбоцитов, и тромбоцитопения, в сочетании с лечением варфарином несет пациенту неприемлемо высокий риск серьезных осложнений в виде кровотечений.
Ожидается, что соединения являются полезными при других заболеваниях, когда свертывание крови может стать основным делающим свой вклад процессом или источником вторичной патологии, при таких как рак, включая метастазы, воспалительные заболевания, включая артрит, и диабет. Антикоагулирующее соединение вводят перорально, парентерально, например, внутривенными вливаниями /iv/, внутримышечной инъекцией /im/ или подвижно /SC/.
Способ настоящего изобретения на практике применяют также вместе с растворяющим тромб средством, например с тканевым плазменным активатором /tPA/, модифицированным tPA, стрептокиназой или урокиназой, чтобы уменьшить реперфузионные повреждения. В случаях, когда происходит образование сгустков и блокируется артерия или вена /либо частично, либо полностью/, обычно используют растворяющее тромб средство. Соединение изобретения может быть введено прежде или одновременно с растворяющим средством, или после его применения, одно или вместе с растворяющим средством, кроме того, предпочтительно его вводят вместе с аспирином, чтобы предотвратить возобновление образования тромбов.
Способ настоящего изобретения на практике применяют также в сочетании с антагонистом тромбоцитного гликопротеинового IIb-IIIa-рецептором, что ингибирует агрегацию тромбоцитов. Соединение изобретения может быть введено раньше или вместе с антагонистом IIb-IIIa-рецептора, или после его применения, чтобы предотвратить появление или возобновление тромбообразования.
Способ настоящего изобретения также применяют на практике в сочетании с аспирином. Соединение изобретения может быть введено раньше или вместе с аспирином, или после его применения, чтобы предупредить появление или возобновление тромбообразования. Как указывалось выше, соединение настоящего изобретения предпочтительно вводить в сочетании с растворяющим тромб средством и с аспирином.
Испытание 1
Для дальнейшего понимания действия /действий/ соединений формулы I на внутреннюю оболочку клетки гладких мышц и их роли в усилении антикоагуляции крови необходимо исследовать изменения активности тромбомодулина TM на поверхности такого типа клеток. Соединения формулы I также могут быть использованы для реверсии /исправления любых влияний посредников, которые ведут к падению активности TM на поверхности TM таких клеток.
Приблизительно 40000 - 80000 ранее пассированных эндотелиальных /артериальных, венозных или капиллярных/ клеток, или клеток интимальных гладких мышц, высеивают и выращивают до слияния на 24-ячеистых культуральных планшетах. Клеточный монослой затем промывают 2 - 3 раза либо буферным соляным раствором Хэнкса /HBSS/, либо бессывороточной средой /SFM/. Через 24 часа к клеткам добавляют, в трех параллельных случаях, различные концентрации соединения формулы I /в интервале от микромолярной до субпикомолярной/. Клетки в контрольных ячейках /отрицательный контроль/ выдерживают в бессывороточной среде с количеством носителя, эквивалентным во всех ячейках.
Измерение активности TM на поверхности клеток выполняют, используя двухстадийное амидолитическое испытание (two-phase amidolitic assay). Во время первой стадии испытания вслед за ополаскиванием клеток HBSS или SFM, к монослою добавляют 0,4 мл SFM, содержащего человеческий протеин C (конечная концентрация 11,2 ug/мл), альфа-тромбин (конечная концентрация 0,1 NIHU/мл), и инкубируют при 37oC и 5% CO2. Через 15, 30 и 45 минут из каждой ячейки отбирают 100 ul среды, и вводят в ячейки микротитратора с 50 ul избыточного гирудина /20 антитромбиновых ед-ц на мл/ на 5 минут при 37oC, чтобы остановить дальнейшее действие тромбина.
В качестве негативного контроля в отсутствии клеток используют SFM с протеином C и альфа-тромбином, как описано выше, и обрабатывают подобным образом.
На второй стадии испытания 50 ul 3 мМ 2366, хромогенного вещества протеина C, добавляют к смесям концентрированных сред с гирудином, и с помощью, автоматического считывающего устройства измеряют оптическую плотность при 405 нм /OD405/, чтобы проверить кинетику активности TM в течение 4 минут. После завершения этого кинетического испытания проводят измерение общего количества протеина, используя метод BCA. Конечную активность TM выражают как % увеличения. Соединение A представляет собой соединение формулы I, в котором R1 и R3 являются водородами, R2 представляет собой 1-пирролидиногруппу.
Соединение A (концентрация (мкМ) - Активность TM (% увеличения)
1•10-4 - 14
1•10-2 - 15
1•10-1 - 15
1,00 - 17
10,00 - 17
Испытание 2
Чтобы показать действие соединений формулы I в качестве антитромботиков и их способность корректировать эндотелиальную дисфункцию, индуцированную воспалением, используют павиановую модель сепсиса, индуцированного E. coli, описанную в патенте США N 5009889 /включенном в настоящее изобретение в качестве ссылки/.
Полезность соединений изобретения иллюстрируется положительным влиянием на экспрессию тромбомодулина, тромботические нарушения или характеристики скорости активации протеина C, которое обнаруживается в упомянутых выше испытаниях.
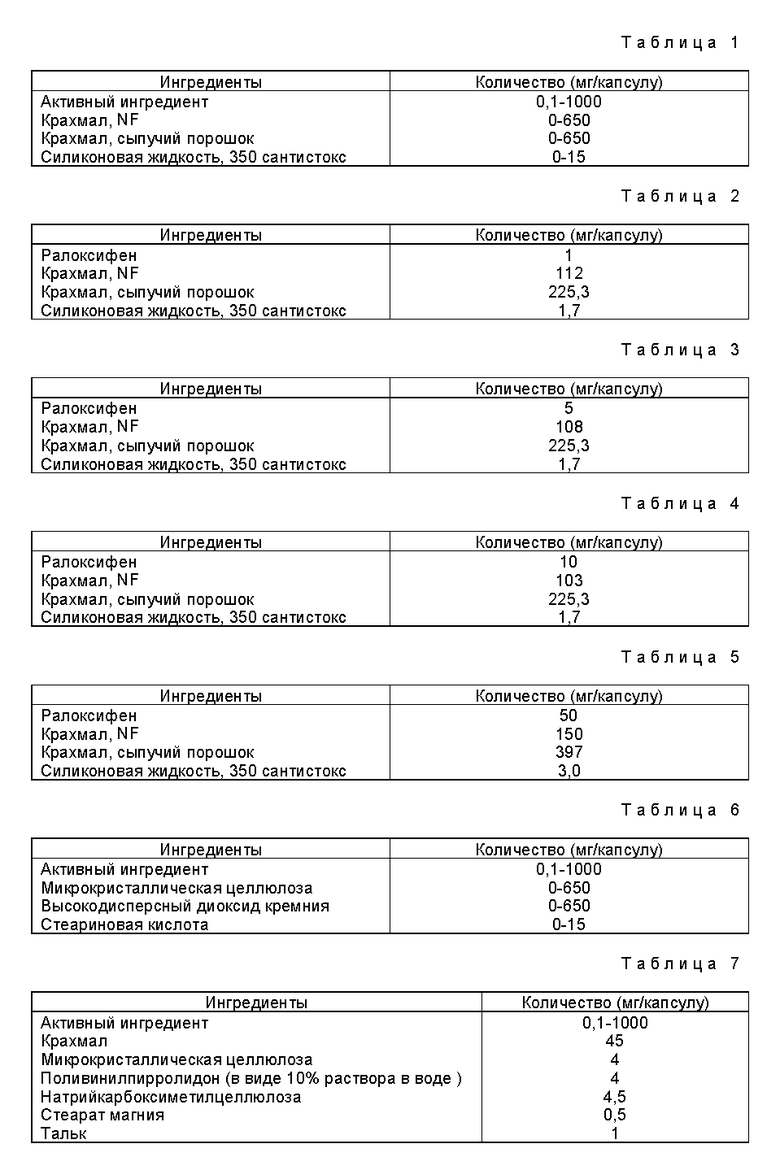

Предлагается новое средство для увеличения экспрессии тромбомодулина, представляющий собой соединение формулы l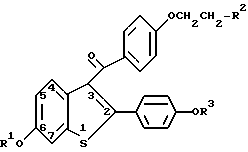
в которой R1 и R 3 независимо представляют собой водород, -СН3,
где Ar представляет собой необязательно замещенный фенил; R2 выбирают из группы, состоящей из пирролидино-, гексаметиленимино- и пиперидиногруппы; или его фармацевтически приемлемые соли или его сольваты. Изобретение расширяет арсенал средств для ингибирования тромботического нарушения путем экспрессии тромбомодулина. 3 з.п.ф-лы, 8 табл.
в которой R1 и R3 независимо являются водородом, -CH3,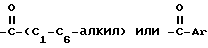
где Ar представляет собой необязательно замещенный фенил;
R2 выбирают из группы, состоящей из пирролидино-, гексаметиленимино и пиперидиногруппы,
или его фармацевтически приемлемой соли или его сольвата для увеличения экспрессии тромбомодулина.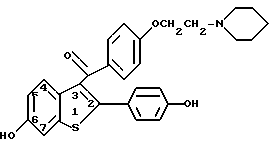
или его гидрохлорид.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| US 4133814 A, 09.01.79 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Ена Я.М | |||
| и др | |||
| Биологическая роль и клиническое значение протеина С | |||
| Врачебное дело | |||
| - Киев: Здоровья, 1992, N 6, с | |||
| Прибор для промывания газов | 1922 |
|
SU20A1 |
Авторы
Даты
1999-01-27—Публикация
1994-12-19—Подача