Изобретение относится к производству гексаазаизовартзитана, содержащему ацильную группу, и способу его получения.
Содержащее ацильную группу производное гексаазаизовартзитана данного изобретения содержит N-A-группу (где A обозначает ацильную группу) и необязательно N-H-группу в высокой концентрации, причем в этом производном каждая из N-A-групп и N-H-групп может быть превращена в N-NO2-группу различными способами нитрования.
Таким образом, содержащее ацильную группу производное гексаазаизовартзитана по данному изобретению полезно в качестве предшественника производного полинитрогексаазаизовартзитана, которое может быть использовано не только в качестве сырья для взрывчатых веществ, но также в качестве добавки к ракетным топливам и взрывчатым веществам. В частности, производное полинитрогексаазаизовартзитана может успешно применяться в качестве добавки для улучшения различных свойств (таких как механические свойства, скорость детонации, давление детонации, скорость горения, показатель экспоненты давления, чувствительность и устойчивость к нагреванию) ракетного топлива и взрывчатых веществ. Вдобавок, предполагается, что гексанитрогексаазаизовартзитан (обозначенный как "HNW"), являющийся типичным примером производного полинитрогексаазаизовартзитана, является перспективным материалом для создания следующего поколения взрывчатых веществ с высокими характеристиками. Как упомянуто выше, содержащее ацильную группу производное гексаазаизовартзитана по данному изобретению полезно в качестве предшественника такого ценного производного полинитрогексаазаизовартзитана.
Кроме того, содержащее ацильную группу производное гексаазаизовартзитана по данному изобретению может быть успешно использовано, благодаря реакционной способности каждой N-A-группы (где A обозначает ацильную группу) и N-H-группы, содержащихся в нем, для получения высокополярного полимера, содержащего в высокой концентрации ацильные группы в своей основной и/или боковой цепи. Этот высокополярный полимер полезен не только как высокогидрофильный полимер, но также как высокодиэлектрический полимер.
К тому же, содержащее ацильную группу производное гексаазаизовартзитана по данному изобретению может быть успешно использовано как полифункциональный сшивающий агент, благодаря реакционной способности производного.
Более того, содержащее ацильную группу производное гексаазаизовартзитана по данному изобретению может также быть использовано в качестве различного рода добавок, таких как модификатор полимеров и тому подобное.
Предшествующий уровень техники
Вдобавок к вышеуказанному HNW, общеизвестные соединения, имеющие такой же гексаазаизовартзитановый (обозначенный далее для простоты "W") скелет, как содержащее ацильную группу гексаазаизовартзитановое производное по данному изобретению, включают следующие:
1) гексакис(арилметил)гексаазаизовартзитан (обозначенный для простоты "HBW");
2) тетраацетилдибензилгексаазаизовартзитан (обозначенный для простоты "TADBW") и
3) гексаазаизовартзитан, имеющий карбамильную группу (обозначенный для простоты "HCW") (см. непрошедшую экспертизу выложенную заявку Японии N 6-321962).
Известно, что HBW может быть получен реакцией конденсации различных арилметиламинов с глиоксалем [см. J. Org. Chem., Vol. 55, 1459-1466(1990)].
Было сообщено, что TADBW полезен в качестве вещества для получения взрывчатки [см. The Military Critical Technologies List, Office of the Under Secretary of Defense for Aquisition, 12-22, October (1992)]. Однако в этом сообщении не описан ни способ превращения TADBW во взрывчатое вещество, ни химическая структура такого взрывчатого вещества, полученного из TADBW, ни способ получения самого TADBW.
Свойства HNW, который, как упомянуто выше, предположительно может служить перспективным сырьем для взрывчатых веществ с высокими характеристиками, описаны в International Symposium on Energetic Materials Technology, PROCEEDINGS, September 24-27, 76-81 (1995): Combustion AND FLAME 87, 145-151 (1991) и т.д., но нигде в литературе нет сведений по получению HNW.
Ранее, с целью разработки способа получения производного полинитрогексаазаизовартзитана, такого как HNW, настоящие заявители пытались нитровать HBW и TADBW при различных условиях нитрования. Однако оказалось невозможным получить достаточное количество производного полинитрогексаазаизовартзитана. Кроме того, HBW и TADBW содержат бензильную группу, так что, когда HBW или TADBW подвергают нитрованию, в качестве побочного продукта неизбежно образуются нитроароматические соединения, обладающие высоким сродством по отношению к различным нитросоединениям. В результате, трудно отделить целевое производное полинитрогексаазаизовартзитана от побочных нитроароматических соединений.
Трудно также получить HCW с высокими выходами. Основанием для подобного заключения служит то, что во время получения HCW образуется хлористо-водородная кислота (являющаяся сильной кислотой) и образовавшаяся хлористо-водородная кислота похоже разлагает HBW, служащий исходным веществом.
Таким образом, ни одно из W-скелетсодержащих соединений HBW, TADBW и HCW не пригодно в качестве предшественника, который мог бы быть успешно использован для получения в промышленном масштабе производного полинитрогексаазаизовартзитана, такого как HNW или тому подобного.
Краткое описание изобретения
В подобной ситуации с целью разработки целесообразного промышленного способа получения производного полинитрогексаазаизовартзитана настоящие заявители предприняли обширные и интенсивные исследования с целью нахождения не только предшественника, который мог бы быть легко превращен в производное полинитрогексаазаизовартзитана, но также способа получения этого предшественника.
В результате неожиданно было найдено, что в качестве предшественника производного полинитрогексаазаизовартзитана полезно производное гексаазаизовартзитана, имеющее полярную группу, состоящую только из N-ацильной группы и необязательно N-H-группы. Настоящие заявители нашли также промышленно целесообразный способ получения вышеупомянутого производного гексаазаизовартзитана с высоким выходом. Кроме того, найдено, что производное гексаазаизовартзитана, содержащее N-ацильную группу, N-алкильную группу и необязательно N-H-группу, может с успехом быть использовано в качестве полифункционального поперечно сшивающего агента. Данное изобретение основано на этих новых полученных результатах.
Цель данного изобретения состоит в получении вышеупомянутого производного гексаазаизовартзитана, другую цель данного изобретения составляет разработка способа получения этого продукта.
Кроме того, цель данного изобретения состоит в получении нового функционального вещества, содержащего в высокой концентрации сильно полярную функциональную группу, такую как N-ацильная группа и N-H-группа.
Подробное описание изобретения
Один из аспектов данного изобретения состоит в получении производного гексаазаизовартзитана, содержащего ацильную группу, представленного следующей формулой I:
WAtQ(6-t),
где t обозначает целое число от 4 до 6, каждый заместитель A независимо обозначает ацильную группу, содержащую от 1 до 10 углеродных атомов, каждый Q независимо обозначает атом водорода или алкильную группу с 1 - 10 углеродными атомами и W обозначает шестивалентный остаток гексаазаизовартзитана, представленный следующей формулой II: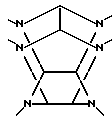
Другой аспект данного изобретения состоит в разработке способа получения вышеупомянутого производного гексаазаизовартзитана, содержащего ацильную группу.
Ниже даны объяснения, касающиеся содержащего ацильную группу производного гексаазаизовартзитана, представленного приведенной ниже формулой I-a, как характерного примера соединения приведенной выше формулы I
WAtH(6-t)
где t обозначает целое число от 4 до 6, A обозначает ацильную группу с 1-10 углеродными атомами и H обозначает атом водорода, W обозначает шестивалентный гексаазаизовартзитановый остаток, представленный следующей формулой II: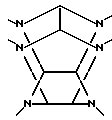
Что касается ацильной группы A в производном гексаазаизовартзитана по данному изобретению, то не существует особого ограничения кроме того, что она содержит от 1 до 10 углеродных атомов. Ацильная группа может быть замещена заместителем, который остается стабильным в реакционных условиях при реакции восстановительного деарилметилирования, выполняемой способом по данному изобретению как описано ниже. Примеры ацильных групп включают ацетильную группу, пропионильную группу, бутирильную группу, изобутирильную группу, валерильную группу, гексаноильную группу и 2-фенилацетильную группу. Из них предпочтительны ацильные группы с 2-5 углеродными атомами, такие как ацетильная группа, пропиональная группа, бутирильная группа и валерильная группа. Более желательны ацильные группы с 2-3 углеродными атомами, такие как ацетильная группа и пропионильная группа. Ацильные группы, обозначенные At в формуле I-а, приведенной выше, могут быть одинаковыми или различными.
Для содержащего ацильную группу производного гексаазаизовартзитана по данному изобретению, представленного формулой I-а: WAtH(6-t), существует множество различных изомеров, которые имеют одинаковые значения t, но различаются по положениям N-ацильных групп и N-H-групп.
Например, в качестве характерного примера соединений представленных формулой I-a: WAtH(6-t), где t равно 4, т.е. соединений формулы WA4H2 , может быть упомянуто соединение представленное приведенной ниже формулой I-a', хотя соединение, представленное формулой WA4H2, может быть любым из структурных изомеров соединения приведенной ниже формулы I-a'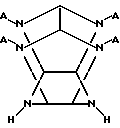
В содержащем ацильную группу производном гексаазаизовартзитана WAtH(6-t) по данному изобретению t обозначает целое число от 4 до 6, предпочтительно 4 или 6.
Другим предпочтительным примером содержащего ацильную группу производного гексаазаизовартзитана по данному изобретению служит соединение, представленное формулой I-a, где t равно 6, т.е. производное гексаацилгексаазаизовартзитана следующей формулы III:
WA6
где A обозначает ацильную группу с 1-10 углеродными атомами, а W обозначает шестивалентный остаток гексаазаизовартзитана.
Гексаацилгексаазаизовартзитан формулы III, приведенной выше, имеет при этом преимущество, поскольку структура соединения простая и соединение легко может быть получено с высокой степенью чистоты. В связи с этим следует отметить, что среди соединений формулы III гексаацетильное соединение легко может быть очищено сублимацией, так что из реакционной смеси легко может быть получено высокоочищенное WA6 (A: ацетильная группа).
Другим предпочтительным примером содержащего ацильную группу производного гексаазаизовартзитана по данному изобретению служит соединение, представленное формулой I-a, где t равно 4. Это соединение имеет при этом преимущество, поскольку содержащиеся в нем N-H-группы обладают высокой реакционной способностью, что делает возможным селективное взаимодействие N-H-групп. Например, путем селективного нитрования N-H-групп легко может быть получено с высоким выходом производное динитрогексаазаизовартзитана.
Как упомянуто выше, содержащее ацильную группу производное гексаазаизовартзитана по данному изобретению содержит N-A-группу (где A обозначает ацильную группу) и необязательно N-H-группу в высокой концентрации, где каждая из N-A- и N-H-групп может быть превращена в N-NO2-группу различными способами нитрования.
Приведенные далее примеры описывают способы получения содержащего ацильную группу производного гексаазаизовартзитана формулы I-a.
Гексаацилгексаазаизовартзитан WA6, являющийся предпочтительным примером содержащего ацильную группу производного гексаазаизовартзитана по данному изобретению, может быть получен ацилированием содержащего ацильную группу производного гексаазаизовартзитана WAnH(6-n) (где n равно 4 или 5) ацилирующим агентом, как показано в следующей реакционной схеме 1: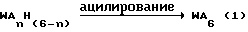
где n обозначает целое число от 4 до 5, A обозначает ацильную группу с 1-10 углеродными атомами, H обозначает атом водорода и W обозначает шестивалентный остаток гексаазаизовартзитана.
WAnH(6-n) (где n равно 4 или 5), использованный в приведенной выше реакционной схеме 1, не описан ни в одном литературном источнике, определяющем известный уровень техники, и был первоначально синтезирован настоящим заявителем. Для объяснения способа получения WAnH(6-n) первоначально требуется объяснение способа получения WA6.
В отношении ацилирующего агента, используемого в реакционной схеме 1, не существует особого ограничения за исключением того, что он должен быть способен к ацилированию вторичной аминогруппы, содержащейся в WAnH(6-n) (где n равно 4 или 5). Примеры ацилирующих агентов включают ацилгалогениды, также как ацетилхлорид, ацетилбромид и пропионилхлорид; сложные эфиры карбоновых кислот и N-гидроксисукцинимида, такие как N-ацетоксисукцинимид, N-пропионилоксисукцинимид и N-(2-фенилацетокси)сукцинимид; ангидриды карбоновых кислот, такие как уксусный ангидрид, пропионовый ангидрид, ангидрид молочной кислоты и ангидрид смеси уксусной и муравьиной кислот; и ацилимидазолы, такие как ацетилимидазол и пропионилимидазол. Среди упомянутых выше ацилирующих агентов предпочтительны ацилгалогениды (такие как ацетилхлорид, пропионилхлорид и тому подобные).
В отношении реакционного растворителя, используемого в реакционной схеме 1, не существует особого ограничения за исключением того, что растворитель должен быть способен растворять WAnH(6-n) (где n равно 4 или 5) и растворитель не должен оказывать неблагоприятного воздействия на реакцию. Примеры таких растворителей включают карбоновые кислоты, такие как уксусная кислота, пропионовая кислота и молочная кислота; апротонные полярные растворители, такие как диметилсульфоксид и диметилацетамид; и ангидриды карбоновых кислот, такие как уксусный ангидрид и пропионовый ангидрид. Из них предпочтительны ангидриды карбоновых кислот (такие как уксусный ангидрид, пропионовый ангидрид и тому подобные). Вышеупомянутые растворители могут быть использованы индивидуально или в комбинации.
Реакционная температура для реакционной схемы 1 соответствует обычно интервалу от -10 до 300oC, предпочтительно от 0 до 150oC.
WA6, полученный по реакционной схеме 1, может быть выделен общепринятыми способами. Например, выделение WA6 может быть выполнено отгонкой растворителя от реакционной смеси после завершения реакции (см., например, пример 1). Также, очистка WA6 может быть выполнена общепринятым способом. Примеры способов очистки включают способ, в котором выделенный WA6 сублимируют при 270oC при пониженном давлении, равном 10 мм рт.ст. (см., например, пример 1); способ, в котором выделенный WA6 перекристаллизовывают из толуола (см., например, пример 2), и способ, в котором выделенный WA6 перекристаллизовывают из хлороформа.
WA6 по данному изобретению может также быть получен восстановительным деарилметилированием производного гексаазаизовартзитана, содержащего ацильную группу и арилметильную группу, представленного формулой WAnB(6-n), и затем ацилированием образовавшегося продукта ацилирующим агентом, как показано в следующей реакционной схеме 2:
где n обозначает целое число от 4 до 5; A обозначает ацильную группу с 1-10 углеродными атомами; B обозначает арилметильную группу, представленную формулой XIII приведенной ниже; H обозначает атом водорода и W обозначает шестивалентный остаток гексаазаизовартзитана.
Для WAnB(6-n), как исходного вещества в приведенной выше реакционной схеме 2, не существует особенного ограничения по источнику или способу его получения.
Например, без каких-либо ограничений может быть использован WAnB(6-n), полученный из гексакис(арилметил)гексаазаизовартзитана (WB6) способом, описанным ниже, или выпускаемый промышленностью.
В вышеупомянутой реакционной схеме 2 восстановительное деарилметилирование (стадии а) может быть выполнено любым общепринятым способом, способствующим протеканию реакции восстановительного деарилметилирования WAnB(6-n). Обычно восстановительное деарилметилирование (стадия а) осуществляют путем контакта WAnB(6-n) с восстанавливающим катализатором в присутствии восстанавливающего агента.
В качестве восстанавливающего агента обычно используют газообразный водород, гидразин, муравьиную кислоту или тому подобное, и предпочтительно используют газообразный водород. В качестве восстанавливающего катализатора обычно используют катализатор, содержащий металл, принадлежащий к семейству платиновых, или содержащий производные этих металлов. Предпочтительные примеры восстанавливающих катализаторов включают соединения Pd [такие как Pd(OAc)2, PdCl2, Pd(NO3)2, PdO, Pd(OH)2, Pd3Pb1 и Pd3Te1] Pd-сплавы и металлический Pd; и соединения Ru (такие как RuCl3), Ru-сплавы и металлический Ru. Из них более предпочтительны соединения Pd [такие как Pd(OAc)2, PdCl2 и тому подобные] , сплавы Pd и металлический Pd. Эти восстанавливающие катализаторы могут быть использованы как таковые. Или же иначе, эти восстанавливающие катализаторы могут быть использованы в нанесенной на различные типы носителей форме, на такие носители как активированный углерод, двуокись кремния, окись алюминия, двуокись кремния - окись алюминия, цеолит и активированная глина. Катализатор перед использованием в вышеупомянутой реакции восстановительного диарилметилирования может быть подвергнут восстановительной обработке. В случае катализатора, нанесенного на носитель, кислотность поверхности носителя можно контролировать путем инактивации кислотных участков, присутствующих на поверхности носителя, силилированием, ацилированием или тому подобным, или обработкой носителя таким образом, чтобы щелочное вещество (например, NaOH) адсорбировалось на поверхности носителя. Количество восстанавливающего катализатора варьируют в зависимости от восстанавливающей активности катализатора. Однако обычно катализатор используют от 0,0001 до 10, предпочтительно от 0,001 до 1 в весовом отношении металла катализатора к WAnB(6-n).
В отношении реакционного растворителя, используемого в восстановительном деарилметилировании (стадия а) приведенной выше реакционной схемы 2, не существует особого ограничения, за исключением того, что растворитель должен быть способен растворять WAnB(6-n) и растворитель не должен оказывать нежелательное воздействие не реакцию. Примеры растворителей включают карбоновые кислоты, такие как уксусная кислота, пропионовая кислота и молочная кислота; амидные соединения, такие как диметилацетамид и аминосоединения, такие как N,N-диметиланилин. Вышеуказанные растворители могут быть использованы индивидуально или в комбинации. С точки зрения достижения высокой скорости реакции предпочтительно использовать карбоновую кислоту (такую как уксусная кислота, пропионовая кислота или тому подобная) в качестве растворителя.
Количество растворителя варьируется в зависимости от его растворяющей способности и реакционной температуры. Растворитель используют обычно в количестве от 1 до 500, предпочтительно от 5 до 100, в значениях соотношения веса растворителя и WAnB(6-n).
Реакционное давление для восстановительного деарилметилирования (стадия а) по способу, описываемому реакционной схемой 2, обычно берется в интервале от 0,1 до 1000 кгс/см2, предпочтительно от 1 до 100 кгс/см2. Когда в качестве восстанавливающего агента используют газообразный водород, реакционное давление предпочтительно находится в интервале от 0,1 до 500 кгс/см2, более предпочтительно от 1 до 100 кгс/см2 в значениях парциального давления водорода. В дополнение к газообразному водороду в реакционной системе может присутствовать инертный газ, такой как азот, аргон или гелий.
Реакционная температура для восстановительного деарилметилирования (стадия а) по способу, описываемому реакционной схемой 2, обычно находится в интервале от -20 до 300oC, предпочтительно от 0 до 200oC.
Реакционное время для восстановительного деарилметилирования (стадия а) по способу, описываемому реакционной схемой 2, варьируется в зависимости от типов катализатора, растворителя и тому подобного. Реакционное время обычно находится в интервале от 0,1 до 500 час, предпочтительно от 1 до 200 час.
Реакцией восстановительного деарилметилирования (стадия а) по способу, описываемому реакционной схемой 2, синтезируют WAnH(6-n) (где n равно 4 или 5). Затем синтезированный WAnH(6-n) ацилируют (стадия b) по способу, описываемому реакционной схемой 2.
Что касается ацилирующего агента, растворителя и реакционных условий (таких как реакционная температура и тому подобные), используемых в ацилировании (стадия b) по способу, описываемому реакционной схемой 2, то можно использовать те же, что указаны для реакции ацилирования по реакционной схеме 1 выше.
Выделение и очистка полученного WA6 могут быть выполнены способом, указанным выше, для реакции, описываемой реакционной схемой 1.
WA6, являющийся одним из примеров содержащего ацильную группу производного гексаазаизовартзитана по данному изобретению, может также быть получен восстановительным деарилметилированием WB6 в присутствии ацилирующего агента с целью получения первого реакционного продукта, и затем восстановительным деарилметилированием первого продукта реакции в отсутствие ацилирующего агента до получения второго продукта реакции и затем ацилированием второго продукта реакции, как показано в следующей реакционной схеме 3:
где n обозначает целое число от 4 до 5; A обозначает ацильную группу с 1-10 углеродными атомами; B обозначает арилметильную группу и W обозначает шестивалентный остаток гексаазаизовартзитана.
Восстановительное деарилметилирование в присутствии ацилирующего агента на стадии a по способу, описываемому реакционной схемой 3 выше, обычно выполняют путем контактирования WB6 с восстанавливающим катализатором в присутствии ацилирующего агента и восстанавливающего агента. Относительно восстанавливающего агента и катализатора не существует особого ограничения при условии, что они способствуют успешному протеканию реакции восстановительного деарилметилирования WB6 и не дезактивируют ацилирующий агент в реакционной системе. В качестве восстановительного агента обычно используют газообразный водород, муравьиную кислоту или тому подобные соединения и предпочтительно использовать газообразный водород. В качестве восстанавливающего катализатора могут быть использованы те соединения, которые упомянуты для восстановительного деарилметилирования (стадия a) по способу, описываемому реакционной схемой 2, приведенной выше.
Количество катализатора варьируется в зависимости от восстанавливающей активности катализатора. Восстанавливающий катализатор используют обычно в количестве от 0,0001 до 20, предпочтительно от 0,001 до 10 в значениях отношения веса металла катализатора к WB6.
В отношении ацилирующого агента, используемого в восстановительном деарилметилировании в присутствии ацилирующего средства стадии a по способу, описываемому реакционной схемой 3, не существует особого ограничения, кроме того, что он должен быть способным к ацилированию вторичной аминогруппы, образующейся при восстановительном деарилметилировании WB6. Примеры ацилирующих агентов включают сложные эфиры карбоновых кислот N-гилдроксисукцинимида, такие как N-ацетоксисукцинимид, N-пропионилоксисукцинимид и N-(2-фенилацетокси)сукцинимид; ангидриды карбоновых кислот, такие как уксусный ангидрид, пропионовый ангидрид, ангидрид молочной кислоты и ангидрид смеси уксусной и муравьиной кислот; и ацилимидазолы, такие как ацетилимидазол и пропионилимидазол. Среди этих ацилирующих агентов предпочтительны сложные эфиры карбоновых кислот N-гидроксисукцинимида (такие как N-ацетоксисукцинимид, N-пропионилоксисукцинимид и тому подобные), поскольку обладают большей селективностью в отношении WAnB(6-n) (где n равно 4 или 5). Эти ацилирующие агенты могут быть использованы индивидуально или в комбинации. Особенно предпочтительна в качестве ацилирующего агента смесь сложного эфира карбоновой кислоты N-гилдроксисукцинимида (такого как N-ацетоксисукцинимид, N-пропионилоксисукцинимид или тому подобного) и ангидрида карбоновой кислоты (такого как уксусный ангидрид, пропионовый ангидрид или тому подобного), поскольку не только скорость реакции восстановительного деарилметилирования на стадии a по способу, описываемому реакционной схемой 3, становится высоко, но также повышается селективность в отношении WAnB(6-n) (где n равно 4 или 5).
Количество ацилирующего агента варьируется в зависимости от реакционной способности ацилирующего агента, вида реакции и реакционных условий. Ацилирующий агент используют обычно в количестве от 0,1 до 100, предпочтительно от 1 до 50, в значениях молярного отношения ацилирующего агента к арилметильным группам WB6. Когда в качестве ацилирующего агента используют смесь сложного эфира карбоновой кислоты N-гилдроксисукцинимида и ангидрида карбоновой кислоты, количество ангидрида карбоновой кислоты обычно находится в интервале от 0,01 до 100, предпочтительно от 0,1 до 10, в значениях молярного отношения ангидрида карбоновой кислоты к сложному эфиру карбоновой кислоты N-гидроксисукцинимида.
В отношении реакционного растворителя, используемого в восстановительном деарилметилировании в присутствии ацилирующего агента на стадии а по способу, описываемому реакционной схемой 3, не существует особого ограничения, за тем исключением, что растворитель должен быть способен растворять WB6 и растворитель не должен оказывать нежелательного воздействия на реакцию. Примеры растворителей включают ароматические соединения, такие как бензол, толуол, этилбензол, ксилол, кумол, цимол, диизопропилбензол и фенилэтиловый эфир; циклические, линейные или разветвленные простые эфиры, такие как тетрагидрофуран, диоксан, тетрагидропиран, диэтиловый эфир, дипропиловый эфир и диизопропиловый эфир; и алифатические спирты, такие как метанол, этанол, пролпанол, изопропиловый спирт и трет-бутиловый спирт. Эти растворители могут быть использованы индивидуально или в комбинации. Среди вышеуказанных растворителей предпочтительны ароматические соединения (такие как бензол, толуол, этилбензол, ксилол и тому подобные), потому что скорость реакции восстановительного деарилметилирования WB6 в этих растворителях возрастает.
Количество растворителя варьируется в зависимости от растворяющей способности растворителя и реакционной температуры. Обычно растворитель используют в количестве от 0,1 до 100, предпочтительно от 1 до 100, в значениях весового отношения растворителя к WB6.
Реакционное давление для восстановительного деарилметилирования (в присутствии ацилирующего агента) на стадии а по способу, описываемому реакционной схемой 3, используют обычно в интервале от 0,1 до 1,000 кгс/см2, предпочтительно от 1 до 300 кгс/см2. Когда в качестве восстановительного агента используют газообразный водород, в некоторых случаях скорость реакции возрастает с увеличением реакционного давления. Реакционное давление используют предпочтительно в интервале от 0,1 до 500 кгс/см2, более предпочтительно от 1 до 200 кгс/см2, в значениях парциального давления водорода. В дополнение к газообразному водороду в реакционной системе могут присутствовать инертные газы, такие как азот, аргон и гелий в газообразном состоянии.
Реакционная температура до восстановительного деарилметилирования (в присутствии ацилирующего агента) в стадии а по способу, описываемому реакционной схемой 3, находится обычно в интервале от -20 до 300oC, предпочтительно от 0 до 200oC.
По способу, описываемому реакционной схемой 3, реакцию восстановительного деарилметилирования (стадия а) обрывают (закачивают), когда WAnB(6-n) образуется в значительном (существенном) количестве. В частности, ход реакции деарилметилирования контролируют путем газовой хроматографии или жидкостной хроматографии, и реакцию обрывают когда WAnB(6-n) образуется в заданных количествах.
Время реакции изменяется в зависимости от типов катализатора, ацилирующего агента, растворителя и тому подобного. Реакционное время обычно составляет 0,1-500 часов, предпочтительно 1-200 часов.
WAnB(6-n) (где n равно 4 или 5) синтезируют путем восстановительного деарилметилирования (в присутствии ацилирующего агента) в стадии a по способу, описываемому реакционной схемой 2. Затем синтезированный WAnB(6-n) подвергают восстановительному деарилметилированию (в отсутствие ацилирующего агента) в стадии b по способу, описываемому реакционной схемой 3.
Что касается катализатора, восстанавливающего агента, растворителя и реакционных условий (реакционная температура, реакционное давление и тому подобные), которые используют в восстановительном деарилацилировании (в отсутствие ацилирующего агента) на стадии b по способу, описываемому реакционной схемой 3, то можно использовать те же соединения и параметры, что указаны для реакции восстановительного деарилметилирования (в присутствии ацилирующего агента) на стадии a по способу, описываемому реакционной схемой 3.
Или же, могут быть использованы катализатор, восстанавливающий агент, растворитель и реакционные условия, указанные для восстановительного деарилметилирования в стадии a по способу, описываемому реакционной схемой 2, приведенной выше.
Из реакционной смеси, полученной восстановительным деарилметилированием (в присутствии ацилирующего агента) на стадии a по способу, описываемому реакционной схемой 3, удаляют ацилирующий агент и образовавшуюся после удаления ацилирующего агента смесь подвергают восстановительному деарилметилированию (в отсутствие ацилирующего агента) на стадии b по способу, описываемому реакционной схемой 3. В этом случае предпочтительно не удалять восстанавливающий катализатор и растворитель, используемые в восстановительном деарилметилировании в стадии a, а оставить их в реакционной смеси, полученной при восстановительном деарилметилировании в стадии a и использовать in situ (на месте) в последующем восстановительном деарилметилировании на стадии b.
Восстановительным деарилметилированием (в отсутствие ацилирующего агента) на стадии b по способу, описываемому реакционной схемой 3, синтезируют WAnH(6-n) (где n равно 4 или 5), который затем ацилируют на стадии c по способу, описываемому реакционной схемой 3.
Что касается ацилирующего агента, растворителя и реакционных условий (температура реакции и тому подобные), используемых в ацилировании на стадии c по способу, описываемому реакционной схемой 3, то могут быть использованы те же соединения и параметры, которые указаны для реакции ацилирования по реакционной схеме 1, приведенной выше.
Полученная при восстановительном деарилметилировании реакционная смесь (в отсутствие ацилирующего агента) на стадии b по способу, описываемому реакционной схемой 3, приведенной выше, может быть подвергнута in situ (на месте) ацилированию с помощью ацилирующего агента на стадии c по способу, описываемому реакционной схемой 3. Или же иначе, реакционная смесь, полученная восстановительным деарилметилированием на стадии b, может быть подвергнута ацилированию на стадии c после удаления из реакционной смеси катализатора восстановления и/или растворителя.
Выделение и очистку полученного WA6 можно осуществить способом, указанным для реакции по реакционной схеме 1 выше.
WA6 может также быть получен восстановительным деарилметилированием WAnB(6-n) в присутствии ацилирующего агента, как показано следующей реакционной схемой 4: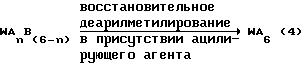
где n обозначает целое число от 4 до 5, A обозначает ацильную группу с 1-10 углеродными атомами, B обозначает арилметильную группу и W представляет шестивалентный остаток гексаазаизовартзитана.
Что касается восстанавливающего агента, катализатора восстановления, ацилирующего агента, растворителя, условий реакции (например, температуры реакции, реакционного давления и тому подобных), то могут быть использованы те же соединения и параметры, что указаны для реакции по реакционной схеме 9 ниже.
WA6 может также быть получен восстановительным деарилметилированием WB6 в присутствии ацилирующего агента, как показано в следующей реакционной схеме 5:
где B обозначает арилметильную группу, A обозначает ацильную группу с 1-10 углеродными атомами и W обозначает шестивалентный остаток гексаазаизовартзитана.
Что касается восстанавливающего агента, катализатора восстановления, ацилирующего агента, растворителя, реакционных условий и тому подобного, используемых в реакции по реакционной схеме 5, приведенной выше, то они могут быть теми же, что указаны для стадии a по способу, описываемому реакционной схемой 3 выше.
Выделение и очистка полученного WA6 могут быть проведены способом, указанным для реакции по реакционной схеме 1 выше.
В качестве другого примера производного гексаазаизовартзитана, содержащего ацильную группу, по данному изобретению может быть упомянуто соединение, представленное формулой WAnH(6-n) (где n равно 4 или 5), которое получают восстановительным деарилметилированием WAnB(6-n) (где n равно 4 или 5) в отсутствие ацилирующего агента, как показано в следующей реакционной схеме 6:
где n обозначает целое число от 4 до 5, A обозначает ацильную группу с 1-10 углеродными атомами, B обозначает арилметильную группу и W обозначает шестивалентный остаток гексаазаизовартзитана.
Что касается восстанавливающего агента, катализатора восстановления, растворителя, реакционных условий и тому подобного, используемых в реакции по реакционной схеме 6, приведенной выше, то здесь могут быть использованы те же, что указаны для стадии a по способу, описываемому реакционной схемой 2, приведенной выше.
WAnH(6-n), полученный реакцией по реакционной схеме 6, может быть выделен общепринятым способом. Например, выделение можно осуществить способом, включающим: удаление катализатора из реакционной смеси после завершения реакции восстановительного деарилметилирования путем фильтрации и получение таким образом фильтрата и отгонку растворителя от полученного фильтрата (см. , например, пример 5).
Содержащее ацильную группу производное гексаазаизовартзитана WAnH(6-n) (где n равно 4 или 5) по данному изобретению может также быть получено путем
a) проведения восстановительного деарилметилирования WB6 и затем,
b) восстановительного деарилметилирования полученного продукта в отсутствие ацилирующего агента, как показано в следующей реакционной схеме 7: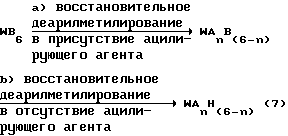
где n обозначает целое число от 4 до 5, A обозначает ацильную группу с 1-10 углеродными атомами, B обозначает арилметильную группу, H обозначает атом водорода и W обозначает шестивалентный остаток гексаазаизовартзитана.
Что касается восстанавливающего агента, катализатора восстановления, ацилирующего агента, реакционных условий и тому подобного, используемых в восстановительном деарилметилировании (в присутствии ацилирующего агента) в стадии a по способу, описываемому приведенной выше реакционной схемой 7, то могут быть использованы те же, что упомянуты для стадии a по способу, описываемому реакционной схемой 3.
Путем восстановительного деарилметилирования (в присутствии ацилирующего агента) на стадии a по способу, описываемому реакционной схемой 7, синтезируют WAnB(6-n) (где n равно 4 или 5) и синтезированный WAnB(6-n) подвергают восстановительному деарилметилированию (в отсутствие ацилирующего агента) на стадии b по способу, описываемому реакционной схемой 7.
Что касается восстанавливающего агента, катализатора восстановления, растворителя, реакционных условий и тому подобного, используемых в восстановительном деарилметилировании (в отсутствие ацилирующего агента) на стадии b по способу, описываемому реакционной схемой 7, то могут быть использованы те, что упомянуты для стадии b по способу, описываемому реакционной схемой 3 выше.
Выделение полученного WAnH(6-n) можно осуществлять способом, указанным для реакции, описываемой реакционной схемой 6 выше.
WAnB(6-n), являющийся исходным веществом для синтеза содержащего ацильную группу производного гексаазаизовартзитана WAnH(6-n) по данному изобретению, может быть получен восстановительным деарилметилированием WB6 в присутствии ацилирующего агента, как показано следующей реакционной схемой 8: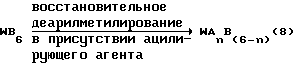
где n обозначает целое число от 4 до 5, A обозначает ацильную группу с 1-10 углеродными атомами, B обозначает арилметильную группу и W обозначает шестивалентный остаток гексаазаизовартзитана.
Что касается восстанавливающего агента, катализатора восстановления, ацилирующего агента, растворителя, реакционных условий и тому подобного, используемых в реакции по схеме 8, приведенной выше, том могут быть использованы те же, что указаны для стадии а по способу, описываемому реакционной схемой 3 выше.
WAnB(n-6), полученный по реакции схемы 8, может быть выделен общепринятым способом. Например, выделение может осуществляться способом, включающим: фильтрацию реакционной смеси, полученной при восстановительном деарилметилировании, с использованием фильтровальной бумаги с целью отделения осадка и катализатора, обработку осадка на фильтровальной бумаге хлороформом с целью растворения в нем осадка; отгонку растворителя и хлороформа из фильтрата до получения твердого остатка; растворение твердого остатка в хлороформе до получения раствора; добавление к полученному раствору водного раствора аммиака; разделение полученной смеси на водную фазу и хлороформную фазу; отделение хлороформной фазы и отгонку растворителя от хлороформной фазы (см. например, пример 19).
В вышеупомянутой реакции восстановительного деарилметилирования в присутствии ацилирующего агента протекает побочная реакция, в которой N-ацильная группа, образовавшаяся в основной реакции, восстанавливается дальше до N-алкильной группы.
Таким образом, как указано выше, данное изобретение обеспечивает также содержащее N-алкильную группу производное гексаазаизовартзитана, представленное следующей формулой XII:
WAnQ(6-n)
где n обозначает целое число от 4 до 5, каждый заместитель A независимо обозначает ацильную группу с 1-10 углеродными атомами, каждый Q независимо обозначает атом водорода или алкильную группу с 1-10 углеродными атомами при условии, что все Q не являются одновременно атомами водорода и W обозначает шестивалентный остаток гексаазаизовартзитана, представленный следующей формулой II: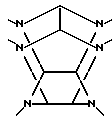
Как упомянуто выше, содержащее N-алкильную группу производное гексаазаизовартзитана можно успешно применять в качестве полифункционального сшивающего агента.
Примеры содержащих N-алкильную группу гексаазаизовартзитанов включают диэтилтетраацетилгексаазаизовартзитан (WA4R2), полученный в примерах 6-12, этилпентаацетилгексаазаизовартзитан (WA5R1), полученный в примерах 13 и 14, и моноалкилтетраацетилгексаазаизовартзитан (WA4RH), показанный в схеме [формула (12)], приведенной в конце описания.
Содержащее N-алкильную группу производное гексаазаизовартзитана может быть получено восстановительным деарилметилированием WAnB(6-n) в присутствии ацилирующего агента, как показано в следующей реакционной схеме 9:
где n обозначает целое число от 4 до 5, A обозначает ацильную группу с 1-10 углеродными атомами, B представляет арилметильную группу, каждый Q независимо обозначает атом водорода или алкильную группу с 1-10 углеродными атомами при условии, что все Q одновременно не могут быть атомами водорода, и W обозначает шестивалентный остаток гексаазаизовартзитана.
Реакция восстановительного деарилметилирования по реакционной схеме 9, приведенной выше, в основном эффективна при тех же условиях, что указаны для реакции восстановительного деарилметилирования на стадии а по способу, описываемому реакционной схемой 2 выше, за тем исключением, что реакцию по схеме 9 проводят в присутствии ацилирующего агента.
В реакции восстановительного деарилметилирования (в присутствии ацилирующего агента) по реакционной схеме 9 упомянутые для стадии а по способу, описываемому приведенной выше реакционной схемой 3, ацилирующие агенты могут быть использованы в основном так же, как описано для этой стадии.
Что касается растворителя, катализатора восстановления, ацилирующего агента, реакционных условий (например, температура реакции и реакционное давление) и тому подобного, используемых в реакции по схеме 9, они могут быть такими же, как указано для стадии а по способу, описываемому реакционной схемой 3 выше.
Полученный по реакционной схеме 9 WAnQ(6-n) может быть выделен общепринятым способом. Например, выделение может быть проведено способом, включающим: удаление катализатора из реакционной смеси путем фильтрации для получения фильтрата и отгонкой от фильтрата растворителя (см. например, пример 6).
WAnQ(6-n) может также быть получен восстановительным деарилметилированием WB6 в присутствии ацилирующего агента, как показано в следующей реакционной схеме 10: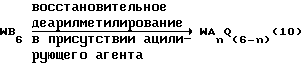
где n обозначает целое число от 4 до 5, A обозначает ацильную группу с 1-10 углеродными атомами, B обозначает арилметильную группу, каждый Q независимо обозначает атом водорода или алкильную группу с 1-10 углеродными атомами при условии, что все Q одновременно не могут быть атомами водорода, и W обозначает шестивалентный остаток гексаазаизовартзитана.
Что касается растворителя, катализатора восстановления, ацилирующего агента, реакционных условий и тому подобного, используемых в реакции по схеме 10, то могут быть использованы те, что указаны для стадии а по способу, описываемому реакционной схемой 3 выше.
Выделение полученного WAnQ(6-n) может быть выполнено способом, указанным для реакции по схеме 9 выше.
В WB6 и WAnB(6-n) (где n равно 4 или 5), каждый из которых может быть использован в качестве исходного вещества для синтеза содержащего ацильную группу производного гексаазаизовартзитана по данному изобретению, арилметильная группа, обозначенная B, является метильной группой, замещенной арильной группой, и обычно содержит 7-21 углеродных атомов. Характерная структура арилметильной группы B изображена следующей структурной формулой XIII:
-CH2Ar
где Ar обозначает ароматическую группу с 6-20 углеродными атомами.
Число углеродных атомов в Ar формулы XIII, приведенной выше, обычно находится в интервале от 6 до 20, предпочтительно от 6 до 10, наиболее желательно составляет 6. Примеры Ar включает фенильную группу; алкилфенильные группы, такие как толилгруппа (о-, м-, и п-изомеры), этилфенильная группа (о-, м- и п-изомеры) и ксилилгруппа; алкоксифенильные группы, такие как метоксифенильная группа (о-, м- и п-изомеры), этоксифенильная группа (о-, м- и п-изомеры) и бутоксифенильная группа (о-, м- и п-изомеры); и незамещенные и замещенные нафтилгруппы. Из них предпочтительны фенильная группа и алкоксифенильная группа. В каждом WB6 и WAnB(6-n) (где n равно 4 или 5) арилметильные группы могут быть одинаковыми или различными.
Содержащее ацильную группу производное гексаазаизовартзитана по данному изобретению, обозначенное формулой I: WAtQ(6-t) (где t является целым числом от 4 до 6), может быть синтезировано различными способами, описанными выше.
Наиболее характерная особенность способов получения содержащего ацильную группу производного гексаазаизовартзитана по данному изобретению, представленного реакционной схемой 1, состоит в том, что реакцию восстановительного деарилметилирования WB6 проводят в присутствии ацилирующего агента.
Это взаимодействие описывается следующей реакционной схемой 11: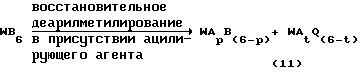
где p обозначает целое число от 1 до 5, t обозначает целое число от 4 до 6, B обозначает арилметильную группу, A обозначает ацильную группу с 1-10 углеродными атомами, каждый Q независимо обозначает атом водорода или алкильную группу с 1-10 углеродными атомами и W обозначает шестивалентный остаток гексаазаизовартзитана.
Молярное отношение WApB(6-p) к WAtQ(6-t) в реакционной смеси, полученной в реакции по схеме 11, приведенной выше, составляет обычно от 0,001 до 1,000, предпочтительно от 0,01 до 100.
Что касается растворителя, катализатора восстановления, ацилирующего агента, реакционных условий и тому подобного, используемых в реакции по схеме 11, то их можно использовать такими же, как указаны выше для реакции по схеме 8.
В ходе получения содержащего ацильную группу производного гексаазаизовартзитана по данному изобретению, представленного формулой I-a, путем восстановительного деарилметилирования WB6 в присутствии ацилирующего агента, важно, чтобы были последовательно выполнены: a) образование N-H-группы при восстановительном элимировании арилметильной группы B, и b) образование N-ацильной группы при ацилировании N-H-группы.
Приведенная выше реакционная схема 11 указывает, что из WB6 образуется не только WApB(6-p) (где p обозначает целое число от 1 до 5), но также WAnH(6-n) путем дальнейшего взаимодействия WApB(6-p).
В реакционной схеме 11, реакцию восстановительного деарилметилирования обрывают после того, как получают реакционную смесь [включающую WApB(6-p) и WAtQ(6-t))] заданного состава. В частности, протекание реакции деарилметилирования контролируют с помощью газовой хроматографии или жидкостной хроматографии, и реакцию обрабатывают после получения реакционной смеси, имеющей заданный состав.
Ниже, сначала приводится объяснение предполагаемого пути протекания реакции по схеме 11, а затем дается объяснение относительно полезности и применения реакции по схеме 11.
Предполагаемый ход реакции по схеме 11 подробно описан в схеме [формула (12)], приведенной в конце описания. Поскольку N-алкильная группа может быть получена путем восстановления (в качестве побочной реакции) N-ацильной группы, чье восстановление может протекать в зависимости от реакционных условий, получаемое побочно содержащее N-алкильную группу производное гексаазаизовартзитана также описано в схеме [формула (12)]. В схеме [формула (12)], A обозначает ацильную группу с 1-10 углеродными атомами, B обозначает арилметильную группу, R обозначает алкильную группу с 1-10 углеродными атомами, H обозначает атом водорода и W обозначает шестивалентный остаток гексаазаизовартзитана.
Когда реакция по схеме 11 выполняется способом периодической загрузки, соотношения получаемых реакционных продуктов изменяются в зависимости от реакционного времени. Когда реакцию по схеме 11 осуществляют непрерывным способом, соотношения полученных реакционных продуктов изменяются в зависимости от времени контакта. Кроме того, соотношения полученных реакционных продуктов могут также изменяться в зависимости от типов используемых катализаторов и растворителя, реакционной температуры и тому подобного. Поэтому в реакции по схеме 11, соотношения реакционных продуктов могут быть изменены в заданной пропорции путем соответствующего подбора реакционных условий.
Практическое применение реакции по схеме 11 описано подробно ниже.
При попытке получить содержащее ацильную группу производное гексаазаизовартзитана по данному изобретению из WB6 сначала восстановительным деарилметилированием WB6 в отсутствие ацилирующего агента, что дает WHnB(6-n) (где n обозначает целое число от 1 до 6), и затем ацилированием полученного WHnB(6-n) заданный продукт не может быть получен с высоким выходом из-за распада W-скелета. Предполагается, что причина этого состоит в том, что образующиеся путем восстановительного деарилметилирования WB6 в отсутствие ацилирующего агента, содержащие вторичную аминогруппу производные гексаазаизовартзитана (такие как WH5, WH2B4 и WH3B3) структурно неустойчивы. В противоположность этому, использованием способа по данному изобретению, основанного на реакции по схеме 11, в котором восстановительное деарилирование WB6 осуществляют в присутствии ацилирующего агента, содержащее ацильную группу производное гексаазаизовартзитана может быть синтезировано без разрушения W-скелета. Предполагается, что причина этого состоит в том, что в реакции по схеме 11 нестабильные, содержащие вторичную аминогруппу производные гексаазаизовартзитана (такие как WHB5 и WH2B4) (которые получаются в начальной стадии реакции) сразу же ацилируются и таким образом стабилизируются в реакционной системе, так что распад W-скелета подавляется, тем самым давая возможность дальнейшему протеканию деарилметилирования и ацилирования.
Как описано выше, производное гексаазаизовартзитана, содержащее ацильную группу, по данному изобретению представленное формулой I-a может быть синтезировано на начальной стадии путем восстановительного деарилметилирования WB6 в присутствии ацилирующего агента. Однако при попытке выполнить реакцию в одну стадию одновременно образуется целый ряд реакционных продуктов и в значительной степени протекают побочные реакции. Задача данного изобретения состоит в разработке способа, позволяющего решить эти проблемы и получить WAtH(6-t) (где t обозначает целое число от 4 до 6) преимущественно в промышленном масштабе, с высокой селективностью и высоким выходом. В результате найдено, что при проведении вышеуказанных реакций по схемам 8, 6 и 1 в перечисленном порядке, могут быть достигнуты очень хорошие результаты.
Далее приведено более подробное объяснение каждой из реакций по схемам 8, 6 и 1.
I. Реакция по схеме 8.
Для получения WAnB(6-n) с высоким выходом в вышеуказанной реакции по схеме 8 могут быть использованы различные способы. Примеры таких способов включают:
1) способ, по которому типы и количества реакционных реагентов выбирают так, что реакция восстановительного деарилметилирования может быть прервана до завершения;
2) способ, по которому ход реакции восстановительного деарилметилирования контролируют с помощью газовой хроматографии или жидкостной хроматографии и реакцию обрывают в заданный момент времени; и
3) способ, по которому используют растворитель, являющийся хорошим растворителем для WB6, но плохим растворителем для WAnB(6-n) (например, ароматическое соединение, такое как этилбензол или толуол), с тем чтобы вызывать осаждение WAnB(6-n), полученного восстановительным деарилметилированием WB6, из реакционной смеси.
Из приведенных выше способов 1), 2) и 3) способ 3) наиболее выгоден в промышленном отношении с точки зрения легкости в эксплуатации.
В реакции по схеме 8 для подавления побочных реакций с целью улучшения селективности в отношении WAnB(6-n) выгодно использовать в качестве ацилирующего агента сложный эфир карбоновой кислоты N-гидроксисукцинимида, такой как N-ацетоксисукцинимид, или смесь сложного эфира карбоновой кислоты N-гидроксисукцинимида и ангидрида карбоновой кислоты. При использовании такого ацилирующего агента могут быть улучшены не только селективность в отношении WAnB(6-n), но также выход WAnB(6-n). Причина, по которой селективность в отношении WAnB(6-n) улучшается при использовании сложного эфира карбоновой кислоты и N-гидроксисукцинимида в качестве ацилирующего агента, пока не установлена. Однако предполагается, что различие в селективности по отношению к WAnB(6-n) между сложным эфиром карбоновой кислоты и N-гидроксисукцинимидом и другими ацилирующими агентами, такими как ангидрид карбоновой кислоты, объясняется не только различиями в реакционной способности, но также специфичностью субстрата, обусловленной стерическими препятствиями (включая специфическую трехмерную структуру и объемность) ацилирующего агента.
Приведенный выше факт, состоящий в том, что при использовании сложного эфира карбоновой кислоты N-гидроксисукцинимида в качестве ацилирующего агента значительно увеличивается селективность в отношении WAnB(6-n), впервые был установлен настоящими заявителями. Это открытие является очень важным при синтезе WAnB(6-n) в промышленных масштабах.
II. Реакция по схеме 6.
Когда восстановительное деарилметилирование WAnB(6-n), полученного в реакции по схеме 8, проводят в присутствии ацилирующего агента с целью синтеза WA6, легко протекают побочные реакции, такие как образование N-алкила в результате восстановления N-ацила, так что становится трудно синтезировать WA6 с высокой селективностью.
В противоположность этому, когда восстановительное деарилметилирование WAnB(6-n) проводят в отсутствие ацилирующего агента, как показано в реакции по схеме 6, побочные реакции, такие как образование N-алкильной группы, подавляются, так что реакция восстановительного деарилметилирования протекает с высокой селективностью. Данное явление установлено настоящими заявителями. Из реакционной смеси, полученной при реакции восстановительного деарилметилирования по схеме 6, путем простой операции выделения может быть получен высокой чистоты WAnH(6-n) с высоким выходом. Поэтому эта реакция по схеме 6 очень полезна при синтезе WAnH(6-n).
Как упомянуто выше, при проведении реакции восстановительного деарилметилирования WB6 в отсутствие ацилирующего агента, полученный WHnB(6-n) (где n обозначает целое число от 1 до 6) нестабилен в реакционной системе, так что трудно получить WHnB(6-n) с высоким выходом. В противоположность этому, как упомянуто выше, WAnH(6-n) (где n обозначает целое число от 4 до 5) стабилен в реакционной системе, так что WAnH(6-n) может быть синтезирован с высоким выходом.
Причина, по которой WHnB(6-n) (где n обозначает целое число от 1 до 6) и WAnH(6-n) (где n обозначает целое число от 4 до 5) обладают отличными друг от друга свойствами, до сих пор не выяснена. Однако предполагается, что различие в свойствах между арилметильной группой B и ацильной группой A вызывает различие в стабильности между соответствующими скелетами гексаазаизовартзитана WHnB(6-n) и WAnH(6-n).
Вышеупомянутое различие в свойствах между WHnB(6-n) (где n обозначает целое число от 1 до 6) и WAnH(6-n) (где n обозначает целое число от 4 до 5) впервые было найдено настоящими заявителями. Кроме того, соединение гексаазаизовартзитана, представленное формулой WAnH(6-n) (где n обозначает целое число от 4 до 5), нигде в литературе не описано и впервые синтезировано по способу настоящих заявителей.
III. Реакция по схеме 1.
Как упомянуто выше в разделе "известный уровень техники", WAnH(6-n) (где n обозначает целое число от 4 до 5) как таковое может успешно применяться в качестве различных функциональных соединений, таких как исходное соединение для производного полинитрогексаазаизовартзитана и сырье для высокополярного полимера. При желании WAnH(6-n) (где n обозначает целое число от 4 до 5) легко может быть превращено в WA6 осуществлением реакции по схеме 1.
WA6 нигде не описан в литературе и впервые синтезирован настоящими заявителями. WA6 также можно успешно использовать в качестве различных функциональных соединений, как и в случае WAnH(6-n) (где n обозначает целое число от 4 до 5).
Содержащее ацильную группу производное гексаазаизовартзитана по данному изобретению, представленное формулой I-a: WAtH(6-t) (где t обозначает целое число от 4 до 6) может быть использовано в качестве исходного соединения в реакции нитрования с целью получения производного полинитрогексаазаизовартзитана.
Приведенное далее пояснение дает пример способов проведения реакции нитрования WAtH(6-t) (где t обозначает целое число от 4 до 6) по данному изобретению с целью превращения его N-H-группы и N-A-группы в N-NO2-группы.
N-H-группа группы WAnH(6-n) (где n обозначает целое число от 4 до 5) по данному изобретению может быть превращена в N-NO2-группу различными способами нитрования. Например, WAnH(6-n) (где n обозначает целое число от 4 до 5) может быть легко превращен в WAn(NO2)(6-n) (где n обозначает целое число от 4 до 5) в одну стадию. Однако с точки зрения повышения выхода заданного WAn(NO2)(6-n) предпочтительно проводить превращение N-H-группы в N-NO2-группу способом, включающим две стадии, как показано ниже в реакционной схеме 13.
Схематично, как показано в реакционной схеме 13 ниже, N-H-группу WAnH(6-n) нитрозируют до N-NO-группы, и N-NO-группу нитруют до N-NO2-группы, получая тем самым WAn(NO2)(6-n).
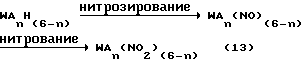
где n обозначает целое число от 4 до 5, A обозначает ацильную группу с 1-10 углеродными атомами, H обозначает атом водорода, (NO) обозначает нитрозогруппу, (NO2) обозначает нитрогруппу и W обозначает шестивалентный остаток гексаазаизовартзитана.
В качестве нитрозирующего агента, используемого по способу схемы 13, может применяться любой нитрозирующий агент при условии, что он способен нитрозировать WAnH(6-n) до WAn(NO)(6-n). Обычно в качестве нитрозирующих агентов используют смесь нитрита натрия и кислоты; N2O4; нитрозилхлорид и тому подобные.
Температура реакции нитрозирования обычно находится в интервале от -50oC до 200oC, предпочтительно от -30oC до 100oC, более желательно от -20oC до 50oC.
В качестве окисляющего агента, используемого в реакции нитрования по способу схемы 13, может быть использован любой окисляющий агент, способный окислять нитрозогруппу до получения нитрогруппы. Обычно примеры окисляющих агентов включают азотную кислоту и перекись водорода. Из них предпочтительна азотная кислота. Эти окисляющие агенты могут быть использованы индивидуально или в комбинации.
Температура реакции окисления обычно находится в интервале от -50oC до 200oC, предпочтительно от -30oC до 130oC, более желательно от -20oC до 60oC.
Также N-A-группа WAtH(6-t) (где t обозначает целое число от 4 до 6) по данному изобретению может быть легко превращена в N-NO2-группу путем нитрования азотной кислотой или смесью азотной кислоты и пятиокиси азота, как очевидно из примера 21 (ниже). Например, WA6 может быть превращен в производное полинитрогексаазаизовартзитана, такое как WA4(NO2)2, различными способами нитрования, например использованием смеси азотной кислоты и пятиокиси азота в качестве нитрующего агента.
Далее, как показано в реакционной схеме 14 ниже, различные производные гексаазаизовартзитана, представленные формулой WAnE(6-n), можно нитровать до получения гексанитрогексаазаизовартзитана [W(NO2)6].
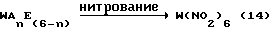
где n обозначает целое число от 4 до 6, A обозначает ацильную группу с 1-10 углеродными атомами, E обозначает нитрозогруппу или нитрогруппу и W обозначает шестивалентный остаток гексаазаизовартзитана.
В качестве нитрующего агента, используемого при превращении N-A-группы WAnE(6-n) в N-NO2-группу, может применяться любой нитрующий агент, способный превращать N-A-группу в N-NO2-группу. Например, могут быть использованы различные нитрующие агенты, содержащие азотную кислоту. Иллюстративные примеры нитрующих агентов включают нитрующие агенты, содержащие сильную протонную кислоту, такие как азотно-кислотные/серно-кислотные нитрующие агенты или нитрующие агенты, содержащие азотную кислоту/трифторуксусную кислоту.
Реакционная температура для реакции по схеме 14 обычно находится в интервале от -50oC до 120oC, предпочтительно от -20oC до 60oC.
Реакционное время для реакции по схеме 14 обычно составляет 0,1-500 часов, предпочтительно 1-200 часов.
Как описано выше, N-H-группа и N-A-группа W-скелета являются функциональными группами, которые легко можно превратить в нитрогруппы. Поэтому, используя WAtH(6-t) (где t обозначает целое число от 4 до 6) в качестве промежуточного продукта, можно получить различные производные полинитрогексаазаизовартзитана с высоким выходом.
Как видно из приведенного выше, данное изобретение дает способ получения гексанитроазаизовартзитана, представленного следующей формулой IX:
W(NO2)6
где NO2 обозначает нитрогруппу и W обозначает шестивалентный остаток гезаазаизовартзитана, представленный следующей формулой II: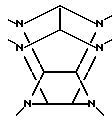
который включает нитрование нитрующим агентом по крайней мере одного соединения, выбираемого из группы, состоящей из соединений, которые соответственно представлены следующими формулами:
формулой III
WA6
где каждый A независимо обозначает ацильную группу с 1-10 углеродными атомами и W - такой, как определено выше,
формулой IV
WAnH(6-n)
где n обозначает целое число от 4 до 5, H обозначает атом водорода и каждый из A и W - такие, как определено выше,
формулой VII
WAn(NO)(6-n)
где NO обозначает нитрозогруппу и каждый из n, A и W - такие, как определено выше, и
формулой VIII
WAn(NO2)(6-n)
где каждый из n, A, NO2 и W - такие, как определено выше.
Производное полинитрогексаазаизовартзитана, полученное из содержащего ацильную группу производного гексаазаизовартзитана по данному изобретению, может быть успешно применено в качестве присадки для модификации свойств ракетного топлива и взрывчатых веществ, таких как механические свойства, скорость детонации, детонационное давление, скорость горения, показатель давления, чувствительность, устойчивость к нагреванию и тому подобных, а также в качестве вещества с высокими характеристиками для взрывчатых веществ.
Ниже описаны преимущества производного полинитрогексаазаизовартзитана, полученного из содержащего ацильную группу производного гексаазаизовартзитана по данному изобретению.
Например, WA4(NO2)2 обладает следующими преимущественными свойствами:
1) WA4(NO2)2 имеет такую же молекулярную структуру, как структура взрывчатого соединения с высокими характеристиками, представляющая собой циклическую структуру, содержащую полинитрамингруппу, как у HNW - циклотетраметилентетранитрамина (далее обозначенного для простоты "HMX") и циклотриметилентринитрамина (далее обозначенного для простоты "RDX"), и обладает отличной температурной устойчивостью по сравнению с HNW, HMX и RDX. [Даже когда WA4(NO2)2 используют в качестве присадки к ракетному топливу или взрывчатым соединениям, не существует опасности того, что оно заметно снизит устойчивость к нагреванию ракетного топлива и взрывчатых веществ].
2) В отличие от вышеуказанных нитраминсоединений (т.е. HNW, HMX и RDX) WA4(NO2)2 содержит в своем скелете не только N-нитрогруппу, но также N-A-группу, так что обладает высоким сродством к связывающему веществу, такому как полиуретан.
Добавлением WA4(NO2)2, имеющего вышеупомянутые преимущества в свойствах, к ракетному топливу или взрывчатым соединениям, содержащим нитраминсоединение (такое как HNW, HMX, RDX или тому подобное) и связывающее вещество, такое как полиуретан, можно улучшить адгезию между твердым компонентом (т.е. нитраминсоединением) и связывающим веществом.
WA4(NO2)2 легко можно превратить в HNW путем нитрования, так что он полезен в качестве сырья для получения HNW. HNW имеет высокую плотность и высокую энергию, так что он очень полезен в качестве окислителя для взрывчатых веществ с высокими характеристиками и недымящего ракетного топлива.
Взаимодействием тетраацилгексаазаизовартзитана WA4H2 по данному изобретению с производным дикарбоновой кислоты, таким как галоидангидрид дикарбоновой кислоты или сложный диэфир дикарбоновой кислоты, можно получить высокополярный полимер, имеющий скелет гексаазаизовартзитана в основной цепи.
При синтезе содержащего ацильную группу производного гексаазаизовартзитана WAnH(6-n) (где n обозначает целое число от 4 до 6) по данному изобретению с использованием ацилирующего агента, имеющего специфическую функциональную группу, можно получить способный сшиваться полиацилгексаазаизовартзитан.
WAnH(6-n) (где n обозначает целое число от 4 до 6) по данному изобретению, сам по себе, может быть использован в качестве присадок, таких как полимерный модификатор.
Схема превращений, показывающая предпочтительные воплощения способов получения, входящих в данное изобретение, приведена к конце описания.
Как видно из приведенной схемы превращений, содержащее ацильную группу производное гексаазаизовартзитана WAtQ(6-t) (где W обозначает шестивалентный остаток гексаазаизовартзитана, каждый Q независимо обозначает атом водорода или C1-C10-алкильную группу и t равно от 4 до 6) по данному изобретению может быть получено из гексакис(арилметил)гексаазаизовартзитана WB6 (где W имеет принятые выше обозначения и B обозначает C7-C21-арилметильную группу), непосредственно или через содержащее ацильную группу и арилметильную группу производное гексаазаизовартзитана WAnB(6-n) (где W и B - такие, как определены выше и n равно 4 или 5) или WApB(6-p), (где W и B - такие, как определены выше и p равно от 1 до 5). Содержащее ацильную группу производное гексаазаизовартзитана WAtQ(6-t) (где W, A, Q и t - такие, как определены выше) легко можно превратить в гексанитрогексаазаизовартзитан W(NO2)6 (где W - такой, как определено выше) с высоким выходом непосредственно, или через содержащее нитрозогруппу производное гексаазаизовартзитана WAn(NO)(6-n) (где W и A - как определены выше и n равно 4 или 5) и/или содержащее нитрогруппу производное гексаазаизовартзитана WAn(NO2)(6-n) (где W и A - такие, как определены выше и n равно 4 или 5).
Ниже данное изобретение описано более подробно в примерах и примерах сравнения, которые не следует считать ограничивающими рамки объема данного изобретения и приложенных пунктов.
Разнообразные измерения проведены следующими способами:
(1) H-ЯМР:
использован JNM-FX-200 (изготовлен и реализован JEOL LTD, Japan).
(2) 13C-ЯМР:
использован JNM-GX-400 (изготовлен и реализован JEOL LTD, Japan).
(3)13C-1H COSY ЯМР: 13С-1H корреляции сдвига:
использован JNM-GX-400. В этом способе измеряют взаимодействие между 13C и 1H. По этому способу, когда идентифицируют пик, относящийся либо к 13C, либо к 1H, можно определить химический сдвиг либо 1H, химически связанного с 13C, либо 13C, имеющего химически связанный с ним 1H.
(4) EI (электронное соударение)-масс-спектрометрия: используют HP 5790B (изготовлен и реализован Hewlett Packard Company, USA).
(5) GC (газовая хроматография)-масс-спектрометрия:
1) используют HP5890A (изготовлен и реализован Hewlett Packard Company, USA).
2) колонка: металлическая капиллярная колонка, 0,25 мм (внутренний диаметр) х 15 мм, Ultra ALLOY (HT) (колонка для использования в условиях повышенной температуры), толщина пленочного покрытия на внутренней стенке капилляра: 1,15 мкм.
3) температура: колонка; используют повышенную температуру от 100oC до 340oC при скорости повышения температуры 20oC/мин, и поддерживают температуру при 340oC в течение 20 мин,
на выходе: 340oC,
GM/MS соединение: 340oC,
4) газ-носитель: гелий (скорость потока поступающего в прибор газообразного гелия 100 мл/мин, давление колонки 100 kPa).
(6) FD (десорбция поля)-масс-спектрометрия, используют JEOL HX-110 (изготовлен и реализован JEOL LTD., Japan). Образец в несколько мг растворяют приблизительно в 10 мкл метанола до получения раствора. Несколько мкл полученного раствора наносят на эмиттер и осуществляют измерение.
(7) Инфракрасная абсорбционная спектрометрия.
Измерения проводят способом KBr-таблеток, используя FT/IR-5M (изготовлен и реализован Japan Spectroscopic Co., Ltd., Japan).
(8) Дифференциальный сканирующий калориметр (DSC). Используют DSC-220 (изготовлен и реализован Seiko Instruments Inc., Japan).
(9) Жидкостная хроматография с высокими рабочими характеристиками.
Измерения проводят в указанных ниже условиях, используя описанную ниже аппаратуру:
1) Аппаратура: 610 ISOCRATIC System (изготовлена и реализована Waters Assoc. Co., USA): 600 - контроллер,
600 - контроллер, 600E - насос,
600E - насос, 486 - регулируемый абсорбционный детектор.
486 - регулируемый абсорбционный детектор.
2) Колонка: μ/ -Bondasphere (изготовлена и реализована Waters Assoc. Co. , USA): диаметр частиц 5 мкм,
диаметр частиц 5 мкм, материал заполнения C18,
материал заполнения C18, размер пор 100
размер пор 100 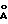 ,
, размер колонки 3,9 мм х 15 см.
размер колонки 3,9 мм х 15 см.
3) Жидкая подвижная фаза: ацетонитрил/вода 60/40.
4) Объемная скорость потока: 0,5 мл/мин.
5) Температура колонки: 40oC.
В приведенных ниже спектрах ЯМР:
с - синглет;
д - дублет;
т - триплет;
м - мультиплет.
Пример 1. Синтез WA6 ацетилированием WA4H2.
1,0 г (2,98 ммоль) тетраацетилгексаазаизовартзитана растворяют в 100 мл уксусного ангидрида. К полученному раствору добавляют 5 г (63,7 ммоль) ацетилхлорида и образовавшуюся смесь перемешивают 1 час для протекания реакции. После чего растворитель отгоняют при пониженном давлении от образовавшейся реакционной смеси до получения остатка. Полученный остаток растворяют в этилацетате. К образовавшемуся раствору добавляют гексан до получения осадка, представляющего собой белую массу гексаацетилгексаазаизовартзитана (1,16 г; выход: 93%).
Полученный гексаацетилгексазаизовартзитан помещают в сублиматор и затем прибор погружают в масляную баню при 270oC. Установлено, что гексаацетилгексаазаизовартзитан сублимируется при пониженном давлении (10 мм рт.ст.).
Ниже приведены результаты анализа гексаазаизовартзитана.
Результаты ПМР [растворитель: CDCl3; стандарт: тетраметилсилан (далее обозначенный, как общепринято, "ТМС"); температура измерения: 60oC; единицы: δ (м.д.)]:
2,05 (с, 6H, COCH3), 2,14 (с, 6H, COCH3), 2,41 (с, 6H, COCH3), 6,42 (с, 2H, CH), 6,48 (с, 2H, CH) и 6,94 (д, 2H, CH).
ПМР идентифицировано 6 атомов водорода W-скелета и 6 ацетильных групп.
Результаты 13C-ЯМР [растворитель, CDCl3; стандарт: ТМС: единицы δ (м.д. )]:
20,74 (CH3), 21,55 (CH3), 61,09 (CH), 66,55 (CH), 72,17 (CH), 167,60 (C= O), 168,31 (C=O) и 169,79 (C=O).
Методом 13C-ЯМР идентифицированы атом углерода метильной группы и атом углерода карбонильной группы, обе группы принадлежат ацетильной группе, и атомы углерода W-скелета.
Методом 13C-1H COSY, можно идентифицировать 13C, связанные с соответствующими 1H, идентифицированными выше ПМР.
Результаты EI-масс спектрометрии (m обозначает молекулярный вес исходной молекулы):
420 (5%, m/z), 377 [5%, (m минус молекулярный вес COCH3)/z], 335 (10%), 295 (15%), 208 (12%), 165 (10%), 123 (12%) и 43 (100%, COCH3).
Методом EI-масс-спектрометрии идентифицируют исходный ионный пик (420) гексаацетилгексаазаизовартзитана, ионный пик (377), отнесенный к остаточной молекуле, структура которой предположительно образуется отщеплением ацетильной группы от исходной молекулы, и ионный пик (43), относящий к ацетильной группе.
Результаты инфракрасной абсорбционной спектрометрии KBr-способом показывают абсорбцию около 1660 см-1, где абсорбция отнесена к колебанию растяжения карбонильной группы (C=O), входящей в ацетильную группу.
Пример 2. Синтез WA6 из WA4B2.
3,67 г (7,11 ммоль) тетраацетилдибензилгексаазаизовартзитана, 1,6 г (7,11 ммоль) Pd(OAc)2 в качестве катализатора восстановления и 150 мл уксусной кислоты вносят вместе с перемешивающим элементом в 300 мл микробомбу. Бомбу продувают газообразным азотом. Затем в бомбу вводят газообразный водород, так чтобы внутреннее давление в бомбе стало 5 кгс/см2 - G, и затем содержимое бомбы перемешивают 15 часов для осуществления реакции. Образовавшуюся реакционную смесь вынимают из бомбы и фильтруют для удаления катализатора. Затем полученный фильтрат перегоняют при пониженном давлении для отгонки растворителя, получая таким образом твердый остаток. Образовавшийся твердый остаток промывают 100 мл этилацетата. Полученный белый твердый остаток растворяют в 200 мл уксусного ангидрида. К образовавшемуся раствору добавляют 5 г (63,7 ммоль) ацетилхлорида и полученную смесь перемешивают 1 час. После чего растворитель отгоняют при пониженном давлении от реакционной смеси. Образовавшийся остаток перекристаллизовывают из толуола, получая 2,09 г гексаацетилгексаазаизовартзитана в виде белой массы (выход, 70%).
Пример 3. Синтез WA6 из WA4B2, в котором реакционную смесь, полученную восстановительным деарилметилированием подвергают на месте ацетилированию без удаления катализатора и растворителя.
Восстановительное дефенилметилирование тетраацетилдибензилгексаазаизовартзитана проводят в основном тем же способом, что и в примере 2, получая таким образом реакционную смесь, содержащую катализатор восстановления и растворитель. К реакционной смеси добавляют 5 г (63,7 ммоль) ацетилхлорида (ацетилирующий агент) и полученную реакционную смесь перемешивают 3 часа для протекания реакции. Образовавшуюся реакционную смесь фильтруют, удаляя таким образом катализатор. Полученный фильтрат перегоняют при пониженном давлении для отгонки растворителя. Образовавшийся твердый остаток перекристаллизовывают из толуола, получая таким образом 1,92 г гексаацетилгексаазаизовартзитана в виде белой массы (выход: 64%).
Пример 4. Синтез WA6 из WB6.
1,89 г (2,66 ммоль) гексабензилгексаазаизовартзитана, 1,70 г (1,60 мг-атом) Pd-C (содержание Pd: 10%) в качестве катализатора восстановления, 5,0 г (31,8 ммоль) N-ацетоксисукцинимида (ацетилирующий агент), 160 мл этилбензола и 3,24 г (31,8 ммоль) уксусного ангидрида (ацетилирующий агент) вносят вместе с перемешивающим элементом в 300 мл микробомбу. Бомбу продувают газообразным водородом. Затем газообразный водород подают в бомбу так, чтобы внутреннее давление в бомбе стало 10 кгс/см2 - G, и затем бомбу погружают в масляную баню при 60oC. Затем содержимое бомбы перемешивают 40 часов для осуществления реакции. Полученной реакционной смеси дают охладиться до комнатной температуры. После чего реакционную смесь, содержащую WAnB(6-n) (где n равно 4 или 5), в виде осадка вынимают из бомбы и фильтруют для отделения фильтрацией осадка и катализатора восстановления. Полученный осадок, извлеченный катализатор восстановления и 50 мл уксусной кислоты в качестве растворителя вносят в 300 мл микробомбу. В бомбу подают газообразный водород, так чтобы внутреннее давление в бомбе стало 5 кгс/см2 - G, и содержимое бомбы перемешивают 20 часов для протекания реакции. После завершения реакции к полученной реакционной смеси добавляют 5 г (63,7 ммоль) ацетилхлорида и смесь перемешивают 1 час. Образовавшуюся смесь перегоняют при пониженном давлении для отгонки растворителя, получая таким образом твердый остаток. К полученному твердому остатку добавляют 200 мл хлороформа, так чтобы твердый остаток, содержащий в основном WA6, растворился в хлороформе. Образовавшийся раствор фильтруют с целью удаления катализатора. Полученный фильтрат перегоняют при пониженном давлении, отгоняя таким образом растворитель. Образовавшийся остаток перекристаллизовывают из толуола, получая 0,50 г гексаацетилгексаазаизовартзитана (выход: 45%) в виде белой массы.
Пример 5. Синтез WAnH(6-n) и WA6 из WB6.
Восстановительное дебензилирование гексабензилгексаазаизовартзитана в присутствии ацетилирующих агентов осуществляют в основном тем же способом, что в примере 4, получая таким образом реакционную смесь, содержащую WAnB(6-n) (где n равно 4 или 5). После завершения реакции реакционную смесь, содержащую осадок, извлекают из бомбы и фильтруют, используя фильтровальную бумагу, чтобы отфильтровать осадок и катализатор восстановления. Осадок на фильтровальной бумаге обрабатывают на месте 200 мл хлороформа, чтобы растворить в нем осадок. Фильтрат (содержащий хлороформ, использованный для обработки) перегоняют с целью отгонки растворителя (этилбензол и хлороформ). Полученный твердый остаток растворяют в 200 мл хлороформа до получения раствора. К раствору добавляют водный 28% раствор аммония и образовавшуюся смесь энергично перемешивают 30 минут, так чтобы реакционная смесь распределилась между водной фазой и хлороформной фазой, где N-ацетоксисукцинимид разлагается и переходит в водную фазу. Хлороформную фазу отделяют и перегоняют, отгоняя растворитель (хлороформ). Образовавшийся белый твердый остаток растворяют в 50 мл уксусной кислоты. К полученному раствору добавляют 0,6 г (2,66 ммоль) Pd(OAc)2 в качестве катализатора восстановления. Раствор, содержащий катализатор восстановления, вносят в 100 мл - микробомбу. Бомбу заполняют газообразным водородом, так чтобы внутреннее давление бомбы стало 5 кгс/см2 - G, и содержимое бомбы перемешивают 20 часов для протекания реакции (к этому времени выход гексаацетилгексаазаизовартзитана составляет 0,3% по данным газовой хроматографии). К реакционной смеси добавляют 5 г (63,7 ммоль) ацетилхлорида и образовавшуюся смесь перемешивают 1 час. После чего растворитель (уксусная кислота) отгоняют от смеси, получая твердый остаток. К образовавшемуся твердому остатку добавляют 200 мл хлороформа. Полученный раствор фильтруют с целью удаления катализатора. Оставшийся фильтрат перегоняют, отгоняя растворитель и получая таким образом твердый остаток. Полученный твердый остаток перекристаллизовывают из толуола, получая 0,39 г гексаацетилгексаазаизовартзитана (выход: 35%).
Это означает, что соединения гексаазаизовартзитана, содержащие вторичную аминогруппу, такие как тетраацетилгексаазаизовартзитан и пентаацетилгексаазаизовартзитан, образовались до добавления ацетилхлорида и что такие соединения, содержащие вторичные аминогруппы, превратились в гексаацетилгексаазаизовартзитан при добавлении ацетилхлорида.
Пример 6. Синтез WA4Et2 (где Et обозначает этильную группу) из WA4B2.
0,50 г (0,97 ммоль) тетраацетилдибензилгексаазаизовартзитана, 0,21 г (0,19 мг-атом) Pd-C (Pd-содержание: 10%) в качестве катализатора восстановления, 2,37 г (23,3 ммоль) уксусного ангидрида (ацетилирующий агент) и 50 мл уксусной кислоты вносят вместе с перемешивающим элементом в 100 мл микробомбу. Бомбу заполняют газообразным водородом. Затем газообразный водород вводят в бомбу так, чтобы внутреннее давление бомбы стало 50 кгс/см2 - G. Затем содержимое бомбы перемешивают 15 часов для протекания реакции. После завершения реакции полученную реакционную смесь вынимают из бомбы и фильтруют, отфильтровывая катализатор восстановления. Полученный фильтрат перегоняют, отгоняя таким образом растворитель (уксусную кислоту). Образовавшийся твердый остаток переосаждают из смеси хлороформа и гексана с целью очистки, получая таким образом диэтилтетраацетилгексаазаизовартзитан. Реакционные условия и выход приведены в таблице.
Результаты анализов диэтилтетраацетилгексаазаизовартзитана приведены ниже.
Результаты EI-масс-спектрометрии:
392 (1%, m/z), 278 (1%), 236 (10%), 193 (25%), 138 (30%), 109 (45%), 97 (20%), 81 (81%), 69 (60%), 56 (20%), 43 (100%, COCH3), 29 (20%, CH2CH3), 28 (52%) и 15 (20%, CH3).
Методом EI-масс-спектрометрии идентифицируют исходный ионный пик (392) тетраацетилдиэтилгексаазаизовартзитана, ионный пик (43) ацетильной группы и ионный пик (29) этильной группы.
Результаты ПМР-спектрометрии [растворитель: CDCl3; стандарт: ТМС; единица: δ (м.д.)]:
1,25 (т. 6H, CH3 этильной группы), 2,14 (с, 12H, COCH3), 2,90 (м, 4H, CH2 этильной группы), 5,20 (д, 2H, CH), 5,74 (д, 2H, CH) и 6,40 (с, 2H, CH).
По ПМР-спектру идентифицируют метиновую группу W скелета, этильную группу и ацетильную группу.
Примеры 7-12. Синтез WA6 и WA4R2 и WA4B2 восстановительным деарилметилированием в присутствии ацилирующего агента и изучения изменения количественного отношения полученного WA6 к полученному WA4R2 в зависимости от реакционных условий.
В примерах 7-12 взаимодействия осуществляют в основном тем же способом, что и в примере 6, за исключением того, что варьируют тип и количество ацилирующего агента, тип растворителя, тип и количество катализатора, давление водорода и время реакции. Реакционные условия и выходы продуктов реакции показаны в таблице.
Как показано в таблице, для получения гексаацетилгексаазаизовартзитана и диэтилтетраацетилгексаазаизовартзитана могут быть использованы различные катализаторы.
Пример 13. Синтез различных производных гексаазаизовартзитана, содержащих ацетильную группу, таких как WA4B2 и WA5B, восстановительным деарилметилированием WB6 в присутствии ацилирующего агента.
Восстановительное дебензилирование гексабензилгексаазаизовартзитана в присутствии ацетилирующего агента проводят в основном по способу примера 4, за исключением того, что реакцию проводят в условиях, при которых давление в бомбе составляет 50 кгс/см2, реакционной температурой служит комнатная температура и время реакции составляет 200 часов.
После завершения реакции анализ реакционных продуктов в реакционной смеси проводят методом GC-масс-спектрометрии. В результате найдено, что реакционная смесь содержит следующие соединения: тетраацетилдибензилгексаазаизовартзитан, пентаацетилбензилгексаазаизовартзитан, гексаацетилгексаазаизовартзитан, этилпентаацетилгексаазаизовартзитан, диэтилтетраацетилгексаазаизовартзитан. Выход каждого из приведенных выше соединений определяют путем газовой хроматографии. В результате, выход каждого из соединений составил: тетраацетилдибензилгексаазаизовартзитана - 70%; пентаацетилбензилгексаазаизовартзитана - 6,2%; гексаацетилгексаазаизовартзитана - 0,9%; этилпентаацетилгексаазаизовартзитана - 1,3% и диэтилтетраацетилгексаазаизовартзитана - 1,1%.
Результаты EI-масс-спектрометрии для данных соединений следующие.
Результаты EI-масс-спектрометрии пентаацетилбензилгексаазаизовартзитана:
468 (2%, m/z), 425 (3%, [m минус молекулярный вес COCH3]/z), 255 (12%), 91 (66%, CH2Ph) и 43 (100%, COCH3).
Результаты EI-масс-спектрометрии этилпентаацетилгексаазаизовартзитана:
406 (1%, m/z), 363 (1%, [m минус молекулярный вес COCH3]/z), 278 (2%), 236 (5%), 193 (10%), 109 (12%), 43 (100%, COCH3), 29 (15%, CH2CH3) и 15 (8%, CH3).
Результаты EI-масс-спектрометрии диэтилтетраацетилгексаазаизовартзитана:
392 (1%, m/z), 278 (1%), 236 (10%), 193 (25%), 138 (30%), 109 (45%), 97 (20%), 81 (81%), 69 (60%), 56 (20%), 43 (100%, COCH3), 29 (20%, CH2CH3), 28 (52%) и 15 (20%, CH3).
Результаты EI-масс-спектрометрии гексаацетилгексаазаизовартзитана:
420 (5%, m/z), 377 (5%, [m минус молекулярный вес COCH3]/z), 335 (10%), 295 (15%), 208 (12%), 165 (10%), 123 (12%) и 43 (100%, COCH3).
Пример 14. Восстановительное деарилметилирование WB6 в присутствии ацилирующего агента с использованием только ангидрида карбоновой кислоты в качестве ацилирующего агента без использования сложного эфира карбоновой кислоты N-гидроксисукцинимида в качестве ацилирующего агента.
Восстановительное дебензилирование проводят в основном способом по примеру 13, за тем исключением, что используют только 32,4 г уксусного ангидрида в качестве ацилирующего агента без использования N-ацетоксисукцинимида. В ходе реакции отбирают образец реакционной смеси. Состав образца анализируют с помощью FD-масс-спектрометрии. В результате найдено, что образец содержит в качестве промежуточных соединений диацетилтетрабензилгексаазаизовартзитан (M+612) и триацетилтрибензилгексаазаизовартзитан (M+564). Найдено также, что образец содержит в качестве соединения по крайней мере с одной ацетильной группой, отщепленной при восстановлении, этилдиацетилтрибензилгексаазаизовартзитан (M+ 550), этилтриацетилдибензилгексаазаизовартзитан (M+502) и диэтилдиацетилбензилгексаазаизовартзитан (M+486).
По завершении реакции, выход каждого из реакционных продуктов в образовавшейся реакционной смеси измеряют газовой хроматографией. В результате установлено, что выход каждого из реакционных продуктов следующий:
триацетилтрибензилгексаазаизовартзитана: 13%;
этилдиацетилтрибензилгексаазаизовартзитана: 3,1%;
тетраацетилдибензилгексаазаизовартзитана: 7,5%;
этилтриацетилдибензилгексаазаизовартзитана: 32%;
диэтилдиацетилдибензилгексаазаизовартзитана: 30%;
пентаацетилбензилгексаазаизовартзитана: 1,6%;
этилтетраацетилбензилгексаазаизовартзитана: 1,1%;
диэтилтриацетилбензилгексаазаизовартзитана: 6,2%;
гексаацетилгексаазаизовартзитана: 0,5%;
этилпентаацетилгексаазаизовартзитана: 1,2% и
диэтилтетраацетилгексаазаизовартзитана: 1,1%.
Приведенные выше результаты показывают, что без использования сложного эфира карбоновой кислоты и N-гидроксисукцинимида в качестве ацилирующего агента при восстановлении заметно протекает превращение ацильной группы в алкильную группу.
Пример 15. Восстановительное деарилметилирование WB6 в присутствии ацилирующего агента с использованием только N-ацетоксисукцинимида в качестве ацилирующего агента.
Восстановительное дебензилирование проводят в основном по способу примера 13, за тем исключением, что в качестве ацилирующего агента используют 7,5 г N-ацетоксисукцинимида без применения уксусного ангидрида. В ходе реакции отбирают образцы реакционной смеси. Состав образца анализируют FD-масс-спектрометрией. В результате найдено, что образец содержит промежуточные соединения, пентабензилгексаазаизовартзитан ([M+H] +619), ацетилпентабензилгексаазаизовартзитан (M+660), диацетилтетрабензилгексаазаизовартзитан (M+612) и триацетилбензилгексаазаизовартзитан (M+564). После завершения реакции, выход каждого реакционного продукта измеряют газовой хроматографией. Выход каждого из реакционных продуктов следующий: диацетилтетрабензилгексаазаизовартзитана: 74%;
триацетилтрибензилгексаазаизовартзитана: 15%;
тетраацетилдибензилгексаазаизовартзитана: 3%.
приведенные выше результаты показывают, что, когда используют только сложный эфир карбоновой кислоты и N-гидроксисукцинимида в качестве ацилирующего агента при восстановительном деарилметилировании WB6, может быть подавлена вызываемая восстановлением конверсия ацильной группы WAnB6-n (в котором n обозначает целое число от 1 до 4) до алкильной группы в ходе последовательного деарилметилирования WB6 до WAnB6-n (где n обозначает целое число от 1 до 5). Однако результаты показывают также, что реакционная скорость приведенной выше реакции ниже, чем скорость реакции, проводимой с использованием в качестве ацилирующего агента смеси сложного эфира карбоновой кислоты и N-гидроксисукцинимида и ангидрида карбоновой кислоты.
Пример 16. Синтез WA4H2 из WA4B2.
3,67 г (7,11 ммоль) тетраацетилдибензилгексаазаизовартзитана, 1,60 г (7,11 ммоль) Pd(OAc)2 в качестве катализатора восстановления и 150 мл уксусной кислоты в качестве растворителя вносят вместе с перемешивающим элементом в 300 мл микробомбу и бомбу продувают газообразным азотом. Затем бомбу наполняют газообразным водородом так, чтобы давление внутри бомбы стало 5 кгс/см2 - G, и затем содержимое бомбы перемешивают 15 часов для протекания реакции. Извлеченную из микробомбы реакционную смесь фильтруют, чтобы отфильтровать катализатор. Образовавшийся фильтрат перегоняют для отгонки растворителя при пониженном давлении. Образовавшийся твердый остаток промывают 100 мл этилацетата и затем получают 1,67 г тетраацетилгексаазаизовартзитана в виде белой массы (выход: 71%).
Результаты анализов полученного тетраацетилгексаазаизовартзитана следующие.
Результаты ПМР-спектрометрии [растворитель: D2O; стандарт: ТМС; единица: δ (м.д.)]:
1,98 (с, 6H, COCH3), 2,00 (с, 6H, COCH3), 5,29 (м, 2H, CH), 5,50 (м, 2H, CH) и 6,35 (м, 2H, CH).
ПМР могут быть идентифицированы метиновая группа W-скелета и 4 ацетильных группы.
Результаты ИК-спектрометрии представляют два пика поглощения в области 3300-3400 см-1, каждый из которых относится к колебаниям растяжения вторичной аминогруппы (N-H) и, кроме того, поглощение около 1660 см-1, отнесенное к колебаниям растяжения карбонильной группы (C=O) ацетильной группы. Приведенные выше результаты показывают, что W-скелет содержит в качестве заместителей ацетильные группы и N-H-группы.
Пример 17. Синтез WA4H2 из WA4B2, проводимый с использованием катализатора, отличного от катализатора, используемого в примере 16, при реакционной температуре, отличной от температуры, используемой в примере 16.
1,20 г (2,33 ммоль) тетраацетилдибензилгексаазаизовартзитана, 0,496 г (0,466 моль) Pd-C (Pd/содержание 10%) в качестве реакционного катализатора и 60 мл уксусной кислоты (растворитель) вносят вместе с перемешивающим элементом в 300 мл микробомбу, и бомбу продувают газообразным азотом. Затем вводят в микробомбу газообразный водород, так чтобы внутреннее давление бомбы стало 3 кгс/см2 - G, и затем микробомбу погружают в масляную баню при 40oC. Затем содержимое микробомбы перемешивают 5 часов, используя перемешивание для протекания реакции. Реакционную смесь извлекают из микробомбы и фильтруют, отфильтровывая катализатор. Полученный фильтрат перегоняют при пониженном давлении, отгоняя растворитель. Образовавшийся твердый осадок промывают 100 мл этилацетата, получая таким образом 0,57 г тетраацетилгексаазаизовартзитана в виде белой массы.
Проведенные выше результаты показывают, что даже когда реакцию проводят, используя катализатор, отличный от используемого в примере 16, при температуре, отличной от температуры, используемой в примере 16, так же, как в примере 16, получают WA4H2.
Пример 18. Подтверждение образования WAnH(6-n) в ходе восстановительного деарилметилирования WB6 в присутствии ацилирующего агента.
Восстановительное дебензилирование гексабензилгексаазаизовартзитана в присутствии ацетилирующих агентов проводят в основном по способу примера 4, за тем исключением, что время реакции составляет 200 часов. По завершении реакции реакционную смесь анализируют газовой хроматографией. В результате найдено, что выход гексаацетилгексаазаизовартзитана составляет только 0,8%. С другой стороны, тетраацетилгексаазаизовартзитан (WA4H2) идентифицировали жидкостной хроматографией при высоких рабочих характеристиках. К вышеуказанной реакционной смеси добавляют ацетилхлорид и затем образовавшуюся смесь перемешивают 1 час для протекания реакции. Полученную реакционную смесь анализируют газовой хроматографией. Результаты анализа показывают, что выход гексаацетилгексаазаизовартзитана составляет 5%. Это также подтверждает, что WA4H(6-n), такой как тетраацетилгексаазаизовартзитан и пентаацетилгексаазаизовартзитан, присутствовал в реакционной системе до добавления ацетилхлорида.
Пример 19. Синтез WA4B2 путем восстановительного деарилметилирования WB6 в присутствии ацилирующего агента.
1,89 г (2,66 ммоль) гексабензилгексаазаизовартзитана, 1,70 г (1,6 мг-атом) Pd-C (Pd-содержание: 10%) в качестве катализатора восстановления, 5,0 г (31,8 ммоль) N-ацетоксисукцинимида (ацетилирующий агент), 160 мл этилбензола (растворитель) и 3,24 г (31,8 ммоль) уксусного ангидрида (ацетилирующий агент) вносят вместе с перемешивающим элементом в 300 мл микробомбу. Бомбу продувают газообразным водородом. Затем, газообразный водород вводят в бомбу, так чтобы внутреннее давление бомбы стало 50 кгс/см2 - G и затем содержимое бомбы перемешивают 20 часов, используя мешалку для протекания реакции. Образовавшуюся реакционную смесь извлекают из бомбы и фильтруют, используя фильтровальную бумагу, с целью отфильтровывания осадка и катализатора восстановления. Осадок на фильтровальной бумаге обрабатывают на месте 200 мл хлороформа, растворяя в нем осадок. Фильтрат (содержащий использованный для обработки хлороформ) перегоняют для отгонки растворителя. Образовавшийся твердый остаток растворяют в 200 мл хлороформа, получая раствор. К раствору добавляют 200 мл водного 28% раствора аммиака и образовавшуюся смесь энергично перемешивают в течение 30 минут, так чтобы реакционную смесь разделить на две фазы: водную и хлороформовую фазу, при этом N-ацетоксисукцинимид разлагается и переходит в водную фазу. Фазу хлороформа отделяют и перегоняют с целью отгонки растворителя, получая таким образом 1,29 г белого твердого остатка. Полученный белый твердый остаток перекристаллизовывают из этилбензола, получая 1,03 г тетраацетилдибензилгексаазаизовартзитана (выход: 75%). Из приведенных ниже результатов анализа путем FD-масс-спектрометрии, ПМР, 13C-ЯМР и 13C - 1H COSY можно заключить, что белая масса, полученная перекристаллизацией, представляет собой тетраацетилдибензилгексаазаизовартзитан. Результаты вышеуказанных анализов следующие.
FD-масс-спектр: 517 ([M+H]+).
ПМР-спектр [растворитель: CDCl3; стандарт: ТМС; единица: δ (м.д.)]:
1,94 (с, 6H, COCH3), 2,15 (с, 6H, COCH3), 4,06 (д, 2H, CH2), 4,29 (д, 2H, CH2), 5,09 (д, 2H, CH), 5,70 (д, 2H, CH), 6,42 (с, 2H, CH) и 7,3-7,5 (м, 10H, P).
Путем ПМР идентифицировано 6 метиновых групп W-скелета, 4 ацетильных группы и 2 бензильных группы.
13C-ЯМР [растворитель: CDCl3; стандарт: ТМС; единица: δ (м.д.)]:
20,737 (CH3), 22,111 (CH3), 56,428 (CH2), 69,679 (CH), 70,592 (CH), 128,056 (Ph), 128,673 (Ph), 128,928 (Ph), 136,742 (Ph) и 168,263 (CO).
С помощью 13C-ЯМР идентифицируют метиновые группы W-скелета, ацетильные группы, фенильные группы и метильные группы бензильных групп.
Путем 1H-13C COSY могут быть идентифицированы 13C, связанные с соответствующими 1H.
Пример 20. Синтез WA4(NO2)2 нитрозированием WA4H2 до получения WA4(NO)2 и окислением WA4(NO)2.
0,336 г (1 ммоль) тетраацетилгексаазаизовартзитана и 10 мл 50% уксусной кислоты в качестве растворителя вносят в 100 мл реакционную колбу. Полученную смесь охлаждают и выдерживают при 0oC. При перемешивании смеси при 0oC к смеси постепенно добавляют по каплям 2 мл водного раствора нитрита натрия (концентрация нитрита натрия: 4 моль/л). После чего образовавшуюся смесь нагревают при 30oC и затем перемешивают 4 часа для протекания реакции нитрозирования. К образовавшейся реакционной смеси добавляют 50 мл хлороформа. Полученную смесь энергично перемешивают и затем оставляют стоять, чтобы смесь разделилась на органическую фазу и неорганическую фазу. Органическую фазу отделяют и растворитель отгоняют при пониженном давлении из органической фазы, получая 0,373 г динитрозотетраацетилгексаазаизовартзитана (выход: 95%).
30 мл 100% азотной кислоты (окисляющий агент) вносят в 100 мл реакционную колбу. Затем в реакционную колбу добавляют 0,9262 г (2,35 ммоль) вышеупомянутого динитрозотетраацетилгексаазаизовартзитана. Образовавшуюся смесь перемешивают при комнатной температуре 5 часов для протекания реакции нитрования. После чего образовавшуюся смесь перегоняют при пониженном давлении для отгонки азотной кислоты, получая таким образом 0,955 г динитротетраацетилгексаазаизовартзитана (выход: 95%).
Результаты анализа полученного динитрозотетраацетилгексаазаизовартзитана следующие.
Результаты ПМР [растворитель: CDCl3; стандарт: ТМС; единица: δ (м.д.)]:
2,05 (с, 6H, COCH3), 2,17 (с, 6H, COCH3), 5,46 (м, 2H, CH), 6,62 (м, 2H, CH) и 7,30 (с, 2H, CH).
С помощью ПМР идентифицируют 6 митиновых групп и 4 ацетильных группы.
Результаты ИК-спектрометрии дают поглощение в области 1,670 см-1, где поглощение соответствует карбонильной группе (C=O) ацетильной группы, а также поглощения в области 1,500 см-1, 1,380 см-1 и 1,350 см-1, где каждое поглощение относится к нитрозогруппе.
Результаты ИК показывают, что поглощение описывающее N-H-группу, идентифицируемое в ИК-спектре тетраацетилгексаазаизовартзитана, полностью исчезает.
Дальнейшие результаты анализов динитротетраацетилгексаазаизовартзитана приведены ниже.
Результаты ПМР [растворитель: DMCO-d6, стандарт: ТМС: единица: δ (м.д.)] :
2,10 (с, 12H, COCH3), 6,75 (м, 2H, CH) и 7,35 (этот пик имеет синглетную вершину (максимум) при 7,35 м.д. и плечо с двинутой в область низкого магнитного поля вершины синглетного пика, 4H, CH).
Результаты ИК дают область поглощения 1,680 см-1, где поглощение относится к колебанию растяжения карбонильной группы (C=O) ацетильной группы, а также поглощения в области 1,570 см-1 и 1,300 см-1, где каждое из поглощений относится к колебанию растяжения нитрогруппы. Этот показывает, что нитрогруппа и ацетильная группа являются заместителями W-скелета динитротетраацетилгексаазоизовартзитана.
FD-масс-спектрометрией идентифицирован исходный ионный пик (m/z 426).
Температуру разложения динитроацетилгексаазаизовартзитана измеряют путем дифференциальной сканирующей калориметрии (DSC) (скорость повышения температуры: 10oC/мин), используя DSC 22OC, изготовленный и реализованный Seiko Instruments Inc., Japan. В результате найдено, что максимальная температура составляет около 314oC, что выше, чем максимальная температура (около 250oC) для HNW. Это означает, что динитротетраацетилгексаазаизовартзитан представляет собой нитраминовое соединение с превосходной температурной устойчивостью.
Пример 21. Синтез WA(NO2)2 нитрованием WA6.
5 мл уксусного ангидрида вносят в 100 мл реакционную колбу и охлаждают до 0oC и выдерживают при этой температуре. При перемешивании уксусного ангидрида при 0oC в реакционную колбу постепенно по каплям добавляют 100% азотную кислоту (нитрующий агент). К образовавшейся смеси добавляют 0,5 г пятиокиси азота. После чего к образовавшейся смеси добавляют 0,1 г (0,238 ммоль) гексаацетилгексаазаизовартзитана. Затем к полученной смеси добавляют 0,5 г пятиокиси азота. Эту операцию по добавлению 0,5 г пятиокиси азота повторяют 4 раза с интервалом 1 час. Образовавшуюся смесь гасят водой со льдом. Жидкие компоненты смеси отгоняют при пониженном давлении и полученный твердый остаток анализируют жидкостной хроматографией при высоких рабочих характеристиках. В результате установлено, что твердый остаток представляет собой динитротетраацетилгексаазаизовартзитан.
Пример 22. Синтез W(NO2)6 нитрованием WA4(NO2)2.
200 мл реакционную колбу погружают в баню при 0oC. В колбу вносят 25 мл серной кислоты и затем 25 мл 100% азотной кислоты добавляют постепенно по каплям в реакционную колбу для получения смешанной кислоты (нитрующий агент). К полученной смешанной кислоте добавляют 0,2 г (0,457 ммоль) динитротетраацетилгексаазаизовартзитана и полученную реакционную смесь перемешивают при 0oC 8 часов. Затем смесь перемешивают при комнатной температуре 67 часов для протекания реакции. После завершения реакции к полученной реакционной смеси добавляют 200 мл хлороформа для экстракции органических веществ реакционной смеси в фазу хлороформа (экстракцию повторяют дважды). Фазу хлороформа перегоняют при пониженном давлении, отгоняя растворитель. Полученный твердый остаток промывают 10% водным раствором NaHCO3, получая 0,06 г гексанитрогексаазаизовартзитана (выход: 30%). Результаты анализа гексанитрогексаазаизовартзитана следующие.
Результаты ИК-спектроскопии способом KBr дают следующие поглощения в области 1605 см-1, относящееся к несимметричному колебанию растяжения нитрогруппы; поглощения в области 1325 см-1 и в области 1270 см-1, каждое из этих поглощений относится к симметричному колебанию растяжения нитрогруппы; поглощения в области 945 см-1 и в области 880 см-1, каждое из которых относится к деформационному колебанию нитрогруппы; и поглощение в области 3030 см-1, относящееся к колебанию растяжения метиновой группы на W-скелете.
Эти ИК-характеристики соответствуют ИК-характеристикам гексанитрогексаазаизовартзитана, приведенных в COMBUSTION AND FLAME 87:145-151 (1991). Приведенные выше результаты ИК-спектрометрии показывают также, что поглощение около 1680 см-1, относящееся к карбонильной группе (C=O) ацетильной группы динитроацетилазаизовартзитана (являющегося исходным соединением) полностью отсутствует.
Приведенные выше результаты показывают, что ацетильные группы динитротетраацетилгексаазаизовартзитана заменяются нитрогруппами, образуя гексанитрогексаазаизовартзитан.
Результаты анализа полученного гексанитрогексаазаизовартзитана (HNW) жидкостной хроматографией с высокими рабочими характеристиками в условиях, описанных в International Symposium on Energetic Materials Technology PROCEEDINGS, SEPTEMBER 24-27 (1995) (где приведены разнообразные характеристики HNW) показывают, что полученный HNW имеет то же время удерживания, что и HNW по указанной публикации.
Результаты EI-масс-спектрометрии показывают наличие фрагментарных пиков, таких как ионные пики 392, молекулярный вес HNW (исходный ион) минус молекулярный вес NO2], 316, 213 и 46 (NO2), где ионные пики соответствуют ионным пикам HNW, приведенным как указано выше в International Symposium on Energetic Materials Technology PROCEEDINGS, SEPTEMBER 24-27, 76-81 (1995).
Пример сравнения 1. Реакция ацилирования после восстановительного деарилметилирования WB6 в отсутствие ацилирующего агента.
3,0 г (4,24 ммоль) гексабензилгексаазаизовартзитана, 0,476 г (2,12 ммоль) Pb(OAc)2, 75 мл тетрагидрофурана (ТГФ) и 75 мл этанола вносят вместе с перемешивающим элементом в 300 мл микробомбу. Бомбу продувают газообразным водородом. Затем в бомбу запускают газообразный водород, так чтобы внутреннее давление бомбы стало 10 кгс/см2 - G. Затем содержимое бомбы перемешивают при комнатной температуре 300 часов для протекания реакции. После завершения реакции количество толуола, образованного деарилметилированием WB6, измеряют газовой хроматографией. В результате найдено, что почти 100% бензильных групп отщепилось. Затем реакционную смесь извлекают из бомбы и катализатор восстановления удаляют из реакционной смеси. Затем растворитель отгоняют при пониженном давлении из смеси. К полученному остатку добавляют 100 мл уксусного ангидрида в качестве ацетилирующего агента, после чего добавляют 10 мл ацетилхлорида. Однако результаты газовой хроматографии показывают, что производное гексаазаизовартзитана, имеющее ацильную группу, не образовалось.
Из приведенных выше результатов установлено, что когда восстановительное деарилметилирование WB6 проводят в отсутствие ацилирующего агента, наблюдается разложение W-структуры.
Пример сравнения 2. Реакция ацилирования, проводимая после восстановительного деарилметилирования WB6 в отсутствие ацилирующего агента.
Восстановительное деарилметилирование гексабензилгексаазаизовартзитана в отсутствие ацилирующего агента проводят в основном по способу примера 19, за тем исключением, что ацилирующий агент не используют. После завершения реакции к реакционной смеси добавляют то же количество того же самого ацилирующего агента, что в примере 19. Смесь перемешивают в атмосфере азота 5 часов для протекания реакции. Образовавшуюся реакционную смесь обрабатывают тем же способом, что в примере 19. Однако присутствие тетраацетилдибензилгексаазаизовартзитана в реакционной смеси не обнаружено.
Промышленная применимость
По данному изобретению может быть получено содержащее ацильную группу производное гексаазаизовартзитана. Содержащее ацильную группу производное гексаазаизовартзитана полезно в качестве предшественника производного полинитрогексаазаизовартзитана, который может быть использован не только как сырье для взрывчатых веществ, но также в качестве присадки к ракетному топливу и взрывчатым веществам. Содержащее ацильную группу производное гексаазаизовартзитана по данному изобретению полезно также в качестве сырья для получения высокополярного полимера, такого как полифункциональный сшивающий агент и как наполнитель для полимеров.
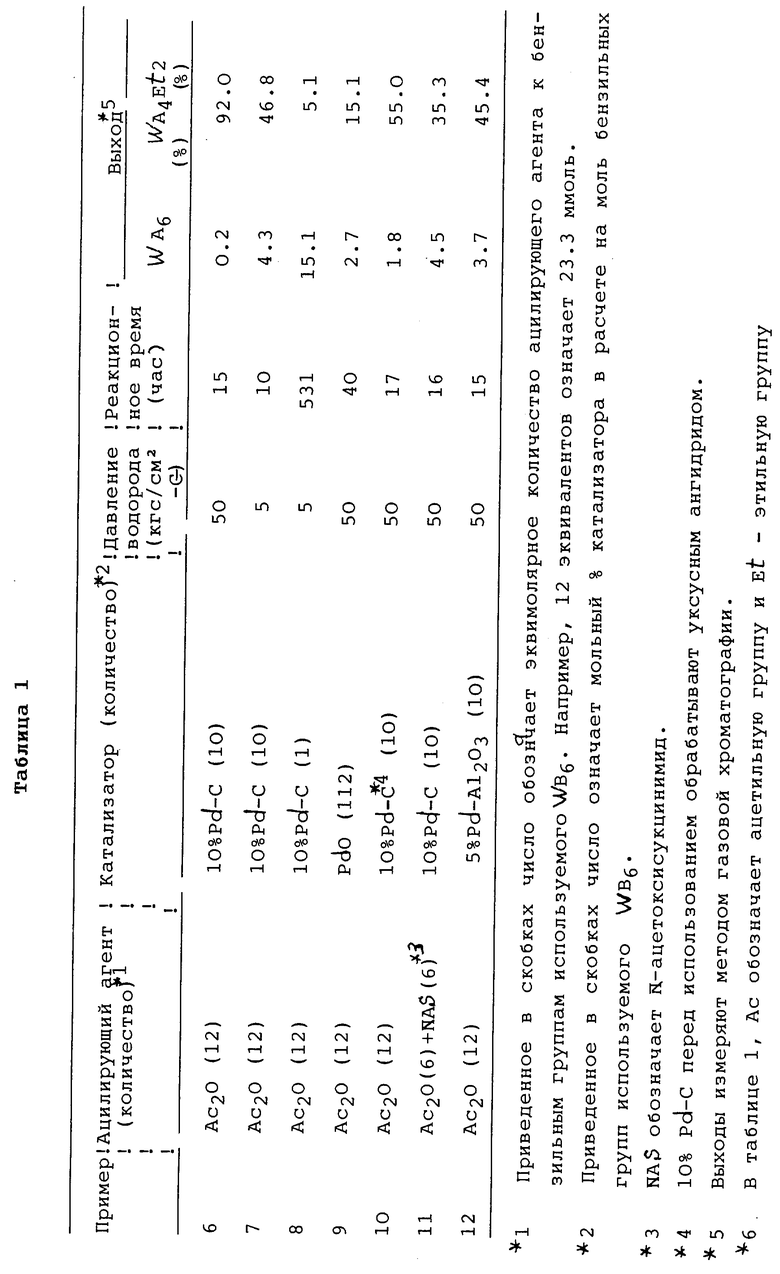
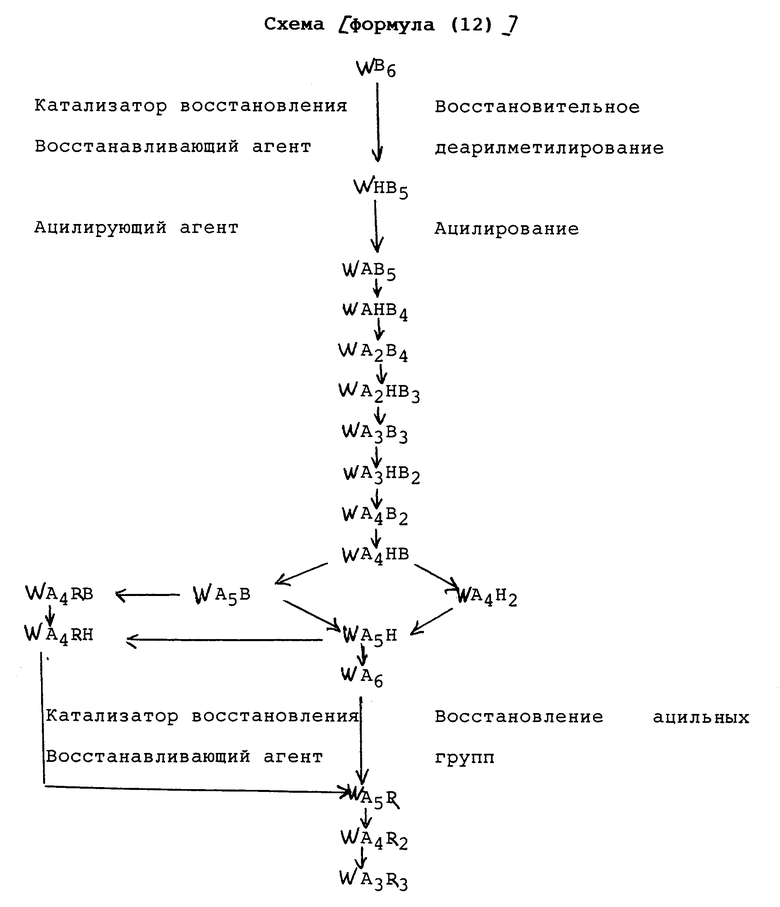
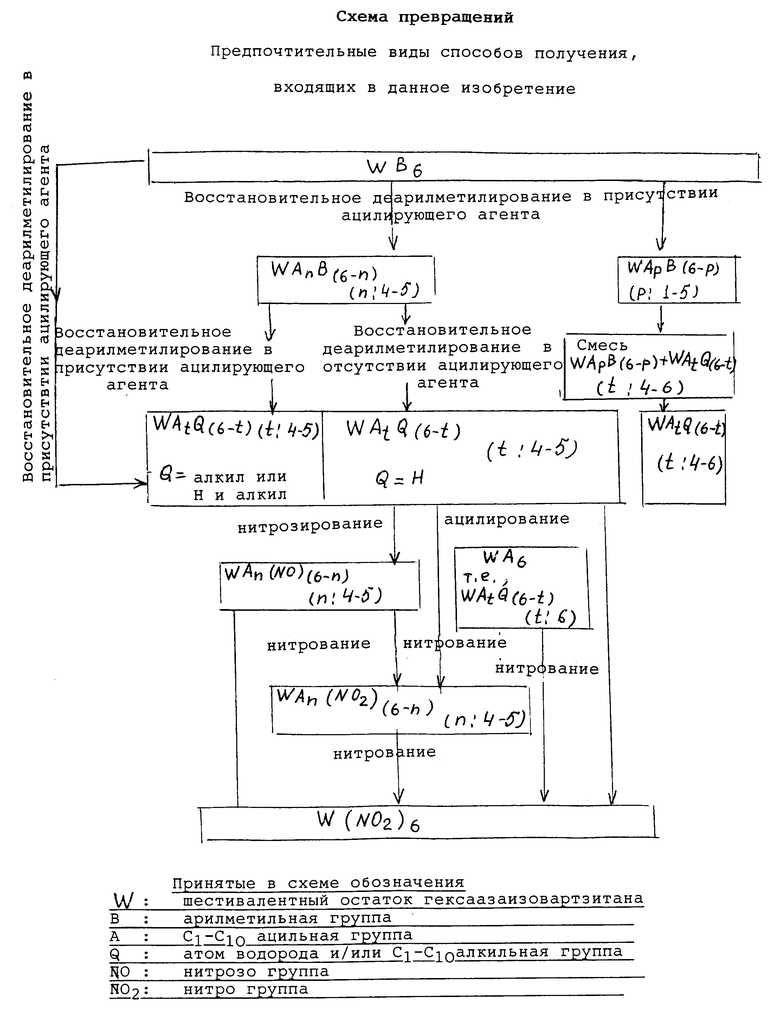
Предложено содержащее ацильную группу производное гексаазаизовартзитана, представленное формулой I: WAtQ(6-t),
где t обозначает целое число от 4 до 6; A независимо обозначает ацильную группу с 1 - 10 углеродными атомами, каждый Q независимо обозначает атом водорода или алкильную группу с 1 - 10 углеродными атомами; W обозначает шестивалентный остаток гексаазаизовартзитана, представленный формулой II. Описывается также способ получения вышеуказанного содержащего ацильную группу производного гексаазаизовартзитана формулы III: WA6, где W и A обозначены выше, заключающийся в том, что соединение формулы IV: WAnH(6-n), где W и A обозначены выше, n - 4 или 5, подвергают взаимодействию с ацилирующим агентом. В изобретении указаны многочисленные способы получения различных производных гексаазаизовартзитана. Содержащее ацильную группу производное гексаазаизовартзитана может быть использовано в качестве предшественника производного полинитрогексаазаизовартзитана, который может быть использован не только в качестве вещества для взрывчатых соединений, но также в качестве добавок для ракетного топлива и взрывчатых веществ. Содержащее ацильную группу производное гексаазаизовартзитана может быть использовано в качестве исходного сырья для получения высокополярного полимера и в качестве полифункционального сшивающего агента и наполнителя для полимеров. 19 с. и 34 з.п. ф-лы, 1 табл.
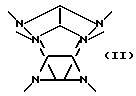
WAtQ(6-t),
где W означает шестивалентный остаток гексаазаизовартзитана формулы II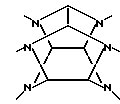
каждый А независимо означает С1-10ациальную группу;
Q - независимо означает атом водорода или С1-10 алкильную группу;
t - целое число от 4 до 6.
WA6,
где W и А имеют указанные в п.1 значения,
отличающийся тем, что производное гексаазаизовартзитана общей формулы IV
WAnH(6-n),
где W и A - имеют указанные выше значения;
n означает целое число 4 или 5,
подвергают взаимодействию с ацилирующим агентом.
WA6,
где A и W имеют приведенные выше значения,
отличающийся тем, что производное гексаазаизовартзитана общей формулы
WAnB(6-n),
где W, A и n имеют указанные выше значения,
каждый В независимо означает арилметильную группу, подвергают восстановительному деарилметилированию в отсутствии ацилирующего агента и полученное производное гексаазаизовартзитана общей формулы IV, где W, A и n имеют приведенные выше значения, подвергают взаимодействию с ацилирующим агентом.
WB6
где В означает арилметильную группу и W определено выше,
подвергают восстановительному деарилметилированию в присутствии ацилирующего агента, завершение указанного восстановительного деарилметилирования осуществляют, когда образующееся содержащее ацильную группу и арилметильную группу производное гексаазаизовартзитана общей формулы V, где A, W, B и n определены выше, образуется в существенном количестве, которое, в свою очередь, подвергают восстановительному деарилметилированию в отсутствие ацилирующего агента с получением производного гексаазаизовартзитана общей формулы IV
WAnН(6-n),
где каждый из W, A и n определен выше,
которое подвергают взаимодействию с ацилирующим агентом.
WApB(6-p),
где W, A, Q, B и t определены выше;
р означает целое число от 1 до 5,
отличающийся тем, что гексакис (арилметил) гексаазаизовартзитан общей формулы XI, где каждый из B и W определен выше, подвергают восстановительному деарилметилированию в присутствии ацилирующего агента в течение периода времени, достаточного для образования содержащего ацильную и арилметильную группы производного гексаазаизовартзитана общей формулы VI в существенном количестве, которое дополнительно подвергают восстановительному деарилметилированию в присутствии ацилирующего агента, причем указанное дополнительное восстановительное деарилметилирование проводят до тех пор, пока содержащее ацильную и арилметильную группу производное гексаазаизовартзитана формулы VI не превратится в производное гексаазаизовартзитана, представленное формулой I, либо указанное дополнительное восстановительное деарилметилирование прекращают, когда не все содержащие ацильную группу и арилметильную группы производные гексаазаизовартзитана общей формулы VI превратятся в производное гексаазаизовартзитана общей формулы I.
WAn(NO)6-n,
где W, A и n имеют указанные выше значения.
WAn(NO2)(6-n),
где W, A и n имеют указанные выше значения.
W(NO2)6,
где W имеет указанное выше значение,
отличающийся тем, что подвергают нитрованию нитрующим агентом по крайней мере одно из соединений, выбираемых из группы, состоящей из соединения общей формулы III, где W и A имеют указанные выше значения, соединения общей формулы IV, где W, A и n определены выше, соединения общей формулы VII, где каждый из n, A и W определен выше, и соединения общей формулы VIII, где каждый из n, A и W определен выше.
WB6,
где W и B определены выше,
подвергают восстановительному деарилметилированию в присутствии ацилирующего агента с получением содержащего ацильную группу и арилметильную группу производного гексаазаизовартзитана общей формулы V, где каждый из B, W и n определен выше, которое дополнительно подвергают восстановительному деарилметилированию в отсутствии ацилирующего агента для получения производного гексаазаизовартзитана общей формулы IV, где каждый из W, A и n определен выше, которое в свою очередь подвергают нитрованию нитрующим агентом.
WAnQ(6-n),
где W, A, Q и n имеют указанные выше значения, при условии, что все Q одновременно не могут быть атомами водорода, отличающийся тем, что гексакис (арилметил)гексаазаизовартзитан общей формулы XI, где W и B определены выше, подвергают восстановительному деарилметилированию в присутствии ацилирующего агента в течение периода времени, достаточного для образования целевого продукта XII в существенном количестве, с последующим его выделением.
| JP, 6-321962, 1994 | |||
| Journal Org.Chem., v.55, p | |||
| Коловратный двигатель | 1924 |
|
SU1459A1 |
| Thermochimica Acta, 213, p.165 - 175, 1993. | |||
Авторы
Даты
1999-01-27—Публикация
1996-01-31—Подача