Настоящее изобретение относится к способу получения тригидрата (2R, 3S)-3-трет. бутоксикарбониламино-2-гидрокси-3-фенилпропионата 4-ацетокси-2α-бензоилокси-5β,20-эпокси-1,7β,10β тригидрокси-9-оксо-такс-11-ен-13α-ила.
В европейских патентах ЕР-0 253 738 и ЕР-0 336 841 описан (2R, 3S)-3-трет.бутоксикарбониламино-2-гидрокси-3-фенилпропионат 4-ацетокси-2α-бензоилокси-5β,20-эпокси-1,7β,10β- тригидрокси-9-оксо-такс-11-ен-13α-ила, который имеет высокие противораковые и противолейкемические свойства, и его получение.
Было найдено, что тригидрат (2R, 3S)-3-трет.бутоксикарбониламино-2-гидрокси-3-фенилпропионата 4-ацетокси-2α-бензоилокси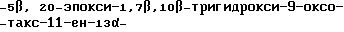
ила имеет стойкость, очень значительно превышающую стойкость безводного продукта.
Согласно изобретению тригидрат (2R, 3S)-3-трет.бутоксикарбониламино-2-гидрокси-3-фенилпропионата 4-ацетокси-2α-бензоилокси-5β,20-эпокси1,7β,10β-тригидрокси-9-оксо-такс-11-ен-13α-ила может быть получен после кристаллизации (2R, 3S)-3-трет.бутоксикарбониламино-2-гидрокси-3-фенилпропионата 4-ацетокси- 2α-бензоилокси-5β,20-эпокси-1,7β,10β-тригидрокси-9-оксо-такс-11-ен-13α-ила в смеси воды и алифатического спирта, содержащего 1 - 3 атома углерода, с последующей сушкой полученного продукта в определенных условиях температуры, давления и влажности.
Для осуществления способа согласно изобретению осуществляют, в частности, следующие операции:
- растворение (2R, 3S)-3-трет. бутоксикарбониламино-2-гидрокси-3-фенилпропионата 4-ацетокси-2α-бензоилокси-5β,20-эпокси-1,7β,10β-тригидрокси-9-оксо-такс-11-ен-13α-ила, предварительно очищенного хроматографией, в алифатическом спирте, содержащем 1 - 3 атома углерода, при температуре предпочтительно от 40 до 60oС,
- удаление, в случае необходимости, остаточных растворителей хроматографии путем совместной перегонки при пониженном давлении, заменяя объем отгоняемого растворителя чистым спиртом,
- введение воды, в случае необходимости, очищенной при той же температуре,
- затем после возможной затравки кристаллизации и охлаждения до температуры около 0oС отделение полученных кристаллов тригидрата (2R, 3S)-3-трет. бутоксикарбониламино-2-гидрокси-3-фенилпропионата 4-ацетокси-2α-бензоилокси-5β,20-эпокси-1,7β,10β-тригидрокси-9-оксо-такс-11-ен-1,3α-ила, затем сушка при пониженном давлении в контролируемой влажной атмосфере.
Обычно, очищенный (2R, 3S)-3-трет.бутоксикарбониламино-2-гидрокси-3-фенилпропионат 4-ацетокси-2α-бензоилокси-5β,20-эпокси1,7β,10β-тригидрокси-9-оксо-такс-11-ен-13α-ила растворяют в избытке алифатического спирта. Предпочтительно, количество спирта составляет от 8 до 12 вес.частей по отношению к используемому (2R, 3S)-3-трет. бутоксикарбониламино-2-гидрокси-3-фенилпропионату 4-ацетокси-2α-бензоилокси-5β,20-эпокси-1, 7β,10β-тригидрокси-9-оксо-такс-11-ен-13α-ила.
Обычно отгонку спирта осуществляют при пониженном давлении при температуре около 40oС до получения густого, трудноперемешиваемого сиропа. Предпочтительно повторить несколько раз эту операцию, которая приводит к удалению остаточных растворителей, содержащихся в очищенном продукте.
По окончании удаления остаточных растворителей полученный сироп поглощают в количестве спирта, составляющем между 3,5 и 6 вес.частями по отношению к (2R, 3S)-3-трет.бутоксикарбониламино-2-гидрокси-3-фенилпропионату 4-ацетокси-2α-бензоилокси-5β,20-эпокси-1,7β,10β-тригидрокси-9-оксо-такс-11-ен-13α-ила.
После возможного отделения нерастворимых примесей фильтрованием добавляют воду, преимущественно очищенную, так чтобы весовое отношение воды/спирта было около 2/1.
Осуществляют затравку кристаллизации, затем смесь медленно охлаждают до температуры около 0oС.
Кристаллизованный тригидрат (2R, 3S)-3-трет.бутоксикарбониламино-2-гидрокси-3-фенилпропионата 4-ацетокси-2α-бензоилокси-5β,20-эпокси-1,7β,10β-тригидрокси-9-оксо-такс-11-ен-13α-ила отделяют, предпочтительно фильтрованием или центрифугированием, затем сушат. Сушку осуществляют при пониженном давлении, составляющем между 4 и 7 кПа, при температуре около 40oС в контролируемой влажной атмосфере, относительная влажность составляет около 80%.
Для осуществления способа целесообразно проводить кристаллизацию в присутствии аскорбиновой кислоты, которую добавляют при растворении очищенного (2R, 3S)-3-трет. бутоксикарбониламино-2-гидрокси-3-фенилпропионата 4-ацетокси-2α-бензоилокси-5β,20-эпокси-1,7β,10β-тригидрокси-9-оксо-такс-11-ен-13α-ила в спирт. Можно использовать до 1 вес.% аскорбиновой кислоты.
Для осуществления способа рекомендуется, в частности, использовать в качестве спирта этанол.
Структура тригидрата (2R, 3S)-3-трет.бутоксикарбониламино-2-гидрокси-3-фенилпропионата 4-ацетокси-2α-бензоилокси-5β, 20-эпокси-1,7β,10β-тригидрокси-9-оксо-такс-11-ен-13α-ила подтверждена дифракцией Х-лучей, термогравиметрическим анализом и дифференциальным калориметрическим анализом.
В частности, термогравиметрический анализ показывает, что потеря веса при температуре от 40 до 140oС составляет 6,1%, соответствует трем молекулам воды на одну молекулу (2R, 3S)-3-трет.бутоксикарбониламино-2-гидрокси-3-фенилпропионата 4-ацетокси-2α-бензоилокси-5β,20-эпокси-1,7β,10β-тригидрокси-9-оксо-такс-11-ен-13α-ила.
Количественный анализ воды в массе продукта и гидратной воды дифференцированным калориметрическим анализом показывает отсутствие воды в массе продукта, а эндотермический сигнал при 132,6oC соответствует диссоциации одного гидрата.
Тригидрат (2R, 3S)-3-трет.бутоксикарбониламино-2-гидрокси-3-фенилпропионата 4-ацетокси-2α-бензоилокси-5β,20-эпокси-1,7β,10β-тригидрокси-9-оксо-такс-11-ен-13α-ила не обладает больше гигроскопичностью.
Исследования по стабильности показывают, что тригидрат (2R, 3S)-3-трет. бутоксикарбониламино-2-гидрокси-3-фенилпропионата 4-ацетокси-2α-бензоилокси-5β,20-эпокси-1,7β,10β-тригидрокси-9-оксо-такс-11-ен-13α-ила является стойким при 4oС, 25oС и 35oС в атмосфере с относительной влажностью 90% до 18 месяцев без изменения кристаллической формы.
В таких же условиях безводный (2R, 3S)-3-трет.бутоксикарбониламино-2-гидрокси-3-фенилпропионат 4-ацетокси-2α-бензоилокси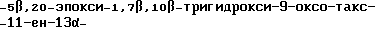 ила,
ила,
кристаллическая форма которого другая, медленно переходит в тригидратную форму.
Следующие примеры иллюстрируют настоящее изобретение.
Пример 1
В реактор, защищенный от света, вводят 303 г (2R, 3S)-3-трет.бутоксикарбониламино-2-гидрокси-3-фенилпропионата 4-ацетокси-2α-бензоилокси-5β,20-эпокси-1,7β,10β-тригидрокси-9-окси-такс-11-ен-13α-ила, титр которого составляет 92,4% (0,314 моль) и 2,875 кг абсолютного этанола (α = 0,79). Смесь нагревают при 40oС до полного растворения (2R, 3S)-3-трет. бутоксикарбониламино-2-гидрокси-3-фенилпропионата 4-ацетокси-2α-бензоилокси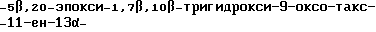
ила. Затем отгоняют этанол при давлении, близком к 12 кПа, с получением сиропа с пределом перемешиваемости. Прибавляют к сиропу 0,983 кг этанола и отгоняют снова при тех же условиях. К полученному сиропу добавляют 1,257 кг этанола и нагревают при 50oС до полного растворения. Смесь фильтруют в горячем виде, затем прибавляют к фильтрату в течение 1 часа 4,39 кг очищенной воды, поддерживая температуру при 50oС. После начала кристаллизации смесь охлаждают до 0oС в течение 4 часов. Кристаллы отделяют фильтрованием, промывают при помощи 0,909 кг смеси этанола-воды (1 - 2 по весу), потом сушат при 38oС при пониженном давлении (5,07 кПа) в атмосфере с относительной влажностью 80% в течение 48 часов. Получают 266,5 г тригидрата (2R, 3S)-3-трет. бутоксикарбониламино-2-гидрокси-3-фенилпропионата 4-ацетокси-2α-бензоилокси-5β,20-эпокси-1,7β,10β-тригидрокси-9-оксо-такс-11-ен-13α-ила, анализ которого показывает, что его содержание по методу высокоэффективной жидкостной хроматографии составляет 98,7% (в сухом виде) и что содержание воды составляет 6,15%.
Пример 2
Растворяют при температуре около 35oС 110,0 (2R, 3S)-3-трет.бутоксикарбониламино-2-гидрокси-3-фенилпропионата 4-ацетокси-2α-бензоилокси-5β,20-эпокси-1,7β,10β-тригидрокси-9-оксо-такс-11-ен-13α-ила с титром 92,5% и 0,2224 г аскорбиновой кислоты в 1340 см3 этанола. Отгоняют приблизительно 70% введенного этанола при пониженном давлении (8 кПа) при температуре около 20oС. Смесь нагревают при 50oС, затем фильтруют. Фильтр промывают 3 раза при помощи 70,5 см3 этанола, затем прибавляют в течение 15 минут 860,5 см3 очищенной воды при 50oС. Затравливают несколькими кристаллами тригидрата (2R, 3S)-3-трет.бутоксикарбониламино-2-гидрокси-3-фенилпропионата 4-ацетокси-2α-бензоилокси-5β,20-эпокси-1,7β,10β-тригидрокси-9-оксо-такс-11-ен-13α-ила, затем перемешивают в течение 30 минут. После этого прибавляют за 3 часа 860,5 см3 очищенной воды при 50oС, затем охлаждают за 3 часа до температуры около 0oС. Поток кашеобразную массу фильтруют. Отфильтрованную лепешку промывают при помощи 330 г смеси воды-этанола (2 - 1 по весу), затем при помощи 220 г такой же смеси, потом сушат при пониженном давлении (5 кПа) при 38oС в атмосфере с относительной влажностью 80o. Получают с выходом 98% 110,2 г тригидрата (2R, 3S)-3-трет.бутоксикарбониламино-2-гидрокси-3-фенилпропионата 4-ацетокси-2α-бензоилокси-5β,20-эпокси-1,7β,10β-тригидрокси-9-оксо-такс-11-ен-13α-ила.а
Изобретение относится к способу получения тригидрата ( 2R, 3S ) -3-трет. бутоксикарбониламино-2-гидрокси-3-фенилпропионата-4-ацетокси-2α-бензоилокси-5β,20-эпокси-1,7β,10β-тригидрокси-9-оксо-такс-11-ен-13α-ила, который обладает противораковой активностью, Тригидрат имеет очень низкую гигроскопичность по сравнению с другими формами этого продукта. Способ получения заключается в том, что кристаллизуют (2R, 3S ) -3-трет. бутоксикарбониламино-2-гидрокси-3-фенил- пропионат- 4-ацетокси-2α-бензоилокси-5β,20-эпокси-1,7β, 10β-тригидрокси-9-оксотакс-11-ен-13α-ила в смеси воды и алифатического спирта, содержащего 1-3 атома углерода, при весовом соотношении 2:1 с последующей сушкой полученного продукта преимущественно при 40oC, давлении преимущественно при 4-7 кПа, в атмосфере относительной влажности преимущественно около 80%. Процесс кристаллизации целесообразно проводить в присутствии аскорбиновой кислоты. 4 з.п. ф-лы.
| УСТРОЙСТВО для ГОРЯЧЕЙ НАВИВКИ ПРУЖИН из ПРУТКА | 0 |
|
SU253738A1 |
| Устройство для контроля контактных соединений линий электропередачи | 1975 |
|
SU534707A1 |
| Лигатура | 1976 |
|
SU558959A1 |
Авторы
Даты
1999-02-20—Публикация
1995-07-07—Подача