Изобретение относится к усовершенствованному способу получения 2,3,5-триметилгидрохинона (ТМГХ) - полупродукта производства витамина Е.
Главной особенностью современных методов получения ТМГХ является то, что все они основаны на предварительном получении 2,3,6-триметилфенола, который далее окисляют разными методами в 2,3,5-триметилбензохинон, последний гидрируют в 2,3,5-триметилгидрохинон.
Так известен способ получения 2,3,5-триметилгидрохинона из псевдокумола с предварительной защитой реакционноспособного положения 5 введением брома или сульфогруппы по схеме: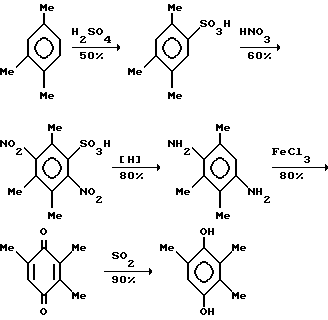
Недостатком указанного метода является его многостадийность, сложность технологии, низкий выход целевого продукта - 17,3% мас. /1/. Химико-фармацевтический журнал, Москва, Медицина 1988 г., с. 1246.
Известен способ получения триметилгидрохинона исходя из диэтилкетона /1/ по схеме: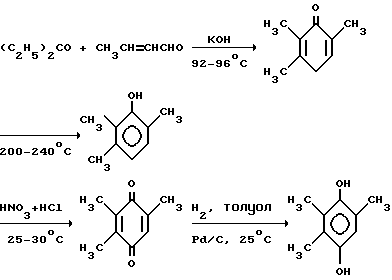
Недостатками данного способа являются низкий выход - 17,2% целевого продукта и отсутствие сырья - диэтилкетона.
В патентной литературе приводится ссылка на один из широко известных методов получения 2,3,5-триметилгидрохинона, исходя Фенола (прототип) /2/ (Патент США 4060561, C 07 C 39/08,77)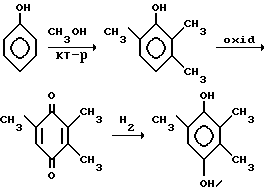
Однако данных о параметрах проведения процесса и выходе целевого продукта нет и сравнение провести по этим показателям не представляется возможным. Суть патента заключается в алкилировании 4-метоксифенола метанолом при температуре 350-550oC и давлении 1-70 атм. над катализатором. В качестве катализатора обычно используется MgO или Al2O3 с активирующими добавками окислов V, Ti, Ce, Mn, Zn и Fe. В результате неполного или избыточного метилирования получают смесь, содержащую 2,3,6-триметилгидрохинон и 8 наименований побочных продуктов, которые после разделения необходимо вернуть в цикл или утилизировать.
Пример по прототипу.
Смесь 21,05 г 4-метоксифенола, 27,2 г MeOH и 1,7 г воды пропускают под давлением при 503oC через слой гранулированного в течение 1 часа. Продукт реакции охлаждают, конденсируют и оставляют на ночь, затем разделяют органическую жидкую фазу от твердой и анализируют методом газовой хроматографии. Суммарное содержание триметилгидрохинона в обоих фазах составляет 22,1%.
Недостатками приведенного способа получения ТМГХ являются:
1) низкая селективность процесса по целевому продукту
2) необходимость введения сложной стадии разделения побочных продуктов, их идентификация
3) необходимость рецикла недометилированных продуктов
4) трудоемкость процесса в плане многоступенчатости технологической схемы
5) низкий выход ТМГХ.
Цель данного изобретения - упрощение технологического процесса, повышение выхода целевого продукта и улучшение условий труда.
Указанная цель достигается тем, что 2,3,5-триметилгидрохинон получают по следующей схеме исходя из 3-нитро-о-ксилола: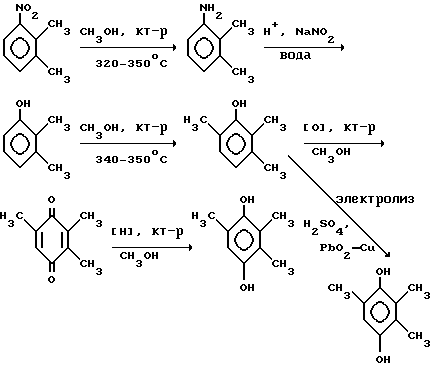
3-нитро-о-ксилол обычно восстанавливают молекулярным водородом в присутствии катализатора Pd/C при температуре 55-60oC и давлении 5-10 атм. в автоклаве до 2,3-ксилидина. Неожиданно для авторов изобретения оказалось возможным проведение реакции восстановления 3-нитро-о-ксилола на не типичном для такого типа реакций окисном железо-хромовом катализаторе, используя в качестве донора водорода - метиловый спирт (или первичные спирты C2-3) в реакторе проточного типа при атмосферном давлении и температуре 340-350oC до 2,3-ксилидина. Выделение 2,3-ксилидина основано на отгонке метанола, применяемого как растворитель и реагент одновременно. Затем 2,3-ксилидин диазотируют в водной среде нитритом натрия до 2,3-ксиленола; 2,3-ксиленол метилируют в паровой фазе над тем же железо-хромовым катализатором или над активной окисью алюминия, промотированной ионами щелочных и щелочно-земельных металлов [Mg2+, Mn2+, Ca2+, Cr2+, Fe2+] при температуре 340-350oC.
Полученный 2,3,6-триметилфенол подвергают химическому или электрохимическому окислению до 2,3,5-триметилбензохинона с последующим восстановлением до 2,3,5-триметилгидрохинона любым подходящим восстановителем (молекулярным водородом, гидросульфитом натрия) или электрохимическим методом.
В качестве химических окислителей применяют кислород воздуха в присутствии катализаторов, содержащих одновалентную медь, соединения хрома, гипогалогениты при температуре 30-65oC. В случае электрохимического окисления конечный продукт реакции 2,3,5-триметилгидрохинон получают без выделения 2,3,5-триметилбензохинона, как промежуточного продукта реакции.
Общий выход целевого продукта (ТМГХ) по всем стадиям составляет 46,6-48,5% мас.
Сущность изобретения поясняется следующими примерами.
Пример N 1. Получение 2,3-ксилидина
Раствор 151 г (1 моль) 3-нитро-о-ксилола в метаноле (35740% концентрации) со скоростью 100-250 мл/час из сырьевой емкости дозатором подается в испарительную зону проточного реактора, предварительно продутого азотом. Реактор представляет собой цилиндрический аппарат из нержавеющей стали, снабженный электрообогревом, термопарой, заполненный гранулированным Fe/Cr катализатором марки CTK-1-7. Температура в зоне испарителя поддерживается 200-250oC, в реакционной зоне 340-350oC
Реакция каталитического парового риформинга метанола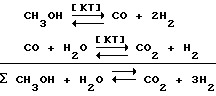
реализуется одновременно с реакцией каталитического восстановления 3-нитро-о-ксилола.
Продукты реакции после прохождения холодильника-конденсатора собирают в приемник и затем на роторно-пленочном испарителе отгоняют избыточный метанол. Получают 119,8 г 2,3-ксилидина. Выход 99%.
Аналогично примеру 1 возможно использование в качестве восстановителя других первичных спиртов, причем спирты изостроения отщепляют атом водорода в более мягких условиях.
Пример N 2. Получение 2,3-ксилидина в среде этилового спирта.
Раствор 151 г (1 моль) 3-нитро-о-ксилола в 226,5 г этанола со скоростью 100-250 мл/час подают в реактор при температуре в зоне испарителя 200-250oC, в зоне реакции 320-330oC. Получают 118,4 г 2,3-ксилидина. Выход 97,8% мас.
Пример N 3. Получение 2,3-ксилидина в среде изопропилового спирта.
Раствор, содержащий 151 г (1 моль) 3-нитро-о-ксилола в 226,5 г изопропилового спирта со скоростью 100-250 мл/чае подают в испарительную зону реактора при температуре 200-250oC. Температура в зоне реакции 320-330oC. Получают 118,6 г 2,3-ксилидина с выходом 98% мае,
Пример N 4. Получение 2,3-ксиленола.
В четырехгорлую круглодонную колбу (V = 2000 мл), снабженную мешалкой, термометром, капельной воронкой и обратным холодильником загружают 350 мл тетрахлорэтилена и 121 г (1,0 моль) 2,3-ксилидина, Затем при хорошем перемешивании загружают 1 л воды и порциями приливают 260,7 г (2,5 моля) концентрированной соляной кислоты, поддерживая температуру реакционной смеси с помощью термостата 5-10oC. К полученной суспензии солянокислого 2,3-ксилидина прикапывают водный раствор нитрита натрия с такой скоростью, чтобы не допустить сильного вспенивания и перегрева реакционной массы выше +10oC. По окончании дозирования нитрита натрия реакционную массу при перемешивании медленно нагревают до температуры 50oC и выдерживают при этой температуре в течение двух часов до полного разложения соли диазония.
В конце реакции диазотирования реакционная масса представляет собой легко расслаивающуюся жидкость. Нижний слой - раствор 2,3-ксиленола в тетрахлорэтилене отделяют от водного слоя и на роторно-пленочном испарителе при температуре 60-80oC и P = 20 мм рт.ст. отгоняют тетрахлорэтилен.
Куб после отгонки тетрахлорэтилена (ксиленол-сырец) представляет собой кристаллический продукт от желтого до коричневого цвета с содержанием основного вещества 95-99%. Его подвергают перегонке с водяным паром для очистки от смол. Отгонку 2,3-ксиленола ведут до тех пор, пока проба дистиллата не перестанет образовывать мути с бромной водой. Дистиллат из приемника-фазоразделителя выливают в стакан, охлаждают в баке со льдом, декантацией сливают воду, отделяя закристаллизовавшийся 2,3-ксиленол. Получают 72,6 г 2,3-ксиленола. Выход 60% от теории.
Пример N 5. Получение 2,3,6-триметилфенола
Реактор парофазного метилирования 2,3-ксиленола аналогичен реактору каталитического парового риформинга метанола, описанному в примере 1, и представляет собой цилиндрический аппарат из нержавеющей стали, снабженный электрообогревом, термопарой, заполненный железо-хромовым катализатором марки CTK-1-7.
Температура в зоне испарителя поддерживается 200-250oC, в зоне реакции 340-350oC. Предварительно готовят 35-40% раствор 2,3-ксиленола в метаноле и заливают его в сырьевую мерную емкость. После достижения в испарителе и реакторе необходимой температуры и продувки их азотом на вход испарителя дозировочным насосом подают сырье со скоростью 100-150 мл/час. Скорость подачи сырья определяется объемом реактора и активностью катализатора. Продукты реакции, выходя из реактора, конденсируют в холодильник-конденсатор и собирают в сборник алкилата, представляют собой раствор 2,3,6-триметилфенола в метаноле с примесями реакционной воды. Алкилат подвергают упарке на установке обычной перегонки при 65-95oC от воды и метанола. Получают кристаллический 2,3,6-триметилфенол. Конверсия 2,3-ксиленола 99%, селективность метилирования по 2,3,6-триметилфенолу 98% мас. Выход - 97,0%.
Пример N 6.
Получение 2,3,6-триметилфенола парофазным метилированием на алюмо-кальциевом катализаторе, промотированном ионами Fe2+, проводят аналогично примеру 5. Количество промотора в готовом катализаторе составляет 5-10% мас. В качестве носителя в катализаторе используется активная γ- окись алюминия марки A, промотированная ионами щелочных и щелочно-земельных металлов [Mg2+, Mn2+, Ca2+, Cr2+, Fe2+]
Получают 2,3,6-триметилфенол с селективностью 94-98%. Конверсия 2,3-ксиленола колеблется от 98 до 89%.
Пример N 7.
Получение 2,3,5-триметилгидрохинона. Предварительно готовят 5-6% раствор 2,3,6-триметилфенола в метаноле. Затем в реактор V=0,5 л, снабженный барботером, термометром, обратным холодильником и мешалкой загружают 250 г раствора 2,3,6-триметилфенола в метаноле и 6,1 г катализатора окисления на основе гидрата окиси алюминия, Cu+, Cl-, PO PO
Пример N 8.
Реакцию окисления 2,3,6-триметилфенола проводят аналогично примеру 7, но после фильтрации катализатора окисления, фильтрат (раствор 2,3,5-триметилбензохинона в метаноле) помещают в "утку" и восстанавливают молекулярным водородом на суспендированном катализаторе Pd/C при температуре 55-60oC. Затем отфильтровывают катализатор гидрирования, отгоняют метанол. Получают 2,3,5-триметилгидрохинон с выходом 98-99% мас. в пересчете на триметилбензохинон.
Пример N 9.
Реакцию окисления 2,3,6-триметилфенола проводят 6-10%-ным водным раствором гипохлорита натрия при температуре 25-50oC и pH=9oC13,5 в водно-щелочной среде в течение 2-3 часов при мольном соотношении 2,3,5-триметилфенол: гипохлорит натрия = 1:5. Затем температуру реакции повышают до 90-95oC, выдерживают при перемешивании еще 1,5 часа. Полученный 2,3,5-триметилгидрохинон экстрагируют тетрахлорэтиленом при объемном соотношении реакционная масса: тетрахлорэтилен = 1:1 3 раза. Экстракт упаривают на роторно-пленочном испарителе в вакууме и получают 2,3,5-триметилгидрохинон с выходом 87,1-90% мас. в пересчете на 2,3,6-триметилфенол.
Пример N 10. Электрохимический окислительно-восстановительный процесс получения 2,3,5-триметилгидрохинона.
В анодную камеру мембранного электролизера заливают 150 мл 10% H2SO4, в катодную - 40 мл 20% H2SO4. В качестве анода используют PbO2 площадью 150 см, катод - свинцовый или медный. При температуре 8-10oC и силе тока 5A проводят электролиз в течение 30 минут. Затем выключают ток, сливают 50 мл анолита и в анодную камеру приливают раствор 5 г (0,036 м) 2,3,6-триметилфенола в 50 мл ацетона. Процесс окисления ведут при температуре 30-40oC, силе тока 3A в течение 2-х часов. Затем реакционную массу сливают из анодного пространства в катодное.
Электровосстановление 2,3,5-триметилхинона ведут током силой 3 A при температуре 30-40oC в течение одного часа. Полученный 2,3,5-триметилгидрохинон экстрагируют органическим растворителем (хлоруглероды, ароматические углеводороды, эфиры или кетоны) и переосаждают из раствора гексаном, гептаном или циклогексаном. Выход 2,3,5-триметилгидрохинона 4,7-5 г (85-90% мас.) в пересчете на 2,3,6-триметилфенол.
Таким образом, предлагаемый авторами способ получения 2,3,5-триметилгидрохинона отличается от прототипа характером используемого сырья, высокой селективностью процесса и практическим отсутствием побочных продуктов реакции, более высоким выходом целевого продукта. 46,6-48,5% по сравнению с 22,1% по прототипу, комплексностью использования метанола в качестве растворителя и реагента.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 2,3,5-ТРИМЕТИЛБЕНЗОХИНОНА ПРИ ПОМОЩИ ОКИСЛЕНИЯ 2,3,6-ТРИМЕТИЛФЕНОЛА | 2014 |
|
RU2668962C2 |
| СПОСОБ ПОЛУЧЕНИЯ α-ТОКОФЕРОЛА (ВИТАМИНА E) | 1998 |
|
RU2163600C2 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3,5-ТРИМЕТИЛБЕНЗОХИНОНА | 1991 |
|
RU2039037C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3,6-ТРИМЕТИЛБЕНЗОХИНОНА И КАТАЛИЗАТОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2000 |
|
RU2164510C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ ХИНОНОВ, КАТАЛИЗАТОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ И СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРА | 2001 |
|
RU2196764C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ ХИНОНОВ | 2014 |
|
RU2568645C1 |
| СПОСОБ ПОЛУЧЕНИЯ о-МЕТИЛЗА.(\\ЕЩЕКНЫХ ФЕНОЛОВ | 1967 |
|
SU200515A1 |
| СПОСОБ СЕЛЕКТИВНОГО ПОЛУЧЕНИЯ О-АЛКИЛФЕНОЛОВ | 2002 |
|
RU2256644C1 |
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ 1-(АЛКОКСИ)-2,3-ДИАЛКИЛ(ФЕНИЛ)АЛЮМАЦИКЛОПРОПЕНОВ, 1-(АЛКОКСИ)-2,3-ДИАЛКИЛ(ФЕНИЛ)АЛЮМАЦИКЛОПЕНТ-2-ЕНОВ И 1-(АЛКОКСИ)-2,3,4,5-ТЕТРААЛКИЛАЛЮМАЦИКЛОПЕНТАДИЕНОВ | 1999 |
|
RU2160268C2 |
| КОНЦЕНТРАТ ВОДОЭМУЛЬСИОННОЙ СМАЗОЧНО-ОХЛАЖДАЮЩЕЙ ЖИДКОСТИ ДЛЯ МЕХАНИЧЕСКОЙ ОБРАБОТКИ МЕТАЛЛОВ | 2002 |
|
RU2226544C2 |
Изобретение относится к усовершенствованному способу получения 2,3,5-триметилгидрохинона - полупродукта производства витамина Е. 2,3,5-триметилгидрохинон получают исходя из 3-нитро-о-ксилола путем восстановления 3-нитро-о-ксилола до 2,3-ксилидина на катализаторе, содержащем окислы железа, хрома или активную окись алюминия, промотированную ионами щелочных и щелочно-земельных металлов, используя в качестве восстановителя первичные спирты С1-С3 при 320-350oC и атмосферном давлении с последующим диазотированием полученного 2,3-ксилидина до 2,3-ксиленола, метилированием последнего в паровой фазе метанолом над тем же катализатором и окислением полученного 2,3,6-триметилфенола до 2,3,5-триметилгидрохинона химическим или электрохимическим методами.
Способ получения 2,3,5-триметилгидрохинона, включающий алкилирование фенола, окисление полученного алкилфенола, гидрирование алкилбензохинона, отличающийся тем, что исходный 3-нитро-о-ксилол восстанавливают первичным C1-C3 спиртом на катализаторе, содержащем окислы железа и хрома, при 320 - 350oC до 2,3-ксилидина, который диазотируют до 2,3-ксиленола, с последующим метилированием последнего в паровой фазе метанолом на катализаторе, содержащем окислы железа и хрома или активную окись алюминия, промотированную ионами щелочных и щелочноземельных металлов (Mg2+, Mn2+, Ca2+, Cr2+, Fe2+) при 340 - 350oC, с последующим окислением полученного 2,3,6-триметилфенола кислородом воздуха в присутствии катализатора на основе гидрата окиси алюминия, содержащем Cu+, Cl-, PO
| US, патент, 4060561, C 07 C 39/08, 1977. |
Авторы
Даты
1999-02-27—Публикация
1994-12-30—Подача