Настоящее изобретение касается способа лечения синдрома раздраженной толстой кишки /слизистого колита/ у млекопитающих и пригодных для этой цепи фармацевтических составов.
Синдром раздражения толстой кишки представляет собой нарушение двигательной активности, включающее отклонение от нормальной деятельности, боли в кишечнике и отсутствие диагностируемой патологии. Синдром проявляется симптоматикой, находящейся под значительным влиянием психологических факторов и стрессовых жизненных ситуаций.
Синдром раздраженной толстой кишки или слизистый колит является одним из наиболее широко распространенных расстройств желудочно-кишечного тракта. От 20 до 50% пациентов, имеющих желудочно-кишечную клинику, страдают синдромом раздраженной толстой кишки. Симптом этого явления проявляются в среднем у 14% здоровых людей. Это одно из мало понятных расстройств, поскольку представляет собой не заболевание, а синдром, состоящий из множества явлений, имеющих подобное проявление.
Большинство симптомов синдрома раздраженной толстой кишки /отклонение от нормальной деятельности кишечника, боли в кишечнике и вспучивание живота/ проявляются в повышении перистальтики кишечника и гиперсекреции желудочного сока.
Активность желудочно-кишечного тракта модулируется деятельностью центральной нервной системы через парасимпатическую и симпатическую иннервацию и периферической нервной системы желудочно-кишечного тракта, находящейся в самом желудочно-кишечном тракте.
Нервная система желудочно-кишечного тракта также отличается хорошей организацией и включает все элементы, необходимые для координации активности органа даже в отсутствии центрального импульса.
Подробнее об этом см.
Goyal, R. K. "Neurology of the Gut", Gastrointestiron Disorners, Ed., Sleisenger and Fordtran, Saunders 1983/, стр. 97 - 114.
Серотонин /5-гидрокситриптамин, 5HT/ прямо или косвенно связан с большинством физиологических явлений, таких как аппетит, чувство страха и состояние депрессии. A. glernon. J. Med. Chem. 30, 1 /1987,. Рецепторы 5HT были обнаружены в центральной нервной системе и периферических тканях, в том числе в желудочно-кишечном тракте, легких, сердце, кровеносных сосудах и множестве других тканей гладкой мускулатуры.
Было установлено, что существует множество типов 5 HT -рецепторов. Рецепторы были классифицированы как 5-HT1, 5-HT-2, 5-HT3 и 5-HT4, причем по крайней мере один 5-HT1-рецептор был позднее подразделен на подклассы и идентифицирован как 5-HT1A, 5-HT1C 5-HT1D.
В центральной нервной системе 5-HT-рецепторы расположены постсинаптический у нейтронов, принимающих серотонергический импульс и пресинаптически у выделяющихся 5-HT-нейронов. Считается, что присенаптические рецепторы действуют таким образом, что способы ощущать концентрацию 5-HT- в синаптической щели и соответственно модулировать в дальнейшем выделение 5-HT.
В общем термин "агонист" следует трактовать как химическое соединение, которое имитирует действие эндогенных нейротрансмиттеров на рецепторах.
Прямо действующие агонисты серотонина представляют собой химические вещества, которые связываются с ними, имитируют действие серотонина или рецепторов серотонина.
Агонисты серотонина, действующие апосредственно, представляют собой химические вещества, повышающие концентрацию серотонина в синаптической щели. Агонисты серотонина, обладающие непрямым действием, включают в себя ингибиторы носителей, специфических к поглощению серотонина, вещества, выделяющие серотонин из гранул, вещества /прекурсоры серотонина/, повышающие образование серотонина, ингибиторы моноаминоксидазы, блокирующие разложение серотонина и повышающие таким образом его возможное количество.
Как известно, серотонин имеет множество функций в желудочно-кишечном тракте. Известно также, что внутривенные вливания 5-HT или 5-HTP /5-гидрокситриптофана/ человеку снижают объем и кислотность секреции желудочно-кишечного тракта, возникающей самопроизвольно или вызванной гистамином, при одновременном повышении количества слизи.
Hordbook of Experomental Pharmarology, T.XIX, "5-Hydroxytryptamine and Related Indolealkylamibes", V. Erspamer Нью-Йорк, 1966, стр. 329-335. Неизвестно, однако, необходимо ли связанные у одного или нескольких комбинаций 5-HT-рецепторов, чтобы вызвать это явление снижения, и какие рецепторы в это включаются.
Известно также, что 5-HT-рецепторы гладкой мускулатуры желудочно-кишечного тракта являются посредниками сокращения этих тканей. Дно желудка крысы и подвздошная кишка морской свинки широко используются для in vitro исследований агонистов и антагонистов 5-HT. Энтерохромафиновые клетки желудочно-кишечного тракта представляют собой самые большие места производства 5-HT в теле.
Способность к сократительной деятельности кишечника находится под сильным влиянием холинергических рецепторов. Известно, что ацетилхолин повышает эту способность желудочно-кишечного тракта путем воздействия на мускариновые рецепторы. Однако известно по крайней мере пять различных мускариновых рецепторов /M1-M5/. См.
Ball B. Wolfe: In the Muscorinic Receptors. Из-во J. Brown, The Huma Press, Нью-Йорк, 1989, стр. 125-150/.
Относительная роль этих рецепторов в модулировании способности желудочно-кишечного тракта к сокращению не установлена, поскольку не были идентифицированы селективные агонисты и антагонисты этих рецепторов. При синдроме раздраженной толстой кишки соединения, действующие как антагонисты мускарина, такие как, например, бентил, оказывают весьма ценное терапевтическое действие, но отличаются целым рядом побочных эффектов.
Лечение синдрома раздраженной толстой кишки ограничивается лекарствами, которые принимают только незначительное количество пациентов. Например, лекарства антихолинергического характера снижают мышечную спастичность и боли в животе при этом стихают. С другой стороны антагонисты гистаминового H2 рецептора уменьшают секрецию желудочного сока и могут таким образом облегчить симптомы расстройства пищеварения. Терапевтические средства, способные снять или облегчить симптомы синдрома раздраженной толстой кишки, в настоящее время еще не найдены.
Было установлено, что агонисты 5 HT1 снижают секрецию желудочного сока путем непосредственного воздействия на 5 4HT-рецептор, облегчая таким образом симптомы расстройства пищеварения /диспепсии/. Авторам удалось найти целую серию таких соединений - агонистов, которые, как оказалось, имеют сродство с M1-холинергическими рецепторами при связывании и проявляют in vitro антиспастическую активность. Поэтому представляемые изобретением соединения будут особенно полезны при лечении синдрома раздраженной толстой кишки и большинства связанных с ним явлений.
Предметом настоящего изобретения является группа соединений, которые являются агонистами прямого воздействия на 5-HT1A и представляют собой вещества, прямо влияющие на M1-холинергические рецепторы. Так как эти две характеристики являются очень важными для нормальной деятельности кишечника, снимая боли и вздутие живота при синдроме раздраженной толстой кишки, эти вещества, обладающие комбинированной активностью, оказывая влияние на способность к сократительной деятельности желудочно-кишечного тракта, будут полезны при лечении указанного синдрома и целого спектра связанных с ним явлений. Кроме того, предметом настоящего изобретения являются новые составы, приемлемые для патентуемого способа.
Другие предметы изобретения, его способности и преимущества представлены в дальнейшем описании изобретения и пунктах его формулы.
Настоящее изобретение представляет собой лечения синдрома раздраженной толстой кишки у млекопитающих и включает в себя введение млекопитающим необходимого для лечения количества соединения с формулой I /эффективной дозы/,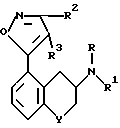
в которой R представляет собой водород, C1-3-алкил, аллил или 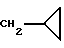
R1 - водород, C1-3-алкил, аллил, 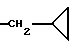 или -(CH2)n-X;
или -(CH2)n-X;
n = 1-5;
X представляет собой замещенный или незамещенный фенил, C1-3-алкокси, или C1-3-алкилтио;
R2 и R3 независимые друг от друга - водород, C1-3-алкил, C1-3-алкокси, C1-3-алкилтио, галоген, CN или фенил, или вместе -(CH2)p-, где p = 3 - 6 целое число;
Y - -CH2-, -O-, -SOm-, где m = 0, 1 или 2,
или фармацевтически приемлемая соль - продукт присоединения кислоты или сольват ее.
Соединения формулы I до этого не использовались для лечения синдрома раздраженной толстой кишки. Таким образом другим предметом настоящего изобретения является фармацевтический состав, пригодный для лечения указанного синдрома, включающий соединение формулы I или фармацевтически приемлемую соль или сольват ее, в комплексе с одним или несколькими фармацевтически приемлемыми наполнителями, растворителями или добавками. Основные химические названия, используемые в формуле, имеют общеупотребительное значение. Например, термин "алкил" представляет собой прямоцепную или разветвленную алкильную цепь, содержащую указанное количество атомов углерода. C1-3-алкильные группы представляют собой метил, этил, этил, н-пропил и изопропил,  представляет собой циклопропилметил
представляет собой циклопропилметил
Галоген - это бром, хлор, фтор или йод.
Замещенный или незамещенный фенил представляет собой фенильное кольцо, которое может содержать один или два заместителя, выбранных из следующей группы C1-3-алкил, C1-3-алкокси, C1-3-алкилтио, галоген, NO2 и CN.
Синдром раздраженной толстой кишки - наиболее подходящий и точный термин, применяемый обычно к нарушениям, которые можно лечить в соответствии с патентуемым способом. Этот термин подчеркивает, что данное нарушение является следствием изменения двигательной активности, которая проявляется в форме раздражения, и что это не заболевание, а синдром, который может охватывать самые различные области желудочно-кишечного тракта. Множество обычно используемых наименований этого вида расстройств, таких как нервный, нестабильный или спастический колит, являются неадекватными и неточными или то и другое вместе.
Сообщения международной рабочей группы определяют синдром раздраженной толстой кишки как нарушение функции желудочно-кишечного тракта, проявляющиеся в /1/ болях живота и/или симптомах патологии опорожнения кишечника /позывов к дефекации, вспучивания живота, ощущения неполного опорожнения кишечника, изменения формы стула /консистенции/ и изменения частоты/ времени работы кишечника/ или /3/ чувства тяжести /переполнения/.
Были предложены новые критерии дисгармонии желудочно-кишечного тракта боли в животе или чувство дискомфорта, ослабленная дефекация или связанное с этим изменение частоты или консистенции стула, и три или более следующих критериев:
/1/ измененная частота стула,
/2/ измененная форма стула /твердый, мягкий или водянистый стул/,
/3/ измененное прохождение стула /позывы к дефекации или вспучивание живота, ощущение неполного опорожнения,
/4/ выход слизи, и
/5/ чувство переполнения или вздутие живота. См.
Schuster, M. M. Gastroenterology Clinies of Health America 20, 269-278 /1991/.
Таким образом становится ясно, что представляемые изобретением соединения могут быть использованы для лечения раздраженной толстой кишки, которые по нынешнему и последующим определениям проявляются указанной симптоматикой.
Симптомы, помогающие отличить синдром раздраженной толстой кишки от органических нарушений, следующие: /1/ видимое вздутие живота, снятие болей при массаже области живота, /3/ снятие болей после дефекации и более частая дефекация, и /4/ мягкий стул, сопровождающийся болью.
Schuster M. M. Gastrointestenal Diseases, изд-во Shesenger u Fordtram, Saunders /1983/, 880-895.
Как уже было указано выше, соединения, пригодные для практического применения, представляемого изобретением способа, включают в себя фармацевтически приемлемые соли-продукты присоединения кислоты,производные указанных соединений,имеющие значения формулы I. Поскольку эти соединения представляют собой амины, они являются основными по своей природе и поэтому могут вступать во взаимодействие с целым рядом неорганических и органических кислот с образованием солей. Так как свободные амины этих соединений являются типичными маслами при комнатной температуре, целесообразно преобразовывать их в соответствующие фармацевтически приемлемые соли для облегчения работы с ними и введения, поскольку последние при комнатной температуре представляют собой твердые вещества. Кислоты, обычно рекомендуемые для получения таких солей, представляют собой неорганические кислоты, типа соляной, бромистоводородной, йодистоводородной, серной, фосфорной и аналогичных им кислот и органические кислоты, такие как пара-толуолсульфокислота, метансульфокислота, щавелевая кислота, пара-бромфенилсульфоновая кислота, карбоновая кислота, сукциновая кислота, лимонная кислота, бензойная кислота, уксусная кислота и им подобные. Таким образом в качестве примера фармацевтически приемлемых солей можно назвать сульфат, пиросульфат, бисульфат, сульфит,бисульфит, фосфат, кислый монофосфат, кислый дифосфат, метафосфат, пирофосфат, гидрохлорид, гидробромид, гидройодид, ацетат, пропионат, деканоат, каприлат, акрилат, формиат, изобутират, капроат, гептаноат, пропиолат, оксалат, малонат, сукцинат, суберат, себацат, фумарат, малеат, 2-бутин-1,4-диоат, 3-гексин-2,5-диоат, бензоат, хлорбензоат, метилбензоат, динитробензоат, гидроксибензоат, метоксибензоат, фталат, сульфонат, ксиленсульфонат, фенилацетат, фенилпропионат, фенилбутират, цитрат, лактат, Y-нидроксибутират, гликолят, тартрат, метансульфонат, пропансульфонат, нафталин-1-сульфонат, нафталин-2-сульфонат, манделат и т.д. Предпочтительными фармацевтическими приемлемыми солями - продуктами кислотного присоединения можно считать те из них, которые образуются с минеральными кислотами, например с солями или бромистоводородной кислотами, или же с органическими кислотами, например малеиновой кислотой.
Кроме того, некоторые из указанных солей способны образовывать сольваты с водой или органическими растворителями, например с этанолом. Такие сольваты также являются одним из предметов настоящего изобретения.
Патентуемые соединения могут быть использованы для лечения синдрома раздраженной толстой кишки благодаря их необычной способности к модулированию функции как 5-HT1A-, так и мускариновых /M1/ рецепторов у млекопитающих. Предпочтительными соединениями формулы I являются те соединения, в которых (а) R - C1-3-алкил или 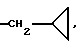 (б) R1 - C1-3 -алкил или
(б) R1 - C1-3 -алкил или 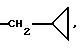 (в) R1 - пропил, (г) R2 и R3 независимые друг от друга - водород или C1-3-алкил, (д) R2 и R3 вместе с представляют собой -(CH2)p, (е) Y - O или -(CH2)-.
(в) R1 - пропил, (г) R2 и R3 независимые друг от друга - водород или C1-3-алкил, (д) R2 и R3 вместе с представляют собой -(CH2)p, (е) Y - O или -(CH2)-.
Особенно предпочтительными можно считать такие классы соединения формулы I, в которых (а) R - пропил, и (б) R2 и R3 независимые друг от друга - водород или метил.
Оптимальным вариантом соединений формулы I являются следующие соединения: (а) 8-/изоксазол-5-ил/-2-ди-н-пропиламино-1,2,3,4-тетрагидронафталин; (б) 8-/4-метилизоксазол-5-ил/2-дипропиламино-1,2,3,4-тетрагидронафталин и (в) 8-/3-метилизоксазо-5-ил/2-дипропиламино-1,2,3,4-тетрагидронафталин.
Совершенно очевидно, что указанные выше классы соединений формулы I можно комбинировать между собой, получая дополнительные варианты соединений.
Патентуемые соединения содержат асимметричный углерод, представленный атомом углерода, который отмечен звездочкой на следующей формуле: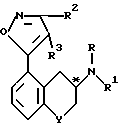
Само по себе каждое из соединений существует в виде отдельных d- и l-стереоизомеров, равно как и в виде их рацемической смеси. В соответствии с этим представляемые изобретением соединения включают не только dl-рацематы, но и их оптически активные изомерные d- и l - формы.
Приведенные ниже соединения более наглядно иллюстрируют соединения, входящие в предмет настоящего изобретения:
8-/изоксазол-5-ил/-2-/ди-п-пропиламино/тетрагидронафталин,
8-/изоксазол-5-ил/-2-/пропиламино/тетрагидронафталин,
8-/изоксазол-5-ил/-2-/диметиламино/тетрагидронафталин,
8-/изоксазол-5-ил/-2-/ди/циклопропилметил/амино/тетрагидронафталин,
8-/изоксазол-5-ил/-2-/ди-аллиламино/тетрагидронафталин,
8-/3-метилизоксазол-5-ил/-2-/дипропиламино/тетрагидронафталин,
8-/3-метилизоксазол-5-ил/-2-/пропиламино/тетрагидронафталин,
8-/3-метилизоксазол-5-ил/-2-/диметиламино/тетрагидронафталин,
8-/3-метилизоксазол-5-ил/-2-/ди/циклопропилметил/амино /тетрагидронафталин,
8-/3-метилизоксазол-5-ил/-2-/диаллил/амино/тетрагидронафталин,
8-/4-метилизоксазол-5-ил/-2-/дипропиламино/тетрагидронафталин,
8-/4-метилизоксазол-5-ил/-2-/пропиламино/тетрагидронафталин,
8-/4-метилизоксазол-5-ил/-2-/диметиламино/тетрагидронафталин,
8-/4-метилизоксазол-5-ил/-2-/ди/циклопропилметил /аминотетрагидронафталин,
8-/4-метилизоксазол-5-ил/-2-/диаллиламино/тетрагидронафталин,
8-/3,4-диметилизоксазол-5-ил/-2-/дипропиламино /тетрагидронафталин,
8-/3,4-диметилизоксазол-5-ил/-2-/пропиламино/тетрагидронафталин,
8-/3,4-диметилизоксазол-5-ил/-2-/диметиламино/ тетрагидронафталин,
8-/3,4-диметилизоксазол-5-ил/2/ди/циклопропилметил/амино/ тетрагидронафталин,
8-/3,4-диметилизоксазол-5-ил-2-диаллиламино/-тетрагидронафталин,
8-/4,5,6,7-тетрагидробенз/с/изоксазол-1-ил/-2-/дипропиламино/ тетрагидронафталин,
8-/4,5,6,7-тетрагидробенз/с/изоксазол-1-ил/2-/пропиламино/ тетрагидронафталин,
8-/4,5,6,7-тетрагидробенз/с/ изоксазол-1-ил/-2-/диметиламино/ тетрагидронафталин,
8-/4,5,6,7-тетрагидробенз/с/изоксазол-1-ил/-2-/ди/циклопропилметил/-амино/ тетрагидронафталин,
5-/4,5,6,7-тетрагидробенз/с/изоксазол-1-ил/-3-/дипропиламино/хроман,
5-/изоксазол-5-ил/-3-/дипропиламино/хроман,
5-/3-метилизоксазол-5-ил/-3-/дипропиламино/хроман,
5-/4-метилизоксазол-5-ил/-3-/дипропиламино/хроман,
5-/3,4-диметилизоксазол-5-ил/-3-/дипропиламино/хроман,
5-/изоксазол-5-ил/-3-/дипропиламино/тиохроман,
5-/3-метилизоксазол-5-ил/-3-/дипропиламино/тиохроман,
5-/4-метилизоксазол-5-ил/-3-/дипропиламино/тиохроман,
5-/3,4-диметилизоксазол-5-ил/-3-/дипропиламино/тиохроман,
Представляемые изобретением соединения можно получать по хорошо известным методам. Для их получения могут быть использованы различные общие реакции. Общие схемы таких реакций приводятся ниже, в каждой из групп символы имеют следующие значения:
R2 и R3 - водород, C1-3- алкил, галоген, OH, C1-3 - алкокси, C1-3-алкилтио, NH2, CN, фенил или (-CH2-)p;
Rc - водород или C1-3 - алкил;
X - галоген, SRc, ORc или N(Rc)2;
Ar - остальная часть соединения формулы I, т.е.
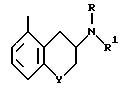
/левая часть не представлена/
Схема 1.
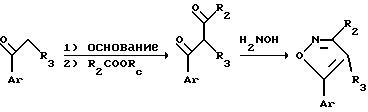
Схема 2.

Схема 3.
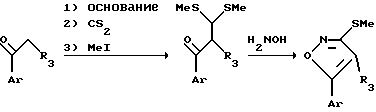
Схема 4.
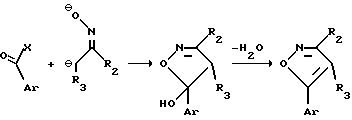
Схема 5.
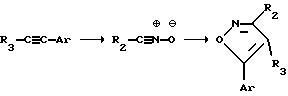
Вышеуказанный способ синтеза дает возможность получать соединения, в которых гетероароматическое кольцо может иметь или не иметь заместителя. Общие реакции, представляющие методологию введения, преобразования и отщепления заместителей, приведены в Comprehensive Orhanic
Transformations, Richard C. Larocke, VCH Publishers, Inc. Нью-Йорк, /1989/
Оптически активные изомеры формулы I также рассматриваются как часть предмета изобретения. Такие оптически активные изомерные формы можно получать из их соответствующих оптически активных прекурсоров /предшествующих форм/ в соответствии с описанными выше методами или путем разложения рацемических смесей. Методики разделения приведены, например, в описании Европейской патентной заявки ЕРА N 498, 490.
Соединения, рекомендуемые в качестве исходных продуктов для синтеза патентуемых соединений, либо хорошо известны, либо могут быть легко получены при использовании стандартных способов, рекомендуемых в аналогичных случаях.
Представляемые изобретением фармацевтически приемлемые соли-продукты кислотного присоединения обычно получают путем реакции основания формулы I, соответствующего предмету изобретения, с эквимолярным или избыточным количеством кислоты. Реакционные компоненты обычно вводят в растворителе, в котором они растворяются, например диэтиловом эфире или бензоле. Выпадающую в виде осадка из раствора соль/процесс осаждения продолжается от одного часа до 10 дней /выделяют методом фильтрации.
Приведенные ниже примеры представляют описанные выше типовые способы получения соединений формулы I. Другие способы их получения аналогичны описанным с точки зрения методики. Они носят только иллюстрированный характер и не излагаются подробно, чтобы сократить описание предмета настоящего изобретения.
Приготовление 1.
Получение 2-/ди-н-пропиламино/-8-/ изоксазол-5-ил/-1,2,3,4-тергагидронафталинмалеата.
Раствор 2-/ди-н-пропиламино/-8-ацетил-1,2,3,4-тетргаидронафталина /0,3 г, 1,1 моля/ и трис/диметиламино/метана /0,32 г, 2,2 ммоля/ в толуоле кипятят с обратным холодильником в течение 5 часов и при 60oC в течение 18 часов. Добавляют дополнительно аликвотное количество трис/диметиламино/метана /0,16 г, 1,1 ммоль/ и реакцию продолжают при перемешивании еще в течение 2 часов при температуре 60oC. Реакционную смесь концентрируют с получением 2-/ди-н-пропиламино/- -8-/1-оксо-3-/диметиламино/проп-2-ен-1-ил/-1,2,3,4-тетрагидронафталина /0,39 г/ в виде вязкого оранжевого масла.
К раствору 2-/ди-н-пропиламино/-8-/1-оксо-3-/диметиламино/-проп-2-ен-1-ил/ -1,2,3,4-тетрагидронафталина /0,75 г, 2,29 ммоля/ в уксусной кислоте /5 мл/ добавляют гидроксиламингидрохлорид /0,32 г, 4,6 ммоля/ и реакцию проводят при перемешивании при комнатной температуре. Реакционную смесь концентрируют, а образовавшийся остаток растворяют в воде. Раствору придают основной характер /подщелачивают/ путем добавления концентрированного раствора гидроокиси аммония, после чего экстрагируют эфиром. Экстракт промывают рассолом, сушат с помощью сульфата натрия и концентрируют, получая вязкое, светло-оранжевое масло. Малеат получают по стандартной методике.
После кристаллизации из смеси этанол /эфир получают в заголовке соединение в виде грязно-белых кристаллов /0,24 г/ Т.пл. 136 - 138o. После перекристаллизации полученной соли из этанола получают бесцветную кристаллическую массу /155 мл/, т.пл. 139 - 141oС.
Данные анализа:
Рассчитано: C 66,65; H 7,29; N 6,76.
Найдено: C 66,86; H 7,33; N 6,79.
Приготовление 2.
Получение 2-/ди-н-пропиламино /-8-/3-бромизоксазол-5-ил/ -1,2,3,4-тетрагидронафталинмалеата.
К раствору 2-/ди-н-пропиламино/-8-йодо-1,2,3,4-тетрагидронафталина /4,3 г, 12,1 ммоля/ и триэтиламина /100 мл/ добавляют йодид /1/ меди /228 мг/, хлорид бис /трифенилфосфин/-палладия /11/ /841 мг/ и триметилсилилацетилен /1,7 мл/. Смесь перемешивают при комнатной температуре в течение ночи. Смесь выливают в воду и экстрагируют эфиром. Экстракт промывают рассолом, сушат с помощью сульфата натрия и концентрируют, получая 5 г сырого продукта. Очистка методом флеш-хроматографии при использовании смеси метиленхлорид /метанол/ /20:1/ в качестве растворителя дает 4,33 г 2-/ди-н-пропиламино/-8-/2-триметилсилилэтинил/ -1,2,3,4-тетрагидронафталина, который используют в последующих реакциях.
Раствор 2-/ди-н-пропиламино/-8-/2-триметилсилилэтинил/- -1,2,3,4-тетрагидронафталина /4,3 г/ и тетраэтиламмонийфторида /12,1 ммоль/ в тетрагидрофуране /150 мл/ перемешивают при комнатной температуре в речение 18 часов и кипятят в обратным холодильником в течение 6 часов. Реакционную смесь концентрируют и образовавшийся остаток растворяют в метиленхлориде. Полученный раствор промывают водой, сушат при использовании сульфата натрия и концентрируют с получением 3,6 г масла коричневого цвета. Очистка методом флеш-хроматографии со смесью метиленхлорида /метанола в качестве растворителя /20:1/ дает 2-/ди-н-пропиламино/-8-этинил-1,2,3,4-тетрагидронафталин /1,1 г, 36% общий выход/.
2-/ди-н-Пропиламино/-8-этинил 1,2,3,4-тетрагидронафталин /900 мг 3,5 ммоль/ перемешивают при комнатной температуре со 90 мл этилацетата, содержащего 1 мл воды. Добавляют Br2CNOH /715,8 мг/ в 10 мл этилацетата и полученную смесь перемешивают при комнатной температуре в течение 2 дней, после чего добавляют 150 мг карбоната натрия и 250 мг Br2CNOH. Затем смесь перемешивают еще в течение 4 часов, выливают в воду и промывают этилацетатом. Промывные воды, содержащие этилацетат, объединяют, сушат и концентрируют, получая при этом 1,0 г остатка. Остаток обрабатывают методом флеш-хроматографии на колонке, элюируя 20:1 CH2Cl2:MeOH. Соответствующие фракции объединяют, получая около 120 мг продукта. Добавляют эфир и получают твердое вещество, которое выделяют путем фильтрации. Фильтрат содержит желаемый продукт, который затем преобразуют в малеат.
После кристаллизации из смеси этилацетат/гексан получают указанное в заголовке соединение /84 г/, т.пл. 113-114oC.
Данные анализа:
Рассчитано: C 55,90; H 5,92; N 5,68.
Найдено: C 55,77; H 5,90; N 5,48.
Приготовление 3.
Получение 2-/ди-н-пропиламино/-8-/4-метилизоксазол-5-ил/ -1,2,3,4-тетрагидронафталинмалеата.
2-/ди-н-Пропиламино/-8-бром-1,2,3,4-тетрагидронафталин /8,5 г, 27,4 ммоль/ растворяют в 80 мл тетрагидрофурана и охлаждают до - 78oC, после чего добавляют 25,7 мл н-бутиллития /1,6 М в гексане/. Смесь перемешивают при -78oC в течение часа, после чего добавляют 2,4 мл /32,9 ммоль/ пропиональдегида. Смесь нагревают до комнатной температуры, затем выливают в воду и экстрагируют метиленхлоридом. Экстракт сушат над сульфатом натрия и выпаривают. Получают 9,1 г желтого масла.
Масло пропускают в колонку с силикагелем и элюируют смесью 3% метанола в метиленхлориде, содержащей следовые количества гидроокиси аммония. Соответствующие фракции объединяют, получая при этом 6,5 г /82% 2-/ди-н-пропиламино/-8-/1-гидроксипропил-1-ил/- 1,2,3,4-тетрагидронафталина в виде прозрачного масла.
Вышеупомянутый продукт растворяют в 250 мл метиленхлорида и добавляют 17,0 г /78,7 ммоль/ хлорхромата пиридиния с 30 г 4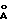 молекулярного сита. Смесь перемешивают в течение 3 часов при комнатной температуре, после чего добавляют 250 мл эфира и целит. Смесь обрабатывают на колонке с силикагелем, элюируя эфиром.
молекулярного сита. Смесь перемешивают в течение 3 часов при комнатной температуре, после чего добавляют 250 мл эфира и целит. Смесь обрабатывают на колонке с силикагелем, элюируя эфиром.
Для растворения коричневого осадка добавляют метанол/ осаждение происходит после добавления в реакционную смесь эфира/. Полученный продукт подают в колонку и элюируют 10% метанола в метиленхлориде. Элюент концентрируют с получением коричневого масла, которое в дальнейшем очищают на хроматографической колонке с силикагелем, элюируя смесью гексанов /эфира /2:1/, а затем чистым эфиром. Фракции, содержащие желаемый продукт, объединяют, получая при этом 4,7 г 2-/ди-н-пропиламино/-8-пропионил-1,2,3,4-тетрагидронафталин.
2-/ди-н-Пропиламино/-8-пропионил-1,2,3,4-тетрагидронафталин/ 1,5 г, 5,2 ммоль/ растворяют в 50 мл толуола и добавляют 2,2 мл трис/диметил амино/метана. Смесь нагревают в течение ночи при 80oC. Затем смесь выпаривают, а остаток помещают в 15 мл уксусной кислоты. Добавляют гидроксиламингидрохлорид /730 мг, 10,4 ммоль/ и полученную смесь перемешивают при комнатной температуре в течение ночи. Затем смесь выливают в воду, с помощью гидроокиси аммония устанавливают pH на уровне 11, и полученную смесь экстрагируют метиленхлоридом. Экстракт сушат над сульфатом натрия и выпаривают с получением 1,5 г оранжевого масла.
Масло подают в колонку с силикагелем, элюируя смесью гексана и эфира, содержащей следовые количества гидроокиси аммония. Соответствующие фракции объединяют вместе. Получают 1,0 г /61,3%/ свободного основания указанного в заголовке соединения.
50 мг полученного свободного основания преобразуют в малеат по стандартной методике и перекристаллизовывают из смеси этанола и эфира. Получают 55 мг белых кристаллов с т.пл. 118oC.
Данные анализа для C24H32N2O5
Рассчитано: C 67,27; H 7,53; N 6,54;
Найдено: C 66,99; H 7,60; N 6,35.
Приготовление 4.
Получение 2-/ди-н-пропиламино/-8-/4-этилизоксазол-5-ил/ -1,2,3,4-тетрагидронафталина.
2-/ди-н-Пропиламино/8-бром-1,2,3,4-тетрагидронафталин /5,0 г, 16,1 ммоль/ растворяют в 50 мл тетрагидрофурана, охлаждают смесь до - 78oC, после чего добавляют 21,0 мл н-бутиллития (0,92 М в гексане/. Смесь перемешивают в течение 30 минут и добавляют 1,85 мл /21,0 ммоль/ бутиральдегида. Затем смесь нагревают до комнатной температуры и перемешивают в течение ночи, после чего выливают в воду и экстрагируют метиленхлоридом. Экстракт сушат над сульфатом натрия и выпаривают. Получают 6,4 г остатка. Остаток обрабатывают на хроматографической колонке с силикагелем, элюируя смесью 2% метанола в метилен хлориде, содержащей следовые количества гидроокиси аммония. Соответствующие фракции объединяют и получают 4,8 г 2-/ди-н-пропиламино/-8-/1-гидроксибут-1-ил/-1,2,3,4-тетрагидрофнаталина в виде густого маслянистого вещества.
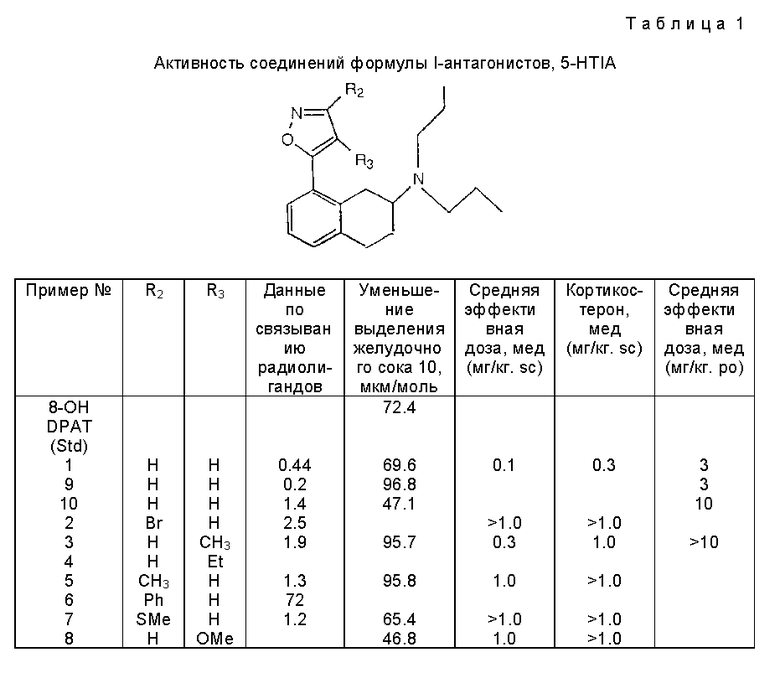
Масло /4,0 г 13,2 ммоль/ растворяют в 200 мл метиленхлорида и добавляют молекулярное сито 4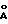 /30 г/. Смесь перемешивают и добавляют 10,0 г /46,2 ммоль/ хлорхромата пиридиния. Перемешивание продолжают в течениеи3 часов при комнатной температуре, после чего смесь выливают на силикагель и последовательно элюируют эфиром и 3% метана в метиленхлориде, содержащем следовые количества гидроокиси аммония, получая при этом продукт в виде коричневого масла.
/30 г/. Смесь перемешивают и добавляют 10,0 г /46,2 ммоль/ хлорхромата пиридиния. Перемешивание продолжают в течениеи3 часов при комнатной температуре, после чего смесь выливают на силикагель и последовательно элюируют эфиром и 3% метана в метиленхлориде, содержащем следовые количества гидроокиси аммония, получая при этом продукт в виде коричневого масла.
Маслянистый продукт обрабатывают на хроматографической колонке с силикагелем, элюируя смесью 3% метанола и метиленхлорида, содержащей следовые количества гидроокиси аммония. Соответствующие фракции объединяют, получая при этом масло, которое при растворении в эфире вызывает осаждение коричневого осадка. Осадок удаляют путем фильтрации, а фильтрат выпаривают с получением 3,0 г - 2-/ди-н-пропиламино/-8-бутирил-1,2,3,4-тетрагидронафталина в виде светло-коричневого масла.
t-бутокись калия /0,82 г, 7,3 ммоль/ суспендируют в 100 мл тетрагидрофурана. Этилформиат /1,0 г, 13,3 ммоль/ и 2-/ди-н-пропиламино/8-бутирил-1,2,3,4-тетрагидронафталин /1,0 г, 3,3 ммоль/ в тетрагидрофуране добавляют в полученную смесь. Смесь перемешивают при комнатной температуре в течение ночи. Добавляют гидроксиламин /1,2 г, 16,6 ммоль/, затем достаточное количество воды для растворения твердого продукта. Полученную смесь /pH 6/ перемешивают при комнатной температуре в течение 20 часов, после чего выливают в воду, поддерживая pH на уровне 12 путем добавления гидроокиси аммония. Затем смесь экстрагируют метиленхлоридом. Экстракт сушат над сульфатом натрия и выпаривают. Остаток растворяют в 100 мг толуола и добавляют 100 мг п-толуолсульфокислоты. Смесь кипятят с обратным холодильником в течение 1,5 часа, после чего выливают в воду и экстрагируют метиленхлоридом. Экстракт метиленхлорида сушат над сульфатом натрия и выпаривают.
Остаток обрабатывают на хроматографической колонке с силикагелем, элюируя смесью /2: 1/ гексана/эфира, содержащей следовые количества гидроокиси аммония. Соответствующие фракции объединяют. Получают 0,9 г указанного в заголовке соединения.
Масс-спектр /FD/: 327 /100/.
Приготовление 5.
Получение 2-/ди-н-пропиламино/-8-/3-метилизоксазол-5-ил/ -1,2,3,4-тетрагидронафталинмалеата.
t-Бутакись калия /450 мг, 4,0 ммоль/ суспендируют в тетрагидрофуране и добавляют 0,7 мл /7,3 ммоль/ этилацетата и 0,5 г /1,8 ммоль/ 2-/ди-н-пропиламино-8-ацетил-1,2,3,4-тетрагидронафталина в тетрагидрофуране. Общее количество используемого тетрагидрофурана составляет 30 мл. Затем смесь перемешивают в течение ночи при комнатной температуре, после чего добавляют 640 мг /9,2 ммоль/ гидроксиламингидрохлорида. Реакционную смесь перемешивают при комнатной температуре в течение 64 часов. Затем смесь выливают в воду, поддерживая с помощью гидроокиси аммония значение pH на уровне 6-12. После этого смесь экстрагируют смесью изопропилового спирта и хлороформа, взятых в соотношении 1:3. Экстракт сушат над сульфатом натрия и выпаривают. Получают 450 мг твердого продукта. Полученный продукт растворяют в толуоле, добавляют небольшое количество п-толуолсульфокислоты, после чего смесь кипятят с обратным холодильником в течение 2 часов. Затем смесь выливают в воду. Значение pH поддерживают на уровне 12, используя для этой цели гидроокись аммония, после чего смесь экстрагируют метиленхлоридом. Экстракт метиленхлорида сушат над сульфатом натрия и выпаривают. Получают 390 мг коричневого масла.
Масло обрабатывают на хроматографической колонке с силикагелем, элюируя метиленхлоридом, содержащим 2% метанола и следовые количества гидроокиси аммония. Соответствующие фракции объединяют и получают 210 мг /35%/ свободного основания указанного в заголовке соединения.
По стандартной методике соединение преобразуют в малеат, который перекристаллизовывают из смеси этанола и эфира с получением 200 мг указанного в заголовке соединения с т.пл. 125,5-127,5oC.
Масс-спектр /FD/: : 313/100/.
Данные анализа для C24H31N2O5
Рассчитано: C 67,27; H 7,53; N 6,54;
Найдено: C 67,52; H 7,29; N 6,48.
Приготовление 6.
Получение 2-/ди-н-пропиламино/ -8-/3-фенилизоксазол-5-ил/- 1,2,3,4-тетрагидронафталингидробромида.
Ацетофеноксим /750 мг, 5,5 моль/ растворяют в тетрагидрофуране и охлаждают смесь до -5oC. Добавляют н-бутиллитий /12,0 мл, 11,1 ммоль/ и перемешивают смесь в течение часа при -5oC. 2-/ди-н-пропиламино/-8-метоксикарбонил-1,2,3,4-тетрагидронафталин /0,8 г, 2,8 ммоль/, растворенный в тетрагидрофуране, добавляют к полученной смеси, так что бы общее количество тетрагидрофурана в смеси составило 100 мл/, после чего нагревают смесь до комнатной температуры. Затем смесь выливают в воду и экстрагируют метиленхлоридом. Экстракт сушат над сульфатом аммония и выпаривают. Получают 1,4 г остатка.
Остаток обрабатывают на хроматографической колонке с силикагелем, элюируя смесью гексана и эфира, содержащей следовые количества гидроокиси аммония. Соответствующие фракции соединяют, получая при этом 220 мг свободного основания указанного в заголовке соединения.
Используя стандартную методику, свободное основание преобразуют в гидробромид, который перекристаллизовывают из смеси метанола и эфира, получая 150 мг указанного в заголовке белого порошка. Т.пл.
171,5 - 173oC. Масс-спектр /FD/: 374/100.
Данные анализа для C25H30N2OBr
Рассчитано: C 65,83; H 6,86; N 6,15;
Найдено: C 65,74; H 6,86; N 5,92.
Приготовление 7.
Получение 2-/ди-н-пропиламино /-8-/3-метилтиоизксазол-5-ил/-1,2,3,4-тетрагидронафталинмалеата.
2-/ди-н-Пропиламино/ 8-/3,3-ди/метилтио/-1-оксопроп-2-ен-1-ил/ -1,2,3,4-тетрагидронафталин /0,64 г, 1,7 ммоль/ растворяют в смеси толуола и уксусной кислоты. Добавляют гидроксиламингидрохлорид /1,2 г, 17 ммоль/ и ацетат натрия /1,2 г, 14 ммоль/ в 10 мл воды. Затем добавляют этанол /10 мл/, чтобы придать смеси однородный характер. Смесь нагревают до 100oC в течение 18 часов, после чего добавляют 0,6 г гидроксиламингидрохлорида. Смесь перемешивают при 100oC еще в течение четырех часов и добавляют еще 0,6 г гидроксиламингидрохлорида. После этого смесь перемешивают в течение 2 часов при 100oC и еще в течение ночи при комнатной температуре. Смесь выливают в воду и водную смесь дважды промывают эфиром, после чего экстрагируют 10% соляной кислотой. Водный слой объединяют и придают им основной характер /pH 12/. Затем смесь экстрагируют метиленхлоридом и экстракт сушат над сульфатом натрия и выпаривают. Получают 560 мг темно-желтого масла.
Масло обрабатывают на хроматографической колонке с силикагелем, элюируя градиентом 1,5 - 2% матанола в метиленхлориде, содержащем следовые количества гидроокиси аммония. Соответствующие фракции объединяют, получая 230 мг продукта. Продукт преобразуют в малеат и перекристаллизовывают из смеси этилацетата и гексана. Получают 210 мг указанного в заголовке соединения с т.пл. 118 - 119,5oC. Масс-спектр /FD/: 344/100.
Данные анализа:
Рассчитано: C 62,59; H 7,00; N 6,08;
Найдено: C 62,84; H 7,04; N 6,02.
Приготовление 8.
Получение 2-/ди-н-пропиламино/-8-/4-метоксиизоксазол-5-ил/- 1,2,3,4-тетрагидронафталингидробромида.
2/ди-н-Пропиламино/-8-юром-1,2,3,4-тетрагидронафталин /5,0 г, 16,1 ммоль/ растворяют в 25 мл тетрагидрофурана и охлаждают до - 78oC, после чего добавляют 3,22 мл н-бутиллития /1M в гексане/. Смесь выдерживают при -78oC в течение 1,5 часов. Полученный раствор подают через канюлю в раствор метилметоксиацетата /7,5 мл, 160 ммоль/ в тетрагидрофуране при -78oC. Реакционную смесь перемешивают при комнатной температуре в течение ночи, выливают в NaHCO3 - раствор и экстрагируют CH2Cl2. Экстракт сушат над сульфатом натрия и концентрируют. Получают 6,8 г сырого продукта.
Затем материал обрабатывают на хроматографической колонке с силикагелем, элюируя 4% метанолом в метиленхлориде, содержащим следовые количества гидроокиси аммония. Соответствующие фракции соединяют, получая при этом 1,4 г 2-/ди-н-пропилмино/ -8-метоксиацетил-1,2,3,4-тетрагидронафталина.
Раствор 2-/ди-н-пропиламино/-8-метоксиацетил-1,2,3,4-тетрагидронафталина /1,0 г/ и трис/ди-метиламино/ метана /1,5 мл/ в толуоле /25 мл/ кипятят с обратным холодильником в течение 1,5 часа. Реакционный продукт концентрируют с получением 2-/ди-н-пропиламино/-8-/1-оксо-2-метокси-3-/диметиламино/-проп-2-енил/ -1,2,3,4-тетрагидронафталина в необработанном виде /1,2 г/.
Гидроксиламингидрохлорид /1,2 г/ добавляют в раствор 2-/ди-н-пропиламино/-8-/1-оксо-2-метокси-3-/диметиламино/-проп-2-енил- 1,2,3,4-тетрагидронафталина /1,1 г/ в метаноле и реакционную смесь перемешивают при комнатной температуре в течение ночи. Реакционную смесь концентрируют и остаток растворяют в толуоле. К раствору добавляют п-толуолсульфокислоту и кипятят с обратным холодильником в течение 2 часов, затем концентрируют и остаток растворяют в воде и метиленхлориде. Смесь выливают в раствор бикарбоната натрия и полученную смесь экстрагируют метиленхлоридом. Экстракт сушат с помощью сульфата магния и концентрируют. Получают 600 мг маслянистого продукта. Продукт очищают методом флеш-хроматографии, элюируя 1:1 смесью эфир/гексаны, с получением 160 мг свободного основания указанного в заголовке соединения. Получают гидробромид. После повторной перекристаллизации из смеси метанол/эфир получают гидробромид указанного в заголовке соединения в виде белых кристаллов /86 мг/, т.пл. 178oC.
Данные анализа:
Рассчитано: C 5868; H 7,14; N 6,84;
Найдено: C 58,88; H 7,23; N 6,60.
Приготовление 9.
Получение S-/-/-8/ изоксазол-5-ил/2-дипропиламино -1,2,3,4-тетрагидронафталинмалеата.
Раствор S-/-/-8-ацетил-2-дипропил-1,2,3,4-тетрагидронафталенмалеата /5,0 г, 18,3 ммоль и трис/диметиламино/метана /7,6 мл, 45,8 ммоль в толуоле /200 мл/ нагревают до 80oC в течение 20 часов. Растворитель удаляют, а остаток растворяют в уксусной кислоте /50 мл/. Добавляют гидроксиламингидрохлорид /2,5 г, 36,6 ммоль/ и реакционную смесь перемешивают при комнатной температуре 20 часов. Затем смесь выливают в воду. Полученную смесь подщелачивают с помощью NaOH и экстрагируют метиленхлоридом. Экстракт сушат с помощью сульфата натрия и концентрируют с получением темно-красного масла. Очищают смесь методом флеш-хроматографии /1:2 эфир/гексаны /NH4OH//, получая при этом 4,3 г /79%/ желаемого продукта. Путем присоединения малеиновой кислоты получают соль. После кристаллизации из смеси этанол/эфир получают кристаллы светло-желтого цвета /5,3 г, т.пл. 127-128,5oC/.
Данные масс-спектра /FD : 298/100/.
Данные оптического вращения: [α]D = -33,04o (с = 1,0 H2O):
(α)365 = 57,34o/ c = 1,0, H2O/
Данные анализа для C19H26N2O • C4O4 • O • 2H2O
Рассчитано: C 66,07; H 7,33; N 6,70;
Найдено: C 65,95; H 6,92; N 7,08.
Приготовление 10.
Получение R-/+/ /-8-/ изоксазол-5-ил/2-дипропиламино-1,2,3,4-тетрагидронафталинмалеата.
Раствор R-/+/ -8-ацетил-2-дипропил-1,2,3,4-тетрагидронафталинмалеата /5,0 г, 18,3 ммоль/ и трис/диметиламино/метана /7,6 мл, 45,8 ммоль/ в толуоле /200 мл/ нагревают до 80oC в течение 20 часов. Растворитель отгоняют и остаток растворяют в уксусной кислоте /25 мл/. Добавляют гидроксиламингидрохлорид /2,5 г, 36,6 ммоль/ и реакционную смесь перемешивают при комнатной температуре в течение 20 часов. Смесь выливают в воду и промывают эфиром. Полученный водный слой подщелачивают при использовании раствора NaOH и экстрагируют метиленхлоридом. Экстракт сушат с помощью сульфата натрия и концентрируют. Получают 5,1 г неочищенного продукта. После очистки методом флеш-хроматографии /1: 2, эфир/гексаны /NH4OH/ получают 4,6 г /83%/ желаемого основания. Соль получают при реакции с малеиновой кислотой. После кристаллизации из смеси этанол/эфир получают белое твердое вещество /5,4 г, т.пл. 127-128,5o/.
Данные масс-спектра: /FD/: 298/100
Данные анализа для C19H26N2O • C4H4O4 • 0,2H2O:
Рассчитано: C 66,07; H 7,33; N 6,70;
Найдено: C 65,71; H 6,93; N 7,14.
Приготовление 11.
Получение R-/+/-8-/4-метил-5-изоксазолил/2-/дипропиламино-1,2,3,4-тетрагидронафталингидробромида.
Раствор R /+/-8-пропионил-2-дипропиламино-1,2,3,4-тетрагидронафталина /2,0 г, 7,0 ммоль/ и трис/диметиламино/метана /2,54 г, 2,9 мл, 17,4 ммоль/ в толуоле /65 мл/ кипятят с обратным холодильником в течение 3 часов. Растворитель отгоняют, а остаток растворяют в уксусной кислоте /20 мл/. Добавляют гидроксиламингидрохлорид /0,97 г, 14 ммоль/ и реакционную смесь перемешивают при комнатной температуре в течение 3 дней. Затем реакционную смесь выливают в воду. Полученную смесь подщелачивают раствором NaOH и экстрагируют 1:3 - смесью изопропанола и хлороформа. Экстракт сушат с помощью сульфата натрия и концентрируют. Получают маслянистый продукт желтовато-оранжевого цвета. Очищают методом флеш-хроматографии /1: 1/, эфир/гексаны /NH4OH/. Получают 1,46 г /67%/ бесцветного масла. Образующийся гидробромид дважды кристаллизуют из смеси тетрагидрофуран/гексаны. Образуются белые кристаллы /1,32 г, т.пл. 167 - 169o/.
Данные оптического вращения: [α]D = +27,26o/ с = 1,0, H2O/,
[α]365 = +40,90o/ с = 1, 0 • H2O/.
Данные анализа для C20H28N2O • HBr:
Рассчитано: C 61,07, H 7,43, N 7,12
Найдено: C 61,21 H 7,50 N 6,97
Приготовление 12.
Получение 5-/5-изоксазолил/-3-/дипропиламино/хромангидробромида.
Раствор 5-ацетил-3-дипропиламинохрома /500 мг, 1,81 ммоль/ и трис/диметиламино/метана /540 мг, 5,4 ммоль/ в толуоле /20 мл кипятя с обратным холодильником в течение 2 часов. Анализ методом тонкослойной хроматографии показывает наличие нового продукта с низким Rf. Реакционную смесь разбавляют разбавленным раствором NaOH и экстрагируют 1:3 смесью изопропанола и хлороформа. Экстракт сушат с помощью сульфата натрия и концентрируют. Получают маслянистый продукт темно-желтого цвета. Продукт растворяют в уксусной кислоте /10 мл/ и добавляют твердый гидроксиламингидрохлорид. Реакционную смесь перемешивают при комнатной температуре в течение 17 часов, разбавляют водой, подщелачивают NaOН и экстрагируют 1:3 смесью изопропанола и хлороформа. Экстракт сушат с помощью сульфата натрия и концентрируют. Получают 534 мг оранжевого масла. Продукт очищают методом флеш-хроматографии /1: 1, эфир: гексаны/ NH4OH. Получают бесцветный маслянистый продукт /482 мг, 88%/. Продукт преобразуют в его гидробромид и кристаллизуют из смеси этилацетат/гексаны с получением белого твердого вещества. Т.пл. 171,5 - 173 oС.
Данные масс-спектра /FD/ : 300/100/
Данные анализа для C18H24N2O2 • HBr:
Рассчитано: C 56,70; H 6,61; N 7,35;
Найдено: C 56,71; H 6,56; N 7,54.
Как было указано выше, представляемые изобретением соединения имеют сродство в отношении связывания как 5-HT1A, так и мускариновых рецепторов /M1/.
Приведенные ниже примеры экспериментальной части демонстрируют способность представляемых изобретений соединений связывать 5-HT1A-рецепторы. Специфические участки, меченые содержащим третий 8-гидрокси-2-дипропиламино-1,2,3,4-тетрагидронафталином /3H-8-OH-DPAT/, идентифицируются как 5-HT1A-рецепторы. Общая методика приводится в работе Wong и сотр.
J.Neural Transm 71: 207 - 218 /1988/.
Связывание рецепторов 5:HT1A при опытах in vitro
Самцов крыс породы Spragne-Dawley /110-150 г/, поставляемых фирмой Harlan Industries (Cumberland, IN), кормят вдосталь по меньшей мере в течение последних 3 дней перед началом исследований. Крыс убивают методом дикапитации. Быстро извлекают головной мозг и вскрывают кору головного мозга при 4oC.
Ткани мозга гомогенизируют в 0,32 М сахарозе. После центрифугирования при 1000g в течение 10 минут, а затем при 17000g в течение 20 минут осаждают необработанную синаптосомальную фракцию. Осадок в пробирке после центрифугирования суспендируют в 100 об. 50 мМ трис- HCl, pH 7,4 инкубируют при 37oC в течение 10 минут, после чего центрифугируют при 5000g в течение 10 минут. Процесс повторяют и конечный осадок в пробирке суспендируют в 50 мМ ледяной трис- HCl.Связывание 3H-8-OH-DRAT происходит в соответствии с методом, описанным Wong и сотр. J. Neural. Fransm 64: 251-269 /1985/. Короче говоря, синаптосомальные оболочки, выделенные из коры головного мозга, выдерживают при 37oC в течение 10 минут в 2 мл 50 мМ трис-HCl, pH 7,4, 10 мМ паргилина, 0,6 мМ аскорбиновой кислоты, 5 мМ CaCl2, 2нМ 3H-8-OH-DPAT и 0,1 нм интересующего авторов соединения. Связывание определяют путем фильтрования пробы при пониженном давлении через фильтры из стекловолокна. Фильтры дважды промывают 5 мл охлажденного льдом буфера и помещают в сцинтиляционные пробирки /емкости/ с 10 мл PCS /Amersham/Searle/ сцинтиляционной жидкости. Радиоактивность измеряют с помощью жидкостного сцинтиляционного спектрометра. Намеченный 8-OH-DPAT в /10 мМ/ также вводят в отдельные пробы с целью определения неспецифического связывания. Специфическое связывание 3H-8-OH-DPAT определяют как разницу радиоактивности в присутствии и отсутствии 10 мМ немеченого 8-OH-DPAT.
Результаты исследований приведены в таблицах 1 и 2.
5 HTIA-активность при опытах in vivo.
Представляемые изобретением соединения исследуют также in vivo на их активность на мозг 5-HIAA и уровень кортикостерона в сыворотке. Самцам крыс весом 150 - 200 г вводят подкожно или орально водные растворы исследуемых соединений. Через час после введения крыс декапитируют и собирают кровь с туловища. Затем кровь коагулируют и центрифугируют с целью выделения сыворотки. Концентрацию кортикостерона в сыворотке определяют методом спектрофлуорометрии по данным J. Solem, I.Brinck Johnson, Scand. J. Clin. Inrest Snppl. 80 (17,1) 1965/. Мозг целиком быстро извлекают из забитой крысы, замораживают на сухом льду и хранят при -15oC. Концентрацию 5-НIAA измеряют методом жидкостной хроматографии с помощью электрохимического определения по методике, описанной R. Fuller, H.Snoddy, K.Derry, Life Sei 40, 1921 /1987/. Результаты приведены в табл. 1.
Связывание /3H/-пирензепина при опытах in vitro.
Для определения связывания 3H-пирензепина in vitro самцов крыс породы Spragne. Dawley (Harlan Spragne, Indianapolis, весом 100-150 г забивали методом декапитации /отсечения головы/, быстро удаляют головной мозг и выделяют кору головного мозга. Оболочку головного мозга подготавливают к исследованию с помощью дифференциального центрифугирования, дважды промывают и замораживают до использования.
Снижение связывания 3H-пирензепина с рецепторами определяют путем добавления исследуемого вещества, 1 нМ 3H-пирензепина /87,0 Ci/ ммоль/. New England Nuclear, Boston, MA и около 100 мкм оболочки головного мозга в 1 мл общего объема 20 мМ трис-HCl буфера, pH 7,4 содержащего 1 мМ MnCl2. После выдерживания в течение 1 часа при 25oC гомогенат фильтруют через фильтр из стекловолокна (Whatman, GF/c) под вакуумом, фильтры 3 раза промывают 2 мл охлажденного буфера и помещают в сцинтилляционные емкости, содержащие 10 мл сцинтилляционной жидкости(Ready Protein + BecKam, Fullerton, CA.). Установленную на фильтрах радиоактивность определяют с помощью жидкостной сцинтилляционной спектрометрии. Неспецифическое связывание определяют с помощью 1 мкм атропина.
Результаты приведены в табл. 2.
Ингибирование выделение желудочного сока.
Уменьшение секреции желудочного сока определяют в привратнике легированных крыс по методике, разработанной Шеем /см. Shay H, A. Komorov, M. Greenstein, Effects of vagatomy intheraf, Arch. Surg 59, 210-226, 1949/. Самцов крыс породы Sprague-Dawley весом около 200 г не кормят в течение 24 часов до начала эксперимента. Воду дают по потребности, под действием легкой эфирной анестезии производят легирование привратника и одновременно животным вводят внутрибрюшинно или подкожно определенную дозу исследуемого соединения, после чего крыс пробуждают от наркоза. Желудочный сок собирают в течение 2 часов. По окончании этого периода крыс забивают.
Содержимое желудка удаляют, измеряют и титруют до конечного значения 7.0. Каждый эксперимент проводят при использовании контрольной группы животных, которым вводят наполнитель, с целью определения процента уменьшения выделения /секреции/ желудочного сока. Результаты приведены в табл. 1.
Изменение увеличенного тонуса мышц, вызванного карбахолом.
Самцов крыс весом 300-350 г не кормят в течение 24 часов. Крыс приносят в лабораторию, забивают методом декапитации и сразу же удаляют толстую кишку. Фекалии вымывают и продольные полоски длиной 4 см помещают в ванночку для извлеченных органов под грузом 1 г при использовании датчиков (Grass FTO3). Ткани уравновешивают и обрабатывают газообразной смесью 95% кислорода и 5% двуокиси углерода. Затем ткани заставляют сокращаться с помощью карбохола с целью выявления тонической реакции. Затем добавляют растворы лекарственного средства, определяя релаксацию. Процент релаксации рассчитывают, принимая во внимание контрольный период перед началом обработки Для большинства соединений испытывают более чем одну концентрацию лекарственного средства. В этих случаях рассчитывают IC50, которую рассматривают как дозу, способную уменьшить вызванную карбахолом реакцию на 50%. Результаты приведены в табл. 2.
В приведенных ниже табл. 1 и 2 представлены результаты оценки различных соединений, являющихся предметом настоящего изобретения.
В табл. 1 в первой колонне приведены номера составов исследуемых соединений, в колонках 2 и 3 указаны замещенные группы R2 и R3, в четвертой колонке даны значения IC50, выраженные в наномолярных концентрациях, необходимых для уменьшения связывания 3H-8-OH-DPAT с 5-HTIA-рецепторами. В колонке 5 приведены процентные количества уменьшения выделения желудочного сока при введении дозы или ED50- значения в мкммоль/кг при опытах in vivo. В колонке 6 указана минимальная эффективная доза /МЕД/ исследуемого соединения, вводимая подкожно для снижения уровня 5-5IAA в мозге, в седьмой колонке даны значения МЕД для исследуемых соединений, вводимых подкожно для подъема уровня кортикостерона в сыворотке. В восьмой колонке приведены те же самые данные, что и в колонке 6, с учетом того, что испытуемое вещество вводится орально. Данные колонок 6-8 представляют активность агониста 5-HTIA.
В табл. 2 нашло отражение действие типовых соединений формулы I на мускариновые рецепторы (M1). Первые три колонки отражают те же самые значения, что и в таблице 1. Колонка 4 дает значения IC50, выраженные в наномолярной концентрации, необходимые для снижения связывания 3H-пирезепина с мускариновыми рецепторами (M1).
В колонке 5 приведены IC50 - значения в мкмМ, необходимые для уменьшения вызванной карбахолом гипертонии /увеличенного тонуса мышечного слоя в гладких мышцах толстой кишки/ при опытах in vitro.
Таким образом одним из предметов настоящего изобретения является способ лечения синдрома раздраженной толстой кишки, состоящий в модулировании активности как 5-HTIA, так и мускариновых рецепторов (M1), включающий введенные млекопитающим необходимого для лечения указанного синдрома фармацевтически эффективного количества соединения формулы I.
Термин "фармацевтически активное количество", используемый в данном случае, обозначает количество патентуемого соединения, способного связывать серотониновый /IA/ и мускариновый (M1) рецепторы. Специфическая доза соединения, вводимого в соответствии с настоящим изобретением, будет естественно определяться конкретными обстоятельствами, с которыми приходится иметь дело в данном случае, включая, например, назначение соединения, способ применения /введения/, а также условия, в которых проводится лечение. Типовая суточная доза обычно составляет от около 0,01 мг/кг до около 20 мг/кг активного соединения, представляемого настоящим изобретением. Предпочтительная суточная доза составляет от около 0,05 до около 10 мг/кг, идеальная - соответственно от 0,1 до 5 мг/кг.
Соединения можно вводить самыми различными способами, в том числе орально, трансдермально, подкожно, внутривенно, внутримышечно, а также через нос.
Представляемые изобретением соединения предпочтительно вводить в виде лекарственных составов. Поэтому одним из предметов настоящего изобретения является фармацевтический состав, содержащий соединение формулы I в комбинации с фармацевтически приемлемыми наполнителями, разбавителями или добавками.
Представляемые изобретением составы можно приготавливать, руководствуясь известными методами, используя известные и доступные ингредиенты. При приготовлении представляемых изобретением составов активный компонент целесообразно смешивать с наполнителем или разбавителем или же заключить его в оболочку, которая может быть в форме капсулы, бумажного пакетика и т.д. Если наполнитель выполняет роль разбавителя или растворителя, он может быть твердым, полутвердым или жидким, действуя при этом как жидкость, добавка или среда для активного ингредиента. Таким образом составы могут быть приготовлены в форме таблеток, драже, порошков, пастилок, саше, эликсиров, суспензий, эмульсий, растворов, сиропов, аэрозолей /в виде твердой или жидкой среды/, притираний, содержащих, например, до 10% на вес активного соединения, мягких или твердых желатиновых капсул, свечей, стерильных растворов для инъекций, стерильно упакованных порошков и т.д.
Примером приемлемых наполнителей, добавок и разбавителей могут служить такие вещества, как лактоза, декстроза, сахароза, сорбит, маннит, крахмалы, гуммиарабик /аравийская камедь/, фосфат кальция, альгинат, трагант, силикат кальция, микрокристаллическая целлюлоза, поливинилпирролидон, целлюлоза, водные растворы сиропов, метилцеллюлоза, метилгидроксибензоаты, пропилгидроксибензоаты, тальк, стеарат магния и минеральные масла. Составы могут дополнительно содержать смазывающие и смачивающие вещества, эмульсирующие, суспендирующие и консервирующие агенты, подслащивающие и ароматизирующие средства и т.д. Представляемые изобретением составы должны быть приготовлены таким образом, чтобы обеспечить быстрое и непрерывное выделение активного ингредиента после введения лекарства пациенту.
Предпочтительно, если составы приготовлены в единой дозировочной форме. Каждая дозировка обычно содержит от около 1 до около 250 мг активного ингредиента. Термин "единая дозировочная форма" относится к состоящей из отдельных элементов единице, приемлемой в качестве унифицированной /стандартной/ дозы для человека и других млекопитающих, причем каждая такая доза содержит заранее предопределенное количество активного вещества, рассчитанное для произведения желаемого терапевтического эффекта, в сочетании с фармацевтически приемлемым наполнителем.
Приведенные ниже примеры составов носят иллюстрированный характер и их описанием предмет изобретения никоим образом не ограничивается.
Состав 1.
Твердые желатиновые капсулы приготовлены при использовании следующих ингредиентов, мг/капсула:
2-/ди-Пропиламино/8-/изоксазол-5-ил- 1,2,3,4-тетрагидронафталингидрохлорида - 250
Крахмал, сухой - 200
Стеарат магния - 10
Всего - 460
Указанные выше ингредиенты смешиваются и заключаются в жесткие желатиновые капсулы в количестве 460 мг.
Состав 2.
Таблетки изготовлены при использовании указанных ниже ингредиентов, мг/капсула
2-/ди-н-Пропиламино/ 8-/4-метил-изоксазол-5-ил/- 1,2,3,4-тетрагидронафталингидрохлорид - 250
Микрокристаллическая целлюлоза - 400
Двуокись кремния, дымящаяся - 10
Стеариновая кислота - 5
Всего - 665
Компоненты смешивают и прессуют в форме таблеток по 665 мг каждая.
Состав 3.
Суспензии (каждая содержит 50 мг активного ингредиента на 5 мл-дозу) были приготовлены следующим образом, на капсулу
2-Диаллиламино-8-/3-фенилизоксазол-5-ил/- 1,2,3,4-тетрагидронафталингидрохлорид, мг - 50
Na-Карбоксиметилцеллюлоза, мг - 50
Сера, мл - 1,25
Раствор бензойной кислоты, мл - 0,10
Ароматизирующие средства
Цветовые добавки
Дистиллированная вода, всего, мл - 5
Активный ингредиент пропускают через сито N 45-меш, США и смешивают с Na-карбоксиметилцеллюлозой и сиропом, получая при этом однородную пасту. Раствор бензойной кислоты, ароматизирующие средства и цветовые добавки разбавляют небольшим количеством воды и добавляют в полученную пасту при перемешивании. Затем добавляют достаточное количество воды, необходимое для получения желаемого объема.
Состав 4.
Состав для внутривенного введения можно приготовить следующим образом, мг/капсула:
2-Диаллиламино-8-/изоксазол-5-ил/- 1,2,3,4-тетрагидронафталингидрохлорид - 100
Изотонический раствор - 1000
Растворы, содержащие указанные выше ингредиенты, обычно вводят внутривенно со скоростью 1 мл/мин пациенту, страдающему снижением активности.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЗАМЕЩЕННЫЕ В КОЛЬЦЕ 2-АМИНО-1,2,3,4-ТЕТРАГИДРОНАФТАЛИНЫ ИЛИ 3-АМИНОХРОМАНЫ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ КИСЛОТНО-АДДИТИВНЫЕ СОЛИ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1992 |
|
RU2057751C1 |
| ЗАМЕЩЕННЫЕ В КОЛЬЦЕ 2-АМИНО-1,2,3,4-ТЕТРАГИДРОНАФТАЛИНЫ ИЛИ 3-АМИНОХРОМАНЫ | 1994 |
|
RU2105756C1 |
| ПРИМЕНЕНИЕ 6-ГЕТЕРОЦИКЛО-4-АМИНО-1,3,4,5-ТЕТРАГИДРОБЕНЗ(CD) ИНДОЛА ДЛЯ ЛЕЧЕНИЯ РВОТЫ ИЛИ ТОШНОТЫ ПРИ ДВИЖЕНИИ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1993 |
|
RU2138262C1 |
| Способ получения оптически активного бромзамещенного 2-амино-1,2,3,4-тетрагидронафталина | 1990 |
|
SU1826966A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 1,2,3,4-ТЕТРАГИДРОНАФТАЛИНОВ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМОЙ КИСЛОТНО-АДДИТИВНОЙ СОЛИ | 1989 |
|
RU2014330C1 |
| 4-АМИНО-6-ЗАМЕЩЕННЫЕ ТЕТРАГИДРОБЕНЗ[C,D]ИНДОЛЫ | 1992 |
|
RU2073672C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТЕТРАГИДРОБЕНЗ (C,D)ИНДОЛОВЫХ АГОНИСТОВ СЕРОТОНИНА | 1990 |
|
RU2007393C1 |
| 6-ГЕТЕРОЦИКЛИЧЕСКИЗАМЕЩЕННЫЕ 4-АМИНО-1,2,2А,3,4,5-ГЕКСАГИДРОБЕНЗ-(CD)-ИНДОЛЫ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 1992 |
|
RU2062775C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕМЦИТАБИН ГИДРОХЛОРИДА | 1995 |
|
RU2154648C2 |
| НЕПЕПТИДНЫЕ АНТАГОНИСТЫ РЕЦЕПТОРОВ ТАХИКИНИНА | 1994 |
|
RU2140921C1 |
Предложено новое средство и фармацевтическая композиция на его основе для лечения синдрома раздраженной кишки. Средство представляет собой производные изоксазола, 2-(ди-н-пропиламино)-8-(изоксазол-5-ил)-1,2,3,4-тетрагидронафталин; S-(-)-2-(ди-н-пропиламино)-8-изоксазол-5-ил)-1,2,3,4-тетрагидронафталин; R(+)-2-(ди-н-пропиламино)-8-(изоксазол -5-)-1,2,3,4-тетрагидронафталин; 2-(ди-н-пропиламино)-8-(3-бромизоксазол-5-ил )-1,2,3,4-тетрагидронафталин; 2-(ди-н-пропиламино)-8-(4-метилизоксазол-5-ил)-1,2,3,4-тетрагидронафталин; 2-(ди-н-пропиламино)-8-(3-метилтиоизоксазол-5-ил)-1,2, 3,4-тетрагидронафталин; 2-(ди-н-пропиламино)-8-(3-метил-изоксазол-5-ил )-1,2,3,4-тетрагидронафталин; 2-(ди-н-пропиламино) -8-(4-метоксиизоксазол-5-ил)-1,2,3,4-тетрагидронафталин, или его фармацевтически приемлемую соль или сольват. Изобретение расширяет арсенал средств для лечения синдрома раздраженной толстой кишки. 2 с. и 1 з.п.ф-лы, 2 табл.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Габузян К.С | |||
| Лечение больных СРТК с учетом психосоматрических взаимосвязей | |||
| Диссертация на соискание ученой степени к.м.н.-Еренван, 1990, с.50 и 110 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| EP 404359 A, 25.05.90 | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Пожарный двухцилиндровый насос | 0 |
|
SU90A1 |
Авторы
Даты
1999-03-10—Публикация
1993-07-15—Подача