Это изобретение касается цеолита типа X, способа получения литий- и трехвалентного ионообменного цеолита типа X, обладающих повышенной термической стабильностью. Изобретение касается также способа отделения азота от смеси газов с помощью новых литий- и трехвалентных катионообменных цеолитов типа X.
Предпосылки создания изобретения
Отделение азота от других газов, таких как кислород, аргон и водород, имеет значительное промышленное значение. Когда разделение проводится в больших объемах, часто используется дробная перегонка. Однако перегонка слишком дорога вследствие больших начальных капитальных затрат на оборудование и значительного расхода энергии. В последнее время изучаются другие методы разделения для того, чтобы попытаться уменьшить общую стоимость такого разделения.
Альтернативным перегонке методом, используемым для отделения азота от других газов, является адсорбция. Например, цеолит натрий X, описанный в пат. США N 2882244 Milton, используется с некоторым успехом для адсорбционного отделения азота от кислорода. Недостатком использования натрий цеолита X для отделения азота от кислорода является низкая эффективность отделения для отделения азота.
Согласно McKee, пат. США N 3140933, улучшение адсорбции азота наблюдается в результате замены основных натриевых ионов ионами лития. Этот патент описывает, что цеолит типа X, обладающий основными ионами, замененными ионами лития, может быть эффективно использован для отделения азота от кислорода при температурах вплоть до 30oC. Так как ионообмен не исчерпывается и цеолит X синтезируется при использовании натрия в качестве шаблона, частично используемый ионообменный материал смешивают с натрий/литий цеолитом.
Пат. США N 4859217 описывает, что очень хорошее адсорбционное разделение азота от кислорода может быть получено при температурах от 15 до 70oC при использовании цеолита типа X, который имеет более 88% своих ионов, присутствующих в качестве ионов лития, особенно когда используется цеолит, обладающий соотношением алюминия к кремнию от 1 до 1.25.
К сожалению, литийобменный цеолит типа X имеет очень высокое сродство к воде и адсорбированной воде, даже в маленьких количествах, что серьезно снижает адсорбционную способность цеолита. Таким образом, для получения оптимального режима адсорбции необходимо активировать цеолит нагреванием его до температуры 600-700oC для удаления, по возможности, адсорбированной воды. Так как литийобменный цеолит типа X не стабилен при температурах свыше приблизительно 740oC, активирование этих адсорбентов должно тщательно контролироваться для предотвращения разрушения адсорбентов.
Пат. США N 5179979 утверждает, что литий/щелочноземельный металл цеолиты X, обладающие молярным соотношением литий/щелочноземельный металл в ряду от приблизительно 95: 5 до 50:50, имеют термическую стабильность большую, чем соответствующие цеолиты чистого лития и хорошую адсорбционную способность и селективность.
Пат. США N 5152813 описывает адсорбцию азота из смеси газов при использовании кристаллических X-цеолитов, обладающих соотношением Si/Al в цеолите ≤ 1.5, и по крайней мере бинарный ионный обмен обмениваемого иона содержит между 5 и 95% лития и между 5 и 95% второго иона, выбранного из кальция, стронция и смеси их, сумма лития и второго обмениваемого иона составляет по крайней мере 60%.
Хотя цеолиты X типа, являющиеся высоко ионообмениваемыми с ионами лития, имеют превосходные адсорбционные свойства для азота, они дороги для получения. Существует необходимость в адсорбентах, которые имеют превосходную термическую стабильность и высокие адсорбционные свойства для азота и которые могут быть получены с разумными затратами. Настоящее изобретение предлагает группу адсорбентов, обладающих этими характеристиками.
Краткое описание изобретения
Согласно первому аспекту изобретения предлагаются новые цеолитные составы, которые обладают превосходными характеристиками термической стабильности и селективностью для адсорбции азота. Новые цеолиты являются цеолитами типа X, чьи катионы содержат на эквивалентной основе, от приблизительно 50 до приблизительно 95% лития, от приблизительно 4 до приблизительно 50% одного или более выбранных трехвалентных ионов и от 0 до приблизительно 15% и предпочтительно от 0 до приблизительно 10% остаточных ионов. Трехвалентные ионы выбирают из алюминия, скандия, галлия, индия, иттрия, железа (III), хрома (III), отдельных лантанидов, смесей двух или более лантанидов и смесей этих элементов. Оптимальными остаточными ионами являются обычно ионы натрия, калия, аммония, гидроксония. Ионы кальция, стронция, магния, бария, цинка и меди (II) могут также присутствовать в качестве компенсирующих заряд катионов в концентрации менее приблизительно 5%.
Минимальный общий процент лития и трехвалентных ионов, связанных с цеолитом в качестве компенсирующих заряд катионов, на эквивалентной основе составляет 85% и предпочтительно 90%. Катионы, компенсирующие заряд, присутствующие в цеолите, отличные от лития и трехвалентных ионов, указанных выше (если любые другие катионы присутствуют), могут быть одним или более из вышеуказанных остаточных ионов, или они могут быть одним или более любыми другими катионами, или они могут быть смесью любых из них. На эти другие катионы накладывается только ограничение в том, что они не должны отрицательно воздействовать на пригодность цеолита в качестве адсорбента азота или же отрицательно воздействовать на цеолит. Эти другие катионы могут присутствовать в количестве вплоть до приблизительно 15% общего количества компенсирующих заряд катионов, на эквивалентной основе. В наиболее предпочтительных воплощениях изобретения минимальный процент лития и трехвалентных ионов, служащих в качестве компенсирующих заряд катионов, составляет 95%,
Атомное соотношение кремния к алюминию у цеолитов изобретения является широким в ряду цеолитов X, т.е. в ряду от приблизительно 0.9 до 1.5 и предпочтительно в ряду от приблизительно 0.9 до 1.25. Наиболее предпочтительными цеолитами являются цеолиты типа X с низким содержанием кремния (обычно обозначаемые как LSX цеолиты). Они имеют атомное соотношение кремния к алюминию в ряду от приблизительно 0.9 до 1.1.
В предпочтительном воплощении цеолит является неолитом, в котором, на эквивалентной основе, от приблизительно 70 до приблизительно 95% компенсирующих заряд катионов являются ионами лития, от приблизительно 5 до приблизительно 30% является трехвалентными ионами и от 0 до приблизительно 10% являются остаточными ионами.
В другом предпочтительном воплощении трехвалентные ионы выбирают из алюминия, церия, лантана, смеси двух или более лантанидов, в которых объединенный вес ионов лантана, церия, празеодима и неодима, присутствующих в смеси, содержит по крайней мере 50% от общих ионов лантанидов на молярной основе, и из их смесей.
В другом предпочтительном воплощении остаточные ионы выбирают из кальция, стронция, магния, цинка и их смесей, и они могут присутствовать в количествах менее приблизительно 5% от общего количества компенсирующих заряд ионов, связанных с цеолитом.
В наиболее предпочтительном воплощении компенсирующие заряд катионы содержат в основном только литий и один или более из вышеназванных трехвалентных ионов. Другими словами цеолит содержит не более приблизительно 1% остаточных ионов в качестве компенсирующих заряд катионов.
Согласно второму аспекту изобретения вышеописанный цеолит используется в качестве адсорбента для выделения азота из смеси газов. Отделение осуществляется пропусканием газовой смеси через по крайней мере одну адсорбционную зону, содержащую адсорбент, тем самым предпочтительно адсорбируя азот из вышеназванной смеси газов. Процесс адсорбции в основном выполняется при температуре в ряду от приблизительно -190 до приблизительно 70oC и абсолютном давлении в ряду от приблизительно 0.7 до 15 бар.
В предпочтительном воплощении этого аспекта изобретения процесс адсорбции является циклическим и включает вышеназванную стадию адсорбции и стадию десорбции азота из адсорбционной зоны (зон). Предпочтительные циклические процессы включают адсорбцию при изменяющемся давлении, адсорбцию при изменяющейся температуре и их комбинацию.
Когда процесс адсорбции является адсорбцией при изменяющемся давлении, адсорбент в основном регенерируется при абсолютном давлении в ряду от приблизительно 100 до приблизительно 5000 миллибар, и когда процесс является адсорбцией при изменяющейся температуре, адсорбент обычно регенерируется при температуре в ряду от приблизительно 0 до приблизительно 300oC.
В других предпочтительных воплощениях стадия адсорбции выполняется при температуре в ряду от приблизительно -20 до приблизительно 50oC и абсолютном давлении в ряду от приблизительно 0.8 до 10 бар.
В наиболее предпочтительном воплощения изобретения процесс адсорбции используется для разделения азота от смеси газов, содержащей азот и один или более газов, таких как кислород, аргон, гелий, неон и водород.
В других предпочтительных воплощениях изобретения регенерация адсорбционного слоя проводится в вакууме или с помощью продувки слоя одним или более инертными газами, неадсорбируемым газовым продуктом из адсорбционной системы или комбинацией регенераций вакуумом и продувкой, и повторное повышение давления осуществляется по крайней мере частично при использовании неадсорбированного газа из адсорбционной системы.
Детальное описание изобретения
Изобретение пригодно для отделения азота от смеси газов. Разделение выполняется с помощью адсорбции при использовании адсорбента, который селективно адсорбирует азот относительно других газов смеси. Типичные разделения включают отделение азота от других компонентов воздуха, таких как кислород и/или аргон, гелий, неон, водород и т.д. Предпочтительные разделения включают отделение азота от кислорода и аргона.
Новые адсорбенты изобретения включают цеолит типа X, обладающий компенсирующими заряд катионами, смесью ионов лития и трехвалентными ионами, выбранными из ионов алюминия, скандия, галлия, иттрия, железа (III), хрома (III), индия и ионов группы лантанидов. Ионы группы лантанидов включают лантан, церий, празеодим, неодим, прометий, самарий, европий, гадолиний, тербий, диспрозий, гольмий, эрбий, тулий, иттербий и лютеций. Для получения адсорбента изобретения могут также быть использованы смеси любых двух или более вышеприведенных трехвалентных ионов. Предпочтительные трехвалентные катионы включают ионы алюминия, церия, лантана и смесей лантонидов, в которых объединенные концентрации лантана, церия, празеодима и неодима составляют по крайней мере приблизительно 50% и предпочтительно по крайней мере приблизительно 75% общего количества ионов лантанидов в смесях.
Цеолит типа X является кристаллическим алюмосиликатом с атомным соотношением кремния к алюминию 1.5 или менее. Соотношение кремния к алюминию в цеолите типа X изменяется от теоретически минимального значения 1.0 до приблизительно 1.5, однако вследствие дефектов в структуре цеолита, примесей, таких как окклюдированные оксид алюминия и/или алюминаты, ошибок в измерении и дефектов в структуре, наблюдаемые соотношения кремния к алюминию в цеолитах типа X измеряются до 0.9. Для целей этого обсуждения принимают, что минимальное соотношение кремния к алюминию для цеолита типа X составляет 0.9. Предпочтительный для использования в получении новых адсорбентов изобретения цеолит типа X обладает атомным соотношением кремния к алюминию менее чем приблизительно 1.25. Наиболее предпочтительным цеолитом типа X является цеолит с соотношением кремния к алюминию от приблизительно 0.9 до приблизительно 1.10, который обычно обозначается как цеолит с низким содержанием кремния X (LSX).
Адсорбенты изобретения обычно получают на основе цеолита типа X, который обычно первоначально имеет в качестве компенсирующих заряд катионов, т.е. ионов, которые компенсируют отрицательный заряд алюмосиликатной решетки, ионы натрия и/или калия. До получения адсорбентов изобретения может быть желательно превращение всех катионов к единому виду катионов, предпочтительно иону натрия или аммония.
В более широком воплощении изобретения от приблизительно 95% до приблизительно 50% компенсирующих заряд катионов составляют ионы лития, от приблизительно 4 до приблизительно 50% катионов являются трехвалентными ионами и от 0 до приблизительно 15% являются остаточными ионами, т.е. ионами, связанными с цеолитом в качестве компенсирующих заряд катионов, отличных от лития и вышеприведенных трехвалентных ионов. Остаточные ионы могут присутствовать в результате методики, используемой при получении катионообменного цеолита типа X или они могут быть специально введены в цеолит для дополнительной модификации его свойств. В типичных воплощениях изобретения от приблизительно 70 до приблизительно 95% компенсирующих заряд катионов составляют ионы лития, от приблизительно 5 до приблизительно 30% катионов являются трехвалентными ионами и от 0 до приблизительно 10% являются остаточными ионами. В большинстве случаев остаточными ионами будут ионы натрия, калия, аммония, гидроксония, кальция, магния или их смеси. В некоторых случаях может быть желательным использование двухвалентных катионов, таких как ионы магния, кальция, стронция, бария, цинка или меди (II), в качестве части или полностью всех остаточных ионов, так как двухвалентный ионообменный цеолит типа X имеет лучшие адсорбционные для азота свойства, чем цеолит типа X с ионами натрия или калия. Как описано выше, предпочтительно ограничивать присутствие двухвалентных катионов до менее чем приблизительно 5% от общего количества компенсирующих заряд катионов.
Новые адсорбенты изобретения могут быть получены, например, с помощью катионного обмена адсорбента с раствором литиевого соединения и растворами соединений вышеприведенных трехвалентных ионов. Предпочтительно, хотя и необязательно, использование водных растворов обмениваемых ионов. Могут быть использованы любые водорастворимые соединения обмениваемых ионов. Предпочтительными водорастворимыми соединениями ионов являются соли, особенно хлориды, сульфаты и нитраты. Более предпочтительными солями являются хлориды вследствие их высокой растворимости и легкой доступности.
Порядок обмена катионов не является определяющим. Одна методика проводится для того, чтобы обменять основной адсорбент с литиевыми ионами, затем для того, чтобы обменять литийобмененный адсорбент с одним или более трехвалентными ионами. В некоторых случаях может быть желательно провести первым катионный обмен трехвалентным ионом для требуемого уровня обмена, затем необязательно кальцинироватъ частично обмененный неолит и затем провести литиевый обмен. Третий метод заключается в одновременном обмене основного адсорбента литиевыми ионами и требуемыми одним или более трехвалентными ионами.
Цеолиты настоящего изобретения могут иметь различные физические формы, точная физическая форма продукта может влиять на его пригодность для PSA способов. Если цеолиты настоящего изобретения используются для промышленных адсорбентов, то может быть предпочтительно, чтобы цеолиты агрегировались (т. е. гранулировались) для контроля диффузии в макропорах, или же измельченные цеолиты могут упаковываться в адсорбционные колонки промышленного размера, тем самым блокируя или по крайней мере значительно снижая поток через колонку. Это квалифицируется в технологии молекулярных сит как обычные методики для агрегации молекулярных сит; такие методики обычно включают смешение молекулярных сит со связующим агентом, которым обычно является глина, образование смеси в агрегате, обычно экструзией или образованием шариков, и нагревание образованной смеси молекулярных сит/связующего агента при температуре приблизительно 600-700oC до превращения сырого агрегата в такой, который является устойчивым к раздавливанию. Используемые для агрегатов цеолитов связывающие агенты могут включать глины, двуоксид кремния, глиноземы, оксиды металлов и их смеси. Кроме того, цеолиты могут соединяться с материалами, такими как двуоксид кремния-глинозем, двуоксид кремния-оксид магния, двуоксид кремния-двуоксид циркония, двуоксид кремния-оксид тория, двуоксид кремния-двуоксид бериллия и двуоксид кремния-оксид титана, также как и трехкомпонентные композиции, такие как двуоксид кремния-оксид алюминия-оксид тория, двуоксид кремния-оксид алюминия-двуоксид циркония и глины присутствуют в качестве связывающих агентов. Относительные пропорции вышеприведенных материалов и цеолитов могут широко изменяться. Если цеолиты связываются в агрегаты до использования, то такие агрегаты имеют желательно диаметр приблизительно от 0.5 до приблизительно 5 мм. Агрегация может осуществляться до или после ионных обменов ионов лития или трехвалентных металлов, требуемых для получения цеолитов настоящего изобретения, т.е. первой стадией может быть получение цеолита лития/трехвалентного металла и затем проведение агрегации, или в качестве исходного материала для ионных обменов может быть использован цеолит X, который уже будет в агрегированной форме. Вообще последнее предпочтительно, так как натрий цеолит X является более термически стабильным, чем цеолит лития/трехвалентного металла настоящего изобретения и, следовательно, менее чувствителен к повреждению от высоких температур, использующихся в процессе агрегации. Однако описано, что требуется активация литий/трехвалентный металл цеолита, даже если натрий цеолит, используемый в качестве исходного материала, активируется в течение процесса агрегации.
Температура, при которой стадия адсорбции процесса адсорбции проводится, зависит от ряда факторов, таких как отдельные газы, требующие разделения, особые адсорбенты, использующиеся в процессе, и давление, при котором проводится адсорбция. Вообще стадия адсорбции проводится при температуре по крайней мере приблизительно -190oC, предпочтительно при температуре по крайней мере приблизительно -20oC и более предпочтительно при температуре по крайней мере приблизительно 15oC. Адсорбция обычно выполняется при температурах не более чем приблизительно 70oC и предпочтительно не более чем приблизительно 50oC и более предпочтительно не более чем приблизительно 35oC.
Стадия адсорбции процесса изобретения может выполняться при любых обычных или хорошо известных давлениях, пригодных для адсорбции с изменяющейся температурой газовой фазы и для процессов адсорбции с изменяющимся давлением. Обычно минимальное абсолютное давление, при котором проводится процесс адсорбции, в большинстве случаев составляет приблизительно 0.7 бар, предпочтительно приблизительно 0.8 бар и более предпочтительно приблизительно 0.9 бар. Адсорбция в большинстве случаев выполняется при давлении не более чем приблизительно 15 бар, предпочтительно не более чем приблизительно 10 бар и более предпочтительно не более чем приблизительно 4 бара. Когда процесс адсорбции является PSA, давление в течение стадии регенерации снижается обычно до абсолютного давления в ряду от приблизительно 100 до приблизительно 5000 миллибар и предпочтительно до абсолютного давления в ряду от приблизительно 175 до приблизительно 2000 миллибар и более предпочтительно до абсолютного давления в ряду от приблизительно 200 до приблизительно 1100 миллибар. Когда адсорбция является TSA, температура слоя поднимается в процессе регенерации слоя. Температура регенерации может быть любой температурой, ниже которой адсорбент начинает перерождаться. Вообще температура адсорбента обычно поднимается в течение регенерации до величины в ряду от приблизительно 0 до приблизительно 300oC, предпочтительно поднимается до величины в ряду от приблизительно 25 до приблизительно 250oC и более предпочтительно поднимается до величины в ряду от приблизительно 70 до приблизительно 180oC. Процесс регенерации может быть комбинацией PSA и TSA и в этом случае и давление, и температура, используемые при регенерации, будут изменяться в пределах вышеуказанных величин.
Изобретение далее иллюстрируется следующими примерами, где части, проценты и соотношения, если не указывается особо, являются объемными.
Пример 1. Получение трехвалентный ион, литий LSX и X
Цеолит с низким содержанием кремния X (LSX) синтезируют с атомным соотношением Si/Al 1.0 согласно методикам, описанным C.H.Kuhe в пат. Великобритании 1580928. Натрий LSX цеолит затем готовят с помощью ионного обмена синтетического натрий, калий LSX цеолита при использовании четырехстатического обмена с 20 мл 1.0 N раствора NaCl на 1 г цеолита при 80oC. После каждого обмена пробы промывают водным NaOH (0.01 N). Получающийся натрий LSX делают в лабораторных пеллетах с помощью прессования в пресс-форме (без связывающего агента) с последующим измельчением и просеиванием до размера 20-40 меш. 13X PS 02 HP коммерческий цеолит X (с приблизительным соотношением Si/Al цеолита 1.25), предлагаемый UOP Inс в качестве шариков размером 8 х 10 меш., используется в качестве основного цеолита для дальнейшего ряда материалов трехвалентный ион, литий X этого изобретения.
Литиевые формы X или LSX делают с помощью прокачивания четырехкратного избытка 0.09 N раствора LiCl (с регулируемым значением pH 9 с LiOH) только через основные пеллеты натриевой ионной формы в течение 72 часов при 80oC. В случае коммерческих X пеллет 2 дополнительных обмена с четырехкратными избытками LiCe требуются для достижения требуемого уровня обмена > 97% основных натриевых ионов. Результирующие литий ионообменные пробы отфильтровывают, но промывают не водой для ограничения обмена гидроксоний иона. Церий или лантан, литий LSX образцы получают контактированием вышеназванного образца LiLSX с 0.1 N водными растворами соответствующих хлоридов лантанидов (с pH величиной в ряду 5.5-6.5), содержащими стехиометрические количества трехвалентного иона, необходимых для достижения требуемого уровня обмена трехвалентного иона. Для обменов трехвалентного иона вытекающий из колонки поток непрерывно рециркулируется обратно к сосуду, содержащему обменный раствор и обмен выполняют при комнатной температуре за 24-30 часов. Методика для получения церий или лантан, литий X идентична за исключением того, что требуется более длительное время контактирования (45-72 часа). Алюминий, литий X и LSX образцы получают при использовании таких же методик за исключением того, что используют 0,04 N водный сульфат алюминия (с величиной pH в ряду 3.9-5) и обмен проводят при 70oC за период 20-24 часа.
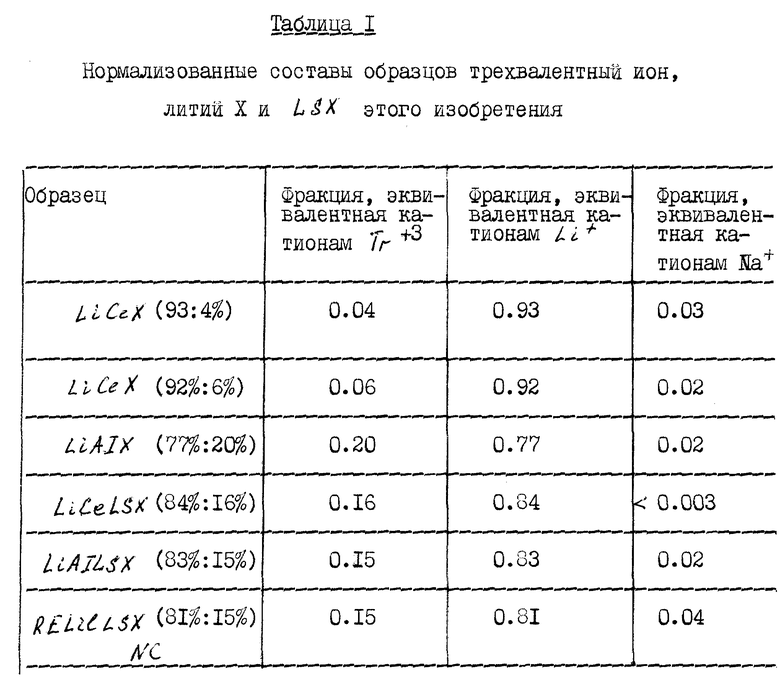
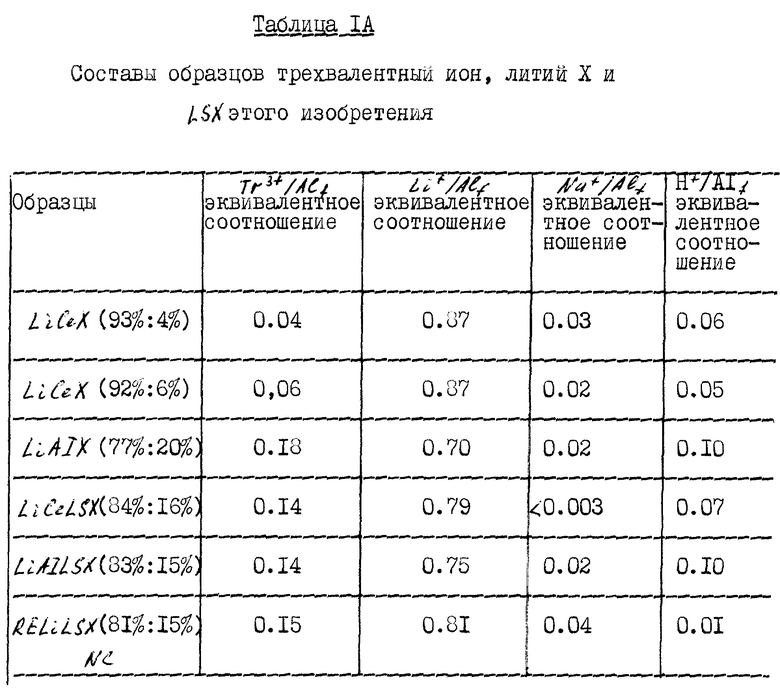
Составы образцов трехвалентный ион, литий и LSX, полученные согласно методикам этого примера, приведены в таблице 1, где измеряемые эквиваленты катионов, обмениевых ионов, приводятся к единообразию. Таблица 1A показывает некоторые данные, но выраженные в показателях соотношений эквивалентов измеряемых ионообмениевых катионов в рамках содержания алюминия.
Образцы анализируют с помощью плазменной атомной эмиссионной спектроскопии (ICP-AES) при использовании API-3510 последовательного ICP спектрометра.
В случае пробы, обозначенной ReLiLSX (81%:15%) NC, NaLSX вначале обменивают с коммерческим смешанным разведенным раствором хлоридов от Moly Corp. ,Inc. (с составом приблизительно 67% LaCl3, 23% NdCl3, 9% PrCl3, 1% CeCl3) и затем обменивают литий до конечного продукта без промежуточной стадии кальцинирования.
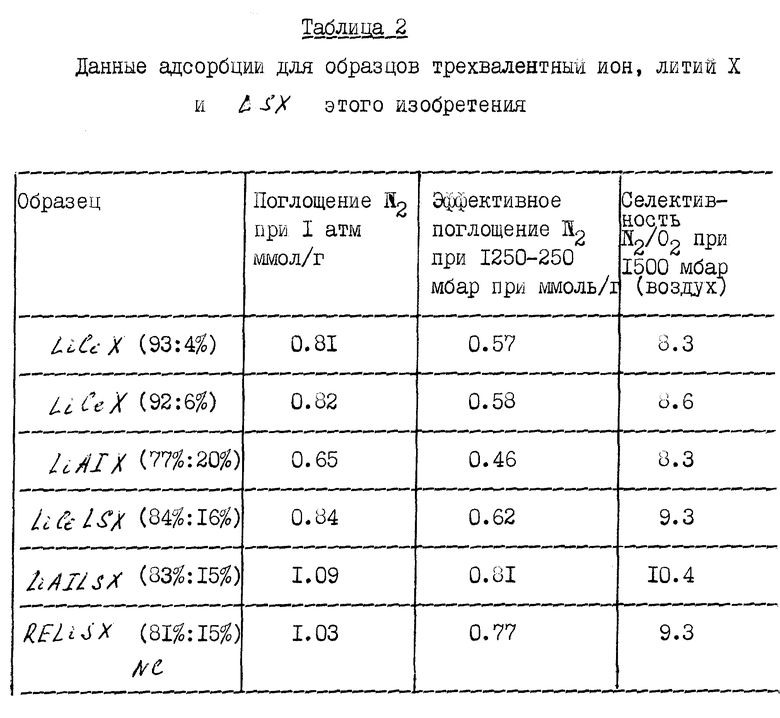
Пример 2. Изотермы адсорбции азота (N2) и кислорода (O2) на образцах трехвалентный ион, литий LSX и X измеряют гравиметрически при использовании микробаланса серии Cahu 2000, заключенного в системе вакуум/давление из нержавеющей стали. Измерения давления в ряду 1 - 10000 мбар проводят при использовании MKS Baratron. Приблизительно 100 мг пробы осторожно удалялись и их температура увеличивалась до 450oC со скоростью 1- 2oC. Изотермы адсорбции для азота и кислорода измеряют при 25oC в ряду давлений 20-6600 мбар для азота и 20-2000 мбар для кислорода и данные соответствуют отдельному или множественному участку изотермической модели Langmuir. Приспосабливание к данным азота используется для расчета способности проб адсорбировать азот при 1 атмосфере и их эффективной способности для азота при 25oC. Эффективная способность для азота, определенная как разница между способностью для азота при 1250 мбар и способностью для азота при 250 мбар, дает хороший показатель способности адсорбента в PSA процессе, работающем между верхними и нижними значениями давлений в этом ряду. Селективности образцов для азота над кислородом в воздухе при 1500 мбар и 25oC получают из изотерм чистого газа для азота и кислорода при использовании смешанных правил Langmuir (ссылка например, A. I. Myers: AIChE: 29(4), (1983, p. 691-693). Используется обычное определение селективности, где селективность (S) дается с помощью уравнения
S = (XN2/YN2) / (XO2/YO2),
где XN2 и XO2 являются молярными фракциями азота и кислорода, соответственно, в адсорбированной фазе и YN2 и YO2 являются молярными фракциями азота и кислорода, соответственно, в газовой фазе.
Результаты адсорбции для образцов трехвалентный ион, литий X и LSX примера 1 приведены в таблице 2.
Пример 3. Термическая стабильность трехвалентного иона, лития LSX и X.
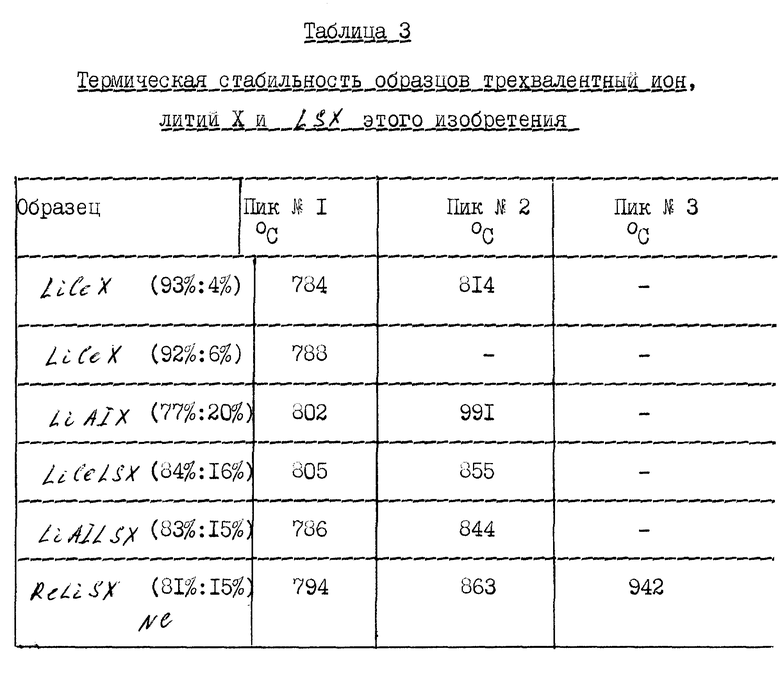
Дифференциальный термический анализ (ДТА) выполняют на образцах трехвалентный ион, литий X и LSX в воздухе при использовании дифференциального термического анализатора Shimadzu ДТА-50. Используют скорость нагревания 20oC/минуту от комнатной температуры до 1200oC, скорость газа для продувки 100 мл/мин и вес пробы в ряду от 2 до 3.1 мг.
Результаты для образцов трехвалентный ион, литий X и примера 1 приведены в таблице 3.
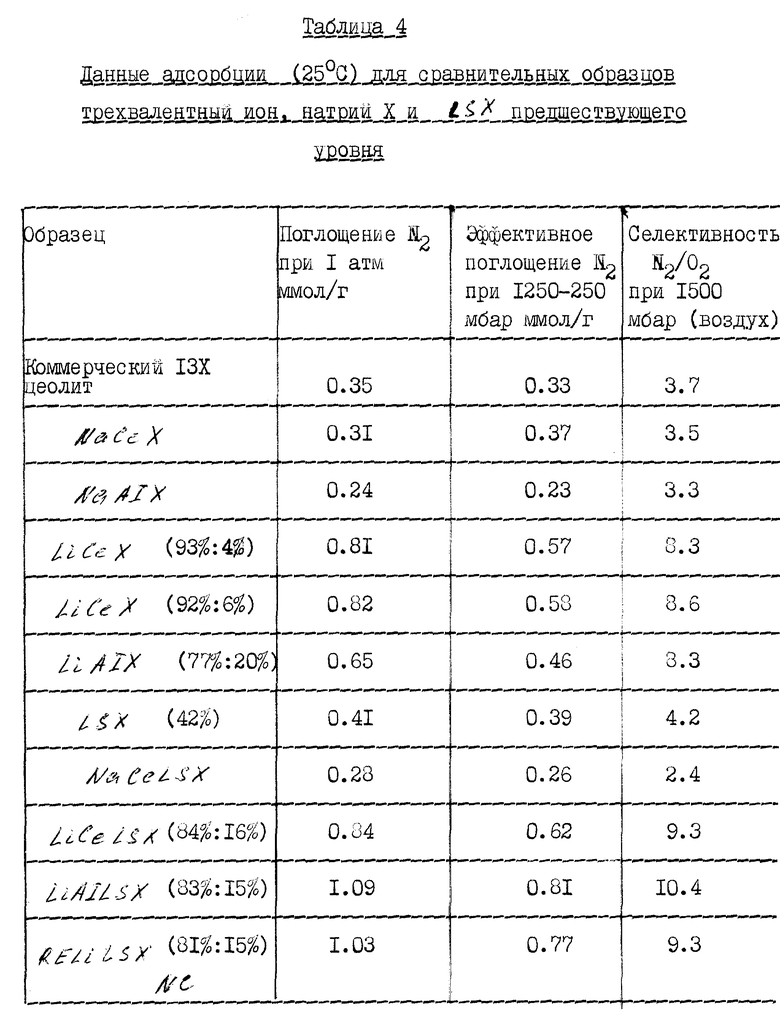
Пример 4. Изотермы сравнительных трехвалентный ион, натрий X и LSX
Сравнительные образцы церий или алюминий, натрий LSX получают по следующей методике, приведенной в примере 1, за исключеньем того, что в таких случаях основные формы X и LSX не обменивают литий до обмена с идентичными количествами трехвалентных ионов.
Данные адсорбции для этих образцов приведены в таблице 4.
Образцы трехвалентный ион, литий X или LSX этого изобретения (ряды 4-6 и 9-11 соответственно таблицы 4) имеют значительно большую "эффективную" адсорбционную способность по азоту и селективности азот/кислород, чем образцы трехвалентный ион, натрий предшествующего уровня с эквивалентным уровнем трехвалентного иона.
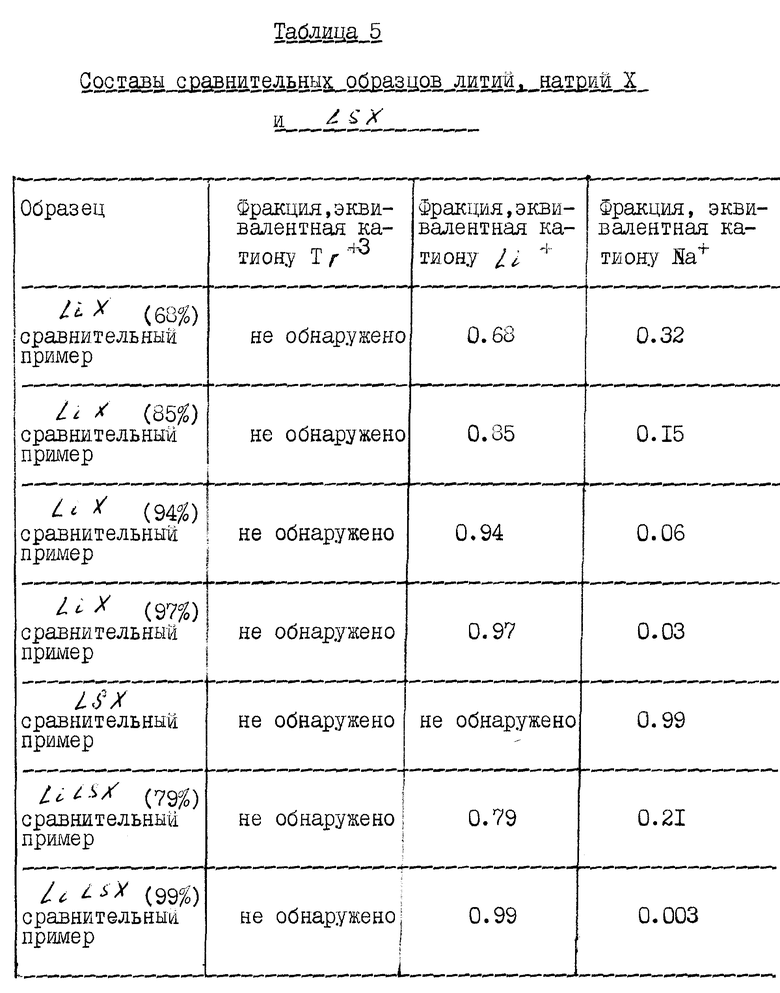
Пример 5. Изотермы и термические стабильности сравнительных литий, натрий X и LSX.
LiLSX и LiX получают при использовании ионообменных методик, описанных детально в примере 1, но в которых исключается конечная стадия ионного обмена трехвалентного иона. Образцы с уменьшенными уровнями обмена лития получают снижением количества LiCе, пропускаемого через основной NALSX или коммерческий 13X цеолит.
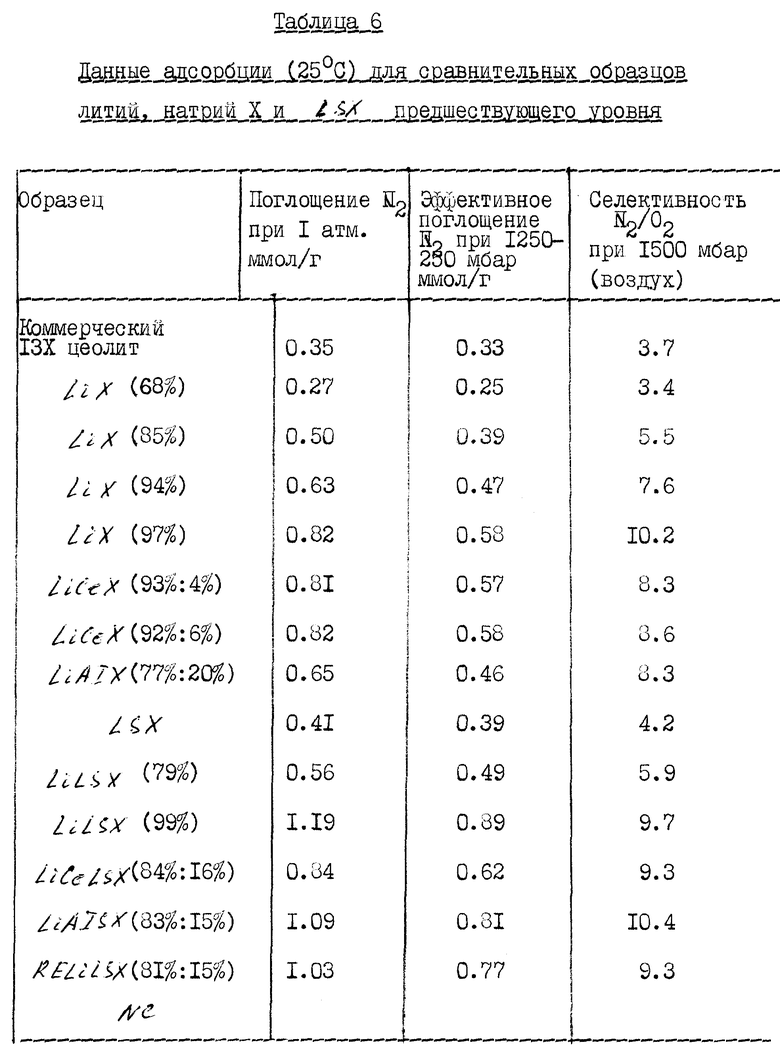
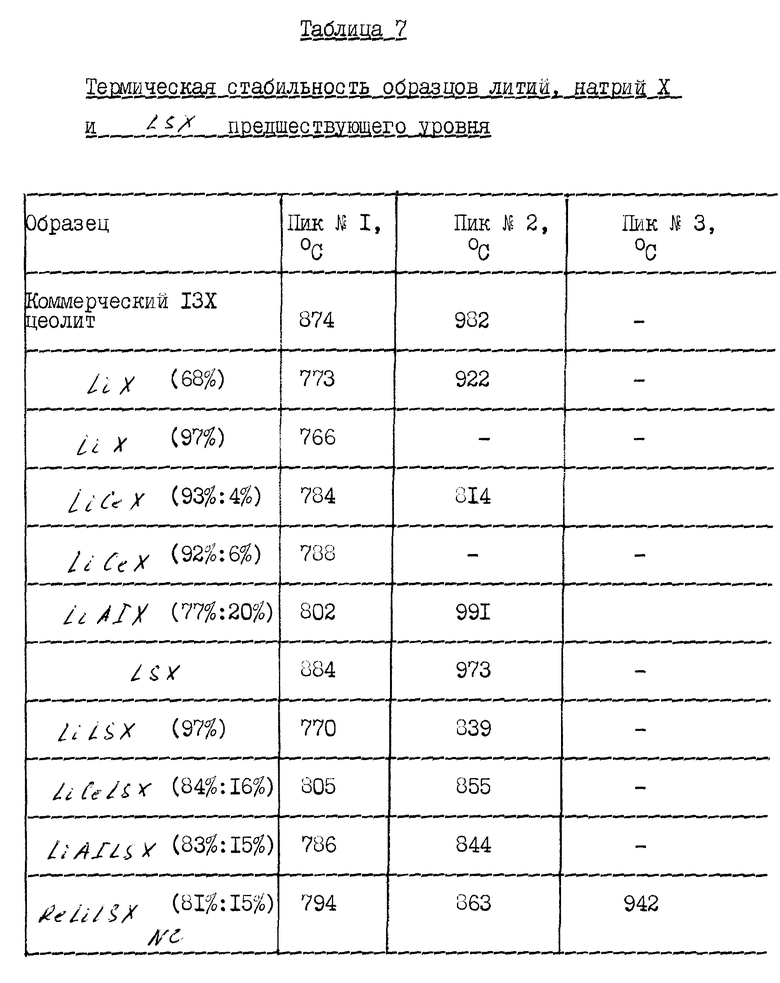
Составы сравнительных образцов литий, натрий X и LSX приведены в таблице 5. Данные адсорбции этих образцов приведены в таблице 6 и данные по термической стабильности приведены в таблице 7.
Сорбционная способность по азоту образцов X и LSX этого изобретения (ряды 6-8 и 12-14 соответственно таблицы 6) превышает сорбционную способность адсорбентов предшествующего уровня с эквивалентным содержанием лития и приближаются к сорбционной способности лучшего примера предшествующего уровня LiLSX (строчка 11 таблицы 6). Факторы разделения образцов этого изобретения значительно выше, чем факторы разделения для образцов предшествующего уровня с эквивалентным содержанием катионов лития и они так же высоки, как и для лучшего адсорбента предшествующего уровня LiLSX (строчка 11 таблица 6).
Термическая стабильность X- и LSX-адсорбентов этого изобретения (строчки 4-6 и 9-11 соответственно таблицы 7) улучшается в сравнении с термической стабильностью образцов Na, Li предшествующего уровня с равными уровнями Li. Значительные преимущества увеличиваются из-за обмена трехвалентного иона при > 5% в виде значительного улучшения термической стабильности без потери адсорбционной способности.
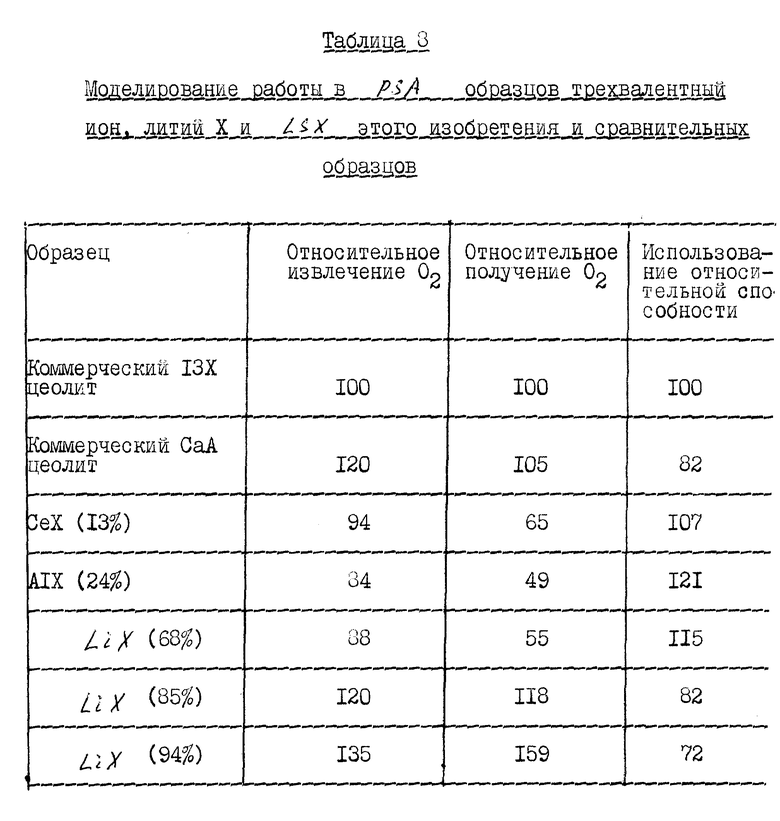
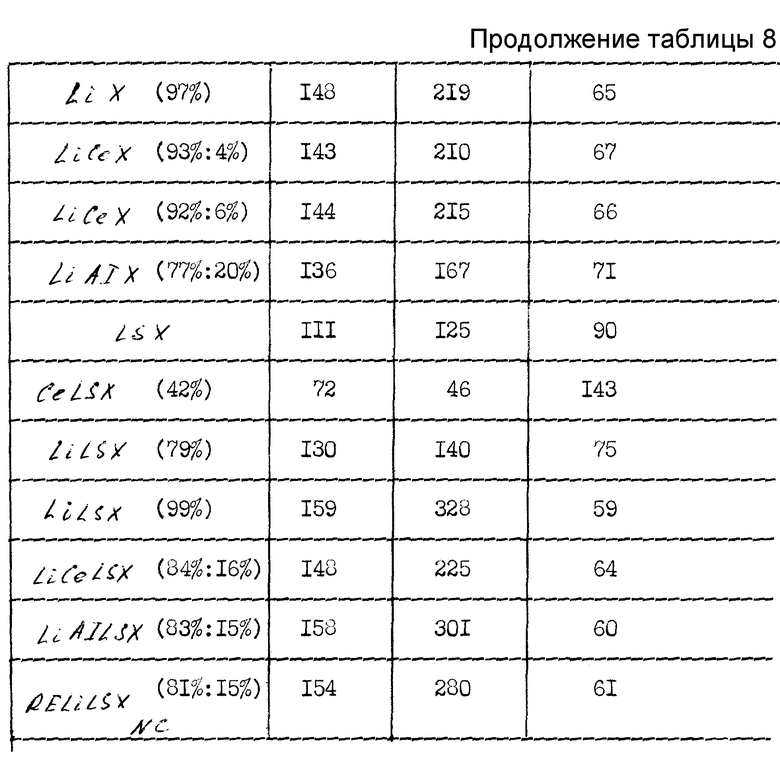
Пример 6. Моделированный процесс PSA трехвалентный ион, литий X и LSX
Методика модели PSA в этом примере составляется строго для равновесных характеристик адсорбента и массового баланса компонентов газа при изотермических условиях. Рассчитывают подаваемый состав и скорость потока, состав продукт/продувка, скорости потока продукта и продувки, состав и скорость потока продукта низкого давления. Это позволяет прямо рассчитать извлечение и получение O2 для времени цикла данного процесса и рассчитать специфическую мощность при использовании эффективностей независимой машины.
Эти модельные методики надежно используются для относительной работы в PSA разработанных адсорбентов в сравнении с предшествующими адсорбентами (чья работа хорошо охарактеризована) в данном процессе или для исследования тенденций в работе адсорбентов как функции изменений в переменных величинах процесса.
Результаты в таблице 8 показывают примеры моделирования PSA процесса, работающего при абсолютном давлении между 1.25 атмосфер и 0.25 атмосфер, при этом воздух подается к адсорбенту при 25oC и в качестве продувки частично используется продукт, обогащенный кислородом и содержащий 2% остаточного азота. Хорошая работа в PSA адсорбентов изобретения ясно показана в этих моделях.
Вышеприведенные примеры показывают, что адсорбенты изобретения обладают значительно лучшей адсорбционной способностью по азоту в сравнении с литий X и литий LSX при эквивалентном содержании катионов лития. Дополнительно примеры показывают, что адсорбенты изобретения имеют более высокие факторы разделения для смеси азот-кислород в сравнении с литий X и литий LSX при эквивалентном содержании катионов лития. Эти факторы разделения являются такими же высокими, как и факторы разделения для LiLSX адсорбента с самым высоким возможным содержанием катионов лития, т.е. приблизительно 97%. Примеры также показывают, что адсорбенты изобретения проявляют улучшенную термическую стабильность в сравнении с соответствующими свободными трехвалентными металлами, литий обмениевыми образцами.
Хотя изобретение описывается с частичной ссылкой на специфические эксперименты, эти эксперименты рассматриваются только образцами изобретения и отклонений. Например, адсорбционный процесс может включать различные стадии адсорбции. Аналогично адсорбентам изобретения могут включаться другие комбинации компонентов, чем те, что проиллюстрированы в примерах и адсорбенты могут быть приготовлены другими способами, такими как ионнообмен в твердом состоянии. Кроме того, адсорбенты изобретения могут использоваться для отделения азота от различных других газов, таких как метан и четырехфтористый углерод. Область изобретения ограничивается только широтой прилагаемой формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ МОЛЕКУЛЯРНЫХ СИТ | 1997 |
|
RU2217233C2 |
| СПОСОБ ИЗВЛЕЧЕНИЯ АЛКЕНА | 1994 |
|
RU2100336C1 |
| СПОСОБ ВЫДЕЛЕНИЯ ГАЗООБРАЗНОГО АЛКЕНА ИЗ ГАЗООБРАЗНОЙ СМЕСИ | 1993 |
|
RU2107059C1 |
| Способ получения серебросодержащего цеолита LSX для разделения компонентов воздуха | 2022 |
|
RU2799829C1 |
| АГЛОМЕРИРОВАННЫЕ ЦЕОЛИТНЫЕ АДСОРБЕНТЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЯ | 2008 |
|
RU2453364C2 |
| АГЛОМЕРИРОВАННЫЕ ЦЕОЛИТОВЫЕ АДСОРБЕНТЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЯ | 2008 |
|
RU2451543C2 |
| ЦЕОЛИТЫ RHO И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2019 |
|
RU2739307C1 |
| КОМПОЗИЦИИ АЛЮМОСИЛИКАТНЫХ ЦЕОЛИТОВ ТИПА Х С НИЗКИМ СОДЕРЖАНИЕМ ЦЕОЛИТА ТИПА LTA | 2012 |
|
RU2554642C2 |
| СПОСОБ ПОЛУЧЕНИЯ АДСОРБЕНТА - МОЛЕКУЛЯРНОГО СИТА ДЛЯ СЕЛЕКТИВНОЙ АДСОРБЦИИ АЗОТА И АРГОНА | 2003 |
|
RU2297276C2 |
| ВКЛЮЧАЮЩИЕ ПРЕВРАЩЕННОЕ СВЯЗУЮЩЕЕ АЛЮМОСИЛИКАТНЫЕ ЦЕОЛИТНЫЕ КОМПОЗИЦИИ ТИПА Х С НИЗКИМ СОДЕРЖАНИЕМ ЦЕОЛИТА ТИПА LTA | 2012 |
|
RU2544673C1 |
Цеолиты типа X, катионы которого компенсирующие заряд, содержат от приблизительно 95 до 50% ионов лития, от 4 до 50% одного или более алюминия, церия, лантана и смеси лантаноидов и от 0 до 15% других ионов. Цеолиты предпочтительно адсорбируют азот из смесей газов. Предложены варианты двухстадийного способа ионообменного получения цеолита. Способ позволяет эффективно выделять азот на цеолитах с повышенной термостабильностью. 5 с. и 18 з.п. ф-лы, 9 табл.
Приоритет по пунктам и признакам:
14.02.94 по пп. 1, 3-7 и 8 с признаками используемого цеолита, охарактеризованного в пп.1, 3-23, согласно
08.08.94 по п. 2.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| US 5174979 A, 1992 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| US 4859217 A, 1989 | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| US 5152813 A, 1992 | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Способ прессования профилей переменного сечения по длине | 1961 |
|
SU149018A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Видеоголовка | 1977 |
|
SU591919A1 |
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Способ модифицирования цеолитов | 1978 |
|
SU889610A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| SU 1155564 A, 1985. | |||
Авторы
Даты
1999-03-10—Публикация
1995-02-13—Подача