Настоящее изобретение относится к новым производным индана, фармацевтическим композициям, содержащим такие соединения, и к применению их в качестве антагонистов эндотелинового рецептора.
Эндотелин (ET) является весьма мощным сосудосуживающим пептидом, синтезируемым и выделяемым эндотелием сосудов. Эндотелин существует в трех изоформах - ET-1, ET-2 и ET-3. Если нет других указаний, "эндотелин" будет означать любую изо всех изоформ эндотелина. Эндотелин оказывает глубокое воздействие на сердечно-сосудистую систему и, в частности, на венозное, почечное и мозговое кровообращание. Повышенное или ненормальное выделение эндотелина находится в связи с сокращением гладкой мышцы, которое включено в патогенез сердечно-сосудистой, дыхательной, почечной патофизиологии, и патофизиологии сосудов мозга. Описано повышенное содержание эндотелина в плазме крови у пациентов с сильной гипертонией, острым инфарктом миокарда, с субарахноидальным кровоизлиянием, атеросклерозом и у пациентов с уремией, подвергающихся диализу.
In vivo эндотелин имеет выраженное действие на кровяное давление и минутный сердечный выброс. Внутривенная инъекция крысам ударной дозы ET (0,1-3 нмоль/кг) вызывает временную, зависящую от дозы реакцию депрессора (длящуюся 0,5-2 минуты) с последующим длительным, зависящим от дозы повышением артериального кровяного давления, которое может оставаться повышенным в течение 2-3 часов после введения дозы. Дозы свыше 3 нмоль/кг часто оказываются смертельными для крыс.
Оказывается, что эндотелин предпочтительно воздействует на почечное сосудистое ложе. Он производит заметное, длительное длящееся уменьшение почечного кровотока, сопровождаемое значительным снижением GFR, объема мочи, натрия в моче и экскреции калия. Эндотелин вызывает длительный антинатриуретический эффект, несмотря на значительное увеличение предсердного натриуретического пептида. Эндотелин также стимулирует активность ренина плазмы. Эти данные предполагают, что ET участвует в регуляции функции почек и задействован при различных заболеваниях почек, включая почечную недостаточность, циклоспориновую нефротоксичность, индуцированную рентгеном (radio contrast) почечную недостаточность и хроническую почечную недостаточность.
Исследования показали, что in vivo церебральная сосудистая сеть весьма чувствительна как к сосудорасширяющему, так и к сосудосуживающему действию эндотелина. Следовательно, ET может быть важным посредником церебрального вазоспазма - часто встречающегося и часто фатального последствия субарахноидального кровотечения.
ET также проявляет непосредственное действие на центральную нервную систему, такое как тяжелое апноэ (остановка дыхания) и ишемические болезни, что наводит на мысль, что ET может способствовать развитию церебральных инфарктов и гибели нервных клеток.
ET также задействован при ишемии миокарда (Nichols et al. Br. J. Pharm, 99: 597-601, 1989, и Clozel and Clozel. Circ. Res., 65: 1193-1200, 1989), спазме коронарной артерии (Fukuda et al., Fur. J. Pharm. 165: 301-304, 1989, и Luscher, Circ. , 83: 701, 1991), сердечной недостаточности, пролиферации клеток гладкой мышцы сосуда (Takagi, Biochem. and Biophys. Aes. Commun., 168: 537-543, 1990, Bobek et al., Am. J. Physiol., 258: 408-415, 1990) и атеросклерозе (Nakaki et al., Biochem. and Biophys. Res. Commun., 158: 880-881, 1989, и Lerman et al., New Eng. J. of med. 325: 997-1001, 1991). Повышенный уровень эндотелина обнаруживается после коронарной баллонной ангиопластики (Kadee et al., No 2491, Cire. 82: 627, 1990).
Также обнаружено, что эндотелин является сильным констриктором изолированной ткани дыхательных путей млекопитающих, в том числе бронхов человека (Uchida et al. , Eur. J. of Pharm. 154: 227-228, 1988, Lagente, Clin. Exp. Allergy 20: 343-348, 1990; и Springall et al, Lancet, 338: 697-701, 1991). Эндотелин может играть роль в патогенезе интерстициального фиброза легких и ассоциированной легочной гипертонии (Glard et al. Third International Conference on Endothelin, 1993, p. 34 и ARDS/Adult Respiratory Distres Syndrome/, Sanai et al., цит. выше. p. 112).
Эндотелин находится в связи с вызыванием геморрагического и некротического повреждения в слизистой желудка (Whittle et al., Br. J. Pharm. 95: 1011-1013, 1988); с феноменом Рейно (Raynaud/. (Cinniniello et al., Lancet 337: 114-115, 1991); с болезнью Крона и неспецифическим язвенным колитом (Munch et al, Lancet, Vol, 339, p. 381; мигренью (Edmeads, Headache, Feb. 1991, p. 127); c заражением крови (Weitzberg et al., Cirс,. Shock 33: 222-227, 1991; Pittel et al, Ann. Surg. 213: 262-264, 1991), с вызываемой циклоспорином почечной недостаточностью или гипертензией (Eur. J. Pharmacol., 180: 191-192, 1990, Kidney Int., 37: 1487-1491, 1990) и эндотоксиновым бактериально-токсическим шоком, и с другими вызываемыми эндотоксином заболеваниями (Biochem. Biophys. Res. Commun., 161: 1220-1227, 1989, Acta Physiol Scand. 137: 317-318, 1989) и воспалительными заболеваниями кожи (Clin. Res. 41: 451 и 484, 1993).
Эндотоксин также вовлечен в преэклампсию беременности (Clark et al., Am. J. Obstet. Gynecol. , March 1992, p. 962-968; Kamor et al., N. Eng. J. of Med. , Nov 22, 1990, p. 1486-1487; Dekker et al, Eur. J. Ob. and Gyn. and Rep. Bio. , 40 (1991) 215-220; Schiff et al., Am. J. Ostet. Gynecol. Feb. 1992, p. 624-628; сахарный диабет (Takahashi et al., Diabetologia (1990) 33: 306-310); и в резкое сосудистое отторжение после пересадки почек (Watschinger et al., Transplantation Vol. 52, N 4. pp. 743-746).
Эндотелин стимулирует как резорбцию кости, так и анаболизм и может играть роль в связывании при исправлении кости (Tatrai et al., Endocrinology, Vol. 131, p. 603-607).
Сообщается, что эндотелин стимулирует перенос спермы в полость матки (Casey et al. , J. Clin. Endo and metabolism., Vol. 74, N 1, p. 223-225), следовательно, антагонисты эндотелина могут быть полезны в качестве мужских противозачаточных средств. Эндотелин модулирует яичниковый и менструальный цикл (Kenegsberg. J. of Clin. Endo. and met., Vol. 74, N 1, p. 12) и может также играть некоторую роль в регулировании тонуса сосудов мужского полового члена (Lau et al., Asia Pacific, J. of Pharm., 1991, 6: 287-292, и Tejada et al. , J. Amer. Physio. Soc. 1991, H1078-H1085). Эндотелин также является посредником при сильном сокращении простатической гладкой мышцы человека (Langenstroer et al., J. Urology, Vol. 149, p. 495-499).
Таким образом, антагонисты эндотелинового рецептора могли бы являться уникальным подходом к фармакотерапии гипертонии, почечной недостаточности, вызванной ишемией почечной недостаточности, вызываемой эндотоксинным сепсисом почечной недостаточности, к профилактике и/или лечению вызываемой рентгеном почечной недостаточности, острой и хронической, вызываемой циклоспорином почечной недостаточности, цереброваскулярных заболеваний, миокардической ишемии, стенокардии, сердечной недостаточности, астмы, атеросклероза, феномена (Raynaud) Рейно, язв, сепсиса, мигрени, глаукомы, эндотоксинового бактериально-токсического шока, вызываемой эндотоксином недостаточности многих органов или распространенной внутрисосудистой коагуляции, индуцируемой циклоспорином почечной недостаточности, и будут представлять интерес в качестве дополнительного средства при ангиопластике для предотвращения рестеноза, при диабете, преэклампсии беременности, исправлении костей, пересадке почек, в мужских противозачаточных средствах, при бесплодии и приапризме, и доброкачественной гипертрофии предстательной железы.
Сущность изобретения.
Настоящее изобретение относится к производным индана общей формулы (1), к способу их получения, фармацевтической композиции на их основе, а также к способу антагонизирования эндотелиновых рецепторов, который может использоваться для лечения различных сердечно-сосудистых и почечных заболеваний, включающих, например, гипертонию, острую и хроническую недостаточность, цереброваскулярный вазоспазм, миокардическую ишемию, стенокардию, сердечную недостаточность, атеросклероз, а также в качестве вспомогательного средства при пластических операциях на сосудах для предотвращения рестеноза.
Подробное описание изобретения
Настоящее изобретение относится к производным индана общей формулы (I):
где R1 представляет собой -X(CH2)nAr, -X(CH2)nR8 или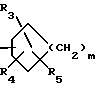
R2 представляет водород:
P1 представляет -X(CH2)nR8;
P2 представляет -X(CH2)nR8;
R3 и R5 представляет, независимо, водород, R11, OH, C1-8-алкокси, галоген или -X(CH2)nR8, где каждая метиленовая группа в -X(CH2)nR8 может быть незамещенной или замещена одной или двумя группами -(CH2)nAr;
R4 представляет водород, -XR11, C1-5-алкокси, который может быть замещен OH;
R6 представляет водород или C1-4-алкил;
R7 представляет водород, C1-10-алкил, -(CH2)nAr или C2-10-алкенил;
R8 представляет R11, CO2R7, OR6, P(O)(OR7)R7, CO2C(R11)2O(CO)XR7, CONR7SO2R11 или -CO2(CH2)mC(O)N(R6)2;
R9 представляет (CH2)n;
R10 представляет R3 или R4;
R11 представляет водород, C1-8-алкил, C2-8-алкенил или Ar, все из которых могут быть незамещенными или замещены одним или несколькими OH или галогенами;
X представляет (CH2)n или O;
Y представляет СН3
Аr представляет
или пиридил, все из которых могут быть незамещенными или замещены одной или несколькими группами R3 или R4;
A представляет [C(R6)2]m;
B представляет -O-;
Z1 и Z2 представляют, независимо, водород или C1-5-алкокси, который может быть замещен OH;
Z3 представляет Z1 или -X-R9-Y;
n равно целому числу от 0 до 6;
m равно 1, 2 или 3; при условии, что когда R3, R5 представляет X(CH2)nR8 и n не равно 0;
X представляет кислород, когда R8 представляет собой OR6 или CO2H;
и соединение формулы (I) не является
(цис, цис) -(1RS, 3RS)-1,3-дифенилиндан-2-карбоновой кислотой;
1,3-дифенил-2-метилинданом;
1,3-дифенилинданом;
1,3-бис(4,5-диметокси-2-гидроксифенил)-5,6-диметоксиинданом, 1,3-бис(3,4-диметоксифенил)-5,6-диметоксиинданом;
и также при условии, что исключаются соединения, где R1 представляет -X(CH2)nAr или -X(CH2)nR8 или
R2 представляет водород;
P1 представляет -X(CH2)nR8;
P2 представляет -X(CH2)nR8;
R3 и R5 представляет, независимо, водород, R11, OH, C1-8-алкокси или -X(CH2)nR8, где метиленовые группы в -X(CH2)nR8 могут быть незамещенными или замещены одной или несколькими группами -(CH2)nAr;
R4 представляет водород, -X(R11), C1-5-алкокси, который может быть замещен OH;
R6 представляет водород или C1-4-алкил;
R7 представляет водород, C1-6-алкил или (CH2)nAr;
R8 представляет R11, CO2H или P(O)(OH)R7;
R10 представляет R3 или R4;
R11 представляет C1-8-алкил, C2-8-алкенил, C2-8-алкинил, все из которых могут быть незамещенными или замещены одним или несколькими OH или галогеном;
X представляет (CH2)n или O;
Y представляет CH3;
Ar представляет
или пиридил, которые могут быть незамещенными или замещенными одной или несколькими группами R3 или R4;
A представляет [C(R6)2]m;
B представляет -O-;
Z1 и Z2 представляет, независимо, водород или C1-8-алкокси;
Z3 представляет Z1 или X-R9-Y;
n равно целому числу от 0 до 6;
m равно 1, 2 или 3;
или их фармацевтически приемлемым солям.
Предпочтительными являются соединения, где R1 представляет собой X(CH2)nAr, дигидробензофуранил, бензодиоксанил, циклогексил или C1-4-алкил; R2 представляет водород; R3 и R5 представляют, независимо, водород, OH, C1-5-алкокси, галоген, OC1-4-алкилфенил, C1-4-алкил, X(CH2)nR8 или фенил; R4 представляет водород или C1-4-алкил; Z1 и Z2 представляет, независимо, водород или C1-5-алкокси; Z3 представляет Z1, или -X-R9-Y; P1 и P2 представляет, независимо, водород или CO2H; Ar представляет радикал формулы (a) или (b), фенил или пиридил, и X представляет (CH2)n или кислород.
Из них предпочтительными являются соединения, где R3 представляет водород или -X-(CH2)nR8; R4 и R5 представляют, независимо, водород, OH, C1-5-алкокси, замещенный фенил, F, Br или C1-3-алкил Z1 и Z3 представляют водород, и Z2 представляет водород или C1-5-алкокси.
Особенно предпочтительно производное 3-(2-R-4-метоксифенил)-1-(3,4-метилендиоксфенил)-5-(проп-1-илокси)индан-2- карбоновой кислоты общей формулы
где R3' обозначает -OCH2COOH, M обозначает H и соединение является (+)(1RS, 2RS, 3SR) изомером; R3' обозначает -OCH2CH2OH, M обозначает H и соединение является (+)(1RS, 2RS, 3SR) изомером;
R3' обозначает
M обозначает Na, и соединение является (1RS, 2RS, 3SR) изомером
или его фармацевтически приемлемая соль, которое может быть как изомером в виде (+) (1RS, 2RS, 3SR)-3-(2-карбометокси-4-метоксифенил)-1-(3,4-метилендиоксифенил)-5- (проп-1-илокси)индан-2-карбоновой кислоты, так и в виде (+) (1RS, 2RS, 3SR)-3-[2-(2-гидроксиэт-1-илокси)-4-метоксифенил] -1-(3,4- метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоновой кислоты, а также может быть в виде динатриевой соли (1RS, 2RS, 3SR)-3-[2-[(4-карбоксипиридин-3-ил)окси] -4-метоксифенил] -1-(3,4- метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоновой кислоты.
Настоящее изобретение относится также к фармацевтической композиции, обладающей свойством антагониста эндотелиновых рецепторов, которая содержит соединение формулы (I) в эффективном количестве и фармацевтически приемлемый носитель.
Предпочтительна такая фармацевтическая композиция, где соединением является производное 3-(2-R-4-метоксифенил)-1-(3,4-метилендиоксифенил)-5-(проп-1-илокси)индан-2- карбоновой кислоты, указанное выше.
Предложен также способ антагонизирования эндотелиновых рецепторов, который включает введение субъекту, нуждающемуся в этом, эффективного для антагонизации эндотелиновых рецепторов количества соединения общей формулы (I). Особенно предпочтительно введение производного 3-(2-R-4-метоксифенил)-1-(3,4-метилендиоксифенил)-5-(проп-1-илокси)индан- 2-карбоновой кислоты, указанном выше.
Способ антагонизирования эндотелиновых рецепторов может использоваться при лечении гипертонии, почечной недостаточности или цереброваскулярного заболевания и в этом случае введение производного 3-(-R-4-метоксифенил)-1-(3,4-метилендиоксифенил-5-(проп-1-илокси)индан-2- карбоновой кислоты предпочтительно.
Предложен также способ получения соединения формулы (I)
или его фармацевтически приемлемой соли, заключающийся во взаимодействии соединения формулы (II)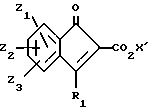
где Z1, Z2, Z3 и R1 являются такими, как описано выше, или способом к превращению в них группами, и X1 представляет алкил, с магнийорганическим соединением формулы (III)
R2-(CH2)n-MgBr
где R2 является таким, как описано выше, или группой, способной к превращению в него, в подходящем растворителе с образованием соединения формулы (IV)
которое восстанавливает и затем, если желательно или необходимо, подвергают
a) введению R10 (иного, чем водород) через присоединение по двойной связи; и/или
b) алкилированию или ацилированию с образованием соединений, в которых P1 и P2 иные, чем CO2H; и/или
с) преобразованию R1, R2, Z1, Z2 и Z3 обычными способами, такими как алкилирование, ацилирование, восстановление,
с получением соединения формулы (I).
Соответственно, производное 3-(2-R-4-метоксифенил)-1-(3,4-метилендиоксифенил)-5-(проп-1-илокси)индан- 2-карбоновой кислоты получают
взаимодействием соединения формулы (II)
где X1 представляет алкил, с магнийорганическим соединением формулы (III)
где R3' является таким, как описано выше, или группой, способной к превращению в него, в подходящем растворителе с образованием соединения формулы (IV)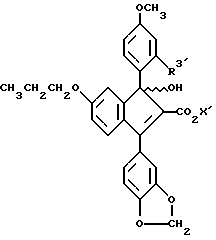
которое восстанавливают и затем гидролизуют.
Чтобы использовать соединение формулы (I) или его фармацевтически приемлемую соль для лечения людей и других млекопитающих, их обычно включают в состав препаратов в соответствии со стандартной фармацевтической практикой в виде фармацевтической композиции.
Соединения формулы (I) и их фармацевтически приемлемые соли при лечении указанных заболеваний могут быть введены обычными способами, например перорально, парентерально, под язык, чрезкозжно, ректально, путем ингаляции или трансбуккальным способом.
Соединения формулы (I) и их фармацевтически приемлемые соли, которые являются активными при пероральном введении, могут входить в состав сиропов, таблеток, капсул и лепешек. Состав в виде сиропа обычно будет представлять собой суспензию или раствор соединения или его соли в жидком носителе, например в этаноле, арахисовом масле, оливковом масле, глицерине или воде, со вкусовыми или красящими средствами. Когда композиция представлена в форме таблетки, может быть использован любой фармацевтический носитель, который обычно применяют для приготовления твердых формулировок. Примеры таких носителей включают стеарат магния, белая глина (terra alba), тальк, желатин, агар, пектин, аравийскую камедь, стеариновую кислоту, крахмал, лактозу и сахарозу. Когда композиция представлена в форме капсулы, подходящим является любое обычное инкапсулирование, например использование вышеупомянутых носителей в твердой оболочке желатиновой капсулы. Когда композиция представлена в форме капсулы с мягкой желатиновой оболочкой, можно рассматривать любой фармацевтический носитель, который обычно применяют для приготовления дисперсий или суспензий, например водорастворимые смолы, целлюлозы, силикаты или масла, и помешать их в оболочку мягкой желатиновой капсулы.
Типичные парентеральные композиции состоят из раствора или суспензии соединения или соли в стерильном водном или неводном носителе, необязательно содержащем парентерально приемлемое масло, например полиэтиленгликоль, поливинилпирролидон, лецитин, арахисовое масло или сезамовое масло.
Типичные композиции для ингаляции представлены в форме раствора, суспензии или эмульсии, которые могут вводиться в виде сухого порошка или в виде аэрозоля, используя обычный пропеллент, такой как дихлордифторметан или трихлорфторметан.
Типичный состав для суппозитория содержит соединению формулы (I) или его фармацевтически приемлемую соль, которые являются активными при этом пути введения, со связующим и/или смазывающим средством, например полимерными гликолями, желатинами, маслом какао или другими низкоплавкими растительными восками или жирами, или их синтетическими аналогами.
Типичные чрезкожные составы включают обычный водный или неводный растворитель, например крем, мазь, лосьон или пасту, или представлены в форме лекарственного пластыря, наклейки или пленки.
Композиция предпочтительно представлена в единичной дозированной форме, например таблетки, капсулы, или отмеренной аэрозольной дозировке, так что пациент может сам ввести себе единичную дозу.
Каждая дозированная единица для перорального введения содержит обычно от 0,1 до 500 мг/кг, предпочтительно от 1 до 100 мг/кг, и каждая дозировочная единица для парентерального введения содержит обычно от 0,1 до 100 мг соединения формулы (I) или его фармацевтически приемлемой соли в расчете на свободную кислоту. Каждая дозировочная единица для интраназального введения содержит обычно 1-400 мг и предпочтительно 10-200 мг на человека. Состав для наружного применения обычно содержит от 0,01 до 1,0% соединения формулы (I).
Суточный режим дозировки для перорального приема обычно включает от 0,01 мг/кг до 40 мг/кг соединения формулы (I) или его фармацевтически приемлемой соли в расчете на свободную кислоту. Суточный режим дозировки для парентерального введения обычно включает от 0,001 мг/кг до 40 мг/кг соединения формулы (I) или его фармацевтически приемлемой соли в расчете на свободную кислоту. Суточный режим дозировки для интраназального введения и пероральной ингаляции обычно оставляет от 10 до 500 мг/человека. Активный ингредиент может вводиться от 1 до 6 раз в сутки, в количестве, достаточном для проявления нужной активности.
Когда соединения по изобретению вводят в соответствии с настоящим изобретением, не ожидается неприемлемых токсических эффектов.
Биологическая активность соединений формулы (I) деконстрируется с помощью следующих испытаний.
1. Испытания на связывание
A) Приготовление мембран
Мозжечок или корковое вещество почки крысы быстро рассекают и сразу же замораживают в жидком азоте или используют свежими. Ткани - 1-2 г мозжечка или 3-5 г коркового вещества почки - гомогенизируют в 15 мл буфера, содержащего 20 мМ Трис-HCl и 5 мМ ЭДТК, pH 7,5 при 4oC, используя гомогенизатор с приводом от двигателя. Гомогенизаты фильтруют через марлю и центрифугируют при 20000 об/мин в течение 10 минут при 4oC. Супернатант удаляют, центрифугируют при 40000 об/мин в течение 30 минут при 4oC. Получающийся в результате осадок снова суспендируют в небольшом объеме буфера, содержащего 50 мМ Трис, 10 мМ MgCl, pH 7,5; разливают в небольшие пробирки и замораживают в жидком азоте. Мембраны разбавляют, чтобы получить 1 и 5 мг белка в каждой пробирке для мозжечка и коркового вещества почки в испытаниях на связывание.
Свежевыделенные брыжеечную артерию крысы и коллатеральное сосудистое ложе промывают в охлажденном льдом физиологическом растворе (на льду) и удаляют лимфатические узлы вдоль главного сосуда. Затем ткань гомогенизируют, используя политрон, в буфере, содержащем 20 мМ Трис и 5 мМ ЭДТК, pH 7,5 при 4oC в объеме 15 мл для ~6 г ложа брыжеечной артерии. Гомогенат процеживают через марлю и центрифугируют при 2000 об/мин в течение 10 мин при 4oC. Супернатант удаляют и центрифугируют при 40000 об/мин в течение 30 мин при 4oC. Получающийся в результате осадок снова суспендируют, как описано выше, для мозжечка и коркового вещества почки. В экспериментах на связывание для каждой пробирки используют приблизительно 10 мг мембранного белка.
B) Протокол связывания [125I] ET-1
Связывание [125I] ET-1 с мембранами из мозжечка крыс (2,5 мг белка на аналитическую пробирку) или из коркового вещества почки (3-8 мг белка на аналитеческую пробирку) измеряют после 60-минутной инкубации при 30oC в 50 мМ Триc-HC, 10 мМ MgCl2, 0,05% бычьего сывороточного альбумина (БСА), pH 7,5 при общем объеме 100 мл. Мембранный белок добавляют в пробирки, содержащие либо буфер, либо указанную концентрацию соединений. [125I] ET-1 (2200 Ки/ммоль) разбавляют в том же буфере, содержащем БСА, до получения конечной концентрации 0,2-0,5 нМ ET-1. Общее и неспецифическое связывание измеряют в отсутствии и в присутствии 100 нМ немеченного ET-1. После инкубации реакцию останавливают 3,0 мл холодного буфера, содержащего 50 мМ трис и 10 мМ MgCl2, pH 7,5. Мембраны с присоединившейся радиоактивностью отделяют от свободного лиганда путем фильтрования через бумажный фильтр Whatman GP/C и промывания (5 раз) 3 мл холодного буфера, используя харвестер клеток Brandel. Бумажные фильтры обсчитывают в счетчике гамма-квантов с эффективностью 75%. IC50 для соединений настоящего изобретения находится в интервале от 0,1 нм до 50 нм.
II. Активность гладкой мышцы сосуда in vitro
Аорту крысы очищают от соединительной ткани и приросшего жира и нарезают на кольцевые сегменты приблизительно 3-4 мм длиной. Кольца из сосуда суспендируют в камерах ванны для органов (10 мл), содержащих бикарбонатный раствор Кребса следующего состава (ммоль): NaCl - 112; KCl - 4,7; KH2PO4 - 1,2; MgSO4 - 1,2; CaCl2 - 2,5; NaHCO3 - 25,0 и декстроза - 11,0. Растворы в ванне с тканями выдерживают при 37oC и непрерывно аэрируют 95% O2 c 5% CO2. Поддерживают остаточное напряжение аорты в 1 г и создают возможность для уравновешивания в течение 2 час, в течение которых раствор в ванне меняют каждые 15-20 мин. Изометрическое напряжение регистрируют на динографе Beckman R-611 с преобразователем силового сдвига Grass FT03. Кумулятивные кривые концентрации - отклик к ET-1 или другим сокращающимся агонистам строят методом постепенного добавления агониста. Концентрацию ET-1 увеличивают только после того, как предыдущая концентрация создаст установившееся состояние реакции сокращения. Для каждой ткани получается только одна кривая концентрация - отклик к ET-1. Антагонисты рецепторов ET добавляют к подобранным под пару тканям за 30 мин до инициирования отклика на концентрацию у сокращающихся агонистов.
Индуцируемые ET-1 сокращения сосуда выражают в виде процента отклика, выявленного 60 мМ KCl для каждой отдельной ткани, который определяют в начале каждого эксперимента. Данные выражают как среднее ± S.E.M. (среднее стандартное отклонение). Константы диссоциации (Kb) конкурентных антагонистов определяют стандартным способом Arunlakshana and Schild. Интервал действенности для соединений по изобретению составляет от 0,1 нМ до 50 мм.
Следующие далее примеры являются иллюстративными и не ограничивают соединения настоящего изобретения.
Пример 1
(+) (1S, 2R, 3S)-3-(2-Карбоксиметокси-4-метоксифенил)-1-(3,4-метилендиоксифенил)-5- (проп-1-илокси)индан-2-карбоновая кислота
a) 3-(Проп-1-илокси)ацетофенон
К суспензии NaH (13,84 г, 0,58 моль) в сухом ДМФА (50 мл) при 0oC добавляют раствор 3-гидроксиацетофенона (0 г, 0,37 моль). После перемешивания в течение 30 мин добавляют 1-иодпропан (70 мл, 0,72 моль) и смесь перемешивают в течение ночи при комнатной температуре. Смесь разбавляют ДМФА (50 мл), затем добавляют NaH (2,77 г, 0,12 моль) и после этого - 1-иодпропан (23 мл, 0,24 моль). Через 1 час ТС3 показывает, что реакция завершилась, и продукт осторожно гасят 6 М HCl и экстрагируют EtOAc. Этилацетатный экстракт последовательно промывают H2O, 10% водным NaOH и затем - солевым раствором. После сушки (MgSO4), фильтрации и упаривания получают указанное в заголовке соединение (65 г, 98%) в виде светло-желтого масла, которое используют без дальнейшей очистки.
Анализ:
Вычислено для C11H14O2: C - 74,13, H - 7,89.
Найдено: C - 73,85, H - 7,86.
b) Метил-3-(проп-1-илокси)бензоилацетат
К суспензии NaH (12 г, 0,5 моль) в сухом диметилкарбонате (50 мл) добавляют постепенно раствор 3-(проп-1-илокси)ацетофенона (65 г, 0,37 моль) в сухом диметилкарбонате (100 мл). В процессе добавления происходит выделение тепла, что при реакции вызывает кипение. После добавления смесь механически перемешивают в течение ночи и затем осторожно гасят 3М HCl и экстрагируют EtOAc. Этилацетатный экстракт последовательно промывают H2O, 5% водным NaHCO3, H2O и солевым раствором. После высушивания (MgSO4), фильтрации и упаривания получают желтое масло (82 г, количественный выход), которое используют без дальнейшей очистки.
c) Метил-3-(3,4-метилендиоксифенил)-2-[3-(проп-1-илокси)-бензоил] пропеноат
К раствору метил-3-(проп-1-илокси)бензоилацетата (10 г, 4,2 ммоль) в бензоле (50 мл) добавляют 3,4-метилендиоксибензальдегид (6,36 г, 4,2 ммоль), затем пиперидин (0,42 мл, 0,42 ммоль) и ледяную уксусную кислоту (приблизительно 8 капель). Смесь кипятят с обратным холодильником в течение 2 часов, удаляют летучие продукты под вакуумом и получают метил-3-(3,4-метилендиоксифенил)-2-[3-(проп-1-илокси)бензоил] пропеноат (7,4 г, 48%) в виде не совсем белого твердого вещества после обработки метанолом (т.пл. 122-123oC).
Анализ.
Вычислено для C21H20O6: - C - 68,47, H - 5,47.
Найдено: - C - 68,81, H - 5,49.
d) Метил-(1RS, 2SR)-1-(3,4-метилендиоксифенил)-5-(проп-1-илокси)-3-оксоиндан-2-карбоксилат
Метил-2-(3,4-метилендиоксифенил)-2-[3-(проп-1-илокси)-бензоил] пропеноат (7,4 г, 2,0 ммоль) растворяют в трифторуксусной кислоте (50 мл) при 0oC и смесь перемешивают при комнатной температуре в течение 20 мин. Трифторуксусную кислоту удаляют под вакуумом и получают указанное в заголовке соединение (6,4 г, 87%), после обработки теплым изопропанолом в виде белого твердого вещества, т.пл. 106-108oC.
Анализ:
Вычислено для C21G20O6: - C - 68,47, H - 5,47.
Найдено: - C - 68,12, H - 5,41
e) Метил-3-(3,4-метилендиоксифенил)-6-(проп-1-илокси)-1-оксоинден-2- карбоксилат
Метил-(1RS, 2SR)-1-(3,4-метилендиоксифенил)-5-(проп-1-илокси)-3-оксоиндан-2-карбоксилат (26,2 г, 71 ммоль) растворяют в толуоле (250 мл) и добавляют ДДХ (дихлордицианохинон) (16,5 г, 71 ммоль). Смесь нагревают при 80oC в течение 2 час, затем охлаждают, фильтруют и удаляют растворитель под вакуумом. Продукт очищают колоночной флэш-хроматографией на силикагеле (элюент - EtOAc: гексан = 20:80) и получают указанное в заголовке соединение в виде оранжевого твердого вещества (11,3 г, 44%); т.пл. 125-126oC.
Анализ:
Вычислено для C21H18O6: - C - 68,85; H - 4,95.
Найдено: - C - 68,45; H - 4,97.
f) Метил-(1RS)-1-гидрокси-1-(4-метокси-2-метоксиметоксифенил)-3-(3,4- метилендиоксифенил)-6-(проп-1-илокси)-инден-2-карбоксилат
К сухой магниевой стружке (1,7 г, 69 ммоль) в атмосфере аргона добавляют частями раствор 1-бром-4-метокси-2-метоксиметоксибензола (16,8 г, 68 ммоль) в 5% ТГФ в эфире (120 мл). Получающийся в результате 4-метокси-2-метоксиметоксифенил-магнийбромид добавляют к раствору метил-3-(3,4-метилендиоксифенил)-6-(проп-1-илокси)-1-оксоинден-2- карбоксилата (18,5 г, 51 ммоль) в ТГФ (400 мл) в атмосфере аргона при 0oC. Получающейся в результате смеси дают возможность нагреться до комнатной температуре и перемешивают в течение 10 мин. Смесь распределяют между 3 М HCl и EtOAc. Органический экстракт последовательно промывают H2O, водным NaHCO3, H2O и насыщенным водным раствором NaCl и сушат (Na2SO4). Растворитель удаляют при пониженном давлении и остаток очищают колоночной флэш-хроматографией на силикагеле (элюент: EtOAc/гексан, 10-20%), и получают указанное в заголовке соединение в виде желтого масла (24,5 г, 91%).
Анализ
Вычислено для C30H30O9: - C - 67,41, H - 5,66.
Найдено: - C - 67,21, H - 5,66
Разделение
Разделение (+) и (-) метил-(1RS)-1-гидрокси-1-(4-метокси-2-метоксиметоксифенил)-3-(3,4- метилендиоксифенил)-6-(проп-1-илокси)инден-2-карбоксилатов осуществляют на колонке с трис(3,5-диметилфенилкарбамат)целлюлозой, нанесенной на силикагель (Daicel Chiralcel OD); время удержания для (+) 8,8 мин [α]
Сведения о ЖХВР: колонка Chiralcel OD/DAICEL/, 21,2 мм - внутренний диаметр, длина 250 мм; растворитель этанол:гексан = 50:40, скорость истечения 10 мл/мин; впрыскивание: 1 г рацемата; обнаружение УФ = 405 нм.
(g) (+)-Метил-(1S, 2S, 3S)-3-(4-метокси-2-метоксиметоксифенил)-1-[3,4-метилендиоксифенил]-5-(проп- 1-илокси)индан-2-карбоксилат
В сосуд Парра загружают (+) метил-(1RS)-1-гидрокси-1-(4-метокси-2-метоксиметоксифенил)-3- (3,4-метилендиоксифенил)-6-(проп-1-илокси)инден-2-карбоксилат (1 г, 1,8 ммоль), растворенный в небольшом объеме EtOAc (25 мл), и 10% палладий-на-угле (93 мг). Получающийся в результате раствор перемешивают в атмосфере водорода в течение 120 часов и фильтруют. Фильтрат концентрируют при пониженном давлении и продукт очищают колоночной хроматографией на силикагеле (элюент: EtOAc/гексан, 5-10%/, и получают указанное в заголовке соединение в виде белой пены (0,80 г, 83%). [α]
Анализ
Вычислено для C30H32O8: - C - 69,22, H - 6,20
Найдено: - C - 68,95, H - 6,11
h) (+) Метил-(1S, 2S,3S)-3-(2-гидрокси-4-метоксифенил)-1-(3,4-метилендиоксифенил)-5- (проп-1-илокси)инден-2-карбоксилат
К раствору метил-(1S, 2S, 3S)-3-(4-метокси-2-метоксиметоксифенил)-1- (3,4-метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоксилата (0,7 г, 1,3 ммоль) в метаноле (10 мл) добавляют концентрированную HCl (0,1 мл) и затем смесь нагревают при кипячении с обратным холодильником в течение 2 час. Растворитель затем удаляют под вакуумом и остаток очищают колоночной хроматографией на силикагеле (элюент: EtOAc/гексан, 10-20%), и получают указанное в заголовке соединение в виде бесцветного стеклообразного продукта (0,50 г, 78%). [α]
Анализ.
Вычислено для C28H28O7 • 1/2H2O: - C - 69,27, H - 6,02
Найдено: - C - 69,59, H - 5,99
i) (+) Метил-(1S,2S,3S)-3-(2-карбоэтоксиметокси-4-метоксифенил)-1-(3,4- метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоксилат
Раствор метил-(1S, 2S, 3S)-3-(2-гидрокси-4-метоксифенил)-1-(3,4- метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоксилата (0,1 г, 0,2 ммоль) в сухом ДМФА (2 мл) добавляют к NaH (6 мг, 0,24 ммоль) в небольшом объеме сухого ДМФА при 0oC. Смесь перемешивают при 0oC в течение 15 мин и затем добавляют этилбромацетат (42 мг, 0,25 ммоль). Образующуюся в результате смесь перемешивают при 0oC в течение 1 часа. Затем реакцию гасят разбавленной HCl и реакционную смесь экстрагируют EtOAc. Этилацетатный экстракт промывают водой, затем соляным раствором, сушат (MgSO4), фильтруют и упаривают. Продукт очищают колоночной хроматографией на силикагеле (элюент: EtOAc/гексан, 10-15%) и получают указанное в заголовке соединение в виде стекловидного твердого вещества (82 мг, 68%). [α]
Анализ:
Вычислено для C32H34O9: - C - 68,32; H - 6,09.
Найдено: - C - 67,98, H - 6,09.
j) (+) (1S,2S,3S)-3-(2-карбоксиметокси-4-метоксифенил)-1-(3,4-метилендоксифенил)- 5-(проп-1-илокси)индан-2-карбоновая кислота.
К раствору метил-(1S,2S,3S)-3-(2-карбоэтоксиметокси-4-метоксифенил)-1-(3,4- метилендиоксифенил)-5-(проп-1-илокси)-индан-2-карбоксилата (20 мг, 0,04 ммоль) в диоксане (1 мл) добавляют 3 М раствор NaOH (0,3 мл, 1 ммоль). Реакционную смесь кипятят с обратным холодильником в течение 4 час и после охлаждения удаляют растворитель в вакууме, растворяют остаток в воде и подкисляют 3 NH HCl. Получающийся в результате осадок собирают фильтрацией и сушат, получают белое твердое вещество (15 мг, 81%); т.пл. 99-102oC. [α]
Анализ:
Вычислено для C29H28O9: - C - 66,92, H - 5,42,
Найдено: - C - 67,37, H - 5,32.
Пример 1A
Получение 1-бром-4-метокси-2-метоксиметоксибензола
a) 1-Бром-2-гидрокси-4-метоксибензол
3-Бром-2-гидрокси-6-метоксибензойную кислоту [T. de Paulis et al., J. med. Chem (1985), 28, N 1263-1269] (5 г, 0,02 моль) нагревают в хинолине (200 мл) при 160oC в течение 1 часа. После охлаждения продукт распределяют между Et2O и 3М HCl. Органический экстракт промывают водой и соляным раствором, затем сушат (MgSO4), фильтруют и упаривают, получают названное в заголовке соединение, которое перекристаллизовывают из 5% этилацетата в гексане (4 г, 97%); т.пл. 40-42oC.
Анализ:
Вычислено для C7H7BrO2: - C - 41,41, H - 3,48
Найдено: - C - 41,39, H - 3,37.
b) 1-Бром-4-метокси-2-метоксиметоксибензол
К суспензии NaH (2,5 г, 0,06 моль) в сухом ДМФА (100 мл) при 0oC добавляют раствор 1-бром-2-гидрокси-4-метоксибензола 10,6 г, 0,05 моль). После перемешивания в течение 30 мин при 0oC добавляют по каплям брометилметиловый эфир (7,8 г, 0,06 ммоль). Смесь нагревают до комнатной температуры в течение 20 мин и затем перемешивают в течение 2 час, затем ее осторожно гасят путем добавления холодной разбавленной HCl и экстрагируют EtOAc. Этилацетатный экстракт последовательно промывают H2О, 5% водным раствором NaHCO3, H2O и, наконец, соляным раствором. После сушки (MgSO4), фильтрации и упаривания получают жидкость. Продукт очищают перегонкой (85oC, 0,2 мм рт.ст.), и получают указанное в заголовке соединение в виде бесцветного масла (13,7 г, 97%).
1H ЯМР (CDCl3) δ 7,40 (д., H, J = 8,9 Гц), 6,75 (д., 1H, J = 2,8 Гц), 6,46 (д. д. , 1H, J = 8,9, 2,8 Гц), 5,23 (с., 2H), 3,77 (с., 3H), 3,52 (с., 3H).
Пример 2
Дициклогексиламиновая соль (1RS, 2SR,3RS)-3-[2-(2-гидроксиэт-1-илокси)-4-метоксифенил] -1-(3,4- метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоновой кислоты
Т.пл. 182-184oC
Анализ:
Вычислено для C41H53NO8: - C - 71,59, H - 7,77; N - 2,04.
Найдено: - C - 71,67, H - 7,66, N - 2,42.
Пример 2A
(+) (1S, 2R,3S-3-[2-(2-Гидроксиэт-1-илокси)-4-метоксифенил]-1-(3,4- метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоновая кислота
a) (+)-(1S, 2R, 3S)-3-[2-(2-трет-бутилдиметилсилоксиэт-1-илокси)-4- метоксифенил] -2-(3,4-метилендиоксифенил)-5-(проп-1-илокси)-индан-2-карбоксилат.
Раствор метил(1S, 2S,3S)-3-(2-гидрокси-4-метоксифенил)-1- (3,4-метилендиоксифенил)-5-(проп-1-илокси)-индан-2-карбоксилата (3 г, 6 ммоль) в сухом ДМФА (30 мл) добавляют к NaH (230 мг, 7 ммоль, 80%) в небольшом объеме сухого ДМФА при 0oC. Смесь перемешивают при 0oC в течение 15 мин и затем добавляют по каплям 2-трет-бутилдиметил-силоксиэтилбромид (1,65 г, 8 ммоль). Получающуюся в результате смесь перемешивают при 0oC в течение 3 час. Реакцию затем гасят разбавленной HCl и смесь экстрагируют EtOAc. Этилацетатный экстракт промывают водой, затем соляным раствором, сушат (MgSO4), фильтруют и упаривают. Продукт очищают колоночной хроматографией на силикагеле (элюент: EtOAc/гексан, 5-10%) и получают указанное в заголовке соединение в виде бесцветного масла (520 мг, 18% по отношению к извлечению эпимеризованного исходного вещества).
b) Метил-(+)-1S, 2R,3S)-3-[2-(2-гидроксиэт-1-илокси)-4-метоксифенил]-1- (3,4-метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоксилат.
К раствору (+) метил-(1S,2R,3S)-3-[2-(2-трет-бутилдиметилсилоксиэт-1-илокси)-4- метоксифенил] -1-(3,4-метилен-диоксифенил)-5-(проп-1-илокси)индан-2-карбоксилата (0,520 г, 0,74 ммоль), в ТГФ (10 мл) при комнатной температуре добавляют 1 М раствор тетра-н-бутиламмонийфторида (2,5 мл) в ТГФ. Реакционную смесь перемешивают при комнатной температуре в течение 1 часа. После концентрирования под вакуумом остаток распределяют между смесью эфира с этилацетатом и водой. Органический слой промывают соляным раствором, сушат (MgSO4) и концентрируют. Остаток очищают колоночной флэш-хроматографией на силикагеле (элюент: 20-30% этилацетата в гексане) и получают указанное в заголовке соединение в виде бесцветной пены (0,35 г, 82%).
c) (+) (1S, 2R, 3S)-3-[2-(2-Гидроксиэт-1-илокси)-4-метоксифенил] -1- (3,4-метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоновая кислота
К раствору метил-(1S,2R,3S)-3-[2-(2-гидроксиэт-1-ил-окси)-4- метоксифенил)-1-(3,4-метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоксилата (0,35 г, 0,67 ммоль) в метаноле с ТГФ (1/2) (15 мл) добавляют 0,5 М раствор LiOH (5 мл). Реакционную смесь перемешивают при комнатной температуре в течение ночи. Растворитель удаляют под вакуумом, продукт растворяют в воде и подкисляют 3 н HCl. Образующийся в результате осадок собирают фильтрацией и сушат, получают белое твердое вещество (0,31 мг, 91%); т.пл. 94-98oC. [α]
Анализ:
Вычислено для C29H29O8Na • 11,8 H2O: - C - 63,47, H - 5,74
Найдено: - C - 63,39, H - 5,66
Пример 3
Динатриевая соль (1RS,2SR,3RS)-3-[2-[(4-карбоксипиридин-3-ил)-окси]-4-метоксифенил] -1- (3,4-метилендиоксифенил)-5-(проп-1-ил-окси)индан-2-карбоновой кислоты
2) Метил-(1RS,2SR,3RS)-3-[2-[(4-формилпиридин-3-ил)оксо]-4-метоксифенил] -1-(3,4-метилендиоксифенил)-5-(проп-1-илокси)-индан-2-карбоксилат
К раствору метил-(1RS, 2SR, 3RS)-3-(2-гидрокси-4-метоксифенил)-1-(3,4- метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоксилата (300 мг, 0,63 ммоль) в ДМФА (4 мл) добавляют K2CO3 (109 мг, 0,79 ммоль) и 3-фтор-4-формилпиридин (150 мг, 1,2 ммоль). Реакционную смесь кипятят с обратным холодильником в атмосфере аргона в течение 2 час. После охлаждения до комнатной температуре ее распределяют между 3 ч HCl и этилацетатом. Этилацетатный экстракт промывают водой, водным раствором NaHCO3 и солевым раствором и сушат (MgSO4). Растворитель удаляют под вакуумом и остаток очищают колоночной флэш-хроматографией (силикагель, градиент элюирования от 10% до 20% этилацетата в гексане), и получают указанное в заголовке соединение (128 мг, 42%).
b) Метил-(1RS, 2SR, 3RS)-3-[2-[(4-карбоксипиридин-3-ил)окси]-4-метоксифенил]-1- (3,4-метилендиоксифенил)-5-(проп-1-илокси)-индан-2-карбоксилат
К раствору метил-(1RS,2SR,3RS)-3-[2-[(4-формилпиридин-3-ил)-окси]-4-метоксифенил] -1-(3,4- метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоксилата (128 мг, 0,24 ммоль) в трет-BuOH (10 мл) добавляют раствор NaClO2 (34 мг, 0,28 ммоль) и NH2SO3Н (40 мг, 0,42 ммоль) в воде (6 мл). Реакционную смесь перемешивают при комнатной температуре в течение 2 час и распределяют между водой и этилацетатом. Этилацетатный экстракт промывают водой и солевым раствором, сушат (MgSO4). Растворитель удаляют под вакуумом, остаток очищают колоночной флэш-хроматографией (силикагель, 25% этилацетата в гексане, содержащем 5% уксусной кислоты), и получают указанное в заголовке соединение (90 мг, 69%),
c) Динатриевая соль (2RS,2SR,3RS)-3-[2-[(4-карбоксипиридин-3-ил)окси]-4-метоксифенил] -1-(3,4- метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоновой кислоты
К раствору метил-(1RS,2SR,3RS)-3-[2-[(4-карбоксипиридин-3-ил)-окси]-4-метоксифенил] -1- (3,4-метилендиоксифенил)-5-(проп-1-ил-окси)индан-2-карбоксилата (90 мг, 0,15 ммоль) в изопропаноле (2 мл) добавляют 1 М водный раствор NaOH 0,3 мл, 0,3 ммоль. Получающуюся в результате смесь кипятят с обратным холодильником в течение 12 час и затем концентрируют при пониженном давлении. Остаток распределяют между разбавленной HCl и этилацетатом. Этилацетатный экстракт промывают водой и сушат (MgSO4). Растворитель удаляют под вакуумом и остаток очищают колочной флэш-хроматографией (силикагель, 30% этилацетата в гексане, содержащем 5% уксусной кислоты), и получают указанное в заголовке соединение (65 мг, 74%); т.пл. 220-222oC (разлож.) (динатриевая соль).
Пример 4
Натриевая соль 2,2-диметилпропаноилоксиметил-(1RS,2SR,3RS)-3-(2-карбоксиметокси-4- метоксифенил)-1-(3,4-метилендиоксифенил)-5-(проп-1-илокси)-индан-2- карбоксилата
a) 2,2-Диметилпропаноилоксиметил-(1RS, 2SR, 3RS)-3-(2-гидрокси-4-метоксифенил)-1- (3,4-метилендиоксифенил)-5-(проп-1-илокси)-индан-2-карбоксилат
Калиевую соль (1RS,2SR,3RS)-3-(2-гидрокси-4-метоксифенил(-1-(3,4-метилендиоксифенил)- 5-(проп-1-илокси)индан-2-карбоновой кислоты (125 мг, 0,54 ммоль) (полученную обработкой соответствующей кислоты KHCO3 (54 мг, 0,54 ммоль)) растворяют в ДМФА (3 мл) и добавляют пивалоилоксиметилиодид (0,54 ммоль) (полученный из пивалоилоксиметилхлорида (73 мг, 0,54 ммоль) и избытка иодида натрия в ацетоне). Реакционную смесь перемешивают в течение ночи и затем распределяют между разбавленной HCl и этилацетатом. Органический слой промывают водой и солевым раствором и затем сушат (безводн. MgSO4), фильтруют и упаривают. Продукт очищают колоночной хроматографией и получают указанное в заголовке соединение (120 мг, 77%) в виде бесцветного масла.
b) 2,2-Диметилпропаноилоксиметил-(1RS, 2SR,3RS)-3-(2-карбобензилоксиметокси-4- метоксифенил)-1-(3,4-метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоксилат
2,2-Диметилпропаноилоксиметил-(1RS, 2SR, 3RS)-3-(2-гидрокси-4-метоксифенил)-1- (3,4-метилендиоксифенил)-5-(проп-1-илокси)-индан-2-карбоксилат (280 мг, 0,5 ммоль) в сухом ДМФА (3 мл) добавляют к NaOH (18 мг, 0,6 ммоль) в небольшом объеме сухого ДМФА. Смесь перемешивают при комнатной температуре в течение 20 мин и затем добавляют бензилбромацетат (137 мг, 0,6 ммоль). После перемешивания в течение 1,5 час продукт между 3М водной HCl и этилацетатом. Органический слой промывают водой, затем солевым раствором, сушат (безв. MgSO4), фильтруют и упаривают и получают масло. Продукт очищают колоночной хроматографией и получают указанное в заголовке соединение (240 мг, 66%) в виде бесцветного масла.
с) 2,2-Диметилпропаноилоксиметил-(1RS, 2SR,3RS)-3-(2-карбоксиметокси-4- метоксифенил-1-(3,4-метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоновая кислота
2,2-Диметилпропаноилоксиметил-(1RS, 2SR, 3RS)-3-(2-карбобензилоксиметокси-4- метоксифенил)-1-(3,4-метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоксилат (240 мг, 0,3 ммоль) растворяют в смеси этилацетата и этанола 2:1 (3 мл) и затем добавляют 50 мг 10% Pd/C. Смесь перемешивают при комнатной температуре в атмосфере H2 в течение 3 час. Катализатор затем отфильтровывают, растворитель концентрируют под вакуумом и полученное в результате масло очищают колоночной флэш-хроматографией. Указанное в заголовке соединение получают (180 мг, 86%) в виде бесцветного масла.
Масс-спектр (точная масса) (M+Na)+: 647, 2335 (натриевая соль), (D = -2,3 m Da для C33H38O11Na); Т.пл. 190-195oC (разл., натриевая соль).
Пример 5
Натриевая соль (1S,2R,3S)-3-[2-(карбо-(1RS)-1-(2-метокси-2-метилпропионилокси)эт-1- илоксиметокси] -4-метоксифенил]-1-(3,4-метилендиоксифенил)-5-(проп-1- илокси)индан-2-карбоновой кислоты
a) Аллил-(1S, 2R, 3S)-3-(4-метокси-2-метоксиметоксифенил)-1-(3,4- метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоксилат
(1S, 2R, 3S)-3-(4-метокси-2-метоксиметоксифенил)-1-(3,4-метилендиоксифенил)-5- (проп-1-илокси)индан-2-карбоновую кислоту (4,8 г, 9,5 ммоль) растворяют в сухом ацетонитриле (30 мл) и добавляют ДБУ (1,7 мл, 11,4 ммоль), и затем аллибромид (3,4 г, 28 ммоль). После перемешивания в течение 0,5 час продукт распределяют между 3 М водной HCl и этилацетатом. Органический слой промывают водой и солевым раствором, затем сушат (безв. MgSO4), фильтруют и упаривают, получают масло. Продукт очищают колоночной хроматографией и получают указанное в заголовке соединение в виде бледно-желтого масла (5,7 г, колич. выход).
b) Аллил-(1S, 2R, 3S)-3-(2-гидрокси-2-метоксифенил)-1-(3,4-метилендиоксифенил)-5- (проп-1-илокси)индан-2-карбоксилат
Аллил-(1S, 2R, 3S)-3-(4-метокси-2-метоксиметоксифенил)-1-(3,4-метилендиоксифенил)- 5-(проп-1-илокси)индан-2-карбоксилат (1,7 г, 3,11 ммоль) растворяют в аллиловом спирте (20 мл) и затем добавляют 15 капель конц. HCl. Образующийся в результате раствор перемешивают при 65oC в течение 2 час. После удаления растворителя остаток распределяют между водой и этилацетатом. Органический слой промывают водой, 5% водным раствором NaHCO3 и солевым раствором; затем сушат (безводн. MgSO4), фильтруют и упаривают и получают масло. Продукт очищают колоночной хроматографией и получают указанное в заголовке соединение в виде светло-желтого масла (1,26 г, 81%).
c) Аллил-(1S,2R,3S)-3-(2-карбо-1-трет-бутоксиметокси-4-метоксифенил)-1- (3,4-метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоксилат
Аллил-(1S, 2R, 3S)-3-(2-гидрокси-4-метоксифенил)-1-(3,4-метилендиоксифенил)- 5-(проп-1-илокси)индан-2-карбоксилат (1,0 г, 2 ммоль) в сухом ДМФА (4 мл) добавляют к NaH (57, мг, 2,4 ммоль) в небольшом объеме ДМФА. Смесь перемешивают при комнатной температуре в течение 20 мин, затем добавляют трет-бутилбромацетат (974 мг, 5 ммоль). После перемешивания в течение 0,5 час продукт распределяют между 3 М водной HCl и этилацетатом. Органический слой промывают водой, солевым раствором, сушат (безводн. MgSO4), фильтруют и упаривают, получают масло. Продукт очищают колоночной хроматографией и получают указанное в заголовке соединение (1,1 г, 93%) в виде светло-желтого масла.
d) Аллил-(1S, 2R,3S)-3-(2-карбоксиметокси-4-метоксифенил)-1-(3,4- метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоксилат
Аллил-(1S, 2R, 3S)-3-(2-карбо-трет-бутоксиметокси-4-метоксифенил)-1- (3,4-метилендиоксифенил)-5-(проп-1-илокси)-индан-2-карбоксилат (765 мг, 1,24 ммол) растворяют в TFA (трифторуксусная к-та) (5 мл), содержащей несколько капель анизола. Реакционную смесь перемешивают при комнатной температуре в течение 20 мин. Растворитель удаляют, остаток разбавляют этилацетатом, промывают водой, солевым раствором, сушат (безводн. MgSO4), фильтруют и упаривают. Продукт очищают колоночной хроматографией и получают указанное в заголовке соединение (575 мг, 83%) в виде бесцветного масла.
e) Натриевая соль аллил-(1S,2R,3S)-3-[2-[карбо-(1RS)-1-(2-метокси-2-метилпропионилокси)эт-1- илоксиметокси-4-метоксифенил-1-(3,4-метилендиоксифенил)-5-(проп-1-илокси)индан- 2-карбоновой кислоты
Аллил-(1S,2R,3S)-3-(2-карбоксиметокси-4-метоксифенил)-1-(3,4- метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоксилат (287 мг, 0,5 ммоль) растворяют в ДМФА (5 мл) и добавляют Cs2CO3 (333 мг, 1 ммоль) и затем -(1S)-1-бромэтил-2-метокси-2-метилпропионат (225 мг, 1 ммоль). Реакционную смесь перемешивают при комнатной температуре в течение ночи, затем распределяют между водой и этилацетатом, промывают разбавленной HCl и солевым раствором, сушат (безводн. MgSO4), фильтруют и упаривают, получают масло. Продукт очищают колоночной хроматографией и получают указанное в заголовке соединение (260 мг, 74%) в виде бесцветного масла.
f) Натриевая соль (1S,2R,3S)-3-[2-[карбо-(1RS)-1-(2-метокси-2- метилпропионилокси)эт-1-илоксиметокси] -4-метоксифенил] -1-(3,4- метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоновой кислоты
Аллил-(1S, 2R, 3S)-3-[2-карбо-(1RS)-1-(2-метокси-2-метилпропионилокси)эт-1- илоксиметокси] -4-метоксифенил] -1-(3,4-метилендиоксифенил)-5-(проп-1-илокси) индан-2-карбоксилат (260 мг, 0,37 ммоль) растворяют в CH2Cl2 (2 мл) и добавляют тетракис (трифенилфосфин)палладий(O) (36 мг, 0,037 ммоль) и затем гидрид три-н-бутилолова (0,11 мл, 0,4 моль). Реакционную смесь перемешивают при комнатной температуре в течение 3 час, затем гасят 3 н HCl и перемешивают в течение 20 мин. Органический слой разбавляют этилацетатом, промывают водой, затем солевым раствором, сушат (безводн. MgSO4), фильтруют и упаривают, получают масло. Продукт очищают колоночной хроматографией и получают указанное в заголовке соединение (210 мг, 85%) в виде бесцветного масла.
Масс-спектр (точная масса) (M+Na)+: 687, 2415 (натриевая соль); (D = +0,3 mDa для C36H40O12NA).
Описанными выше способами получают соединения, перечисленные ниже.
(1RS,2SR,3RS)-3-[2-[(3-арбоксипиридин-2-ил)окси]-4-метоксифенил]-1-(3,4- метилендиоксифенил)-5-(проп-1-илокси)-индан-2-карбоновая кислота; т. пл. 152-155oC.
(1RS, 2SR, 3RS)-3-[2-[Карбо-(N,N-диэтилкарбамоил)метокси]-метокси-4- метоксифенил] -1-(3,4-метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоновая кислота; т.пл. 181-182oC.
Транс, транс-1,3-Бис(4-метоксифенил)индан-2-карбоксамид; т. пл. 223-224oC.
Динатриевая соль (1RS,2SR,3SR)-3-[4-метокси-2-[2-(метилфосфининил)эт-1-ил] фенил]-1-(3,4- метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоновой кислоты; (точная масса) M+ + Na: 619, 1462 ( Δ = -1,2 mDa для C30H31PNa3).
Примеры 6-30
Натриевая соль индан-5-ил-(1RS,2SR,3RS)-3-(2-карбоксиметокси-4- метоксифенил)-1-(3,4-метилендиоксифенил)-5-(проп-1-илокси)индан-2- карбоновой кислоты;
т.пл. 181-183oC (разл.).
Натриевая соль 3,5-диметоксифенил-(1RS,2SR,3RS)-3-(2-карбоксиметокси-4-метоксифенил)-1-(3,4- метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоксилата;
т.пл. 185-189oC (разл.).
Натриевая соль (1RS)-1-(2-метокси-2-метилпропионилокси)-эт-1-ил (1RS, 2SR, 3RS)-3-(2-карбоксиметокси-4-метоксифенил)-1-(3,4- метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоксилата;
т.пл. 178-181oC, разл.
Натриевая соль N, N-диметилкарбамоилметил-(1RS,2SR,3RS)-(2-карбоксиметокси-4-метоксифенил)-1- (3,4-метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоксилата;
т.пл. 170-174oC, разл.
Натриевая соль этоксикарбоксиметил-(1RS,2SR,3RS)-3-(2-карбоксиметокси-4-метоксифенил)-1- (3,4-метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоксилата;
масс-спектр (точная масса) (M + Na)+: 645, 1959 (натриевая соль);
(D = 1,1 m Da для C33H34O12Na).
Натриевая соль бензоилоксиметил-(1RS,2SR,3RS)-3-(2-карбоксиметокси-4-метоксифенил)-1- (3,4-метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоксилата;
Масс-спектр. m/e: 672 (M + NH4)+.
Натриевая соль циклогексилоксикарбоксиметил-(1RS,2SR,3RS)-3-(2-карбоксиметокси-4-метоксифенил)- 1-(3,4-метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоксилата;
масс-спектр. (точная масса) (M + Na)+: 699, 2453 (натриевая соль);
(D = -3,5 m Da для C37H49O12Na).
Натриевая соль этил-(1RS, 2SR, 3RS)-3-(2-карбоксиметокси-4- метоксифенил)-1-(3,4-метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоксилата;
масс-спектр. (точная масса) M+: 548, 2040 (свободная кислота), (D = + 0,6 m Da для C31H32O9).
Натриевая соль (1S,2R,3S)-3-[2-[карбо-(2',6'-диметилфенокси)-метокси]-4-метоксифенил] -1- (3,4-метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоновой кислоты;
масс-спектр. (точная масса) (M + Na)+: 647, 2264 (натриевая соль);
D = -0,7 m Da для C37H36O9Na).
Натриевая соль (1S, 2R,3S)-3-[2-(карбоциклопентилоксиметокси)-4-метоксифенил] -1- (3,4-метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоновой кислоты;
масс-спектр. (точная масса) (M + Na)+: 611, 2282 (натриевая соль);
(D = -2,5 m Da для C34H36O9Na).
Натриевая соль (1S, 2R, 3S)-3-[2-[карбо(индан-5-илокси)-метокси]-4-метоксифенил] -1- (3,4-метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоновой кислоты;
масс-спектр. (точная масса) (M + Na)+: 659, 2281 (натриевая соль):
(D = -2,4 m Da для C38H36O9Na).
Натриевая соль (1S,2R,3S)-3-[2-карбо(эт-1-илокси)метокси]-4-метоксифенил] -1-(3,4- метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоновой кислоты;
масс-спектр. (точная масса) (M + 2Na-H)+: 593, 1769 (натриевая соль;
(D = -0,6 m Da для C31H31O9Na2).
(1RS, 2SR, 3RS)-3-(2-Карбоэтоксиметокси-4-метоксифенил)-1- (3,4-метилендиоксифенил)-5-(проп-1-илокси-индан-2-карбоновая кислота;
т.пл. 148-149oC.
(1RS, 2SR, 3RS)-2-Трифторметилсульфонамидометил-3-(2-карбоксиметокси-4- метоксифенил)-1-(3,4-метилендиоксифенил)-5-(проп-1-илокси)индан;
т.пл. 184-186oC.
Натриевая соль индан-5-ил-(1S,2R,3S)-3-(2-карбоксиметокси-4-метоксифенил)-1-(3,4- метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоксилата.
Натриевая соль циклопентил-(1S, 2R,3S)-3-(2-карбоксиметокси-4-метоксифенил)-1- (3,4-метилендиоксифенил)-5-(проп-1-илокси)-индан-2-карбоксилата.
Натриевая соль этоксикарбоксиметил-(1S,2R,3S)-3-(2-карбоксиметокси-4-метоксифенил)-1- (3,4-метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоксилата.
Натриевая соль (1RS)-1-(1метилэтоксикарбокси)эт-1-ил-(1RS,2SR,3RS)-3-(2-карбоксиметокси-4- метоксифенил)-1-3,4-мителендиоксифенил)-5-(проп-1-илокси)индан-2-карбоксилата;
т.п. 151-155oC.
Натриевая соль этил-(1S,2R,3S)-3-(2-карбоксиметокси-4-метоксифенил)-1- (3,4-метилендиоксифенил)-5-(проп-1-илокси)-индан-2-карбоксилата.
Натриевая соль (1S, 2R,3S)-3-(2-карбометоксиметокси-4-метоксифенил]-1- (3,4-метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоновой кислоты.
Натриевая соль (1S,2R,3S)-3-[2-[-карбобензоилоксиметоксиметокси]-4-метоксифенил] -1-(3,4- метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоновой кислоты.
Натриевая соль (1S,2R,3S)-3-[2-(карбоэтоксикарбоксилоксиметоксиметокси)-4-метоксифенил] -1- (3,4-метилендиоксифенил)-5-(проп-1-илокси)индан-2-карбоновой кислоты.
Натриевая соль (1S,2R,3S)-3-[2-(карбоацетоксиметоксиметокси)-4- метоксифенил] -1-(3,4-метилендиоксифенил)-5-(проп-1-илокси)индан-2- карбоновой кислоты.
Натриевая соль (1S,2R,3S)-3-[2-(карбофталидилметокси)-4-метоксифенил]-1-(3,4- метилендиоксифенил)-5-(проп-1-илокси)-индан-2-карбоновой кислоты.
Натриевая соль (1S,2R,3S)-3-[2-(карбо-(2-метокси-2-метил- пропионилоксиметоксиметокси)-4-метоксифенил]-1-(3,4-метилендиоксифенил)-5- (проп-1-илокси)индан-2-карбоновой кислоты.
Пример 31
Натриевая соль (1S, 2R,3S)-3-[2-карбо-(2,2-диметилпропано-илоксиметоксиметокси)-4- метоксифенил] -1-(3,4-метилендиоксифенил)-5-(проп-1-илокси)индан-2- карбоновой кислоты
К раствору монокалиевой соли (1S,2R,3S)-3-[2-карбоксиметокси-4-метоксифенил] -1-(3,4-метилендиоксифенил)- 5-(проп-1-илокси)индан-2-карбоновой кислоты (170 мг, 0,3 ммоль) (полученной путем обработки соответствующей дикислоты (156 мг, 0,3 ммоль) 1 экв. KHCO3 (30 мг, 0,3 ммоль)) в ДМФА (4 мл) добавляют пивалоилоксиметилиодид (74 мг, 0,3 ммоль). Реакционную смесь перемешивают при комнатной температуре в течение 0,5 час, затем добавляют еще пивалоилоксиметилиодид (20 мг, 0,08 ммоль) и затем еще перемешивают в течение 0,5 часа. Реакционную смесь распределяют между разбавленной водной HCl и этилацетатом. Этилацетатный экстракт промывают водой и солевым раствором и сушат (безводный MgSO4). Растворитель удаляют под вакуумом, остаток очищают колоночной флэш-хроматографией (силикагель, этилацетат: гексан: HOAc = 30 : 65 : 5) и получают нужное соединение в виде белой пены (140 мг, 73%), как свободную кислоту, которую превращают в ее натриевую соль; т.пл. 128-133oC.
Масс-спектр. (точная масса) M+ + Na: 679, 2116 (натриевая соль);
(D = +1,2 mDa для C35H37O11Na2).
Пример 32
Составы для применения в качестве лекарственных препаратов, включающие соединения по настоящему изобретению, могут быть получены в различных формах и со многими добавками. Примеры таких составов приводятся ниже.
Состав лекарственной формы для ингаляции
Соединение формулы I (от 1 мг до 100 мг) используют в виде аэрозоля из мерного ингалятора, чтобы доставить нужное количество лекарственного препарата при применении.
Таблетки
Ингредиенты - на таблетку
1. Активный ингредиент (соединение формулы I) - 40 мг
2. Кукурузный крахмал - 20 мг
3. Альгиновая кислота - 20 мг
4. Альгинат натрия - 20 мг
5. Стеарат Mg 1,3 мг - 1,3 мг - --- - 2,3 мг
Приготовление таблеток
Стадия 1. Смешивают ингредиенты NN 1, 2, 3 и 4 в подходящем смесителе.
Стадия 2. К смеси со стадии 1 добавляют частями достаточное количство воды при тщательном перемешивании после каждого добавления. Такое добавление воды и перемешивание продолжают до тех пор, пока масса не примет консистенцию, допускающую превращение ее во влажные гранулы.
Стадия 3. Влажную массу превращают в гранулы, пропуская ее через виброгранулятор, используя сито N 8 меш (2,38 мм).
Стадия 4. Влажные гранулы затем сушат в печи при 140oF (60oC) до сухого состояния.
Стадия 5. Сухие гранулы смазывают ингредиентом N 5.
Стадия 6. Смазанные гранулы уплотняют на подходящей машине для таблетирования.
Парентеральный состав
Фармацевтическую композицию для парентерального введения готовят путем растворения соответствующего количества соединения формулы I в полиэтиленгликоле при нагревании. Этот раствор затем разбавляют водой для инъекций PhEur (до 100 мл). Раствор затем стерилизуют путем фильтрации через мембранный фильтр 0,22 мкм и запаивают в стерильные контейнеры.
Возможность применения антагонистов эндотелинового рецептора по настоящему изобретению для лечения гипертонии, почечной недостаточности и цереброваскулярных заболеваний показана на соответствующих животных моделях и подробно описана в прилагаемых ссылочных материалах.
Так, согласно этим данным соединения по изобретению демонстрируют высокую эффективность в отношении обратного развития острой почечной недостаточности, вызванной ишемией [Gellai M. et al., The Journal of Pharmacology and Experimental Therapeutics, Vol. 275, N 1, pages 1-7, 1995], в отношении ишемического поражения мозга [F.C. Barone, et al., Journal of Cardiovascular Pharmacology, 26 (Suppl. 3)L S404-S407, 1995] и в отношении понижения кровяного давления [E.H. Ohlstein, et al., Proc. Natl. Acad. Sci. USA, vol. 91, pp. 8052-8056, 1994].
Изобретение относится к новым производным индана и индена, фармацевтическим композициям, содержащим такие соединения, и к применению их в качестве антагонистов эндотелинового рецептора. Описываются новые производные индан-2-карбоновой кислоты общей формулы I,
где значения R1, R2, R10, P1, P2, Z1, Z2, Z3 указаны в п.1 формулы.
Описывается также способ их получения, фармацевтическая композиция на базе соединений формулы I, а также способ антагонизирования эндотелиновых рецепторов при лечении гипертонии, почечной недостаточности или цереброваскулярного заболевания с использованием соединения формулы I. 10 с. и 5 з. п ф-лы.
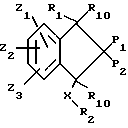
где R1 представляет собой - X(CH2)nAr, -X(CH2)nR8 или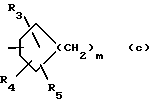
R2 представляет водород;
P1 представляет -X(CH2)nR8;
P2 представляет -X(CH2)nR8;
R3 и R5 представляет независимо водород, R11, OH, C1-8-алкокси, галоген или -X(CH2)nR8, где каждая метиленовая группа в -X(CH2)nR8 может быть незамещенной или замещена одной или двумя группами -(CH2)nAr;
R4 представляет водород, -XR11, C1-5-алкокси, который может быть замещен OH;
R6 представляет водород или C1-4-алкил;
R7 представляет водород, C1-10-алкил, -(CH2)nAr или C2-10-алкенил;
R8 представляет R11, CO2R7, OR6, P(O)(OR7)R7, CO2C(R11)2O-(CO)XR7, CONR7SO2R11 или -CO2(CH2)mC(O)N(R6)2;
R9 представляет (CH2)n,
R10 представляет R3 или R4;
R11 представляет водород C1-8-алкил, C2-8-алкенил или Ar, все из которых могут быть незамещенными или замещены одним или несколькими OH или галогенами;
X представляет (CH2)n или 0;
Y представляет CH3;
Ar представляет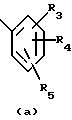

или пиридил, все из которых могут быть незамещенными или замещены одной или несколькими группами R3 или R4;
A представляет [C(R6)2]m;
B представляет -O-;
Z1 и Z2 представляют независимо водород или C1-8-алкокси, который может быть замещен OH,
Z3 представляет Z1 или -X-R9-Y;
n равно целому числу от 0 до 6;
m равно 1, 2 или 3 при условии, что когда R3, R5 представляет X(CH2)nR8 и n не равно 0, X представляет кислород, когда R8 представляет собой DR6 или CO2H;
и соединение формулы (1) не является (цис, цис)-(1RS, 3RS)-1,3-дифенилиндан-2-карбоновой кислотой;
1,3-дифенил-2-метилинданом;
1,3-дифенилинданом;
1,3-бис(4,5-диметокси-2-гидроксифенил)-5,6-диметоксиинданом;
1,3-бис(3,4-диметоксифенил)-5,6-диметоксиинданом;
и также при условии, что исключаются соединения, где R1 представляет -X(CH2)nAr или -X(CH2)nR8 или
R2 представляет водород,
P1 представляет -X(CH2)nR8;
P2 представляет -X(CH2)nR8;
R3 и R5 представляют независимо водород, R11, OH, C1-8-алкокси, или -X(CH2)nR8, где метиленовые группы в -X(CH2)nR8 могут быть незамещенными или замещены одной или несколькими группами -(CH2)nAr;
R4 представляет водород, -X(R11), C1-5-алкокси, который может быть замещен OH;
R6 представляет водород или C1-4-алкил;
R7 представляет водород, C1-6-алкил или -(CH2)nAr;
R8 представляет R11, CO2H или P(O)(OH)R7;
R10 представляет R3 или R4;
R11 представляет C1-8-алкил, C2-8-алкенил, C2-8-алкинил все из которых могут быть незамещенными или замещены одним или несколькими OH или галогеном;
X представляет (CH2)n или 0;
Y представляет CH3;
Ar представляет

или пиридил, которые могут быть незамещенными или замещенными одной или несколькими группами R3 или R4;
A представляет [C(R6)2]m;
B представляет -O-;
Z1 и Z2 представляют независимо водород, или C1-8-алкокси, Z3 представляет Z1 или -X-R9-Y;
n равно целому числу от 0 до 6;
m равно 1, 2 или 3,
или их фармацевтически приемлемые соли.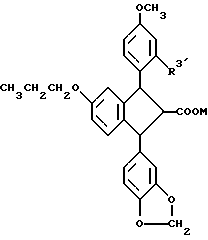
где R3'означает -OCH2COOH; M означает H и соединение является (+) (1RS, 2SR, 3SR) изомером;
R3'означает OCH2CH2OH; M означает H и соединение является (+) (1RS, 2RS, 3SR) изомером;
R3' означает
М означает Na и соединение является (1RS, 2RS, 3SR) изомером,
или его фармацевтически приемлемая соль.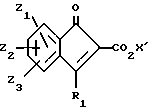
где Z, Z2, Z3 и R1 являются такими, как описано в п.1, или способной к превращению в них группами,
x' представляет алкил,
с магнийорганическим соединением формулы III
R2-(CH2)n-MgBr
где R2 является таким, как описано в п.1, или группой, способной к превращению в него,
в подходящем растворителе с образованием соединения формулы IV
которое восстанавливают и затем, если желательно или необходимо, подвергают а) введению R10 (иного, чем водород) через присоединение по двойной связи; и/или b) алкилированию или ацилированию с образованием соединений, в которых P1 и P2 иные, чем CO2H; и/или c) преобразованию R1, R2, Z1, Z2 и Z3 обычными способами, такими, как алкилирование, ацилирование, восстановление, с получением соединения формулы I.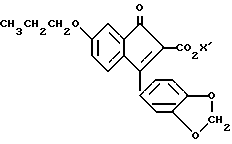
где Х' представляет алкил,
с магнийорганическим соединением формулы III
R3' является таким, как описано в п.4, или группой, способной к превращению в него,
в подходящем растворителе с образованием соединения формулы IV
которое восстанавливают и затем гидролизуют.
| US 3737455 A, 1977 | |||
| Способ получения производных бензодиоксола | 1973 |
|
SU507232A3 |
| ШТАНГОВЫЙ ТРАНСПОРТЕР | 0 |
|
SU206241A1 |
Авторы
Даты
1999-05-27—Публикация
1994-04-26—Подача