Изобретение относится к области синтеза гетероциклических соединений, которые могут быть использованы в качестве активаторов низкотемпературного перекисного беления.
Реакция ацилирования 5,5-диметилгидантоина приводит к получению двух изомеров, различающихся положением ацетильной группы [1]: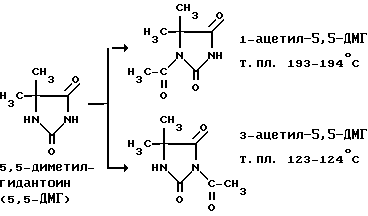
Более стабильным является изомер с т.пл. 193 - 194oC. Он не отщепляет ацетильную группу даже при нагревании в водных щелочных растворах. Изомер с т. пл. 123 - 124oC нестабилен, он легко гидролизуется водой с отщеплением ацетильной группы уже при комнатной температуре [Salmon M.R., Kozlowski A.Z. J. Am. Chem. Soc. 1945, v 67, N 12, p. 2270 - 2271].
Легкая гидролизуемость, а также особенности структуры 3-ацетил-5,5-ДМГ придают ему свойства активатора низкотемпературного перекисного беления. Как известно, добавление активатора к неорганическим перекисным отбеливателям позволяет снизить температуру обработки текстильных изделий при белении или стирке до 50 - 60oC [авт. св. N СССР 1565926 по заявке N 4268126/05, опубл. в Б.И. 1990, N 19; авт. св. N СССР 1689477 по заявке N 4444748/04, опубл. в Б.И. 1991, N 41.
Изомер с т.пл. 193 - 194oC свойствами активатора не обладает. Добавление же его в качестве примеси к изомеру с т.пл. 123 - 124oC заметно снижает эффективность последнего как активатора.
Поэтому особый интерес представляет разработка такого способа ацилирования 5,5-ДМГ, при котором образуется только изомер с т.пл. 123 - 124oC.
Согласно литературным данным основным продуктом ацилирования 5,5-ДМГ является стабильный изомер - 1-ацетил-5,5-ДМГ. Так, при ацилировании 5,5-ДМГ уксусным ангидридом при мольном соотношении реагентов 1:10 в течение 1 часа при температуре кипения реакционной смеси (≈ 140oC) образуется изомер с т. пл. 192oC (Biltz H., Slotta K. J. pract Chem. 1926, bd 113, s 233 - 267). Ацилирование 5,5-ДМГ уксусным ангидридом при комнатной температуре в течение трех суток также приводит к получению соединений с т.пл. 193 - 195oC (Ellstad G. A. , Cosulich D.B., Broschard R.W., J. Chem. Soc 1978, v 100, p 2515 - 2524). В работе Umemoto S, Yakugaki Zaschi, 1964, v 84, N 6, p 509 - 512 при ацилировании 5,5-ДМГ ацетилхлоридом в бензоле при температуре кипения получают смесь 20% 3-ацетил- и 80% 1-ацетил-ДМГ. В работе имеются данные о том, что в условиях, описанных в работе, может получиться также изомер с т.пл. 123 - 124oC.
Из уровня техники видно, что при ацилировании 5,5-ДМГ изомер 3-ацетил-5,5-ДМГ или не образуется совсем, или получается в виде смеси с 1-ацетил-5,5-ДМГ.
Наиболее близким техническим решением, выбранным в качестве прототипа Buchener H. Th. , Steiner W. J. pract Chem, 1934, bd 140, N 19-12, s 291 - 316 является способ получения изомера с т.пл. 123 - 124oC взаимодействием 5,5-ДМГ с уксусным ангидридом при мольном соотношении 5,5-ДМГ: уксусный ангидрид, равном 1:10 при температуре кипения (≈140oC) в течение 15 - 30 мин. Авторы отмечают, что параллельно образуется и второй изомер с т.пл. 183 - 187oC. Полученные авторами данные говорят о том, что указанным способом были получены 3-ацетил-5,5-ДМГ (т.пл. 123 - 124oC) и загрязненный примесями 1-ацетил-5,5-ДМГ (т.пл. 183 - 187oC).
Недостатком данного способа является получение 3-ацетил-5,5-ДМГ не в чистом виде, а с примесью 1-ацетил-5,5-ДМГ.
Техническим результатом заявляемого способа является повышение качества 3-ацетил-5,5-ДМГ, то есть получение его в чистом виде, не загрязненного примесью 1-ацетил-5,5-ДМГ.
Указанный технический результата достигается тем, что 3-ацетил-5,5-ДМГ получают взаимодействием 5,5-ДМГ с уксусным ангидридом при температуре 110 - 120oC и мольным соотношением 5,5-ДМГ:уксусный ангидрид 1:3 - 1:5.
Сопоставительный анализ с прототипом позволяет сделать вывод, что заявляемый способ получения 3-ацетил-5,5-ДМГ отличается от известного тем, что реакция проводится не при температуре кипения реакционной смеси, а при 110 - 120oC, и при использовании значительно меньшего избытка уксусного ангидрида.
Проведение реакции в мягких условиях, то есть при температуре 110 - 120oC, а не при температуре кипения, позволяет исключить образование второго изомера - 1-ацетил-5,5-ДМГ. Дальнейшее понижение температуры проведения реакции приводит к неполному ацилированию 5,5-ДМГ, то есть к загрязнению продукта реакции непрореагировавшим исходным соединением. Повышение температуры реакции выше 120oC сопровождается образованием второго изомера (1-ацетил-5,5-ДМГ), количество которого растет и достигает 100% при проведении реакции при температуре кипения (≈ 140oC).
Уменьшение избытка уксусного ангидрида, по сравнению с заявляемым условием, также приводит к неполному ацилированию, а увеличение избытка - к снижению выхода 3-ацетил-5,5ДМГ за счет частичного растворения продукта реакции в увеличенной по объему реакционной массе.
Кроме того косвенным подтверждением преимущества заявляемого способа служит значительно меньший выход продукта реакции при использовании соотношений исходных веществ прототипа (таблица, оп. 7), то есть при большем избытке уксусного ангидрида, чем в заявляемых условиях.
Заявляемый способ получения 3-ацетил-5,5-ДМГ осуществляется следующим образом.
Пример 1.
В реактор емкостью 0,010 л, снабженный мешалкой со скоростью вращения 100 мин-1, помещают 10 г (0,078 моля) 5,5-диметилгидантоина и 32 г (0,312 моля) уксусного ангидрида (мольное соотношение 1:4). Реакционную массу нагревают при перемешивании в течение 1 часа при температуре 110oC. Затем смесь охлаждают до комнатной температуры. При этом выпадает белый кристаллический осадок 3-ацетил-5,5-диметилгидантоина. После фильтрации и сушки продукт перекристаллизовывают из хлороформа. Качество продукта контролируется по температуре плавления.
Температуры плавления сравниваемых изомеров определялись известным способом [Лабораторные работы по органической химии. /Под ред. О.Ф. Гинзбурга и А.А. Петрова. - М.: Высшая школа, 1974, с. 48 - 50].
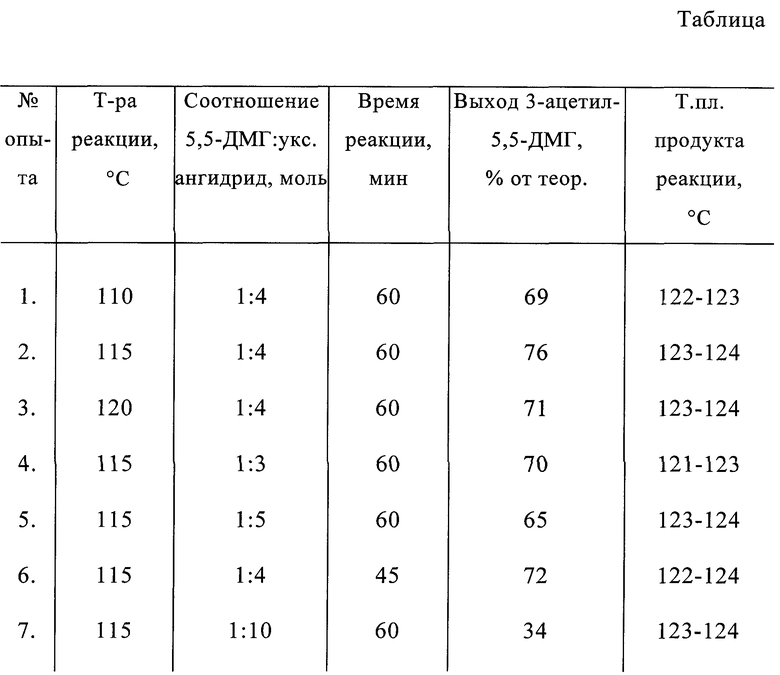
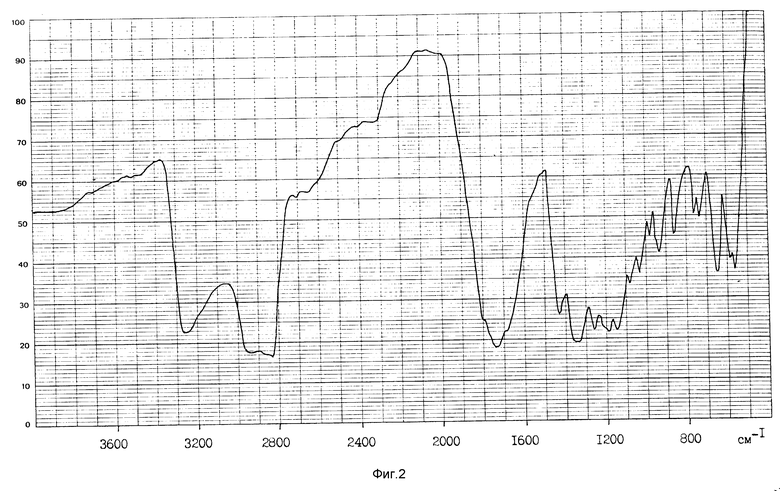
Идентификация полученных соединений проводилась методом ИК-спектроскопии. ИК-спектры регистрировались на спектрофотометре Specord 75 IR. При записи спектров суспензий в вазелиновом масле концентрация исследуемых веществ обычно составляла ≈ 2 моль/л (см. фиг. 1-3).
Примеры конкретного осуществления способа получения 3-ацетил-5,5-ДМГ сведены в таблицу.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 1,2,4-ТРИАЗОЛОНА-5 | 1992 |
|
RU2085556C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ТЕКСТИЛЬНОГО КАТАЛИЗАТОРА НА ПОДЛОЖКЕ ИЗ СТЕКЛОВОЛОКОН | 1998 |
|
RU2134613C1 |
| СПОСОБ ПОЛУЧЕНИЯ РАСТВОРА СВЕРХВЫСОКОМОЛЕКУЛЯРНОГО ПОЛИЭТИЛЕНА | 1997 |
|
RU2121483C1 |
| СОРБЦИОННО-АКТИВНЫЙ МАТЕРИАЛ ДЛЯ ОЧИСТКИ ВОДЫ ОТ НЕФТЕПРОДУКТОВ | 1999 |
|
RU2158177C1 |
| СПОСОБ ПОЛУЧЕНИЯ АНТИМИКРОБНОЙ КОМПОЗИЦИИ И НАБОР ДЛЯ ЕЕ ПОЛУЧЕНИЯ | 2009 |
|
RU2408388C1 |
| КОМПОЗИЦИЯ ДЛЯ КРАШЕНИЯ МАТЕРИАЛОВ НА ОСНОВЕ АРОМАТИЧЕСКИХ ГЕТЕРОЦИКЛИЧЕСКИХ ВОЛОКОН | 1999 |
|
RU2158793C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИЭФИРА | 1999 |
|
RU2167892C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИС-1,2-(1,2,4-ТРИАЗОЛ-1-ИЛ)ЭТАНА | 1997 |
|
RU2141955C1 |
| СПОСОБ КОНДИЦИОНИРОВАНИЯ ПИТЬЕВОЙ ВОДЫ | 1998 |
|
RU2129994C1 |
| СПОСОБ ПОЛУЧЕНИЯ РАСТВОРОВ ЦЕЛЛЮЛОЗЫ | 2000 |
|
RU2184750C2 |
Изобретение относится к области синтеза гетероциклических соединений, которые могут быть использованы в качестве активаторов низкотемпературного перекисного беления. Техническим результатом заявляемого способа является повышение качества 3-ацетил-5,5-диметилгидантоина, то есть получение его в чистом виде, не загрязненного примесью 1-ацетил-5,5-диметил-гидантоина. Указанный технический результат достигается тем, что 3-ацетил-5,5-диметилгидантоин получают взаимодействием 5,5-диметилгидантоина с уксусным ангидридом при температуре 110-120oС и мольном соотношении 5,5-диметилгидантоин : уксусный ангидрид 1:3-1:5. 1 табл., 3 ил.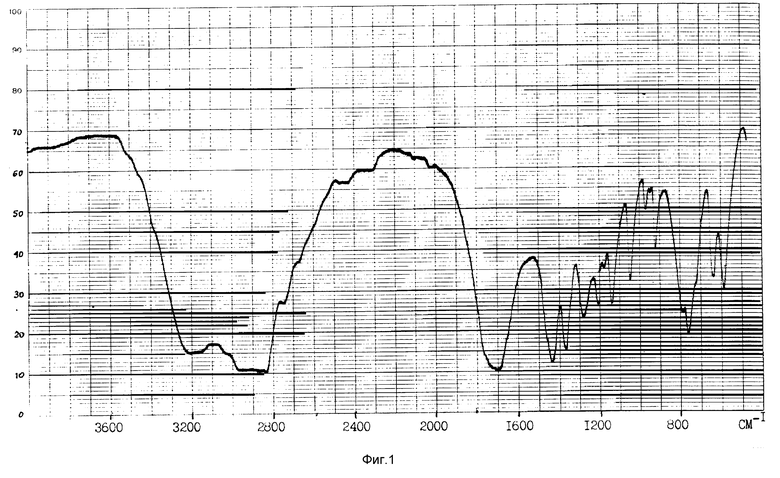
Способ получения 3-ацетил-5,5-диметилгидантоина путем взаимодействия 5,5-диметилгидантоина и уксусного ангидрида, отличающийся тем, что реакцию взаимодействия ведут при температуре 110 - 120oC и мольном соотношении 5,5-диметилгидантоин: уксусный ангидрид 1:3-1:5.
| Способ получения производных имидазола или их солей | 1980 |
|
SU999966A3 |
| Bucherer H | |||
| Gh., Steiner W, J | |||
| Приспособление к рогульчатым ватерам для торможения катушки | 1924 |
|
SU1934A1 |
| СТЕРЕООЧКИ | 1920 |
|
SU291A1 |
Авторы
Даты
1999-06-20—Публикация
1998-06-04—Подача