Изобретение относится к области органической химии, в частности к способу получения производных 3-азабицикло[3.3.1]нонана.
Азааналоги бицикло[3.3.1]нонана являются промежуточными продуктами органического синтеза и применяются в качестве биологически активных веществ [Зефиров Н. С. , Рогозина С.В.// Усп. хим. 1973. Т.42. Вып. 3. С. 423-441]. Подобные системы служат также удобными моделями для конформационного анализа [Зефиров Н.С.// Усп.хим. 1975. Т. 44 Вып. 3. С. 413-444].
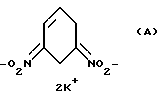
Одной из типовых реакций, используемых в синтезе бициклононановых структур, является реакция Манниха [Зефиров Н.С., Рогозина С.В.// Усп. хим. 1973. Т. 42. Вып. 3. С. 423-441]. Предлагаемый способ получения производных 3-азабицикло[3.3.1] нонана включает в себя восстановление м-динитробензола (м-ДНБ) тетрагидроборатом калия до дикалиевой соли 3,5-бис(аци-нитро)циклогексена-1 (А), которая затем подвергается аминометилированию.
Использование формальдегида и первичных аминов позволяет получать 1,5-динитро-3-R-3-азабицикло[3.3.1] нонены-6 (I a-e). Введение в реакцию Манниха первичных диаминов позволяет синтезировать соединения (I ж-и), содержащие два бициклононеновых фрагмента (схема).
Состав и строение полученных оснований Манниха подтверждены данными ИК и ПМР спектроскопии, а также результатами элементного анализа.
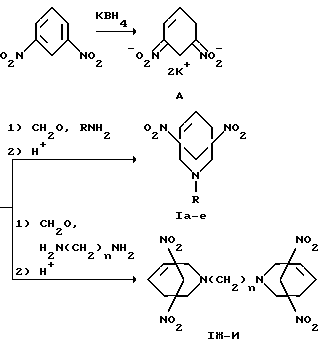
R=C2H5(a), CH2CH2OH(б), CH2CH2Br(в), CH2Ph(г), CH2COOH(д), CH(C2H5)CH2OH(е); N=2(ж), 4 (з), 6(и).
Отличительной особенностью предлагаемого метода синтеза является селективное восстановление ароматического кольца м-ДНБ под действием тетрагидробората калия, ведущее к образованию дикалиевой соли 3,5-бис(аци-нитро)циклогексена-1, которая далее используется для конденсации по Манниху. Вследствие низкой растворимости KBH4 в органических растворителях восстановление м-ДНБ проводится в смеси тетрагидрофуран (ТГФ) - вода.
Сущность метода заключается в следующем. К раствору м-ДНБ в смесь ТГФ-H2O (1:1) при перемешивании и охлаждении в течение 15 мин добавляют двукратный избыток твердого KBH4 (по отношению к стехиометрическому количеству) и перемешивают еще 15 мин. Температуру реакционной смеси все время поддерживают в пределах 5-15oC. Затем приливают охлажденную смесь водных растворов формальдегида и первичного амина (или гидрохлорида, гидробромида или ацетата амина), взятых также в двукратном избытке, после чего реакционный раствор подкисляют ледяной уксусной кислотой до pH 6. Продукт экстрагируют дихлорметаном, экстракт промывают водой, сушат над хлоридом кальция и отгоняют растворитель. Остаток хроматографируют на колонке с силикагелем (элюент - толуол). Далее соединение очищают, как указано в примерах.
Пример 1. 1,5-динитро-3-этил-3-азабицикло[3.3.1]нонен-6 (Ia).
К раствору 4 ммоль (0,67 г) м-ДНБ в 10 мл смеси ТГФ-H2O (1:1) при перемешивании и охлаждении в течение 15 мин добавляют 16 ммоль (0,86 г) KBH4 и перемешивают еще 15 мин. Температуру реакционной смеси поддерживают в пределах 5-15oC. После окончания восстановления приливают охлажденный раствор 16 ммоль формальдегида (1,5 мл 30% формалина) и 8 ммоль (0,65 г) гидрохлорида этиламина в 20 мл воды и подкисляют ледяной уксусной кислотой до pH 6. Проводят экстракцию дихлорметаном (3 х 15 мл), экстракт упаривают, остаток хроматографируют на колонке с силикагелем (АСКГ) (элюент - толуол), затем растворяют в 15 мл этанола, добавляют немного активированного угля, кипятят 1 - 2 мин и фильтруют. Целевой продукт высаждают из охлажденного фильтрата путем добавления воды.
Т.пл. 39-49oC, выход 51%.
Найдено, %: C 50,7, H 6,3, N 17,5.
Вычислено, %: C 49,8, H 6,3, N 17,4.
ИК-спектр, ν: 3455, 2840, 3000, 1640, 1555, 1345 см-1.
Спектр ПМР, δ, м.д.: 0,50 т, 1,60-2,80 м, 5,13 д.т, 5,55 д.д.д.
Аналогично получают соединения I г, е.
1,5-динитро-3-бензил-3-азабицикло[3.3.1.]нонен-6 (I г).
Т.пл. 43-44oC, выход 50%.
Найдено, %: C 59,2, H 5,6, N 14,5.
Вычислено, %: C 59,4, H 5,7, N 13,9. И
ИК-спектр, ν: 3040, 2840, 1640, 1560, 1355 см-1.
Спектр ПМР, δ, м.д.: 1,65-2,80 м, 2,95 с, 5,15 д.т, 5,50 д.д.д, 6,89-7,10 м.
2-(1,5-динитро-3-азабицикло[3.3.1]нон-6-ен-3-ил)бутанол-2 (I e).
Т.пл. 68-69oC, выход 59%.
Найдено, %: C 50,5, H 6,8, N 15,3.
Вычислено, %: C 50,5, H 6,7, N 14,7.
ИК-спектр, ν: 3480, 2855, 2935, 1635, 1560, 1350 см-1.
Спектр ПМР, δ, м.д.: 0,30-0,80 м, 1,60-3,30 м, 5,06 д.т, 5,50 д.д.д.
Пример 2. 2-(1,5-динитро-3-азабицикло[3.3.1]нон-6-ен-3-ил)-этанол (I б).
К раствору 4 ммоль (0,67 г) м-ДНБ в 10 мл смеси ТГФ-H2O (1:1) при перемешивании и охлаждении в течение 15 мин добавляют 16 ммоль (0,86 г) KBH4 и перемешивают еще 15 мин. Температуру реакционной смеси поддерживают в пределах 5 - 15oC. После окончания восстановления приливают охлажденный раствор 16 ммоль формальдегида (1,5 мл 30% формалина) и 8 ммоль (0,78 г) гидрохлорида моноэтаноламина в 20 мл воды и подкисляют ледяной уксусной кислотой до pH 6. Проводят экстракцию дихлорметаном (3х15 мл), экстракт упаривают, остаток хроматографируют на колонке с силикагелем (АСКГ) (элюент - толуол), затем кристаллизуют из этанола.
Т.пл. 105-106oC, выход 52%.
Найдено, %: C 47,2, H 5,9, N 16,4.
Вычислено, %: C 46,7, H 5,9, N 16,3.
ИК-спектр, ν: 3455, 2970, 2890, 2825, 1655, 1555, 1355 см-1.
Спектр ПМР, δ, м.д.: 1,55 ш.с, 1,60-2,80 м, 3,05 т, 5,43 д.т, 5,00 д.д. д.
Аналогично получают соединения I в,д.
1,5-динитро-3-(2-бромэтил)-3-азабицикло[3.3.1]нонен-6 (Iв).
Т.пл. 78-79oC, выход 25%.
Найдено, %: C 37,4, H 4,2, N 13,7.
Вычислено, %: C 37,5, H 4,4, N 13,1.
ИК-спектр, ν: 2845, 2950, 1655, 1555, 1350 см-1.
Спектр ПМР, δ, м.д.: 1,55-2,60 ш.с, 5,10 д.т, 5,45 д.д.д.
(1,5-динитро-3-азабицикло[3.3.1]нон-6-ен-3-ил)уксусная кислота (I д).
Т.пл. 162-163oC, выход 44%.
Найдено, %: C 45,1, H 4,7, N 15,2.
Вычислено, %: C 44,3, H 4,8, N 15,5.
ИК-спектр, ν: 3300 - 2500, 2855, 2905, 2970, 1755, 1660, 1560, 1355 см-1.
Спектр ПМР, δ, м.д.: 1,70-2,50 м., 5,00 д.т, 5,38 д.д.д.
Пример 3. 1,2-бис(1,5-динитро-3-азабицикло[3.3.1]нон-6-ен-3-ил)этан (I ж).
К раствору 4 ммоль (0,67 г) м-ДНБ в 10 мл смеси ТГФ -H2O (1:1) при перемешивании и охлаждении в течение 15 мин добавляют 16 ммоль (0,86 г) KBH4 и перемешивают еще 15 мин. Температуру реакционной смеси поддерживают в пределах 5-15oC. После окончания восстановления приливают охлажденный раствор 16 ммоль формальдегида (1,5 мл 30% формалина) и 4 ммоль (0,57 г) гидробромида этилендиамина в 20 мл воды и подкисляют ледяной уксусной кислотой до pH 6. Проводят экстракцию дихлорметаном (3х15 мл), экстракт упаривают, остаток хроматографируют на колонке с силикагелем (АСКГ) (элюент - толуол), затем растворяют в 10 мл ацетона и высаживают путем добавления этанола.
Т.пл. 246-248oC (с разл.), выход 14%.
Найдено, %: C 48,1, H 5,4, N 18,8.
Вычислено, %: C 47,8, H 5,3, N 18,6.
ИК-спектр, ν: 2820, 2935, 1635, 1555, 1355 см-1.
Спектр ПМР, δ, м.д.: 1,50-2,70 м, 5,20 д.т, 5,50 д.д.д.
Аналогично получают соединения I з, и.
1,4-бис(1,5-динитро-3-азабицикло[3.3.1]нон-6-ен-3-ил)бутан (Iз).
Т.пл. 179 - 180oC, выход 25%.
Найдено, %: C 50,0, H 5,8, N 17,4.
Вычислено, %: C 50,0, H 5,9, N 17,5.
ИК-спектр, ν: 2960, 2840, 1635, 1555, 1360 см-1.
Спектр ПМР, δ, м.д.: 0,68 - 0,95 м., 1,48 - 2,80 м., 5,20 д.т., 5,59 д. д.д.
1,2-бис(1,5-динитро-3-азабицикло[3.3.1]нон-6-ен-3-ил)гексан (Iи).
Т.пл. 111-112oC, выход 28%.
Найдено, %: C 52,7, H 6,2, N 16,6.
Вычислено, %: C 52,0, H 6,3, N 16,5.
ИК-спектр, ν: 2945, 2835, 1635, 1540, 1360 см-1.
Спектр ПМР, δ, м.д.: 0,90 ш.с., 1,60-2,90 м., 5,15 д.т., 5,60 д.д.д.
ИК-спектры (таблетки KBr) записаны на спектрофотометре UR-20. Спектры ПМР записаны на спектрометре JMN FX-90 Q (90 МГц) в бензоле-d6, внутренний стандарт-ГМДС.
Таким образом, предлагаемый метод синтеза бициклических соединений исходя из м-динитробензола является новым способом получения производных 3-азабицикло[3.3.1]нонана.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 3-АЗАБИЦИКЛО[3.3.1]НОНАНА | 1999 |
|
RU2174117C2 |
| СПОСОБ ПОЛУЧЕНИЯ 6(7)-R-1,5-ДИНИТРО-3-(2-ГИДРОКСИЭТИЛ)-3-АЗАБИЦИКЛО(3.3.1)-НОНЕНОВ-6 | 1999 |
|
RU2159766C1 |
| СПОСОБ ПОЛУЧЕНИЯ АМИНОКИСЛОТ, СОДЕРЖАЩИХ 3-АЗАБИЦИКЛО(3.3.1)НОНАНОВЫЙ ФРАГМЕНТ | 1999 |
|
RU2159767C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 3-НИТРОАЗОБЕНЗОЛА | 1997 |
|
RU2140906C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФТОРСОДЕРЖАЩИХ ПРОИЗВОДНЫХ 3-АЗАБИЦИКЛО/3.3.1/НОНАНА | 1999 |
|
RU2174118C2 |
| ЙОДИД N-МЕТИЛ-N,N-ДИЭТИЛ-N-[β-(2,4-ДИАМИНОФЕНОКСИ)ЭТИЛ] АММОНИЯ КАК МОНОМЕР ДЛЯ СИНТЕЗА ВЫСОКОМОЛЕКУЛЯРНЫХ ПОЛИАМИДОВ И СОПОЛИАМИДОВ, СОДЕРЖАЩИХ АНИОНООБМЕННЫЕ ГРУППЫ | 1992 |
|
RU2119910C1 |
| СПОСОБ ПОЛУЧЕНИЯ 6,8,10-ТРИНИТРО-1,4-ДИОКСАСПИРО[4,5]-ДЕКА-6,9-ДИЕНАТОВ КАТИОНОВ P, D И F-ЭЛЕМЕНТОВ | 1994 |
|
RU2133250C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-(n-R-ФЕНИЛАЗО)-3-НИТРОНАФТАЛИНОВ | 1998 |
|
RU2163611C2 |
| ГИДРОХЛОРИД 3-(2-ГИДРОКСИЭТИЛ)-1,5-ДИНИТРО-3-АЗАБИЦИКЛО[3.3.1]НОН-6-ЕНА, ПРОЯВЛЯЮЩИЙ АНТИАРИТМИЧЕСКУЮ АКТИВНОСТЬ | 2002 |
|
RU2228334C2 |
| АМИДОАЛКАНОЛНИТРАТЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1998 |
|
RU2147301C1 |
Описывается новый способ получения новых производных 3-азабицикло/3,3,1/нонана общей формулы I, где R=C2H5, CH2CH2OH, CH2CH2Br, CH2Ph, CH2COOH, CH(C2H5)CH2OH или 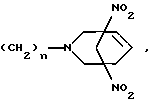 где n = 2, 4 или 6, с использованием реакиии Манниха. Исходный м-динитробензол восстанавливают с помощью КВН4 до дикалиевой соли 3,5-бис(аци-нитро)циклогексена-1 формулы А, на которую действуют смесью формальдегида и первичного амина с последующим подкислением реакционного раствора уксусной кислотой до рН 6, и получают соединения формулы I, где R= C2H5, CH2CH2OH, CH2CH2Br, CH2Ph, CH2COOH, CH(C2H5)CH2OH, или действуют смесью формальдегида и диамина с последующим подкислением реакционного раствора уксусной кислотой до рН 6 и получают соединения формулы I, где
где n = 2, 4 или 6, с использованием реакиии Манниха. Исходный м-динитробензол восстанавливают с помощью КВН4 до дикалиевой соли 3,5-бис(аци-нитро)циклогексена-1 формулы А, на которую действуют смесью формальдегида и первичного амина с последующим подкислением реакционного раствора уксусной кислотой до рН 6, и получают соединения формулы I, где R= C2H5, CH2CH2OH, CH2CH2Br, CH2Ph, CH2COOH, CH(C2H5)CH2OH, или действуют смесью формальдегида и диамина с последующим подкислением реакционного раствора уксусной кислотой до рН 6 и получают соединения формулы I, где 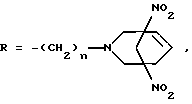 где n = 2, 4 или 6. Способ позволяет получить новые соединения с ценными свойствами.
где n = 2, 4 или 6. Способ позволяет получить новые соединения с ценными свойствами. 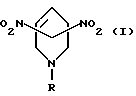
Способ получения производных 3-азабицикло [3.3.1]нонана общей формулы I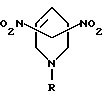
где R - C2H5, CH2CH2OH, CH2CH2Br, CH2Ph, CH2COOH, CH(C2H5)CH2OH или 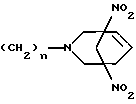
где n = 2, 4 или 6,
с использованием реакции Манниха, отличающийся тем, что исходный м-динитробензол восстанавливают с помощью КВН4 до дикалиевой соли 3,5-бис(аци-нитро)циклогексена-1 формулы А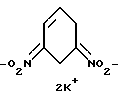
на которую действуют смесь формальдегида и первичного амина, с последующим подкислением реакционного раствора уксусной кислотой до рН 6 и получают соединения формулы I, где R - С2Н5, CH2CH2ОН, CH2CH2Br, CH2Ph, CH2COOH, CH(C2H5)CH2OH или действуют смесью формальдегида и диамина с последующим подкислением реакционного раствора уксусной кислотой до рН 6 и получают соединения формулы I, где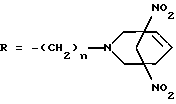
где n = 2, 4 или 6.
| Способ получения азабициклооктанкарбоновых кислот в виде рацематов или оптического изомера,или их солей | 1981 |
|
SU1138022A3 |
| Зефиров Н.С | |||
| и др | |||
| Успехи химии, 1973, т.42, вып.3, с | |||
| Самоцентрирующийся лабиринтовый сальник | 1925 |
|
SU423A1 |
| Зефиров Н.С | |||
| и др | |||
| Успехи химии, 1975, т | |||
| Приспособление для плетения проволочного каркаса для железобетонных пустотелых камней | 1920 |
|
SU44A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| СТАНОК ДЛЯ ИЗГОТОВЛЕНИЯ ГАЛЕЙ | 1923 |
|
SU413A1 |
Авторы
Даты
1999-07-10—Публикация
1997-12-15—Подача