Изобретение относится к медицине, в частности к производству вирусных вакцинных препаратов и касается создания новой липосомальной формы живой коревой вакцины.
Известна липосомальная форма гриппозной вакцины [1]. Липосомы готовят как из синтетических (дистеароилфосфатидилхолин, дипальмитоилфосфатидилхолин и др.), так и природных (сфингомиелин) фосфохолин-содержащих липидов. Липиды смешивают, высушивают в вакууме, эмульгируют препаратом вируса группа, проводят диализ и обрабатывают ультразвуком. Такой способ заключения вируса и липосомы не пригоден для вируса кори, так как продолжительный диализ и озвучивание разрушают его. В то же время такой состав липосом в настоящее время не пригоден для отечественных вакцин, так как эти синтетические липиды не разрешены для клинического применения в России.
Известно получение пероральной липосомальной вакцины, содержащей НА-антиген вируса гриппа. Липиды смешивают, высушивают в вакууме, гидратируют раствором НА-антигена гриппа, смесь перемешивают до получения многослойных липосом. Продукт разбавляют до концентрации 1:3,5 (PBS) фосфатно-солевым буферным раствором для получения пероральной липосомальной вакцины, содержащей НА-антиген гриппа. Такой способ отличается от предлагаемого по составу (дистеароилфосфатидилхолин, гидрированный фосфатидилсерин соевых бобов и холестерин) и общему количеству используемых липидов (160 мг/мл); по их соотношению (1: 1: 2) и температурному режиму. Увеличение количества липидов в составе препарата делает процесс приготовления препарата более сложным и дорогим, а сам препарат менее стандартизованным, температурный режим (37oC) приводит к потере инфекционного титра вируса кори [2].
Известен способ получения живой коревой вакцины (ЖКВ) на основе различных вакцинных штаммов вируса кори для парентерального применения. Способ включает культивирование вируса на культуре фибробластов эмбрионов японских перепелов, сбор вируссодержащей жидкости, введение стабилизатора, ампулирование и лиофилизацию. Перед применением вакцину разводят растворителем. Специфическая активность ЖКВ составляет 3,3-4,0 lg ТЦД50/0,5 мл [3,4].
Недостатком известного способа является инъекционная форма применения ЖКВ, что создает угрозу заражения вирусами гепатитов и ВИЧ при вакцинации, инфицирование раны, стрессирование детей в процессе вакцинации. Указанная вакцина содержит помимо протективных антигенов и другие вирусные белки, а также остаточные компоненты сыворотки крупного рогатого скота, которые могут вызывать анафилактогенные реакции [5].
Задачей предлагаемого изобретения является получение живой коревой вакцины для перорального применения, обладающей выраженными иммуногенными свойствами, сравнимыми с коммерческим препаратом ЖКВ [4], но лишенной указанных выше недостатков, присущих инъекционной форме.
Указанная задача решается путем создания вакцины для перорального применения, заключенной в липосомы, где в качестве активного компонента используют жидкую форму ЖКВ, содержащую вакцинный штамм вируса кори, липосомы формируют из смеси фосфатидилхолина и холестерина (отечественного производства) в молярном отношении 7:3. Яичный лецитин (фосфатидилхолин) в виде 10%-ного спиртового раствора и холестерин (растворенный в следовых количествах хлороформа) смешивают, упаривают под вакуум в роторном испарителе до получения тонкой, сухой пленки на стенках колбы, пленку досушивают продуванием (для предотвращения окисления липидов) инертного газа (азот, аргон) и гидратируют добавлением жидкой формы живой коревой вакцины. Смесь встряхивают на шейкере при температуре 15-17oC до полного эмульгирования липидной пленки. Суспензию липидов с конечной концентрацией 100 мг/мл подвергают формирующей и стерилизующей фильтрации через поликарбонатные мембраны с диаметром пор 1-0,2 мкм под давлением инертного газа. Вакцина содержит культуральную вируссодержащую жидкость со специфической активностью не менее 3,3 lg ТЦД50/0,5 мл, в качестве стабилизатора используют смесь желатозы с сорбитом в соотношении 1: 1 и не менее 10% от полуфабриката ЖКВ, причем вируссодержащую жидкость со стабилизатором смешивают с фосфатидилхолином и холестерином для получения липосомальной формы для перорального применения при следующем количественном соотношении компонентов, мг/мл:
Фосфатидилхолин - 80 - 100
Холестерин - 12 - 20
Существенными признаками изобретения являются создание новой формы ЖКВ для перорального применения, количественные соотношения компонентов, обеспечивающие возможность получения стабильного препарата липосомальной формы ЖКВ для перорального применения. Концентрация фосфатидилхолина менее 80 мг/мл приводит к падению титра вируса кори, а при увеличении его более 100 мг/мл не отмечается значительного повышения стабильности вируса кори. Уменьшение соотношения между количеством фосфатидилхолина и холестерина ведет к ухудшению образования липосом, так как происходит створаживание, а увеличение этого соотношения ведет к получению нестабильной липосомальной формы ЖКВ (происходит вытекание препарата из липосом).
Заявленная форма липосомальной живой коревой вакцины для перорального применения позволяет получить сравнимую иммуногенность сходных доз с живой коревой вакциной, вводимой подкожно. Кроме того, применение новой липосомальной формы ЖКВ позволяет избежать инфицирования при проведении инъекций и заражения вирусами гепатитов и ВИЧ.
Заявляемая совокупность признаков неизвестна из литературных источников, впервые получена экспериментальным путем, позволяет сделать заключение о соответствии технического решения критериям "изобретательский уровень" и "новизна".
Иммунизацию организма против кори осуществляют путем введения пероральной липосомальной формы вакцины в дозе 20000 ТДЦ50 вируса кори. Иммуногенные свойства проверяют исследуя сыворотки крови в ИФА и в реакции торможения гемагглютинации (РТГА), определяя наличие антител к вирусу кори. Исследование иммуногенных свойств показывает, что образование противокоревых антител вызывает как живая коревая вакцина, вводимая подкожно, так и липосомальная ее форма, применяемая перорально.
Заявляемый способ иммунизации неизвестен из литературных источников, позволяет сделать заключение о соответствии технического решения критериям "изобретательский уровень" и "новизна".
Примеры конкретного применения
Пример 1. Получение жидкой формы коревой вакцины, пригодной для заключения в липосомы.
Для получения вакцины используют первичную культуру клеток фибробластов эмбрионов японских перепелов (ФЭП). В качестве ростовой среды используют среду Игла МЕМ или среду 199 с добавлением 2-10% сыворотки КРС. В качестве вируса используют вакцинный штамм Ленинград - 16 (Л-16) вируса кори из посевного банка, аттестованного для производства иммунобиологических препаратов. Монослой клеток или суспензию заражают вирусом с множественностью заражения 0,1 - 0,001 ТЦД50/кл. При появлении выраженного цитопатического действия вируса на клетки осуществляют сбор вируссодержащих сливов через 24-48 ч (5-7 сливов). Стерильные вирусные сливы со специфической активностью не менее 4,5 lg ТЦД50/0,5 мл объединяют, добавляют стабилизатор сорбит-желатозу с конечной концентрацией 5% каждого компонента и используют для получения липосомальной формы вакцины.
Пример 2. Приготовление липосомальной формы живой коревой вакцины.
Липосомы получают способом экструзии мультиламеллярных везикул через поликарбонатные мембраны [6]. Яичный лецитин (фосфатидилхолин) в виде 10%-ного спиртового раствора (10 г) и холестерин (2 г, растворенный в следовых количествах хлороформа) смешивают в круглодонной колбе (V=200 мл). Смесь упаривают под вакуумом в роторном испарителе до получения тонкой, сухой пленки на стенках колбы. После выпаривания липидную пленку досушивают продуванием (для предотвращения окисления липидов) инертного газа (азот, аргон). Пленку гидратируют добавлением 100 мл готовой формы живой коревой вакцины (пример 2). Смесь мягко встряхивают на шейкере типа 357 (Польша) при температуре 15-17oC до полного эмульгирования липидной пленки. Суспензию липидов с конечной концентрацией 100 мг/мл подвергают формирующей и стерилизующей фильтрации через поликарбонатные мембраны с диаметром пор 1-0,2 мкм под давлением инертного газа.
Пример 3. Липосомы готовят из фосфатидилхолина и холестерина с добавкой отрицательно заряженного липида - дицетилфосфата (ДФ) в молярном отношении 7:2:1. Далее аналогично примеру 2.
Пример 4. Все операции проводят аналогично примерам 2 и 3, за исключением того, что перед получением липосомальной суспензии предварительно гидратируют липидную пленку в парах физиологического раствора в течение одного часа.
Пример 5. Определение специфической активности липосомальной формы ЖКВ.
Специфическую активность вакцины определяют по цитопатическому действию вируса на культуре клеток Vero. Для определения специфической активности вирус на липомосы извлекают в водную фазу (питательная среда, фосфатно-солевой буфер pH 7,0-7,3), после чего проводят титрование в 96-луночных планшетах на культуре клеток Vero. Специфическая активность липосомальной формы вакцины составляет 4,5 ± 0,5 lg ТЦД50/0,5 мл.
Пример 6. Иммуногенные свойства липосомальной формы живой коревой вакцины.
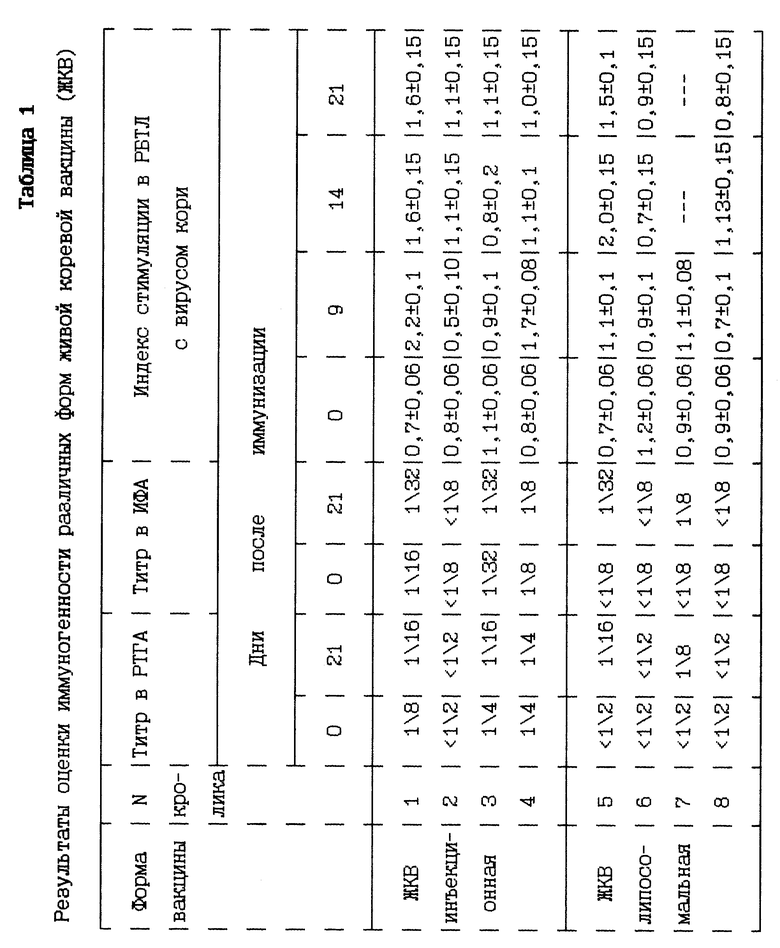
Иммуногенность липосомальной формы вакцины определяют путем пероральной иммунизации кроликов препаратом в дозе 20000 ТЦД50 вируса кори. На 0, 3, 9, 14, 21, 28 сутки после иммунизации осуществляют забор крови у животных и исследуют сыворотки крови в ИФА, РТГА на наличие специфических антител. Клеточный ответ оценивают в РБТЛ. В качестве контроля используют животных, иммунизированных подкожно живой коревой вакциной в дозе 20000 ТЦД50 вируса кори. У части животных, иммунизированных как традиционной, так и липосомальной формой ЖКВ, отмечены изменения гуморального и клеточного звеньев иммунитета (см. таблица). Из таблицы видно, что эффективность липосомальной формы ЖКВ, применяемой перорально, сравнима с эффективностью коммерческого препарата ЖКВ, применяемого подкожно.
Таким образом, липосомальная форма ЖКВ для перорального применения является перспективным препаратом для иммунизации и ревакцинации населения.
Литература
1. Патент США N 4261975, опубл. 04.14.81.
2. Заявка RU N 94040856, A 61 K 39/00, опубл. 20.08.96., "Вакцина для перорального введения".
3. Авторское свидетельство СССР N 278964, C 12 K 5/00, опубл. 1973 г., "Способ получения живой коревой вакцины".
4. Фармакопейная статья. ФС-42-3092-94, "Вакцина коревая культуральная живая сухая".
5. А.Дж.Биль Вакцины против кори. //в кн. Последние достижения в области клинической вирусологии. - 1980. - с. 230-237.
6. Olson F., Hunt C.A. - Preparation of liposomes of defined size distribution by extrusion through policarbonate membranes. Biohim. et Biophys. Acta 557, 1979, p. 9-23.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ЖИВОЙ КОРЕВОЙ ВАКЦИНЫ | 1998 |
|
RU2140288C1 |
| СПОСОБ ПОЛУЧЕНИЯ МИКРОКАПСУЛИРОВАННОЙ ФОРМЫ КОРЕВОЙ ВАКЦИНЫ ДЛЯ ПЕРОРАЛЬНОГО ПРИМЕНЕНИЯ | 2001 |
|
RU2210361C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЖИВОЙ КОРЕВОЙ ВАКЦИНЫ | 1996 |
|
RU2123331C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЖИВОЙ КОРЕВОЙ ВАКЦИНЫ | 1995 |
|
RU2112545C1 |
| ЛИПОСОМАЛЬНОЕ ПРОТИВОВИРУСНОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ПЕРОРАЛЬНОГО ПРИМЕНЕНИЯ | 1996 |
|
RU2123328C1 |
| ЖИВАЯ ВАКЦИНА ДЛЯ ПРОФИЛАКТИКИ КОРИ | 1996 |
|
RU2129876C1 |
| Способ получения микрокапсулированной формы живой культуральной вакцины против сезонного и пандемического гриппа для интраназального применения | 2016 |
|
RU2617051C1 |
| ТАБЛЕТИРОВАННАЯ ЖИВАЯ РЕКОМБИНАНТНАЯ БИВАКЦИНА "РЕВАКС ВКТ" ПРОТИВ НАТУРАЛЬНОЙ ОСПЫ И ГЕПАТИТА В И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2002 |
|
RU2242246C2 |
| ЖИВАЯ КУЛЬТУРАЛЬНАЯ КОРЕВАЯ ВАКЦИНА | 1998 |
|
RU2144369C1 |
| ВАКЦИНА ПРОТИВ ИНФЕКЦИОННОЙ БУРСАЛЬНОЙ БОЛЕЗНИ ПТИЦ | 1998 |
|
RU2127604C1 |
Изобретение предназначено для производства живой коревой вакцины. В качестве жидкой формы живой коревой вакцины (ЖКВ) используют культуральную вируссодержащую жидкость со специфической активностью не менее 3,3 lg ТЦД50/0,5 мл. ЖКВ смешивают со стабилизатором желатозой и сорбитом в соотношении 1: 1 в количестве не менее 10% от полуфабриката ЖКВ. Для получения липосомальной формы вируссодержащую жидкость и стабилизатор смешивают с фосфатидилхолином и холестерином при определенном соотношении компонентов. Полученная вакцина вводится в организм перорально в дозе не менее 20000 ТЦД50 вируса кори однократно. Вакцина сравнима по иммуногенности с коммерческой инъекционной формой ЖКВ, но не вызывает побочных явлений. 2 с.п. ф-лы, 1 табл.
Фосфатидилхолин - 80 - 100
Холестерин - 12 - 20
2. Способ иммунизации организма против кори путем введения через рот пероральной вакцины, полученной по п.1, содержащей вирус кори в составе липосом в дозе не менее 20000 ТЦД50 однократно.
| 0 |
|
SU278964A1 | |
| СПОСОБ КУЛЬТИВИРОВАНИЯ ВИРУСА КОРИ | 1994 |
|
RU2053297C1 |
Авторы
Даты
1999-07-27—Публикация
1997-07-16—Подача