Изобретение относится к биотехнологии и может найти применение при производстве коревой вакцины.
Известна вакцина для профилактики кори "Рувакс" (см. каталог препаратов фирмы "Пастер Мерье" "Сыворотки и вакцины", с. 33). В каждой дозе вакцины содержится: лиофилизат по меньшей мере 1000 DICT/50 живого аттенуированного вируса кори (штамм Шварц); стабилизатор для лиофилизации - человеческий альбумин [1].
Гиператтенуированный вакцинный вирус культивируется на тканевой культуре фибробластов куриных эмбрионов. Иммунитет развивается в течение 15 дней и в соответствии с имеющимися данными сохраняется не менее 20 лет. Профилактика кори этой вакциной осуществляется, начиная с 12 месячного возраста.
К недостаткам этой вакцины следует отнести: длительное пассирование штамма Шварца - продуцента вакцины - на тканевых культурах человека (52 пассажа на тканевых культурах почечной ткани и амниона человека); непригодность этой вакцины для иммунизации детей 4-5-10 месяцев из-за низкой иммуногенности, что не позволяет, по данным ВОЗ, применять ее в странах Африки и ограничивает возможность ее использования в рамках программы EPJ. Следует отметить также, что две серии вакцины "Рувакс", поступившие в Санкт-Петербург в 1990 - 1991 гг. (N 136- и N 140), оказались слабо иммуногенными и для детей старше 12 месяцев: средний геометрический титр сывороток детей, привитый этими сериями вакцины, через месяц после иммунизации составил 1:16 и 1:34 соответственно.
Наиболее близкой по сущности является коревая вакцина из штамма Л-16 [2] . Вирусом-продуцентом этой коревой вакцины является штамм Л-16, выделенный от больного корью на первичной почечной ткани морских свинок (ПМС), аттенуирован на этой культуре (21 пассаж) и затем прошедший 2 пассажа на тканей культуре ФЭП. Основой для приготовления вирусной биомассы для вакцины является культура ФЭП. Стабилизаторами: смесь растворов сорбита и желатозы (30% к объему жидкого полуфабриката) или желатина с сахарозой из расчета конечной концентрации 1 об.%.
К основным недостаткам этой вакцины следует отнести: гиператтенуация вируса-продуцента, низкий выход и концентрация биомассы, что существенно отражается на качестве вакцины и, в частности, на ее иммуногенной активности. Причиной последнего может являться также гиператтенуация вируса в последние годы на предприятиях в процессе производства коревой вакцины.
Изобретение направлено на усовершенствование живой вакцины для профилактики кори, при этом усилена иммуногенная активность коревой вакцины, а также обеспечена возможность интраназального введения вакцины и вакцинации детей в возрасте младше 9 месяцев.
Поставленная задача решается за счет того, что в качестве продуцента коревой вакцины используют штамм Ленинград-16в (Л-16в), который выращивают в среде Игла или Игла МЕМ в присутствии 6,5 ± 1,5 об.% аминопептида при заражающей дозе 0,2 ± 0,1 ТЦД50/кл.
Штамм-продуцент коревой вакцины Д-16в получен пассированием прототипного штамма Л-16, взятого спустя 22 года хранения в коллекции производственных штаммов, в тканевой культуре ФЭП при пониженной температуре. При этом проводили селекцию вирусных частиц по критерию отсутствия нейровирулентности, что проверялось авторами на обезьянах. В результате получен новый штамм, который который характеризуется отсутствием не только нейровирулентных частиц, но и высокой репродукционной активностью (6,2 - 6,6 ТЦД50/0,5 мл вместо 3,5 - 5,2 lg ТЦД50/0,5 мл в исходном штамме). При проверке иммуногенных свойств на обезьянах отмечается их усиление у нового штамма в 8 раз по сравнению с Л-16. при контроле иммуногенных свойств на детях также отмечено их усиление у нового штамма в 4 раза по сравнению с Л-16 (средняя геометрическая титра антител у привитых 1:84 против 1:19,7 соответственно).
Штамм Л-16в депонирован 26.03.91 г. под N 2277 в государственном музее вирусов Института вирусологии им. Ивановского.
Живая вакцина для профилактики кори содержит штамм-продуцент вируса кори Л-16в в заражающей дозе 0,2 ± 0,1 ТЦД50/кл., поддерживающую питательную среду Игла или Игла МЕМ в количестве 5...8% и добавлением стабилизатора перед лиофилизацией. Состав и количественное содержание ингредиентов вакцины установлен авторами в результате проведения экспериментальных исследований. В качестве стабилизатора можно использовать любой известный, например сорбит с желатозой или желатину с сахарозой, т.к. выбор последнего не сказывается на качестве и свойствах вакцины.
Изобретение может быть реализовано следующим образом.
Пример 1. В 1-литровые матрацы с тканевой культурой ФЭП в ростовой среде 199 с добавлением 10 об.% сыворотки крупного рогатого скота вносят вирус кори штамм Л-16в в заражающих дозах от 0,04 до 0,6 ТЦД50/кл. (для каждой заражающей дозы по 5 матрацев) и инкубируют в роллерах при температуре 35oC и скорости 0,3 об/мин до образования монослоя клеток, что происходит не позже, чем на 3 сутки инкубирования. Затем ростовую среду удаляют, а монослой 6-кратно отмывают от сыворотки раствором Хенкса pH 7,4.
Далее в матрацы с зараженным клеточным монослоем добавляют по 160 мл поддерживающей среды Игла с 6 об.% аминопептида и производят культивирование вируса в роллере при 35oC и 0,3 об/мин. В течение срока сохранения тканевой культуры (этот срок в различных матрацах колеблется от 18 до 22 дней). По мере нарастания цитопатогенных изменений клеточного монослоя, характерных для вируса кори (наблюдают под микроскопом), вируссодержащую жидкость сливают во флаконы и хранят под резиновой пробкой при минус 20oC для последующего использования, а в матрацы добавляют по 160 мл свежей поддерживающей среды Игла с вышеуказанным количеством аминопептида и культивируют при тех же условиях. Такую процедуру многократно повторяют. При этом интервал замены среды составляет 1-2 дня. При данных условиях число полезных съемов (циклов, в которых содержание вируса не менее 4 lg ТЦД50/0,5 мл) не менее 5.
Все операции способа выполняют в стерильных условиях.
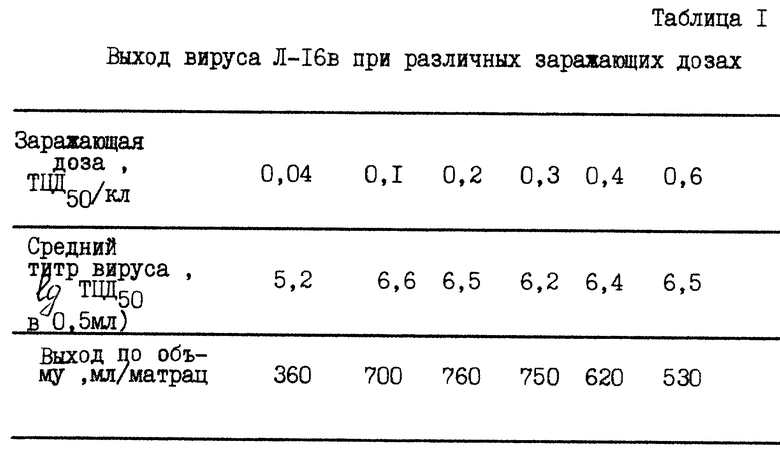
Результаты культивирования приведены в таблице 1.
Как видно из таблицы, увеличение заражающей дозы в 10 - 30 раз по сравнению с прототипом позволяет на данной среде получить вирусную биомассу с титром 6,2 - 6,5 lg ТЦД50/0,5 кл., тогда как при меньшей заражающей дозе (0,04 ТЦД50/кл) этот титр составляет лишь 5,2 lg ТЦД50/0,5 мл. Вместе с тем, максимум выхода по объему (700 - 760 мл/матрац) достигается в диапазоне заражающих доз от 0,1 до 0,3 ТЦД50/кл из-за повышения числа полезных съемов вируса (возможных циклов культивирования).
Пример 2. В 25 1-литровых матрацев с тканевой культурой ФЭП в ростовой среде 199 с добавлением 10 об.% сыворотки крупного рогатого скота вносят вирус кори штамм Л-16в в заражающей дозе 0,2 ТЦД50/кл. и инкубируют как в примере 1.
Далее матрацы с зараженным клеточным монослоем добавляют по 160 мл поддерживающей среды Игла с 2, 3, 5, 8, и 13 об.% аминопептида (параметрический ряд Фибоначчи, используемый, как известно, для повышения точности однофактного эксперимента), используя по 5 матрацев для каждого значения этого параметра. Культивирование вируса осуществляют как в примере 1.
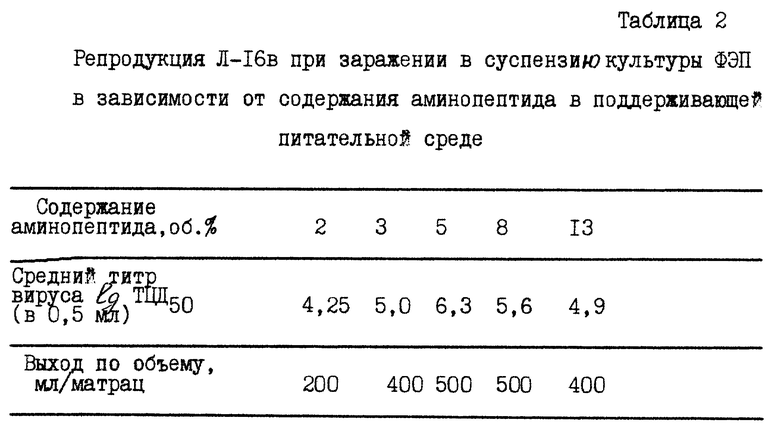
Результаты культивирования приведены в табл. 2.
Из таблицы видно, что при содержании аминопептида в поддерживающей среде Игла 5 - 8 об.% урожай вируса максимальный и составляет 500 мл/матрац при титре 5,6 - 6,3 lg ТЦД50/0,5 мл. Вне этого диапазона концентрации аминопептида выход вируса значительно меньше как по объему, так и по титру.
Пример 3. В 25 1-литровых матрацев вносят по 50 млн клеток ФЭП в ростовой среде 199 с добавлением 10 об.% сыворотки крупного рогатого скота. После формирования монослоя клеток ростовую среду удаляют, клеточный монослой отмывают от сыворотки как в примере 1 и заражают вирусом кори штамм Л-16в в тех же дозах, что и в примере 2.
Остальные операции осуществляют как в примере 2.
Результаты культивирования приведены в табл.3.
Из таблицы видно, что при содержании аминопептида в поддерживающей среде Игла 5 - 8 об.% урожай вируса максимальный и составляет 550 мл/матрац при титре 5,5 - 6,2 lg ТЦД50/0,5 мл. Вне этого диапазона концентрации аминопептида выход вируса значительно меньше как по объему, так и по титру.
Пример 4. Клеточную культуру ФЭП в 10 матрацах заражают вирусом Л-16в как в примере 1.
В 5 матрацах в качестве поддерживающей среды используют среду Игла с добавлением 5 об.% аминопептида, а в остальных 5 матрацах вирус культивируют с использованием среды 199 с тем же количеством аминопептида. Другие условия культивирования устанавливают как в примере 1.
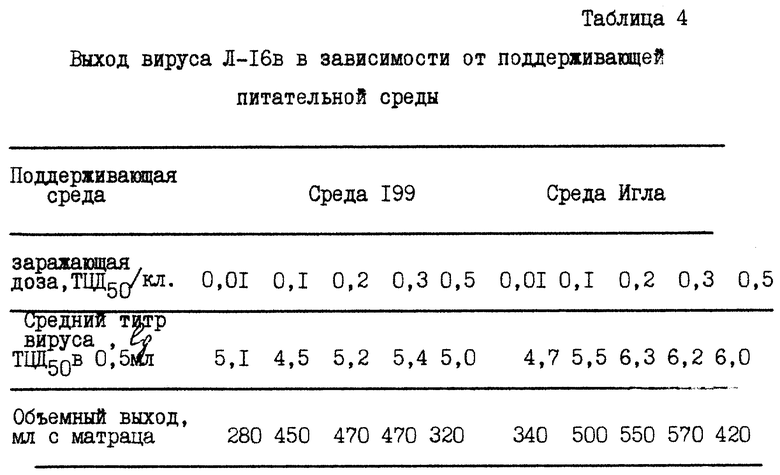
Результаты культивирования приведены в таблице 4.
При использовании среды Игла МЕМ получены аналогичные результаты (как при использовании среды Игла).
Как видно из таблицы, при равных заражающих дозах выход вируса на среде Игла больше, чем на среде 199, как по объему, так и по концентрации.
Пример 5. Характеристика получаемых вакцин из штаммов Л-16 и Л-16в.
5 1-литровых матрацев с клеточной культурой ФЭП заражают вирусом кори Л-16 (штамм-прототип) в дозе 0,01 ТЦД50/кл. Другие 5 матрацев заражают вирусом кори Л-16в в дозе 0,1 ТЦД50/кл.
Для культивирования штамма Л-16 используют поддерживающую среду 199 с 5 об. % аминопептида, а для штамма Л-16в - среду Игла с тем же количеством аминопептида.
Условия съема вируссодержащей жидкости и культивирования - как в примере 1.
Средний выход вируса кори Л-16 с одного матраца составляет 360 мл при титре 5,2 lg ТЦД50/0,5 мл, а вируса Л-16в - 560 мл при титре 6,5 lg ТЦД50/0,5 мл.
Собранные вируссодержащие материалы объединяют поштаммно, добавляют стабилизатор (желатину с сахарозой из расчета конечной концентрации 1 об.%), разводят средой Игла до концентрации 4,5 lg ТЦД50/0,5 мл, разливают в ампулы и лиофильно высушивают.
В результате получают 36000 доз вакцины штамма Л-16 и 526000 доз вакцины штамма Л-16в (в одной дозе 20000 lg ТЦД50/0,5 мл). В данном примере объем вакцины из нового штамма в 14 раз больше, чем из прототипного.
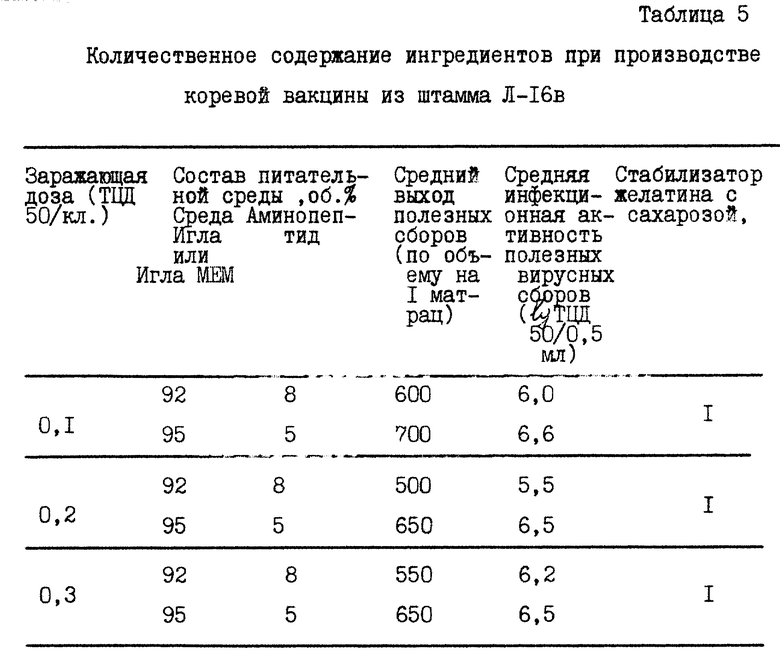
В таблице 5 приведено количественное содержание ингредиентов при производстве вакцины на основе Л-16в.
Пример 6. Штамм Л-16в культивируют как в примере 1 при заражающей дозе 0,2 ТЦД50/кл. Выращенный вирус полуфабрикат вакцины контролируют на 10 серонегативных к кори обезьянах на контагиозность, нейровирулентность и иммуногенную активность. Для контроля используют 4 серонегативных обезьяны.
Десяти серонегативным обезьянам вводят вируссодержащий материал по 0,5 мл в зрительный бугор каждого полушария и 1,0 мл внутримышечно. Общая доза коревого вируса составляет 10 минимальных доз человека (по 2000 lg ТЦД50/0,5 мл). Контрольных обезьян содержат вместе с опытными.
Все обезьяны контрольной и опытной групп выжили.
В результате клинических, морфологических и серологических исследований установлено, что данный полуфабрикат вакцины не обладает нейровирулентностью (отсутствуют симптомы поражения нервной системы, что подтверждается гистологически) и контагиозностью (отсутствуют противокоревые антитела у обезьян контрольной группы). В ответ на введение вируса у 100% обезьян образуются антитела в обратном титре от 64 до 256 (средний геометрический обратный титр 120).
Параллельно на 9 обезьянах контролируют иммуногенные свойства полуфабриката вакцины из прототипного штамма Л-16 при той же дозировке. Установлено, что штамм Л-16 также вызывает образование антител у 100% обезьян, но в меньших концентрациях (средний геометрический обратный титр равен 16).
Пример 7. Живая коревая вакцина, приготовленная из штамма Л-16в (серия N 9), прошедшая все необходимые контроли согласно действующей НТД, была разрешена ГИСК им. Тарасевича для испытания реактогенности и иммуногенной активности на детях (разрешение ГИСК им. Тарасевича от 26.03.92 N 01-33/8).
Специфическая реакция на введение вакцины (сер. N 9) 83 серонегативным к кори детям наблюдалась у 7 детей (кратковременные катаральные явления и гиперемия зева). У 4 из этих детей выявлено повышение температуры до 37,2 - 37,8o. Сильные температурные реакции выше 38,5oC отсутствовали (согласно действующей НТД допускается количество сильных температурных реакций (> 38,5oC) не выше 2%.
Сероконверсия у 83 привитых серонегативных детей составила 100%. Средняя геометрическая титра (СГТ) антител у этих детей равна 6,44 log2 (1:84). Тогда как у детей, привитых коревой вакциной из штамма Л-16 (производство Московского предприятия "Д. Мазай") при сероконверсии 95,6% СГТ составила 4,3 log2 (1: 19,7). Процент детей с высокими титрами антител (выше 1:80) составил 78,2% против 10,1% соответственно.
Таким образом, иммуногенная активность вакцины из штамма Л-16в значительно превышала показатели иммуногенности вакцины из штамма Л-16, отличаясь от последнего более низкой реактогенностью.
Ниже приведена сравнительная характеристика живых коревых вакцин из штаммов Л-16 и Л-16в (табл. 6).
Штамм Л-16в обеспечивает по сравнению с прототипом повышение выхода вируса по титру и объему, что позволяет в 20 раз увеличить выход вакцины. При этом получаемый целевой продукт обладает более высокой иммуногенностью (см. пример 6 и 7).
Высокая иммуногенная активность разработанной вакцины из штамма Л-16в обеспечивает, в отличии от вакцины из штамма Л-16, без увеличения прививочной дозы препарата возможность интраназального введения вакцины и вакцинации детей младше 9 месяцев.
Источники информации, принятые во внимание
1. Каталог препаратов фирмы "Пастер Мерье" Сыворотки и вакцины, с. 33.
2. Тарос Л.Ю. Новый вакцинный штамм для иммунизации против кори. Автореф. дис. ..канд. мед. наук, Л., 1965; Васильева Г.А., Бойчук Л.М. Характеристика реактогенных и антигенных свойств вакцинного штамма Л-16, адаптированного к тканевой культуре из эмбрионов японских перепелок. Отработка технологии производства живой коревой вакцины Л-16 на тканевой культуре из эмбрионов японских перепелок. - "Специфическая профилактика кори", материалы научно-практической конференции, ЛНИИЭМ им. Пастера, Л., 1970, с. 174 - 179, 206 - 210.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ РЕГЕНЕРАЦИИ ВАКЦИННОГО ШТАММА ВИРУСА КОРИ | 1995 |
|
RU2088662C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВИРУСА КОРИ И ПОДДЕРЖИВАЮЩАЯ ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ЕГО КУЛЬТИВИРОВАНИЯ (ВАРИАНТЫ) | 1996 |
|
RU2129607C1 |
| ШТАММ ВИРУСА КРАСНУХИ "ОРЛОВ-В" ДЛЯ ПОЛУЧЕНИЯ ВАКЦИНЫ | 1995 |
|
RU2081912C1 |
| СПОСОБ КУЛЬТИВИРОВАНИЯ ВИРУСА КОРИ | 1994 |
|
RU2053297C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВИРУСА КРАСНУХИ И ПОДДЕРЖИВАЮЩАЯ ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ЕГО КУЛЬТИВИРОВАНИЯ (ЕЕ ВАРИАНТЫ) | 1996 |
|
RU2129608C1 |
| ВАКЦИННЫЙ ШТАММ ВИРУСА КРАСНУХИ "ОРЛОВ-Д" И СПОСОБ ПОЛУЧЕНИЯ ВАКЦИНЫ ПРОТИВ КРАСНУХИ | 1999 |
|
RU2173344C2 |
| ШТАММ РОТАВИРУСА ЧЕЛОВЕКА ДЛЯ ПОЛУЧЕНИЯ ДИАГНОСТИЧЕСКИХ И ПРОФИЛАКТИЧЕСКИХ СЫВОРОТОК | 1991 |
|
RU2026345C1 |
| ШТАММ ВИРУСА КРАСНУХИ ДЛЯ ПОЛУЧЕНИЯ МЕДИЦИНСКИХ ИММУНОБИОЛОГИЧЕСКИХ ПРЕПАРАТОВ (МИБП) | 2012 |
|
RU2492235C1 |
| Способ получения живой ассоциированной паротитно-коревой вакцины | 1976 |
|
SU604343A1 |
| СПОСОБ ПОЛУЧЕНИЯ СУБЪЕДИНИЧНОЙ ГЕННОИНЖЕНЕРНОЙ ВАКЦИНЫ ПРОТИВ ГЕПАТИТА В | 1992 |
|
RU2067767C1 |



Изобретение относится к области биотехнологии. Живая вакцина содержит следующие ингредиенты, об. %: штамм Л - 16в (ГКВ N 2277) в заражающей дозе 0,2 ± 0,1 ТЦД50/кл, аминопептид 5 - 8, среда Игла или Игла МЕМ 92 - 95, стабилизатор остальное. Вакцина имеет повышенную иммуногенную активность, а также обеспечивает возможность интраназального введения и вакцинации детей младше 9 месяцев. 6 табл.
Живая вакцина для профилактики кори, содержащая штамм - продуцент вируса кори, поддерживающую питательную среду с аминопептидом и стабилизатор, отличающаяся тем, что в качестве штамма-продуцента содержит штамм Л-16в (ГКВ N 2277) в заражающей дозе 0,2 ± 0,1 ТЦД50/кл. поддерживающей питательной среды - среду Игла или Игла МЕМ при следующем соотношении ингредиентов, об.%:
Штамм Л-16в в заражающей дозе 0,2 ± 0,1 ТЦД50/кл
Аминопептид - 5 - 8
Среда Игла или Игла МЕМ - 92 - 95
Стабилизатор - Остальное
| СПОСОБ КУЛЬТИВИРОВАНИЯ ВИРУСА КОРИ | 1994 |
|
RU2053297C1 |
| Руководство по вакцинному и сывороточному делу./Под ред | |||
| П.Н.Бургасова | |||
| - М.: Медицина, 1978, с | |||
| Ветряный много клапанный двигатель | 1921 |
|
SU220A1 |
Авторы
Даты
1999-05-10—Публикация
1996-07-30—Подача