Новые производные камптотенцина общей формулы I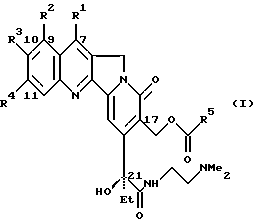
где R1 представляет собой атом водорода или C1-C6-алкильную группу;
R2 означает водород или C1-C6-алкоксигруппу;
R3 - водород, галоген, C1-C6-алкил, C1-C6-алкокси, гидроксил, C2-C6-ацилокси или метоксиэтоксиметоксигруппа;
R4 - атом водорода или галогена;
R5 - C1-C6-алкил, C3-C6-ненасыщенный алкил, алкилтиоалкил, алкоксиалкил, пиридил или замещенная фенильная группа при условии, что заместители R2, R3 и R4 не должны быть атомом водорода; способ получения новых производных камптотецина с помощью превращения производных камптотетица общей формулы II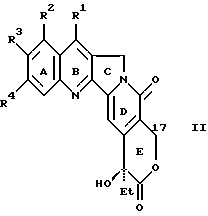
где R1, R2, R3 и R4 имеют приведенные выше значения,
реакцией с N, N-диметилэтилендиамином без растворителя с открытием E-лактонового кольца и с последующим ацилированием 17-гидроксильной группы; и противоопухолевые агенты, содержащие эти производные в качестве активного ингредиента.
Настоящее изобретение касается новых водорастворимых производных камптотецина, способа их получения и противоопухолевых препаратов, содержащих их в качестве активного ингредиента.
Авторами настоящего изобретения изучен и предложен ряд новых камптотецинов (далее обозначаются как CPT) с превосходной противоопухолевой активностью, найдено, что полностью синтетические производные CPT, содержащие низкую алкильную группу в 7-положении B-кольца, а также гетеро и/или алкильную группу в 9-, 10- и 11-положениях A-кольца проявляют наиболее сильную противоопухолевую активность (смотри JP, A, HI-186892).
Авторы настоящего изобретения провели также широкие исследования для решения проблемы водорастворимости производных, в случае их использования в медицине. Особенно превосходную растворимость в воде без снижения противоопухолевой активности в противоположность известным водорастворимым производным CPT с открытым E-кольцом (JP, A, HI-131179) проявляют производные CPT, синтезированные реакцией 7-этилCPT с диамином с открытием E-лактонового кольца с последующим ацилированием гидроксиметильной группы.
Кроме того, проведены дополнительные исследования для получения других новых CPT-производных с более превосходной противоопухолевой активностью и с пригодной растворимостью в воде при введении, кроме того, существует большой спрос в данной области на создание новых производных CPT, которые бы решили проблемы как токсичности, так и употребления.
Таким образом, предметом этого изобретения являются водорастворимые новые производные CPT, обладающие превосходной противоопухолевой активностью. Другим предметом является получение новых производных CPT, которые решают как проблему токсичности, так и проблему потребления.
Для того, чтобы решить эти задачи, предложен способ получения новых водорастворимых CPT-производных из CPT-производных, содержащих низшую алкильную группу в 7-положении, а также гетеро и/или алкильную группу в 9-, 10- и 11-положении A-кольца, превращением их путем открытия E-лактонового кольца реакцией с диаминами с последующим ацилированием гидроксиметильной группы.
И как результат наших широких исследований по безопасности и по галеновым препаратам, проведенным для разработки новых водорастворимых CPT-производных вышеприведенные цели изобретения достигнуты и получены превосходные новые CPT-производные с противоопухолевой активностью.
В соответствии с настоящим изобретением предложены новые CPT-производные общей формулы I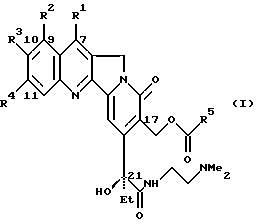
где R1 означает атом водорода или C1-C6-алкильную группу,
R2 представляет собой водород или C1-C6-алкокси группу,
R3 описывает атом водорода или галогена, C1-C6-алкил, C1-C6-алкокси, гидроксил, C2-C6-ацилокси или метоксиэтоксиметокси группу,
R4 представляет собой атом водорода или галогена и
R5 означает C1-C6-алкил, C3-C6-ненасыщенный алкил, алкилтиоалкил, алкоксиалкил, пиридил или замещенную фенильную группу при условии, что все R2, R3 и R4 заместители не должны быть водородами;
способ получения новых производных камптотецина. Кроме того, в соответствии с настоящим изобретением предложены противоопухолевые препараты, содержащие в качестве активного ингредиента новые CPT-производные общей формулы I.
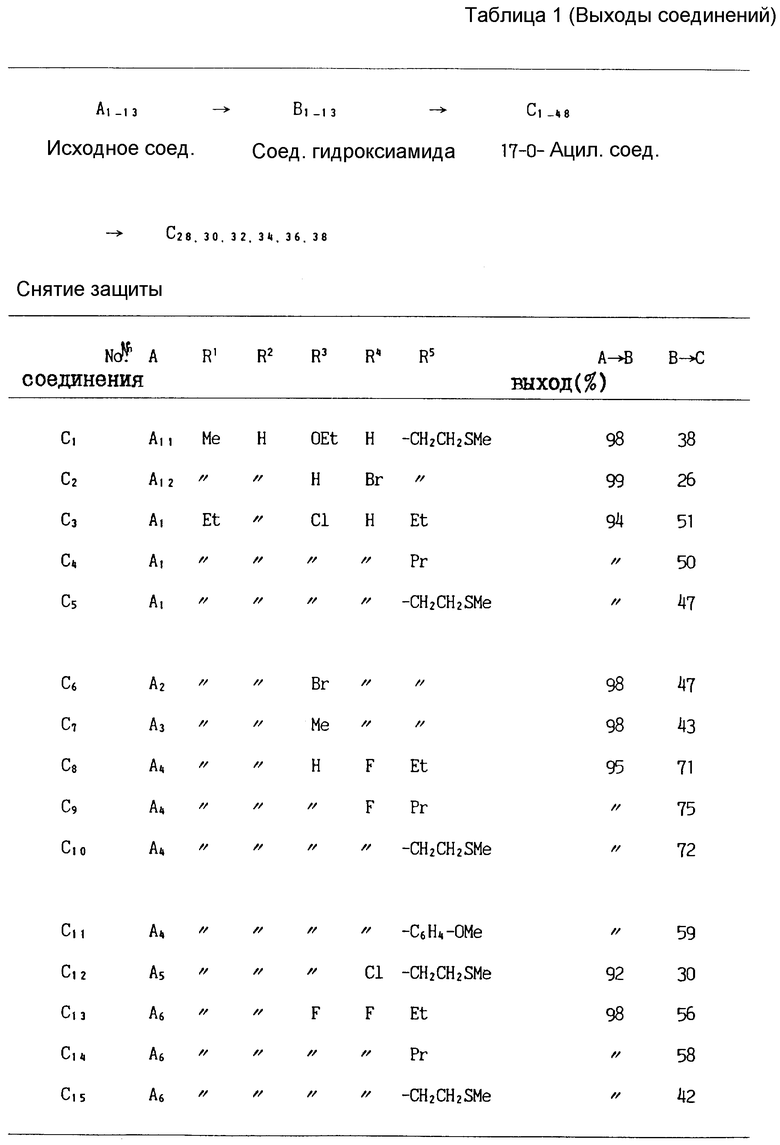
Новые CPT-производные изобретения получают из CPT-производных, содержащих атом водорода или низший алкил в 7-положении, а также гетеро и/или алкильную группу в 9-, 10- и 11-положении, с помощью реакции с N,N-диметилэтилендиамином без растворителя с последующим ацилированием 17-гидроксиметильной группы с соответствующим ацилирующим агентом.
Исходные CPT-производные, содержащие атом водорода или низшую алкильную группу в 7-положении, а также гетеро и/или алкильную группу в 9-, 10- и 11-положении, являются известными CPT-производными, полученными из веществ природного происхождения (9-метоксиCPT, 10-гидроксиCPT, 10-метоксиCPT, 11-гидроксиCPT, 11-метоксиCPT и т.д.) или их получают полусинтетическими или синтетическими методами по известным методам (смотри JP, A, 58-39684; JP, A, 58-134095; JP, A, 59-51287; JP, A, 59-51289; JP, A, HI-279891; JP, A, HI-186892; JP, A, H4-503505; JP, A, H5-502017; WO-91/04260; WO-92/11263; VSP, 5122606 и другие).
Хотя условия реакции, предложенные в JP, A, H1-13117, для открытия E-кольца с помощью N,N-диметилэтилендиамина с последующим ацилированием 17-гидроксильной группы с соответствующим ацилирующим агентом могут быть использованы, найдено, что по этой методике целевые соединения необязательно получаются с удовлетворительными выходами.
Нами изучены условия этой методики и найдено, что на первой стадии реакции открытия E-лактонового кольца с помощью N,N-диметилэтилендиамина целевые соединения получают с очень хорошими выходами при использовании избытка N, N-диметилэтилендиамина одного, без растворителя при проведении раскрытия E-кольца с последующим ацилированием 17-гидроксильной группы соответствующими ацилирующими агентами.
В качестве ацилирующих агентов для ацилирования используют не специальные агенты, а соответствующие ангидриды кислот, галогенангидриды кислот, например, хлорангидриды, бромангидриды и другие эквивалентные ацилирующие агенты могут использоваться. Реакционная смесь соответствующих карбоновых кислот, обработанных с соответствующим агентом, например дициклогексилкарбодиимидом, также может использоваться для вышеназванного ацилирования.
Наглядным примером соответствующих карбоновых кислот, использующихся в качестве вышеназванного ацилирующего агента, являются, например насыщенные алифатические кислоты с 2-20 атомами углерода, ненасыщенные алифатические кислоты с 3-20 атомами углерода, алифатические кислоты с циклоалкильной группой или алифатические кислоты с, например, атомом галогена или с алкилтио, амино, ациламино, гидроксил, алкоксил или алкоксикарбонил группой, ароматические кислоты с 6-20 атомами углерода или ароматические кислоты с, например, атомом галогена или гидроксил, алкоксил или низшей алкильной группой, гетероароматические кислоты или аминокислоты.
Примерами ацилирующих агентов являются ацетилхлорид, бензоилхлорид, пропионилхлорид, бутирилхлорид, метоксибензоилхлорид, фторбензоилхлорид, бромбензоилхлорид, хлорбензоилхлорид, нитробензоилхлорид, трифторметилбензоилхлорид, нафтоилхлорид, циклопропанкарбонилхлорид, теноилхлорид, кротонилхлорид, циннамоилхлорид, фенилацетилхлорид, фенилбензоилхлорид, циклогексанкарбонилхлорид, стеароилхлорид, олеолхлорид, метоксикарбонилбензоилхлорид, этилсукцинилхлорид, линолеилхлорид, хлорбутирилхлорид, этилбензоилхлорид, метилтиопропионилхлорид, пивалоилхлорид, никотиноилхлорид, изоникотиноилхлорид и пиколиноилхлорид.
При вышеназванном ацилировании в реакции в качестве катализатора может присутствовать N,N-диметиламинопиридин или подобные соединения.
Дополнительно, тщательное выдерживание безводных условий не только при открытии кольца, но и при ацилировании, и, кроме того, например, при измельчении, очистки и кристаллизации, может увеличить выход целевого соединения.
Новые CPT-производные этого изобретения показывают превосходную растворимость в воде с помощью превращения их в соли кислот с соответствующими кислотами, такими как соляная кислота. Соединения этого изобретения безопасны, показывают превосходную противоопухолевую активность и поэтому могут предлагаться в качестве новых противоопухолевых агентов.
Настоящее изобретение более подробно будет проиллюстрировано примерами.
Пример 1. Получение соединений с открытыми кольцами (B1-B13).
В качестве исходного материала CPT-производных (A1-A12, каждый заместитель приведен в таблице 1) с каждым заместителем в 7-положении и в 9-, 10- и 11-положении A-кольца получены соединения по вышеуказанным ссылкам литературы.
9-МетоксиCPT(A13), выделенный из природных веществ, используют в этом примере. Для соединений, содержащих гидроксильную группу A-кольца, соединения (A10) проводят O-метоксиэтоксиметилирование с помощью обычного метода.
К 3,0 г, например, исходного CPT-производного (A1-A13) прибавляют избыток безводного N,N-диметилэтилендиамина (5-100 экв., например 15 мл). Реакционную смесь перемешивают 1,5 часов при 50oC в атмосфере азота, после чего реакционную смесь упаривают досуха в вакууме. Остаток растворяют в сухом хлористом метилене (например, 15 мл), раствор выливают в большое количество сухого н-гексана (например, 500 мл).
Выпавшие кристаллы отфильтровывают, промывают сухим н-гексаном, сушат и получают гидроксиамид (B1-B13, соединения с открытым E-лактоновым кольцом) с практически количественным выходом.
Выходы и спектральные данные каждого соединения приведены в последующей таблице 2.
Пример 2. Ацилирование 17-гидроксильной группы.
К раствору вышеполученного гидроксиамида (например, 1,0 г) в сухом хлористом метилене (например, 20 мл) прибавляют по каплям ацилирующий агент (1,2 экв. ) в присутствии диметиламинопиридина (ДМРА, например 10 мг) при охлаждении льдом. Реакционную смесь перемешивают при комнатной температуре ночь, промывают 7% водным бикарбонатом натрия, насыщенным водным раствором хлористого натрия.
Слой хлористого метилена сушат над безводным сульфатом натрия, отфильтровывают нерастворенный материал, упаривают досуха в вакууме. Остаток хроматографируют на колонке с силикагелем (10% MeOH-CHCl3), кристаллизуют из хлороформа-н-гексана с получением 17-0-ацил-21-N,N-диметиламиноэтиламидного производного (C1-C48) изобретения.
Как и для O-метоксиэтоксиметильного производного, раствор соединения в 10% трифторуксусной кислоте-хлористом метилене перемешивают ночь. После перемешивания прибавляют по каплям при охлаждении льдом к реакционной массе триэтиламин. Реакционную смесь упаривают в вакууме досуха.
Остаток растворяют в хлористом метилене, промывают 7% водным бикарбонатом натрия, насыщенным водным раствором хлористого натрия. Органический слой сушат над безводным сульфатом натрия с последующим удалением нерастворенного материала, упаривают досуха в вакууме. Остаток хроматографируют на колонке с силикагелем (10% MeOH-CHCl3), кристаллизуют из ацетона-CHCl3 и получают 17-O-ацил-21-N,N-диметиламиноэтиламидное производное (C28, C30, C32, C34, C36, C38) изобретения.
Выходы синтезированных производных и их спектральные данные приведены в таблицах 1 и 3.
Данные по растворимости в воде полученных новых производных камптотецина изобретения приведены в таблице 4.
Противоопухолевое действие
Далее описаны для полученных новых производных камптотецина изобретения результаты противоопухолевой активности, токсикологические тесты, потребляемые дозы и галеновые препараты.
Противоопухолевая активность
Хорошо признано, что противоопухолевое действие для грызунов приводит к надежным результатам для противоопухолевого действия на теплокровных животных. Авторы настоящего изобретения изучали противоопухолевое действие на мышах в качестве модельных животных.
Противоопухолевая активность для L1210
Лейкемические клетки мышей L1210(5•105) трансплантируют внутрибрюшинно группе 6 самок мышей линии CDFI (возраст 7 недель, вес тела 17-19 г). Тестируемые соединения вводят внутрибрюшинно на 1, 5 и 9 день и наблюдают их влияние на продление жизни.
В случае введения тестируемого соединения в виде соли кислоты его растворяют в воде. Общее введенное количество составляет 1,56 мг/кг - 400 мг/кг. Противоопухолевая активность выражается как величина (T/C%), где Т описывает среднее количество прожитых дней у группы при введении препарата и C описывает среднее количество прожитых дней у группы, которой не вводили препарат.
Для случаев, равных или больших чем 125%, препарат считается эффективным. Терапевтический индекс рассчитывают при рассмотрении по крайней мере эффективной дозы и максимальной переносимой дозы.
Экспериментальные результаты
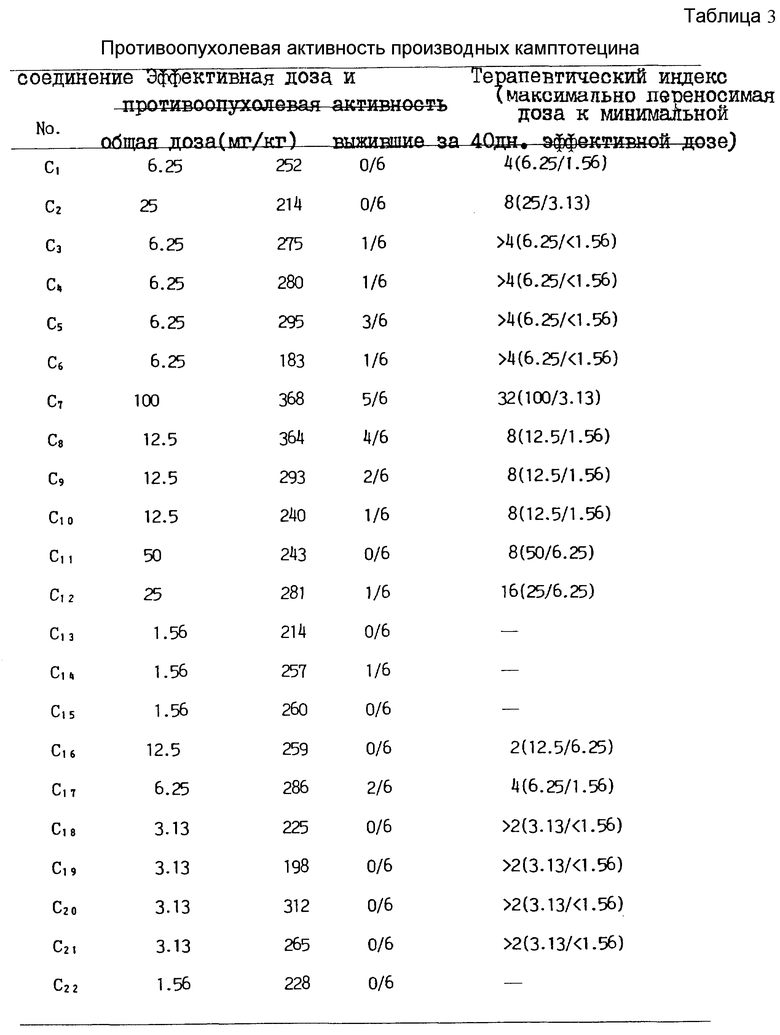
Экспериментальные результаты определения антиопухолевой активности у соединений в тестах, описанных ранее, приведены в таблице 5. Как видно из этой таблицы, новые производные камптотецина настоящего изобретения показывают примерно в 6 раз более благоприятный терапевтический индекс, чем сам камптотецин. При оптимальной дозе препарата в группе из 6 мышей выживало 5 мышей. Результаты также показывают, что они эффективны при более низких дозах, заметное увеличение противоопухолевой активности и повышение терапевтических пределов.
Эксперименты по токсичности
Тесты по острой токсичности проводят с помощью внутрибрюшинного введения при использовании группы из 20 мышей (самцы, возраст 4 недели, вес тела примерно 20 г). Результаты приведены в таблице 6.
LD50 рассчитывается по методу Richfield-Willcokson по летальному соотношению, наблюдая состояние мышей в течение 1 недели после введения тестируемого соединения.
Из вышеприведенных экспериментальных результатов становится понятным, что новые производные камптотецина имеют лучшую противоопухолевую активность и могут использоваться в качестве менее токсичных препаратов, чем их исходное соединение, камптотецин, для лечения раковых заболеваний.
Противоопухолевые препараты настоящего изобретения могут вводиться с помощью инъекций, таких как внутривенные, внутрикожные и внутримышечные инъекции, а также с помощью орального введения. Особенно предпочтительными примерами для введения соединений в виде их солей с кислотами, уместных в качестве медикаментов, являются внутривенное и оральное введение.
При внутривенном введении доза каждого вышеприведенного соединения зависит от цели терапевтического лечения и составляет в ряду 5-400 мг/тело в день, предпочтительно 20-200 мг/тело, для взрослого. При оральном введении ряд составляет 50-2000 мг/тело в день, предпочтительно 100-1000 мг/тело, для взрослого.
В качестве метода приготовления противоопухолевого препарата настоящего изобретения может быть выбран обычный метод для каждого препарата в зависимости от его препаративной формы.
В качестве препаративной формы для абсорбции препарата через желудочно-кишечный тракт противоопухолевый препарат изобретения может быть приготовлен, например, в виде таблеток, порошков, гранул, капсул или мягких капсул, а примеры оральных жидких форм включают водные и масляные суспензии, растворы, сиропы, эликсиры и т.д. Приготовленные инъекции могут храниться в ампулах или больших контейнерах. В этих препаративных формах могут использоваться эксципиенты, такие как антисептики или растворители.
Препаративными формами жидких препаратов могут быть суспензии, растворы и эмульсии на основе масляных или водных сред и могут включать эксципиенты, такие как эмульгаторы. В препаратах противоопухолевых агентов их изобретения содержание активного ингредиента составляет 0,1% или более, предпочтительно 1-50%.
Примеры препаратов противоопухолевых агентов изобретения дополнительно иллюстрируют, но не ограничиваются этим, следующими примерами.
Препарат 1. Инъекция.
После растворения соединения C7(R1 = C2H5, R2 = H, R3 = CH3, R4 = H, R5 = C2H4SCH3) в 0,1N HCl, раствор, содержащий эквивалентное молярное количество HCl, фильтруют, лиофилизируют и получают 50 мг соли HCl соединения C7. Соль запаивают в ампулы в антимикробных условиях и хранят при охлаждении в темноте.
Препарат 2. Таблетки, мг:
Соединение C7 - 50
Лактоза - 89
Гидроксипропилцеллюлоза - 2,7
Кристаллическая целлюлоза - 15
Тальк - 1,6
Стеарат магния - 1,7
Вышеприведенные ингредиенты смешивают и прямо формуют таблетки (160 мг/таблетка) при использовании таблеточной машины.
Спектральные характеристики гидроксиамидных соединений приведены ниже.
B1 (7-Et-10-Cl-)
Порошок желтого цвета (из н-гексана-хлороформа)
C26H31N4O4Cl, MS [M+H]+ = 499
ИК νmax /KBr (см-1): 1650, 1590, 1510.
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,10 (3H6, т, J = 7 Гц), 1,34 (3H, т, J = 8 Гц), 2,20 - 2,32 (1H, т), 2,27 (6H, с), 1,39 - 2,61 (3H, м), 1,90 - 3,05 (1H, м), 3,20 - 3,33 (1H, м), 3,60 - 3,75 (1H, м), 4,78 (1H, д, J= 13 Гц), 5,00 (1H, д, J = 19 Гц), 5,06 (1H, д, J = 19 Гц), 5,10 (1H, д, J = 13 Гц), 7,44 (1H, шир. т, J = 5 Гц), 7,50 (1H, с), 7,62 (1H, дд, J = 2,9 Гц), 7,82 (1H, д, J = 2 Гц), 7,95 (1H, д, J = 9 Гц).
B2 (7-Et-10-Br-)
Порошок светло-желтого цвета (из н-гексана-хлороформа)
C26H31N4O4Br, MS [M+H]+ = 543,
ИК νmax /KBr (см-1): 1654, 1585, 1510.
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,10 (3H, т, J = 7 Гц), 1,35 (3H, т, J = 8 Гц), 2,20 - 2,33 (1H, м), 2,29 (6H, с), 2,35 - 2,63 (3H, м), 2,99 (2H, кв, J = 8 Гц), 3,20 - 3,35 (1H, м), 3,60 - 3,75 (1H, м), 4,78 (1H, кв, J = 13 Гц), 5,02 (1H, д, J = 19 Гц), 5,07 (1H, д, J = 19 Гц), 5,10 (1H, д, J = 13 Гц), 7,43 (1H, шир, т, J = 6 Гц), 7,50 (1H, с), 7,75 (1H, дд, J = 2,9 Гц), 7,88 (1H, д, J = 9 Гц), 8,02 (1H, д, J = 2 Гц).
B3 (7-Et-10-Me-)
Бесцветный порошок (из н-гексана-хлороформа)
C27H34N4O4, MS [M+H]+ = 479,
ИК νmax /KBr (см-1): 1645, 1580, 1560, 1510.
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,10 (3H, т, J = 7 Гц), 1,32 (3H, т, J = 8 Гц), 2,20 - 2,33 (1H, м), 2,27 (6H, с), 2,38 - 2,60 (3H, м), 2,57 (3H, с), 2,92 - 3,05 (2H, м), 3,20 - 3,35 (1H, м), 3,61 - 3,75 (1H, м), 4,80 (1H, д, J = 14 Гц), 5,02 (1H, д, J = 19 Гц), 5,08 (1H, д, J = 19 Гц), 5,12 (1H, д, J = 14 Гц), 7,34 (1H, шир, т, J = 6 Гц), 7,51 (1H, с), 7,54 (1H, дд, J = 2,9 Гц), 7,64 (1H, шир.с), 7,99 (1H, д, J = 9 Гц).
B4 (7-Et-11-F-)
Порошок светло-желтого цвета (из н-гексана-хлороформа)
C26H31N4O4P, MS [M+H]+ = 483,
ИК νmax /KBr (см-1): 1645, 1590, 1510.
1H ЯМР ( δ ч. на млн.): 1,10 (3H, т, J = 7 Гц), 1,35 (3H, т, J = 8 Гц), 2,20 - 2,33 (1H, м), 2,28 (6H, с), 2,38 - 2,62 (3H, м), 2,97 - 3,14 (2H, м), 3,20 - 3,33 (1H, м), 3,63 - 3,76 (1H, м), 4,78 (1H, д, J = 13 Гц), 5,03 (1H, д, J = 19 Гц), 5,08 (1H, д, J = 19 Гц), 5,12 (1H, д, J = 13 Гц), 7,32 (1H, ддд, J = 3,8, 10 Гц), 7,39 (1H, шир. т, J= 6 Гц), 7,51 (1H, с), 7,67 (1H, дд, J = 3,10 Гц), 7,93 (1H, дд, J = 6,9 Гц).
B5 (7-Et-11-Cl-)
Порошок светло-желтого цвета (из н-гексана-хлороформа)
C26H31N4O4Cl, MS [M+H]+ = 499,
ИК νmax /KBr (см-1): 1645, 1600, 1590.
1H ЯМР ( δ ч. на млн.): 1,10 (3H, т, J = 7 Гц), 1,36 (3H, т, J = 8 Гц), 2,20 - 2,33 (1H, м), 2,28 (6H, с), 2,39 - 2,62 (3H, м), 2,97 - 3,12 (2H, м), 3,21 - 3,33 (1H, м), 3,62 - 3,78 (1H, м), 4,76 (1H, д, J = 14 Гц), 5,00 (1H, д, J = 19 Гц), 5,10 (1H, д, J = 14 Гц), 7,39 - 7,52 (3H, м), 7,84 (1H, д, J = 9 Гц), 7,97 (1H, д, J = 2 Гц).
B6 (7-Et-10, 11-F2-)
Порошок желтого цвета (из н-гексана-хлороформа)
C26H30N4O4F2, MS [M+H]+ = 501,
ИК  /KBr (см-1): 1645, 1590, 1515
/KBr (см-1): 1645, 1590, 1515
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,10 (3H, т, J = 7 Гц), 1,36 (3H, т, J = 8 Гц), 2,18 - 2,64 (4H, м), 2,29 (6H, с), 3,06 (2H, кв., J= 8 Гц), 3,22 - 3,37 (1H, м), 3,60 - 3,78 (1H, м), 4,76 (1H, д, J = 14 Гц), 5,06 (1H, д, J= 19 Гц), 5,11 (1H, д, J = 19 Гц), 5,13 (1H, д, J= 14 Гц), 7,36 - 7,44 (1H, шир.), 7,69 (1H, дд, J = 8, 11 Гц), 7,81 (1H, дд, J = 8, 11 Гц).
B7 (7-Et-10, 11-Cl2-)
Порошок желтого цвета (из н-гексана-хлороформа)
C26H30N4O4Cl2, MS [M+H]+ = 533,
ИК νmax /KBr (см-1): 1650, 1595, 1520
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,09 (3H, т J = 7 Гц), 1,38 (3H, т, J = 8 Гц), 2,18 - 2,34 (1H, м), 2,29 (6H, с), 2,38 - 2,64 (3H, м), 2,94 - 3,11 (2H, м), 3,23 - 3,38 (1H, м), 3,60 - 3,75 (1H, м), 4,17 (1H, д, J = 14 Гц), 4,97 (1H, д, J = 19 Гц), 5,03 (1H, д, J = 19 Гц), 5,06 (1H, д, J = 14 Гц), 7,51 (1H, шир. т, J = 5 Гц), 7,94 (1H, с), 8,02 (1H, с).
B8 (7-Et-10-OMe-11-F-)
Порошок желтого цвета (из н-гексана-хлороформа)
C27H33N4O5F, MS [M+H]+ = 513,
ИК νmax /KBr (см-1): 1650, 1590, 1510
1H ЯМР ( δ ч. на млн.) 1,11 (3H, т, J = 7 Гц), 1,31 (3H, т, J = 8 Гц), 2,20 - 2,37 (1H, м), 2,27 (6H, с), 2,41 - 2,60 (3H, м), 2,85 - 2,60 (3H, м), 2,85 - 3,04 (2H, м), 3,21 - 3,33 (2H, м), 3,60 - 3,73 (1H, м), 4,00 (3H, с), 4,73 (1H, д, J = 13 Гц), 4,86 (1H, д, J = 19 Гц), 4,94 (1H, д, J = 19 Гц), 5,05 (1H, д, J = 9 Гц), 7,38 (1H, с), 7,51 (1H, шир. т, J = 6 Гц), 7,55 (1H, д, J = 12 Гц).
B9 (7-Et-10-Me-11-F-)
Порошок светло-желтього цвета (из н-гексана-хлороформа)
C27H33N4O4F, MS [M+H]+ = 497,
ИК νmax /KBr (см-1): 1645, 1585, 1505
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,10 (3H, т, J = 7 Гц), 1,35 (3H, т, J = 8 Гц), 2,21 - 2,35 (1H, м), 2,28 (6H, с), 2,40 - 2,62 (3H, м), 2,48 (3H, с), 2,94 - 3,12 (2H, м), 3,23 - 3,37 (1H, м), 3,59 - 3,74 (1H, м), 4,76 (1H, д, J = 13 Гц), 4,95 (1H, д, J = 19 Гц), 5,01 (1H, д, J = 19 Гц), 5,09 (1H, д, J = 13 Гц), 7,46 (1H, с), 7,47 (1H, шир. т, J = 6 Гц), 7,52 (1H, д, J = 11 Гц), 7,65 (1H, д, J= 8 Гц).
B10 (7-Et-10-OMEM-)
Порошок желтого цвета (из н-гексана-хлороформа)
C30H40N4O7, MS [M+H]+ = 569,
ИК νmax /KBr (см-1): 1650, 1625, 1585, 1510
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,10 (3H, т, J = 7 Гц), 1,30 (3H, т, J = 7 Гц), 2,20 - 2,33 (1H, м), 2,26 (6H, с), 2,39 - 2,61 (3H, м), 2,87 - 3,03 (2H, м), 3,24 - 3,33 (1H, м), 3,39 (3H, с), 3,52 - 3,73 (3H, м), 3,83 - 3,94 (2H, м), 4,80 (1H, д, J = 13 Гц), 4,98 (1H, д, J = 19 Гц), 5,04 (1H, д, J = 19 Гц), 5,09 (1H, д, J = 13 Гц), 5,40 (1H, д, J = 7 Гц), 5,43 (1H, д, J = 7 Гц), 7,38 - 7,44 (2H, м), 7,46 (2H, с), 7,48 (1H, шир. т, J = 6 Гц), 7,97 (1H, д, J = 9 Гц).
B11 (7-Me-10-OEt-)
Порошок светло-желтого цвета (из н-гексана-хлороформа)
C27H34N4O5, MS [M+H]+ = 495,
ИК νmax /KBr (см-1): 1645, 1620, 1590, 1510
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,11 (3H, т, J = 7 Гц), 1,54 (3H, т, J = 7 Гц), 2,23-2,33 (1H, м), 2,28 (6H, c), 2,39 (3H, c), 2,43 - 2,59 (3H, м), 3,21 - 3,37 (1H, м), 3,55 - 3,72 (1H, м), 3,97 - 4,17 (2H, м), 4,80 (1H, д, J = 13 Гц), 4,81 (1H, д, J = 18 Гц), 4,89 (1H, д, J = 18 Гц), 5,01 (1H, д, J = 13 Гц), 6,72 (1H, д, J = 3 Гц), 7,30 (1H, дд, J = 3, 9 Гц), 7,40 (1H, c), 7,49 (1H, шир. т, J = 6 Гц), 7,90 (1H, д, J = 9 Гц).
B12 (7-Me-10-Br-)
Порошок светло-желтого цвета (из н-гексана-хлороформа)
C25H29N4O4Br, MS [M+H]+ = 529,
ИК νmax /KBr (см-1): 1645, 1595, 1515
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,11 (3H, т, J = 7 Гц), 2,18 - 2,33 (1H, м), 2,29 (6H, c), 2,40 - 2,65 (3H, м), 2,60 (3H, c), 3,20 - 3,35 (1H, м), 3,60 - 3,75 (1H, м), 4,77 (1H, д, J = 13 Гц), 4,87 (1H, д, J = 19 Гц), 4,93 (1H, д, J = 19 Гц), 5,06 (1H, д, J = 13 Гц), 7,40 - 7,48 (2H, м), 7,51 (1H, дд, J = 2, 9 Гц), 7,61 (1H, д, J = 9 Гц), 8,14 (1H, д, J = 2 Гц).
B13 (9-OMe-)
Порошок светло-желтого цвета (из н-гексана-хлороформа)
C25H30N4O5, MS [M+H]+ = 467,
ИК νmax /KBr (см-1): 3360, 1650, 1615, 1585, 1515
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,08 (3H, т, J = 7 Гц), 2,18 - 2,34 (1H, м), 2,23 (6H, с), 2,38 - 2,57 (3H, м), 3,16 - 3,29 (1H, м), 3,58 - 3,72 (1H, м), 3,96 (3H, c), 4,79 (1H, д, J = 13 Гц), 5,02 (1H, д, J = 19 Гц), 5,08 (1H, д, J = 13 Гц), 5,09 (1H, д, J = 19 Гц), 6,77 (1H, д, J = 8 Гц), 7,38 (1H, шир. т, J = 5 Гц), 7,57 (1H, дд, J = 8, 8 Гц), 7,63 (1H, д, J = 8 Гц), 8,50 (1H, c).
Спектральные характеристики 17-O-ацил-21-амидных соединений приведены ниже.
C1
Т. пл. 101-106oC, светло-желтые иглы (из н-гексана-хлороформа)
C31H40N4O6S•H2O, MS [M+H]+ = 597,
Элементный анализ (C, H, N): найдено (вычислено): 60.67, 6.58, 8.96, (60.57, 6.89, 9.11),
ИК νmax /KBr (см-1): 1725, 1650, 1620, 1590, 1510.
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,09 (3H, т, J = 7 Гц), 1,54 (3H, т, J = 7 Гц), 2,09 (3H, c), 2,22 - 2,38 (1H, м), 2,28 (6H, c), 2,41 - 2,68 (5H, м), 2,57 (3H, c), 2,72 - 2,80 (2H, c), 3,24 - 3,34 (1H, м), 3,42 - 3,53 (1H, м), 4,13 (2H, кв., J = 7 Гц), 4,82 - 5,37 (1H, шир.), 4,96 (1H, д, J = 19 Гц), 5,07 (1H, д, J = 19 Гц), 5,49 (1H, д, J = 12 Гц), 5,53 (1H, д, J = 12 Гц), 6,88 (1H, шир. c), 7,35 (1H, дд, J = 3, 9 Гц), 7,38 (1H, шир. т, J = 6 Гц), 7,49 (1H, c), 7,98 (1H, д, J = 9 Гц).
C2
Т. пл. 108 - 118oC, желтого цвета (из н-гексана-хлороформа)
C29H35N4O5BrS•1/2H2O, MS [M+H]+ = 631,
Элементный анализ
найдено: C 54,08 H 5,76 N 8,48
вычислено: C 54,37 H 5,66 N 8,75
ИК νmax /KBr (см-1): 1725, 1650, 1600, 1515.
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,17 (3H, т, J = 7 Гц), 2,09 (3H, c), 2,22 - 2,38 (1H, м), 2,29 (6H, c), 2,43 - 2,82 (7H, м), 2,65 (3H, c), 3,24 - 3,35 (1H, м), 3,44 - 3,57 (1H, м), 4,91 (1H, д, J = 19 Гц), 5,01 (1H, д, J = 19 Гц), 5,49 (2H, c), 7,48 (1H, дд, J = 2, 9 Гц; 1H, c), 7,53 (1H, шир. т, J = 6 Гц), 7,59 (1H, д, J = 9 Гц), 8,14 (1H, д, J = 2 Гц).
C3
Т. пл. 130 - 133oC, желтый порошок (из н-гексана-хлороформа)
[α]
C29H35N4O5Cl•1/2H2O, MS [M+H]+ = 555,
Элементный анализ
найдено: C 61,74 H 6,43 N 9,66
вычислено: C 61,75 H 6,43 N 9,93
ИК νmax /KBr (см-1): 1730, 1650, 1600, 1515.
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,11 (3H, т, J = 7 Гц), 1,12 (3H, т, J = 7 Гц), 1,34 (3H, т, J = 8 Гц), 2,20 - 2,59 (6H, м), 2,26 (6H, c), 2,92 - 3,10 (2H, м), 3,21 - 3,35 (1H, м), 3,38 - 3,51 (1H, м), 4,99 (1H, д, J = 19 Гц), 5,10 (1H, д, J = 19 Гц), 5,26 - 5,60 (1H, шир.), 5,47 (1H, д, J = 12 Гц), 5,50 (1H, д, J = 12 Гц), 7,43 (1H, шир. т, J = 5 Гц), 7,49 (1H, c), 7,62 (1H, дд, J = 2, 9 Гц), 7,73 (1H, д, J = 2 Гц), 7,92 (1H, д, J = 9 Гц).
C4
Т. пл. 136 - 138oC, желтый порошок (из н-гексана-хлороформа)
[α]
C30H37N4O5Cl•1/2H2O, MS [M+H]+ = 569,
Элементный анализ
найдено: C 62,69 H 6,58 N 9,73
вычислено: C 62,33 H 6,63 N 9,69
ИК νmax /KBr (см-1): 1725, 1650, 1595, 1515.
1H ЯМР ( δ ч. на млн.) в CDCl3: 0,92 (3H, т, J = 7 Гц), 1,12 (3H, т, J = 7 Гц), 1,33 (3H, т, J = 8 Гц), 1,64 (2H, секстет, J = 7 Гц), 2,16 - 2,35 (3H, м), 2,25 (6H, c), 2,38 - 2,59 (3H, м), 2,90 - 3,07 (2H, м), 3,21 - 3,32 (1H, м), 3,39 - 3,50 (1H, м), 4,96 (1H, д, J = 19 Гц), 5,07 (1H, д, J = 19 Гц), 5,31 - 5,06 (1H, шир.), 5,45 (1H, д, J = 12 Гц), 5,50 (1H, д, J = 12 Гц), 7,46 (1H, шир. т, J = 5 Гц), 7,47 (1H, c), 7,60 (1H, дд, J = 2, 9 Гц), 7,68 (1H, д, J = 2 Гц), 7,89 (1H, д, J = 9 Гц).
C5
Т. пл. 139 - 144oC, желтый порошок (из н-гексана-хлороформа)
[α]
C30H37N4O5ClS•1/2H2O, MS [M+H]+ = 601,
Элементный анализ
найдено: C 59,28 H 6,31 N 9,01
вычислено: 59,05 H 6,28 N 9,18
ИК νmax /KBr (см-1): 1725, 1650, 1600, 1515.
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,10 (3H, т, J = 7 Гц), 1,34 (3H, т, J = 8 Гц), 2,09 (3H, c), 2,23 - 2,35 (1H, м), 2,31 (6H, c), 2,44 - 2,68 (5H, м), 2,70 - 2,80 (2H, м), 2,93 - 3,09 (2H, м), 3,24 - 3,35 (1H, м), 3,43 - 3,57 (1H, м), 5,00 (1H, д, J = 19 Гц), 5,09 (1H, д, J = 19 Гц), 5,51 (2H, c), 7,51 (1H, c), 7,52 (1H, шир. т, J = 5 Гц), 7,62 (1H, дд, J = 2, 9 Гц), 7,74 (1H, д, J = 2 Гц), 7,93 (1H, д, J = 9 Гц).
C6
Т. пл. 149 - 151oC, светло-желтые иглы (из н-гексана-хлороформа)
[α]
C30H37N4O5BrS, MS [M+H]+ = 645,
Элементный анализ
найдено: C 55,95 H 5,70 N 8,50
вычислено: C 55,81 H 5,78 N 8,68
ИК νmax /KBr (см-1): 1725, 1650, 1610, 1515.
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,09 (3H, т, J = 7 Гц), 1,36 (3H, т, J = 8 Гц), 2,10 (3H, c), 2,22 - 2,35 (1H, м), 2,25 (6H, c), 2,38 - 2,55 (3H, м), 2,57 - 2,68 (2H, м), 2,71 - 2,81 (2H, м), 2,97 - 3,10 (2H, м), 3,24 - 3,34 (1H, м), 3,38 - 3,50 (1H, м), 4,98 - 5,34 (1H, шир.), 5,05 (1H, д, J = 19 Гц), 5,13 (1H, д, J = 19 Гц), 5,49 (1H, д, J = 12 Гц), 5,57 (1H, д, J = 12 Гц), 7,40 (1H, шир. т, J = 6 Гц), 7,53 (1H, c), 7,77 (1H, дд, J = 2, 9 Гц), 7,90 (1H, д, J = 9 Гц), 8,00 (1H, д, J = 2 Гц).
C7
Т. пл. 130 - 134oC, желтый порошок (из н-гексана-хлороформа)
[α]
C31H40N4O5S, MS [M+H]+ = 581,
Элементный анализ
найдено: C 63,88 H 7,02 N 9,43
вычислено: C 64,11 H 6,94 N 9,65
ИК νmax /KBr (см-1): 1725, 1650, 1600, 1515.
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,09 (3H, т, J = 7 Гц), 1,32 (3H, т, J = 8 Гц), 2,09 (3H, c), 2,20 - 2,36 (1H, м), 2,26 (6H, c), 2,41 - 2,55 (3H, м), 2,54 (3H, c), 2,57 - 2,67 (2H, м), 2,71 - 2,81 (2H, м), 2,93 - 3,09 (2H, м), 3,25 - 3,35 (1H, м), 3,41 - 3,52 (1H, м), 4,99 (1H, д, J = 19 Гц), 5,07 (1H, д, J = 19 Гц), 5,50 (1H, д, J = 12 Гц), 5,54 (1H, д, J = 12 Гц), 7,44 (1H, шир. т, J = 6 Гц), 7,51 (1H, дд, J = 2, 8 Гц), 7,52 (1H, c), 7,55 (1H, шир. c), 7,94 (1H, д, J = 8 Гц).
C8
Т. пл. 164 - 166oC, светло-желтый порошок (из н-гексана-хлороформа)
[α]
C29H35N4O5F•2H2O, MS [M+H]+ = 539,
Элементный анализ
найдено: C 60,24 H 6,80 N 9,84
вычислено: C 60,61 H 6,84 N 9,75
ИК νmax /KBr (см-1): 1725, 1650, 1595, 1510.
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,08 (3H, т, J = 7 Гц), 1,13 (3H, т, J = 7 Гц), 1,36 (3H, т, J = 8 Гц), 2,24 - 2,63 (6H, м), 2,30 (6H, c), 3,02 - 3,20 (2H, cм), 3,25 - 3,55 (2H, м), 5,07 (1H, д, J = 19 Гц), 5,14 (1H, д, J = 19 Гц), 5,21 - 5,41 (1H, шир.), 5,51 (2H, шир. c), 7,31 (1H, ддд, J = 2, 9, 10 Гц), 7,41 (1H, шир. т, J = 5 Гц), 7,55 (1H, c), 7,69 (1H, дд, J = 2, 10 Гц), 7,93 (1H, дд, J = 6, 9 Гц).
C9
Т. пл. 134 - 137oC, светло-желтый порошок (из н-гексана-хлороформа)
[α]
C30H37N4O5F•3/2H2O, MS [M+H]+ = 553,
Элементный анализ
найдено: C 62,06 H 6,85 N 9,70
вычислено: C 62,16 H 6,96 N 9,67
ИК νmax /KBr (см-1): 1725, 1650, 1595, 1510.
1H ЯМР ( 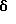 ч. на млн.) в CDCl3: 0,93 (3H, т, J = 7 Гц), 1,09 (3H, т, J = 7 Гц), 1,36 (3H, т, J = 8 Гц), 1,65 (2H, секстет, J = 7 Гц), 2,20 - 2,36 (3H, м), 2,39 - 2,53 (3H, м), 3,02 - 3,17 (2H, м), 3,25 - 3,17 (2H, м), 3,25 - 3,35 (1H, м), 3,38 - 3,49 (1H, м), 5,05 (1H, д, J = 19 Гц), 5,12 (1H, д, J = 19 Гц), 5,22 - 5,40 (1H, шир.), 5,47 (1H, д, J = 12 Гц), 5,53 (1H, д, J = 12 Гц), 7,30 (1H, ддд, J = 3, 9, 10 Гц), 7,38 (1H, шир. т, J = 5 Гц), 7,53 (1H, c), 7,67 (1H, дд, J = 3, 10 Гц), 7,91 (1H, дд, J = 6, 9 Гц).
ч. на млн.) в CDCl3: 0,93 (3H, т, J = 7 Гц), 1,09 (3H, т, J = 7 Гц), 1,36 (3H, т, J = 8 Гц), 1,65 (2H, секстет, J = 7 Гц), 2,20 - 2,36 (3H, м), 2,39 - 2,53 (3H, м), 3,02 - 3,17 (2H, м), 3,25 - 3,17 (2H, м), 3,25 - 3,35 (1H, м), 3,38 - 3,49 (1H, м), 5,05 (1H, д, J = 19 Гц), 5,12 (1H, д, J = 19 Гц), 5,22 - 5,40 (1H, шир.), 5,47 (1H, д, J = 12 Гц), 5,53 (1H, д, J = 12 Гц), 7,30 (1H, ддд, J = 3, 9, 10 Гц), 7,38 (1H, шир. т, J = 5 Гц), 7,53 (1H, c), 7,67 (1H, дд, J = 3, 10 Гц), 7,91 (1H, дд, J = 6, 9 Гц).
C10
Т. пл. 134 - 137oC, светло-желтый порошок (из н-гексана-хлороформа)
[α]
C30H37N4O5SF•3/2H2O, MS [M+H]+ = 585,
Элементный анализ
найдено: C 58,74 H 6,48 N 9,21
вычислено: C 58,90 H 6,59 N 9,16
ИК νmax /KBr (см-1): 1730, 1650, 1595, 1510.
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,09 (3H, т, J = 7 Гц), 1,36 (3H, т, J = 8 Гц), 2,10 (3H, c), 2,20 - 2,36 (1H, м), 2,40 - 2,54 (3H, м), 2,58 - 2,68 (2H, м), 2,72 - 2,82 (2H, м), 3,04 - 3,18 (2H, м), 3,25 - 3,36 (1H, м), 3,39 - 3,50 (1H, м), 4,99 - 5,31 (1H, шир.), 5,06 (1H, д, J = 19 Гц), 5,14 (1H, д, J = 19 Гц), 5,49 (1H, д, J = 12 Гц), 5,58 (1H, д, J = 12 Гц), 7,31 (1H, ддд, J = 3, 9, 10 Гц), 7,39 (1H, шир. т, J = 5 Гц), 7,55 (1H, c), 7,68 (1H, дд, J = 3, 10 Гц), 7,93 (1H, дд, J = 6, 9 Гц).
C11
Т. пл. 180 - 182oC, светло-желтый порошок (из н-гексана-хлороформа)
[α]
C34H37N4O6F•H2O, MS [M+H]+ = 617,
Элементный анализ
найдено: C 64,34 H 6,40 N 8,98
вычислено: C 64,34 H 6,19 N 8,83
ИК νmax /KBr (см-1): 1700, 1650, 1600, 1510.
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,12 (3H, т, J = 7 Гц), 1,34 (3H, т, J = 8 Гц), 2,18 (6H, c), 2,29 - 2,44 (3H, м), 2,47 - 2,59 (1H, м), 2,99 - 3,22 (3H, м), 3,30 - 3,42 (1H, м), 5,03 (1H, д, J = 19 Гц), 5,12 (1H, д, J = 19 Гц), 5,58 - 5,93 (1H, шир.), 5,73 (1H, д, J = 12 Гц), 5,18 (1H, д, J = 12 Гц), 6,82 (2H, д, J = 9 Гц), 7,22 - 7,28 (1H, м), 7,51 (1H, шир. т, J = 5 Гц), 7,57 (1H, c), 7,63 (1H, дд, J = 3, 10 Гц), 7,85 (1H, дд, J = 6, 9 Гц), 7,96 (2H, д, J = 9 Гц).
C12
Т. пл. 131 - 133oC, светло-желтые кристаллы (из н-гексана-хлороформа)
[α]
C30H37N4O5ClS•H2O, MS [M+H]+ = 601,
Элементный анализ
найдено: C 57,80 H 6,05 N 8,91
вычислено: C 58,20 H 6,35 N 9,05
ИК νmax /KBr (см-1): 1730, 1650, 1605, 1515.
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,09 (3H, т, J = 7 Гц), 1,37 (3H, т, J = 8 Гц), 2,10 (3H, c), 2,22 - 2,36 (1H, м), 2,26 (6H, c), 2,40 - 2,54 (3H, м), 2,56 - 2,68 (2H, м), 1,70 - 2,81 (2H, м), 3,02 - 3,18 (2H, м), 3,25 - 3,35 (1H, м), 3,40 - 3,52 (1H, м), 4,97 - 5,35 (1H, шир.), 5,05 (1H, д, J = 19 Гц), 5,13 (1H, д, J = 19 Гц), 5,49 (1H, д, J = 11 Гц), 5,57 (1H, д, J = 11 Гц), 7,42 (1H, шир. т, J = 6 Гц), 7,46 (1H, дд, J = 2, 9 Гц), 7,54 (1H, c), 7,85 (1H, д, J = 9 Гц), 8,02 (1H, д, J = 2 Гц).
C13
Т. пл. 168 - 170oC, желтый порошок (из н-гексана-хлороформа)
[α]
C29H34N4O5F2•H2O, MS [M+H]+ = 557,
Элементный анализ
найдено: C 60,91 H 6,22 N 9,75
вычислено: C 60,62 H 6,31 N 9,75
ИК νmax /KBr (см-1): 1725, 1655, 1600, 1515.
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,07 (3H, т, J = 7 Гц), 1,13 (3H, т, J = 7 Гц), 1,36 (3H, т, J = 8 Гц), 2,18 - 2,52 (6H, м), 2,24 (6H, c), 3,07 (2H, кв, J = 8 Гц), 3,25 - 3,36 (1H, м), 3,38 - 3,49 (1H, м), 5,06 - 5,38 (1H, шир.), 5,10 (1H, д, J = 19 Гц), 5,16 (1H, д. т, J = 19 Гц), 5,48 (1H, д, J = 12 Гц), 5,56 (1H, д, J = 12 Гц), 7,36 (1H, шир. т, J = 5 Гц), 7,55 (1H, c), 7,69 (1H, д, J = 8, 11 Гц), 7,86 (1H, д, J = 8, 11 Гц).
C14
Т. пл. 160 - 162oC, желтый порошок (из н-гексана-хлороформа)
[α]
C30H36N4O5F2•1/2H2O, MS [M+H]+ = 571,
Элементный анализ
найдено: C 61,73 H 6,53 N 9,75
вычислено: C 62,16 H 6,43 N 9,67
ИК νmax /KBr (см-1): 1720, 1655, 1600, 1520.
1H ЯМР ( δ ч. на млн.) в CDCl3: 0,93 (3H, т, J = 7 Гц), 1,07 (3H, т, J = 7 Гц), 1,36 (3H, т, J = 8 Гц), 1,65 (2H, секстет, J = 7 Гц), 2,16 - 2,36 (3H, м), 2,24 (6H, c), 2,38 - 2,52 (3H, м), 3,07 (2H, кв, J = 8 Гц), 3,25 - 3,36 (1H, м), 3,37 - 3,48 (1H, м), 5,05 - 5,34 (1H, шир.), 5,10 (1H, д, J = 19 Гц), 5,16 (1H, д, J = 19 Гц), 5,47 (1H, д, J = 12 Гц), 5,57 (1H, д, J = 12 Гц), 7,35 (1H, шир. т, J = 5 Гц), 7,55 (1H, c), 7,70 (1H, дд, J = 8, 11 Гц), 7,86 (1H, дд, J = 8, 11 Гц).
C15
Т. пл. 119 - 125oC, желтые иглы (из н-гексана-хлороформа)
[α]
C30H36N4O5F2S•H2O, MS [M+H]+ = 603,
Элементный анализ
найдено: C 57,83 H 6,03 N 9,08
вычислено: C 58,05 H 6,17 N 9,03
ИК νmax /KBr (см-1): 1725, 1650, 1600, 1515.
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,08 (3H, т, J = 7 Гц), 1,36 (3H, т, J = 8 Гц), 2,10 (3H, c), 2,20 - 2,34 (1H, м), 2,25 (6H, c), 2,40 - 2,54 (3H, м), 2,58 - 2,70 (2H, м), 2,71 - 2,83 (2H, м), 3,07 (2H, кв, J = 8 Гц), 3,26 - 3,52 (1H, м), 5,08 (1H, д, J = 19 Гц), 5,15 (1H, д, J = 19 Гц), 5,49 (1H, д, J = 12 Гц), 5,60 (1H, д, J = 12 Гц), 7,43 (1H, шир. т, J = 5 Гц), 7,55 (1H, c), 7,67 (1H, дд, J = 8, 11 Гц), 7,83 (1H, дд, J = 8, 11 Гц).
C16
Т. пл. 175 - 178oC, бесцветные иглы (из н-гексана-хлороформа)
[α]
C34H37N4O6F2S•1/2H2O, MS [M+H]+ = 635,
Элементный анализ
найдено: C 63,74 H 5,79 N 8,93
вычислено: C 63,44 H 5,79 N 8,70
ИК νmax /KBr (см-1): 1695, 1650, 1600, 1510.
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,10 (3H, т, J = 7 Гц), 1,35 (3H, т, J = 8 Гц), 2,19 (6H, c), 2,26 - 2,55 (4H, м), 3,05 (2H, кв, J = 8 Гц), 3,14 - 3,25 (1H, м), 3,30 - 3,42 (1H, м), 5,08 (1H, д, J = 19 Гц), 5,15 (1H, д, J = 19 Гц), 5,70 (1H, д, J = 12 Гц), 5,84 (1H, д, J = 12 Гц), 6,84 (2H, д, J = 9 Гц), 7,48 (1H, шир. т, J = 5 Гц), 7,57 (1H, c), 7,65
(1H, дд, J = 8, 12 Гц), 7,83 (1H, дд, J = 8, 11 Гц), 7,97 (2H, д, J = 9 Гц).
C17
Т. пл. 153 - 156oC, желтый порошок (из н-гексана-хлороформа)
[α]
C29H34N4O5Cl2•1/2H2O, MS [M+H]+ = 589,
Элементный анализ
найдено: C 58,12 H 5,74 N 9,35
вычислено: C 58,20 H 5,89 N 9,36
ИК νmax /KBr (см-1): 1725, 1650, 1600, 1515.
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,11 (3H, т, J = 7 Гц), 1,12 (3H, т, J = 7 Гц), 1,38 (3H, т, J = 8 Гц), 2,19 - 2,38 (3H, м), 2,27 (6H, c), 2,40 - 2,58 (3H, м), 2,96 - 3,14 (2H, м), 3,21 - 3,32 (1H, м), 3,40 - 3,51 (1H, м), 4,99 (1H, д, J = 19 Гц), 5,08 (1H, д, J = 19 Гц), 5,45 (1H, д, J = 12 Гц), 5,49 (1H, д, J = 12 Гц), 7,46 (1H, c), 7,49 (1H, шир. т, J = 5 Гц), 7,89 (1H, c), 8,05 (1H, c).
C18
Т. пл. 142 - 147oC, желтый порошок (из н-гексана-хлороформа)
[α]
C30H36N4O5Cl2•1/2H2O, MS [M+H]+ = 603,
Элементный анализ
найдено: C 58,97 H 5,95 N 9,06
вычислено: C 58,82 H 6,09 N 9,15
ИК νmax /KBr (см-1): 1725, 1650, 1600, 1515.
1H ЯМР ( δ ч. на млн.) в CDCl3: 0,92 (3H, т, J = 7 Гц), 1,11 (3H, т, J = 7 Гц), 1,38 (3H, т, J = 8 Гц), 1,64 (2H, секстет, J = 7 Гц), 2,18 - 2,35 (3H, м), 2,26 (6H, c), 2,39 - 2,56 (3H, м), 2,98 - 3,14 (2H, м), 3,21 - 3,32 (1H, м), 3,38 - 3,52 (1H, м), 5,00 (1H, д, J = 19 Гц), 5,09 (1H, д, J = 19 Гц), 5,48 (2H, c), 7,45 (1H, шир. т, J = 5 Гц), 7,47 (1H, c), 7,92 (1H, c), 8,07 (1H, c).
C19
Т. пл. 139 - 142oC, желтые иглы (из н-гексана-хлороформа)
[α]
C30H36N4O6Cl2•1/2H2O, MS [M+H]+ = 635,
Элементный анализ
найдено: C 55,94 H 5,69 N 8,79
вычислено: C 55,90 H 5,79 N 8,69
ИК νmax /KBr (см-1): 1725, 1650, 1600, 1515.
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,09 (3H, т, J = 7 Гц), 1,38 (3H, т, J = 8 Гц), 2,09 (3H, c), 2,21 - 2,37 (1H, м), 2,29 (6H, c), 2,43 - 2,67 (5H, м), 2,70 - 2,81 (2H, м), 2,99 - 3,16 (2H, м), 3,24 - 3,35 (1H, м), 3,42 - 3,55 (1H, м), 5,03 (1H, д, J = 19 Гц), 5,11 (1H, д, J = 19 Гц), 5,54 (1H, д, J = 12 Гц), 7,49 (1H, шир. т, J = 6 Гц), 7,50 (1H, c), 7,96 (1H, c), 8,11 (1H, c).
C20
Т. пл. 112 - 117oC, светло-желтый порошок (из н-гексана-хлороформа)
[α]
C30H37N4O6F•3/2H2O, MS [M+H]+ = 569,
Элементный анализ
найдено: C 60,15 H 6,78 N 9,40
вычислено: C 60,49 H 6,77 N 9,41
ИК νmax /KBr (см-1): 1725, 1650, 1595, 1515.
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,12 (3H, т, J = 7 Гц), 1,13 (3H, т, J = 7 Гц), 1,31 (3H, т, J = 8 Гц), 2,21 - 2,63 (6H, м), 2,28 (6H, c), 2,88 - 3,08 (2H, м), 3,18 - 3,30 (1H, м), 3,40 - 3,52 (1H, м), 4,00 (3H, c), 4,89 (1H, д, J = 19 Гц), 5,02 (1H, д, J = 19 Гц), 5,41 (1H, д, J = 12 Гц), 5,50 (1H, д, J = 12 Гц), 6,89 (1H, д, J = 9 Гц), 7,40 (1H, c), 7,46 (1H, шир. т, J = 6 Гц), 7,57 (1H, д, J = 12 Гц).
C21
Т. пл. 109 - 113oC, светло-желтый порошок (из н-гексана-хлороформа)
[α]
C31H39N4O6F•2H2O, MS [M+H]+ = 583,
Элементный анализ
найдено: C 60,09 H 6,99 N 9,29
вычислено: C 60,18 H 7,01 N 9,06
ИК νmax /KBr (см-1): 1725, 1650, 1595, 1510.
1H ЯМР ( δ ч. на млн.) в CDCl3: 0,92 (3H, т, J = 7 Гц), 1,13 (3H, т, J = 7 Гц), 1,31 (3H, т, J = 8 Гц), 1,63 (2H, секстет, J = 7 Гц), 2,18 - 2,37 (3H, м), 2,28 (6H, с), 2,39 - 2,63 (3H, м), 2,87 - 3,07 (2H, м), 3,17 - 3,30 (1H, м), 3,41 - 3,53 (1H, м), 4,00 (3H, c), 4,89 (1H, д, J = 19 Гц), 5,02 (1H, д, J = 19 Гц), 5,34 - 5,57 (1H, шир.), 5,40 (1H, д, J = 12 Гц), 5,49 (1H, д, J = 12 Гц), 6,89 (1H, д, J = 9 Гц), 7,40 (1H, c), 7,46 (1H, шир. т, J = 6 Гц), 7,57 (1H, д, J = 12 Гц).
C22
Т. пл. 125 - 129oC, светло-желтый порошок (из н-гексана-хлороформа)
[α]
C31H39N4O6F•3/2H2O, MS [M+H]+ = 615,
Элементный анализ
найдено: C 59,82 H 6,40 N 9,02
вычислено: C 59,89 H 6,60 N 8,73
ИК νmax /KBr (см-1): 1725, 1650, 1600, 1510.
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,11 (3H, т, J = 7 Гц), 1,33 (3H, т, J = 8 Гц), 2,09 (3H, c), 2,22 - 2,36 (1H, м), 2,26 (6H, c), 2,39 - 2,69 (5H, м), 2,71 - 2,80 (2H, м), 2,94 - 3,10 (2H, м), 3,21 - 3,34 (1H, м), 3,21 - 3,34 (1H, м), 3,39 - 3,51 (1H, м), 4,03 (3H, c), 4,93 - 5,38 (1H, шир.), 4,97 (1H, д, J = 19 Гц), 5,07 (1H, д, J = 19 Гц), 5,50 (1H, д, J = 19 Гц), 5,50 (2H, c), 7,01 (1H, д, J = 9 Гц), 7,38 (1H, шир. т, J = 6 Гц), 7,44 (1H, c), 7,64 (1H, д, J = 12 Гц).
C23
Т. пл. 164 - 165oC, светло-желтый порошок (из н-гексана-хлороформа)
[α]
C30H37N4O5F•3/2H2O, MS [M+H]+ = 553,
Элементный анализ
найдено: C 61,88 H 6,85 N 9,71
вычислено: C 62,16 H 6,96 N 9,67
ИК νmax /KBr (см-1): 1725, 1650, 1595, 1510.
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,09 (3H, т, J = 7 Гц), 1,13 (3H, т, J = 7 Гц), 1,36 (3H, т, J = 8 Гц), 2,19 - 2,57 (6H, м), 2,25 (6H, c), 2,48 (3H, c), 2,99 - 3,16 (2H, м), 3,23 - 3,34 (1H, м), 3,38 - 3,49 (1H, м), 5,02 (1H, д, J = 19 Гц), 5,10 (1H, д, J = 19 Гц), 5,49 (2H, c), 7,38 (1H, шир. т, J = 5 Гц), 7,49 (1H, c), 7,58 (1H, д, J = 11 Гц), 7,67 (1H, д, J = 8 Гц).
C24
Т. пл. 148 - 154oC, светло-желтые иглы (из н-гексана-хлороформа)
[α]
C31H39N4O5F•1/2H2O, MS [M+H]+ = 567,
Элементный анализ
найдено: C 64,28 H 7,07 N 9,65
вычислено: C 64,68 H 7,00 N 9,73
ИК νmax /KBr (см-1): 1725, 1650, 1600, 1510.
1H ЯМР ( δ ч. на млн.) в CDCl3: 0,93 (3H, т, J = 7 Гц), 1,09 (3H, т, J = 7 Гц), 1,36 (3H, т, J = 8 Гц), 1,64 (2H, секстет, J = 7 Гц), 2,19 - 2,35 (3H, м), 2,24 (6H, c), 2,38 - 2,54 (3H, м), 2,99 - 3,16 (2H, м), 3,23 - 3,34 (1H, м), 3,38 - 3,50 (1H, м), 5,02 (1H, д, J = 19 Гц), 5,10 (1H, д, J = 19 Гц), 5,21 - 5,42 (1H, шир.), 5,47 (1H, д, J = 12 Гц), 5,51 (1H, д, J = 12 Гц), 7,38 (1H, шир. т, J = 5 Гц), 7,49 (1H, c), 7,58 (1H, д, J = 11 Гц), 7,68 (1H, д, J = 8 Гц).
C25
Т. пл. 107 - 121oC, желтые иглы (из н-гексана-хлороформа)
[α]
C31H39N4O5FS•2H2O, MS [M+H]+ = 599,
Элементный анализ
найдено: C 60,75 H 6,67 N 9,15
вычислено: C 60,55 H 6,83 N 8,83
ИК νmax /KBr (см-1): 1725, 1650, 1595, 1510.
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,10 (3H, т, J = 7 Гц), 1,36 (3H, т, J = 8 Гц), 2,09 (3H, c), 2,22 - 2,35 (1H, м), 2,28 (6H, c), 2,40 - 2,66 (5H, м), 2,72 - 2,81 (2H, м), 2,97 - 3,14 (2H, м), 3,24 - 3,34 (1H, м), 3,43 - 3,54 (1H, м), 4,98 (1H, д, J = 19 Гц), 5,07 (1H, д, J = 19 Гц), 5,51 (2H, c), 7,47 (1H, c), 7,48 (1H, шир. т, J = 5 Гц), 7,54 (1H, д, J = 11 Гц), 7,63 (1H, д, J = 8 Гц).
C26
Т. пл. 189 - 192oC, светло-желтый порошок (из н-гексана-хлороформа)
[α]
C35H39N4O6F•H2O, MS [M+H]+ = 631,
Элементный анализ
найдено: C 64,43 H 6,57 N 8,73
вычислено: C 64,80 H 6,37 N 8,64
ИК νmax /KBr (см-1): 1700, 1650, 1605, 1510.
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,12 (3H, т, J = 7 Гц), 1,34 (3H, т, J = 8 Гц), 2,17 (6H, c), 2,28 - 2,42 (3H, м), 2,45 (3H, c), 2,48 - 2,60 (1H, м), 2,96 - 3,18 (3H, м), 3,28 - 3,39 (1H, м), 4,98 (1H, д, J = 19 Гц), 5,09 (1H, д, J = 19 Гц), 5,52 - 5,98 (1H, шир.), 5,74 (1H, д, J = 12 Гц), 5,78 (1H, д, J = 12 Гц), 6,82 (2H, д, J = 9 Гц), 7,48 - 7,55 (3H, м), 7,60 (1H, д, J = 8 Гц), 7,95 (1H, д, J = 9 Гц).
C27
Т. пл. 82 - 87oC, желтые призмы (из н-гексана-хлороформа)
[α]
C33H44N4O8•H2O, MS [M+H]+ = 625,
Элементный анализ
найдено: C 61,85 H 7,12 N 8,81
вычислено: C 61,67 H 7,21 N 8,72
ИК νmax /KBr (см-1): 1730, 1650, 1620, 1585, 1510.
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,08 (3H, т, J = 7 Гц), 1,12 (3H, т, J = 7 Гц), 1,30 (3H, т, J = 8 Гц), 2,25 - 2,41 (3H, м), 2,35 (6H, c), 2,43 - 2,66 (3H, м), 2,91 - 3,07 (2H, м), 3,27 - 3,37 (1H, м), 3,39 (3H, c), 3,46 - 3,63 (3H, м), 3,83 - 3,93 (2H, м), 4,99 (1H, д, J = 19 Гц), 5,08 (1H, д, J = 19 Гц), 5,27 - 5,62 (1H, шир.), 5,38 (1H, д, J = 7 Гц), 5,41 (1H, д, J = 7 Гц), 5,46 (1H, д, J = 12 Гц), 5,50 (1H, д, J = 12 Гц), 7,34 (1H, д, J = 3 Гц), 7,39 (1H, дд, J = 3, 9 Гц), 7,44 - 7,55 (2H, c, шир. т), 7,95 (1H, д, J = 9 Гц).
C28
Т. пл. 214 - 215oC, светло-желтый порошок (из н-гексана-хлороформа)
[α]
C29H36N4O6, MS [M+H]+ = 537,
Элементный анализ
найдено: C 64,67 H 6,69 N 10,22
вычислено: C 64,91 H 6,76 N 10,44
ИК νmax /KBr (см-1): 1720, 1645, 1620, 1585.
1H ЯМР ( δ ч. на млн.) в DMCO-d6: 0,87 (3H, т, J = 7 Гц), 1,05 (3H, т, J = 7 Гц), 1,31 (3H, т, J = 8 Гц), 2,08 - 2,24 (2H, м), 2,27 (2H, кв., J = 8 Гц), 2,74 (6H, c), 2,99 - 3,15 (4H, м), 3,22 - 3,54 (2H, м), 5,25 (2H, c), 5,31 (1H, д, J = 11 Гц), 5,37 (1H, д, J = 11 Гц), 6,28 (1H, c), 7,38 - 7,47 (3H, м), 8,02 (1H, д, J = 10 Гц), 8,30 (1H, шир. т, J = 6 Гц), 9,43 - 9,88 (1H, шир.), 10,36 (1H, c).
C29
Т. пл. 78 - 82oC, жетые иглы (из н-гексана-хлороформа)
[α]
C34H46N4O8•3/2H2O, MS [M+H]+ = 639,
Элементный анализ
найдено: C 61,61 H 7,03 N 8,38
вычислено: C 61,34 H 7,42 N 8,42
ИК νmax /KBr (см-1): 1725, 1650, 1620, 1585, 1510.
1H ЯМР ( δ ч. на млн.) в CDCl3: 0,93 (3H, т, J = 7 Гц), 1,08 (3H, т, J = 7 Гц), 1,30 (3H, т, J = 8 Гц), 1,64 (2H, секстет, J = 7 Гц), 2,23 - 2,38 (3H, м), 2,34 (6H, c), 2,43 - 2,64 (3H, м), 2,89 - 3,08 (2H, м), 3,25 - 3,36 (1H, м), 3,39 (3H, c), 3,45 - 3,63 (3H, м), 3,83 - 3,93 (2H, м), 4,98 (1H, д, J = 19 Гц), 5,08 (1H, д, J = 19 Гц), 5,30 - 5,58 (1H, шир.), 5,37 (1H, д, J = 7 Гц), 5,41 (1H, д, J = 7 Гц), 5,46 (1H, д, J = 12 Гц), 5,49 (2H, д, J = 12 Гц), 7,34 (1H, д, J = 3 Гц), 7,39 (1H, дд, J = 3, 9 Гц), 7,44 - 7,52 (2H, с, шир-т), 7,95 (1H, д, J = 9 Гц).
C30
Т. пл. 218 - 219oC, бесцветный порошок (из н-гексана-хлороформа)
[α]
C30H38N4O6, MS [M+H]+ = 551,
Элементный анализ
найдено: C 65,34 H 6,99 N 10,04
вычислено: C 65,44 H 6,96 N 10,17
ИК νmax /KBr (см-1): 1715, 1645, 1620, 1585.
1H ЯМР ( δ ч. на млн.) в DMCO-d6: 0,87 (3H, т, J = 7 Гц), 0,90 (3H, т, J = 7 Гц), 1,30 (3H, т, J = 8 Гц), 1,55 (2H, секстет, J = 7 Гц), 2,12 (6H, c), 2,25 - 2,32 (6H, м), 3,02 - 3,25 (4H, м), 5,26 (2H, c), 5,29 (1H, д, J = 11 Гц), 6,28 (1H, c), 7,37 (1H, c), 7,38 - 7,45 (2H, м), 7,78 (1H, шир-т, J = 6 Гц), 8,04 (1H, д, J = 10 Гц), 10,29 (1H, шир-c).
C31
Т. пл. 84 - 90oC, светло-желтый порошок (из н-гексана-хлороформа)
[α]
C34H46N4O8S•H2O, MS [M+H]+ = 671,
Элементный анализ
найдено: C 59,33 H 6,77 N 7,96
вычислено: C 58,28 H 7,02 N 8,13
ИК νmax /KBr (см-1): 1725, 1650, 1620, 1585, 1510.
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,07 (3H, т, J = 7 Гц), 1,31 (3H, т, J = 8 Гц), 2,09 (3H, c), 2,24 - 2,41 (1H, м), 2,36 (6H, c), 2,42 - 2,68 (5H, м), 2,71 - 2,80 (2H, м), 2,93 - 3,07 (2H, м), 3,27 - 3,41 (1H, м), 3,39 (3H, c), 3,49 - 3,61 (3H, м), 3,83 - 3,92 (2H, м), 5,00 (1H, д, J = 19 Гц), 5,10 (1H, д, J = 19 Гц), 5,22 - 5,50 (1H, шир.), 5,38 (1H, д, J = 7 Гц), 5,42 (1H, д, J = 7 Гц), 5,52 (2H, c), 7,37 (1H, д, J = 3 Гц), 7,41 (1H, дд, J = 3, 9 Гц), 7,44 - 7,54 (2H, шир-м), 7,97 (1H, д, J = 9 Гц).
C32
Т. пл. 172 - 175oC, светло-желтый порошок (из н-гексана-хлороформа)
[α]
C30H38N4O6S, MS [M+H]+ = 583,
Элементный анализ
найдено: C 61,62 H 6,52 N 9,44
вычислено: C 61,84 H 6,57 N 9,61
ИК νmax /KBr (см-1): 1725, 1645, 1620, 1585.
1H ЯМР ( δ ч. на млн.) в DMCO-d3: 0,87 (3H, т, J = 7 Гц), 1,30 (3H, т, J = 8 Гц), 2,02 - 2,32 (4H, м), 2,07 (3H, c), 2,13 (6H, c), 2,52 - 2,59 (2H, м), 2,64 - 2,72 (2H, м), 3,00 - 3,26 (4H, м), 5,26 (2H, c), 5,34 (1H, д, J = 11 Гц), 5,42 (1H, д, J = 11 Гц), 6,22 (1H, c), 7,34 - 7,48 (3H, м), 7,79 (1H, шир-т, J = 6 Гц), 8,04 (1H, д, J = 10 Гц), 10,30 (1H, шир.).
C33
Т. пл. 78 - 86oC, желтые иглы (из н-гексана-хлороформа)
C34H44N4O8•1/2H2O, MS [M+H]+ = 637,
Элементный анализ
найдено: C 63,02 H 7,02 N 8,67
вычислено: C 63,24 H 7,02 N 8,68
ИК νmax /KBr (см-1): 1710, 1650, 1620, 1585, 1510.
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,08 (3H, т, J = 7 Гц), 1,31 (3H, т, J = 8 Гц), 1,83 (3H, дд, J = 2, 7 Гц), 2,25 (6H, c), 2,26 - 2,37 (1H, м), 2,39 - 2,53 (3H, м), 2,94 - 3,08 (2H, м), 3,21 - 3,47 (1H, м), 3,39 (3H, c), 3,54 - 3,61 (2H, м), 3,84 - 3,91 (2H, м), 5,04 (1H, д, J = 19 Гц), 5,12 (1H, д, J = 19 Гц), 5,39 (1H, д, J = 7 Гц), 5,42 (1H, д, J = 7 Гц), 5,53 (1H, д, J = 12 Гц), 5,61 (1H, д, J = 12 Гц), 5,80 - 5,88 (1H, м), 6,98 (1H, д.кв., J = 7, 14 Гц), 7,32 - 7,55 (4H, м), 8,00 (1H, д, J = 9 Гц).
C34
Желтый порошок (из н-гексана-хлороформа)
C30H36N4O6, MS [M+H]+ = 549
ИК νmax /KBr (см-1): 1705, 1675, 1645, 1590, 1510.
1H ЯМР ( δ ч. на млн.) в DMCO-d3: 0,88 (3H, т, J = 7 Гц), 1,31 (3H, т, J = 8 Гц), 1,84 (3H, дд, J = 2, 7 Гц), 2,08 - 2,26 (2H, м), 2,74 (6H, c), 2,98 - 3,04 (4H, м), 3,29 - 3,52 (2H, м), 5,26 (2H, c), 5,35 (1H, д, J = 11 Гц), 5,42 (1H, д, J = 11 Гц), 5,80 - 5,90 (1H, м), 6,30 (1H, c), 6,87 (1H, д, кв, J = 7, 16 Гц), 7,38 - 7,48 (3H, м), 8,20 (1H, д, J = 3 Гц), 9,46 - 9,63 (1H, шир.), 10,35 (1H, c).
C35
Т. пл. 102 - 105oC, желтые призмы (из н-гексана-хлороформа)
C37H43N4O8F, MS [M+H]+ = 691,
ИК νmax /KBr (см-1): 1710, 1650, 1620, 1600, 1505.
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,14 (3H, т, J = 7 Гц), 1,27 (3H, т, J = 8 Гц), 2,16 (6H, c), 2,22 - 2,42 (3H, м), 2,49 - 2,62 (1H, м), 2,82 - 3,18 (3H, м), 3,18 - 3,42 (1H, м), 3,39 (3H, c), 3,50 - 3,64 (2H, м), 3,80 - 3,93 (2H, м), 4,94 (1H, д, J = 19 Гц), 5,08 (1H, д, J = 19 Гц), 5,35 (1H, д, J = 7 Гц), 5,40 (1H, д, J = 7 Гц), 5,55 - 5,77 (1H, шир.), 5,78 (2H, c), 7,01 (2H, дд, J = 9, 9 Гц), 7,22 (1H, д, J = 3 Гц), 7,27 (1H, c), 7,35 (1H, дд, J = 3, 9 Гц), 7,48 (1H, шир-т, J = 6 Гц), 7,50 (1H, c), 7,90 (1H, д, J = 9 Гц), 8,02 (2H, дд, J = 6, 9 Гц).
C36
Т. пл. 231 - 232oC, бесцветный порошок (из н-гексана-хлороформа)
[α]
C33H35N4O6F, MS [M+H]+ = 603,
ИК νmax /KBr (см-1): 1710, 1645, 1620, 1595, 1520.
1H ЯМР ( δ ч. на млн.) в DMCO-d6: 0,91 (3H, т, J = 7 Гц), 1,30 (3H, т, J = 8 Гц), 2,11 - 2,30 (2H, м), 2,53 (6H, c), 2,62 - 2,90 (2H, м), 2,99 - 3,40 (4H, м), 5,29 (2H, c), 5,57 (1H, д, J = 11 Гц), 5,62 (1H, д, J = 11 Гц), 6,36 (1H, c), 7,33 (1H, дд, J = 9, 9 Гц), 7,38 - 7,48 (3H, м), 7,97 (2H, дд, J = 6, 9 Гц), 8,04 (1H, д, J = 9 Гц), 8,94 - 10,27 (1H, шир.), 10,34 (1H, c).
C37
Т. пл. 105 - 109oC, желтые призмы (из н-гексана-хлороформа)
[α]
C37H43N4O8F, MS [M+H]+ = 691,
ИК νmax /KBr (см-1): 1720, 1650, 1620, 1590, 1510.
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,14 (3H, т, J = 7 Гц), 1,27 (3H, т, J = 8 Гц), 2,16 (6H, c), 2,23 - 2,43 (3H, м), 2,50 - 2,66 (1H, м), 2,83 - 3,05 (1H, м), 3,06 - 3,19 (1H, м), 3,27 - 3,44 (1H, м), 3,39 (3H, c), 3,50 - 3,63 (2H, м), 3,80 - 3,92 (2H, м), 4,95 (1H, д, J = 19 Гц), 5,08 (1H, д, J = 19 Гц), 5,35 (1H, д, J = 7 Гц), 5,40 (1H, д, J = 7 Гц), 5,50 - 5,82 (1H, шир.), 5,77 (1H, д, J = 12 Гц), 5,81 (1H, д, J = 12 Гц), 7,13 - 7,25 (2H, м), 7,27 - 7,39 (2H, м), 7,48 (1H, шир-т, J = 6 Гц), 7,50 (1H, c), 7,66 - 7,73 (1H, м), 7,80 (1H, д, J = 8 Гц), 7,90 (1H, д, J = 9 Гц).
C38
Т. пл. 223 - 224oC, бесцветный порошок (из н-гексана-хлороформа)
C33H35N4O6F, MS [M+H]+ = 603,
ИК νmax /KBr (см-1): 1710, 1645, 1620, 1590, 1520.
1H ЯМР ( δ ч. на млн.) в DMCO-d6: 0,91 (3H, т, J = 7 Гц), 1,30 (3H, т, J = 8 Гц), 2,08 - 2,34 (2H, м), 2,54 (6H, c), 2,54 - 2,75 (2H, м), 2,95 - 3,43 (4H, м), 5,29 (2H, c), 5,58 (1H, д, J = 11 Гц), 5,65 (1H, д, J = 11 Гц), 6,35 (1H, c), 7,34 - 7,68 (6H, м), 7,76 (1H, д, J = 7 Гц), 8,05 (1H, д, J = 9 Гц), 8,08 - 8,22 (1H, шир.), 9,22 - 9,66 (1H, шир.), 10,32 (1H, c).
C39
Т. пл. 162 - 164oC, желтый порошок (из н-гексана-хлороформа)
C33H37N5O5•H2O, MS [M+H]+ = 584,
Элементный анализ
найдено: C 65,44 H 6,53 N 11,54
вычислено: C 65,87 H 6,53 N 11,64
ИК νmax /KBr (см-1): 1720, 1645, 1595, 1515.
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,13 (3H, т, J = 7 Гц), 1,31 (3H, т, J = 8 Гц), 2,16 (6H, c), 2,27 - 2,42 (3H, м), 2,51 (3H, c), 2,52 - 2,63 (1H, м), 2,90 - 3,14 (3H, м), 3,30 - 3,41 (1H, м), 4,89 (1H, д, J = 19 Гц), 5,10 (1H, д, J = 19 Гц), 5,62 - 5,84 (1H, шир.), 5,81 (1H, д, J = 12 Гц), 5,86 (1H, д, J = 12 Гц), 7,44 - 7,53 (3H, м), 7,55 (1H, c), 7,81 (2H, дд, J = 1, 5 Гц), 7,89 (1H, д, J = 9 Гц), 8,67 (2H, дд, J = 1, 5 Гц).
C40
Т. пл. 165 - 167oC, желтый порошок (из н-гексана-хлороформа)
C32H34N5O5Cl•1/2H2O, MS [M+H]+ = 604,
Элементный анализ
найдено: C 62,54, H 5,78 N 11,35
вычислено: C 62,69 H 5,75 N 11,42
ИК νmax /KBr (см-1): 1720, 1650, 1595, 1515.
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,14 (3H, т, J = 77 Гц), 1,34 (3H, т, J = 8 Гц), 2,16 (6H, c), 2,27 - 2,41 (3H, м), 2,52 - 2,64 (1H, м), 2,93 - 3,13 (3H, м), 3,30 - 3,40 (1H, м), 5,01 (1H, д, J = 19 Гц), 5,12 (1H, д, J = 19 Гц), 5,51 - 5,57 (1H, шир.), 5,80 (1H, д, J = 12 Гц), 5,86 (1H, д, J = 12 Гц), 7,49 (1H, т, J = 5 Гц), 7,53 (1H, c), 7,62 (1H, дд, J = 2, 9 Гц), 7,70 (1H, д, J = 2 Гц), 7,81 (2H, дд, J = 1, 5 Гц), 7,90 (1H, д, J = 9 Гц), 8,68 (2H, дд, J = 1, 5 Гц).
C41
Т. пл. 171oC, светло-желтый порошок (из н-гексана-хлороформа)
C30H34N4O4F, MS [M+H]+ = 588,
ИК νmax /KBr (см-1): 1720, 1650, 1595, 1510.
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,15 (3H, т, J = 7 Гц), 1,35 (3H, т, J = 8 Гц), 2,16 (6H, c), 2,27 - 2,42 (3H, м), 2,52 - 2,66 (1H, м), 2,98 - 3,18 (3H, м), 3,29 - 3,40 (1H, м), 5,02 (1H, д, J = 19 Гц), 5,12 (1H, д, J = 19 Гц), 5,72-5,91 (1H, шир. D2O избыток), 5,81 (1H, д, J = 12 Гц), 5,87 (1H, д, J = 12 Гц), 7,23 (1H, ддд, J = 3, 8, 10 Гц), 7,52 (1H, т, J = 5 Гц, D2O избыток), 7,55 (1H, c), 7,57 (1H, дд, J = 3, 10 Гц), 7,80 (2H, дд, J = 2, 4 Гц), 7,82 (1H, дд, J = 6, 9 Гц), 8,67 (2H, дд, J = 2, 4 Гц).
C42
Т. пл. 169oC, светло-желтый порошок (из н-гексана-хлороформа)
C31H36N4O4F, MS [M+H]+ = 602,
ИК νmax /KBr (см-1): 1720, 1650, 1600, 1505.
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,13 (3H, т, J = 7 Гц), 1,36 (3H, т, J = 8 Гц), 2,17 (6H, c), 2,28 - 2,60 (4H, м), 2,98 - 3,17 (3H, м), 3,29 - 3,40 (1H, м), 5,02 (1H, д, J = 19 Гц), 5,13 (1H, д, J = 19 Гц), 5,30 - 5,50 (1H, шир. ), 5,81 (1H, д, J = 12 Гц), 5,84 (1H, д, J = 12 Гц), 7,39 (1H, шир-т, J = 5 Гц, D1O избыток), 7,52 (1H, c), 7,54 (1H, д, J = 12 Гц), 7,64 (1H, д, J = 8 Гц), 7,81 (2H, дд, J = 2, 5 Гц), 8,68 (2H, дд, J = 2, 5 Гц).
C43
Т. пл. 159 - 164oC, желтые иглы (из н-гексана-хлороформа)
C31H36N4O5F, MS [M+H]+ = 618,
ИК νmax /KBr (см-1): 1720, 1650, 1595, 1510.
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,17 (3H, т, J = 7 Гц), 1,30 (3H, т, J = 8 Гц), 2,17 (6H, c), 2,26 - 2,42 (3H, м), 2,54 - 2,68 (1H, м), 2,87 - 3,08 (3H, м), 3,28 - 3,41 (1H, м), 4,00 (3H, c), 4,90 (1H, д, J = 19 Гц), 5,48 - 5,82 (1H, шир., D2O избыток), 5,76 (1H, д, J = 12 Гц), 5,86 (1H, д, J = 12 Гц), 6,85 (1H, д, J = 9 Гц), 7,45 (1H, c), 7,52 (1H, т, J = 6 Гц, H2O избыток), 7,55 (1H, д, J = 12 Гц), 7,81 (2H, дд, J = 2, 5 Гц), 8,67 (2H, дд, J = 2, 5 Гц).
C44
Т. пл. 147 - 150oC, желтый порошок (из н-гексана-хлороформа)
C31H33N5O6•H2O, MS [M+H]+ = 572,
Элементный анализ
найдено: C 62,85 H 6,03 N 11,78
вычислено: C 63,15 H 5,98 N 11,88
ИК νmax /KBr (см-1): 3390, 1710, 1650, 1615, 1590, 1520.
1H ЯМР ( δ ч. на млн.) в CDCl3: 1,08 (3H, т, J = 7 Гц), 2,15 (6H, c), 2,29 - 2,55 (4H, м), 3,22 - 3,41 (2H, м), 4,02 (3H, c), 5,14 (1H, д, J = 19 Гц), 5,20 (1H, д, J = 19 Гц), 5,34 (1H, шир-c), 5,77 (1H, д, J = 12 Гц), 5,94 (1H, д, J = 12 Гц), 6,87 (1H, д, J = 8 Гц), 7,39 - 7,47 (2H, м), 7,60 - 7,68 (2H, м), 7,73 (1H, д, J = 9 Гц), 7,80 (1H, ддд, J = 2, 8, 8 Гц), 8,13 (1H, д, J = 8 Гц), 8,65 - 8,70 (2H, м).
C45
Бесцветный порошок (из н-гексана-хлороформа)
C28H34N4O6, MS [M+H]+ = 523.
C46
Желтый порошок (из н-гексана-хлороформа)
C30H38N4O6, MS [M+H]+ = 551.
C47
Желтый порошок (из н-гексана-хлороформа)
C31H40N4O7, MS [M+H]+ = 581.
C48
Т. пл. 179 - 182oC, бесцветный порошок (из н-гексана-хлороформа)
C35H37N4O7F, MS [M+H]+ = 645.
В табл. 2 приведена растворимость в воде соединений с C1 по C38. В табл. 3 приведена противоопухолевая активность производных камптотецина. В табл. 4 приведена острая токсичность производных камптотецина.



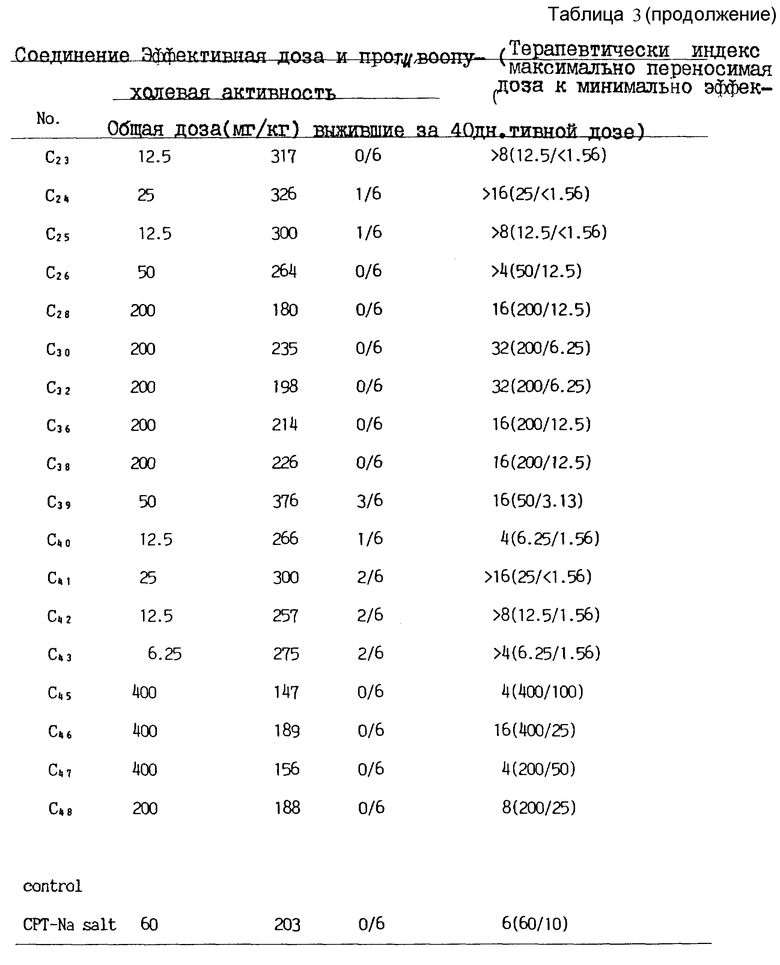
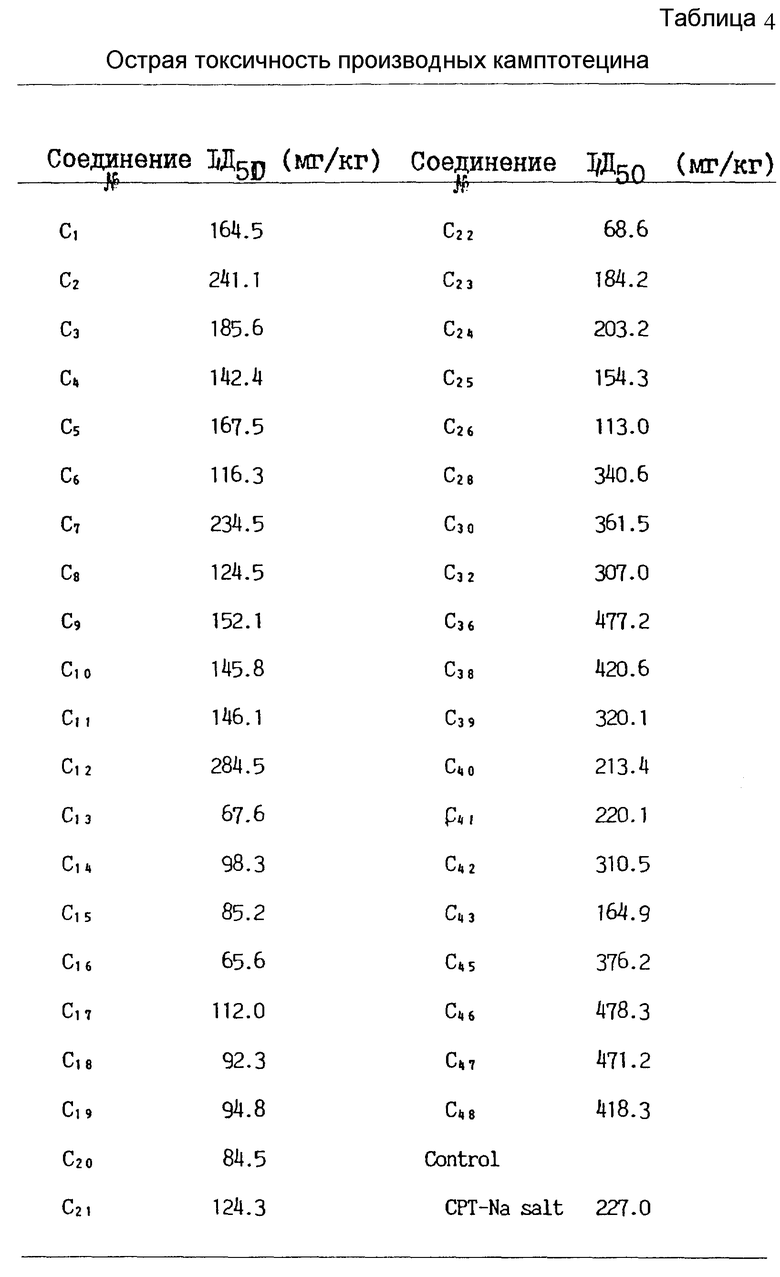
Производные камптотецина общей формулы I, где R1 представляет собой атом водорода или C1-6-алкильную группу, R2- водород или C1-6-алкоксигруппа, R3 - водород или галоген, С1-6-алкил, C1-6-алкокси, гидроксил, С2-6-ацилокси- или метоксиэтоксиметоксигруппа, R4 - атом водорода или галогена и R5 - С1-6-алкил,С3-С6-ненасыщенный алкил, алкилтиоалкил, алкоксиалкил, пиридил или замещеная фенильная группа при условии, что заместители R2, R3 и R4 не должны быть атомами водорода, обладают превосходной противоопухолевой активностью. 3 c.п. ф-лы, 4 табл.
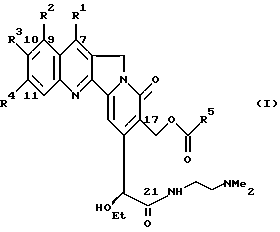
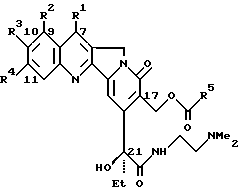
где R1 представляет собой атом водорода или C1-6-алкильную группу;
R2 является водородом или C1-6-алкоксигруппой;
R3 - водород или галоген, C1-6-алкил, C1-6-алкокси, гидроксил, C2-6-ацилокси или метоксиэтоксиметоксигруппа;
R4 - атом водорода или галогена;
R5 - C1-6-алкил, C3 - C6-ненасыщенный алкил, алкилтиоалкил, алкоксиалкил, пиридил или замещенная фенильная группа при условии, что заместители R2, R3 и R4 не должны быть атомами водорода.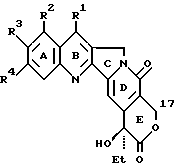
где R1, R2, R3 и R4 имеют определенные выше значения,
подвергают взаимодействию с N,N-диметилэтилендиамином с открытием Е-лактонового кольца с последующим ацилированием 17-гидроксильной группы соответствующими ацилирующими агентами.
Авторы
Даты
1999-07-27—Публикация
1995-09-05—Подача