Изобретение относится к порошку комплексного оксида металла, содержащему по крайней мере два металлических элемента, который используют в качестве исходного порошка оксидной керамики, которую используют в качестве функционального материала для конструктивного материала, который используют в диспергированном состоянии в качестве наполнителя или пигмента, или который используют в качестве исходного порошка для получения монокристалла или покрытия, нанесенного методом пламенного распыления, и к способу его получения.
Вообще оксидную керамику, которую используют в качестве функционального материала или конструкционного материала, получают через стадию прессования и стадию обжига из порошка оксида металла в качестве сырья. Свойства порошка оксида металла, используемого в качестве сырья, оказывают большое влияние на стадии получения, функции и физические свойства керамического продукта. К тому же очень желательно обеспечить порошок комплексного оксида металла, имеющий порошковые свойства, которые четко регулируют для того, чтобы они были подходящими для намеренного применения.
Контроль свойств порошка является более важным, когда порошок оксида металла используют в диспергированном состоянии, например, в виде тонкого магнитного порошка, наполнителя или пигмента, так как свойства каждой частицы непосредственно отражаются на диспергированном состоянии.
Необходимые свойства порошка комплексного оксида металла изменяются с изменением вида и формы применения оксида металла. Обычно необходимыми свойствами являются однородная степень дисперсности порошка оксида металла, т.е. узкое распределение по крупности, и слабая связь между первичными частицами, т. е. незначительная агломерация и хорошая диспергируемость. Например, иттрий-алюминиевый гранат в узком смысле является комплексным оксидом металла, представленным общей формулой Y3Al5O12, а в широком смысле он включает комплексный оксид металла, в котором часть иттриевых элементов замещена церием, неодимом, тербием и т.п. Иттрий-алюминиевый гранат является пригодным в электронной оптике в качестве маточного материала. Например, монокристаллический иттрий-алюминиевый гранат, в котором часть иттриевых элементов замещена неодимом, используют в качестве облучаемого лазером материала, а кристаллические частицы иттрий-алюминиевого граната, в котором часть иттриевых элементов замещена церием или тербием, используют в качестве флуоресцентного вещества и т.д.
Гранат железо-редкоземельного элемента (R3Fe5O12, в котором R является редкоземельным элементом), который представлен иттрий-железным гранатом (Y3Fe5O12) или гранатом, в котором часть редкоземельного элемента и/или железа замещена другим металлом, является пригодным в качестве магнитного микроволнового материала или материала детали, в которой используют магнитооптический эффект.
Твердый раствор металлических соединений, например, твердый раствор оксида циркония и оксида по крайней мере одного металла, выбранного из иттрия, магния, кальция, церия и редкоземельных элементов, например, скандия и иттербия, является пригодным в качестве материала, который используют в материале, стойком к воздействию высоких температур, ионопроводящем материале, пьезоэлектрическом материале и т.д. Кроме того, его используют в качестве сырья спеченного материала или покрытия, нанесенного методом пламенного распыления.
Из aвторского свидетельства СССР N 544614 (кл. С 01 F 17.00, опубл. 17.02.1977) известен порошок комплексного оксида металла, содержащий по крайней мере два металлических элемента, порошок иттрий-алюминиевого граната, и способ получения порошка комплексного оксида металла, включающего по крайней мере два металлических элемента.
Однако с известными порошками возникают проблемы образования агломератов, широкого распределения по крупности в продукте, необходимость удаления примесей, регулирования крупности частиц и т.д.
Кроме того, известный способ получения вызывает проблемы, связанные с реакционными условиями, например, с использованием сложных методик и трудного регулирования, проблемы с аппаратурой, стоимостью сырья и т.д. Кроме того, желательно создать порошок комплексного оксида металла, который содержит менее агломерированные частицы и имеет узкое распределение по крупности, и вообще разработать способ получения порошка комплексного оксида металла, который был бы выгодным в промышленном производстве.
Технической задачей настоящего изобретения является создание комплексного оксида металла, содержащего по меньшей мере два металлических элемента, который содержит менее агломерированные частицы и имеет узкое распределение по крупности и единообразную форму частиц и который предпочтительно используют в качестве порошка оксида металла, используемого в качестве исходного порошка оксидной керамики, которую используют в качестве функционального материала или конструкционного материала, порошка оксида металла, используемого в диспергированном состоянии в качестве наполнителя или пигмента, или порошка оксида металла, используемого в качестве исходного порошка для получения монокристалла или покрытия, нанесенного методом пламенного распыления.
Другой технической задачей настоящего изобретения является создание способа получения, который вообще можно применять при получении такого порошка оксида металла и который является превосходным для промышленных целей.
Данные технические задачи решаются за счет того, что порошок комплексного оксида металла, содержащий по крайней мере два металлических элемента, согласно изобретению включает полиэдрические частицы, каждая из которых имеет по крайней мере 6 плоскостей, среднечисленную крупность частиц от 0,1 до 500 мкм и отношение D90/D10, равное 10 или менее, где D10, и D90 представляют крупность частиц при 10 и 90%-ном аккумулировании соответственно исходя из самой маленькой крупности частиц на суммарной кривой гранулометрического состава частиц.
Кроме того, среднечисленная крупность частиц может составлять от 0,1 до 300 мкм, и упомянутое соотношение D90/D10 может составлять 5 или менее, а отношение крупности агломерированных частиц к крупности исходных частиц составляет от 1 до 6, в частности от 1 до 3.
Среднечисленная крупность частиц может составлять от 20 до 300 мкм. При этом по крайней мере два металла могут быть комбинацией металлов, при исключении комбинации только из щелочных металлов.
Порошок комплексного оксида металла может представлять собой порошок твердого раствора оксидов металлов или порошок комплексного оксида металла, имеющий структуру граната, представленную формулой:
(MA)3 (MB)2, [(MC)O4]3, (1)
в которой МA, МB и МC каждый представляет по крайней мере один металлический элемент при условии, что все из МA, МB и МC не являются одним и тем же металлическим элементом.
При этом МA может быть по крайней мере одним элементом, выбранным из группы, состоящей из меди, марганца, кальция, редкоземельных элементов, висмута и марганца, и МB и МC могут быть одинаковыми или разными и каждый является по крайней мере одним элементом, выбранным из группы, состоящей из цинка, скандия, алюминия, галлия, индия, титана, циркония, кремния, германия, олова, ванадия, хрома, марганца, железа, кобальта и никеля.
В частности, МA может быть редкоземельным элементом, а оба МB и МC могут быть алюминием или МA может быть диспрозием, а оба МB и МC могут быть алюминием или МA может быть редкоземельным элементом, а оба МB и МC могут быть железом. Кроме того, МA может быть иттрием или гадолинием, или диспрозием.
В порошке комплексного оксида металла твердым раствором может быть твердый раствор оксида циркония и оксида иттрия.
Кроме того, технические задави решаются за счет того, что порошок иттрий-алюминиевого граната согласно изобретению, содержит полиэдрические частицы, каждая из которых имеет по крайней мере 6 плоскостей и имеет среднюю крупность частиц от 20 до 500.
При этом порошок иттрий-алюминиевого граната может иметь распределение по крупности, представленное отношением D90/D10, равное 10 или менее, где D10 и D90 представляют крупность частиц при 10 и 90%-ном аккумулировании, исходя соответственно, от самой маленькой крупности частиц на суммарной кривой гранулометрического состава частиц, составляющих упомянутый порошок иттрий-алюминиевого граната. Часть иттриевых элементов замещена по крайней мере одним металлом, выбранным из редкоземельных элементов, хрома, кобальта и никеля.
Порошок иттрий-алюминиевого граната может содержать полиэдрические частицы, каждая из которых имеет по крайней мере 6 плоскостей, который получают обжигом оксида иттрия и/или предшественника оксида иттрия, который генерирует оксид иттрия при нагревании и оксида алюминия и/или предшественника оксида алюминия, который генерирует оксид алюминия при нагревании в атмосфере, содержащей по крайней мере один газ, выбранный из группы, состоящей из:
(1) галогенида водорода,
(2) компонента, полученного из молекулярного галогена и водяного пара, и
(3) молекулярного галогена.
В порошке иттрий-алюминиевого граната атмосферный газ может содержать по крайней мере 1 об.% галогенида водорода или по крайней мере 1 об.% упомянутого молекулярного галогена или компонент, полученный из по крайней мере 1 об. % молекулярного галогена и по крайней мере 0,1% водяного пара, причем галогенид водорода (1) представляет хлористый водород или бромистый водород, а упомянутым молекулярным галогеном в (2) или (3) является хлор или бром.
Технические задачи изобретения решаются также за счет того, что в способе получения порошка комплексного оксида металла, включающего по крайней мере два металлических элемента, согласно изобретению осуществляют обжиг смеси по крайней мере двух порошков оксида металла и/или порошков предшественника оксида металла, или порошка предшественника оксида металла, содержащего по крайней мере два металлических элемента в атмосфере, содержащей по крайней мере один газ, выбранный из группы, состоящей из:
(1) галогенида водорода,
(2) компонента, полученного из молекулярного галогена и водяного пара, и
(3) молекулярного галогена.
При этом содержащийся в атмосферном газе представляет галогенид водорода, в частности, галогенид водорода представляет хлористый водород, бромистый водород или йодистый водород.
Концентрация галогенида водорода в атмосферном газе может быть по крайней мере 1 об.%.
Газ, содержащийся в атмосферном газе, может представлять компонент, полученный из молекулярного галогена и водяного пара.
Молекулярным галогеном может быть хлор, бром или иод. Компонент, полученный из молекулярного галогена и водяного пара, может быть компонентом, полученным из по крайней мере 1 об.% молекулярного галогена и по крайней мере 0,1 об.% водяного пара относительно упомянутого атмосферного газа.
Газ, содержащийся в атмосферном газе, может представлять молекулярный галоген, молекулярным галогеном является хлор, бром или иод, и концентрация молекулярного галогена в атмосферном газе составляет по крайней мере 1 об.%.
Объемная плотность смеси по крайней мере двух порошков оксида металла и/или порошков предшественника оксида металла, или порошка предшественника оксида металла, содержащего по крайней мере два металлических элемента, может составлять 40% или менее от теоретической плотности.
В способе, согласно изобретению, порошок комплексного оксида металла можно получать на участке, где присутствует смесь по крайней мере двух порошков оксида металла и/или порошков предшественника оксидов металла или порошок предшественника оксида металла, содержащий по крайней мере два металлических элемента.
По крайней мере два металла могут быть комбинацией металлов при исключении комбинации только из щелочных металлов.
В способе порошок комплексного оксида металла может представлять порошок твердого раствора оксидов металла.
В способе комплексный оксид металла может быть порошком комплексного оксида металла, имеющим структуру граната, представленную формулой:
(MA)3 (MB)2 [(MC)O4]3,
в которой МA, МB и МC каждый представляет по крайней мере один металлический элемент при условии, что все из МA, МB и МC не являются одним и тем же металлическим элементом.
В способе МA может быть по крайней мере одним элементом, выбранным из группы, состоящей из меди, магния, кальция, редкоземельных элементов, висмута и марганца, и МB и МC могут быть одинаковыми или разными и каждый является по крайней мере одним элементом, выбранным из группы, состоящей из цинка, скандия, алюминия, галлия, индия, титана, циркония, кремния, германия, олова, ванадия, хрома, марганца, железа, кобальта и никеля.
В способе МA может быть иттрием, а оба МB и МC могут быть алюминием или МA может быть иттрием, часть которого замещена другим редкоземельным элементом, а оба МB и МC могут быть алюминием, при этом другой редкоземельный элемент может быть тербием или диспрозием.
В способе МA может быть диспрозием, а оба МB и МC могут быть алюминием, или МA может быть редкоземельным элементом, а оба МB и МC могут быть железом, причем редкоземельным элементом может быть иттрий, гадолиний или диспрозий.
В способе твердый раствор может представлять твердый раствор оксида циркония и оксида иттрия.
Кроме того, в способе согласно изобретению обжиг можно осуществлять в присутствии затравочного кристалла, причем объемная плотность затравочного кристалла составляет 40% или менее от теоретической плотности.
Далее изобретение будет пояснено подробно со ссылкой на чертежи, на которых:
фиг. 1 представляет фотоснимок, полученный на растровом электронном микроскопе (х 172), показывающий структуру частицы порошка иттрий-алюминиевого граната, наблюдаемого в примере 1;
фиг. 2 показывает график, показывающий распределение по крупности порошка иттрий-алюминиевого граната примера 1;
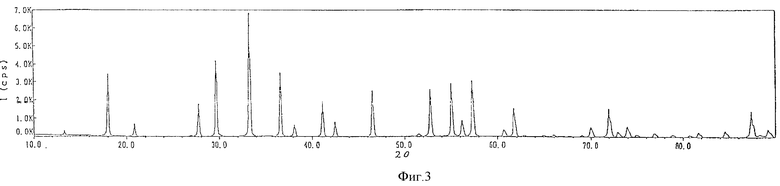
фиг. 3 представляет рентгенограмму порошка иттрий-алюминиевого граната примера 1;
фиг. 4 представляет фотоснимок, полученный (х 172), показывающий структуру частицы порошка иттрий-алюминиевого граната, наблюдаемую в примере 2;
фиг. 5 представляет график, показывающий распределение по крупности порошка иттрий-алюминиевого граната примера 2;
фиг. 6 представляет рентгенограмму порошка иттрий-алюминиевого граната примера 2;
фиг. 7 представляет фотоснимок, полученный на растровом электронном микроскопе (х 172), показывающий структуру частицы порошка иттрий-алюминиевого граната, наблюдаемую в примере 4;
фиг. 8 представляет фотоснимок, полученный на растровом электронном микроскопе (х 172), показывающий структуру частицы порошка иттрий-алюминиевого граната, наблюдаемую в примере 5;
фиг. 9 представляет фотоснимок, полученный на растровом электронном микроскопе (х 850), показывающий структуру частицы порошка иттрий-алюминиевого граната, наблюдаемую в примере 6;
фиг. 10 представляет фотоснимок, полученный на растровом электронном микроскопе (х 850), показывающий структуру частицы порошка иттрий-алюминиевого граната, наблюдаемую в примере 10;
фиг. 11 представляет фотоснимок, полученный на растровом электронном микроскопе (х 425), показывающий структуру частицы порошка иттрий-алюминиевого граната, замещенного диспрозием, наблюдаемую в примере 12;
фиг. 12 представляет фотоснимок, полученный на растровом электронном микроскопе (х 1720), показывающий структуру частицы порошка оксида, наблюдаемую в сравнительном примере 1;
фиг. 13 представляет график, показывающий распределение по крупности порошка оксида, наблюдаемое в сравнительном примере 1;
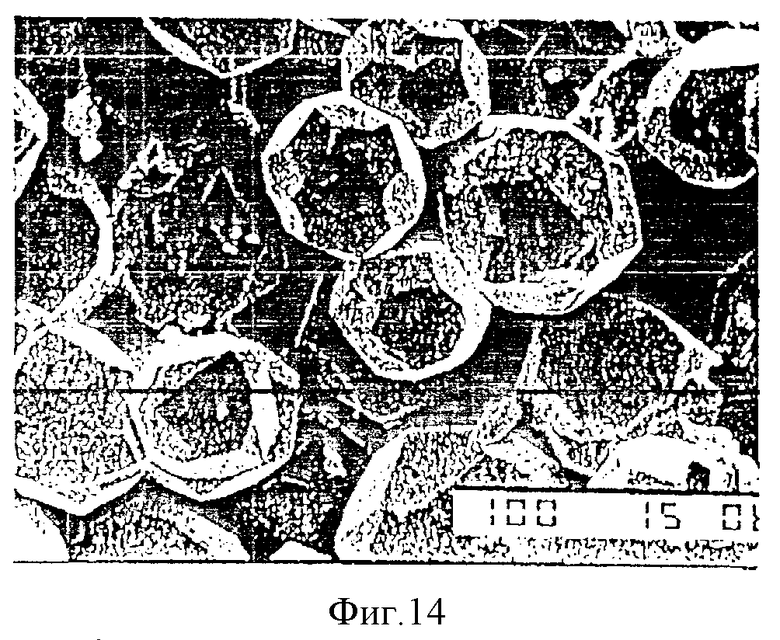
фиг. 14 представляет фотоснимок, полученный на растровом электронном микроскопе (х 425), показывающий структуру частицы порошка диспрозий-алюминиевого граната, наблюдаемую в примере 16;
фиг. 15 представляет фотоснимок, полученный на растровом электронном микроскопе (х 4250), показывающий структуру частицы порошка оксида, наблюдаемую в сравнительном примере 5;
фиг. 16 представляет фотоснимок, полученный на растровом электронном микроскопе (х 425), показывающий структуру частицы порошка железо-иттриевого граната, наблюдаемую в примере 17;
фиг. 17 представляет фотоснимок, полученный на растровом электронном микроскопе (х 1720), показывающий структуру частицы порошка оксида, наблюдаемую в сравнительном примере 6;
фиг. 18 представляет фотоснимок, полученный на растровом электронном микроскопе (х 850), показывающий структуру частицы порошка железо-гадолиниевого граната, наблюдаемую в примере 18;
фиг. 19 представляет фотоснимок, полученный на растровом электронном микроскопе (х 4250), показывающий структуру частицы порошка оксида, наблюдаемую в cравнительном примере 7;
фиг. 20 представляет фотоснимок, полученный на растровом электронном микроскопе (х 8500), показывающий структуру частицы порошка твердого раствора оксида иттрия и оксида циркония, наблюдаемую в примере 20;
фиг. 21 представляет фотоснимок, полученный на растровом электронном микроскопе (х 4250), показывающий структуру частицы порошка твердого раствора оксида иттрия и оксида циркония, наблюдаемую в сравнительном примере 9.
Подробное описание изобретения.
Настоящее изобретение будет объяснено подробно. Порошок комплексного оксида металла настоящего изобретения содержит по крайней мере два металлических элемента и является соединением по крайней мере двух металлических элементов и кислорода. Порошок комплексного оксида металла, содержащий по крайней мере два металлических элемента, включает порошок твердого раствора оксида металла, содержащий по крайней мере два соединения, каждое из которых включает металлический элемент и кислород в состоянии твердого раствора.
В способе настоящего изобретения получают комплексный оксид металла путем обжига смеси по крайней мере двух порошков - оксида металла и/или порошков предшественника оксида металла или предшественника оксида металла, содержащего по крайней мере два металлических элемента, в присутствии или отсутствии затравочного кристалла в атмосфере, содержащей, по крайней мере, один газ, выбранный из группы, состоящей из (1) галогенида водорода, (2) компонента, полученного из молекулярного галогена и (3) молекулярного галогена.
Когда порошок комплексного оксида металла, содержащий по крайней мере два металлических элемента, получают способом настоящего изобретения, в качестве исходного порошка используют смесь по крайней мере двух порошков оксида металла и/или порошков предшественника оксида металла, или порошок предшественника оксида металла, содержащий по крайней мере два металлических элемента.
Под предшественником оксида металла имеют в виду материал, который дает оксид металла, состоящий по крайней мере из одного металлического элемента и кислорода, путем реакции разложения или реакции окисления при обжиге, и включает, например, гидроксиды металла, гидратированные оксиды металла (гидроксиды металла), оксигидроксиды металла, оксигалогениды металла и т.д.
Под затравочным кристаллом, который может быть использован в настоящем изобретении, подразумевают кристалл, который функционирует как участок роста для роста кристалла оксида металла. Вокруг затравочного кристалла растет оксид металла. Может быть использован любой затравочный кристалл, если он имеет эту функцию. В качестве продукта предпочтительным является, например, комплексный оксид металла или твердый раствор оксида металла.
Для способа добавления затравочного кристалла к исходному порошку не существует ограничений. Может быть использован, например, способ смешивания, такой как механическое измельчение в шаровой мельнице, ультразвуковое диспергирование и т.п.
В качестве исходного порошка оксида металла обычно упоминаются два порошка оксида металла и/или порошок предшественника оксида металла, представленные как исходный материал, при этом порошок предшественника оксида металла содержит по крайней мере два металлических элемента, представленные в качестве исходного материала, и также исходные материалы, к которым добавляют затравочный кристалл.
Порошок комплексного оксида металла, содержащий в соответствии с изобретением по крайней мере два металлических элемента, представляют комплексный оксид металла, который содержит по крайней мере два металлических элемента, кроме комбинации из только щелочных металлов и кислорода, или твердый раствор оксида металла, в котором по крайней мере два соединения, каждое из которых включает металлический элемент и кислород, присутствуют в состоянии твердого раствора. Примером такого порошка комплексного оксида металла является комплексный оксид металла, имеющий структуру граната, представленный общей формулой:
(МA)3 (MB)2 [(MC)O4]3 (1)
в которой МA, MB и MC являются одинаковыми и различными и каждый представляет по крайней мере один металлический элемент при условии, что все из МA МB МC не являются одним и тем же металлическим элементом.
Конкретно, в формуле (1) МA представляет по крайней мере один элемент, выбранный из группы, состоящей из меди, магния и редкоземельных элементов (например, скандия, иттрия и лантана), висмута и марганца, и МA и МB являются одинаковыми или разными и каждый представляет по крайней мере один элемент, выбранный из группы, состоящей из цинка, скандия, алюминия, галлия, индия, титана, циркония, кремния, германия, олова, ванадия, хрома, марганца, железа, кобальта и никеля.
В некоторых случаях соединения не имеют структуру граната из-за ионного радиуса металлических элементов МA, МB и МC.
Более конкретно, примером могут служить алюминиевые гранаты, например, комплексный оксид металла вышеприведенной формулы, в которой МA является например, иттрием, МB и МC являются алюминием; иттрий-алюминиевый гранат вышеприведенной формулы, в которой МA является иттрием, часть которого замещена другим(и) редкоземельным(и) металлом(ами), и оба МB и МC являются алюминием, диспрозий-алюминиевый гранат вышеприведенной формулы, в которой МA является диспрозием, а оба МB и МC являются алюминием и т.п.
Кроме того, примером может служить железный гранат, например железо-иттриевый гранат, в виде комплексного оксида металла вышеприведенной формулы, в которой МA является иттрием, оба МB и МC являются железом, железо-гадолиниевый или железо-диспрозиевый гранат в виде комплексного оксида металла вышеприведенной формулы, в которой МA является гадолинием или диспрозием, и МB и МC являются железом, и т.д.
Кроме того, примером может служить гранат вышеприведенной формулы, в которой каждый МA, МB и МC состоит из по крайней мере двух металлических элементов.
В способе настоящего изобретения исходный порошок оксида металла не ограничивают и может быть использован порошок, полученный традиционным способом. Может быть использован, например, порошок оксида металла, полученный жидкофазным методом, или порошок оксида металла, полученный газофазным методом или твердофазным методом.
В настоящем изобретении исходный порошок оксида металла обжигают в атмосферном газе, содержащем по крайней мере 1 об.%, предпочтительно по крайней мере 5 об.%, более предпочтительно по крайней мере 10 об.% галогенида водорода относительно общего объема атмосферного газа.
В качестве галогенида водорода независимо используют хлористый водород, бромистый водород, йодистый водород и фтористый водород или смесь двух или нескольких из них. Предпочтительно используют хлористый водород, бромистый водород и йодистый водород.
В качестве компонента атмосферного газа иного, чем галогенид водорода, можно использовать разреженный газ, азот, инертный газ, например аргон, водород, водяной пар или воздух.
Давление атмосферного газа, содержащего галогенид водорода, не ограничивается, и его выбирают из диапазона давлений, которые используют в промышленности.
Обжиг можно проводить в атмосферном газе, содержащем вместо галогенида водорода компонент, полученный из молекулярного галогена и водяного пара.
В качестве молекулярного галогена используют по крайней мере один из молекулярного хлора, брома, иода и фтора. Предпочтительно используют хлор, бром и иод.
Газ получают из по крайней мере 1 об.%, предпочтительно из по крайней мере 5 об.%, более предпочтительно из по крайней мере 10 об.% молекулярного галогена и по крайней мере 0,1 об.%, предпочтительно по крайней мере 1 об.%, более предпочтительно по крайней мере 5 об.% водяного пара относительно общего объема атмосферного газа.
Вместо галогенида водорода можно использовать молекулярный галоген. Исходный порошок оксида металла обжигают в атмосферном газе, содержащем по крайней мере 1 об.%, предпочтительно по крайней мере 5 об.%, более предпочтительно по крайней мере 10 об.% молекулярного галогена относительно общего объема атмосферного газа. В качестве молекулярного галогена можно использовать по крайней мере один из молекулярного хлора, брома и иода.
В качестве компонента атмосферного газа иного, чем компонент, полученный из молекулярного галогена и водяного пара, или молекулярного галогена, можно использовать разреженный газ, азот, инертный газ, например аргон, водород, водяной пар или воздух.
Давление в реакционной системе не ограничивается, и его свободно выбирают из диапазона давлений, который используют в промышленности.
Способ подачи атмосферного газа не является решающим, поскольку атмосферный газ можно подавать в реакционную систему, в которой присутствует исходный порошок оксида металла.
Источник каждого компонента атмосферного газа и способ подачи каждого компонента также не является решающими.
В качестве источника каждого компонента атмосферного газа можно использовать, например, газ в ампуле. Альтернативно можно получить атмосферный газ, содержащий галогенид водорода или молекулярный галоген, с использованием испарения или разложения галогенового соединения, например, галогенида аммония, или галогенсодержащего полимера, например, винилхлоридного полимера.
Атмосферный газ можно получить путем обжига смеси исходного оксида металла и галогенового соединения или галогенсодержащего полимера в обжиговой печи.
Галогенид водорода и молекулярный галоген ввиду действенности предпочтительно подают из ампулы непосредственно в обжиговую печь. Атмосферный газ можно подавать непрерывным или периодическим путем.
В соответствии с настоящим изобретением, когда исходный порошок оксида металла обжигают в вышеуказанном атмосферном газе, оксид металла растет на участке, где присутствует исходный порошок оксида металла, вследствие реакции между исходным порошком оксида металла и атмосферным газом, что вызывает образование порошка оксида металла, имеющего узкое распределение по крупности, но неагломерированные частицы. Соответственно желаемый порошок оксида металла можно получить, например, простой загрузкой исходного порошка оксида металла и в емкость, и обжигом его в атмосферном газе.
В качестве исходного порошка оксида металла, который используют в настоящем изобретении, можно использовать любой материал, который находится в форме порошка, при этом объемная плотность порошка составляет предпочтительно по крайней мере 40% или менее относительно теоретической плотности.
Когда обжигают формованный материал, имеющий объемную плотность, превосходящую 40% относительно теоретической плотности, на стадии обжига происходит реакция агломерации, вследствие чего для получения порошка комплексного оксида металла необходимо измельчение, и в некоторых случаях порошок оксида металла, имеющий узкое распределение по размерам, не может быть получен.
Соответствующая температура обжига не является неизбежно решающей, так как зависит от вида получаемого комплексного оксида металла, видов и концентраций галогенида водорода, молекулярного галогена и компонента, полученного из молекулярного галогена и водяного пара, или времени обжига. Она предпочтительно составляет от 500 до 1500oC, более предпочтительно от 600 до 1400oC. Когда температура обжига ниже 500oC, может быть затруднительным получение желательного комплексного оксида металла, содержащего по крайней мере два металлических элемента, и для обжига необходим большой период времени. Когда температура обжига превосходит 1500oC, имеется склонность к образованию в полученном порошке комплексного оксида металла большого количества агломерированных частиц.
Соответствующее время обжига не является неизбежно решающим, так как зависит от вида получаемого комплексного оксида металла, видов и концентраций галогенида водорода, молекулярного галогена и компонента, полученного из молекулярного галогена и водяного пара, или температуры обжига. Оно составляет предпочтительно по крайней мере 1 мин, более предпочтительно по крайней мере 10 мин, и его выбирают из диапазона, в котором получают желательный порошок оксида металла. Чем выше температура обжига, тем меньше время обжига.
Когда обжигают исходный порошок оксида металла, содержащий затравочный кристалл, температура обжига может быть ниже, и время обжига может быть меньше, чем температура обжига и время обжига, когда затравочный кристалл не используют, так как оксид металла, растет вокруг затравочных кристаллов в качестве участков роста.
Вид устройства для обжига не ограничен и может быть использована так называемая обжиговая печь. Обжиговую печь предпочтительно выполняют из материала, который не корродирует под воздействием галогена, и она предпочтительно содержит механизм для регулирования атмосферы.
Так как используют кислый газ, такой как галогенид водорода или молекулярный галоген, обжиговая печь является предпочтительно воздухонепроницаемой. В промышленном производстве обжиг осуществляют предпочтительно непрерывно, и можно использовать туннельную печь, вращающуюся обжиговую печь или толкательную печь.
В качестве сосуда, используемого на стадии обжига, в который загружают исходный порошок оксида металла, предпочтительно используют тигель или лодочку, выполненную из оксида алюминия, кварца, кислотоустойчивого кирпича, графита или благородного металла, например платины, так как реакция протекает в кислой атмосфере.
Когда порошок комплексного оксида металла получают при добавлении к исходному порошку затравочного кристалла, крупность частиц и распределение по крупности порошка комплексного оксида металла как продукта можно регулировать путем изменения крупности частиц и добавленного количества зародышевого кристалла. Например, когда количество зародышевого кристалла возрастает, крупность частиц полученного порошка комплексного оксида металла уменьшается. Когда используют затравочный кристалл, имеющий уменьшенную крупность частиц, крупность частиц полученного порошка комплексного оксида металла уменьшается.
Путем вышеописанного способа, который показан на приложенных фотоснимках, может быть получен порошок комплексного оксида металла, содержащий по крайней мере два металлических элемента, который не является агломерированными частицами, и имеет узкое распределение по крупности и однородный размер частиц, при этом крупность частиц можно регулировать.
Хотя порошок комплексного оксида металла может быть агломерированными частицами или содержать агломерированные частицы, степень агломерации незначительна и, следовательно, порошок комплексного оксида металла, который не содержит агломерированных частиц, легко получить путем простого измельчения.
В зависимости от исходных материалов или производственных условий в добавление к желательному комплексному оксиду металла, содержащему по крайней мере два металлических элемента, может остаться побочный продукт или непрореагировавший исходный оксид. В таком случае его оставшееся количество является очень незначительным и желательным, и желательный комплексный оксид металла можно получить путем соответствующего выбора реакционных условий, или отделением побочного продукта или непрореагировавшего исходного материала посредством, например, простой промывки.
Среднечисленный размер частиц порошка комплексного оксида металла, полученного способом настоящего изобретения, не является неизбежно ограниченным.
В общем можно получить порошок комплексного оксида металла, имеющий крупность частиц от 0,1 до 500 мкм, предпочтительно от 0,1 до 300 мкм.
Порошок комплексного оксида металла, полученный способом настоящего изобретения, имеет в качестве распределения по крупности соотношение D90/D10, равное 10 или меньше, предпочтительно 5 или меньше, где D10 и D90 представляют крупность частиц при 10 и 90%-ном аккумулировании соответственно исходя из самой маленькой крупности частиц на суммарной кривой гранулометрического состава частиц.
Когда распределение по крупности определяют методом центробежного осаждения или методом лазерного дифракционного рассеяния, полученное значение представляет распределение по крупности агломерированных частиц. Когда распределение по крупности, измеренное посредством такого метода, является узким, но порошок содержит агломерированные частицы, диспергируемость ухудшается, и такой порошок является неподходящим в качестве промышленного сырья.
В настоящем изобретении в качестве критерия агломерации порошка измеряют крупность исходных частиц в виде среднечисленного значения из фотоснимка, полученного на растровом электронном микроскопе, и полученное значение сравнивают с крупностью агломерированной частицы, т.е. с крупностью частицы при 50%-ном аккумулировании на суммарном кривой гранулометрического состава частиц (D50).
То есть степень агломерации вычисляют посредством отношения крупности агломерированной частицы к крупности исходной частицы. Когда это отношение превосходит 1, порошок находится в идеальном состоянии и не содержит агломерированных частиц. В фактически существующем порошке это соотношение превосходит 1. Когда это соотношение равно 6 или меньше, порошок можно предпочтительно использовать в качестве исходного материала для промышленных применений.
Порошок комплексного оксида металла, полученный способом настоящего изобретения, имеет отношение крупности агломерированной частицы к крупности исходной частицы, предпочтительно от 1 до 6, более предпочтительно от 1 до 3, наиболее предпочтительно от 1 до 2.
Каждая из частиц порошка оксида металла настоящего изобретения имеет полиэдрическую форму, имеющую по крайней мере 6 плоскостей. Количество плоскостей обычно оставляют от 6 до 60, предпочтительно от 6 до 30.
Далее будут приведены конкретные примеры порошка комплексного оксида металла настоящего изобретения.
Порошок иттрий-алюминиевого граната настоящего изобретения представляет массу частиц, составляющих порошок, и отличается тем, что их форма и крупность являются однородными. Форма является полиэдрической и имеет по крайней мере 6 плоскостей. В зависимости от используемого исходного материала и условий обжига, частицы, которые заключены в кубы, имеют полиэдрические формы, имеющие по крайней мере 8 плоскостей, которые заключены в сферы и имеют однородную форму и крупность.
Крупность частиц и распределение по крупности порошка иттрий-алюминиевого граната настоящего изобретения находятся в определенных диапазонах. Крупность частицы регулируют в диапазоне между около 1 мкм и несколькими сотнями мкм. Такое регулирование может быть достигнуто путем выбора исходного материала и условий обжига вышеописанного способа настоящего изобретения.
В качестве исходного порошка для получения монокристалла подходящим является порошок, имеющий повышенную крупность частиц. Для этой цели может быть использован иттрий-алюминиевый гранат, содержащий частицы, имеющие крупность по крайней мере 20 мкм, более предпочтительно по крайней мере около 50 мкм. То есть вышеописанный способ может давать порошок иттрий-алюминиевого граната, имеющий относительно большую среднюю крупность частиц, подходящую для получения монокристалла промышленно выгодным способом.
В соответствии с настоящим изобретением легко получить порошок иттрий-алюминиевого граната, имеющий в качестве распределения по крупности отношение D90/D10, равное 10 или менее, предпочтительно равное 5 или менее. Кроме того, легко получить порошок граната, имеющий отношение крупности агломерированных частиц, предпочтительно от 1 до 3, более предпочтительно от 1 до 2.
Соответственно порошок иттрий-алюминиевого граната настоящего изобретения является подходящим для флуоресцентных свойств вещества, на которые оказывают влияние крупность частиц, однородность и диспергируемость исходного сырья. Порошок железного граната, например порошок железо-иттриевого и железо-гадолиниевого граната настоящего изобретения, представляет массу частиц, составляющих порошок, и отличается тем, что форма и крупность частиц являются однородными.
Форма является полиэдрической и имеет 8 плоскостей. Крупность частиц и распределение по крупности находятся в конкретных диапазонах. Крупность частиц регулируют в диапазоне между около 1 мкм и несколькими сотнями мкм. Такое регулирование может быть достигнуто путем выбора исходного материала и условий обжига вышеописанного способа настоящего изобретения.
В соответствии с настоящим изобретением легко получить порошок железного граната, имеющий в качестве распределения по крупности отношение D90/D10, равное 10 или менее, предпочтительно 5 или менее. Кроме того, легко получить порошок граната, имеющий отношение крупности агломерированных частиц и крупности исходных частиц, равное предпочтительно от 1 до 3, более предпочтительно от 1 до 2.
Порошок твердого раствора оксида иттрия и оксида циркония представляет массу частиц, составляющих порошок, и отличается тем, что форма и размер частиц однородны. Форма является полиэдрической и имеет по крайней мере 8 плоскостей. Крупность частиц и распределение по крупности находятся в конкретных диапазонах. Крупность частиц регулируют в диапазоне между около 1,0 мкм и несколькими десятками мкм. Такое регулирование может быть достигнуто путем выбора исходного материала и условий обжига вышеописанного способа настоящего изобретения.
В соответствии с настоящим изобретением можно получить различные порошки комплексного оксида металла, каждый из которых содержит по крайней мере два металлических элемента, которые не являются агломерированными частицами и имеют узкое распределение по крупности, которое не могло быть достигнуто до настоящего времени.
Полученный порошок комплексного оксида металла, содержащий по крайней мере два металлических элемента, представляет массу однородных полиэдрических частиц и может быть использован в ряде применений, например, в качестве исходных материалов металлооксидной керамики, которую используют в качестве функционального материала или конструкционного материала, в качестве наполнителя, абразивного материала или пигмента, или в качестве исходного порошка для получения монокристалла или покрытия, нанесенного методом пламенного распыления.
Путем выбора крупности частиц и количества затравочного кристалла можно получить комплексный оксид металла, имеющий вышеуказанные свойства и произвольно регулируемую крупность частиц.
Примеры.
В дальнейшем настоящее изобретение будет объяснено более подробно с помощью примеров, которые никоим образом не ограничивают область настоящего изобретения. В примерах осуществляли следующие измерения.
1. Среднечисленная крупность частиц порошка оксида металла.
Фотоснимок порошка оксида металла на растровом электронном микроскопе получали с использованием электронного микроскопа (Т-300, изготовленного Nippon Electron Co., Ltd).
Из фотоснимка отбирали от 80 до 100 частиц, и изображение анализировали для вычисления среднего значения диаметров эквивалентных окружностей частиц и распределения.
Диаметр эквивалентной окружности представляет диаметр окружности, имеющей ту же самую площадь, которую имеет каждая частица на фотоснимке.
2. Распределение по крупности порошка оксида металла.
Распределение по крупности измеряли с использованием основного классификатора (изготовленного Malvern Instrument, Inc.) или лазерно-дифракционного анализатора распределения по крупности (SALD-1100, изготовленного Shimadzu Corporation).
Порошок оксида металла диспергировали в водном растворе полиаммонийакрилата или в 50 вес.%-ном водном растворе глицерина и измеряли крупность частиц при 10, 50 и 90%-ном аккумулировании соответственно исходя от самой маленькой крупности частиц на суммарной кривой гранулометрического состава частиц в виде D10•D50 и D90•D50 использовали в качестве крупности агломерированной частицы, а отношение D90/D10 рассчитывали как критерий распределения по крупности.
3. Кристаллическая фаза порошка оксида металла.
Кристаллическую фазу порошка оксида металла измеряли с помощью метода дифракции рентгеновских лучей (RAD-C, изготовлен Rigaku Co, Ltd).
4. Удельная поверхность порошка оксида металла по БЭТу (уравнение Брунауэра-Эммета-Теллера).
Удельную поверхность порошка оксида металла по БЭТу измеряли с помощью FLOWSORB-11 (изготовленного Micromelitics).
5. Анализ композиции порошка оксида металла.
Порошок оксида металла растворяли, например в кислотной смеси фосфорной и серной кислот, и композицию порошка оксида металла анализировали с использованием индуктивно связанной плазменной аппаратуры SPS 1200-YR, изготовленной Seiko.
В качестве хлористоводородного газа использовали хлористый водород в ампуле (чистота 99,9%), поставляемый Tsurumi Soda Co., Ltd, или газ, полученный при разложении хлорида аммония (WAKO JUNYAKU, особо чистого). Когда использовали газ, полученный при разложении хлорида аммония, в муфель печи для получения атмосферного газа вводили газ возгонки хлорида аммония при температуре выше температуры возгонки. Хлорид аммония полностью разложился при 1100oC, что обеспечило получение газа, состоящего из 3 об.% хлористоводородного газа, 17 об.% азота и 50 об.% водорода.
В качестве хлористого газа использовали газообразный хлор в ампуле (чистотa 99,4%), поставляемый Fujimoto Industries, Co, Ltd).
В качестве бромистоводородного газа использовали газ разложения бромида аммония (WAКO JUNYAKU, особой чистоты).
В муфель печи для получения атмосферного газа вводили газ возгонки бромида аммония, полученный путем нагревания бромида аммония при температуре выше температуры возгонки. Бромид аммония полностью разложился при 1100oC, что обеспечило получение газа, состоящего из 33 об.% бромистоводородного газа, 17 об.% азота и 50 об.% водорода.
В качестве иодистоводородного газа использовали газ разложения иодида аммония (WAKO JUNYAKU, особой чистоты). В муфель печи для получения атмосферного газа вводили газ возгонки иодида аммония, полученный путем нагрева иодида аммония при температуре выше температуры его возгонки. Иодид аммония полностью разложился при 1100oC, что обеспечило получение газа, состоящего из 25 об.% иодистоводородного газа, 16 об.% азота, 52 об.% водорода и 6 об.% иода (I, I2), который образуется путем разложения йодистого водорода.
Исходный порошок оксида металла загрузили в алюминиевый или платиновый сосуд. Когда использовали галоген, порошок загружали в алюминиевый сосуд. Глубина заполнения порошка составила 5 мм.
Обжиг осуществляли в цилиндрической печи, имеющей кварцевый или алюминиевый муфель (изготовленный Моtoyama Co., Ltd). Температуру поднимали со скоростью нагрева от 300 до 500oC/ч при подаче воздуха или азота, и когда температура достигла температуры ввода атмосферного газа, ввели атмосферный газ.
Концентрацию атмосферного газа регулировали путем контроля скорости газового потока посредством расходомеров. Скорость потока атмосферного газа регулировали до линейной скорости 20 мм/мин. Общее давление атмосферного газа составляло всегда 1 атм.
После того как температура достигла предварительно определенной температуры, порошок выдерживали при этой температуре в течение предварительно определенного периода времени. Их отнесли к "температуре выдержки" (температура обжига) и "времени выдержки" (время обжига).
После предварительно определенного времени выдержки порошок самопроизвольно охладили для получения желательного порошка оксида металла.
Парциальное давление пара регулировали путем изменения давления насыщенного пара в зависимости от температуры воды, и в печь с воздухом или азотом вводили водяной пар.
Пример 1.
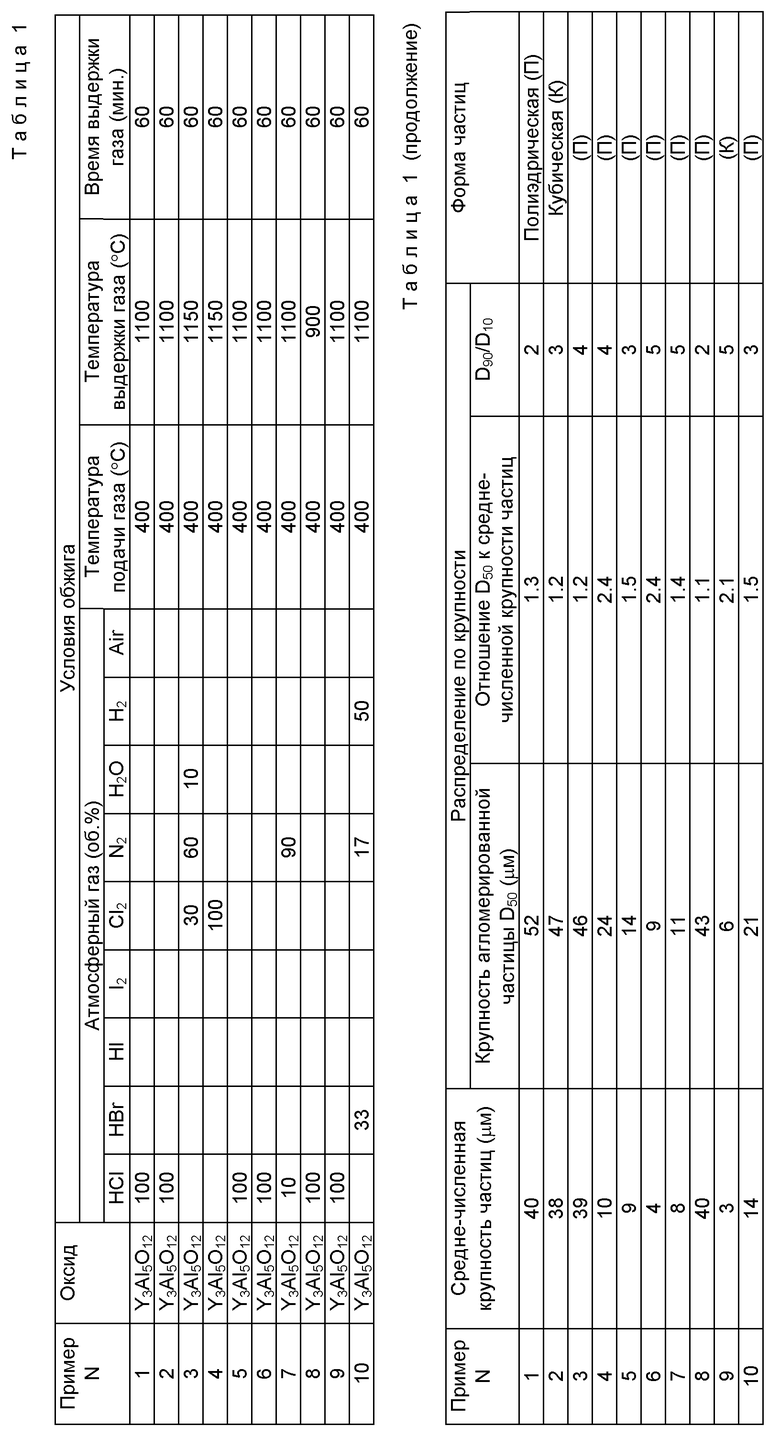
Порошок оксида иттрия (чистотой 99,9%, средняя крупность частицы 0,4 мм, производимый Nippon Yttrium Co., Ltd) (3,387 г), и γ-оксид алюминия (AKP-G 15, производимый Sumitomo Chemical Co., Ltd), (2,683 г) загрузили в изопропанол (WAKO JUNYAKU), особо чистый (100 г) и перемешивали в течение 10 мин при дисперсии путем применения ультразвуковой волны, после чего осуществляли удаление изопропанола с помощью испарителя и вакуумной сушилки для получения смешанного порошка оксида алюминия.
Этот порошок загрузили в платиновый сосуд. Его объемная плотность составила 12% от теоретической плотности. Затем порошок поместили в кварцевый муфель и нагревали от комнатной температуры со скоростью 20 мм/мин. Когда температура достигла 400oC, азот заменили на атмосферный газ, состоящий из 100 об. % хлористого водорода. Порошок обжигали при 1100oC в течение 60 мин при протекании атмосферного газа с линейной скоростью 20 мм/мин, после чего осуществили самопроизвольное охлаждение для получения порошка иттрий-алюминиевого граната.
Вес порошка в платиновом сосуде после обжига составил 86% от веса порошка перед обжигом.
Полученный порошок в соответствии с результатом рентгеноструктурного анализа был иттрий-алюминиевым гранатом, представленным Y3Al5O12, при этом другой пик не наблюдали. В соответствии с наблюдениями с помощью растрового электронного микроскопа установили, что иттрий-алюминиевый гранат состоял из полиэдрических частиц, имеющих по крайней мере 8 плоскостей и имел среднечисленную крупность частиц 40 мкм. Крупность агломерированной частицы (D50) в соответствии с измерением распределения по крупности составила 52 мкм, а соотношение D90/D10 составило 2, что указывало на узкое распределение по крупности.
Отношение крупности агломерированной частицы к среднечисленной крупности частиц составило 1,3. Результаты представлены в таблице 1. Электронно-микроскопический снимок полученного порошка показан на фиг. 1, распределение по крупности показано на фиг. 2 и рентгеновская дифракционная картина (рентгенограмма) показана на фиг. 3.
Пример 2.
Тем же самым образом, что и в примере 1, за исключением того, что вместо, γ-оксида алюминия использовали α-оксид алюминия (AKP-50, производимый Sumitomo Chemical Co., Ltd) (2,549 г), получили смешанный порошок оксида иттрия и оксида алюминия. Объемная плотность этого порошка составила 17% от теоретического значения.
В дальнейшем тем же самым образом, что и в примере 1, получили порошок иттрий-алюминиевого граната.
Полученный порошок в соответствии с результатом рентгеноструктурного анализа был иттрий-алюминиевым гранатом, представленным Y3Al5O12, при этом другой пик не наблюдали. В соответствии с наблюдениями с помощью растрового электронного микроскопа установили, что иттрий-алюминиевый гранат состоял из полиэдрических частиц, имеющих кубическую форму или кубическую форму, узлы которой срезаны, и имел среднечисленную крупность частиц 38 мкм.
Крупность агломерированной частицы (D50) в соответствии с измерением распределения по крупности составила 47 мкм, и соотношение D90/D10 было равно 3, что указывало на узкое распределение по крупности. Отношение крупности агломерированной частицы к среднечисленной крупности частицы составило 1,2. Результаты представлены в таблице 1. Электронно-микроскопический снимок полученного порошка показан на фиг. 4, распределение по крупности показано на фиг. 5, и рентгеновская дифракционная картина (рентгенограмма) показана на фиг. 6.
Пример 3.
Тем же самым образом, что и в примере 1, за исключением того, что вместо атмосферного газа, состоящего из 100 об.% хлористого водорода, использовали атмосферный газ, состоящий из 30 об.% хлора, 10 об.% водяного пара и 60 об.% азота, получили порошок иттрий-алюминиевого граната.
Результаты показаны в таблице 1.
Пример 4.
Тем же самым образом, что и в примере 1, за исключением того, что вместо атмосферного газа, состоящего из 100 об.% хлористого водорода, использовали атмосферный газ, состоящий из 100 об.% хлора, и температуру обжига изменили на 1150oC, получили порошок иттрий-алюминиевого граната. Электронно-микроскопический снимок полученного порошка показан на фиг. 7.
Результаты приведены в таблице 1.
Пример 5.
Для получения зародышевого кристалла обжигали при 1200oC в течение 3 ч смешанный порошок оксида иттрия и оксида алюминия, который использовали в качестве исходного материала в примере 1. В соответствии с рентгеноструктурным анализом зародышевый кристалл показал пики, приписываемые YAlO3; Y4A2O9; Y2O3, Al2O3 и т.д., в добавление к пикам, приписываемым иттрий-алюминиевому гранату, представленному формулой Y3Al5O12.
Этот зародышевый кристалл добавили в количестве 3 вес.% к смешанному порошку оксида иттрия и оксида алюминия, который использовали в качестве исходного материала в примере 1, для получения исходного порошка, содержащего зародышевый кристалл. Способ добавления включал диспергирование исходного порошка и зародышевого кристалла посредством ультразвуковой волны в изопропаноле для получения суспензии и сушку суспензии испарителем и вакуумной сушилкой.
Тем же самым образом, что и в примере 1, за исключением того, что использовали исходный порошок, содержащий зародышевый кристалл, получили порошок иттрий-алюминиевого граната. Полученный порошок в соответствии с результатом рентгеноструктурного анализа был иттрий-алюминиевым гранатом, представленным Y3Al5O12, при этом другой пик не наблюдали. Результаты представлены в таблице 1. Электронно-микроскопический снимок полученного порошка показан на фиг. 8.
Пример 6.
Для получения зародышевого кристалла при 1400oC в течение 3 ч обжигали смешанный порошок оксида иттрия и оксида алюминия, который использовали в качестве исходного материала в примере 1. В соответствии с рентгеноструктурным анализом зародышевый кристалл показал пики, приписываемые Y2O3, Al2O3 и т. д. , в добавление к пикам, приписываемым иттрий-алюминиевому гранату, представленному Y3Al5O12.
Тем же самым образом, что и в примере 5, за исключением того, что использовали зародышевый кристалл, получили порошок иттрий-алюминиевого граната.
Результаты представлены в таблице 1. Электронно-микроскопический снимок полученного порошка представлены на фиг. 9.
Пример 7.
Порошок оксида иттрия (производимый Nippon Yttrium Co., Ltd чистотой 99,9%, имеющий среднюю крупность частиц 0.4 мкм (3,387 г) и оксида алюминия (АКР-G 15, γ-оксид алюминия, производимый Sumitomo Chemical Co., Ltd., чистотой 99,99%) (2,952 г) загрузили в изопропанол (100 г) и смешали во влажном состоянии, после чего для получения смешанного порошка оксида иттрия и оксида алюминия (соотношение A, равное Y:Al = 3,5: 5), осуществили удаление изопропанола. Этот порошок использовали в качестве исходного порошка.
Этот порошок загрузили в платиновый сосуд, поместили в кварцевый муфель и нагрели от комнатной температуры со скоростью нагрева 300oC/ч при протекании азота с линейной скоростью 20 мм/мин.
Когда температура достигла 400oC, азот заменили атмосферным газом, состоящим из 10 об.% хлористого водорода и 90 об.% азота. Порошок обжигали при 1100oC в течение 60 мин при протекании атмосферного газа с линейной скоростью 20 мм/мин, после чего для получения порошка иттрий-алюминиевого граната осуществили самопроизвольное охлаждение.
Результаты представлены в таблице 1.
Пример 8.
Тем же самым образом, что и в примере 1, за исключением того, что тот же самый исходный смешанный порошок обжигали при 900oC, получили порошок иттрий-алюминиевого граната. В соответствии с рентгеноструктурным анализом было подтверждено, что полученный порошок представлял единую фазу иттрий-алюминиевого граната. Результаты показаны в таблице 1.
Пример 9.
Смешанный порошок оксида иттрия и оксида алюминия, который использовали в примере 2, предварительно обжигали при 1200oC на воздухе в течение 3 ч.
Обожженный порошок в соответствии с рентгеноструктурным анализом показал пики, приписываемые YAlO3, Y4Al2O9, Y2O3 и т.д., в добавление к пикам, приписываемым иттрий-алюминиевому гранату, представленному формулой Y3Al5O12.
Обожженный порошок частично содержал образованный иттрий-алюминиевый гранат, т.е. зародышевый кристалл иттрий-алюминиевого граната.
Тем же самым образом, что и в примере 1, за исключением того, что в качестве исходного порошка использовали вышеприведенный порошок, получили порошок иттрий-алюминиевого граната. В соответствии с рентгеноструктурным анализом полученный порошок представлял единую фазу иттрий-алюминиевого граната. В соответствии с наблюдением с помощью растрового электронного микроскопа иттрий-алюминиевый гранатовый оксид состоял из полиэдрических частиц, имеющих кубическую форму, углы которой срезаны. Результаты показаны в таблице 1.
Пример 10.
Исходный порошок, который использовали в примере 7, загрузили в алюминиевый сосуд, поместили в кварцевый муфель и нагревали со скоростью нагрева 300oC/ч. Когда температура достигла 400oC, в муфель ввели газ возгоночного разложения бромида аммония, и в этой газовой атмосфере порошок обжигали при 1100oC в течение 60 мин, после чего самопроизвольно охладили для получения порошка иттрий-алюминиевого граната. Компонентами газа, полученного при разложении бромида аммония при 1100oC, были бромистоводородный газ, азот и водород при объемном отношении 33:17:50.
Фиг. 8 представляет электронно-микроскопический снимок, показывающий структуру частицы полученного порошка. Рентгеноструктурный анализ подтвердил, что порошок представлял единую фазу иттрий-алюминиевого граната. Результаты показаны в таблице 1.
Пример 11.
Порошок оксида иттрия (производимый Nippon Yttrium Co., Ltd, чистотой 99,9%, имеющий среднюю крупность частиц 0,4 мкм) (6,436 г), порошок оксида тербия (производимый Kanto Chemical Co., Ltd, чистотой 99,9%) (0,561 г) и порошок оксида алюминия (AKO-G 15) γ-оксид алюминия, производимый Sumitomo Chemical Co., Ltd, чистотой 99,99 %) (5,903 г) загрузили в изопропанол (100 г) и смешали во влажном состоянии, после чего для получения смешанного порошка, используемого в качестве исходного смешанного порошка, в котором 5 ат.% иттрия заменили тербием, осуществили удаление изопропанола.
Тем же самым образом, что и в примере 1, за исключением того, что использовали этот исходный смешанный порошок, получили замещенный тербием порошок иттрий-алюминиевого граната.
Рентгеноструктурный анализ подтвердил, что полученный порошок представлял единую фазу иттрий-алюминиевого граната. В соответствии с индуктивно связанным плазменным анализом было подтверждено, что полученные частицы содержали 3,2 ат.% тербия.
Результаты показаны в табл. 2.
Пример 12.
Тем же самым образом, что и в примере 11, за исключением того, что вместо порошка оксида тербия использовали порошок оксида диспрозия (производимый Nippon Yttrium Co., Ltd чистотой 99,99%) (0.5595 г), получили исходный смешанный порошок, в котором 5 ат.% иттрия заменили диспрозием.
Тем же самым образом, что и в примере 1, за исключением того, что использовали вышеприведенный исходный смешанный порошок, получили иттрий-алюминиевый гранат, замещенный диспрозием.
Фиг. 11 представляет электронно-микроскопический снимок, показывающий структуру полученного порошка.
Рентгеноструктурный анализ подтвердил, что полученный порошок представлял единую фазу иттрий-алюминиевого граната.
Индуктивно связанный плазменный анализ подтвердил, что полученные частицы содержали 4,5 ат.% диспрозия.
Результаты показаны в таблице 2.
Пример 13.
Порошок оксида иттрия (производимый Nippon Yttrium Co., Ltd, чистотой 99,9%, имеющий среднюю крупность частиц 0,4 мкм (4,968 г) и порошок оксида алюминия (AKP-G 15, γ-оксид алюминия, производимый Sumitomo Chemical Co., Ltd чистотой 99,99%) (1,181 г) загрузили в изопропанол (100 г) и смешали во влажном состоянии, после чего для получения смешанного порошка, используемого в качестве исходного смешанного порошка (отношение Y:Al в смеси = 3: 1,5) осуществили удаление изопропанола. Тем же самым образом, как и в примере 1, за исключением того, что использовали исходный смешанный порошок, исходный порошок обжигали.
Полученный порошок содержал полиэдрические частицы и побочный продукт. Рентгеноструктурный анализ подтвердил, что полиэдрические частицы представляли иттрий-алюминиевый гранат, а подобный продукт представлял оксихлорид иттрия (YOCl). YOCl легко удалили путем промывки и отобрали иттрий-алюминиевый гранат.
Результаты представлены в таблице 2.
Пример 14.
Порошок оксида иттрия (производимый Nippon Yttrium Co., Ltd, чистотой 99,9 %, имеющий среднюю крупность частиц 0,4 мкм) (2,936 г) и порошок оксида алюминия (AKP-G 15, γ-оксид алюминия), производимый Sumitomo Chemical Co., Ltd, чистотой 99,999%) (3,256 г) загрузили в изопропанол (100 г) и смешали во влажном состоянии, после чего для получения смешанного порошка оксида иттрия и оксида алюминия (при соотношении в смеси Y:Al = 3:7) в качестве исходного порошка осуществили удаление изопропанола.
Тем же самым образом, что и в примере 1, за исключением того, что использовали исходный смешанный порошок, исходный порошок обжигали.
Полученный порошок содержал полиэдрические частицы и частицы, имеющие относительно маленькую крупность. Рентгеноструктурный анализ подтвердил, что полиэдрические частицы представляли иттрий- алюминиевый гранат, а частицы маленькой крупности представляли α-Al2O3, α-Al2O3 удалили путем просеивания и отобрали и алюминиевый гранат.
Результаты показаны в таблице 2.
Пример 15.
Исходный порошок, который использовали в примере 1, загрузили в платиновый сосуд, поместили в кварцевый муфель и нагревали со скоростью нагрева 300oC/ч. Когда температура достигла 400oC, в муфель ввели газ возгоночного разложения иодида аммония, и в этой газовой атмосфере порошок обжигали при 1200oC в течение 60 мин, после чего для получения порошка иттрий-алюминиевого граната осуществили самопроизвольное охлаждение. Компонентами газа, полученного при разложении иодида аммония при 1200oC, были иодистоводородный газ, иод, азот и водород при объемном соотношении 25:6:16:52.
Рентгеноструктурный анализ подтвердил, что полученный порошок представлял единую фазу иттрий-алюминиевого граната.
Результаты показаны в таблице 1.
Сравнительные примеры 1 и 2.
Для получения порошка соответствующего оксида в течение 3 ч при 1200oC на воздухе обжигали смешанный порошок оксида иттрия и оксида алюминия, который использовали в каждом из примеров 1 и 2.
Рентгеноструктурный анализ порошка оксида показал пики, приписываемые YAlO3, Y4Al2O9, Y2O3, Al2O3 и т.д., в добавление к пикам, приписываемым иттрий-алюминиевому гранату, представленному Y3Al5O12. В соответствии с наблюдениями, осуществляемыми посредством растрового электронного микроскопа, полиэдрические частицы не образовывались, и частицы имели неправильную форму и были в агломерированном состоянии.
Порошок cравнительного примера 1 имел среднечисленную крупность частиц 0,2 мкм. Крупность агломерированных частиц (D50) в соответствии с измерением распределения по крупности составила 4 мкм, соотношение D90/D10 было равно 15, что указывало на широкое распределение по крупности.
Отношение крупности агломерированной частицы к среднечисленной крупности частицы было равно 20. Результаты представлены в таблице 2. Электронно-микроскопический снимок порошка, полученного в сравнительном примере 1, показан на фиг. 12. Распределение по крупности порошка, полученного в сравнительном примере 2, показано на фиг. 13.
Сравнительный пример 3.
Исходный смешанный порошок, который использовали в примере 1, обжигали на воздухе при 1400oC. Согласно рентгеноструктурному анализу полученный порошок содержал в качестве основной фазы иттрий-алюминиевый гранат, но при этом наблюдали YalO3, α-Al2O3 и Y2O3.
Рост кристалла был неясным, частицы имели неправильную форму и были в агломерированном состоянии, при этом иттрий-алюминиевый гранат, имеющий однородную крупность частиц, не образовывался.
Результаты показаны в таблице 2.
Сравнительный пример 4.
Тем же самым образом, что и в примере 6, за исключением того, что вместо атмосферного газа, состоящего из 100 об.% хлористого водорода, подавали атмосферный газ комнатной температуры, состоящий из 100 об.% воздуха, для получения порошка оксида исходный порошок обжигали.
Полученный порошок, согласно рентгеноструктурному анализу, показал пики, приписываемые YAlO3, Y4Al2O9, Y2O3, Al2O3 и т.д., в добавление к пикам, приписываемым иттрий-алюминиевому гранату, представленному Y3Al5O12.
В соответствии с наблюдениями посредством растрового электронного микроскопа, полиэдрические частицы не образовывались, и частицы имели неправильную форму и были в агломерированном состоянии.
Результаты показаны в таблице 2.
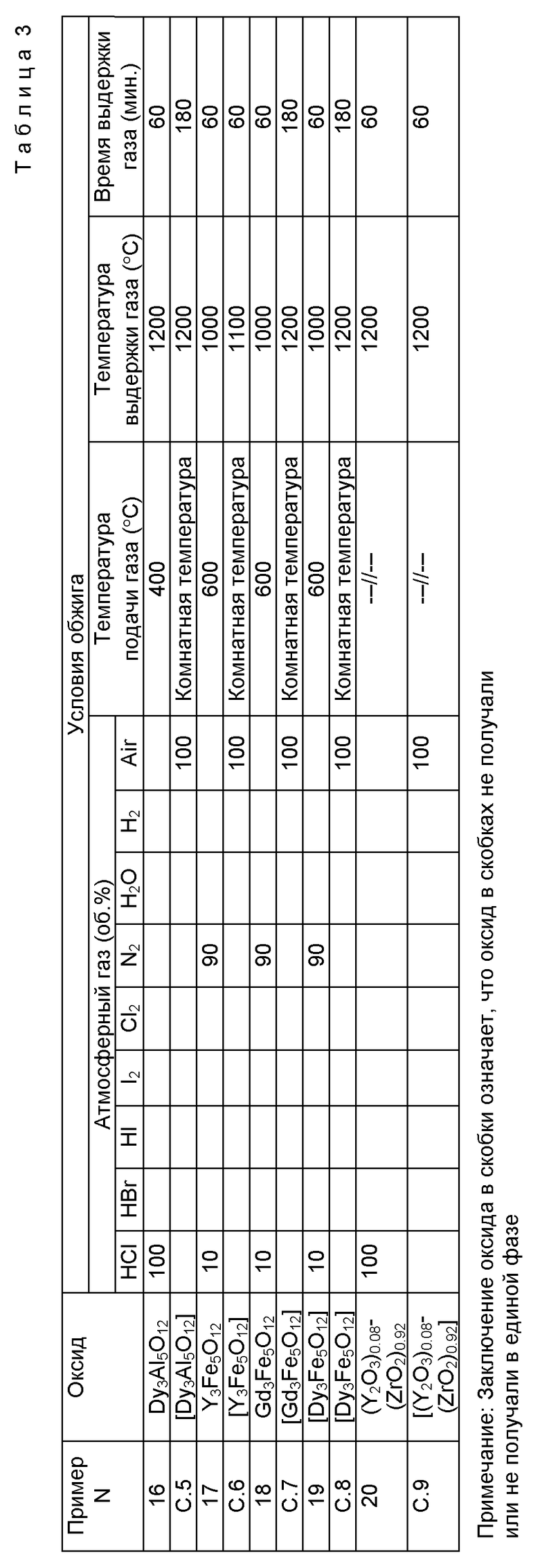
Пример 16.
Порошок оксида диспрозия (чистотой 99,99%, производимый Nippon Yttrium Co. , Ltd) и γ-оксид-алюминия (AKP-G 15, производимый Sumitomo Chemical Co., Ltd) взвесили таким образом, чтобы молекулярное отношение диспрозия к алюминию было 3:5, и смешали в изопропаноле (WAKO JUNYAKU, особо чистом) при диспергировании порошков путем использования ультразвуковой волны, после чего для получения смешанного порошка оксида диспрозия и оксида алюминия осуществили удаление изопропанола с помощью испарителя и вакуумной сушилки. Этот порошок загрузили в платиновый сосуд.
Затем порошок поместили в кварцевый муфель и нагрели от комнатной температуры со скоростью нагрева 300oC/ч при протекании азота с линейной скоростью 20 мм/мин. Когда температура достигла 400oC, азот заменили на атмосферный газ, состоящий из 100%-ного хлористого водорода. Порошок обжигали при 1200oC в течение 60 мин при протекании атмосферного газа с линейной скоростью 20 мм/мин, после чего для получения порошка оксида его самопроизвольно охладили.
Полученный порошок в соответствии с рентгеноструктурным анализом был диспрозий-алюминиевым гранатом, представленным формулой Dy3Al5O12, при этом другой пик не наблюдали. В соответствии с наблюдениями с помощью растрового электронного микроскопа диспрозий-алюминиевый гранатовый оксид состоял из полиэдрических частиц, имеющих по крайней мере 8 плоскостей и имел среднечисленную крупность частиц 44 мкм. Крупность агломерированной частицы (D50) в соответствии с измерением распределения по крупности составила 53 мкм, а отношение D90/D10 было равно 3, что указывало на узкое распределение по крупности. Отношение крупности агломерированных частиц к среднечисленной крупности частиц составило 1, 2. Результаты приведены в таблице 3. Электронно-микроскопический снимок полученного порошка показан на фиг. 14.
Сравнительный пример 5.
Смешанный порошок оксида диспрозия и оксида алюминия, который получен в примере 16, обжигали на воздухе при 1200oC в течение 3 ч, чтобы получить порошок оксида.
В соответствии с рентгеноструктурным анализом полученного порошка оксида наблюдали пики, приписываемые Al2Dy4O9, AlDyO3, Dy2O3, Al2O3 и т.д., но пик, приписываемый диспрозий-алюминиевому гранату, представленному формулой Dy3Al5O12, не наблюдали. Согласно наблюдениям с помощью растрового электронного микроскопа полиэдрические частицы не образовывались, и частицы имели неправильную форму и были в агломерированном состоянии. Результаты показаны в таблице 3. Электронно-микроскопический снимок полученного порошка показан на фиг. 15.
В дальнейшем будут объяснены примеры и cравнительные примеры для железо-иттриевого граната, железо-гадолиниевого граната и железо-диспрозиевого граната.
Пример 17.
γ-оксид железа (III) (удельная поверхность по БЭТу 34,4 м2/г) загрузили в тигель, изготовленный из оксида алюминия, и нагрели в воздухе при скорости нагрева 300oC/ч при температуре 1000oC в течение 3 ч, чтобы получить порошок оксида железа. Этот порошок имел удельную поверхность по БЭТу 0,8 м2/г.
Вышеприведенный порошок оксида железа и порошок оксида иттрия (чистотой 99,9%, средняя крупность частиц 0,4 мкм, производимый Nippon Yttrium Co., Ltd) взвесили таким образом, чтобы молярное отношение иттрия к железу было равно 3:5, и смешали в изопропаноле (WAKO JUNYAKU, особо чистом) при диспергировании порошков с применением ультразвуковой волны, после чего для получения смешанного порошка оксида иттрия и оксида железа осуществили удаление изопропанола с помощью испарителя и вакуумной сушилки.
Этот порошок загрузили в платиновый сосуд. Затем порошок поместили в кварцевый муфель и нагревали от комнатной температуры со скоростью нагрева 300oC/ч при протекании азота с линейной скоростью 20 мм/мин. Когда температура достигла 600oC, азот заменили на атмосферный газ, состоящий из 10 об. % хлористого водорода и 90 об.% азота. При протекании атмосферного газа с линейной скоростью 20 мм/мин порошок обжигали при 1000oC в течение 60 мин, после чего для получения порошка оксида осуществили самопроизвольное охлаждение.
Полученный порошок в соответствии с рентгеноструктурным анализом был железо-иттриевым гранатом, представленным формулой Y3Fe3O12, при этом пик не наблюдали. В соответствии с наблюдениями с помощью растрового электронного микроскопа порошок железо-иттриевого граната состоял из полиэдрических частиц, имеющих по крайней мере 8 плоскостей, и имел среднечисленную крупность частиц 13 мкм. Крупность агломерированных частиц (D50) в соответствии с измерением распределения по крупности составила 16 мкм, и отношение D90/D10 было равно 2, что указывало на узкое распределение по крупности. Отношение крупности агломерированных частиц к среднечисленной крупности частиц составило 1, 2. Результаты показаны в таблице 3. Электронно-микроскопический снимок полученного порошка показан на фиг. 16.
Сравнительный пример 6.
Для получения порошка оксида на воздухе при 1100oC в течение одного часа обжигали смешанный порошок оксида иттрия и оксида железа, который получили в примере 17.
В соответствии с рентгеноструктурным анализом полученного порошка оксида наблюдали главным образом пики, приписываемые Y2O3 и Fe2O3, при этом наблюдали лишь маленькие пики, приписываемые YFeO3 и Y3Fe5O12. В соответствии с наблюдениями с помощью растрового электронного микроскопа было установлено, что полиэдрические частицы не образовывались, и частицы имели неправильную форму и находились в агломерированном состоянии. Результаты приведены в таблице 3. Электронно-микроскопический снимок полученного порошка показан на фиг. 17.
Пример 18.
γ-оксид железа (III) (удельная поверхность по БЭТу 34,4 м2/г) загрузили в тигель, изготовленный из оксида алюминия, и нагревали на воздухе со скоростью нагрева 300oC/ч при 1000oC в течение 3 ч, чтобы получить порошок оксида железа.
Вышеприведенный оксид железа и порошок оксида гадолиния (чистотой 99,99%, производимый Nippon Yttrium Co., Ltd.) завесили таким образом, чтобы молярное отношение гадолиния к железу составило 3:6 и смешали в изопропаноле (WAKO JUNYAKU, особо чистом) при диспергировании порошков с применением ультразвуковой волны, после чего для получения смешанного порошка оксида гадолиния и оксида железа осуществили удаление изопропанола посредством испарителя и вакуумной сушилки.
Затем смешанный порошок использовали в качестве исходного порошка и обжигали тем же самым образом, что и в примере 17, чтобы получить порошок оксида.
Полученный порошок в соответствии с рентгеноструктурным анализом был железо-гадолиниевым гранатом, представленным формулой Gd3Fe5O12, при этом другой пик не наблюдали. В соответствии с наблюдениями с помощью растрового электронного микроскопа железо-гадолиниевый гранатовый оксид состоял из полиэдрических частиц, имеющих по крайней мере 8 плоскостей.
Результаты показаны в таблице 3.
Электронно-микроскопический снимок полученного порошка показан на фиг. 18.
Сравнительный пример 7.
Смешанный порошок оксида гадолиния и оксида железа, который получили в примере 18, обжигали на воздухе при 1200oC в течение 3 ч, чтобы получить порошок оксида.
В соответствии с рентгеноструктурным анализом полученного порошка наблюдали пики, приписываемые GdFeO3, Gd2O3 и Fe2O3, при этом не наблюдали пики, приписываемые Gd3Fe5O12.
В соответствии с наблюдениями посредством растрового электронного микроскопа полиэдрические частицы не образовывались, и частицы имели неправильную форму и были в агломерированном состоянии. Результаты показаны в таблице. 3. Электронно-микроскопический снимок полученного порошка представлен на фиг. 19.
Пример 19.
Тем же самым образом, как и в примере 18, за исключением того, что вместо порошка оксида гадолиния использовали порошок оксида диспрозия (чистотой 99,99%, производимый Nippon Yttrium Co., Ltd) получили исходный порошок, который обжигали для получения порошка оксида.
Полученный порошок в соответствии с рентгеноструктурным анализом был железо-диспрозиевым гранатом, представленным формулой Dy3Fe5O12, при этом другой пик не наблюдали. В соответствии с наблюдениями с помощью растрового электронного микроскопа железо-диспрозиевый гранатовый оксид состоял из полиэдрических частиц, имеющих по крайней мере 8 плоскостей. Результаты показаны в таблице 3.
Сравнительный пример 8.
Для получения порошка оксида при 1200oC в воздухе в течение 3 ч обжигали смешанный порошок оксида диспрозия и оксида железа, который получили в примере 19.
В соответствии с рентгеноструктурным анализом полученного порошка оксида наблюдали пики, приписываемые DyFeO3, Dy2O3 и Fe2O3, при этом пик, приписываемый Dy3Fe5O12, не наблюдали. В соответствии с наблюдением с помощью растрового электронного микроскопа полиэдрические частицы не образовывались и частицы имели неправильную форму и были в агломерированном состоянии. Результаты показаны в таблице 3.
Далее будет объяснен пример и cравнительный пример для порошка твердого раствора оксида иттрия и оксида циркония.
Пример 20.
Октагидрат оксихлорида циркония (WAKO JUNYAKU, особо чистый) (39,2 г) и водный раствор нитрата иттрия (100 г/л в пересчете на оксид иттрия, чистотой 99,9%, производимый Nippon Yttrium Co., Ltd) (28,26 г) растворили в чистой воде (400 г) для получения водного раствора иттриевой соли и циркониевой соли. Для нейтрализации солей и соосаждения их к водному раствору аммиака (25 вес.% WAKO JUNYAKU, особо чистому) (500 мл) в 2-литровом химическом стакане в течение 2 ч при перемешивании добавили вышеприведенный водный раствор иттриевой соли и циркониевой соли. Осадок отфильтровывали через фильтровальную бумагу и промыли чистой водой, после чего сушили в вакууме при 100oC, чтобы получить предшественник твердого раствора оксида иттрия и оксида циркония. Когда предшественник подвергли обжигу, образовался твердый раствор оксида, состоящий из 92 мол. % оксида циркония и 8 мол.% оксида иттрия.
Порошок предшественника загрузили в платиновый сосуд. Объемная плотность этого порошка составила 15% от теоретического значения.
Затем порошок поместили в кварцевый муфель и нагревали от комнатной температуры со скоростью нагрева 300oC/ч при протекании воздуха при линейной скорости 20 мм/мин. Когда температура достигла 400oC, азот заменили на атмосферный газ, состоящий из 100 об.% хлористого водорода. Порошок обжигали при 1200oC в течение 60 мин при протекании атмосферного газа с линейной скоростью 20 мм/мин, после чего для получения порошка твердого раствора оксида иттрия и оксида циркония осуществили самопроизвольное охлаждение.
В соответствии с наблюдениями с помощью растрового электронного микроскопа порошок твердого раствора оксида иттрия и оксида циркония состоял из полиэдрических частиц, имеющих по крайней мере 8 плоскостей. Результаты приведены в таблице 3. Электронно-микроскопический снимок полученного порошка показан на фиг. 20.
Сравнительный пример 9.
Порошок предшественника твердого раствора оксида иттрия и оксида циркония, который получили в примере 20, обжигали на воздухе при 120oC в течение одного часа, чтобы получить порошок твердого раствора оксида иттрия и оксида циркония.
В соответствии с наблюдениями с помощью растрового электронного микроскопа полиэдрические частицы не образовывались, и частицы имели неправильную форму и были в агломерированном состоянии. Результаты показаны в таблице 3. Электронно-микроскопический снимок полученного порошка показан на фиг. 21.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПОРОШОК ОКСИДА МЕТАЛЛА, ПОРОШОК ОКСИДА ТИТАНА, СПОСОБ ПОЛУЧЕНИЯ ПОРОШКА ОКСИДА МЕТАЛЛА | 1994 |
|
RU2127221C1 |
| ПОРОШОК α- -ГЛИНОЗЕМА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1994 |
|
RU2118612C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРОШКА α--ОКСИДА АЛЮМИНИЯ И ПОРОШОК α--ОКСИДА АЛЮМИНИЯ | 1994 |
|
RU2136596C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРОШКА АЛЬФА-ОКИСИ АЛЮМИНИЯ (ВАРИАНТЫ) | 1994 |
|
RU2126364C1 |
| α ОКСИД АЛЮМИНИЯ | 1993 |
|
RU2107661C1 |
| α ОКСИД АЛЮМИНИЯ | 1993 |
|
RU2107662C1 |
| СПОСОБ ПОЛУЧЕНИЯ αОКСИДА АЛЮМИНИЯ (ВАРИАНТЫ) | 1993 |
|
RU2114059C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРОШКООБРАЗНОЙ АЛЬФА-ОКИСИ АЛЮМИНИЯ | 1994 |
|
RU2142413C1 |
| АЛЮМООКСИДНАЯ КОМПОЗИЦИЯ (ВАРИАНТЫ) И СПОСОБ ПОЛУЧЕНИЯ АЛЮМООКСИДНОЙ КЕРАМИКИ | 1994 |
|
RU2138461C1 |
| ПОРОШОК α-ОКСИДА АЛЮМИНИЯ | 2007 |
|
RU2441841C2 |



















Использование: конструкционные материалы. Предложен порошок комплексного оксида металла, имеющий по крайней мере два металлических элемента, который содержит полиэдрические частицы, каждая из которых имеет по крайней мере 6 плоскостей, при этом среднечисленная крупность частиц составляет от 0,1 до 500 мкм и отношение D90/D10 равно 10 или меньше, D10 и D90 представляют крупность частиц при 10 и 90%-ном аккумулировании исходя соответственно от самой маленькой крупности частиц на суммарной кривой гранулометрического состава частиц, и порошок иттрий-алюминиевого граната, содержащий полиэдрические частицы, каждая из которых имеет по крайней мере 6 плоскостей и среднечисленную крупность частиц от 20 до 500 мкм. Эти комплексные оксиды металлов содержат менее агломерированные частицы и имеют узкое распределение по крупности и однородную форму частиц. 4 с. и 42 з.п. ф-лы, 3 табл., 21 ил.
(MA)3 (MB)2 [(MC)O4]3,
в которой MA, MB и MC каждый представляет по крайней мере один металлический элемент при условии, что все MA, MB и MC не являются одним и тем же металлическим элементом.
(MA)3 (MB)2 [(MC)O4]3,
в которой MA, MB и MC каждый представляет по крайней мере один металлический элемент при условии, что все из MA, MB и MC не являются одним и тем же металлическим элементом.
Приоритет по пунктам:
11.08.94 - по пп.1 - 16, 24 - 33, 37 - 44 и 46;
12.11.93 - по пп.17 - 23;
09.11.93 - по пп.34 и 36;
11.08.93 - по п.35;
28.10.93 - по п.45.
| Способ получения алюмо-иттриевого граната | 1975 |
|
SU544614A1 |
| МОНОКРИСТАЛЛИЧЕСКИЙ ЮВЕЛИРНЫЙ МАТЕРИАЛ НА ОСНОВЕ ГАДОЛИНИЙ-ГАЛЛИЕВОГО ГРАНАТА | 1991 |
|
RU2019588C1 |
| ШИХТА ДЛЯ ПОЛУЧЕНИЯ ЮВЕЛИРНЫХ КРИСТАЛЛОВ | 1991 |
|
RU2034099C1 |
| ШИХТА ДЛЯ ВЫРАЩИВАНИЯ ФЕРРИТОВЫХ МОНОКРИСТАЛЛОВ | 0 |
|
SU391847A1 |
| Монокристаллический ювелирный матриела на основе иттрий-алюминиевого граната | 1976 |
|
SU594628A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРОШКОВ АЛЮМИНАТА ЛАНТАНА | 0 |
|
SU220968A1 |
| Способ получения соединений со структурой граната | 1977 |
|
SU683190A1 |
| US 5061473 A, 29.10.91 | |||
| Поршневое уплотнение | 1974 |
|
SU478152A1 |
| Способ окисления боковых цепей ароматических углеводородов и их производных в кислоты и альдегиды | 1921 |
|
SU58A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
1999-09-20—Публикация
1994-08-11—Подача