Изобретение относится к лекарственным средствам в форме таблеток для орального применения с замедленным /пролонгированным/ высвобождением не чувствительной к влаге, физиологически переносимой соли трамадола, которые содержат по меньшей мере один фармацевтически приемлемый матричный образователь.
Трамадол-гидрохлорид - [1RS; 2RS]-2-{/диметиламино/-метил}- 1-[3-метоксифенил] -циклогексанол-гидрохлорид - представляет собой анальгетик, который эффективен при сильных и средней силы болях. Все имеющиеся в продаже в настоящее время лекарственные формы высвобождают трамадол-гидрохлорид незамедлительно, так что эти лекарственные средства, для достижения хорошей терапевтической эффективности при длительных болях, нужно вводить пациентам 3-4 раза в день. Поэтому для пациентов означало бы облегчение, если бы можно было снизить частоту введения лекарства от 1-2-х раз в день.
Специалисту известны различные принципиальные формы осуществления пролонгированных препаратов. Так, например, в уже заявленном 19 апреля 1960 г. патенте США 3065143 раскрывается пролонгированная таблетка, которая содержит фармацевтически приемлемый гидрофильный каучук, который быстро адсорбирует воду и набухает при 37oC и его весовая доля в таблетке составляет по крайней мере одну треть. Когда таблетка находится в контакте с водной средой желудочно-кишечного тракта, то образуется гель-барьер на поверхности таблетки, который предотвращает быстрый распад таблетки и быстрое выделение биологически активного вещества и делает возможным медленный распад с высвобождением биологически активного вещества в течение промежутка времени, по меньшей мере, 4 часа. Однако, примеры показывают, что на высвобождение биологически активного вещества влияет pH-значение. Далее описывается, что для высвобождения биологически активного вещества наружный слой геля "срезается" за счет движений в желудочно-кишечном тракте, благодаря чему биологически активное вещество высвобождается из геля. Одновременно на свободной затем поверхности таблетки образуется новый слой геля. На высвобождение биологически активного вещества поэтому также влияет механическая нагрузка. Далее описывается, что скорость высвобождения зависит от весового соотношения биологически активного вещества к каучуку, а также от содержания гидрофильного каучука в таблетке.
В патенте США 4 389 393 [повторное рассмотрение свидетельства BI 4 389 393] раскрывается носитель для чувствительных к влаге биологически активных веществ, который формуют и прессуют до твердой дозировочной единицы, показывает регулярное и замедленное высвобождение биологически активного вещества после введения. Носитель состоит из одной или нескольких гидроксипропилметилцеллюлоз или из смеси из одной или нескольких гидроксипропилметилцеллюлоз и вплоть до 30 вес.% метилцеллюлозы, натрийкарбоксиметилцеллюлозы и/или другого простого эфира целлюлозы, причем, по крайней мере, одна из гидроксиметилпропилцеллюлоз имеет содержание метокси-групп 16-24 вес.%, гидроксипропокси-групп 4-32 вес. % и среднечисловой молекулярный вес, по меньшей мере, 50000. Носитель содержится в дозировочной форме в количестве вплоть до 30 вес.% или менее и воздействует так, что для высвобождения 94,4% чувствительного к влаге биологически активного вещества из дозировочной формы после введения необходимы, по крайней мере, 4 часа.
В журнале Int f. Pharm. Tech. and Prod. Mfr. 5, 1 /1984/ описываются гидрофильные матрицы, в особенности гидроксипропилметилцеллюлозы, для оральных дозировочных форм с контролируемым высвобождением биологически активного вещества. На страницах 4-6 этого документа указывается, что скорость высвобождения лекарственного вещества зависит как от вязкости, так и также от весовой доли используемого полимера. Далее, на высвобождение влияют величина и форма дозировочной единицы, тогда как практически нет никакой зависимости от процесса приготовления путем гранулирования или прямого таблетирования. В противоположность этому, различные наполнители в рецептуре оказывают сильное влияние на высвобождение биологически активного вещества. Согласно рис. 16 и 18, нерастворимые вспомогательные вещества вызывают ускорение высвобождения вплоть до полной ликвидации эффекта контролируемого высвобождения, независимо от того, могут ли эти вещества, как например, микрокристаллическая целлюлоза, набухать или эти вещества, как например, гидрофосфат кальция не могут набухать.
Из Int. f. Pharm. 40, 223 /1987/ известно, что скорость высвобождения биологически активного вещества из пролонгированной таблетки, матричным образователем которой является гидроксипропилметилцеллюлоза, зависит от весового соотношения биологически активного вещества к гидроксиметилпропилцеллюлозе. Чем больше это соотношение сдвинуто в пользу биологически активного вещества, тем выше скорость высвобождения. В препаратах, которые содержат более чем 50 вес.% наполнителя, на скорость высвобождения влияют благодаря роду используемых вспомогательных веществ. Частичная замена гидроксипропилметилцеллюлозы на наполнитель и связанное с этим уменьшение содержания гидроксипропилметилцеллюлозы в композиции приводит к повышению скорости высвобождения.
Описанные в f. Pharm. Sci. 57, 1292 /1968/ пролонгированные таблетки с матрицей при увеличении растворимых частей в гидрофильной матрице приводят к повышению скорости высвобождения.
Положенная в основу изобретения задача заключается в том, чтобы получить лекарственные средства в форме таблеток для орального применения, из которых замедленно высвобождается не чувствительная к влаге, физиологически приемлемая соль трамадола, независимо от pH-значения окружающей среды при высвобождении и независимо от рода и количества наполнителей. Далее, при заданной массе и форме таблетки профиль высвобождения должен быть независим от содержания биологически активного вещества и количества матричного образователя. Под "профилем высвобождения" понимают высвободившуюся долю биологически активного вещества в весовых процентах от общего содержания биологически активного вещества по отношению к времени исследования.
Найдено, что высоким требованиям, предъявляемым к содержащей соль трамадола пролонгированной форме, удовлетворяет содержащее не чувствительную к влаге соль трамадола лекарственное средство в форме таблеток, которое содержит выбранный, фармацевтически приемлемый матричный образователь.
Предметом изобретения, соответственно этому, являются лекарственные средства в форме таблеток с замедленным высвобождением биологически активного вещества, содержащие в качестве биологически активного вещества, по меньшей мере, одну не чувствительную к влаге, физиологически приемлемую соль трамадола и в качестве фармацевтически приемлемого матричного образователя, по меньшей мере, один простой эфир целлюлозы и/или сложный эфир целлюлозы, который в 2 вес. %-ном водном растворе при 20oC имеет вязкость 3000-150000 мПа•с.
Предпочтительно использовать в качестве фармацевтически приемлемого матричного образователя простые и/или сложные эфиры целлюлозы, которые в 2 вес. %-ном водном растворе при 20oC обладают вязкостью 10000 - 150000 мПа•с. Особенно пригодные, фармацевтически приемлемые матричные образователи выбираются из группы, включающей метилгидроксипропилцеллюлозы, гидроксиэтилцеллюлозы, гидроксипропилцеллюлозы, метилцеллюлозы, этилцеллюлозы и карбоксиметилцеллюлозы, и в особенности выбираются из группы, включающей метилгидроксипропилцеллюлозы, гидроксиэтилцеллюлозы и гидроксипропилцеллюлозы.
В предлагаемых согласно изобретению лекарственных средствах замедленно высвобождающееся количество биологически активного вещества предпочтительно составляет 10-85 вес.%, а содержание фармацевтически приемлемого матричного образователя составляет 10-40 вес.%. Особенно предпочтительны лекарственные средства с замедленно высвобождающимся количеством биологически активного вещества 25-70 вес. % и содержанием фармацевтически приемлемого матричного образователя 20-40 вес.%.
В предлагаемых согласно изобретению лекарственных средствах в качестве других составных частей могут содержаться фармацевтически обычные вспомогательные вещества, такие как наполнители, например, как лактоза, микрокристаллическая целлюлоза или гидрофосфат кальция, а также придающие скользкость вещества, смазки и средства для регулирования текучести, например, как высокодисперсный диоксид кремния, тальк, стеарат магния и/или стеариновая кислота, общее содержание которых в таблетке составляет 0-80 вес.%, предпочтительно 5-65 вес.%.
Часто скорость высвобождения биологически активного вещества в лекарственном средстве зависит от pH-значения. Оно во время прохождения лекарственного средства в желудочно-кишечном тракте может колебаться в пределах pH-значений от ниже 1 до примерно 8. Эти колебания могут быть различными от одного, принимающего лекарство, субъекта к другому. Также, в случае одного и того же субъекта от одного приема лекарства к другому может быть задан различный профиль pH-значение - время во время прохождения в желудочно-кишечном тракте. Если скорость высвобождения биологически активного вещества из лекарственного средства зависит от pH-значения, то это может приводить ин виво к различным скоростям высвобождения. Профили высвобождения соли трамадола из предлагаемого согласно изобретению лекарственного средства, однако, неожиданно оказались независимыми от pH-значения, которое может наступать физиологически во время прохождения желудочно-кишечного тракта. Профили высвобождения при pH-значении окружающей среды 1,2; 4,0 и 6,8 являются как идентичными друг по отношению к другу, так и также по сравнению с высвобождением во время профиля pH-значение-время могут иметь от pH 1,2, через pH 2,3 и pH 6,8 вплоть до pH 7,2.
В противоположность вышеуказанному уровню техники, скорость высвобождения соли трамадола из предлагаемого согласно изобретению лекарственного средства независима как от составляющей в 2 вес.%-ном растворе 3000 - 150000 мПа•с вязкости матричного образователя, так и также независима от содержания матричного образователя, а также от наполнителя в лекарственном средстве.
Далее для профиля высвобождения содержащей предлагаемую согласно изобретению соль трамадола пролонгированной таблетки несущественно, используется ли, при прочных неизмененных величинах и неизменном составе, в расчете на биологически активное вещество, матричный образователь и необязательные составные части, как наполнитель, водорастворимый наполнитель, как например, лактоза, нерастворимый, не набухающий в водной среде наполнитель, например, как гидрофосфат кальция или нерастворимый, набухающий в водной среде наполнитель, например, микрокристаллическая целлюлоза. Все такого рода лекарственные средства имеют удовлетворительные /конгруэнтные/ профили высвобождения.
Так как, в частности, трамадол-гидрохлорид хорошо растворим в водной среде и на основании уровня техники доля растворимых составных частей в лекарственной композиции оказывает влияние на скорость высвобождения, препараты с различным содержанием соли трамадола должны иметь разные профили высвобождения. Также на основании уровня техники изменение соотношения соли трамадола к матричному образователю приводит к изменению профиля высвобождения. Неожиданно, однако, оказалось, что предлагаемые согласно изобретению лекарственные средства с различным содержанием биологически активного вещества, в которых общее количество не чувствительной к влаге, физиологически приемлемой соли трамадола и растворимого или нерастворимого наполнителя поддерживается постоянным, при прочих неизмененных величинах, неизмененном общем весе и неизмененном составе таблетки, в расчете на матричный образователь и необязательные вспомогательные вещества, обладают идентичными профилями высвобождения.
Предлагаемые согласно изобретению лекарственные средства могут находиться как в виде простой таблетки, как и также в виде покрытой покрытием таблетки, например, в виде таблетки в пленке или драже. Для таблеток с покрытием можно применять один или несколько слоев покрытия. В качестве материала для покрытия пригодны известные метилгидроксипропилцеллюлозы, которые только незначительно влияют на профиль высвобождения предлагаемых согласно изобретению лекарственных средств. Известные специалисту диффузионные покрытия, например, на основе набухаемых, однако, водонерастворимых поли/мет/акрилатов, приводят к очень сильно заторможенным высвобождениям биологически активного вещества из предлагаемых согласно изобретению лекарственных средств. Содержащее биологически активное вещество, замедленно высвобождающее его ядро таблетки с содержанием биологически активного вещества предпочтительно 10-85 вес. %, особенно предпочтительно 25-70 вес.%, может быть покрыто дополнительным биологически активным веществом, которое не высвобождается замедленно в виде начальной дозы, с помощью различных, известных специалисту способов, например, как дражирование, нанесение путем опрыскивания из растворов или суспензий или за счет способа нанесения порошка. Другие формы осуществления представляют собой многослойные и в оболочке таблетки, в случае которых замедленно высвобождается, по меньшей мере, соль трамадола в одном или нескольких слоях многослойной таблетки с содержанием биологически активного вещества предпочтительно 10-85 вес.%, особенно предпочтительно 25-70 вес. %, соответственно, в ядре таблетки в оболочке с содержанием биологически активного вещества предпочтительно 10-85 вес.%, особенно предпочтительно 25-70 вес.%, за счет фармацевтически приемлемого матричного образователя; и высвобождение соли трамадола в одном или нескольких слоях многослойной таблетки, соответственно, во внешнем слое оболочки покрытой оболочкой таблетки происходит незамедленно. Многослойные таблетки и таблетки в оболочке могут содержать одно или несколько не содержащих биологически активного вещества покрытий.
Получение предлагаемых согласно изобретению лекарственных средств отличается высокой воспроизводимостью относящихся к высвобождению свойств получаемых, содержащих соль трамадола композиций. В течение времени хранения, по меньшей мере, год не происходит никакого изменения профиля высвобождения предлагаемых согласно изобретению лекарственных средств.
При ежедневном одноразовом или двухразовом приеме предлагаемой согласно изобретению таблетки пациентами достигается хорошая терапевтическая эффективность при длительных сильных болях.
Примеры
Пример 1
Содержащие матрицу таблетки следующего состава на таблетку:
Трамадол-гидрохлорид - 100 мг
Метилгидроксипропилцеллюлоза, тип 2208, 100000 мПа•с {изготовитель DOW Chemical Company, Midland /США/} - 85 мг
Гидрофосфат кальция - 62 мг
Высокодисперсный диоксид кремния - 5 мг
Стеарат магния - 3 мг
При количестве исходной смеси 200 г получают следующим образом:
Все составные части просеивают через сито с размером отверстий 0,63 мм, в Kubus - смесителе смешивают в течение 10 минут и на эксцентриковом прессе для таблеток Korsch EK O прессуют в таблетки диаметром 9 мм, с радиусом выпуклости 8,5 мм и средним весом 255 мг.
Таким же образом получают содержащие матрицу таблетки весом 255 мг на таблетку и следующего состава на таблетку:
Трамадол-гидрохлорид - 150 мг
Метилгидроксипропилцеллюлоза, тип 2208, 100000 мПа•с - 85 мг
Гидрофосфат кальция - 12 мг
Высокодисперсный диоксид кремния - 5 мг
Стеарат магния - 3 мг
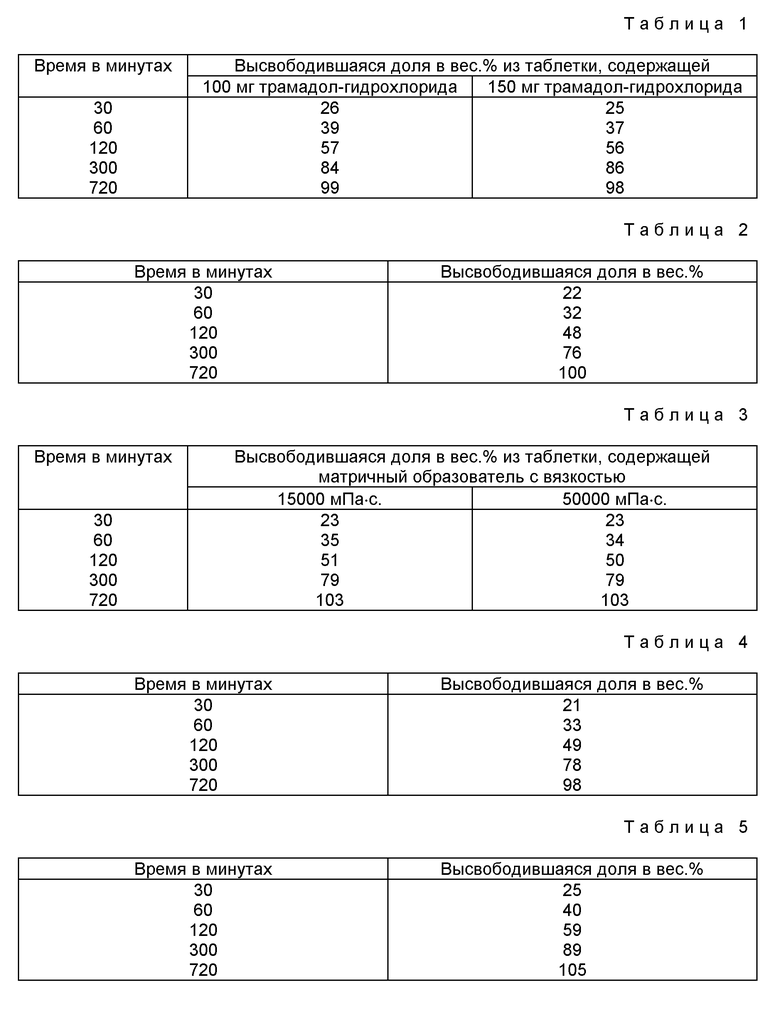
Ин витро-высвобождение трамадол-гидрохлорида из лекарственных композиций определяют согласно DAB 10 в аппаратуре с пластинчатой мешалкой. Температура среды раствора составляет 37oC и скорость вращения мешалки составляет 75 оборотов в минуту. В начале исследования каждую таблетку помещают в, смотря по обстоятельствам, 600 мл искусственного желудочного сока с pH-значением = 1,2. Спустя 30 минут путем добавки раствора гидроксида натрия pH-значение повышают до 2,3, спустя следующие 90 минут его повышают до 6,5 и спустя еще раз 60 следующих минут pH-значение повышают до 7,2. Находящееся в вышеуказанные моменты времени в растворе высвобожденное количество биологически активного вещества определяют спектрофотометрически. Определяют величины высвобождения /средние значения из "n" = 3/ (см. табл. 1 в конце описания).
Кривые ин витро-высвобождения из таблеток, содержащих 100 мг или 150 мг трамадол-гидрохлорида, представлены на фиг. 1.
Пример 2.
Содержащие матрицу таблетки следующего состава на таблетку:
Трамадол-гидрохлорид - 200 мг
Метилгидроксипропилцеллюлоза, тип 2208, 100000 мПа•с /изготовитель: Shin Etsu, Токио, Япония/ - 105 мг
Гидрофосфат кальция - 36 мг
Высокодисперный диоксид кремния - 5 мг
Стеарат магния - 4 мг
при количестве исходной смеси 525 г получают следующим образом:
Трамадол-гидрохлорид, метилгидроксипропилцеллюлозу, гидрофосфат кальция, а также по 50% общего количества диоксида кремния и стеарата магния пропускают через сито с размером отверстий 0,5 мм и смешивают в Kubus - смесителе в течение 10 минут. Полученную смесь на эксцентриковом прессе для таблеток Korsch EK O уплотняют до прессованных изделий диаметром 20 мм.
После дробления полученных прессованных изделий с помощью одномиллиметрового сита примешивают остаточные количества диоксидов кремния и стеарата магния. После этого полученную смесь прессуют на эксцентриковом прессе для таблеток Korsch EK O в таблетки диаметром 10 мм, радиусом выпуклости 8 мм и средним весом 350 мг.
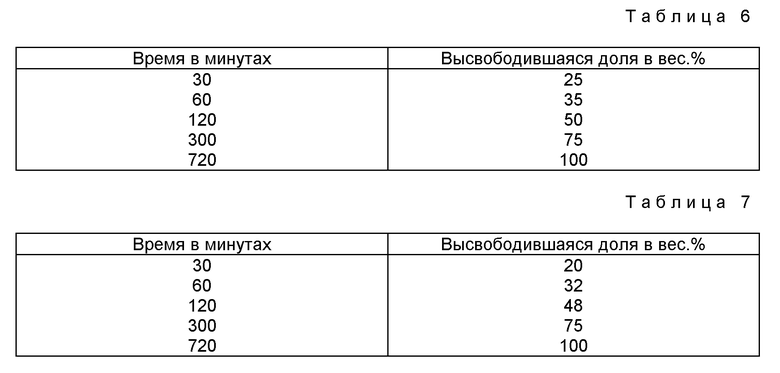
Высвобождение ин витро биологически активного вещества исследуют согласно примеру 1. Получают величины высвобождения /средние значения из "п" = 2/ (см. табл. 2 в конце описания).
Пример 3
Полученные согласно примеру 2 таблетки покрывают с помощью вурстерспособа лаковой суспензией следующего состава:
Eudragit RL 30D /изготовитель Роп, Дармштадт/ - 18,2 вес.%
Тальк - 8,2 вес.%
Диоксид титана - 6,5 вес.%
Полиэтиленгликоль 6000 /изготовитель: Хехст АГ, Франкфурт/ - 1,6 вес.%
Триэтилцитрат - 1,1 вес.%
Деминерализованная вода - 64,4 вес.%
Средний вес используемых ядер таблеток за счет нанесения лака повышается на 20 мг. Ин-витро - высвобождение биологически активного вещества из таблетки в пленке исследуют согласно примеру 1. Получают следующие величины высвобождения /средние значения из "п" = 2/:
30 - 10
60 - 22
120 - 39
300 - 69
720 - 96
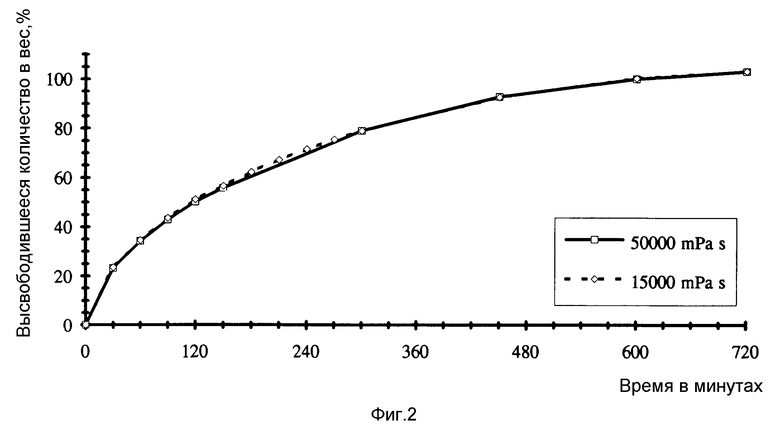
Как описано в примере 2, получают таблетки со средним весом 350 мг, в которых, однако, гидрофосфат кальция заменен на 36 мг микрокристаллической целлюлозы pH 101 /изготовитель: FMC, Филадельфия, США/, метилгидроксипропилцеллюлоза заменена либо на 105 мг метилгидроксипропилцеллюлоза типа 2208 с вязкостью 15000 мПа•с /изготовитель: Shin Etsu/ либо на 105 мг метилгидроксипропилцеллюлозы типа 2208 с вязкостью 50000 мПа•с /изготовитель: Shin Etsu/. Ин-витро-высвобождения биологически активного вещества исследуют согласно примеру 1. Получают величины высвобождения /средние значения из "п" = 3/: (см. табл. 3 в конце описания).
Кривые ин-витро-высвобождения из композиций таблеток, которые содержат метилгидроксипропилцеллюлозы с вязкостью 15000 мПа•с или метилгидроксипропилцеллюлозу с вязкостью 50000 мПа•с, представлены на фиг.2.
Пример 5
Как описано в примере 2, получают таблетки со средним весом 350 мг и следующего состава на таблетку:
Трамадол-гидрохлорид - 200 мг
Метилгидроксипропилцеллюлоза, тип 2208, 50000 мПа•с /изготовитель: Slin Etsu/ - 50 мг
Микрокристаллическая целлюлоза pH 101 - 91 мг
Высокодисперсный диоксид кремния - 5 мг
Стеарат магния - 4 мг
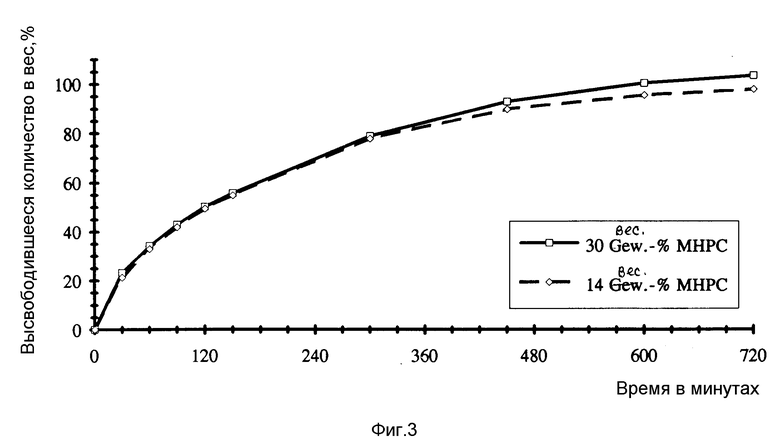
Ин-витро-высвобождение биологически активного вещества исследуют согласно примеру 1, причем получают величины высвобождения /средние значения из "п" = 3/ (см. табл. 4 в конце описания).
Кривые высвобождения ин витро из таблеток, которые содержат либо 50 мг, соответственно, 14 вес.%, либо 105 мг, соответственно, 30 вес.% [см. пример 4] метилгидроксипропилцеллюлозы с вязкостью 50000 мП•с, представлены на фиг. 3.
Пример 6
Содержащие матрицу таблетки следующего состава на таблетку:
Трамадол-гидрохлорид - 100 мг
Метилгидроксипропилцеллюлоза, тип 2910, 10000 мПа•с /изготовитель: DOW Chemical Company/ - 40 мг
Микрокристаллическая целлюлоза pH 101 - 26 мг
Высокодисперсный диоксид кремния - 2 мг
Стеарат магния - 2 мг
При количестве исходной смеси 510 г получают согласно примеру 2. Полученные таблетки имеют диаметр 8 мм, радиус выпуклости 7,5 мм и средний вес 170 мг.
Высвобождение ин витро биологически активного вещества исследуют согласно примеру 1. Получают величины высвобождения /средние значения из "п" = 2/ (см. табл. 5 в конце описания).
Пример 7
Содержащие матрицу таблетки следующего состава на таблетку:
Трамадол-гидрохлорид - 150 мг
Гидроксипропилцеллюлоза, 30000 мПа•с /Klucel R HXF (не rcules, Дюссельдорф) - 105 мг
Микрокристаллическая целлюлоза pH 101 - 86 мг
Высокодисперсный диоксид кремния - 5 мг
Стеарат магния - 4 мг
при количестве исходной смеси 350 г получают согласно примеру 2. Исследование ин витро-высвобождения согласно примеру 1 дает значения /средние значения из "п" = 2/ (см. табл. 6 в конце описания).
Пример 8
Содержащие матрицу таблетки следующего состава на таблетку:
Трамадол-гидрохлорид - 150 мг
Гидроксиэтилцеллюлоза, 100000 мПа•с [NatrosolR HHX] [Не rcules, Дюссельдорф] - 105 мг
Микрокристаллическая целлюлоза pH 101 - 86 мг
Высокодисперсный диоксид кремния - 5 мг
Стеарат магния - 4 мг
При количестве исходной смеси 350 г получают согласно примеру 2. Исследование высвобождения ин витро согласно примеру 1 дает значения /средние значения из "п" = 2/ (см. табл. 7 в конце описания).
Изобретение относится к медицине. Лекарственное средство в форме таблеток для орального применения обеспечивает замедленное высвобождение активнодействующего вещества. В качестве активнодействующего вещества средство содержит не чувствительную к влаге фармацевтически приемлемую соль трамадола в количестве 10-85 маc.%. Средство также содержит обычные для таблетированной формы вспомогательные добавки и в качестве фармацевтически приемлемого матричного образователя - по меньшей мере один простой и/или сложный эфир целлюлозы с вязкостью в 2 мас.%-ном водном растворе при 20°С 3000-150000 МПа•с в количестве 10-40 маc.%. Новое лекарственное средство высвобождает соль трамадола независимо от pH-значения окружающей среды, от рода и количества наполнителей. При заданной массе и форме таблетки профиль высвобождения соли трамадола не зависит от содержания биологически активного вещества и количества матричного образователя. 4 з.п.ф-лы, 3 ил., 7 табл.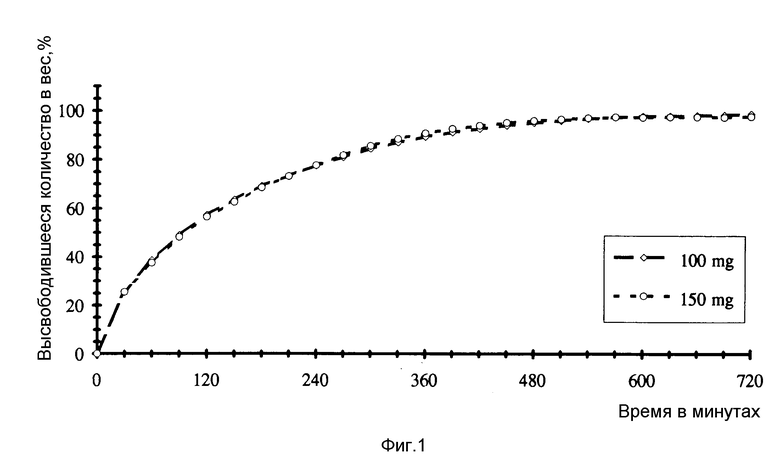
| US 4389393 A, 21.06.83 | |||
| RU 95105449 A1, 10.06.97. |
Авторы
Даты
1999-09-27—Публикация
1994-09-01—Подача