Изобретение касается способа каталитического обессеривания газа, содержащего серосодержащие соединения H2S и SO2 и, возможно, COS и/или CS2, c выделением вышеупомянутых соединений в форме серы. Оно относится также к катализатору для осуществления этого способа.
Известно, что H2S реагирует с SO2 в присутствии катализаторов, например, на основе одного или нескольких оксидов металлов, таких как оксид алюминия или оксид титана, с образованием серы по реакции Клауса, которая записывается: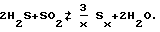
Многочисленные способы обессеривания газа, содержащего H2S и SO2, используют реакцию Клауса в контакте с катализатором с целью выделения вышеупомянутых соединений H2S и SO2 в форме серы.
В таких способах обессериваемый газ, содержащий H2S и SO2, контактируют с катализатором-промотором реакции Клауса, осуществляя этот контакт либо при температурах выше точки росы серы, образующейся в реакционных газах, в этом случае образующаяся сера присутствует в реакционной среде в парообразном состоянии, или же при температурах, ниже точки росы образующейся серы, в этом случае вышеупомянутая сера осаждается на катализаторе, что заставляет периодически регенерировать катализатор, загрязненный серой, путем продувки неокисляющего газа, имеющего температуру в интервале от 200 до 500oC.
В частности, реакция между H2S и SO2 при температурах выше точки росы серы, то есть при температурах выше 180oC, может быть реализована при контактировании с катализатором, состоящим из оксида алюминия или боксита (американская заявка на патент 2403451); из оксида алюминия, связанного с соединением цинка, кадмия, кальция или магния (французская заявка на патент 2126257); из активированного оксида алюминия, связанного с оксидным соединением или с сульфатом кобальта, никеля, железа или урана (французская заявка на патент 2190517); из оксида алюминия, связанного с соединением титана (французская заявка на патент 2224203); оксида алюминия, связанного с соединением иттрия, лантана или элемента семейства лантанидов с атомным номером от 58 до 71 (французская заявка на патент 2242144); оксида титана (французская заявка на патент 2481145) или из оксида титана, связанного с сульфатом щелочноземельного металла (европейская заявка на патент 0060741). Катализаторы, описанные в французских заявках на патенты 2126257, 2190517, 2224203, 2481145 и в европейской заявке на патент 0060741, особенно интересны в случаях, когда обрабатываемый газ, помимо серосодержащих соединений H2S и SO2, содержит также органические соединения серы, такие как COS и/или CS2.
Что касается реакции между H2S и SO2, которую проводят при таких температурах, что образующаяся сера осаждается на катализаторе, то она может быть осуществлена при контакте с катализатором, состоящим, например, из активированного оксида алюминия, оксида кремния, смеси оксида кремния и оксида алюминия, или природного или синтетического цеолита (французские заявки на патенты 2180473 и 2224196), оксида алюминия, связанного с соединением железа, никеля, кобальта, меди или цинка (французская заявка на патент 2327960), оксида алюминия, связанного с соединением титана, иттрия, лантана или лантанида с атомным номером от 58 до 71 (международная заявка на патент 9112201), оксида алюминия, связанного с соединением никеля, железа или кобальта (европейские заявки на патенты 0215317 и 0218302) или из активированного угля (французская заявка на патент 1603452).
Вышеуказанные катализаторы, которые промотируют реакцию Клауса с образованием серы между H2S и SO2 и, возможно, гидролиз соединений COS и CS2 до H2S, при продолжительном использовании обнаруживают ряд недостатков. Под комбинированным воздействием температуры и воды катализатора на основе оксида алюминия, оксида кремния, оксида титана или активированного угля подвергаются со временем превращениям, которые выражаются в уменьшении удельной поверхности и пористости вышеупомянутых катализаторов и вызывают потерю их каталитической активности. Кроме того, катализаторы на основе оксида алюминия способны изменяться с течением времени в результате сульфатации, что является дополнительной причиной потери каталитической активности. Что касается катализаторов на основе активированного угля, то при их использовании должны быть приняты меры предосторожности, чтобы избежать сгорания активированного угля. С другой стороны, когда в обрабатываемых газах присутствуют углеводороды, вышеупомянутые катализаторы на основе оксида алюминия, оксида кремния, оксида титана или активированного угля подвергаются отравлению в результате осаждения углерода и углеводородов в их матрицу. Катализаторы, отравленные таким образом, не могут быть регенерированы вследствие физико-химического разложения, к которому могло бы привести применение повышенных температур, необходимых для реактивации этих катализаторов, например, путем прямого окисления углеводородных веществ катализатора. Кроме того, в катализаторах, содержащих каталитическую фазу, способную промотировать реакцию Клауса, и соединенную с носителем, вышеупомянутая каталитическая фаза имеет тенденцию проникать в решетку носителя, что сопровождается потерей каталитической активности и делает трудным и даже зачастую невозможным извлечение каталитической фазы из использованного катализатора. Наконец, вышеупомянутые катализаторы имеют посредственную теплопроводность, что ограничивает перенос тепла от гранул катализатора к газовой фазе. Это приводит к подъему температуры внутри гранул катализатора, который лимитирует протекание реакций.
Задача изобретения состоит в устранении недостатков катализатора Клауса, используемого для осуществления реакций между H2S и SO2 с образованием серы. С этой целью заявителем разработан способ обессеривания газов с улучшенной селективностью по сере, и катализатор для его осуществления, способный промотировать реакцию Клауса между H2S и SO2 и, возможно, гидролиз соединений COS и CS2 до H2S.
Таким образом, объектом изобретения является способ каталитического обессеривания газа, содержащего серосодержащие соединения H2S и SO2, с выделением вышеупомянутых соединений в форме серы, в котором обессериваемый газ контактируют с катализатором Клауса, состоящим из каталитической фазы, способной осуществлять реакцию Клауса между H2S и SO2, связанной с носителем; вышеупомянутый способ отличается тем, что носитель катализатора Клауса состоит из карбида кремния.
Обессериваемый газ, который контактирует с катализатором Клауса, согласно изобретению содержит H2S и SO2 в общей концентрации, составляющей обычно 0,01 - 25 об.%, предпочтительно, между 0,02 и 15 об.%. В вышеупомянутом газе наиболее предпочтительное молярное отношение H2S : SO2 равно 2 : 1, которое соответствует стехиометрическому соотношению реакции Клауса, и может изменяться от 0,2 : 1 до 4 : 1 или более.
Обессериваемый газ, который обрабатывают согласно изобретению, может иметь различное происхождение. В частности, этот газ может быть получен в результате мягкого сжигания, в соответствии со стехиометрией реакции Клауса, кислого газа, содержащего H2S. Он может также состоять из остаточного газа серного завода, производящего серу по процессу Клауса. Обессериваемый газ может также получаться в результате добавления требуемого количества SO2 к кислому газу, содержащему небольшое количество H2S, поступающему например, после газификации угля или тяжелых масел, или, может быть получен добавлением соответствующего количества H2S к газу, содержащему небольшое количество SO2; добавление SO2 к кислому газу, содержащему H2S, или добавление H2S к газу, содержащему SO2, может быть осуществлено во время контактирования с промотирующим катализатором реакции Клауса или, предпочтительно, перед этим контактированием. Обессериваемый газ может также содержать органические соединения серы, например COS и/или CS2, общая концентрация которых в большинстве случаев не превышает 4% от объема обессериваемого газа, но в известных случаях может превышать эту величину.
В катализаторе Клауса согласно изобретению каталитическая фаза, которая связана с носителем из карбида кремния, содержит по меньшей мере один металл, способный в форме оксида или соли или/и в элементном состоянии осуществлять реакцию Клауса образования серы между H2S и SO2. Когда обессериваемый газ содержит одно или несколько органических соединений серы, таких как COS и/или CS2, помимо соединений H2S и SO2, то активная фаза катализатора содержит также по меньшей мере один металл, способный в определенном интервале температур промотировать гидролиз вышеупомянутых органических соединений серы до H2S; вышеупомянутый металл в форме оксида или соли или/и элементном состоянии одновременно может быть способен осуществлять реакцию Клауса между H2S и SO2. Особенно, активная фаза катализатора на носителе из карбида кремния содержит по меньшей мере один металл, выбранный среди титана, циркония, иттрия, лантана, урана, свинца, молибдена, железа, кобальта, никеля, кальция, цинка, магния, кадмия, лантанидов с атомным номером в интервале от 58 до 71 и, например, неодима, празеодима, самария или гадолиния; такой металл в форме оксида или соли или/и элементном состоянии способен осуществлять реакцию Клауса между H2S и SO2 и одновременно, в определенном интервале температур, гидролиз органических соединений серы, таких как COS и/или CS2, до H2S. Каталитическая фаза или активная фаза, связанная с носителем из карбида кремния, в катализаторе согласно изобретению, в расчете на массу металла, наиболее часто составляет 0,1 - 20%, в особенности 0,2 - 15% и, преимущественно, 0,2 - 10% от общей массы вышеупомянутого катализатора. Носитель из карбида кремния преимущественно составляет, по меньшей мере 40% и, особенно, по меньшей мере 50% от массы катализатора.
Удельная поверхность катализатора согласно изобретению может изменяться в достаточно широких пределах в зависимости от условий осуществления способа обессеривания. Преимущественно вышеупомянутая удельная поверхность, определенная методом БЭТ по адсорбции азота, может быть равна 2 - 600 м2/г.
Катализатор Клауса согласно изобретению может быть получен с использованием различных известных методов введения одного или нескольких металлических соединений в твердое вещество, представляющее собой носитель катализатора. В частности, можно произвести пропитку носителя из карбида кремния, находящегося в виде порошка, таблеток, гранул, экструдированных изделий, сотовых монолитов или агломератов других форм, посредством раствора или золя одного или нескольких желанных металлических соединений в растворителе, таком как вода, затем высушить пропитанный носитель и прокалить высушенный продукт при температурах в интервале от 250 до 500oC, действуя в инертной или неинертной атмосфере. Прокаленный катализатор может быть подвергнут восстановительной обработке водородом, например, при температуре между 200 и 500oC чтобы перевести в элементное состояние металл металлического соединения, присутствующего в активной фазе. Можно также иметь в виду получение катализатора используя метод внедрения каталитически активных атомов металлов, упомянутых выше, в кристаллическую решетку карбида кремния. Это внедрение активных веществ может быть осуществлено либо во время получения карбида кремния, либо во время последующей стадии.
Карбид кремния, используемый для создания носителя для катализатора Клауса согласно изобретению, может представлять собой любой из известных карбидов кремния, при условии, что он имеет требуемые характеристики удельной поверхности, а именно, удельную поверхность, определенную методом БЭТ по адсорбции азота, в интервале, например, от 2 до 600 м2/г.
Вышеупомянутый карбид кремния может быть получен в частности, по любому из способов, описанных в европейских заявках на патенты 0313480 (соответствует американской заявке на патент 4914070, 0440569, 0511919, 0543751 и 0543752.
Катализатор может иметь гранулометрию, заключенную в интервале между 0,3 и 15 мм и, преимущественно, между 0,5 и 10 мм.
Времена контакта газообразной реакционной среды, состоящей из обессериваемого газа, с катализатором согласно изобретению, могут изменяться от 0,2 до 20 секунд и, предпочтительно, от 0,4 до 12 секунд; эти величины даны для нормальных условий давления и температуры (время контакта ТДН).
Способ обессеривания согласно изобретению может быть осуществлен при температурах выше точки росы серы, образующейся во время реакции между H2S и SO2, вышеупомянутая сера в таком случае находится в реакционной среде, которая выходит из зоны каталитической реакции, в форме паров и может быть выделена из вышеупомянутой реакционной среды путем конденсации. Можно также осуществить способ обессеривания согласно изобретению, действуя при температурах ниже точки росы серы, образующейся во время реакции между H2S и SО2, в таком случае вышеупомянутая сера осаждается на катализаторе и газообразный эфлюент, получаемый на выходе из зоны, каталитической реакции, по существу, не содержит серы. Предпочитают выбирать температуру осуществления способа в интервале между 30 и 500oC. Для осуществления способа при температурах выше точки росы серы, образующейся в реакционных газах, выбирают из температуры, заключенные между 180 и 500oC и, преимущественно, между 190 и 400oC. Для осуществления способа при температурах ниже точки росы образующейся серы, выбирают температуры в интервале от 30 до 180oC и, особенно, в интервале от 80 до 160oC, который охватывает область отверждения серы в окрестности 120oC.
Когда способ согласно изобретению осуществляют при температурах, заключенных между 180 и 500oC и, в особенности, между 190 и 400oC, контактирование обессериваемого газа, содержащего H2S и SO2, с катализатором Клауса на носителе из карбида кремния может быть осуществлено в одной или нескольких каталитических реакционных зонах, содержащих вышеупомянутый катализатор. Число каталитических реакционных зон зависит, среди прочих факторов, от состава обессериваемого газа и от результата, который стремятся получить. Когда прибегают к нескольким каталитическим реакционным зонам, вышеупомянутые зоны, преимущественно расположены последовательно. Катализатор, находящийся в единственной каталитической реакционной зоне, может полностью представлять собой катализатор Клауса согласно изобретению на носителе из карбида кремния или, может быть образован из слоя такого катализатора, связанного с одним или несколькими слоями обычного катализатора Клауса, такого как, например, боксит, оксид алюминия, цеолит, оксид титана или оксид циркония. Когда реакцию проводят в нескольких каталитических реакционных зонах, которые, как было указано выше, преимущественно расположены последовательно, по меньшей мере одна из вышеупомянутых каталитических реакционных зон содержит катализатор Клауса согласно изобретению на носителе из карбида кремния, в то время как другие каталитические реакционные зоны содержат один или несколько обычных катализаторов Клауса, таких, например, которые указаны выше. В одной или нескольких каталитических реакционных зонах, содержащих катализатор Клауса согласно изобретению на носителе из карбида кремния, вышеупомянутый катализатор может полностью занимать каталитический слой в данной каталитической реакционной зоне или образовывать собой только один слой вышеупомянутого каталитического слоя, а остальная часть может состоять из одного или нескольких слоев обычных катализаторов Клауса, таких, например, которые назывались выше. Единственная каталитическая реакционная зона или каждая каталитическая реакционная зона, когда используют несколько таких зон, действует при температурах, заключенных в вышеупомянутых интервалах, а именно между 180 и 500oC и, в особенности, между 190 и 400oC. Когда обессериваемый газ содержит также органические соединения серы, например COS и/или CS2, в общей концентрации, не превышающей 4 об.% и от объема обессериваемого газа, одна каталитическая реакционная зона или по меньшей мере одна из каталитических реакционных зон содержит катализатор Клауса согласно изобретению на носителе из карбида кремния, способный промотировать реакцию Клауса между H2S и SO2 и гидролиз органических соединений серы до H2S, при этом каталитическая фаза вышеупомянутого катализатора содержит промотор или сама является промотором гидролиза вышеупомянутых органических соединений серы, катализатор согласно изобретению на носителе из карбида кремния, активная фаза которого содержит оксид по меньшей мере одного металла, такого как Ti, Zr, Zn, Cd, Ca, Mg, Mo, или La, причем каждая каталитическая реакционная зона, содержащая такой катализатор согласно изобретению, работает при температурах, заключенных между 180 и 500oC и достаточных для осуществления гидролиза органических соединений серы до H2S. В каждой каталитической реакционной зоне, содержащей промотирущий катализатор реакции между H2S и SO2 и гидролиз органических соединений серы до H2S, вышеупомянутый катализатор может занимать собой весь каталитический слой рассматриваемой каталитической реакционной зоны или образовывать только один слой вышеупомянутого каталитического слоя, а остальная часть может состоять из одного или нескольких слоев обычных катализаторов Клауса, таких, например, которые назывались перед этим.
На выходе из одной каталитической реакционной зоны или из каждой из каталитических реакционных зон, когда используют несколько таких зон, получают газообразный эфлюент, содержащий пары серы, который перед каждой последующей реакцией Клауса, направляют в зону охлаждения с целью выделения большей части серы, которую он содержит, путем конденсации.
При необходимости, газообразный эфлюент, который получают на выходе из одной каталитической реакционной зоны или на выходе из последней каталитической реакционной зоны, если последовательно используют несколько каталитических реакционных зон, и при осуществлении реакции при температурах выше точки росы, образующейся серы, то после выделения серы, которую он в известных случаях содержит, эффлюент может быть подвергнут дополнительной обработке с целью очистки; вышеупомянутая обработка зависит от природы и количества газообразных серосодержащих соединений, оставшихся в газообразном эфлюенте.
Осуществление способа согласно изобретению при температурах выше точки росы образующейся серы может представлять собой, в частности, стадию реакции Клауса при температурах выше точки росы серы, используемой в каталитических способах получения серы из газа, содержащего H2S, типа тех, которые описаны в французских заявках на патенты 2511663 и 2540092.
Когда способ согласно изобретению осуществляют при температурах ниже точки росы серы, образующейся в ходе реакции между H2S и S2O, то есть при температурах в интервале от 30 до 180oC и, особенно, в интервале от 80 до 160oC, контактирование обессериваемого газа, который в этой форме осуществления имеет общее содержание H2S и SO2, обычно, не более 5 об.% и, в особенности, не более 2,5 об.%, с катализатором Клауса на носителе из карбида кремния, приводит к образованию серы, которая осаждается на катализатор.
Если общая концентрация H2S и SO2 или/и температура обессериваемого газа, приводимого в контакт с катализатором обессеривания согласно изобретению таковы, что из-за экзотермичности реакции Клауса температура реакционной среды в результате способна превысить предельную температуру, выше которой степень конверсии в серу имеет тенденцию к уменьшению, тепло, выделяющееся в ходе вышеупомянутой реакции, отводят, подвергая катализатор охлаждению любым известным способом. Например, это охлаждение можно осуществить при помощи холодной жидкости, циркулирующей в системе косвенного теплообмена с каталитической массой. Можно также действовать, помещая катализатор в трубчатый реактор, состоящий из труб, расположенных в паровой камере, при этом либо катализатор находится в трубах, а холодная жидкость циркулирует между трубами паровой камеры, или холодная жидкость циркулирует в трубах, а катализатор находится между трубами паровой камеры. Можно также осуществлять каталитическую реакцию в реакторе с несколькими ярусами катализатора с охлаждением реакционной среды между последовательными каталитическими ярусами за счет косвенного теплообмена с холодной жидкостью, который имеет место внутри или вне каталитического реактора.
Если обессериваемый газ содержит значительное количество воды, например, более 10 об. %, помимо серосодержащих соединений H2S и SO2, то температуры реакции ниже точки росы образующейся серы выбирают, предпочтительно, такие, чтобы остаться выше точки росы воды, содержащейся в обессериваемом газе.
Если обессериваемый газ помимо серосодержащих соединений H2S и SO2, содержит органические соединения серы, например, COS и/или CS2, то в общей концентрации, не превышающей 4 об.% обессериваемого газа, вышеупомянутый газ, перед контактированием с катализатором на носителе из карбида кремния, действующим при температурах в интервале от 30 до 180oC, преимущественно подвергают стадии каталитического гидролиза. Эта стадия гидролиза может быть осуществлена путем контактирования обессериваемого газа, содержащего органические соединения серы, с катализатором гидролиза вышеупомянутых органических соединений серы до H2S. Вышеупомянутый газ, содержащий воду в количестве, достаточном для этого гидролиза, вводят в контакт с катализатором гидролиза при температурах, заключенных между 180 и 500oC и достаточных для того, чтобы проходил гидролиз. Катализатор гидролиза состоит из катализатора Клауса на носителе из карбида кремния, он способен промотировать гидролиз органических соединений серы в H2S и, особенно, из такого катализатора, активной фазой которого является оксид Ti, Zr, Zn, Cd, Ca, Mg, Mo или La. Использование, согласно изобретению, гидролиза с последующей реакцией Клауса между H2S и SO2 при температурах ниже точки росы образующейся серы, может быть реализовано, например, как указано в французских заявках на патенты 2632626 и 2653422.
Во время протекания реакции между H2S и SO2 при температурах ниже точки росы образующейся серы, катализатор Клауса постепенно загрязняется серой. Периодически проводят регенерацию катализатора, загрязненного серой, путем продувки вышеупомянутого катализатора при помощи газа при температурах, заключенных между 200 и 500oC и, предпочтительно, между 250 и 450oC, чтобы испарить серу, оставшуюся на катализаторе. Затем регенерированный катализатор охлаждают до температуры ниже точки росы серы, чтобы вновь использовать его для проведения реакции между H2S и SO2. Это охлаждение осуществляют посредством газа, имеющего соответствующую температуру ниже 180oC.
Газ для продувки, используемый для регенерации катализатора, загрязненного серой, может быть таким, как метан, азот, CO2 или их смесь, или представлять собой часть газового потока, выходящего с низкотемпературной стадии, реакции Клауса, или часть обессериваемого газа или обессеренного газа. Продуваемый газ, используемый для вышеупомянутой регенерации, может, в известных случаях, содержать некоторое количество восстановителя, такого как, например, H2, CO или H2S, по меньшей мере в течение заключительной фазы регенерации, то есть после испарения большей части серы, осевшей на катализатор Клауса, в целях возможного восстановления сульфатов и/или доведения до кондиции активного вещества катализатора.
В зависимости от активной фазы, используемой для катализатора Клауса на носителе из карбида кремния, использование восстановителя в конце фазы регенерации предназначено для возвращения металла активной фазы катализатора из формы сульфат/сульфит, в которой вышеупомянутый металл находится в конце периода обессеривания, в форму элементного металла или/и сульфида металла, которые составляют активные формы катализатора Клауса, в которые он должен быть возвращен перед его использованием в течение следующего периода обессеривания.
Проведение реакции Клауса согласно изобретению при температурах ниже точки росы образующейся серы может быть реализовано в одной каталитической реакционной зоне, содержащей катализатор Клауса на носителе из карбида кремния, которая действует поочередно в фазе реакции Клауса и в фазе регенерации/охлаждения. Такой вариант осуществления применим, если обессериваемый газ содержит небольшое общее количество серосодержащих соединений H2S и SO2 и вследствие этого регенерация катализатора проводится не часто. Преимущественно каталитическую реакцию осуществляют в нескольких каталитических реакционных зонах, расположенных параллельно, каждая из которых содержит катализатор Клауса согласно изобретению на носителе из карбида кремния. Эти каталитические реакционные зоны действуют таким образом, что по меньшей мере одна из вышеупомянутых зон функционирует в фазе регенерация/охлаждения, в то время как другие зоны находятся в фазе реакции Клауса. Можно также действовать имея одну или несколько зон в фазе каталитической реакции Клауса, по меньшей мере одну зону в фазе регенерации и по меньшей мере одну зону в фазе охлаждения. Каждая каталитическая реакционная зона может содержать несколько ярусов катализатора, например два или три яруса, с охлаждением реакционной среды между последовательными каталитическими ярусами, путем косвенного теплообмена с холодной жидкостью, который происходит внутри или вне каталитической реакционной зоны. Использование нескольких параллельно расположенных каталитических реакционных зон, как указано выше, позволяет осуществлять обработку обессериваемого газа непрерывно.
Газ, используемый для регенерации катализатора Клауса, циркулирует, предпочтительно, по замкнутому контуру, начиная с зоны нагрева, проходя последовательно через каталитическую зону во время регенерации, из которой в результате испарения удаляется сера, и зону охлаждения, в которой большая часть серы, присутствующей в вышеупомянутом газе, выделяется в результате конденсации, и возвращается в зону нагрева. Разумеется, регенерирующий газ может также циркулировать по открытому контуру, если например, использовать обессериваемый газ или обессеренный газ в качестве регенерирующего газа. В случае использования обессериваемого газа в качестве регенерирующего газа, этот газ после отделения серы, испарившейся при регенерации, возвращают в контур перед реакционными зонами.
Газ, используемый для охлаждения регенерированного катализатора Клауса, является газом того же типа, что и используемый для регенерации катализатора, загрязненного серой. Контуры регенерирующего газа и охлаждающего газа могут быть независимыми друг от друга. Тем не менее, сообразно способу реализации, контур регенерирующего газа, описанный выше, может также содержать ответвление, соединяющее выход его зоны охлаждения с входом зоны во время регенерации, шунтируя его зону нагрева, что позволяет миновать вышеупомянутую зону нагрева и таким образом использовать регенерирующий газ в качестве охлаждающего газа.
Форма осуществления способа согласно изобретению в части реакции образования серы между H2S и SO2 при температурах ниже точки росы серы, образующейся в ходе реакции, может преимущественно представлять собой стадию реакции Клауса при температуре ниже точки росы серы (реакция Клауса при низкой температуре) способов, описанных в французских заявках на патенты 2180473, 2224196, 2277877, 2511663, 2540092, 2589082, 2589140, 2589141, 2632626 и 2653422.
Согласно особой форме осуществления способа согласно изобретению, которая может быть использована как при температурах выше точки росы серы, образующейся в реакции между H2S и SO2, так и при температурах ниже вышеупомянутой точки росы, каждая из зон каталитической реакции Клауса, или по меньшей мере первая из вышеупомянутых зон, если последовательно используют несколько каталитических реакционных зон, снабжена каталитической массой, содержащей (1) активный слой, образованный катализатором Клауса согласно изобретению на носителе из карбида кремния, каталитическая фаза которого содержит, в форме оксида или соли и/или в элементном состоянии, по меньшей мере один металл, выбранный среди Fe, Mi, Co, Cu и Zn, и (2) дополнительный слой обычного катализатора Клауса на основе оксида алюминия, промотора реакции Клауса и/или гидролиза органических соединений серы, таких как COS и CS2, в H2S. Дополнительный слой состоит из оксида алюминия, боксита или цеолита. Эта особая форма осуществления позволяет, используя уменьшенное количество катализатора согласно изобретению, продлить во времени сохранение активности обычных катализаторов Клауса на основе оксида алюминия, применяемых в способах получения серы реакцией между H2S и SO2, в особенности, когда обрабатываемый газ содержит небольшое количество кислорода, которое может доходить приблизительно до 1 об.%, Вышеупомянутый катализатор на носителе из карбида кремния, используемый в активном слое, позволяет удалить присутствующий кислород и таким образом защищает катализаторы дополнительного слоя. В случае когда дополнительный слой образован из катализаторов на основе оксида алюминия, вышеупомянутый активный слой образует защиту, предотвращающую их отравление в результате сульфатации оксида алюминия, и позволяет таким образом сохранить каталитическую активность оксида алюминия по отношению к реакции Клауса и к гидролизу соединений COS и CS2.
Изобретение иллюстрируется следующими примерами, приведенными в качестве не ограничивающих его объема охраны.
Пример 1.
Проведены опыты по осуществлению реакции Клауса при температурах выше точки росы серы, образующейся в реакции между H2S и SO2, с использованием либо катализатора согласно изобретению (опыты 1.A.1, 1.A.2, и 1.А.3 согласно изобретению), либо контрольного катализатора на основе оксида алюминия (контрольные опыты 1.B.1, 1.B.2 и 1.В.3) в условиях, используемых на заводе по производству серы на первом каталитическом конвертере (опыты 1.A.1 и 1.B. 1), втором каталитическом конвертере (опыты 1.А.2 и 1.В.2) и третьем каталитическом конвертере (опыты 1.А.3 и 1.В.3). Контрольный катализатор на основе оксида алюминия состоял из шариков диаметром 4 - 6 мм активированного оксида алюминия с удельной поверхностью БЭТ 253 м2/г.
Катализатор согласно изобретению был изготовлен на основе носителя из карбида кремния, пропитанного соединением титана, и содержал титан в количестве 4,8 % от массы катализатора.
Катализатор согласно изобретению получают следующим образом. Сначала зерна карбида кремния с гранулометрией, заключенной между 0,8 и 1 мм, и удельной поверхностью БЭТ 150 м2/г пропитывают оксихлоридом титана в количестве необходимом для получения желаемого количества титана в конечном катализаторе. Чтобы получить катализатор, полученный пропитанный продукт сушат при комнатной температуре в течение 10 часов потом при 120oC в течение 15 часов и затем подвергают прокаливанию при 500oC в течение 6 часов. Полученный катализатор содержит, как указано выше, 4,8 мас.% титана и имеет удельную поверхность БЭТ равную 132 м2/г.
Каждый из опытов проводят в каталитическом реакторе, содержащем катализатор согласно изобретению (опыты 1.A.1, 1.А.2 и 1.А.3 согласно изобретению), или контрольный катализатор (опыты 1.B.1, 1.B.2 и 1.В.3). Каждый реактор имеет вход и выход, разделенные каталитическим слоем, патрубок подачи газа, соединенный с входом в реактор и оснащенный подогревателем, и патрубок для удаления газов, являющийся продолжением выхода из реактора, который оснащен конденсатором для выделения серы в результате охлаждения ее паров.
Обрабатываемый газ, содержащий H2S и SO2, используемый для осуществления реакции Клауса, предварительно нагревают до температуры θ (тета) путем пропускания через подогреватель, связанный с каталитическим реактором, после чего инжектируют в вышеупомянутый реактор при этой температуре. Газообразный эфлюент, выходящий из каталитического реактора через выходной патрубок вышеупомянутого реактора, охлаждают до 175oC в конденсаторе, связанном с каталитическим реактором, с целью выделения серы, содержащейся в вышеупомянутом эфлюенте. Выход серы в реакции вычисляют, исходя из содержаний H2S и SO2 в газе, входящем в каталитический реактор, и в газообразном эфлюенте, выходящем из конденсатора серы.
Специфические условия проведения опытов были следующими.
Опыты 1.A.1 и 1.B.1 : Газ, содержащий H2S и SO2, подаваемый в каталитический реактор, содержит, по объему, 9% H2S, 4,5% SO2, 20% H2О и 66,5% N2. Температура на выходе из каталитического реактора равна 300oC. Эти условия приводят к термодинамическому выходу серы равному 85,9%.
Опыты 1. А.2 и 1.В.2: Газ, содержащий H2S и SO2, подаваемый в каталитический реактор, содержит, по объему, 2,5% H2S : 1,25% SO2, 27% H2О и 69,25% N2. Температура на выходе из каталитического реактора равна 250oC. Эти условия приводят к термодинамическому выходу серы равному 78,7%.
Опыты 1. А.3 и 1.В.3: Газ, содержащий H2S и SO2, подаваемый в каталитический реактор, содержит, по объему, 1% H2S, 0,5% SO2, 30% H2О и 68,5% N2. Температура на выходе из каталитического реактора равна 220oC. Эти условия приводят к термодинамическому выходу серы равному 70,8%.
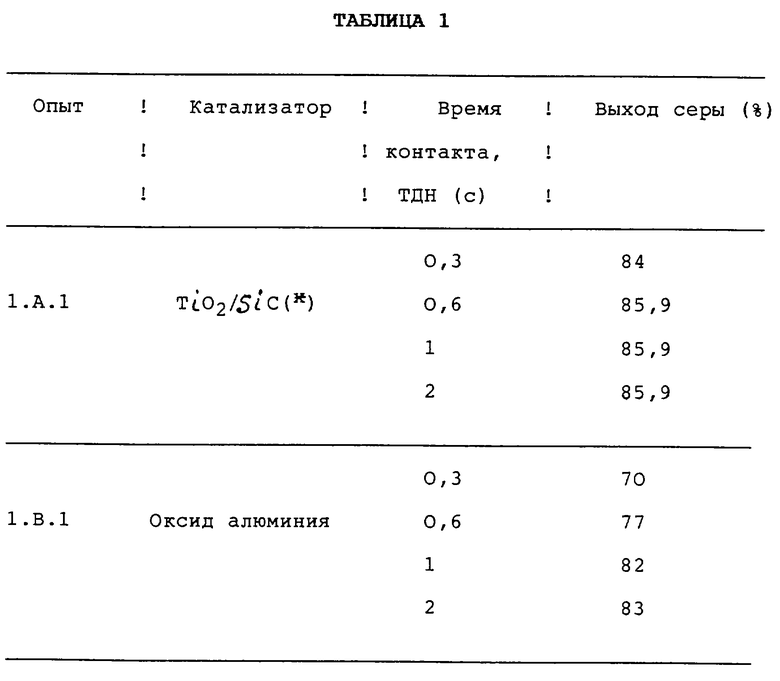
Результаты, полученные в различных опытах, собраны в таблице 1.
Рассмотрение результатов, приведенных в таблице 1, показывает, что проведение реакции Клауса, осуществляемое, как это предложено в изобретении, с катализатором Клауса на носителе из карбида кремния, приводит к значительно большим выходам серы, при сравнимых временах контакта, чем выходы серы, полученные с обычным катализатором Клауса типа оксида алюминия.
Кроме того, также замечено, что введение 0,2 об.% кислорода в обрабатываемый газ, содержащий H2S и SO2, не изменяет выходов серы, полученных с катализатором согласно изобретению, тогда как эти выходы значительно уменьшаются во времени с катализатором на основе оксида алюминия, особенно при относительно низких температурах, используемых во втором и третьем каталитических реакторах, действующих при температурах выше точки росы серы.
Пример 2.
С использованием каталитических реакторов, структура которых сравнима со структурой каталитических реакторов, использованных в примере 1, проведены опыты согласно эксперименту (опыты 2.А.1 и 2.А.2) и контрольные опыты (опыты 2. В. 1 и 2.В.2) по гидролизу органических соединений серы, присутствующих в газах, содержащих H2S и SO2, подвергающихся каталитической обработке в операционных условиях первого каталитического конвертера заводов по производству серы, используя либо катализатор согласно изобретению (опыты 2.А.1 и 2.А.2), идентичный катализатору с титаном на носителе из карбида кремния, описанному в примере 1, либо контрольный катализатор (опыты 2.В.1 и 2.В.2), идентичный катализатору на основе оксида алюминия, использовавшемуся в вышеупомянутом примере 1.
Обрабатываемый газ, помимо H2S и SO2, содержит органическое соединение серы, состоящее из CS2 (опыты 2.А.1 и 2.В.1) или из COS (опыты 2.А.2 и 2.В. 2). Газообразный эфлюент, выходящий из каталитического реактора через выходной патрубок вышеупомянутого реактора, охлаждают, как указано в примере 1, с целью выделения серы, содержащейся в вышеупомянутом эфлюенте. Выход реакции гидролиза соединения COS или CS2 определяют, исходя из содержаний COS или CS2 в газе, входящим в каталитический реактор и в газообразном эфлюенте, выходящем из конденсатора серы; вышеупомянутые содержания определяют хроматогарфическим анализом.
Специфические условия проведения опытов следующие.
Опыты 2. А. 1 и 2.В.1: Обрабатываемый газ, подаваемый в каталитический реактор содержит, по объему, 7% H2S, 4% SO2, 0,8% CS2, 28% H2О и 60,2% N2. Температура, на выходе из каталитического реактора равна 320oC.
Опыты 2. А. 2 и 2.В.2: Обрабатываемый газ, подаваемый в каталитический реактор содержит, по объему, 7% H2S, 3,75% SO2, 0,5% COS, 28% H2O и 60,75% N2. Температура на выходе из каталитического реактора равна 320oC.
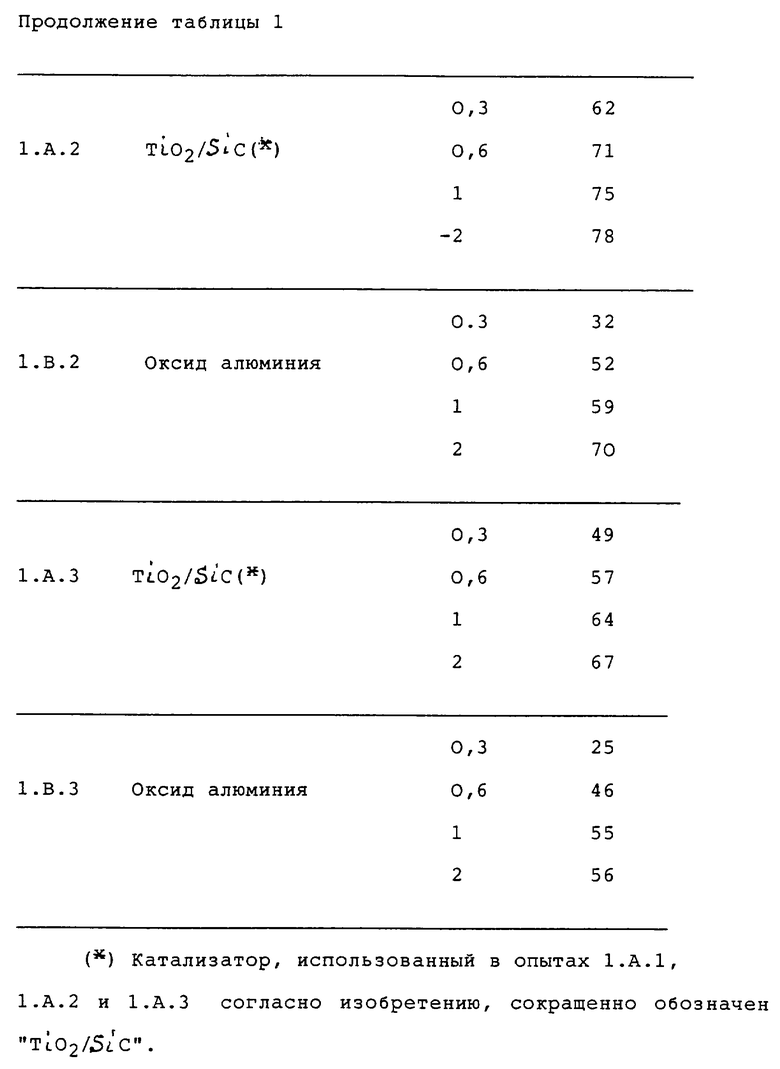
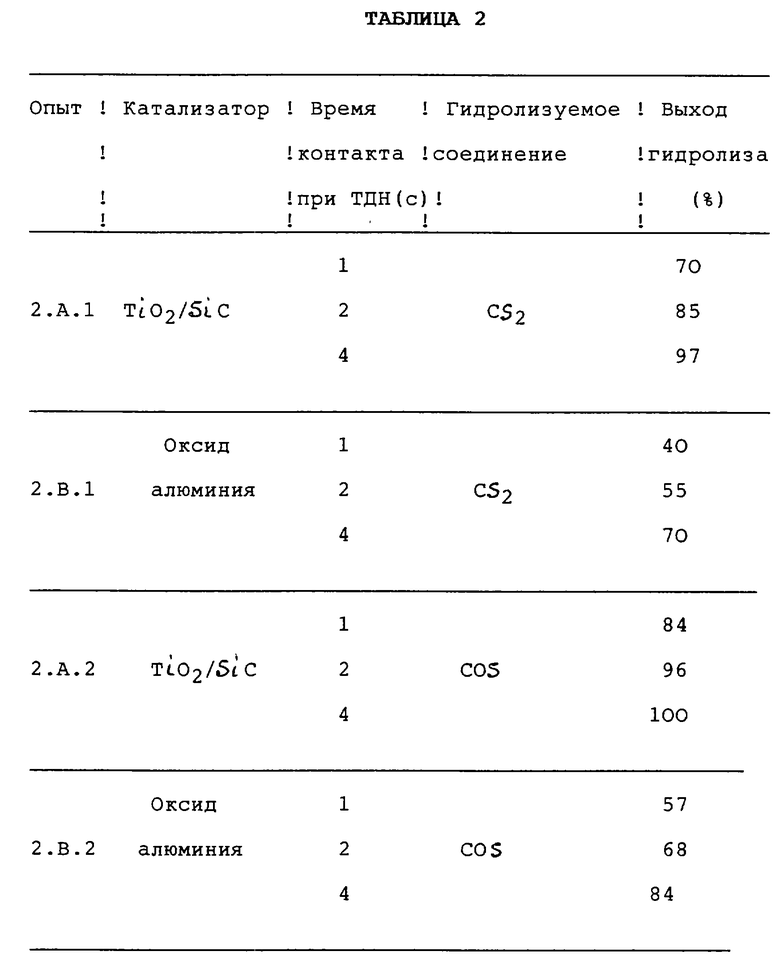
Результаты, полученные в различных опытах, собраны в таблице 2.
Рассмотрение результатов, приведенных в таблице 2, показывает, что выход реакции гидролиза, согласно изобретению, органических соединений серы CS2 и COS значительно выше при сравнимом времени контакта, по отношению к выходам полученным с обычным катализатором Клауса типа оксида алюминия.
Пример 3.
Проводят опыты по осуществлению реакции Клауса при температурах ниже точки росы серы, образующейся в реакции между H2S и SO2, используя либо катализатор согласно изобретению (опыт 3.А.1 согласно изобретению), либо контрольный катализатор на основе оксида алюминия (контрольный опыт 3.В.1).
Контрольный катализатор на основе оксида алюминия состоит из шариков, имеющих диаметр 2 - 4 мм, активированного оксида алюминия с удельной поверхностью БЭТ 242 м2/г.
Катализатор согласно изобретению получают на основе носителя из карбида кремния, пропитанного соединением титана, так чтобы титан составлял 5% от массы катализатора.
Катализатор, используемый в опыте согласно изобретению получают как указано ниже. Сначала зерна карбида кремния, имеющие гранулометрию, заключенную между 2 и 4 мм, и удельную поверхность БЭТ 150 м2/г, пропитывают оксихлоридом титана в количестве, необходимом для достижения желаемого количества титана в получаемом катализаторе. Для получения катализатора полученный продукт сушат при комнатной температуре, потом при 120oC и затем прокаливают, как указано в примере 1. Титановый катализатор содержит, как указано выше, 5 мас.% титана и имеет удельную поверхность БЭТ равную 130 м2/г.
Каждый из опытов проводят в реакторе каталитической конверсии, имеющем вход и выход, которые разделены неподвижным слоем промотирующего катализатора реакции Клауса. Вышеупомянутый реактор действует таким образом, что поочередно, с помощью клапанов, срабатывающих по времени на часах, он находится в фазе реакции, то есть его вход соединен с патрубком для подачи обессериваемой газообразной смеси, или в фазе регенерации/охлаждения, то есть он продувается посредством газообразной смеси, имеющей температуру 300oC и состоящей, по объему, из 70% азота и 30% воды. В ходе регенерации сера, осевшая на катализатор, испаряется и увлекается продувающим газом. На выходе из реактора серу отделяют от вышеупомянутого газа, путем конденсации. Регенерированный реактор затем охлаждают, чтобы вернуть его к температуре, подходящей для следующей очистки. Охлаждение реактора осуществляют путем продувки охлаждающим газом, поддерживаемым при температуре около 80oC.
В каждом из опытов 3.А.1 и 3.В.1 газ, содержащий H2S и SO2, подаваемый в каталитический реактор в фазе реакции Клауса, содержит, по объему, 0,28% H2S, 0,14% SO2, 30% H2О и 69,58% N2. Расход газа соответствует времени пребывания в контакте с катализатором Клауса, в нормальных условиях давления и температуры, равному 4 секундам. Температура на выходе из реактора в фазе реакции Клауса равна 140oC. По окончании регенерации перед тем, как вновь использовать его в фазе очистки (реакции Клауса), регенерированный катализатор охлаждают до температуры около 140oC.
Каталитический реактор действует поочередно в течение 30 часов в фазе каталитической реакции Клауса и в течение 30 часов, из которых 8 часов охлаждается, в фазе регенерации/охлаждения.
После 50 циклов функционирования, каждый из которых содержит фазу реакции Клауса (обессеривание) в фазу регенерации/охлаждения, общее содержание соединений H2S и SO2 стабилизируется на величине CR. Вышеупомянутую величину определяют хроматографическим анализом и, исходя из этой величины и общего содержания Co соединений H2S и SO2 в обрабатываемом газе, вычисляют выход серы в реакции Клауса.
Результаты, полученные в опытах, собраны в таблице 3.
Рассмотрение результатов, приведенных в таблице 3, показывает, что осуществление реакции Клауса с катализатором Клауса согласно изобретению на носителе из карбида кремния при температурах, ниже точки росы серы, образующейся в реакции между H2S и SO2 снова приводит к выходам серы, улучшенным по сравнению с выходами, полученными с обычным катализатором Клауса типа оксида алюминия.
Пример 4.
Проводят опыты по осуществлению реакции Клауса, используя газ, содержащий помимо H2S и SO2, небольшое количество кислорода при температурах выше точки росы серы, образующейся в реакции между H2S и SO2, на каталитической массе, состоящей либо из активного слоя никелевого катализатора на носителе из карбида кремния и следующего за ним слоя обычного катализатора Клауса на основе оксида алюминия (опыт 4.А.1 согласно изобретению), либо только из обычного катализатора Клауса на основе оксида алюминия (контрольный опыт 4.В. 1).
Контрольный катализатор на основе оксида алюминия состоит из шариков, имеющих диаметр 2 - 4 мм, активированного оксида алюминия с удельной поверхностью БЭТ 263 м2/г.
Катализатор согласно изобретению, содержащий 4% никеля и имеющий удельную поверхность БЭТ 138 м2/г, получают на основе носителя из карбида кремния, пропитанного соединением никеля.
Катализатор согласно изобретению получают пропиткой микропористых зерен карбида кремния при помощи соответствующего количества водного раствора ацетата никеля, затем сушат пропитанный продукт при 100oC и прокаливают высушенный продукт при 300oC в течение трех часов. Зерна карбида кремния со средним размером от 2 до 4 мм имеют удельную поверхность БЭТ 150 м2/г.
Каждый из опытов проводят в каталитическом реакторе, содержащем каталитическую массу согласно изобретению (опыт 4.A.1) или контрольную каталитическую массу (опыт 4.В.1), который работает в изотермическом режиме. Вышеупомянутый реактор имеет структуру, сравнимую со структурой реактора, использовавшегося в примере 1. Реактор оснащен приспособлениями, позволяющими поддерживать его температуру на заданной величине.
Обрабатываемый газ, инжектируемый в каталитический реактор содержит, по объему, 9% H2S, 4,5% SO2, 27% H2О, 0,2% кислорода, 0,5% COS, 0,2% CS2 и 58,6% N2.
В ходе каждого опыта каталитический реактор поддерживают при температуре 320oC.
Газообразный эфлюент, выходящий из каталитического реактора через выходной патрубок этого реактора, охлаждают приблизительно до 175oC в конденсаторе, присоединенном к каталитическому реактору, чтобы выделить серу, содержащуюся в вышеупомянутом эфлюенте. Выход серы в реакции определяют, как указано в примере 1, после 800 часов работы реактора.
Специфические условия проведения опытов следующие.
Опыт 4.А.1: Время контакта при ТНД обрабатываемого газа с активным слоем и затем со слоем на основе оксида алюминия каталитической массы согласно изобретению равны 0,5с и 1с соответственно.
Опыт 4.В.1: Время контакта при ТНД обрабатываемого газа с каталитической массой на основе оксида алюминия равно 1,5 с.
Полученные результаты представлены в таблице 4.
Рассмотрение результатов, приведенных в таблице 4, показывает эффективность катализатора согласно изобретению (Ni O/SiC) для предотвращения негативных воздействий кислорода на активность обычного катализатора Клауса типа оксида алюминия.
Пример 5.
Проводят опыты, а именно, опыт 5.А.1 согласно изобретению и два контрольных опыта 5.В.1 и 5.C.1, по осуществлению реакции Клауса, используя газ, содержащий помимо H2S и SO2, небольшое количество кислорода при температурах ниже точки росы серы, образующейся в реакции между H2S и SO2, на каталитической массе, различающейся от одного опыта к другому и составленной как указано ниже.
Опыт 5.А.1 (согласно изобретению): Каталитическая масса состоит из активного слоя никелевого катализатора на носителе из карбида кремния, описанного в примере 4, и следующего за ним слоя оксида алюминия, имеющего удельную поверхность БЭТ 263 м2/г и находящегося в форме шариков диаметром от 2 до 4 мм.
Опыт 5.В.1 (контрольный): Каталитическая масса состоит из активного слоя железосодержащего катализатора на носителе из оксида алюминия и следующего за ним слоя оксида алюминия, идентичного использовавшемуся в опыте 5.А.1.
Опыт 5. С. 1 (контрольный): Каталитическая масса состоит только из слоя оксида алюминия, идентичного использовавшемуся в опытах 5.А.1 и 5.В.1.
Железосодержащий катализатор, содержащий 4,5 мас.% железа, получают пропиткой шариков активированного оксида алюминия, имеющих диаметр от 2 до 4 мм и удельную поверхность БЭТ равную 263 м2/г, посредством соответствующего количества водного раствора сульфата железа (II), затем сушкой пропитанного продукта при 100oC и прокаливанием сухого продукта при 300oC в течение 3 часов.
Каждый из опытов проводят в реакторе каталитической конверсии, имеющем вход и выход, которые разделены неподвижным слоем каталитической массы. Вышеупомянутый реактор действует таким образом, что поочередно, через посредство клапанов, срабатывающих по часам, он находится в фазе реакции, то есть его вход соединен с патрубком для подачи обессериваемой газообразной смеси, или в фазе регенерации/охлаждения, то есть он продувается посредством газообразной смеси, имеющей температуру 300oC и состоящей, по объему, из 10% H2S, 33% H2О и 57% N2. В ходе регенерации сера, осевшая на каталитическую массу, испаряется и увлекается продуваемым газом. На выходе из реактора серу отделяют от вышеупомянутого газа, путем конденсации, регенерированный реактор затем охлаждают, чтобы вернуть его к температуре, подходящей для следующей очистки. Вышеупомянутое охлаждение реактора осуществляют путем продувки охлаждающим газом, состоящим из 38 об.% H2O и 62 об.% N2 и имеющим температуру около 80oC.
В каждом из опытов 5.А.1, 5.В.1 и 5.С.1 газ, содержащий H2S и SO2, подаваемый в каталитический реактор в фазе реакции Клауса, содержит, по объему, 0,8% H2S, 0,4% SO2, 0,08% кислорода, 29% H2O и 69,72% N2.
В опыте 5. A. 1 время контакта при НТД обрабатываемого газа с активным слоем никелевого катализатора и затем со слоем оксида алюминия равны 2,2с и 4,4с соответственно.
В опыте 5. В. 1 время контакта при НТД обрабатываемого газа с активным слоем железосодержащего катализатора и затем со слоем оксида алюминия равны 2,2с и 4,4с соответственно.
В опыте 5.C.1 время контакта при НТД обрабатываемого газа с единственным слоем оксида алюминия равно 6.6с.
В каждом из опытов температуру реактора во время фазы реакции Клауса поддерживали равной 136oC. В конце регенерации регенерированный катализатор охлаждают до этой температуры, перед тем как вернуть его в фазу очистки (реакцию Клауса).
В каждом опыте каталитический реактор работает поочередно в течение 18 часов в фазе каталитической реакции Клауса и в течение 6 часов, из которых 1,5 часа занимает охлаждение, в фазе регенерации/охлаждения.
После 20 циклов функционирования, каждый из которых содержит фазу реакции Клауса (очистка) и фазу регенерации/охлаждения, хроматографическим анализом определяют общее содержание CG, соединений H2S и SO2 в обессеренном газе, выходящем из каталитического реактора. Исходя из этой величины CG и общего содержания Co соединений H2S и SO2 в обрабатываемом газе, вычисляют выход серы в реакции Клауса.
Полученные результаты, собраны в таблице 5.
Рассмотрение результатов, приведенных в таблице 5, показывает эффективность активного слоя катализатора согласно изобретению (Ni O/SiC) для предотвращения негативных воздействий кислорода на активность обычного катализатора Клауса, состоящего из оксида алюминия. Отмечается также, что в этом опыте катализатор согласно изобретению более эффективен, чем железосодержащий катализатор на носителе из оксида алюминия, используемый до сих пор.




Изобретение предназначено для обессеривания газов, содержащих Н2S и SO2 и, в случае необходимости, соединения COS и CS2; газ вводят в контакт с катализатором, образованным каталитической фазой, связанной с носителем из карбида кремния, составляющим по меньшей мере 40% от массы катализатора. Процесс проводят при температурах, которые в зависимости от условий осуществления способа могут быть выше или ниже температуры точки росы образующейся серы в реакционных газах. Изобретение позволяет обессеривать газ с улучшенной селективностью по сере. 17 з.п.ф-лы, 5 табл.
| ПРУЖИННЫЙ ВИБРОИЗОЛЯТОР С РЕГУЛИРУЕМЫМ ДЕМПФЕРОМ СУХОГО ТРЕНИЯ | 2017 |
|
RU2653422C1 |
| Способ получения элементарной серы из сероводородсодержащих газов | 1986 |
|
SU1398304A1 |
| СТЕНД ДЛЯ ОЦЕНКИ ТЕХНИЧЕСКОГО СОСТОЯНИЯ РУЛЕВОГО УПРАВЛЕНИЯ ТРАНСПОРТНЫХ СРЕДСТВ | 1971 |
|
SU422999A1 |
| Способ получения элементарной серы из сероводородсодержащих газов | 1986 |
|
SU1398304A1 |
| SU 757187 А, 23.08.80 | |||
| Объектив с внутренней фокусировкой | 1959 |
|
SU129037A1 |
| Грунтозаборное устройство землесосного снаряда | 1975 |
|
SU543752A1 |
| DE 3403328 А, 02.08.84 | |||
| СПОСОБ ДИАГНОСТИКИ ПОВРЕЖДЕНИЙ ТАЗОБЕДРЕННОГО СУСТАВА | 1996 |
|
RU2143225C1 |
| US 4311683 А, 19.01.82 | |||
| ЦИФРОВОЙ ВОЛЬТМЕТР ИНТЕГРИРУЮЩЕГО ТИПА | 0 |
|
SU218302A1 |
| US 4054642 А, 18.10.77 | |||
| СПОСОБ ИЗГОТОВЛЕНИЯ КОНСЕРВОВ "ПТИЦА С ГАРНИРОМ И СОУСОМ БЕЛЫМ С ЯЙЦОМ" | 2013 |
|
RU2511663C1 |
| Огнетушитель | 0 |
|
SU91A1 |
Авторы
Даты
1999-12-10—Публикация
1996-05-28—Подача