Изобретение касается очищенной хондроитиназы ABC и кристаллической хондроитиназы ABC предельно высокой чистоты и превосходной стабильности, способа получения хондроитиназы ABC и кристаллов хондроитиназы ABC и фармацевтической композиции, включающей хондроитиназу в качестве эффективного компонента.
Хондроитиназа ABC (EC 4.2.2.4) является ферментом, разрушающим гиалуроновую кислоту, хондроитинсульфат, хондроитин, дерматансульфат или подобное в смесь ненасыщенных дисахаридов и олигосахаридов. Известно, что этот фермент продуцируют такие бактерии как Proteus vulgaris.
Известен способ получения хондроитиназы ABC, включающий постепенное воздействие стрептомицина на суспензию разрушенных бактериальных клеток, фракционирование сульфатом аммония, хроматографию на DEAE-целлюлозе и хроматографию на фосфоцеллюлозе (J.Biol. Chem. 243, (7), 1523-1535 (1968)), способ? включающий постепенное хроматографирование суспензии разрушенных бактериальных клеток на DEAE-целлюлозе, хроматографию на оксиапатите, хроматографию на цинк-иммобилизованной агарозе, и гель-проникающую хроматографию (Agric. Biol. Chem. 50, (4), 1057-1059 (1986); открытый патент Японии (Kokai) N 122588/1987) и подобные.
С другой стороны, разработан способ разрушения межпозвоночных дисков (внутридисковая терапия: хемонуклеолиз) для лечения образования грыжи, которую считают причиной болей в пояснице человека. В этом способе в полость межпозвоночных дисков вводят химопапаин, который является производным протеазы из папайи, или производное колагеназы из бактерий для снятия припухлости дисков. Химопапаин продается в Европе и США в виде коммерческого препарата - лекарства с торговой маркой Химодиактин (Chymodiactin - лаборатории Smith) или Discase (Травенол - Travenol).
Однако внутридисковая терапия, использующая указанную протеазу, разрушает не только грыжу на диске, но и протеины в окружающих тканях. Это может являться причиной побочных эффектов, таких как нейропаралич, аллергия и подобное.
Mark R. Brown изучал ферменты, которые могут избирательно воздействовать на образование дисковой грыжи, и обратил свое внимание на разрушение протеогликана, являющегося основной частью диска с образованной грыжей. Результатом его исследования стали внутридисковая терапия с использованием хондроитиназы ABC или хондроитиназы AC (патент США N 4696816, A 61 K 37/48).
В частности, считают, что хондроитиназа ABC, производимая Proteus vulgaris, подходит для медицинского и коммерческого применения из-за ее способности селективно убирать боковые цепи хондроитинсульфата или дерматансульфата из протеогликана, ее неактивности по отношению к кератансульфату, гепарину и гепаринсульфату и ее высокой производительности. Поэтому получают ферменты, обладающие активностью хондроитиназы ABC, описанными ранее способами из культур Proteus vulgaris. Однако эти ферментативные препараты не подходят для использования в качестве лекарства для лечения дисковой грыжи или для использования в качестве реагента высокой чистоты, так как они обладают протеазной активностью или эндотоксинной активностью и содержат нуклеиновую кислоту. Они нестабильны как ферментные белки (J. Biol. Chem. 243, (7), 1523-1535 (1968); патент Великобритании 1067253, Agris. Biol. Chem. 50, (4), 1057-1059 (1986); открытый патент Японии (Kokai) NN 122588/1987 и 57180/1990).
По-видимому, причиной серьезных проблем использования хондроитиназы ABC в качестве лекарства является, главным образом, наличие примесей и нестабильность.
Краткое содержание изобретения. Следовательно, предметом настоящего изобретения является обеспечение новой хондроитиназы ABC высокой чистоты и кристаллической хондроитиназы ABC, не содержащей примесей, имеющей высокую специфическую активность и превосходную стабильность, и полезной в качестве лекарства, а также способа получения хондроитиназы ABC и кристаллической хондроитиназы ABC с хорошим выходом.
Другим предметом настоящего изобретения является обеспечение фармацевтической композиции, включающей хондроитиназу в качестве эффективного компонента.
Для разрушения этой проблемы заявители настоящего изобретения приложили усилия по очистке хондриэтиназы ABC и обнаружили, что очищенную хондроитиназу ABC получают, применяя способ, включающий экстракцию фермента из клеток микроорганизмов, удаление нуклеиновой кислоты из экстракта, содержащего фермент, хроматографирование экстракта, комбинируя слабую катионообменную смолу с сильной катионообменной смолой, при этом из хондроитиназы ABC полностью удаляют такие примеси как эндотоксин, нуклеиновая кислота, протеаза и подобные, и препарат демонстирует одну полосу в SDS-PAGE (додецилсульфат натрия - полиакриламид-гель - электрофорез) и один пик в HPLC-жидкостной хроматографии высокого давления (CPC - гель-проникающая хроматография; катионный обмен).
Обнаружено, что полученная таким образом хондроитиназа ABC кристаллизуется в кристаллическую хондроитиназу ABC, которая имеет специфическую активность в три раза больше, чем активность препаратов хондроитиназы, полученных обычным способом, сохраняет свою активность при хранении в течение длительного времени и высокоактивна в качестве лекарственного препарата. Эти полученные данные привели к завершению настоящего изобретения.
В соответствии с этим предметом настоящего изобретения является обеспечение хондроитиназы ABC высокой чистоты и стабильности, характеристики которой обсуждаются здесь далее.
Другим предметом настоящего изобретения является обеспечение способа получения хондроитиназы ABC высокой чистоты и стабильности, отличающегося тем, что включает:
(i) стадию получения экстракта, содержащего фермент, из клеток микроорганизма, продуцирующего хондроитиназу ABC (стадия 1),
(ii) стадию удаления нуклеиновой кислоты из эстракта, содержащего фермент (стадия 2),
(iii) стадию хроматографирования, которая включает:
а) адсорбцию хондроитиназы ABC при хроматографировании указанного экстракта, содержащего фермент, при использовании слабой катионообменной смолы, элюирование адсорбированного фермента, абсорбцию фермента в элюате и элюирование адсорбированного фермента при хроматографировании с использованием сильной катионообменной смолы (стадия 3-1) или
б) адсорбцию хондроитиназы ABC при хроматографировании указанного экстракта, содержащего фермент, с использованием сильной катионообменной смолы, элюирование адсорбированного фермента, адсорбция фермента в элюате и элюирование адсорбированного фермента при хроматографии с использованием слабой катионообменной смолы (стадия 3-2).
В предпочтительном варианте настоящего изобретения указанный экстракт хондроитиназы ABC получают способом, который включает добавление буферного раствора с pH, близким к нейтральному, к увлажненным клеткам для получения суспензии клеток и физическую обработку клеток для их размельчения; или способом, который включает добавление раствора поверхностно-активного вещества с pH, близким к нейтральному, к увлажненным клеткам для получения суспензии клеток и перемешивание суспензии.
Указанное двухступенчатое хроматографирование при комбинации слабой и сильной катионообменных смол после удаления нуклеиновой кислоты из экстракта клеток, содержащего хондроитиназу ABC, дает хондроитиназу ABC высокой чистоты, более чистую и более стабильную, чем обычные препараты хондроитиназы ABC, и имеющую специфическую активность, которая более чем в три раза выше активности препаратов хондроитиназы ABC, полученных обычным способом.
Еще одним предметом настоящего изобретения является обеспечение кристаллической хондроитиназы ABC с иглообразными или призматическими кристалалми и характеристиками указанной очищенной хондроитиназы ABC, которую получают кристаллизацией указанной очищенной хондроитиназы ABC в полиэфире, имеющем гидроксильные группы на обоих концах (например, полиэтиленгликоль, полипропиленгликоль). Такая хондроитиназа ABC и ее кристаллы имеют высокую гомогенность, стабильные характеристики и высокую специфическую активность и демонтирует превосходную стабильность при хранении (например, ее активность слегка понижается при хранении в течение месяца при температуре 25-40oC).
Еще одним объектом настоящего изобретения является обеспечение композиций, содержащих хондроитиназу.
В частности, настоящее изобретение обеспечивает композицию, включающую хондроитиназу и сывороточный альбумин или желатин.
Настоящее изобретение обеспечивает, кроме того, композицию, включающую хондроитиназу и неионное поверхностно-активное вещество. Кроме того, предметом настоящего изобретения является обеспечение фармацевтической композиции для лечения смещения межпозвоночных дисков, включающей хондроитиназу.
Для этих композиций можно использовать не только упомянутую выше очищенную хондроитиназу, но также обычную хондроитиназу ABC или хондроитиназу AC.
Такие композиции включают раствор, который предотвращает абсорбцию хондроитиназы на стенках контейнера и, кроме того, предотвращает образование нерастворимых веществ при механических воздействиях, сохраняя, таким образом, высокую активность и применимость в качестве лекарства.
Другие и дополнительные объекты, признаки и преимущества настоящего изобретения проявятся более полно из следующего описания.
Краткое описание чертежей.
Фиг. 1 представляет микроскопическую фотографию кристаллов хондроитиназы ABC настоящего изобретения.
Фиг. 2 показывает соотношение между активностью и реактивным pH хондроитиназы ABC настоящего изобретения.
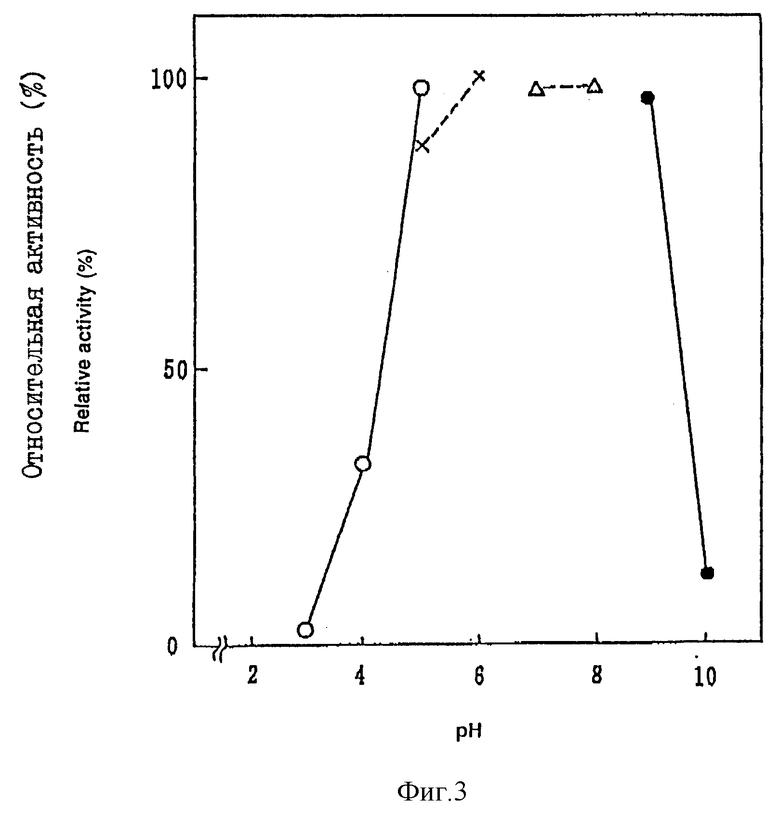
Фиг. 3 показывает соотношение между pH и остаточной активностью хондроитиназы ABC настоящего изобретения, когда фермент оставляют стоять при 25oC в течение 24 часов в различных буферных растворах при определенном pH; на чертеже линия, соединяющая белые кружочки, показывает остаточную активность для случая хранения фермента в ацетатном буферном растворе; штриховая линия, соединяющая крестики, - хранение в буферном растворе трисуксусная кислота; штриховая линия, соединяющая треугольники, - хранение в буферном растворе трис-HCl; и линия, соединяющая черные кружочки, - глицериновый буферный раствор.
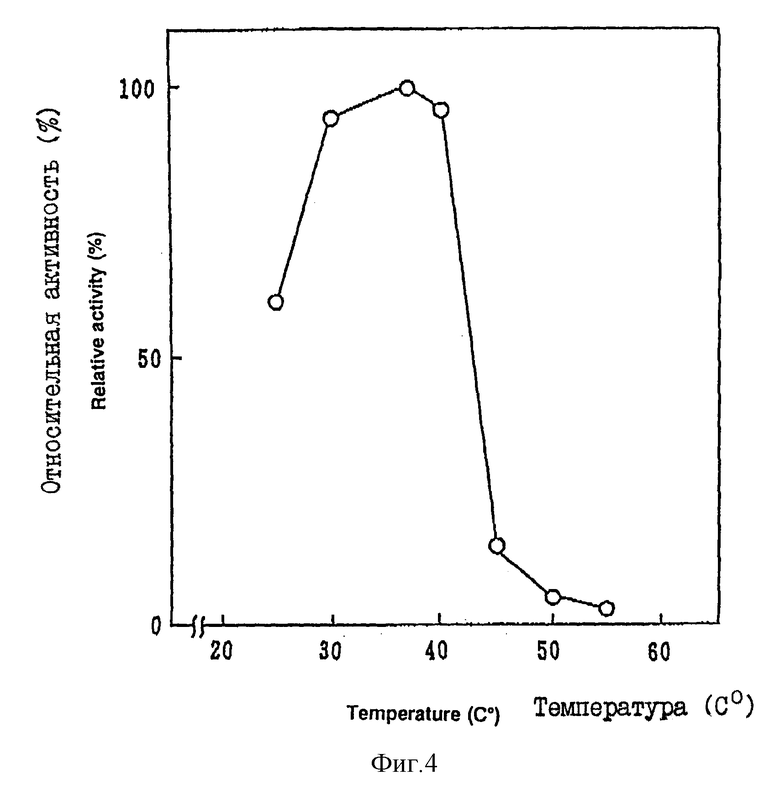
Фиг. 4 показывает соотношение между остаточной активностью и реактивной температурой хондроитиназы ABC настоящего изобретения.
Фиг. 5 показывает соотношение между остаточной активностью хондроитиназы ABC настоящего изобретения и температурой, когда фермент хранили при различных температурах в течение 1 часа.
Фиг. 6 показывает хроматограмму, когда хондроитиназу ABC настоящего изобретения хроматогарфируют гель-проникающим методом при HPLC.
Фиг. 7 показывает SDS-PAGE полосы на различных стадиях процесса для очистки хондроитиназы ABC примера 1, где полоса A соответствует супернатанту обработки протамином; полоса B соответствует жидкости обработки CM-сефарозой (CM-Sepharose); полоса C соответствует жидкости (невосстановленной) после обработки S-сефарозой; и полоса D соответствует жидкости (восстановленной) после обработки S-сефарозой.
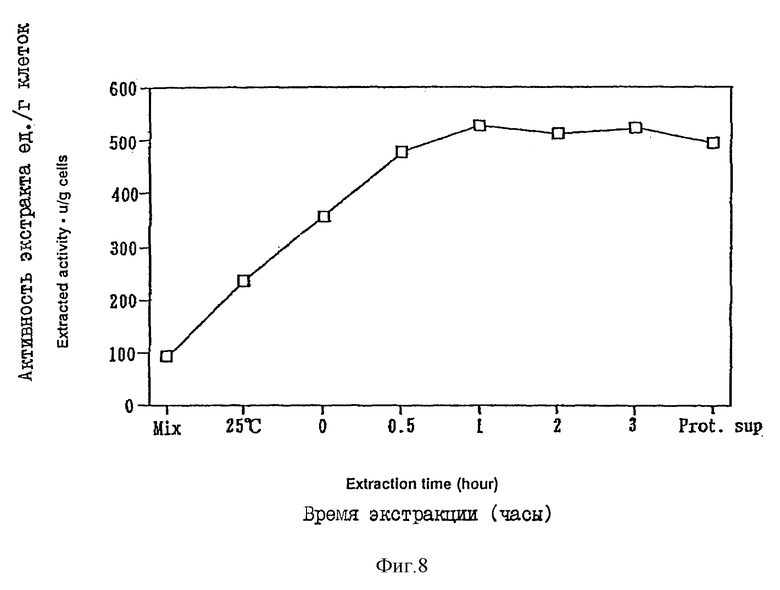
Фиг. 8 показывает соотношение между временем экстракции хондроитиназы ABC из клеток бактерий и активностью хондроитиназы ABC в примере 3.
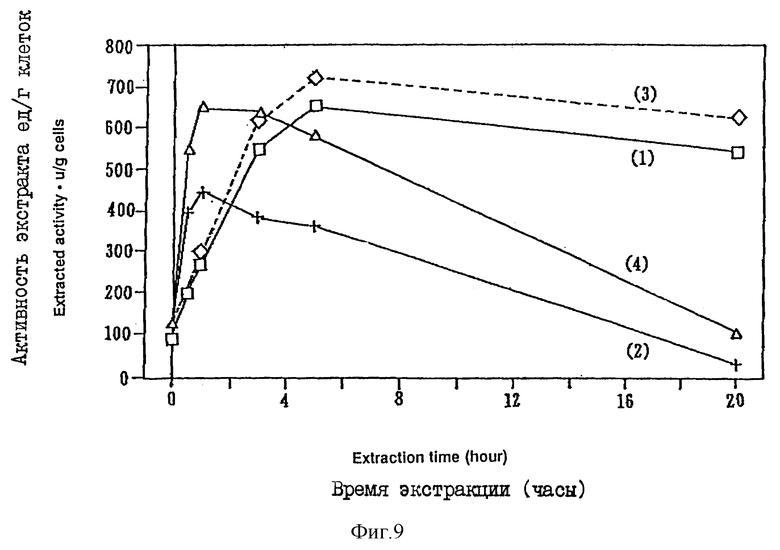
Фиг. 9 показывает соотношение между временем, необходимым для экстракции клеток бактерий с использованием буферного раствора, содержащего Triton X-100, с различной концентрацией и активностью хондроитиназы ABC в примере 4, где кривая 1 соответствует экстракции с использованием буферного раствора при концентрации поверхностно-активного вещества 2% при 25oC; кривая 2 соответствует использованию буферного раствора с концентрацией поверхностно-активного вещества 2% при 37oC; кривая 3 соответствует использованию буферного раствора с концентрацией поверхностно-активного вещества 5% при 25oC; и кривая 4 соответствует использованию буферного раствора с концентрацией поверхностно-активного вещества 5% при 37oC.
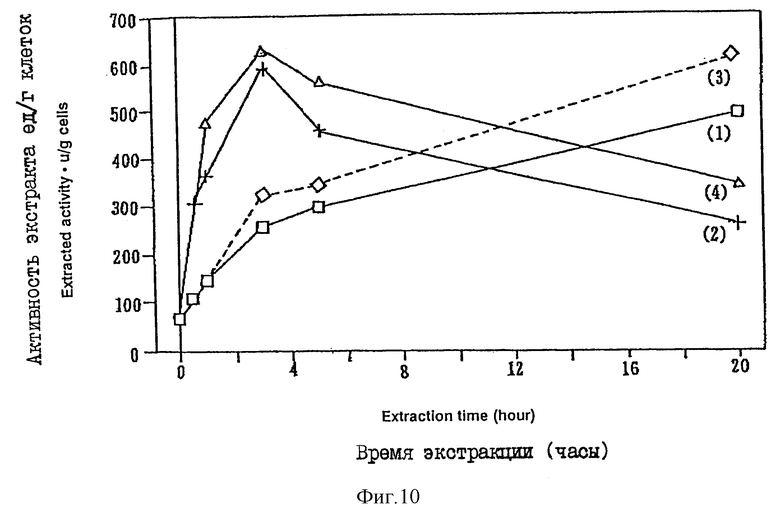
Фиг. 10 показывает соотношение между временем, необходимы для экстракции клеток бактерий при использовании буферного раствора, содержащего Brij-35, с различными концентрациями и активностью хондроитиназы ABC в примере 4, где кривая 1 соответствует экстракции с использованием буферного раствора с концентрацией поверхностно-активного вещества 2% при 25oC; кривая 2 соответствует использованию буферного раствора с концентрацией поверхностно-активного вещества 2% при 37oC; кривая 3 соответствует использованию буферного раствора с концентрацией поверхностно-активного вещества 5% при 25oC; и кривая 4 соответствует использованию буферного раствора с концентрацией поверхностно-активного вещества 5% при 37oC.
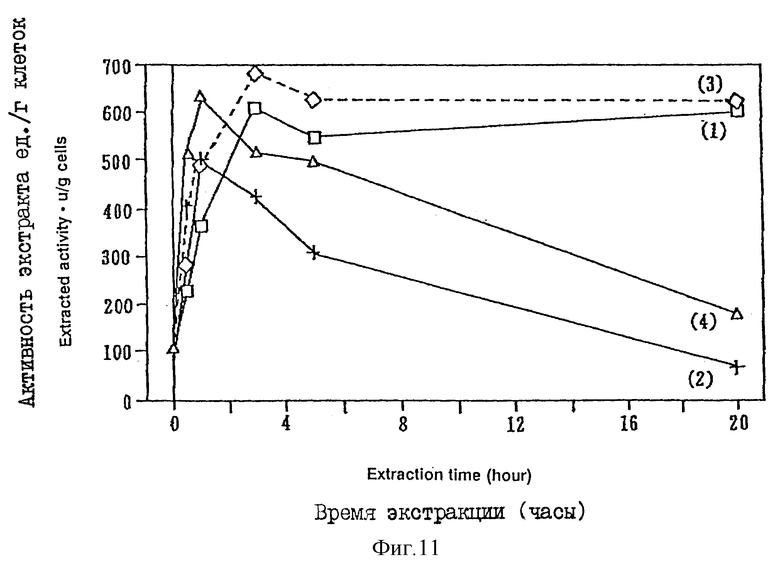
Фиг. 11 показывает соотношение между временем, необходимым для экстракции клеток бактерий с использованием буферного раствора, содержащего Nonidet P-40 с различными концентрациями, и активностью хондроитиназы ABC в примере 4, где кривая 1 соответствует экстракции с использованием буферного раствора с концентрацией поверхностно-активного вещества 2% при 25oC; кривая 2 соответствует использованию буферного раствора с концентрацией поверхностно-активного вещества 2% при 37oC; кривая 3 соответствует использованию буферного раствора с концентрацией поверхностно-активного вещества 5% при 25oC; и кривая 4 соответствует использованию буферного раствора с концентрацией поверхностно-активного вещества 5% при 37oC.
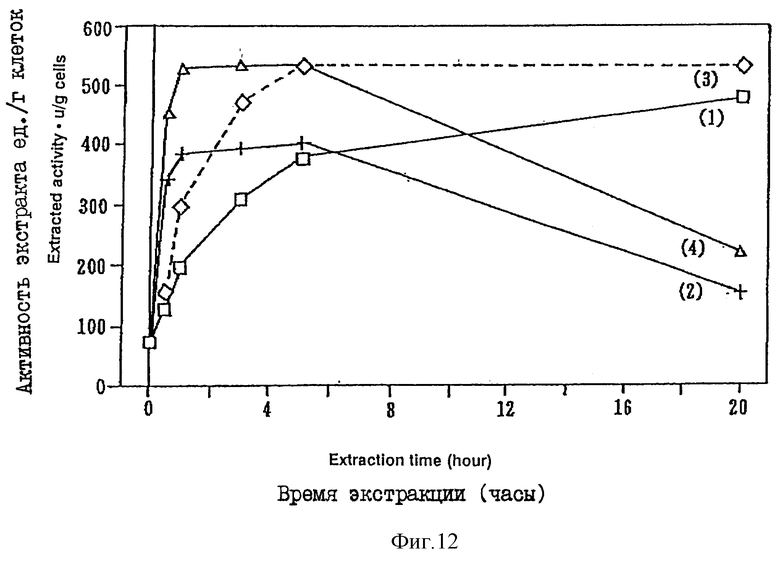
Фиг. 12 показывает соотношение между временем, необходимым для экстракции клеток бактерий с использованием буферных растворов, содержащих POELE с различными концентрациями, и активностью хондроитиназы ABC в примере 4, где кривая 1 соответствует экстракции с использованием буферного раствора с концентрацией поверхностно-активного вещества 2% при 25oC; кривая 2 соответствует использованию буферного раствора с концентрацией поверхностно-активного вещества 2% при 37oC; кривая 3 соответствует использованию буферного раствора с концентрацией поверхностно-активного вещества 5% при 25oC; и кривая 4 соответствует использованию буферного раствора с концентрацией поверхностно-активного вещества 5% при 37oC.
В деталях показан способ получения очищенной хондроитиназы ABC и кристаллов хондроитиназы ABC настоящего изобретения.
Для получения хондроитиназы ABC настоящего изобретения можно использовать любые клетки обычных известных микроорганизмов, например микроорганизмов, принадлежащих к Proteus vulgaris или подобным. Отдельным примером такого микроорганизма является Proteus vulgaris NCTC 4636 (ATCC 6896, 1ГО 3988).
Микроорганизмы можно культивировать обычным способом (например, J.Biol. Chem. , 243, (7), 1523-1535 (1968); открытый патент Японии (Kokai) N 122588/1987 или N 57180/1990). Увлажненные клетки собирают из культуры и суспендируют в буферном растворе с pH, близким к нейтральному, экстрагируя фермент из суспензии. Обычно в качестве буферного раствора с pH, близким к нейтральному, используют фосфатный буферный раствор, трис-HCl буферный раствор, ацетатный буферный раствор или подобные с pH от 6,0 до 8,0 и концентрацией от 1 до 100 мМ. Клетки размельчают при помощи шаровой мельницы (используют DYNO® MILL или другие) для экстракции раствора фермента, содержащего хондроитиназу ABC, протеазу, другие ферменты, нуклеиновую кислоту, белки и подобное.
Эффективность экстракции хондроитиназы ABC из клеток можно увеличить, используя растворы поверхностно-активных веществ, то есть, используя буферные растворы, к которым добавлены поверхностно-активные вещества.
В настоящем изобретении можно использовать любые поверхностно-активные вещества, которые эффективно стимулируют экстракцию ферментов.
Неионные поверхностно-активные вещества, которые можно применять, включают алкильные эфиры полиоксиэтилена, п-трет-октилфенильные эфиры полиоксиэтилена, полисорбат и подобное. В качестве специфических примеров алкильных эфиров полиоксиэтилена приведены поверхностно-активные вещества эмульгирующего типа (Emulgen-уре), Liponox-типа, Brij-типа и подобные. Подходящими с коммерческой точки зрения являются среди них Emulgen 120, Emulgen 109P, Liponox DCH, Brij 35, 78, 76, 96, 56, 58, 98, Nikkol BL-9 EX, BL-21, BL-25 и подобные. Приведенные в качестве отдельных примеров п-трет-октилфонильные эфиры полиоксиэтилена являются поверхностно-активными веществами Triton-типа, Nonidet P-40 типа, Igepal/CA-типа, Polytergent C, Neutronyx-типа, Conco-типа и подобными. Среди них Triton X-100, X-45, X-114, X-102, X-165, X/305 X-405, Nonidet P-40, Igepal CA-630, Neutronyx 605, Conco IX-100 и подобные являются подходящими с коммерческой точки зрения. В качестве специфических примеров полисорбатов приведены поверхностно-активные вещества Tween-типа, Emasol-типа, Sorbester-типа, Crill-типа и подобные. Предпочтительными полисорбатами являются производные сорбитан-моно-9- октадеканоат-поли- (окси-1,2-этандиила) с коммерческой маркой Tween 80. Другими примерами коммерческих полисорбатов являются Tween 20, 40, 60, Emasol 4115, 4130 и подобные.
Среди приведенных выше поверхностно-активных веществ особенно предпочтительными являются алкильные эфиры полиоксиэтилена (например, лауриловый эфир полиоксиэтилена, полидоканал (polidocanal), называемые здесь далее "POELE") и подобные. Применение этих поверхностно-активных веществ не только эффективно промотирует экстракцию ферментов, но также дает в результате экстракт фермента, содержащий хондроитиназу ABC с меньшим количеством протезы, сопутствующего белка и нуклеиновой кислоты по сравнению с другими способами экстракции.
Экстракт фермента, полученный таким образом, хроматографируют, используя слабую катионообменную смолу или сильную катионообменную смолу, а затем можно получить хондроитиназу ABC с предельно высокой активностью, дающую одну полосу при электрофорезе.
В такой хондроитиназе ABC не обнаружено протеазной активности. Содержание эндотоксина в такой хондроитиназе очень маленькое, и не возникает проблем ее использования в качестве компонента лекарственных препаратов.
Для экстракции увлажненные культивированные клетки добавляют к буферному раствору, содержащему от 2 до 7% указанного поверхностно-активного вещества для получения суспензии клеток. Эту суспензию нагревают до температуры 15-45oC, предпочтительно до примерно 37oC, перемешивают в течение примерно 1-10 часов, предпочтительно около 2-6 часов, и охлаждают до комнатной температуры, отделяют экстракт от клеточного остатка такими способами разделения, как центрифугирование или подобные. Полученный таким образом экстракт, содержащий хондроитиназу ABC в качестве основного компонента, другие ферменты, белки и нуклеиновые кислоты, используют в следующей стадии очистки.
На стадии очистки из экстракта клеток удаляют белки, нуклеиновые кислоты и подобное. Для удаления белков и нуклеиновых кислот применяют любые традиционные способы. Когда принимают во внимание использование фермента в качестве компонента лекарства, особо предпочтительным способом удаления нуклеиновых кислот является добавка протаминсульфата.
Обработку протамином проводят, добавляя 3-7% раствор протаминсульфата к экстракту клеток до концентрации примерно 0,25 - 1%, и перемешивают смесь при температуре от примерно 4oC до комнатной в течение 10 - 30 минут, получая осадок нуклеиновых кислот и подобного. Затем осадок отделяют и удаляют при центрифугировании или др.
Полученный таким образом супернатант, содержащий хондроитиназу ABC, протеазу и другие ферменты, затем хроматографируют, используя катионообменную смолу.
Для получения очищенной хондроитиназы ABC очистку осуществляют хроматографическим способом, применяя комбинацию слабой катионообменной смолы и сильной катионообменной смолы.
Слабой катионообменной смолой, используемой в настоящем изобретении, является катионообменная смола с карбоксиалкильными группами, например карбоксиметильной группой, в качестве обменной группы. В качестве специфического примера приведено производное полисахарида (производное агарозы, производное сшитого декстрана и др.) с карбоксиметильной группой в качестве обменной группы.
Коммерческими примерами таких катионообменных смол являются CM-сефароза (CM-sepharose), CM-sephadex (торговые марки, производство Pharmacia) и подобные.
Катионообменная смола с сульфоалкильной группой в качестве обменной группы представлена как сильная катионообменная смола, применяемая в настоящем изобретении. В качестве специфических примеров приведены производные полисахаридов (производное агарозы, производное сшитого декстрана и др.) с сульфоэтильной группой или подобные. Коммерческими примерами таких сильных катионообменных смол являются S-Sepharose, SP-Sepharose (торговые марки, производство Pharmacia), SP-Sephadex (торговая марка, производство Pharmacia), SP-Toyopearl (торговая марка, производство Tosoh Co.) и подобные.
Далее приведен один пример хроматографического использования этих двух типов смол в комбинации.
Первое хроматографирование проводят, уравновешивая слабую катионообменную смолу таким буферным раствором (pH 6,5 - 7,5), который используют в экстракции клеток (например, 1-50 мМ фосфатный буферный раствор, трис-HCl буферный раствор, ацетатный буферный раствор и др.), с последующим контактом фермента, содержащего указанное поверхностно-активное вещество, с катионообменной смолой для абсорбции фермента и промывая катионообменную смолу обычно используемым солевым раствором (например, 20-26 мМ раствором NaCl) и/или упомянутым выше раствором поверхностно-активного вещества (например, 0,5% раствором POELE). Элюат, полученный растворением хлорида натрия в указанном буферном растворе, с концентрацией примерно 0,1 М контактирует с указанной смолой, элюируя фракции, обладающие ферментной активностью. В качестве способа элюирования можно применять как градиентное элюирование, так и ступенчатое элюирование. Хроматографирование можно осуществлять колоночным способом или периодическим способом.
Полученные таким образом фракции затем контактируют с сильной катионообменной смолой, которая находится в равновесии с тем же буферным раствором, для адсорбции хондроитиназы ABC. После промывания катионообменной смолы обычно применяемым солевым раствором (например, 20-50 мМ раствором NaCl) и/или водой выделяют хондроитиназу ABC путем градиентного элюирования, используя такой же буферный раствор (например, фосфатный буферный раствор, трис-HCl буферный раствор, ацетатный буферный раствор и др.), но содержащий NaCl с градиентом концентрации от 0 до 0,5 М, предпочтительно от 25 до 350 мМ. Это хроматографирование предпочтительно проводить колоночным способом. Возможно обратное применение хроматографии с использованием двух типов катионообменных смол.
Затем клетки экстрагируют буферным раствором, содержащим поверхностно-активное вещество, экстракт при этом содержит только очень небольшое количество примесей. В этом случае фермент можно очистить простыми способами, например без обработки для удаления нуклеиновых кислот из экстракта (такой как обработка протамином), только пропуская экстракт через колонку со слабой катионообменной смолой (например, СМ-Sepharose), адсорбируя хондроитиназу ABC, промывая колонку и элюируя фермент градиентным способом.
Раствор очищенного фермента, полученный хроматографическим способом, может служить лекарством, реагентом или подобным после концентрирования и удаления соли. По-другому, из концентрированного раствора без соли можно получить порошок при помощи обычной сушки (например, лиофилизацией) в условиях, которые не дезактивируют или денатурируют фермент.
Кроме того, указанный раствор очищенного фермента можно смешать с полиэфиром, имеющим гидроксильные группы на обоих концах (например, полиэтиленгликоль, полипропиленгликоль и др.) для кристаллизации хондроитиназы ABС. Кристаллы имеют ромбическую или моноклинную структуру, иглообразные, параметры кристаллической решетки приведены далее в примерах.
Далее приведен один пример проведения кристаллизации. К раствору фермента добавляют полиэтиленгликоль с соответствующим молекулярным весом, таким как 4000, 6000 или подобный. Раствор концентрируют до концентрации фермента 250-500 ед./мл и концентрации полиэтиленгликоля 5-20%, предпочтительно 10-15% и дают ему стоять при температуре от 4oC до комнатной до тех пор, пока не вырастут кристаллы фермента.
Очищенная таким образом хондроитиназа не содержит таких примесей, как эндотоксин, нуклеиновые кислоты, протеаза, другие белки и подобное и дает одну полосу в SDS-PAGE и один пик в HPLC (GPC, катионный обмен), а также имеет специфическую активность, увеличенную более чем в три раза по сравнению с хондроитиназой ABC, полученной обычными способами. Кроме того, в соответствии со способом настоящего изобретения в ходе получения продукта не требуется проведение таких процедур, как фракционирование сульфатом аммония, концентрирование/обессоливание и подобных, как в обычных способах, следовательно, можно сократить время производства хондроитиназы ABC, увеличить выход и снизить стоимость производства. Кроме того, способ настоящего изобретения можно применять со всеми его преимуществами независимо от количества получаемой хондроитиназы.
Кристаллическую хондроитиназу ABC получают упомянутым выше способом кристаллизации в виде иглообразных или призматических кристаллов (см. фиг. 1), гомогенную и со стабильными характеристиками. Она также имеет высокую специфическую активность и превосходную стабильность при хранении.
Далее приведены характеристики хондроитиназы ABC, полученной способом настоящего изобретения.
1) Воздействия. Действует на гиалуроновую кислоту, хондроитинсульфат, хондроинит и дерматансульфат, давая небольшое количество ненасыщенного олигосахарида с большим молекулярным весом на ранней стадии реакции и, в конечном счете, смесь ненасыщенного дисахарида (Δ4-глюкуронил-N- ацетилгексозамина и его 4- и 6-сульфатов) и олигосахарида.
2) Оптимальный pH и стабильный pH. Оптимальным является pH от 8,0 до 8,2, когда субстратом в трис-HCl буферном растворе является хондроитинсульфат (фиг. 2). После хранения при pH от 5 до 9 и температуре 25oC в течение 24 часов фермент проявляет 80% или более остаточной активности (фиг. 3).
3) Проверка ферментативной активности. Измерение основано на производстве в ходе ферментативной реакции ненасыщенных дисахаридов, демонстрирующих значительное поглощение света в ультрафиолетовой области. В частности, ферментативную реакцию проводят в реакционном растворе фермента, содержащем фермент, 1,2 мг хондроитинсульфата C (субстрат), 50 мМ трис-HCl буферного раствора (pH 8-8,5) с 50 мМ ацетата натрия и 10 μг казеина при 37oC в течение 20 минут. Реакцию прекращают, добавляя 0,05 M HCl (pH 1,8). Измеряют поглощение света при 232 нм. Отдельно выдерживают прогретый раствор денатурированного фермента (в качестве контроля) в растворе субстрата такого же состава, как описано выше, обрабатывают его таким же образом, как описано выше, и измеряют поглощение света при 232 нм. Количество ненасыщенных дисахаридов рассчитывают по увеличению поглощения света в образце по сравнению с контролем. Миллимолярный молекулярный коэффициент экстинкции 2-ацетамидо-2-деокси-3-O- (β-D-глюко-4-ен-пиранозилуроновокислой)-6-O- сульфо-D-галактозы, использованный в рассчетах, равен 5,5. В результате определено, что одна единица (U) фермента катализирует выделение в реакции 1 микромоля ненасыщенных дисахаридов за одну минуту в описанных выше условиях проведения реакции.
4) Оптимальная температура реакции и температура устойчивости. Оптимальной температурой реакции является температура 37oC. Фермент демонтирует 90% и более активности при 30 - 37oC (фиг. 4). Фермент устойчив при 2 - 30oC и дезактивируется при 50oC, когда его хранят в трис-HCl буферном растворе (pH 7,0) в течение 1 часа (фиг. 5).
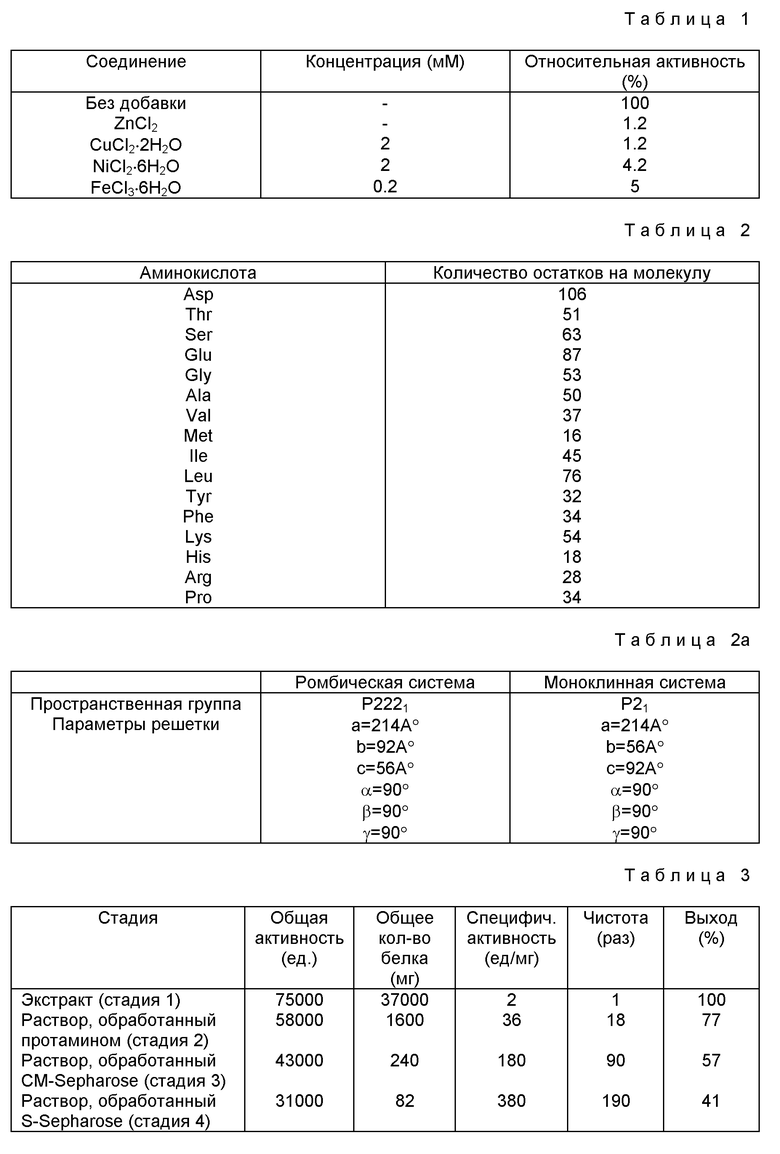
5) Ингибирование. Активность ингибируют ионами цинка (Zn2+), ионами никеля (Ni2+), ионами железа (Fe3+) и ионами меди (Cu2+), как показано в таблице 1.
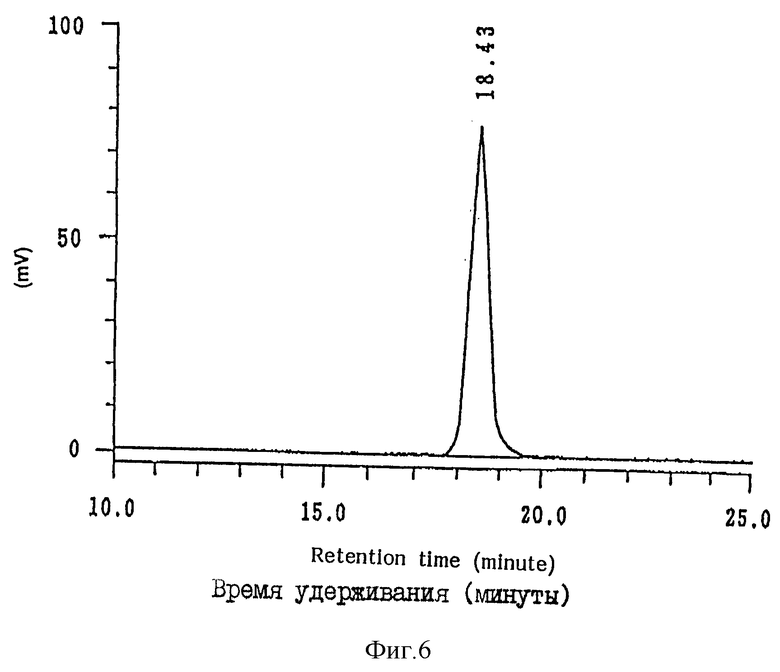
6) Молекулярный вес. Электрофорез с использованием додецилсульфата натрия - полиакриламидного геля (SDS-PAGE) дает одну полосу. Молекулярный вес составляет около 100000 Да в обоих состояниях, восстановленном и невосстановленном. Молекулярный вес, определенный методом гель-проникающей хроматогарфии (HPLC) составляет 100000 дальтон (см. фиг. 6 условия обсуждаются ниже).
7) Изоэлектрическая точка. Изоэлектрическая точка 8,2 и 8,5 (в Phast System используют p1-калибровочный набор 3-10 в качестве стандарта, Phast Gel IEF pH 3-9; все использованные реагенты и приборы получены в Pharmacia).
8) Аминокислотный анализ. Результаты приведены в таблице 2.
Приведенный анализ проводят, гидролизуя хондроитиназу ABC в 6 М соляной кислоты при пониженном давлении и 110oC в течение 24 часов. В таблице приведены средние величины от трех исследованных образцов. Рассчеты выполнены для общего молекулярного веса 100000. Трипсин и цистеин не определяли.
9) Концевая аминокислота. N-концевым аминокислотным остатком, определенным по методу Edman (Edman degradation analysis, "Biochem. Experiments N1, Protein chemistry II, Determination of primary structure" 132-142, август 28, 1976, опубликовано Tokyo Kagaku Dojin) является аланин. Аминокислотная последовательность Ala-Thr-X-Asp-Pro-Ala-Phe-Asp-Pro-, где X - неопределенное звено.
C-концевой аминокислотной последовательностью, определенной карбоксипептидазным способом ("Biochem. Experiment N1, Protein Chemistry II, Determination of primary structure", 203-211) является -Ser-Leu-Pro.
Таким образом, доказано, что терминальной аминокислотной последовательностью хондроитиназы ABC настоящего изобретения является следующая: Ala-Thr-X-Asp-Pro-Ala-Phe-Asp-Pro-----Ser-Leu-Pro, где X - неопределенное звено.
10) Устойчивость при хранении. Фермент устойчив по крайней мере в течение трех месяцев при комнатной температуре как в растворе фосфатного буфера (pH 6-8), так и в сухом состоянии.
11) Специфическая активность. Содержание белка определяли методом Lowry, используя бычий сывороточный альбумин в качестве стандарта. Специфическая активность составляет по крайней мере 300 ед./мг белка.
12) Другое. Фермент дает один пик как в HPLC, так и в гель-проникающей (GPC) HPLC (катионный обмен). Условия и результаты проведения гель-проникающей хроматографии приведены далее.
Условия. Колонка TKS C3000 SWXL (производство Tosoh Co.). Элюент: 0,1 М раствор фосфатного буфера (pH 7.0), содержащий 0,2 М NaCl. Скорость элюирования: 0,5 мл/минуту. Температура процесса 35oC. Длина волны при детектировании: 280 нм. Заряжаемое количество: 20 μл. Вещества-метки молекулярного веса: цитохром C (12,4 кДа), аденилактиназа (32 кДа) енолаза (67 кДа), лактатдегидрогеназа (142 кДа), глутаматдегидрогеназа (290 кДа). Все ферменты произведены Oriental Yeast Manufacturing Co. Ltd.
Результаты. Хондроитиназу ABC настоящего изобретения элюируют одним пиком при времени удерживания 18,43 мин (фиг. 6). Определен молекулярный вес фермента примерно 100000 дальтон на основании сравнения времени удерживания приведенных выше веществ-меток и их молекулярных весов.
Препарат практически не содержит эндотоксина. Содержание ДНК и протеазы ниже пределов обнаружения, в то время как коммерческая хондроитиназа ABC (Sei kagaku Corporation N 10032 по каталогу) содержит ДНК в количестве, превышающем предел обнаружения в 5000 раз, а протеазу в количестве, превышающем предел обнаружения в 200 раз.
Для сравнения хондроитиназы ABC настоящего изобретения и хондроитиназы ABC, свободной от протеазы (Seikagaku Corp. N 100332 по каталогу), которая, как известно, имеет наивысшую чистоту среди известных в настоящее время хондроитиназ, первая из двух имеет молекулярный вес около 100000 Да, определенный двумя методами SDS-PAGE и HPLC (GPC), в то время как вторая имеет молекулярный вес 80000, определенный методом SDS-PAGE, и около 120000-145000 дальтон, определенный методом гель-фильтрации. Это большая разница. К тому же, в то время как первая имеет специфическую активность 300 ед./мг белка или более, вторая имеет специфическую активность около 110 ед./мг белка. В отношении стабильности при хранении первая стабильна при комнатной температуре в течение по крайней мере трех месяцев, а вторая, как заявлено, стабильна в течение по крайней мере трех месяцев при температуре -70oC. Это также существенная разница. Кроме того, первая хондроитиназа ABC дает одну полосу в SDS-PAGE и один пик в HPLC (GPC), ее можно кристаллизовать и определить, таким образом, терминальную аминокислоту и изоэлектрическую точку, в то время как вторая не является ферментом, который можно определить как индивидуальное вещество, и, следовательно, невозможно идентифицировать ее терминальную аминокислоту и измерить изоэлектрическую точку.
Теперь будут описаны композиции и лекарства настоящего изобретения.
Первая иллюстративная композиция и лекарство, включающее хондроинтиназу и сывороточный альбумин или желатин. Такую композицию можно приготовить, получая водный раствор, содержащий добавки, описанные ниже, и имеющий нужный pH; смешивая этот раствор с очищенной хондроитиназой со специфической активностью, например 300 ед./мг или более, получая водный раствор, содержащий 5 ед. /мл или более (предпочтительно 10-1000 ед./мл) очищенной хондроитиназы; обычно фильтруя раствор, стерилизуя и получая жидкую композицию. Затем эту жидкую композицию можно перевести в сухую композицию, предпочтительно лиофилизированную композицию путем сушки при отсутствии нагревания (лиофилизацией или подобным образом). По-другому, жидкую композицию можно заморозить при температуре от -20oC до -80oC.
Основными добавками, смешиваемыми с очищенной хондроитиназой в композициях настоящего изобретения, являются белки, такие как сывороточный альбумин или желатин. Их можно применять вместе.
Для примера приводим сывороточный альбумин млекопитающих, например человека, кошки, лошади, свиньи, овцы, козы и др. Человеческий сывороточный альбумин, применимый для парентерального применения, является предпочтительным, когда композицию используют для инъекций человеку. Например, можно использовать человеческий сывороточный альбумин, полученный из плазмы здоровых людей, в качестве сырого материала, фракционировать его и очистить методом фракционирования с применением этанола (Cohn's ethanol fractionation method). Особенно предпочтительным является сывороточный альбумин, обработанный при нагревании, предпочтительно при 60oC в течение примерно 10 часов, для дезактивации вируса гепатита и подобных. HSA может содержать натрий-N-ацетилтриптофан и/или каприлат натрия, добавленные к нему в качестве стабилизаторов.
В качестве примера желатина можно привести желатин, полученный из таких животных как кошки и свиньи. В частности, используемый здесь желатин получен соответствующей обработкой коллагена, выделенного из кожи, костей и др. частей животных, для придания ему растворимости. Такой желатин включает желатин, обработанный кислотой (А-тип), который обрабатывают минеральными кислотами (pH 1-3, например, соляной кислотой, серной кислотой, сернистой кислотой, фосфорной кислотой и др.) и который имеет изоэлектрическую точку 7,0-9,0; и желатин, обработанный щелочью (B-тип), который обработан щелочами (например, известью и др.) и имеет изоэлектрическую точку 4,5-5,0. Желатин, обработанный кислотой, предпочтительнее для использования в настоящем изобретении. В качестве примеров обработанного кислотой желатина приводим коммерческий продукт Nippi желатин высокого качества (тип A) и подобные.
В композициях настоящего изобретения обычно регулирует pH от 5 до 9, предпочтительно от 6 до 8, если композиция является раствором. Для этой цели композиция обычно содержит буферный агент, который поддерживает величину pH в этом диапазоне. Не существует специфических ограничений по типу буферных агентов, используемых в настоящем изобретении, до тех пор, пока они пригодны физиологически. Примеры таких буферных агентов включают препараты с одним или более соединениями, выбранными из группы, состоящей из соляной кислоты, гидроокиси натрия, карбоната натрия, гидрокарбоната натрия, фосфорной кислоты, дигидрофосфата калия, гидрофосфата калия, дигидрофосфата натрия, гидрофосфата натрия, аминоуксусной кислоты, бензоата натрия, лимонной кислоты, винной кислоты, тартрата натрия, молочной кислоты, тактата натрия, этаноламина, аргинина и этилендиамина. Особенно предпочтительным является фосфатный буфер. Если pH меньше 5 или больше 9, хондроитиназа может дезактивироваться или могут образоваться нерастворимые вещества в растворе. Хотя действие хондроитиназы на белок регистрируют уже при его содержании от 0,001 доли от веса белка хондроитиназы и выше, предпочтительным количеством является 0,01 - 500-кратное количество по весу и в частности от 0,05 до 100 весовых частей. Даже если количество превышает 500-кратное весовое содержание, можно ожидать действия настоящего изобретения, но активность фермента на единицу веса уменьшена при таком большом количестве. Концентрация буферного агента в композиции составляет 1-100 мМ, предпочтительно 10-50 мМ. В дополнение к этим добавкам композиция настоящего изобретения может содержать обычно применяемые добавки к фармацевтическим композициям, такие как изотонизирующие агенты, наполнители, консерванты, успокаивающие агенты и подобные. Например, не существует ограничений наполнителей до тех пор, пока их используют обычным образом в препаратах для инъекций, предпочтительными примерами являются креатинин, лактоза, маннит, очищенная сахароза, ксилоза и подобные.
Композиции настоящего изобретения обычно используют в качестве препаратов для инъекций или сырых материалов для препаратов для инъекций, содержащих хондроитиназу в качестве эффективного компонента. Композиции растворов заливают в такие емкости, как ампулы или пробирки, распространяют или хранят и используют в качестве препаратов для инъекций в том виде, в каком они есть. Можно высушивать или замораживать композиции растворов в подходящих для распространения и хранения контейнерах. Такие сухие или замороженные композиции растворяют в дистиллированной воде для инъекций, физиологическом растворе или подобном или разжижают перед употреблением. Эти препараты для инъекций можно использовать в качестве агентов, содержащих хондроитиназу, как эффективный компонент при лечении дисковой грыжи. Такой медицинский препарат можно применять в методе растворения межпозвоночных дисков, когда диск с образовавшейся грыжей растворяют, делая инъекции в межпозвоночное дисковое пространство пациента. Хотя обычно дозу нельзя точно установить и ее изменяют в зависимости от симптомов, возраста и других обстоятельств, обычным количеством является 10-300 ед.м. на дозу для случаев применения хондроитиназы ABC.
К иллюстративным композициям и лекарственным препаратам настоящего изобретения, содержащим хондроитиназу и неионное поверхностно-активное вещество, нужно подмешивать к хондроитиназе в данных композициях такие добавки, как неионные поверхностно-активные вещества и буферные агенты. Предпочтительные неионные поверхностно-активные вещества, которые можно добавить, включают эфиры жирных кислот и полиоксиэтиленсорбитана (полисорбаты), соединение полиоксиэтилена и гидрированного касторового масла, эфиры жирных кислот и сахарозы, полиоксиэтиленполиоксипропиленгликоль и подобное. В качестве примером эфиров жирных кислот и полиоксиэтиленсорбитана приводим полиоксиэтиленсорбитан (степень полимеризации около 20) монолаурат, монопальмитат, моноолеат, моностеарат, триолеат и подобные. Из коммерческих продуктов назовем Polysorbate 80 (Tween 80) (полиоксиэтилен) (20) сорбитаминоолеат), Polysorbate 60 (полиоксиэтилен (20) сорбитаминомоностеарат), Polysorbate 40, Twee 21, 81, 65, 85 и подобные. В качестве примеров соединения полиоксиэтилена и гидрированного касторового масла даем коммерческие продукты HCO-10, HCO-50, HCO-60 и подобные. В качестве эфиров жирных кислот и сахарозы представляем коммерческие продукты эфир DKF-160 и подобные. Pluronic F-68 и подобные даны в качестве примеров коммерческого полиоксиэтиленполиоксипропиленгликоля.
В качестве буферных агентов можно применять физиологически пригодные буферные агенты. Упомянутые буферные агенты можно применять для композиций такого типа также с фосфатным буфером, например, особенно предпочтительными являются натриевый фосфатный буферный раствор и калиевый фосфатный буферный раствор. В жидких фармацевтических композициях этого типа регулируют pH от 5 до 9, предпочтительно от 6 до 8, добавляя буферный раствор. Когда pH меньше 5 или больше 9, можно дезактивировать хондроитиназу или в растворе могут образоваться нерастворимые продукты.
Что касается количество этих включенных добавок, хотя количество 0,06 весовых долей неионного поверхностно-активного вещества или более относительно количества хондроитиназы демонстрирует регистрируемый эффект, предпочтительным является количество 0,6 - 300-кратное. Концентрация буферного агента в композиции растворов составляет 1 мМ или более, предпочтительно от 10 до 50 мМ.
Этот тип композиции можно преобразовать в конечный продукт после добавки упомянутых выше соединений, таких как изотонизирующие агенты, наполнители, консерванты, успокаивающие агенты и подобное. Полученные таким образом препараты можно использовать в качестве лекарственных препаратов в случае смещения межпозвоночных дисков таким же образом, как описано выше; указанные препараты могут давать растворы, которые предупреждают адсорбцию хондрооитиназы на стенках контейнеров и образование нерастворимых веществ от механических воздействий.
Суммируем эффекты настоящего изобретения. Так как очищенная хондроитиназа ABC настоящего изобретения имеет очень высокую чистоту и не содержит существенного количества протеазы, нуклеиновых кислот и эндотоксина, она является предельно полезной как лекарство и реагент для использования в исследованиях и экспериментах.
Так как, очищенная хондроитиназа ABC настоящего изобретения имеет превосходную стабильность при хранении, ее активность лишь слегка теряется, когда ее применяют в качестве лекарства. Ее высокая специфическая активность и минимальное содержание примесей делает возможным прием минимальной дозы и предотвращение побочных эффектов.
Что касается действия очищенной хондроитиназы ABC настоящего изобретения как реагента для экспериментов и исследований, она может промотировать репродуцируемость экспериментальных результатов при ее использовании для экспериментов с клетками животных, например, потому, что фермент не содержит эндотоксина и протеазы. Кроме того, исключение в соответствии с настоящим изобретением обычно необходимых стадий фракционирования сульфатом аммония и концентрирования/обессоливания из процесса очистки дает в результате уменьшение количества стадий и сокращение времени процесса, увеличение выхода и снижение стоимости продукции.
Другие характерные признаки изобретения будут видны из следующего описания типичных вариантов, которые приведены для иллюстрации изобретения, но не ограничивают его.
Пример 1. Proteus vulgaris (NCTC 4636, ATCC 6896, 1ГО 3988) культивируют обычным способом (J. Biol. Chem. 243, (7), 1523-1535 (1968)) для получения культивированных увлажненных клеток. К 200 г клеток добавляют 60 мл 5 мМ фосфатного буферного раствора (pH 6,5-7,0), получая суспензию. Клетки размельчают, используя DYNO® MILL, и центрифугируют, получая раствор экстракта, содержащий фермент (стадия 1).
Для удаления нуклеиновой кислоты из раствора экстракта клеток применяют протаминсульфат. 5%-ный водный раствор протаминсульфата добавляют к указанному раствору экстракта, содержащему фермент, до концентрации 0,5%. Смесь перемешивают при 4oC в течение 30 мин и образовавшийся осадок удаляют центрифугированием, получая таким образом супернатант (стадия 2).
После добавки 5-кратного (по объему) количества воды супернатант очищают методом колоночной хроматографии. Конкретно, колонку, заполненную CM-Sepharose, уравновешивают 5 мМ раствором фосфатного буфера (pH 6,5-7,0), затем в колонку заливают супернатант для абсорбции фермента. Колонку промывают тем же буферным раствором, потом тем же буферным раствором, содержащим 0,025 M NaCl, и потом элюируют тем же буферным раствором, содержащим 0,1 M NaCl, получая проявление активности фермента по фракциям (стадия 3).
После добавки примерно 5-кратного (по объему) количества воды фракции с ферментативной активностью абсорбируют при движении на колонке с S-Sepharose, уравновешенной 5 мМ раствором фосфатного буфера (pH 6,5-7,0). Колонку промывают тем же буферным раствором, содержащим 0,025 M NaCl, затем проводят градиентное элюирование тем же буферным раствором, содержащим линейный градиент концентрации от 0,025 до 0,35 M NaCl, получая проявление ферментативной активности по фракциям. Элюированный раствор хондроитиназы ABC дает одну полосу (SDS-PAGE) в отсутствие нуклеиновой кислоты (ДНК), протеазы и др. и имеет специфическую активность 380 ед./мг, которая примерно в три раза выше специфической активности хондроитиназы ABC, полученной обычным способом. Таким образом, получают хондроитиназу ABC, фермент высокой чистоты.
К раствору фермента (фосфатный буферный раствор, pH 7,0) добавляют полиэтиленгликоль (молекулярный вес 4000) таким образом, чтобы получить концентрацию 15%, и смесь оставляют стоять при комнатной температуре примерно в течение одной недели, получая белые или бесцветные иглообразные или призматические кристаллы хондроитиназы ABC. Микрофотография (увеличение: 2,5) кристаллов приведена на фиг. 1.
Кристаллы имеют ромбическое или моноклинное строение, иглообразные с параметрами кристаллической решетки, определенными методом рентгеноструктурного анализа (см. таблицу 2a).
Результаты SDS-PAGE на каждой стадии очистки приведены на фиг. 7. SDS-PAGE анализ проводят в соответствии с обычным методом (Laemmli U.K., Nature 227, 680-685 (1970)), применяя 10% гель.
Видим одну чистую полосу в обоих случаях, для невосстановленного и восстановленного состояний, когда фермент обработан S-Sepharose (см. фиг. 7; C и D).
Степень очистки хондроитиназы ABC на каждой стадии процесса настоящего изобретения показана в таблице 3.
Содержание эндотоксина и остаточные количества протеазы приведены в таблице 4.
В растворе фермента, полученном на стадии 4, не содержится существенного количества эндотоксина. Имеются только его следы; 5,0 пг/100 ед., как показано в таблице 4. Также в результате определения нуклеиновых кислот (ДНК) пороговым методом (прибор для определения ДНК, Threshold 0 торговая марка, производство Molecular Device Co.) не обнаружено ДНК, то есть содержание ДНК ниже порога чувствительности.
Таблица 5 показывает стабильность хондроитиназы ABC, полученной на 4 стадии настоящего изобретения, когда раствор фермента хранят при разных температурах. В таблице приведена стабильность, выраженная % активности относительно активности препарата при -40oC (100%); раствор с активностью 380 ед./мл хранили в течение 5 дней.
Пример 2. 7,5 кг увлажненных клеток Proteus vulgaris (NCTC 4636, АТСС 6896, 1ГО 3988), используемых в примере 1, загружают в резервуар, содержащий около 15 л 40 мМ раствора фосфатного буфера (pH 7,0 ± 0,5), к которому добавляют 10% лаурилового эфира полиоксиэтилена (POELE; Nikkol BL-9EX) и около 7,5 л очищенной воды. Смесь перемешивают, получая суспензию клеток, которую нагревают при 35 + 3oC и перемешивают около двух часов при этой температуре. Примерно через два часа добавляют около 30 л 20 мМ раствора фосфатного буфера (pH 7,0 ± 0,5), разбавляя суспензию. Затем суспензию охлаждают до 20oC. Суспензию центрифугируют на менее быстрой центрифуге, получая супернатант. Температуру раствора поддерживают ниже 20oC до и после центрифугирования.
Полученный таким образом суспернатант разбавляют, добавляя около 30 л очищенной воды, охлажденной до 2 - 15oC, и пропускают через колонку с СМ-Sepharose (количество геля: около 5 л) для адсорбции хондроитиназы ABC на колонке.
Колонку промывают 1 л очищенной воды, 10 л 0,5% водного раствора POELE и 5 л 0,04 М раствора фосфатного буфера (pH 6,2 ± 0,2). Затем проводят градиентное элюирование 20 л 0,04 М раствора фосфатного буфера (pH 6,2 ± 0,2), содержащего градиент концентраций от 0 до 0,25 М NaCl, получая проявление активности хондроитиназы ABC по стадиям. Элюат пропускают через стерилизующий фильтр с размером пор 0,22μм и собирают в стерилизованный контейнер, получая, таким образом, раствор хондроитиназы ABC.
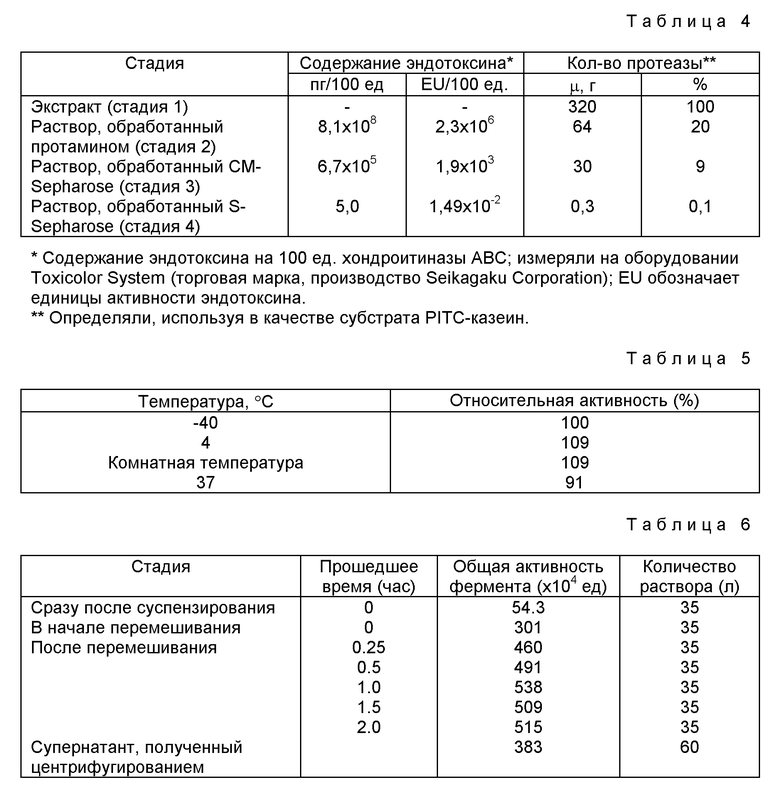
Соотношение между временем экстракции клеток (час) и активностью фермента показано в таблице 6.
Концентрация фермента уравновешивается в течение 1 - 2 часов после начала экстракции клеток.
Общее количество нуклеиновой кислоты в экстракте достигает максимального значения (около 25 г) через 0,25 часа после начала перемешивания, затем уменьшается и уравновешивается (около 2-3 г) примерно через один час.
Пример 3. 5 г увлажненных клеток Proteus vulgaris (NCTC 4636, АТСС 6896, 1ГО 3988), используемых в примере 1, загружают в 5-кратный объем 20 мМ раствора фосфатного буфера (pH 7,0), к которому добавляют 5% POELE, и экстрагируют в течение 3 часов при 37oC. Экстракт обрабатывают протамином, хроматографируют на СМ-Sepharose и S-Sepharose таким же образом, как в примере 1 (условия разделения представлены в таблице 7), и проводят градиентное элюирование, получая хондроитиназу ABC. Раствор дает одну полосу хондроитиназы ABC в SDS-PAGE. Раствор пропускают через стерилизующий фильтр с размерами пор 0,22μ,м, закачивая помпой, и собирают в стерилизованный контейнер, получая, таким образом, раствор хондроитиназы ABC.
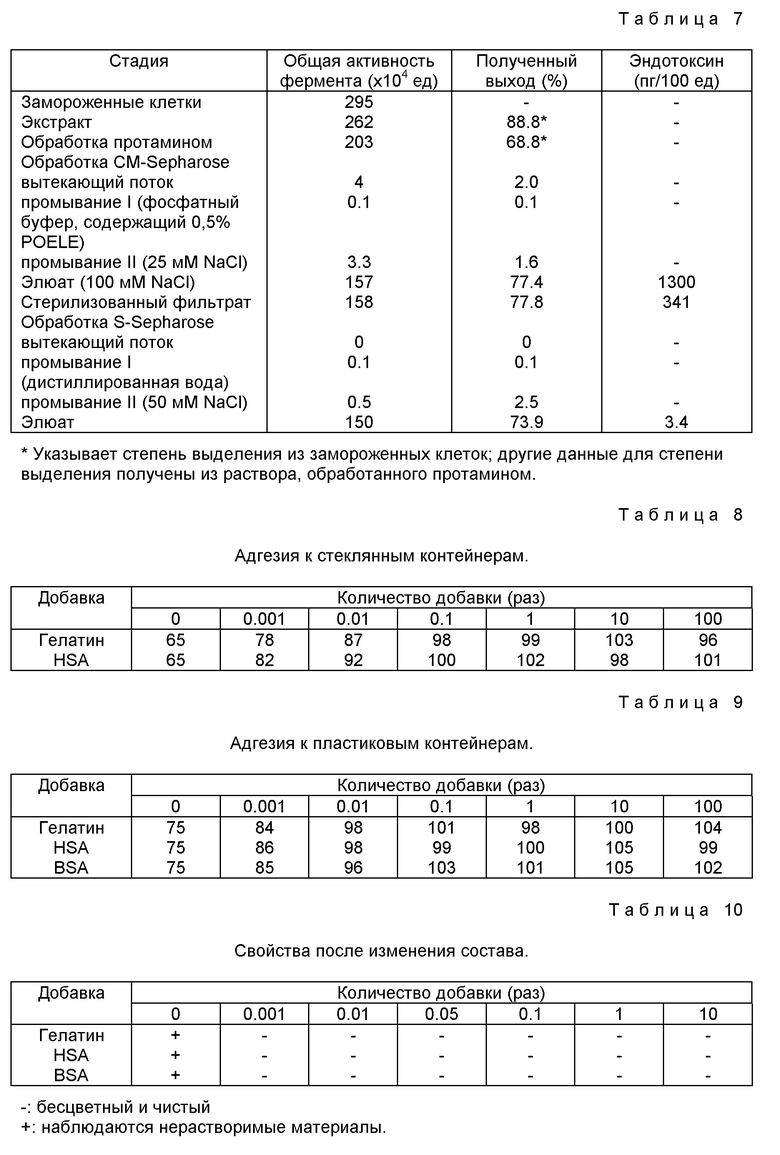
Данные расчетов, приведенные в таблице 7, показывают экстракцию хондроитиназы ABC около 500 ед. на 1 г клеток. Степень очистки на каждой стадии примера 3 приведена в таблице 7.
Соотношение между временем, необходимым для выделения хондроитиназы ABC их клеток, и активностью хондроитиназы ABC показано на фиг. 4.
Пример 4. Таким же способом, как описано в примере 3, готовят суспензию, применяя POELE, и добавляют Triton X-100, Brij-35, Nonidet P-40, получая концентрацию 2-5%. Экстракцию хондроитиназы проводят при 25-37oC. Результаты, представленные на фиг. 9 - 12, показывают, что в случаях, когда экстракцию проводят при 37oC и используют концентрацию поверхностно-активного вещества 5%, получают экстракты с большей активностью и чистотой, которые устанавливаются в течение 2 - 4 часов.
Пример 5. Эффект предотвращения адгезии к стеклянным и пластиковым контейнерам (растворы).
Растворы композиции хондроитиназы ABC получают из 5 ед. хондроитиназы ABC, полученной в примере 1 (специфическая активность 300 ед./мг), очищенного желатина (желатин, обработанный кислотой), человеческого сывороточного альбумина (HSA) или бычьего сывороточного альбумина (BSA), каждый в количестве 0,001 - 100-кратном от содержания белка фермента, как показано в таблицах 8 и 9. pH доводят до 7,0, добавляя 50 мМ раствор калийфосфатного буфера. Эти растворы загружают в стеклянные или пластиковые (полипропилен) пробирки и хранят в течение 24 часов при 4oC, затем измеряют активность фермента в растворе для определения эффекта предотвращения адгезии к контейнерам. Результаты, выраженные % активности в растворах после хранения (по сравнению с величиной до хранения), приведены в таблице 8 (стеклянные пробирки) и таблице 9 (пластиковые пробирки).
Пример 6. Эффект предотвращения образования нерастворимых веществ и эффект сохранения активности при перестройке (лиофилизированные композиции).
Растворы композиции хондроитиназы ABC, полученные из 50 ед. хондроитиназы ABC (специфическая активность: 380 ед./мг), и материалы, указанные в таблицах 10 и 11, каждый в количестве 0,001 - 10-кратном по отношению к количеству белка фермента, как показано в таблицах 10 и 11. pH доводят до 6,5, добавляя 20 мМ раствор натрий-фосфатного буфера. После добавки креатинина (10 мг/мл) в качестве наполнителя, растворы заливают в пробирки и высушивают при замораживании, получая сухую композицию хондроитиназы ABC. Композицию хранят в пробирках при 40oC в течение одного месяца, наблюдая их свойства и не находя аномальностей, таких как изменение цвета, деформации и подобное. Для наблюдения их свойств при перестройке системы добавляют воду для инъекций и определяют активность для проверки эффекта сохранения активности в присутствии добавок. Результаты представлены в таблицах 10 и 11. Таблица 10 показывает результаты наблюдения невооруженным глазом присутствия или отсутствия нерастворимых материалов при изменении состава композиции, а таблица 11 показывает активность после хранения, выраженную в процентах от активности до хранения.
Аналогичным образом, как описано выше, готовят композиции (хондроитиназа ABC: 50 ед., специфическая активность: 380 ед./мг; HSA: 0,05-кратное количество от количества белка), к которой добавляют креатинин, для наблюдения свойств и определения активности после хранения. Установлено, что раствор бесцветный и чистый, а остаточная активность составляет 80%.
Приведенные выше экспериментальные результаты показывают, что добавка желатина, HSA или BSA к очищенной хондроитиназе и доведение pH раствора до значения, близкого к нейтральному, предотвращают адгезию очищенной хондроитиназы к контейнерам, делают раствор бесцветным и прозрачным после растворения и сохраняют активность фермента без понижения в течение хранения.
Эти эффекты особенно значительны, когда желатин, HSA или BSA используют в количестве 0,05 - 10-кратном содержанию белка в очищенной хондроитиназе. В этом случае особо предпочтительной композицией хондроитиназы ABC является такая, которую готовят, используя хондроитиназу ABC высокой чистоты, имеющую специфическую активность, вместе с желатином, HSA или BSA и раствором натрий-фосфатного буфера с pH 5 - 9 (предпочтительно 6 - 8), в котором они растворены, для получения раствора (10 - 50 мМ раствор натрий-фосфатного буфера), который затем лиофилизуют. Желательно, чтобы лиофилизованная композиция при растворении обеспечивала раствор с указанным выше значением pH.
Пример 7. Эффект предотвращения адгезии к стеклянным контейнерам.
Хондроитиназу ABC растворяют в 0,1 М водном растворе NaCl. К раствору добавляют Polysorbate 80 в количестве 0,075 - 75-кратном относительно количестве белка фермента (1,33 г или 13,3 г), затем добавляют раствор фосфатного буфера, доводя pH до 6,9. Этим раствором заполняют стеклянные ампулы, получая фармацевтические композиции. Ампулы хранят при 20oC в течение 20 часов, определяя затем их титр и проверяя наличие эффекта предотвращения адгезии к контейнерам. Результаты представлены в таблице 12.
Пример 8. Эффект предотвращения образования нерастворимых веществ при встряхивании.
Хондроитиназу ABC (40 ед.) растворяют в 0,1 М водном растворе NaCl. К раствору добавляют Polysorbate 80 в количестве 0,0075 - 7,5-кратном по отношению к содержанию белка фермента (133 μг), как показано в таблице 13, затем добавляют фосфатный буфер, доводя pH до 6,9. Этот раствор заливают в стеклянные ампулы. Ампулы встряхивают, используя инкубатор для встряхивания, с частотой 160 раз в минуту в течение 8 часов, наблюдая присутствие или отсутствие появления нерастворимых материалов. Результаты представлены в таблице 13.
Пример 9. Эффект предотвращения образования нерастворимых веществ при вибрациях в процессе транпортировки.
Хондроитиназу ABC (5 ед. ) растворяют в 0,1 М водном растворе NaCl. К раствору добавляют Polysorbate 80 в количестве 0,06 - 6,0-кратном относительно белка фермента (16,7 μг), затем доводят pH до 6,9, добавляя раствор фосфатного буфера. Этим раствором заполняют стеклянные ампулы. Ампулы транспортируют в грузовом автомобиле при температуре ниже 25oC в течение 7 дней, наблюдая присутствие или отсутствие образовавшихся нерастворимых материалов. Результаты приведены в таблице 14.
Пример 10. Эффект предотвращения образования нерастворимых материалов при вибрациях в процессе транспортировки.
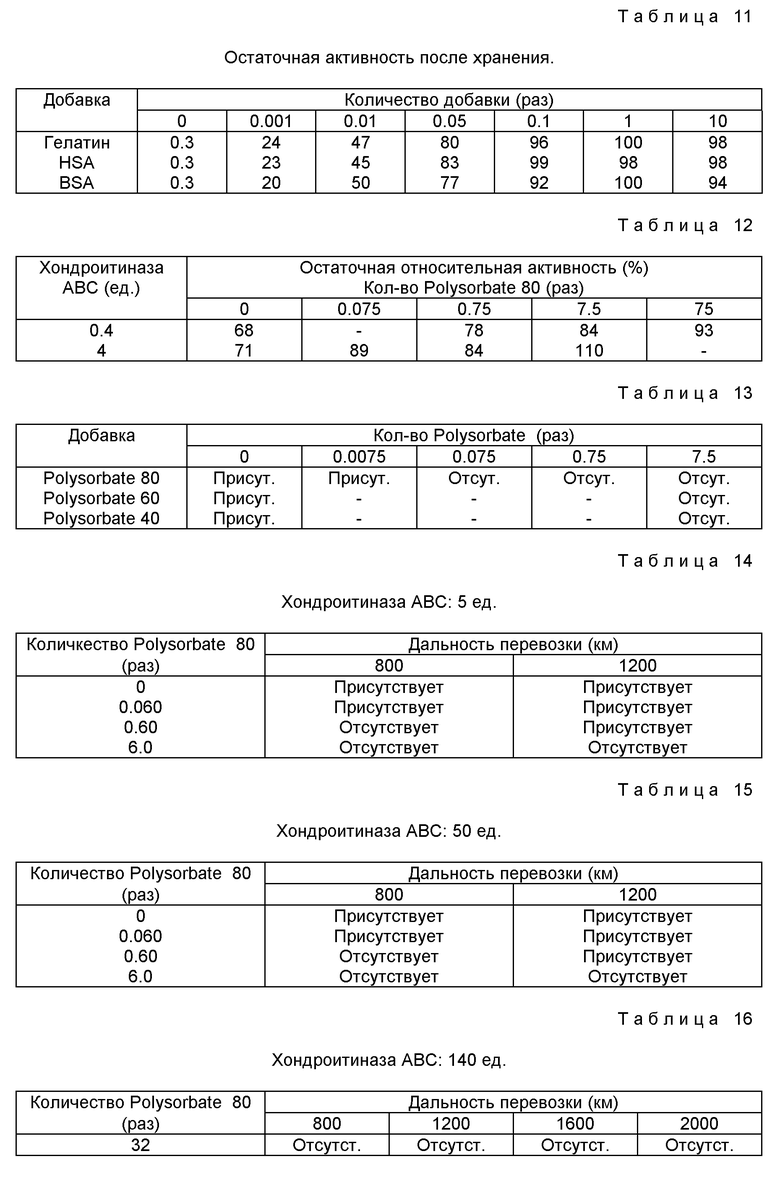
Хондроитиназу ABC (50 ед.) растворяют в 0,1 М водном растворе NaCl. К раствору добавляют Polysorbate 80 в количестве 0,006 - 0,60-кратном по отношению к количеству белка фермента (167 мкг), затем доводят pH до 6,9, добавляя раствор фосфатного буфера. Этим раствором заполняют стеклянные ампулы. Ампулы транспортируют в грузовом автомобиле при температуре ниже 25oC в течение 7 дней, наблюдая присутствие или отсутствие образовавшихся нерастворимых материалов. Результаты приведены в таблице 15.
Пример 11. Эффект предотвращения образования нерастворимых материалов при вибрациях в процессе транспортировки.
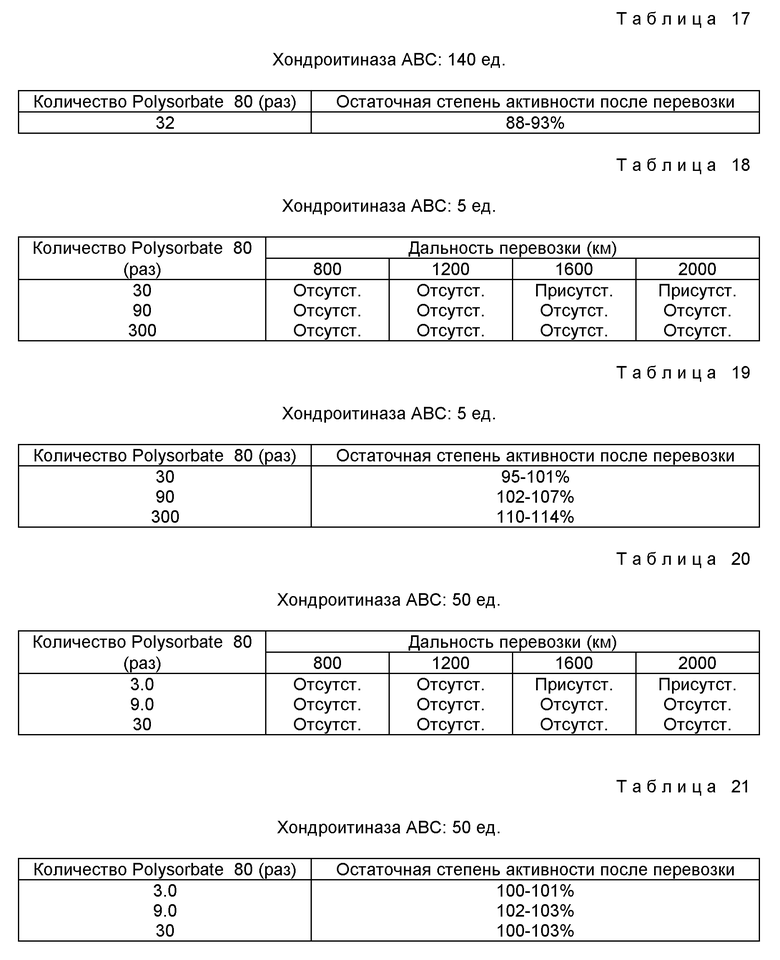
Хондроитиназу ABC (140 ед.) растворяют в 0,1 М водном растворе NaCl. К раствору добавляют Polysorbate 80 в количестве 32-кратном относительно количества белка фермента (467 μг), затем доводят pH до 6,9, добавляя раствор фосфатного буфера. Этим раствором заполняют стеклянные ампулы. Ампулы транспортируют в грузовом автомобиле при температуре ниже 22,6oC в течение 16 дней, наблюдая присутствие или отсутствие образовавшихся нерастворимых материалов. Затем измеряют титр и рассчитывают остаточную активность. Результаты приведены в таблицах 16 и 17.
Пример 12. Эффект предотвращения образования нерастворимых материалов при вибрациях в процессе транспортировки.
Хондроитиназу ABC (5 ед.) растворяют в 0,1 М водном растворе NaCl. К раствору добавляют Polysorbate 80 в количестве 30 - 300-кратном от количества белка фермента (16,7 μг), затем доводят pH до 6,9, добавляя раствор фосфатного буфера. Этим раствором заполняют стеклянные ампулы. Ампулы транспортируют в грузовом автомобиле при температуре ниже 11,7oC в течение 19 дней, наблюдая присутствие или отсутствие образовавшегося нерастворимого материала. Результаты приведены в таблицах 18 и 19.
Пример 13. Эффект предотвращения образования нерастворимых материалов при вибрациях в течение транспортировки.
Хондроитиназу ABC (50 ед.) растворяют в 0,1 М водном растворе NaCl. К раствору добавляют Polysorbate 80 в количестве 3,0 - 30-кратном от количества белка фермента (167 μг), затем доводят pH до 6,9, добавляя раствор фосфатного буфера. Этим раствором заполняют стеклянные ампулы. Ампулы транспортируют в грузовике при температуре ниже 11,7oC в течение 19 дней, наблюдая присутствие или отсутствие образовавшихся нерастворимых материалов. Затем определяют титр, рассчитывают остаточную степень активности. Результаты приведены в таблицах 20 и 21.
Пример 14. Хондроитиназу ABC (30 ед.) растворяют в 0,1 М водном растворе NaCl. К раствору добавляют Pluronic P68 в количестве 15-кратном от количества фермента (100 μг), затем доводят pH до 7, добавляя раствор фосфатного буфера. Этим раствором заполняют стеклянные ампулы, получая фармацевтическую композицию.
Хондроитиназу ABC (80 ед.) растворяют в 0,1 М водном растворе NaCl. К раствору добавляют HCO-60 в количестве 15-кратном от количества фермента (267 мкг ), затем доводят pH до 7, добавляя раствор фосфатного буфера. Этим раствором заполняют ампулы, получая фармацевтическую композицию.
Хондроитиназу ABC (30 ед.) растворяют в 0,1 М водном растворе NaCl. К раствору добавляют Polysorbate 80 в количестве 15-кратном от количества фермента (100 μг), затем доводят pH до 7, добавляя раствор фосфатного буфера. Этим раствором заполняют стеклянные ампулы, получая фармацевтическую композицию.
Хондроитиназу ABC (60 ед.) растворяют в 0,1 М водном растворе NaCl. К раствору добавляют Polysorbate 80 и Pluronic P68, каждый в количестве 7,5-кратном от количества фермента (200 μг), затем доводят pH до 7, добавляя раствор фосфатного буфера. Этим раствором заполняют стеклянные ампулы, получая фармацевтическую композицию.
Хондроитиназу ABC (50 ед.) растворяют в 0,1 М водном растворе NaCl. К раствору добавляют HCO-60 и К-эфир P-160, каждый в количестве 7,5-кратном от количества фермента (167 μг), затем доводят pH до 7, добавляя раствор фосфатного буфера. Этим раствором заполняют стеклянные ампулы, получая фармацевтическую композицию.
В свете приведенного выше описания очевидно, что возможны многочисленные модификации и вариации настоящего изобретения. Следовательно, должно быть ясно, что в рамках приложенной формулы изобретения его можно осуществить способом, отличным от описанных здесь конкретных способов.



Изобретение относится к области медицины и биотехнологии и касается фермента хондроитиназы, применяемой в химико-фармацевтической промышленности, высокоочищенной хондроитиназы и способа получения фермента и фармацевтических композиций, содержащих фермент. Сущность изобретения включает фермент хондроитиназу АВС из клеток Proteus vulgaris с молекулярным весом 100000, изоэлектрической точкой 8,3-8,5, аланин в качестве N-концевой аминокислоты и пролин в качестве С-концевой аминокислоты. Способ получения включает экстракцию клеток указанного микроорганизма, удаление нуклеиновой кислоты, а также хроматографию с использованием сильной и слабой катионообменных смол. Очищенный фермент хондроитиназы АВС представляет собой иглообразные и призматические кристаллы с определенной структурой кристаллической решетки. Фармацевтические композиции представляют собой очищенный фермент и дополнительно неионный ПАВ, а также стабилизаторы. Технический результат заключается в повышении степени очистки и стабильности препарата. 6 с. и 14 з.п. ф-лы, 21 табл., 12 ил.
Ромбическая система:
пространственная группа: P2221;
параметры кристаллической решетки:
a = 214 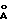 ; b = 92
; b = 92 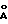 ; c = 56
; c = 56 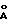 ; α 90o; β 90o; γ 90o.
; α 90o; β 90o; γ 90o.
Моноклинная система:
пространственная группа: P21;
параметры кристаллической решетки:
a = 214 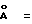 ; b = 56
; b = 56 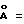 ; c = 92
; c = 92 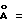 ; α = 90o; β = 90o; γ = 90o.
; α = 90o; β = 90o; γ = 90o.
Приоритет по пунктам:
26.06.92 - по пп.1 - 6, 8 - 9;
26.10.92 - по пп.11 - 17, 19 - 20;
25.06.93 - по пп.10 и 18.
| US 4696816 А, 1987 | |||
| Способ лечения поясничного остеохондроза | 1973 |
|
SU506417A1 |
| J | |||
| Biol | |||
| Chem | |||
| V | |||
| Вагонетка для кабельной висячей дороги, переносной радиально вокруг центральной опоры | 1920 |
|
SU243A1 |
| Приспособление для перевода стрелок с вагона | 1924 |
|
SU1523A1 |
Авторы
Даты
2000-01-27—Публикация
1993-06-25—Подача