Область изобретения
Изобретение относится к фотодимеризуемому производному коричной кислоты, фотосшиваемому производному коричная кислота - полимер и к сшитому производному коричная кислота - полимер. Указанные выше производное коричной кислоты и производное коричной кислоты и полимера, образующееся при введении вышеуказанного производного коричной кислоты в полимер-хозяин, являются соединениями с высокой реакционной способностью. Следовательно, при воздействии ультрафиолетового излучения производное коричной кислоты подвергается внутримолекулярной сшивке (реакция фотодимеризации) с образованием циклобутанового кольца, обеспечивая таким образом образование нерастворимого производного коричной кислоты и полимера из вышеуказанного производного коричная кислота/полимер. Когда в качестве указанного выше полимера-хозяина выбирается глюкозаминогликан, то получаемое в конечном итоге фотосшитое полимерное производное коричной кислоты может быть использовано в качестве медицинского материала, обладающего биосовместимостью, биопоглощением и другими необходимыми свойствами.
Предпосылки изобретения
Хотя в настоящее время известно большое число фотодимеризуемых соединений, имеется совсем немного информации по введению фотосшивающих групп в водорастворимый полимер-хозяин. Известна технология, по которой различные фотосшитые изделия получают путем введения стильбазоний-производных в водорастворимый полимер поливинилового спирта (JP-B-Sho-56-5762, JP-B-Sho-56-54155 и JP-B-Sho-61-12888, где сокращение "JP-B" означает рассмотренную и опубликованную японскую патентную заявку), но объектом такой технологии является иммобилизация ферментов и бактерий, и, более того, полимер-хозяин, в который вводятся фотосшивающие группы, представляет собой полимер, полученный химическим путем. В этих случаях для обеспечения хорошей фотореакционной способности соединения, подвергающиеся фотодимеризации, структурно модифицируют таким образом, чтобы вызвать изменения в УФ-поглощении и чувствительности. В JP-A-Hei-6-73102 описывается технология, по которой коричную кислоту вводят в природный полимер глюкозаминогликан и получаемое производное подвергают сшивке посредством УФ-облучения (сокращение "JP-A" означает нерассмотренную опубликованную японскую патентную заявку). Хотя эта заявка предшествует настоящему изобретению, большое число приведенных в ней примеров относится к получению фотосшитого глюкозаминогликанового комплекса путем прямого введения коричной кислоты за счет эфирной связи с гидроксильной группой глюкозаминогликана без использования спейсерной группы и последующем воздействии на комплекс ультрафиолетового излучения с образованием фотосшитого конечного продукта. Эта технология имеет недостаток, заключающийся в том, что коричная кислота должна быть введена с высокой степенью замещения (CЗ = 100 • (число молей коричной кислоты на фрагмент дисахарида)) для того, чтобы последующая фотосшивка имела достаточную степень, при этом эффективность фотореакции невысока.
В той же патентной заявке также присутствуют примеры, в которых коричная кислота вводится по карбоксильной группе глюкозаминогликана с использованием диамина в качестве спейсера, но описанный метод не имеет удовлетворительной селективности с точки зрения реакции замещения коричной кислотой.
Краткое описание изобретения
Первым объектом настоящего изобретения является получение фотодимеризуемого производного коричной кислоты, содержащего спейсер, введенный в молекулу коричной кислоты.
Вторым объектом настоящего изобретения является получение производного коричной кислоты и полимера, которое подвергается фотодимеризации с высокой селективностью и с большой эффективностью, за счет введения вышеуказанного производного коричной кислоты в полимер-хозяин, такой как глюкозаминогликан, и при фотосшивке указанного производного коричной кислоты и полимера может быть получено сшитое производное коричная кислота - полимер.
В результате интенсивных исследований авторы настоящего изобретения достигли успеха в осуществлении указанных целей за счет следующих открытий.
1. Производное коричной кислоты любой из следующих общих формул (1) - (3) или его соль:
R1 - A - H, (1)
R1 - B - OH, (2)
R2 - C -H, (3)
где заместитель R1 представляет собой группу формулы (4):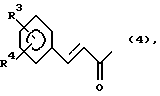
где заместители R3 и R4 независимо друг от друга представляют собой атом водорода,
заместитель R2 представляет собой группу формулы (5):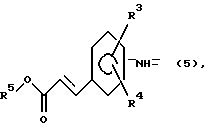
где заместители R3 и R4 принимают значения, определенные выше, а заместитель R5 представляет собой низшую алкильную группу;
фрагмент A - H представляет собой внутримолекулярный остаток амино- и гидрокси-содержащего соединения любой из формул (6) - (9):
-O-(CH2)n-NH2, (6)
где n представляет собой целое число 3-18,
-O-(CH2CH2)m-NH2, (7)
где m представляет собой целое число 2-10,
-O-CHR6CH(COOR7)-NH2, (8)
где заместитель R6 представляет собой атом водорода или низший алкил, заместитель R7 представляет собой низшую алкильную группу,
-O-(CH2)1-NHCO-CHR8NH2, (9)
где 1 представляет собой целое число 2 - 18, а заместитель R8 представляет собой боковую цепочку остатка α - аминокислоты и выбран из водорода и низшего алкила;
фрагмент B - OH представляет собой аминокислотный остаток формулы (10):
-NH-(CH2)k-COOH, (10)
где k представляет собой целое число 1-18,
фрагмент C - H представляет собой аминокислотный остаток формулы (11) или (12):
-CO-(CH2)k-NH2, (11)
где k принимает значения, определенные выше,
-(COCHR9NH)i-H, (12)
где i представляет собой целое число 1-6, заместитель R9 представляет атом водорода.
2. Производное коричная кислота - полимер любой из формул (13) - (15):
R1 - A - P1, (13)
R1 - B - P2, (14)
R2 - C - P1, (15)
где заместитель R1 представляет собой группу формулы (4):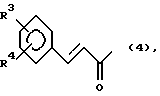
где заместители R3 и R4 независимо друг от друга представляют собой атом водорода, нитро-, амино-, гидрокси- или C1-4-алкокси-группы,
заместитель R2 представляет собой группу формулы (5):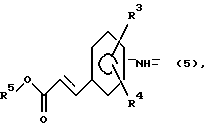
где заместители R3 и R4 принимают значения, определенные выше, а заместитель R5 представляет собой низшую алкильную группу;
фрагмент A представляет собой остаток соединения, содержащего амино- и гидрокси-содержащего любой из формул (6') - (9'):
-O-(CH2)n-NH, (6')
где n представляет собой целое число 3-18,
-O-(CH2CH2)m-NH, (7')
где m представляет собой целое число 2-10,
-O-CHR6CH(COOR7)-NH, (8')
где заместитель R6 представляет собой атом водорода или низший алкил, заместитель R7 представляет собой низший алкил,
-O-(CH2)l-HNCO-CHR8-NH, (9')
где l представляет собой целое число 2-18, а заместитель R8 представляет собой боковую цепочку остатка α-аминокислоты и выбран из водорода и низшего алкила;
фрагмент B - представляет собой аминокислотный остаток формулы (10'):
-NH-(CH2)k-CO, (10')
где k представляет собой целое число 1-18;
фрагмент C - представляет собой аминокислотный остаток формулы (11') или (12'):
-NH-(CH2)k-NH, (11')
где k принимает значения, определенные выше,
-(COCHR9NH)i, (12')
где i представляет собой целое число 1-6, заместитель R9 представляет собой атом водорода;
заместитель Р1 представляет собой полисахаридный остаток, содержащий карбоксильную группу; заместитель Р2 представляет собой полисахаридный остаток, содержащий амино- или гидрокси-группу;
связь A - P1 представляет собой амидную связь, образованную между концевой амино-группой формул (6'), (7'), (8') или (9') и карбоксильной группой заместителя P1;
связь B - P2 представляет собой амидную или сложноэфирную связь, образованную между концевой карбоксильной группой формулы (10') и или амино-группой, или гидроксильной группой заместителя P2; и
связь C - P1 представляет собой амидную связь, образованную концевой амино-группой формулы (11') или (12') и карбоксильной группой заместителя P1.
3. Производное коричной кислоты и полисахарида (2), где заместители P1 и P2 независимо друг от друга представляют собой полисахарид.
4. Производное коричной кислоты и полисахарида (3), где полисахарид представляет собой глюкозаминогликан.
5. Производное коричной кислоты и полисахарида (4), где глюкозаминогликан выбирается из группы, включающей гиалуроновую кислоту, хондроитин-сульфат, хондроитин, гепарин, гепарин-сульфат и кератан-сульфат.
Краткое описание фигур
На фиг. 1 схематично представлена иллюстрация реакции внутримолекулярной фотосшивки производного коричной кислоты.
На фиг. 2 в графической форме представлены данные, полученные в примере 51, показывающие влияние числа атомов углерода в спейсере на реакционную способность.
На фиг. 3 в графическом виде представлены данные, полученные в примере 52, которые показывают соотношение между скоростью абсорбции воды и степенью замещения.
На фиг. 4 в графическом виде представлены данные, полученные в примере 53, показывающие соотношение между пределом прочности при растяжении и степенью замещения.
На фиг. 5 в графическом виде представлены данные, полученные в примере 53, показывающие зависимость между пределом прочности при растяжении и скоростью абсорбции воды.
На фиг. 6 в графическом виде представлены данные, полученные в примере 54, которые показывают отношение обратной величины предела прочности при растяжении к скорости абсорбции воды.
На фиг. 7 в графическом виде представлены данные, полученные в примере 55, показывающие критическую точку перехода в нерастворимую форму.
На фиг. 8 в графическом виде представлены данные, полученные в примере 56, которые показывают относительную реакционную способность фрагмента спейсера, отличного от метиленовой цепочки.
На фиг. 9 в графическом виде показаны данные, полученные в примере 57, показывающие соотношение между степенью замещения и скоростью поглощения воды различных спейсерных структур, отличных от метиленовой цепочки.
Подробное описание изобретения
Известно, что фотодимеризуемые соединения на основе коричной кислоты и аминокоричной кислоты поглощают ультрафиолетовый цвет в определенном интервале полосе полос около 280 нм с димеризацией до труксиловой кислоты, труксиновой кислоты или их производных. Такая реакция фотодимеризации протекает только при определенном количестве ультрафиолетового излучения определенной длины волны и обычно не имеет места при обычном свете, например, при солнечном. Следовательно, фотосшитые изделия, получаемые при воздействии на циннамоилированное производное глюкозаминогликана УФ-излучения, а именно соединения, получаемого при введении молекулы коричной кислоты в функциональную группу глюкозаминогликана, обладают преимуществом, которое состоит в том, что они могут быть получены с помощью селективной реакции с использованием света и что с исходным материалом - циннамоилированным производным глюкозаминогликана - легко работать, так как при хранении он практически не чувствителен к солнечному излучению и дневному свету.
Однако для того, чтобы получить фотоотвержденное изделие с использованием циннамоилированного производного глюкозаминогликана, описанного ранее в JP-A-Hei-6-73102, например, гиалуроновой кислоты со средним молекулярным весом 800000 в качестве полимера-хозяина, необходимы введение 0,1-4 фрагментов (CЗ 10 - 400%) коричной кислоты на полисахаридный фрагмент и облучение комплекса ультрафиолетовым светом в течение не менее 30 минут.
Авторы настоящего изобретения установили, что введение гибкого спейсера между макромолекулой соединения-хозяина (например, глюкозаминогликана) и молекулой коричной кислоты приводит к заметному увеличению способности к фотоотверждению так, что реакция фотосшивки протекает удовлетворительно даже при пониженной степени замещения фотосшиваемыми группами.
Фотосшиваемое производное глюкозаминогликана, которое представляет собой производное коричной кислоты и полимера, содержащее производное коричной кислоты с такой спейсерной структурой, может подвергаться фотосшивке при пониженной степени замещения, при использовании в качестве указанного соединения-хозяина гиалуроновой кислоты со средним молекулярным весом 100000 - 5000000 из расчета приблизительно 0.0005 - 0.05 фрагментов на фрагмент дисахарида (CЗ 0.05 - 5%), и даже при времени воздействия УФ излучения менее приблизительно 1 - 8 минут.
Обычное производное коричной кислоты и полимера также подвергается фотосшивке при воздействии ультрафиолетового излучения с образованием огромных молекул, имеющих трехмерную структурную сетку за счет поперечно-сшитых групп, и этот продукт - сшитое производное коричная кислота - полимер - не растворяется в воде. Однако производное коричной кислоты и полимера (мономер) с полимером-хозяином, имеющим молекулярный вес в интервале 20 - 30 тысяч, при сшивке дает только грубую сетчатую структуру и не подходит для получения огромных молекул. Для повышения плотности сшивания и достижения необходимой степени нерастворимости большое значение имеет использование производного коричная кислота - полимер с довольно высокой степенью замещения (CЗ).
В соответствии с настоящим изобретением, где спейсер вводится в сшивающую группу, достигается значительное повышение способности к фотосшивке так, что даже при использовании мономера с молекулярным весом 20 - 30 тысяч может быть получена достаточная нерастворимость при уровне CЗ около 10% и ниже. Даже производное коричной кислоты и полимера с такой низкой CЗ подвергается сшивке в достаточной степени при кратковременном воздействии УФ-излучения благодаря высокой реакционной способности, а получаемое сшитое производное коричной кислоты и полимера не только не растворяется в воде, но и имеет высокую способность абсорбировать воду и высокие прочностные характеристики.
Производные коричной кислоты формул (1) - (3) далее описываются более подробно.
В формулах (1) - (3) фрагменты A - H, B - OH и C-H представляют собой остатки, содержащие названные выше спейсерные фрагменты.
В формуле (1) заместитель R1, представленный формулой (4), означает остаток коричной кислоты, содержащий виниленовую группу, способную фотодимеризоваться с образованием циклобутанового кольца, а заместители R3 и R4 представляют собой атом водорода.
Фрагмент A - H представляет собой остаток соединения, содержащего как амино-группу, так и гидрокси-группу, который представлен формулами (6) - (9) и который выполняет функцию спейсера.
-O-(CH2)n-NH2,
где n принимает целые значения 3-18, предпочтительно 4-8, и наиболее предпочтительно 5 или 6. Если n принимает значение 2 или меньше, то производное коричная кислота - полимер (формула (13)), получаемое при введении соединения формулы (1) в полимер-хозяин, будет обладать низкой эффективностью в реакции фотосшивки. Если n принимает значение 19 или выше, эффективность реакции введения соединения формулы (1) в полимер будет утрачена.
Остаток формулы (6), приведенной выше, является остатком аминоспирта, такого как аминоэтанол, аминопропанол, аминобутанол, аминопентанол, аминогексанол, аминооктанол или аминододеканол.
Когда фрагмент A - H представляет собой остаток формулы (6) и является остатком аминоспирта, производное коричной кислоты R1-A-H также может быть представлено формулой (1'-1)
H-NH-(C'R1R'2)nOCOCH-CHPh, (1'-1)
где каждый заместитель R'1 и R'2 представляет собой атом водорода, Ph представляет собой фенильную группу, которая может содержать один или несколько заместителей, таких как алкильная или алкокси-группа с 1 - 4 атомами водорода, амино-группа, гидрокси-группа или нитро-группа, n принимает значения, определенные для формулы (6).
Типичными примерами таких соединений являются 3-амино-пропиловый эфир коричной кислоты, 4-аминобутиловый эфир коричной кислоты, 5-аминопентиловый эфир коричной кислоты, 6-аминогексиловый эфир коричной кислоты, 8-аминооктиловый эфир коричной кислоты, 12-аминододециловый эфир коричной кислоты и др.
В формуле (1'-1) заместители R'1 и R'2 независимо друг от друга могут быть атомами водорода или низшими алкильными группами, предпочтительно содержащими от 1 до 4 атомов углерода.
-O-(CH2CH2)m-NH2, (7)
где m принимает целые значения 2-10, предпочтительно 2-5, наиболее предпочтительно 2 или 3. Если m принимает значение 1 или меньше, производное коричной кислоты и полимера будет обладать низкой продуктивностью в реакции фотосшивки, тогда как значения m = 11 или выше приводят к низкой эффективности реакции введения соединения формулы (1) в полимер-хозяин.
Остаток формулы (7), наряду с другими, представляет собой остаток полиэтиленгликольамина, такого как диэтиленгликольамин.
-O-CHR6CH(COOR7)-NH2, (8)
где заместитель R6 представляет собой атом водорода или низший алкил, предпочтительно H или метил, а заместитель R7 представляет собой низший алкил.
Остаток формулы (8), приведенный выше, является остатком низшего алкилового эфира гидроксиаминокислоты, такой как серин или треонин.
Когда A-H представляет собой остаток формулы (8), являющийся остатком гидрокси-аминокислоты, типичным примером производного коричной кислоты R1-A-H служит метиловый эфир O-циннамоилсерина, метиловый эфир O-циннамоилтреонина и др.
-О-(CH2)l-NHCO-CHR8-NH2, (9)
где l представляет собой целое число 2-18, предпочтительно 2-8, наиболее предпочтительно 2 или 3, а заместитель R8 представляет собой боковую цепочку остатка α-амино-кислоты и является предпочтительно атомом водорода, метилом или изопропилом.
Рассматривая указанную выше формулу (9), можно отметить, что остаток -CO-CHR8-NH2 представляет собой остаток глицина, аланина, лейцина и др., а остаток -О-(CH2)l-NH- представляет собой остаток аминоэтанола, аминопропанола и др.
Далее описывается производное коричной кислоты формулы (2).
Заместитель R1 принимает значения, определенные выше; остаток B-OH представляет собой остаток амино-кислоты формулы (10) и содержит спейсерный фрагмент, описанный выше.
-NH-(CH2)k-COOH, (10)
где k представляет собой целое число 1-18, предпочтительно 1-11, наиболее предпочтительно 3-5. Остаток формулы (10) представляет собой остаток амино-кислоты, такой как β- аланин (аминопропионовая кислота), аминомасляная кислота (аминобутановая кислота), аминокапроновая кислота (аминогексановая кислота), амино-лауриновая кислота (аминододекановая кислота) и так далее.
В формуле (3) заместитель R2 представляет собой остаток эфира аминокоричной кислоты, содержащей виниленовую группу, способную фотодимеризоваться с образованием циклобутанового кольца, необязательно содержащего заместитель или заместители, представленными заместителями R2 и R4, которые принимают значения, определенные выше, и каждый предпочтительно представляет собой атом водорода; заместитель R5 представляет собой низшую алкильную группу и предпочтительно представляет собой метил. Положения заместителей R3 или R4 в бензольном кольце не являются критическими, за исключением случаев, когда заместители могут взаимодействовать друг с другом или при наличии стерических затруднений.
Понятие "низшая алкильная группа", которое используется здесь, означает алкильную группу, содержащую от 1 до 4 атомов углерода.
Фрагмент C-H представляет собой остаток амино-кислоты формул (11) или (12), которая выделяет спейсерный фрагмент.
-NH-(CH2)k-NH2, (11)
где k принимает значения, определенные выше.
Остаток формулы (11), приведенной выше, может представлять собой остаток любой амино-кислоты, аналогичной аминокислотам, которые упоминались при описании остатка формулы (10).
Когда фрагмент C-H представляет собой остаток формулы (11) и является остатком амино-кислоты, производное коричной кислоты R2-C-H может быть также представлено формулой (2'-1-1):
H-A'-NH-Ph-CH=CHCOOR'3, (2'-1-1)
где заместитель R3 представляет собой алкильную группу, предпочтительно содержащую от 1 до 4 атомов углерода; фрагмент A' представляет собой -NH(CR'4R'5)h'CO, где заместители R'4 и R'5 представляют собой атом водорода, Ph представляет собой пара-фенильный остаток, который может содержать один или несколько заместителей, таких как низший алкил или алкокси-группа, содержащие от 1 до 4 атомов углерода, амино-группа, гидрокси-группа или нитро-группа, a h' представляет собой целое число от 1 до 12.
Типичными примерами таких соединений являются 4-(4-аминобутанамидо)коричной кислоты метиловый эфир, 4-(6-аминогексамидо)коричной кислоты метиловый эфир, 4-(12-аминододеканамидо)коричной кислоты метиловый эфир и др.
В формуле (2'-1-1) заместители R'4 и R'5 независимо друг от друга представляют собой атом водорода или низшую алкильную группу, предпочтительно содержащую от 1 до 4 атомов углерода.
-(COCHR9NH)i-H, (12)
где i представляет собой целое число 1-6, предпочтительно 2 - 4, и наиболее предпочтительно 2 или 3; заместитель R9 принимает значения, определенные выше, и предпочтительно представляет собой атом водорода.
Остаток формулы (12), приведенной выше, может быть остатком обычных амино-кислот или их олигомеров (например, глицина, глицилглицина, триглицина и др.).
Когда фрагмент C-H представляет собой остаток амино-кислоты формулы (12), производное коричной кислоты R2-C-H может быть также представлено формулой (2'-1-2):
H-A''-NH-Ph-CH-CHCOOR'3, (2'-1-2)
где A'' представляет собой -(NHCR'4R'5CO)m-, заместители R'3, R'4, R'5 и Ph принимают значения, определенные для формулы (2'-1-1), a m' представляет собой целое число от 1 до 6, предпочтительно от 1 до 3.
Типичными примерами таких соединений являются глициламинокоричной кислоты метиловый эфир, глицилглициламинокоричной кислоты метиловый эфир, триглициламинокоричной кислоты метиловый эфир и др.
В формуле (2'-1-2) заместители R'4 и R'5 независимо друг от друга могут представлять собой атом водорода или низшую алкильную группу, предпочтительно содержащую от 1 до 4 атомов углерода.
[1] Синтез производных коричной кислоты
Ниже описываются способы получения производных коричной кислоты формул (1) - (3).
[1-1] Производное коричной кислоты формулы (1) может быть получено описанным ниже способом.
Следует понимать, что в данном описании фрагмент, представленный формулой -A-H (1), для лучшего объяснения реакции иногда обозначается как -O-A1NH2.
Рассматриваемое соединение формулы (1) может быть получено при селективном взаимодействии карбоксильной группы производного коричной кислоты формулы R1-OH с гидроксильной группой соединения, содержащего как амино-группу, так и гидроксильную группу (H2N-A1-OH). Обычно для того, чтобы эта реакция проходила эффективно и селективно, захватывая только вышеуказанную гидроксильную группу, предпочтительно использовать последнее соединение с амино-группой, соответствующим образом защищенной (RaNH-A1-OH). Затем, по незащищенной гидроксильной группе этого соединения образуется эфирная связь. Получают соединение (1) с защищенной амино-группой Ra-NH-A1-OR1. Из этого соединения группа, защищающая амино-группу, снимается при соответствующих условиях с образованием названного соединения. Таким образом, названный эфир коричной кислоты, содержащий свободную амино-группу или амино-группу, образующую соль, может быть получен с хорошим выходом с помощью двух стадий - этерификации и снятия защитной группы.
Рассматриваемая схема реакции приведена ниже:
Ниже каждая стадия описана более подробно.
Первая стадия
Карбоксильная группа производного коричной кислоты, представленного формулой R1-OH, в начале переводится в активную форму (например, в галогенид коричной кислоты формулы R1-X, например, в циннамоилхлорид, коричный ангидрид (R1)2O или смешанный ангидрид R1-O-R'), а затем активированная карбоксильная группа реагирует с незащищенной гидроксильной группой соединения, содержащего как амино-группу, так и гидроксильную группу (H2N-A1OH) с образованием эфирной связи. Получают соединение (1), содержащее защищенную амино-группу, а именно RaNH-A1-O-R1. Эту реакцию предпочтительно проводят в присутствии катализатора ацилирования, такого как, например, N,N-диалкиламинопиридин (например, 4-диметиламинопиридин, 4-пирролидинопиридин и др.) и др. , и акцептора образующейся в качестве побочного продукта кислоты (например, третичного амина, такого как пиридин, триэтиламин и др., или неорганического основания, такого как гидрокарбонат натрия).
Группа, защищающая амино-группу, которая может быть использована на рассмотренной выше стадии, практически не имеет ограничений при том условии, что она легко снимается без разложения эфира коричной кислоты при проведении второй стадии снятия защиты.
Вторая стадия
Группа, защищающая амино-группу соединения (RaNH-A1-O-R1), полученного на первой стадии, снимается в условиях, при которых не происходит расщепления эфирной связи эфира коричной кислоты. В качестве групп, защищающих амино-группу, могут быть использованы наряду с другими трет.-бутоксикарбонильная, бензилоксикарбонильная и 9-флуоренилметоксикарбонильная группы. Если в качестве защитной группы используется такая группа, как трет.-бутоксикарбонильная, которая может быть снята с помощью кислоты, рассматриваемое соединение может быть обработано хлористым водородом, бромистым водородом, трифторуксусной кислотой и др. с одновременным удалением защитной группы и получением соответствующей соли.
Если рассматривать более подробно, то, например, гидрохлорид соединения формулы R1-A-H может быть получен следующим образом.
К соединению формулы (Boc-NH-A1-OH), с амино-группой, защищенной трет. -бутоксикарбонильной группой (Boc-), которая снимается кислотой, добавляют органический растворитель, например, хлороформ, а затем при охлаждении льдом добавляют органическое основание, такое как триэтиламин, галогенид кислоты R1-OH (R1-X) и основный катализатор (катализатор ацилирования), например, 4-диметиламинопиридин. После перемешивания при комнатной температуре смесь разбавляют органическим растворителем, таким как, например, этилацетат, и промывают несколькими порциями слабокислого водного раствора, воды, а затем несколькими порциями слабощелочного водного раствора, водой и насыщенным водным раствором хлористого натрия. Органический слой затем сушат безводным сульфатом натрия. Далее сульфат натрия отфильтровывают и фильтрат концентрируют в вакууме. Получают соединение (RaNH-A1-O-R1) (первая стадия). Для удаления защитной группы и одновременного превращения амина в гидрохлорид к полученному соединению (RaNH-A1-O-R1) при перемешивании и при охлаждении льдом добавляют раствор кислоты в органическом растворителе, например, 1 - 5 М раствор HCl/диоксан. Далее для кристаллизации добавляют органический растворитель, например, диэтиловый эфир, и отфильтровывают полученные кристаллы. Если необходимо, то собранные кристаллы промывают органическим растворителем и сушат в вакууме. Получают соединение (R1-A-H, гидрохлорид) (вторая стадия).
[1-2] Производное коричной кислоты формулы (2) может быть получено описанным ниже способом.
Следует понимать, что в приведенном ниже описании остаток -B-ОН в формуле (2) иногда записывается как -NH-B1-COOH.
При селективном взаимодействии карбоксильной группы производного коричной кислоты с амино-группой амино-кислоты, содержащей свободную амино-группу и свободную карбоксильную группу (H2N-B-COOH) образуется амидная связь и, следовательно, рассматриваемое соединение формулы (2). Селективное взаимодействие с амино-группой вышеуказанной амино-кислоты может быть осуществлено двумя альтернативными способами, а именно: при растворении амино-кислоты в щелочном растворе и добавлении соединения, способного активировать карбоксильную группу R1-OH (способ синтеза 1) или путем получения эфира амино-кислоты (H2N-B1-COORb) для защиты карбоксильной группы свободной амино-кислоты с последующим взаимодействием карбоксильной группы R1-OH с амино-группой вышеуказанного эфира амино-кислоты и удалением группы, защищающей карбоксильную группу известными способами (способ синтеза 2). Каждый из этих способов может быть представлен следующим образом.
Способ синтеза 1
Способ синтеза 2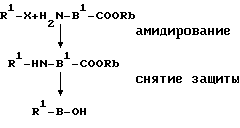
Ниже каждая стадия описана более подробно.
[Способ синтеза 1]
Амино-кислоту (H2N-B1COOH) растворяют в воде и при охлаждении льдом медленно по каплям добавляют производное коричной кислоты R1-OX, в котором карбоксильная группа заранее активирована (например, в виде галогенида коричной кислоты R1-X (например, циннамоилхлорида), коричного ангидрида (R1)2O или смешанного ангидрида кислот R1-O-R') и щелочной раствор так, чтобы реакционная система все время была щелочной. Предпочтительно присутствие органического растворителя, чтобы обладающее высокими гидрофобными свойствами производное коричной кислоты не отделялось от реакционной системы. Предпочтительными примерами таких растворителей являются диоксан и диметилформамид, причем наиболее часто используют диоксан. Щелочной раствор предпочтительно представляет собой водный раствор гидроксида натрия или гидроксида калия. Так как основность реакционной системы поддерживается с помощью щелочного раствора, карбоксильная группа амино-кислоты образует с щелочным металлом соль и, одновременно, с амино-группы снимается защитная функция, поэтому реакция селективно протекает по амино-группе. Реакционную массу затем промывают органическим растворителем в делительной воронке, подкисляют и экстрагируют для выделения названного соединения R1-B-OH-.
[Способ синтеза 2]
Эфир амино-кислоты (H2N-R1-COORb), который обеспечивает защиту карбоксильной группы амино-кислоты, растворяют или суспендируют в безводном органическом растворителе и затем при охлаждении льдом добавляют соединение, обеспечивающее активацию карбоксильной группы производного коричной кислоты (определено выше) и органическое основание. Защитные группы для карбоксильной группы, которые рассматривались выше, практически не имеют ограничений при условии, что они не оказывают влияния на свойства получаемого соединения. Следовательно, можно назвать соединения, например, с этерифицированными карбоксильными группами, такие как метиловый эфир, этиловый эфир, трет.-бутиловый эфир, бензиловый эфир и др. Непрореагировавшее соединение может быть удалено при промывке реакционной смеси в делительной воронке кислотой или щелочью. В зависимости от конкретного варианта продукт может быть очищен, например, путем перекристаллизации.
Рассматриваемое соединение R1-B-OH может быть получено при снятии с карбоксильной группы полученного соединения (R1HN-B1-COORb) защитной функции при соответствующих условиях. Например, метиловый или этиловый эфир могут быть расщеплены щелочью, трет.-бутиловый эфир - кислотой, а бензиловый эфир - путем гидрогенолиза.
В качестве конкретных примеров могут быть рассмотрены следующие способы синтеза соединения R1-B-OH.
[Способ синтеза 1]
Амино-кислоту растворяют в воде и затем при охлаждении льдом медленно по каплям добавляют раствор эквимолярного количества галогонида R1-OH (то есть R1-X) в диоксане и водный раствор гидроксида натрия так, чтобы реакционная система постоянно была щелочной. По окончании добавления реакционную смесь перемешивают при комнатной температуре в течение 24 часов. Затем диоксан отгоняют и водный остаток промывают несколькими порциями этилацетата для удаления исходных продуктов. Водный слой подкисляют, например, лимонной кислотой, и экстрагируют несколькими порциями этилацетата. Органический экстракт сушат безводным сульфатом натрия и упаривают в вакууме. Получают рассматриваемое соединение R1B-OH.
[Способ синтеза 2]
Когда используется низший алкиловый эфир указанной аминокислоты такой как, например, метиловый или этиловый эфир (то есть H2N-B1-COORb), или его соль, то эти соединения вначале растворяются или суспендируются в хлороформе. Затем при охлаждения льдом добавляется органическое основание, например, триэтиламин, так, чтобы система оставалась нейтральной, а затем добавляют раствор эквимольного количества галогенида R1-OH (то есть R1-X) в хлороформе. Смесь перемешивают в течение 24 часов. Затем реакционную массу разбавляют этилацетатом и промывают последовательно несколькими порциями слабокислого раствора, водой, несколькими порциями слабощелочного раствора, водой и насыщенным раствором хлористого натрия. Органический экстракт сушат сульфатом натрия. Затем сульфат натрия отфильтровывают и фильтрат концентрируют в вакууме. Получают соединение R1-HN-B1-COORb.
Это соединение растворяют в метаноле, затем при охлаждении льдом добавляют избыток водного раствора гидроксида натрия. Полученную смесь перемешивают при комнатной температуре в течение 24 часов. Реакционную массу упаривают в вакууме и полученный остаток разбавляют хлороформом и водой и экстрагируют рассматриваемое соединение в водную фазу. Полученный водный раствор подкисляют кислотой, например, лимонной кислотой, и экстрагируют несколькими порциями этилацетата. Объединенные органические экстракты промывают насыщенным водным раствором сульфата натрия и сушат безводным сульфатом натрия. Затем сульфат натрия отфильтровывают и фильтрат упаривают в вакууме. Получают рассматриваемое соединение R1B-OH.
[1-3] Производное коричной кислоты формулы (1) может быть получено описанным ниже способом.
Следует отметить, что в данном описании остаток формулы -C-H (3) может быть иногда представлен в виде формулы -CO-C1-NH2.
Рассматриваемое соединение формулы R2-C-H может быть получено при селективном взаимодействии амино-группы аминокоричного эфира формулы R2-H с карбоксильной группой амино-кислоты (H2N-C1-COOH) с образованием амидной связи. Для обеспечения селективного протекания реакции по карбоксильной группе амино-кислоты предпочтительно использование амино-кислоты, в которой амино-группа предварительно защищена, например, N-защищенную амино-кислоту (RaHN-C1-COOH). Таким образом, амино-группа соединения R2-H реагирует с карбоксильной группой амино-кислоты (RaHN-C1-COOH) с образованием амидной связи, что приводит к соединению формулы RaHN-C1COR2, то есть N-защищенного соединения R2-C-H (первая стадия). В соответствующих условиях снимают защитную группу и получают названное соединение (вторая стадия). Следовательно, названное соединение может быть получено с помощью двух стадий - амидирования и снятия защиты. Схему реакции можно представить следующим образом.
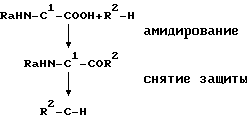
Каждая из этих стадий ниже описана более подробно.
[Первая стадия]
Вначале активируют карбоксильную группу N-защищенной амино-кислоты (RaHN-C1-COOH) (то есть получают, например, N-защищенный галогенид, представляемый формулой RaHN-C1-CO-X;
N-защищенный ангидрид амино-кислоты, имеющий формулу (RaHN-C1-CO)2O; или смешанный ангидрид, имеющий формулу RaHN-C1-CO-O-R'), а затем в присутствии органического основания активированная карбоксильная группа взаимодействует с амино-группой аминокоричного эфира R2-H. Защитная группа в указанной N-защищенной амино-кислоте практически не имеет ограничений при условии, что эфирная связь вышеуказанного аминокоричного эфира не расщепляется при осуществлении снятия защитной группы. Предпочтительными защитными группами являются трет. -бутоксикарбонильная, бензилоксикарбонильная, а также 9-флуоренилметоксикарбонильная группа. Наиболее предпочтительной является трет.-бутоксикарбонильная группа. Полученную реакционную массу промывают кислотой и щелочью и получают соединение RaHN-C1-CO-R2. В зависимости от конкретного случая этот продукт предпочтительно очищают с помощью обычных методик очистки, например, перекристаллизацией и колоночной хроматографией.
[Вторая стадия]
Защитную группу с амино-группы соединения, полученного на первой стадии (RaHM-C1-CO-R2), снимают в подходящих условиях и получают рассматриваемое соединение R2-C-H. Tax как эфирный остаток аминокоричного эфира представляет собой низшую алкильную группу, снятие защиты не может быть осуществлено щелочным омылением. Предпочтительно кислотное снятие защиты или снятие защиты путем гидрогенолиза. Наиболее предпочтительно кислотное снятие защиты, которое приводит к одновременному образованию соответствующей соли. Говоря более конкретно, при использовании в качестве защитной группы трет.-бутоксикарбонильной группы снятие защиты можно проводить с помощью хлористого водорода, бромистого водорода, трифторуксусной кислоты и др. аналогичных кислот. С учетом последующего введения соединения в полимер-хозяин образование соли с кислотой, содержащей карбоксильную группу, является нежелательным. Таким образом, предпочтительно для снятия защиты и образования соли использовать галогенид водорода, предпочтительно хлористый водород.
Пример методики синтеза соединения (R2C-H) приведен ниже.
Соединение (RaHN-C1COOH) растворяют в органическом растворителе, таком как хлороформ, а затем при охлаждении льдом последовательно добавляют органическое основание, например триэтиламин, и конденсирующий агент такой, как диметилфосфинотиоилхлорид или пивалоидхлорид. Смесь перемешивают при комнатной температуре. К полученному раствору добавляют соединение R2-H или его соль и основание, например, триэтиламин, и полученную смесь перемешивают при комнатной температуре от 10 минут до 10 часов. По окончании реакции органический растворитель упаривают в вакууме и полученный остаток разбавляют органическим растворителем, например, этилацетатом и, используя делительную воронку, промывают последовательно несколькими порциями слабокислого водного раствора, водой, несколькими порциями слабощелочного водного раствора, водой и насыщенным раствором хлористого натрия. Органический слой отделяют и сушат безводным сульфатом натрия или др. Сульфат натрия отфильтровывают и фильтрат упаривают в вакууме. Получают соединение (RaNH-C1-CO-R2). К соединению (RaNH-C1-CO-R2) при перемешивании и при комнатной температуре добавляют раствор кислоты в органическом растворителе, например, 1 - 5 М раствор HCl/диоксан. По окончании реакции добавляют органический растворитель, например, эфир, и полученные кристаллы отфильтровывают, промывают органическим растворителем, сушат в вакууме, получают хлоргидрат соединения (R2-C-H).
[2] Синтез производных коричная кислота - полимер
Рассмотренные выше производные коричной кислоты со спейсерным фрагментом формул (1) - (3) являются новыми соединениями. При взаимодействии этих производных с макромолекулярным соединением (полимером-хозяином), которое содержит функциональную группу, могут быть получены производные коричная кислота - полимер, соответствующие формулам (13) - (15).
R1-A-P1, (13)
R1-B-P2, (14)
R2-C-P1, (15)
где заместители R1, R2, A, B и C принимают значения, определенные выше; заместитель P1 представляет собой остаток полимера, содержащего карбоксильную группу; заместитель P2 представляет собой полимерный остаток, содержащий амино- или гидрокси-группу; связь A-P1 представляет собой амидную связь, образованную между амино-группой остатка формул (6) - (9) и карбоксильной группой заместителя P1; связь B-P2 представляет собой амидную или эфирную связь, образованную между концевой карбоксильной группой остатка формулы (10) и или амино-группы или гидроксильной группой P2; а связь C-P1 представляет собой амидную связь, образованную между концевой амино-группой остатка формулы (11) или (12) и карбоксильной группой заместителя P1.
Макромолекулярные соединения, содержащие остатки P1 или P2, представляют собой, но не ограничиваются только этими примерами, полисахариды, содержащие карбоксильную, амино- и/или гидроксильную группы (например, гликозаминоглицины, полиаминосахариды, кислые полисахариды и др.), синтетические полимеры (например, полиакриловая кислота, полиимины) и полигидрокси-кислоты (например, полигликолевая кислота, полимолочная кислота и др.). Среди них наиболее предпочтительными являются полисахариды, а гликозаминогликаны используются наиболее часто. Среди названных гликозаминогликанов следует назвать гиалуроновые кислоты, хондроитин-сульфаты (A, C, D, E и K), дерматан-сульфат (хондроитин B), хондроитин, гепарин, сульфат гепарина и кератан-сульфат. Особенно предпочтительными являются гиалуроновая кислота, хондроитин-сульфат A, хондроитин-сульфат C и гепарин. Все эти соединения легко доступны. Также могут быть использованы такие полисахариды, как хитин и хитозан.
Последующая очистка полученных соединений может быть проведена обычными способами, например, путем осаждения этанолом, диализом и др. После сушки CЗ может быть определена из спектров ПМР по величине интегральной интенсивности или по УФ-поглощению при 280 им.
[2-1] Производное коричная кислота - полимер формулы (13) или (15) может быть получено при растворении полимера, содержащего заместитель P1, или в воде, или в воде, содержащей смешиваемый с водой органический растворитель, с последующим его взаимодействием с производным коричной кислоты формулы (1) или (3) в присутствии растворимого в воде карбодиимида и вспомогательного конденсирующего агента. Методика введения производного коричной кислоты включает растворение вышеуказанного полимера или в воде, или в воде, содержащей смешиваемый с водой органический растворитель, и последовательное добавление при мягком перемешивании и при постоянной температуре около 0 - 40oC (обычно 0 - 35oC) вышеуказанного водорастворимого карбодиимида, вышеуказанного вспомогательного конденсирующего агента и вышеуказанного производного коричной кислоты.
Смешиваемый с водой органический растворитель представляет собой диоксан, диметилформамид (ДМФА), N-метилпирролидон, ацетамид, спирт (например, метанол, этанол и др.) и пиридин.
Доля смешиваемого с водой органического растворителя в воде, содержащей вышеуказанный смешиваемый с водой органический растворитель (доля смешиваемой органической кислоты), может быть выражена следующим образом:
Величина ΔO составляет приблизительно 0 - 75%, предпочтительно 30 - 50%.
В качестве вспомогательного конденсирующего агента наряду с другими могут быть использованы N-гидроксисукцинимид (ГСИ) и N-гидроксибензотриазол (ГБТ). Вспомогательный конденсирующий агент не только выполняет функцию активатора карбоксильной группы полимера, но также предотвращает нежелательную ON-ацильную перегруппировку.
Растворимый в воде карбодиимид (РКД) представляет собой хлоргидрат 1-этил-3-(3-диметиламинопропил)карбодиимида (ЭДХ), 1-этил-3-(3-диметиламинопропил)карбодиимида метиодид, а также хлоргидрат 1-циклогексил-3-(2-морфолинэтил)карбодиимида.
[2-2] Производное коричной кислоты и полимера формулы (14) может быть синтезировано при взаимодействии макромолекулярного соединения, содержащего остаток P2, с производным коричной кислоты формулы (2). Способ проведения реакции зависит от типа связи B-P2, то есть от функциональной группы P2.
[2-2-1] Когда связь представляет собой амидную связь, то есть, когда амино-группа вышеуказанного макромолекулярного соединения должна взаимодействовать с карбоксильной группой производного коричной кислоты формулы (2), то вышеуказанная карбоксильная группа вначале активируется и затем активированное соединение взаимодействует с указанным макромолекулярным соединением с образованием амидной связи.
Если рассматривать этот процесс более подробно, то макромолекулярное соединение, содержащее амино-группу, растворяют в подкисленной воде или в кислой водной среде, содержащей спирт или другой органический растворитель, и к полученному раствору при температуре от 0oC до комнатной температуры добавляют вышеуказанное производное коричной кислоты формулы (2), содержащее активированную карбоксильную группу. Методика активирования карбоксильной группы не является критической для данного изобретения, однако необходимо, чтобы образовывалась амидная связь с вышеуказанной амино-группой. Обычно рекомендуются способ с использованием галогенида кислоты, ангидридный способ и способ активного эфира. Например, рассматриваемое производное коричной кислоты и полимера может быть получено в соответствии со способом, который включает добавление конденсирующего агента (например, диметилфосфинотиоилхлорида) и основания (например, триэтиламина) к раствору указанного производного коричной кислоты в органическом растворителе (например, в ДМФА) при охлаждении льдом для активации карбоксильной группы производного в виде смешанного ангидрида и добавление полученного раствора к макромолекулярному соединению в кислой среде водного спирта (например, в среде метанол - уксусная кислота) обычно при температуре от 0oC до комнатной.
[2-2-2] Когда связь является эфирной, то есть, когда гидроксильная группа вышеуказанного макромолекулярного соединения должна реагировать с карбоксильной группой вышеуказанного производного коричной кислоты формулы (2), то карбоксильная группа вначале активируется и активированное соединение реагирует с гидроксильной группой указанного макромолекулярного соединения с образованием эфирной связи. Эта реакция может быть проведена более эффективно в присутствии катализатора.
Если рассматривать этот процесс более подробно, то макромолекулярное соединение растворяют в органическом растворителе и при температуре от 0oC до комнатной температуры в присутствии катализатора постепенно добавляют производное коричной кислоты формулы (2), содержащее активированную карбоксильную группу.
Активация карбоксильной группы производного коричной кислоты может быть проведена по методике [2-2-1], описанной выше. Упоминавшийся там органический растворитель может быть любым растворителем, который не оказывает влияния на реакцию этерификации и может растворять вышеуказанное макромолекулярное соединение. К таким растворителям, наряду с другими, относятся, например, ДМФА, N-метилпирролидон, диоксан, а также диметилсульфоксид (ДМСО). Вид катализатора не ограничивается. Он должен только способствовать протеканию реакции этерификации, хотя наиболее предпочтительным катализатором является 4-диметиламинопиридин.
[3] Получение сшитых производных коричная кислота - полимер
[3-1] Для проведения реакции фотосшивки производное коричной кислоты и полимера настоящего изобретения может быть представлено в различных формах, к которым относятся растворы, пленки, гели, мелко измельченные частицы и т. д. Когда макромолекулярное соединение, которое должно использоваться, является высоко гидрофильным соединением и биосовместимым веществом, таким как гликозаминогликан, отвержденные предметы, приготовленные при фотосшивке указанного производного коричной кислоты и полимера, могут быть использованы в медицинских целях (например, в качестве ингибиторов сращивания биологических тканей, материала для протезирования сосудов, покрывающего агента, основы для фармацевтических препаратов с длительным высвобождением активного соединения, материала для контактных линз, перевязочного материала и др.) и фотосшивка под действием ультрафиолетового излучения может быть проведена после того, как производное коричная кислота - полимер перерабатывается в форму конечного продукта.
Для переработки производного коричной кислоты и полимера в такие различные формы могут быть использованы известные технологии. Такая переработка может быть осуществлена с использованием большого, но разумного количества воды или доли смешивающегося с водой органического растворителя (соотношение смешивающегося органического растворителя) в растворе производного коричной кислоты и полимера, или объема твердого производного коричной кислоты и полимера, температуры и давления.
При получении такого сшитого производного коричной кислоты и полимера, которое приемлемо для медицинского потребления, изделие из фотосшитого производного коричной кислоты и полимера может быть обеспечено в виде стерильного и практически не содержащего эндотоксинов изделия при тщательном выборе и обработке реагентов, воды и сосудов для синтеза исходных материалов, а также воды, сосудов и аппаратуры, которые используются для формования и фотосшивки производного коричная кислота - полимер.
Если говорить более подробно, то реакционная смесь, в которой должно образовываться производное коричной кислоты и полимера, может быть использована в том виде, в каком она существует. Или, напротив, образованное производное отделяется от реакционной смеси, подвергается очистке и повторному растворению, например, в воде с получением водного раствора. Пленка может быть получена путем литья раствора (то есть водного раствора) производного коричной кислоты и полимера с последующим удалением растворителя из указанного раствора. Гели могут быть получены, например, при погружении описанной выше пленки в воду. И наконец, мелко измельченный порошок может быть получен путем физического измельчения указанных пленки или геля.
[3-2] Сшитое производное коричной кислоты и полимера настоящего изобретения представляет собой такое соединение, в котором способные к фотодимеризации сшивающихся групп молекулы производного коричной кислоты и полимера образуют мостиковое циклобутановое кольцо и которое может быть получено при воздействии на вышеуказанное производное коричной кислоты и полимера ультрафиолетового излучения.
Вид ультрафиолетового излучения практически не имеет ограничений. Обычно используются источники света с длинной волны 200 - 600 нм, предпочтительно 200 - 450 нм. Для отсечения света с длиной волны, не требуемой для проведения фотосшивки, свет может пропускаться через ультрафиолетовый фильтр (например, фильтр Pyrexglass (торговое название) и др.).
Источниками ультрафиолетового излучения служат ртутная лампа высокого давления или галогеновая лампа и обычно вышеуказанные пленка, гель или порошок производного коричной кислоты и полимера подвергаются воздействию УФ-света с длиной волны 250 - 450 нм в течение 1-10 минут. По сравнению с фотосшивкой обычного способного к фотосшивке производного гиалуроновой кислоты с высокой степенью замещения, которое требует облучения в течение 30 минут, технология настоящего изобретения отличается значительным уменьшением времени облучения. Этот результат может быть объяснен использованием спейсера, описанного выше (остаток A, B и C в производном коричной кислоты формул (1) - (3)).
Каждое производное коричной кислоты формул (1) - (3) обычно существует в транс-форме и когда внутримолекулярное расстояние составляет 4 ангстрема, то при облучении светом длиной волны из ультрафиолетовой области (около 280 нм) это производное подвергается димеризации. Однако при других внутримолекулярных расстояниях производное не димеризуется и даже, если его молекула находится в возбужденном состоянии, оно изомеризуется в геометрическую форму, инертную к облучению, то есть в цис-форму. Хотя производное коричной кислоты настоящего изобретения образует производное коричной кислоты и полимера при введении в макромолекулярное соединение, реакция фотодимеризации на цепочке макромолекулярного соединения-хозяина, например, гликозаминогликана, по-существу, идентична рассмотренной выше реакции димеризации. Следовательно, необходимо, чтобы молекула производного коричной кислоты изначально имела вышеуказанное внутримолекулярное расстояние, определяющее способность к димеризации.
В соответствии с настоящим изобретением заместители R1 и R1, R2 и R2, или R1 и R2 в молекулах одного или нескольких производных коричная кислота - полимер, выбираемых из производных формул (13) - (15), а именно молекулы соединения (13), соединения (14), соединения (15), соединений (13) и (14), соединений (13) и (15), соединений (14) и (15) или соединений (13) - (15) фотодимеризуются с образованием мостикового циклобутанового кольца и обеспечивают посредством этого образование сшитого производного коричной кислоты и полимера. Когда фотосшивка имеет место между соединениями одной формулы для соединений формул (13) - (15), то конкретные соединения, которые подвергаются фотосшивке, могут быть одинаковыми соединениями или различными.
Мостиковое циклобутановое кольцо сшитого производного коричной кислоты и полимера настоящего изобретения обычно существует в виде двух структурных изомеров, а именно в виде производного труксиновой кислоты и производного труксиловой кислоты, прячем они могут существовать в виде множества стереоизомеров. Сшитое производное коричной кислоты и полимера настоящего изобретения может иметь любую из этих структур.
Например, хотя фотосшивка производного коричной кислоты и полимера может быть вызвана УФ-излучением после того, как это производное переработано в пленку путем литья, реакционная способность такой реакции фотосшивки, как оказалось, управляется ориентацией молекул, сформировавшейся в процессе литья.
Схематическое изображение фотореакции при образовании сшитого производного коричной кислоты и полимера настоящего изобретения представлено на фиг. 1. По сравнению со случаем, когда коричная кислота вводится непосредственно в цепочку полимера-хозяина, реакционная способность в реакции фотодимеризации увеличивается за счет свободного внутреннего пространства. Однако этот фактор не является единственным, и высокая гидрофильность спейсера также имеет большое значение для проведения фотореакции.
Примерами таких спейсеров являются органические группы, имеющие углеродный скелет и две или несколько функциональных групп. Примерами могут служить амино-кислоты или их производные, пептиды, амино-спирты, диамины, олигосахариды, диолы, гидрокси-кислоты и др. Предпочтительными являются амино-кислоты и их производные, пептиды и амино-спирты.
Фиг. 1 представляет собой схематичное изображение реакции фотосшивки в соответствии с настоящим изобретением и под номером 1 на нем изображено производное коричная кислота - полимер. Это полимерное производное 1 представляет собой комплекс, образованный между макромолекулярным соединением 2 и производным коричной кислоты и это производное коричной кислоты 4 молекулы транс-коричной кислоты, связанные со спейсером 3. Когда производное коричной кислоты 1 подвергается воздействию ультрафиолетового излучения (УФ), способные к фотосшивке группы соседних молекул транс-коричной кислоты связываются друг с другом, образуя циклобутановое кольцо и давая димер 6, с тем результатом, что производное коричной кислоты и полимера 1 превращается в сшитое полимерное производное коричной кислоты 5. Некоторое количество молекул коричной кислоты не реагирует, поскольку они представляют собой цис-коричную кислоту 7, которая инертна в реакциях фотосшивки.
Когда производное коричной кислоты вводится в гидрофильную макромолекулу, такую как гликозаминогликан, и полученный комплекс подвергается формованию (например, отливается в пленку) с удалением воды, высокая гидрофильность производного коричной кислоты приводит к множественному присоединению и агрегации молекул за счет гидрофобного связывания, при этом производное имеет тенденцию давать молекулярную ориентацию, которая предпочтительна для фотополимеризации. Таким образом, увеличение гидрофильности производного коричной кислоты может быть фактором увеличения реакционной способности при фотодимеризации. Реакция фотодимеризации между сшивающимися группами производного коричная кислота - полимер приводит к созданию трехмерной сетки за счет мостиковых циклобутановых колец в производном коричной кислоты и полимера и плотность сшивки такой сетки регулируется способностью к фотодимеризации производного коричной кислоты. Различия в плотности сшивки приводят к различию в скорости поглощения воды и прочности отвержденного продукта. Обычно, чем выше плотность сшивки, тем ниже скорость поглощения воды и выше прочность. Таким образом, даже если сшивающиеся группы вводятся в полимер-хозяин при одной и той же степени замещения и полученный комплекс облучается ультрафиолетовым светом в течение одного и того же периода времени, различия в физических свойствах достигаются за счет разных типов спейсеров. Следовательно, физические характеристики сшитого полимерного производного коричной кислоты можно контролировать разумным выбором соответствующего спейсера.
Использование физиологического соединения - гликозаминогликана - в качестве полимера-хозяина для введения производного коричной кислоты обеспечивает определенные преимущества при применении в медицине благодаря тому, что могут быть использованы и собственные характеристики гликозаминогликана, а опасностью с точки зрения физиологии можно пренебречь.
Более того, то что высокочувствительное производное коричной кислоты может быть получено за счет введения спейсера, дает возможность получать сшитое производное коричной кислоты и полимера при низкой степени замещения и при уменьшенном времени УФ-облучения. Это означает, что физические характеристики сшитого производного коричная кислота - полимер можно контролировать степенью замещения, которая является такой низкой, что может быть почти незначительной с точки зрения воздействия на физиологию так, что собственные свойства полимера-хозяина такого, как гликозаминогликан, могут быть почти полностью сохранены.
Следующие примеры предназначены для более детальной иллюстрации настоящего изобретения и не ограничивают объем притязаний настоящего изобретения.
В рассматриваемых ниже примерах сокращение "Boc" означает трет.-бутоксикарбонил.
[1-1] Примеры 1-6
Синтез соединения формулы (1) и (6):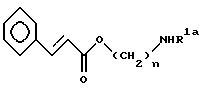
(в заместителе R1, заместители R3 = R4 = H и заместитель R1a = H или представляет собою амино-защищающую группу).
Пример 1
Синтез хлоргидрата 3-аминопропилового эфира коричной кислоты [соединение (1а-1), n = 3, R1a = H].
1-1: Синтез соединения (1-1) [n = 3, R1a = Boc]
К 1.21 г (6.9 ммоля) трет.-бутоксикарбонил-3-аминопропанола добавляют 6 мл хлороформа и затем при охлаждении льдом добавляют в указанном порядке 956 мкл (6.9 ммоля) триэтиламина, 1.15 г (6.9 ммоля) циннамоилхлорида и 253 мг (2.1 ммоля) 4-диметиламинопиридина. Смесь перемешивают при комнатной температуре в течение 20 минут. Полученную реакционную смесь разбавляют этилацетатом и промывают последовательно двумя порциями 5%-ного водного раствора лимонной кислоты, двумя порциями 5%-ного водного раствора гидрокарбоната натрия, водой и насыщенным водным раствором хлористого натрия. Затем органический слой отделяют и сушат с помощью безводного сульфата натрия. Далее сульфат натрия отфильтровывают и фильтрат концентрируют в вакууме. Полученный белый осадок промывают гексаном и сушат в вакууме, получают 1.38 г соединения (1-1) (выход 65%).
1-2: Синтез хлоргидрата 3-аминопропилового эфира коричной кислоты [соединение (1a-1), n = 3, R1a = H].
К 860 мг (2.8 ммоля) соединения (1-1) при охлаждении льдом добавляют 6 мл 4 М раствора HCl/диоксан и затем смесь перемешивают при комнатной температуре в течение 35 минут. К полученной реакционной смеси добавляют эфир и образующиеся кристаллы отфильтровывают, промывают эфиром и сушат в вакууме. Получают соединение (1a-1) в виде белых кристаллов.
Выход 76%, т.пл. 115.2 - 116.3oC.
Спектр ПМР (400 МГц, D2O, δ м.д.): 2.16 (2Н, м, 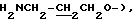 3.21 (2Н, т,
3.21 (2Н, т, 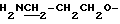 ), 4.37 (2Н, т.
), 4.37 (2Н, т. 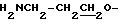 ), 6.62 (1Н, д,
), 6.62 (1Н, д, 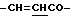 ), 7.52 (3Н, м, ароматические H, положения 3, 4, 5), 7.72 (2H, дд, ароматические H, положения 2, 6), 7.80 (1H, д,
), 7.52 (3Н, м, ароматические H, положения 3, 4, 5), 7.72 (2H, дд, ароматические H, положения 2, 6), 7.80 (1H, д, 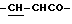 ).
).
Пример 2
Синтез хлоргидрата 4-аминобутилового эфира коричной кислоты [соединение (1a-2), n = 4, R1a = H].
2-1: Синтез соединения (1-2), n = 4, R1a = Boc
Указанное соединение синтезируют по методике примера 1-1. Выход 93%.
2-2: Синтез хлоргидрата 4-аминобутилового эфира коричной кислоты [соединение (1a-2), n = 4, R1a = H].
Для получения указанного соединения повторяют методику примера 1-2. Выход 88%, т.пл. 91.2 - 92.4oC.
Спектр ПМР (400 МГц, D2O, δ м.д.): 1.85 (4H, м, H2NCH2 - 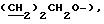 3.10 (2H, т,
3.10 (2H, т, 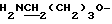 ), 4.30 (2H, т,
), 4.30 (2H, т, 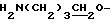 ), 6.83 (1H, д,
), 6.83 (1H, д, 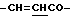 ), 7.53 (3H, м, ароматические H, положения 3, 4, 5), 7.70 (2H, дд, ароматические H, положения 2, 6), 7.80 (1H, д,
), 7.53 (3H, м, ароматические H, положения 3, 4, 5), 7.70 (2H, дд, ароматические H, положения 2, 6), 7.80 (1H, д, 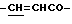 ).
).
Пример 3
Синтез хлоргидрата 5-аминопентилового эфира коричной кислоты [соединение (1а-3), n = 5, R1a = H].
3-1: Синтез соединения (1-3), n = 5, R1a = Boc
Для получения указанного соединения повторяют методику примера 1-1. Выход 100%.
3-2: Синтез хлоргидрата 5-аминопентилового эфира коричной кислоты [соединение (1а-3), n = 5, R1a = H].
Для получения указанного соединения повторяют методику примера 1-2. Выход 88%, т.пл. 150.3 - 153.4oC.
Спектр ПМР (400 МГц, D2O, δ м.д.): 1.52 (2Н, м, 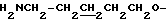 ), 1.70 - 1.86 (4Н, м,
), 1.70 - 1.86 (4Н, м, 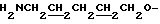 ), 3.05 (2Н, т,
), 3.05 (2Н, т, 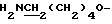 ), 4.29 (2Н, т,
), 4.29 (2Н, т, 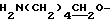 ), 6.61 (1Н, д,
), 6.61 (1Н, д, 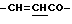 ), 7.51 (3Н, м, ароматические H, положения 3, 4, 5), 7.69 (2H, дд, ароматические H, положения 2, 6), 7.78 (1H, д,
), 7.51 (3Н, м, ароматические H, положения 3, 4, 5), 7.69 (2H, дд, ароматические H, положения 2, 6), 7.78 (1H, д, 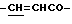 ).
).
Пример 4
Синтез хлоргидрата 6-аминогексилового эфира коричной кислоты [соединение (1a-4), n = 6, R1a = H].
4-1: Синтез соединения (1-4), n = 6, R1a = Boc
Для получения указанного соединения повторяют методику примера 1-1. Выход 99%.
4-2: Синтез хлоргидрата 6-аминогексилового эфира коричной кислоты (соединение (1a-4), n = 6, R1a = H].
Для получения указанного соединения повторяют методику примера 1-2. Выход 86%, т.пл. 98.8 - 100.4oC.
Спектр ПМР (400 МГц, D2О, δ м.д.): 1.48 - 1.53 (4Н, м, 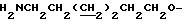 ), 1.63 - 1.83 (4Н, м,
), 1.63 - 1.83 (4Н, м, 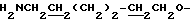 ), 3.02 (2Н, т,
), 3.02 (2Н, т, 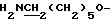 ), 4.28 (2Н, т,
), 4.28 (2Н, т, 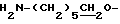 ), 6.60 (1Н, д,
), 6.60 (1Н, д, 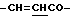 ), 7.53 (3H, м, ароматические H, положения 3, 4, 5), 7.68 (2Н, д, ароматические H, положения 2, 6), 7.76 (1H, д,
), 7.53 (3H, м, ароматические H, положения 3, 4, 5), 7.68 (2Н, д, ароматические H, положения 2, 6), 7.76 (1H, д, 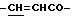 ).
).
Пример 5
Синтез хлоргидрата 8-аминооктилового эфира коричной кислоты [соединение (1a-5), n = 8, R1a = H].
5-1: Синтез соединения (1-5), n = 8, R1a = Boc
Для получения указанного соединения повторяют методику примера 1-1. Выход 87%.
5-2: Синтез хлоргидрата 8-аминооктилового эфира коричной кислоты [соединение (1а-5), n = 8, R1a = H].
Для получения указанного соединения повторяют методику примера 1-2. Выход 88%, т.пл. 86.5 - 87.3oC.
Спектр ПМР (400 МГц, D2O, δ м.д.): 1.31 - 1.48 (8Н, м, 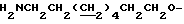 ), 1.62 - 1.79 (4Н, м,
), 1.62 - 1.79 (4Н, м, 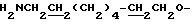 ), 2.99 (2Н, т,
), 2.99 (2Н, т, 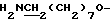 ), 4.26 (2Н, т,
), 4.26 (2Н, т, 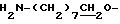 ), 6.58 (1Н, д,
), 6.58 (1Н, д, 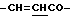 ), 7.52 (3Н, м, ароматические H, положения 3, 4, 5), 7.68 (2Н, д, ароматические H, положения 2, 6), 7.76 (1H, д,
), 7.52 (3Н, м, ароматические H, положения 3, 4, 5), 7.68 (2Н, д, ароматические H, положения 2, 6), 7.76 (1H, д, 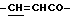 ).
).
Пример 6
Синтез хлоргидрата 12-аминододецилового эфира коричной кислоты [соединение (1а-6), n = 12, R1a = H].
6-1: Синтез соединения (1-6), n = 12, R1a = Boc
Для получения указанного соединения повторяют методику примера 1-1. Выход приблизительно 100%.
6-2: Синтез хлоргидрата 12-аминододецилового эфира коричной кислоты [соединение (1а-6), n = 12, R1a = H].
Для получения указанного соединения повторяют методику примера 1-2. Выход 82%, т.пл. 90.7 - 93.1oC.
Спектр ПМР (400 МГц, D2O, δ м.д.): 1.24 - 1.50 (16Н, м. 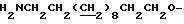 ), 1.64 (2Н, м,
), 1.64 (2Н, м, 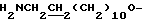 ), 1.76 (2Н, м,
), 1.76 (2Н, м, 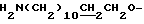 ), 2.96 (2Н, т,
), 2.96 (2Н, т, 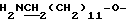 ), 4.28 (2Н, т,
), 4.28 (2Н, т, 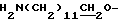 ), 6.61 (1Н, д,
), 6.61 (1Н, д, 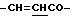 ), 7.53 (3Н, м, ароматические H, положения 3, 4, 5), 7.68 (2Н, д, ароматические H, положения 2, 6), 7.76 (1H, д,
), 7.53 (3Н, м, ароматические H, положения 3, 4, 5), 7.68 (2Н, д, ароматические H, положения 2, 6), 7.76 (1H, д, 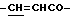 ).
).
[1-2] Синтез соединения формул (1) и (7):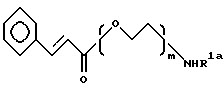
(в заместителе R1, заместители R3 = R4 = H).
Пример 7
Синтез хлоргидрата 2-(2-аминоэтокси)этилового эфира коричной кислоты [соединение (1a-7), m = 2, R1a = H].
7-1: Синтез соединения (1-7), m = 8, R1a = Boc
Указанное соединение синтезируют по методике примера 1-1 с использованием Boc-NH(CH2CH2O)2H вместо Boc-NH(CH2)3-OH. Выход 85%.
7-2: Синтез хлоргидрата 2-(2-аминоэтокси)этилового эфира коричной кислоты [соединение (1a-7), m = 2, R1a = H].
Синтез указанного соединения синтезируют по методике примера 1-2 с использованием соединения (1-7) вместо соединения (1-1). Выход приблизительно 100%, т.пл. 80.8 - 82.5oC.
Спектр ПМР (400 МГц, D2O, δ м.д.): 3.26 (2Н, т, 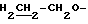 ), 3.84 (2Н, т,
), 3.84 (2Н, т, 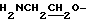 ), 3.88 (2Н, т,
), 3.88 (2Н, т, 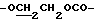 ), 4.40 (2Н, т,
), 4.40 (2Н, т, 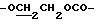 ), 6.54 (1Н, д,
), 6.54 (1Н, д, 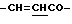 ), 7.49 (3Н, м, ароматические H, положения 3, 4, 5), 7.64 (2Н, д, ароматические H, положения 2, 6), 7.73 (1H, д,
), 7.49 (3Н, м, ароматические H, положения 3, 4, 5), 7.64 (2Н, д, ароматические H, положения 2, 6), 7.73 (1H, д, 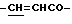 ).
).
[1-3] Синтез соединения формул (1) и (8):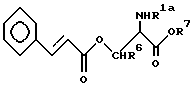
(в заместителе R1 заместители R3 = R4 = H; в формуле (8) R6 = H, R7 = CH3).
Пример 8
Синтез хлоргидрата метилового эфира о-циннамоилсерина [соединение (1а-8), R1a = H].
8-1: Синтез соединения (1-8), R1a = Boc
В 9 мл хлороформа растворяют 1.93 г (8.8 ммоля) метилового эфира трет. -бутоксикарбонилсерина и затем при охлаждении льдом в указанном порядке добавляют раствор 2.94 г (10,6 ммоля) коричного ангидрида в 10 мл хлороформа, 1.46 мл (10.6 ммоля) триэтиламина и раствор 645 мг (4.4 ммоля) 4-диметил-аминопиридина в 2 мл хлороформа. Смесь перемешивают при комнатной температуре в течение 35 минут и затем упаривают в вакууме для уменьшения объема жидкости. Полученный раствор разбавляют этилацетатом и промывают последовательно 2 порциями 5%-ной лимонной кислоты, водой и 2 порциями насыщенного водного раствора хлористого натрия. Органический слой отделяют и сушат безводным сульфатом натрия. Затем сульфат натрия отфильтровывают и фильтрат концентрируют в вакууме. К полученному остатку добавляют эфир и образующиеся кристаллы перекристаллизовывают из смеси этилацетат-петролейный эфир, получают 2.10 г (выход 68%) соединение (1-8).
Идентификация строения полученного соединения осуществляется с помощью спектра ПМР.
Спектр ПМР (400 МГц, CDCl3, δ м.д.): 1.45 (9Н, с. Boc-), 3.80 (3Н, с, -COOCH3), 4.51 (2Н, дд, β-CH2), 4.65 (1Н, уш., α-CH), 5.38 (1Н, уш., CONH), 6.40 (1Н, д, 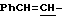 ), 7.45 (5Н, м, Ph-), 7.70 (1Н, c,
), 7.45 (5Н, м, Ph-), 7.70 (1Н, c, 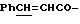 ).
).
8-2: Синтез хлоргидрата метилового эфира о-циннамоилсерина [соединение (1a-8), R1a = H].
При охлаждении льдом к 1.48 г (4.2 ммоля) кристаллического соединения (1-8) добавляют трифторуксусную кислоту до уровня, при котором кристаллы полностью покрыты. Смесь выдерживают в течение 30 минут. Затем добавляют 1.1 мл 4 М раствора HCl/диоксан с последующей кристаллизацией, вызываемой добавлением гексана. Полученные кристаллы отфильтровывают и промывают смесью эфир-гексан на стеклянном фильтре, получают 1.39 г (выход 91%) соединения (1a-8) в виде белых кристаллов. Т.пл. 144.5 - 147.0oC.
Спектр ПМР (400 МГц, D2O, δ м.д.): 3.92 (3Н, с, -COOCH3), 4.58 - 4.75 (3Н, дд, Ser α-H, β-H), 6.80 (1Н, д, 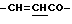 ), 7.50 (3Н, м, ароматические H, положения 3, 4, 5), 7.68 (2Н, дд, ароматические H, положения 2, 6), 7.82 (1H, д,
), 7.50 (3Н, м, ароматические H, положения 3, 4, 5), 7.68 (2Н, дд, ароматические H, положения 2, 6), 7.82 (1H, д, 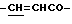 ).
).
[1-4] Синтез соединения формул (1) и (9):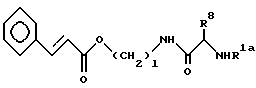
(в заместителе R1 заместителе R3 = R4 = H).
Пример 9
Синтез хлоргидрата соединения (1а-9), 1 = 2, R1a = H, R8 = H.
В 2 мл хлороформа растворяют 175 мг (1.0 ммоль) трет.-бутоксикарбонилглицина и затем при охлаждении льдом добавляют 139 мкл (1.0 ммоль) триэтиламина и 1.0 мл (1.0 ммоль) 1 М раствора диметилфосфинотиоилхлорида в хлороформе. Смесь перемешивают при комнатной температуре в течение 20 минут. Затем при охлаждении льдом добавляют 139 мкл (1.0 ммоль) триэтиламина и отдельно приготовленный раствор хлоргидрата 2-аминоэтилового эфира коричной кислоты (1.0 ммоль) и 139 мкл (1.0 ммоль) триэтиламина в 2 мл хлороформа. Полученную смесь перемешивают при комнатной температуре в течение 2 часов. После завершения реакции добавляют 4 мл метанола и 1 мл водного раствора аммиака и смесь перемешивают в течение 30 минут. Полученный раствор концентрируют один раз в вакууме, остаток разбавляют этилацетатом и промывают последовательно водой, 2 порциями 5%-ного водного раствора лимонной кислоты, водой и насыщенным водным раствором хлористого натрия. Органический слой сушат безводным сульфатом натрия и упаривают в вакууме. Получают соединение (1-9) [1 = 2, R1a = Boc, R8 = H]. К полученному соединению при охлаждении льдом добавляют 3 мл 4 М раствора HCl в диоксане и смесь перемешивают при комнатной температуре в течение 30 минут. Реакционную смесь концентрируют в вакууме, получают 106 мг (выход 35%) названного соединения (1а-9) в виде белого твердого вещества. Т.пл. 162.5 - 165.8oC.
Спектр ПМР (400 МГц, D2O, δ м.д.): 3.83 (2Н, с, 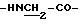 ), 3.66 (2Н, т,
), 3.66 (2Н, т, 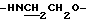 ), 4.38 (2Н, т,
), 4.38 (2Н, т, 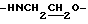 ), 6.62 (1Н, д,
), 6.62 (1Н, д, 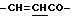 ), 7.53 (3Н, м, ароматические H, положения 3, 4, 5), 7.70 (2Н, д, ароматические H, положения 2, 6), 7.81 (1H, д,
), 7.53 (3Н, м, ароматические H, положения 3, 4, 5), 7.70 (2Н, д, ароматические H, положения 2, 6), 7.81 (1H, д, 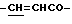 ).
).
Пример 10
Синтез хлоргидрата соединения (1а-10), 1 = 2, R1a = H, R8 = CH3.
Указанное соединение синтезируют по методике примера 9, используя трет. -бутоксикарбонилаланин вместо трет.-бутоксикарбонилглицина. Выход 45%.
Спектр ПМР (400 МГц, D2O, δ м.д.): 2.53 (3Н, д, -CH3), 3.55 (1Н, дт, 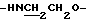 ), 3.72 (1Н, дт,
), 3.72 (1Н, дт, 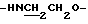 ), 4.08 (1Н, м, α-H аланина), 4.36 (2Н, т,
), 4.08 (1Н, м, α-H аланина), 4.36 (2Н, т, 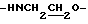 ), 6.58 (1Н, д,
), 6.58 (1Н, д, 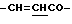 ), 7.50 (3Н, м, ароматические H, положения 3, 4, 5), 7.67 (2Н, д, ароматические H, положения 2, 6), 7.76 (1H, д,
), 7.50 (3Н, м, ароматические H, положения 3, 4, 5), 7.67 (2Н, д, ароматические H, положения 2, 6), 7.76 (1H, д, 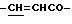 ).
).
Пример 11
Синтез хлоргидрата соединения (1а-11), 1=2, R1a = H, R8 = (CH3)2CHCH2-
Указанное соединение синтезируют по методике примера 9, используя трет. -бутоксикарбониллейцин вместо трет.-бутоксикарбонилглицина. Выход 58%.
Спектр ПМР (400 МГц, D2O, δ м.д.): 0.90 (6Н, дд, 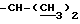 ), 1.55 - 1.80 (3Н, м,
), 1.55 - 1.80 (3Н, м, 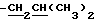 ), 3.44 (1Н, дт,
), 3.44 (1Н, дт, 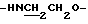 ), 3.88 (1Н, дт,
), 3.88 (1Н, дт, 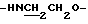 ), 3.99 (1Н, т, α-H лейцина), 4.39 (2Н, т,
), 3.99 (1Н, т, α-H лейцина), 4.39 (2Н, т, 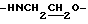 ), 6.60 (1Н, д,
), 6.60 (1Н, д, 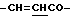 ), 7.51 (3Н, м, ароматические H, положения 3, 4, 5), 7.70 (2Н, д, ароматические H, положения 2, 6), 7.78 (1H, д,
), 7.51 (3Н, м, ароматические H, положения 3, 4, 5), 7.70 (2Н, д, ароматические H, положения 2, 6), 7.78 (1H, д, 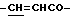 ).
).
[2] Примеры 12 - 15: Синтез соединения формул (2) и (10)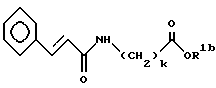
(в заместителе R1 заместители R3 = R4 = H).
Пример 12
Синтез циннамоилглицина [соединение (2-1), k = 1, R1b = H]
12-1: метиловый эфир циннамоилглицина [соединение (2-1b), k = 1, R1b = CH3]
В 10 мл хлороформа суспендируют 1.26 г (10 ммолей) хлоргидрата метилового эфира и затем последовательно добавляют при охлаждении льдом 2.77 мл (20 ммолей) триэтиламина и 10 мл 2.78 г (10 ммолей) коричного ангидрида в хлороформе. Смесь перемешивают при комнатной температуре в течение 24 часов. Затем реакционную смесь разбавляют 50 мл этилацетата и промывают 2 порциями 5%-ного водного раствора лимонной кислоты, водой, 2 порциями 5%-ного водного раствора гидрокарбоната натрия, водой и насыщенным водным раствором хлористого натрия. Органический слой отделяют и сушат безводным сульфатом натрия. Сульфат натрия отфильтровывают и фильтрат концентрируют в вакууме. Осадок перекристаллизовывают из смеси этилацетат-петролейный эфир, получают 1.67 г (выход 71%) соединения (2-1b) в виде чешуек. Идентификация строения полученного соединения проводится с помощью спектра ПМР.
Спектр ПМР (400 МГц, CDCl3, м.д.): 3.80 (3Н, с, -OCH3), 4.20 (2Н, с, 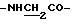 ), 6.15 (1Н, уш., -CONH-), 6.45 (1Н, д,
), 6.15 (1Н, уш., -CONH-), 6.45 (1Н, д, 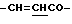 ), 7.45 (5Н, дд, ароматические H), 7.75 (1Н, д,
), 7.45 (5Н, дд, ароматические H), 7.75 (1Н, д, 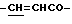 ).
).
12-2: Синтез циннамоилглицина [соединение (2-1), k = 1, R1b = H]
В 10 мл метанола растворяют 402 мг (1.7 ммоля) соединения (2-1b) и затем при охлаждении льдом добавляют 468 мкл (1.87 ммоля) 4 М водного раствора гидроксида натрия. Смесь перемешивают при комнатной температуре в течение 24 часов. Полученную реакционную смесь концентрируют в вакууме и экстрагируют названное соединение в водную фазу после добавления хлороформа в воды. К водной фазе добавляют лимонную кислоту до кислой среды, с последующей экстракцией 3 порциями этилацетата. Органический слой отделяют, промывают насыщенным водным раствором хлористого натрия в сушат безводным сульфатом натрия. Сульфат натрия отфильтровывают и фильтрат упаривают в вакууме. Полученные на стеклянном фильтре кристаллы промывают эфиром и сушат в вакууме, получают 324 мг (выход 86%) соединения (2-1), т.пл. 194.7 - 197.3oC.
Спектр ПМР (400 МГц, CDCl3-ДМСО, δ м.д.): 4.11 (2Н, дд, 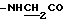 ), 6.60 (1H, дд,
), 6.60 (1H, дд, 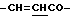 ), 7.05 (1Н, уш., -CONH-), 7.37 (3Н, м, ароматические H в положениях 3, 4, 5), 7.52 (2H, дд, ароматические H в положениях 2, 6), 7.61 (1H, д,
), 7.05 (1Н, уш., -CONH-), 7.37 (3Н, м, ароматические H в положениях 3, 4, 5), 7.52 (2H, дд, ароматические H в положениях 2, 6), 7.61 (1H, д, 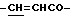 ).
).
Пример 13
Синтез циннамоил-β-аланина [соединение (2-2), k = 2, R1b = H]
13-1: Синтез этилового эфира циннамоил-β-аланина [соединение (2-2b), k - 2, R1b = C2H5]
Указанное соединение синтезируют по методике примера 12-1 с использованием хлоргидрата этилового эфира β-аланина вместо хлоргидрата этилового эфира глицина. Выход 58%.
13-2: Синтез циннамоил-β-аланина [соединение (2-2), k = 2, R1b = H]
Указанное соединение синтезируют по методике примера 12-2 с использованием соединения (2-2b). Вместо соединения (2-1b). Выход 85%, т.пл. 140.2 - 143.7oC.
Спектр ПМР (400 МГц, CDCl3-ДМСО, δ м.д.): 2.78 (2Н, т, 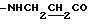 ), 3.63 (2Н, дд,
), 3.63 (2Н, дд, 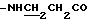 ), 6.43 (1Н, д,
), 6.43 (1Н, д, 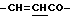 ), 6.80 (1H, уш., COOH), 7.35 (3Н, м, ароматические H в положениях 3, 4, 5), 7.50 (2Н, д, ароматические H в положениях 2, 6), 7.59 (1H, д,
), 6.80 (1H, уш., COOH), 7.35 (3Н, м, ароматические H в положениях 3, 4, 5), 7.50 (2Н, д, ароматические H в положениях 2, 6), 7.59 (1H, д, 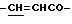 ).
).
Пример 14
Синтез циннамоил-γ-аминомаслянной кислоты [соединение (2-3), k = 3, R1b = H]
В 2 мл воды растворяют 1.03 г (10 ммолей) γ-aминомаслянной кислоты и затем при охлаждении льдом добавляют по каплям 2.5 мл 4 М водного раствора гидроксида натрия и 3 мл раствора 1.58 мл циннамоилхлорида в диоксане в 3 порции каждый, поддерживая таким образом щелочную среду. По окончании добавления реакционную смесь перемешивают в течение 24 часов при комнатной температуре и диоксан отгоняют при пониженном давлении. Оставшийся водный раствор для удаления исходных компонентов дважды промывают этилацетатом. Водный раствор подкисляют лимонной кислотой и названное соединение экстрагируют этилацетатом. Органический слой сушат безводным сульфатом натрия и раствор концентрируют в вакууме. Полученные кристаллы перекристаллизовывают из смеси этанол/эфир/гексан, получают 1.98 г (выход 85%) соединения (2-3) в виде белых кристаллов, т.пл. 82.5 - 83.6oC.
Спектр ПМР (400 МГц, CDCl3, δ м.д.): 1.93 (2Н, м, 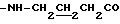 ), 2.45 (2Н, т,
), 2.45 (2Н, т, 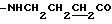 ), 3.48 (2Н, м,
), 3.48 (2Н, м, 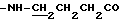 ), 5.97 (1Н, уш., CONH), 6.40 (1Н, д,
), 5.97 (1Н, уш., CONH), 6.40 (1Н, д, 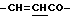 ), 7.33 (3H, м, ароматические H в положениях 3, 4, 5), 7.49 (2Н, д, ароматические H в положениях 2, 6), 7.64 (1H, д,
), 7.33 (3H, м, ароматические H в положениях 3, 4, 5), 7.49 (2Н, д, ароматические H в положениях 2, 6), 7.64 (1H, д, 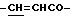 ).
).
Пример 15
Синтез циннамоил-6-аминокапроновой кислоты [соединение (2-4), k = 5, R1b = H]
Указанное соединение синтезируют по методике примера 14 с использованием 6-аминокапроновой кислоты вместо γ -аминомасляной кислоты. Выход 77%, т.пл. 91.6 - 92.3oC.
Спектр ПМР (400 МГц, CDCl3, δ м.д.): 1.44 (2Н, м, 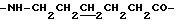 ), 1.61 (2Н, м,
), 1.61 (2Н, м,  ), 1.69 (2Н, м,
), 1.69 (2Н, м, 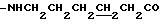 ), 2.38 (2Н, т, -NH(CH2)4CH2CO), 3.40 (2Н, м,
), 2.38 (2Н, т, -NH(CH2)4CH2CO), 3.40 (2Н, м, 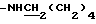 ), 5.68 (1Н, уш., CONH), 6.37 (1Н, д,
), 5.68 (1Н, уш., CONH), 6.37 (1Н, д, 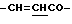 ), 7.35 (3Н, м, ароматические H в положениях 3, 4, 5), 7.48 (2H, д, ароматические H в положениях 2, 6), 7.61 (1H, д,
), 7.35 (3Н, м, ароматические H в положениях 3, 4, 5), 7.48 (2H, д, ароматические H в положениях 2, 6), 7.61 (1H, д, 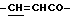 ).
).
[3-1] Примеры 16 - 18: Синтез соединения формул (3) и (11):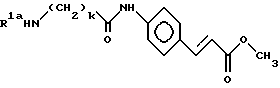
(в заместителе R2, R3 = R4 = H, R5 = CH3)
Пример 16
Синтез хлоргидрата метилового эфира 4-(4-аминобутириламино)коричной кислоты [соединение (3а-1), k = 3, R1a = H]
16-1: Синтез соединения (3-1), k = 3, R1a = Boc
В 3 мл хлороформа растворяют 2.02 г (10 ммолей) трет.-бутоксикарбонил-аминомасляной кислоты и затем при охлаждении льдом последовательно добавляют 1.38 мл (10 ммолей) триэтиламина и 1.28 г (10 ммолей) диметилфосфинотиоилхлорида. Смесь перемешивают при комнатной температуре в течение 10 минут. При охлаждении раствора льдом добавляют 532 мг (3 ммоля) хлоргидрата метилового эфира п-аминокоричной кислоты и 3 мл раствора 417 мкл (3 ммоля) триэтиламина в хлороформе, после чего добавляют еще 417 мкл (3 ммоля) триэтиламина. Смесь перемешивают при комнатной температуре в течение 24 часов. По окончании реакции хлороформ отгоняют в вакууме, остаток разбавляют этилацетатом и последовательно в указанном порядке промывают 2 порциями 5%-ного водного раствора лимонной кислоты, водой, 2 порциями 5%-ного водного раствора гидрокарбоната натрия, водой и насыщенным водным раствором хлористого натрия. Органический слой сушат безводным сульфатом натрия. Затем сульфат натрия отфильтровывают и фильтрат сушат в вакууме, получают 483 мг (выход 44%) соединения (3-1).
16-2: Синтез хлоргидрата метилового эфира 4-(4-аминобутириламино) коричной кислоты [соединение (3а-1), k = 3, R1a=H]
К 409 мг (1.13 ммоля) соединения (3-1) добавляют при охлаждении льдом 4 мл 4 Н раствора HCl в диоксане и смесь перемешивают при комнатной температуре в течение 30 минут. По окончании реакции добавляют 30 мл безводного эфира, образующийся осадок отфильтровывают с помощью стеклянного фильтра и промывают 2 или 3 порциями эфира, сушат в вакууме, получают соединение (3а-1) в виде белого твердого вещества. Выход 92%, т.пл. 206.0 - 208.0oC.
Спектр ПМР (400 МГц, D2O, δ м.д.): 2.07 (2Н, м, 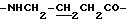 ), 2.62 (2Н, т,
), 2.62 (2Н, т, 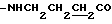 ), 3.10 (2Н, т,
), 3.10 (2Н, т, 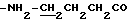 ), 3.82 (3Н, с, -COOCH3), 6.53 (1Н, м,
), 3.82 (3Н, с, -COOCH3), 6.53 (1Н, м, 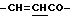 ), 7.53 (2Н, м, ароматические H в положениях 2, 6), 7.58 - 7.76 (3Н, м, ароматические H в положениях 3, 5,
), 7.53 (2Н, м, ароматические H в положениях 2, 6), 7.58 - 7.76 (3Н, м, ароматические H в положениях 3, 5, 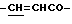 ).
).
Пример 17
Синтез хлоргидрата метилового эфира 4-(6-аминогексаноиламино)коричной кислоты [соединение (3а-2), k = 5, R1a = H]'
17-1: Синтез соединения (3а-2), k = 5, R1a = Boc
Повторяют методику примера 16-1 и получают названное соединение, выход 40%.
17-2: Синтез хлоргидрата метилового эфира 4-(6-аминогексаноиламино)коричной кислоты [соединение (3а-2), k = 5, R1a = H]
Повторяют методику примера 16-2 и получают названное соединение. Выход 97%, т.пл. 215.4 - 219.6oC.
Спектр ПМР (400 МГц, D2O, δ м.д.): 1.47 (2Н, м, 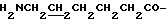 ), 1.72 (4Н, м,
), 1.72 (4Н, м, 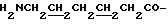 ), 2.48 (2Н, т,
), 2.48 (2Н, т, 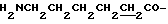 ), 3.03 (2Н, т,
), 3.03 (2Н, т, 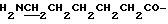 ), 3.82 (3Н, с, -COOCH3), 6.53 (1Н, м,
), 3.82 (3Н, с, -COOCH3), 6.53 (1Н, м, 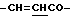 ), 7.51 (2Н, д, ароматические H в положениях 2, 6), 7.61-7.76 (3Н, м, ароматические H в положениях 3, 5,
), 7.51 (2Н, д, ароматические H в положениях 2, 6), 7.61-7.76 (3Н, м, ароматические H в положениях 3, 5, 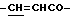 ).
).
Пример 18
Синтез хлоргидрата метилового эфира 4-(12-аминододеканоиламино)коричной кислоты [соединение (3а-3), k = 11, R1a = H]
18-1: Синтез соединения (3-3), k = 11, R1a = Boc
Повторяют методику примера 16-1 и получают названное соединение. Выход 72%.
18-2: Синтез хлоргидрата метилового эфира 4-(12-аминододеканоиламино)коричной кислоты [соединение (3а-3), k = 11, R1a = H]
Повторяют методику примера 16-2 и получают названное соединение. Выход 94%, т.пл. 210.2 - 217.0oC.
Спектр ПМР (400 МГц, CDCl3-DMSO-D2O, δ м.д.): 1.20 - 1.38 (14Н, м, 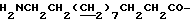 ), 1.53 - 1.69 (4Н, м,
), 1.53 - 1.69 (4Н, м, 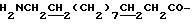 ), 2.34 (2Н, т,
), 2.34 (2Н, т, 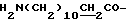 ), 2.80 (2Н, т,
), 2.80 (2Н, т, 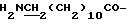 ), 3.73 (3Н, с, -COOCH3), 6.38 (1Н, д,
), 3.73 (3Н, с, -COOCH3), 6.38 (1Н, д, 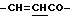 ), 7.52 (2Н, д, ароматические H в положениях 2, 6), 7.58 (1H, д,
), 7.52 (2Н, д, ароматические H в положениях 2, 6), 7.58 (1H, д, 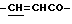 ), 7.68 (2Н, м, ароматические H в положениях 3, 5).
), 7.68 (2Н, м, ароматические H в положениях 3, 5).
[3-2] Примеры 19 - 21: Синтез соединений формул (3) и (12):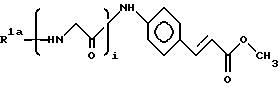
(в заместителе R2, R3 = R4 = H, R5 = CH3; в формуле (12) R8 = H)
Пример 19
Синтез хлоргидрата метилового эфира глициламинокоричной кислоты [соединение (3а-4), i = 1, R1a = H]
19-1: Синтез соединения (3-4), i = 1, R1a = Boc
Используя трет. -бутоксикарбонилглицин вместо трет.-бутоксикарбонил- γ -аминомасляной кислоты, повторяют методику Примера 16-1 и получают названное соединение. Выход 73%.
19-2: Синтез хлоргидрата метилового эфира глициламинокоричной кислоты [соединение (3а-4), i = 1, R1a = H]
Используя соединение (3-4) вместо соединения (3-1), повторяют методику примера 16-2. Получают названное соединение (3а-4), выход 98%, т.пл. 218.6 - 225.6oC.
Спектр ПМР (400 МГц, D2O, δ м.д.): 3.86 (3Н, с, COOCH3), 4.02 (2Н, с, Gly- α -H), 6.63 (1Н, д, -CH-CHCO-), 7.66 (2Н, м, ароматические H в положениях 2, 6), 7.75 (2Н, м, ароматические H в положениях 3, 5 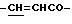 ).
).
Пример 20
Синтез хлоргидрата метилового эфира глицилглициламинокоричной кислоты [соединение (3а-5), i = 2, R1a = H]
20-1: Синтез соединения (3-5), i = 1, R1a = Boc
В 3 мл хлороформа растворяют 526 мг (3 ммоля) трет.-бутоксикарбонилглицина и затем при охлаждении льдом добавляют последовательно 416 мкл (3 ммоля) триэтиламина и 1 мл раствора 386 мг (3 ммолей) диметилфосфинотиоилхлорида в хлороформе. Смесь перемешивают при комнатной температуре в течение 15 мин, после чего при охлаждении льдом добавляют 416 мкл (3 ммоля) триэтиламина и 10 мл отдельно приготовленного раствора 812 мг (3 ммоля) соединения (3а-4) и 416 мкл (3 ммоля) триэтиламина в хлороформе, полученную смесь перемешивают при комнатной температуре в течение 20 минут. Полученную реакционную смесь упаривают в вакууме, остаток разбавляют этилацетатом и последовательно промывают 2 порциями 5%-ного водного раствора лимонной кислоты, водой, 2 порциями 5%-ного водного раствора гидрокарбоната натрия, водой и насыщенным водным раствором хлористого натрия. Органический слой сушат безводным сульфатом натрия, сульфат натрия отфильтровывают и фильтрат упаривают в вакууме. Полученные белые кристаллы промывают эфиром и сушат в вакууме. Получают 986 мг (выход 84%) соединения (3-5). Строение соединения подтверждается данными спектра ПМР.
Спектр ПМР (400 МГц, CDCl3, δ м.д.): 1.45 (9Н, с. Boc-), 3.80 (3Н, с, -COOCH3), 3.85 (2Н, c, BocGly- α -H), 4.15 (2Н, с, 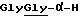 ), 5.15 (1H, уш.,
), 5.15 (1H, уш., 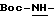 ), 6.40 (1H, д,
), 6.40 (1H, д, 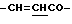 ), 7.55 (4Н, дд, ароматические H), 7.65 (1H, д,
), 7.55 (4Н, дд, ароматические H), 7.65 (1H, д, 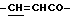 ), 8.55 (1H, уш.,
), 8.55 (1H, уш., 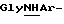 ).
).
20-2: Синтез хлоргидрата метилового эфира глицилглициламинокоричной кислоты [соединение (3а-5), i = 2, R1a = H]
К 543 мг (1.4 ммоля) соединения (3-5) при охлаждении льдом добавляют 4 мл 4 М раствора HCl/диоксан и полученную смесь перемешивают в течение 40 мин. К этой смеси добавляют этиловый эфир, образующиеся кристаллы отфильтровывают, промывают эфиром и сушат в вакууме. Получают 199 мг (выход 61%) соединения (3а-5) в виде белых кристаллов, т.пл. 219.3 - 231.0oC.
Спектр ПМР (400 МГц, D2O, δ м.д.): 3.83 (3Н, с, -COOCH3), 3.94 (2Н, c. 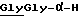 ), 4.19 (2H, с,
), 4.19 (2H, с, 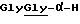 ), 6.54 (1H, д,
), 6.54 (1H, д, 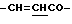 ), 7.54 (2Н, д, ароматические H в положениях 2, 6), 7.68 (2Н, д, ароматические H в положениях 3, 5), 7.73 (1Н, д,
), 7.54 (2Н, д, ароматические H в положениях 2, 6), 7.68 (2Н, д, ароматические H в положениях 3, 5), 7.73 (1Н, д,  ).
).
Синтез хлоргидрата метилового эфира триглициламинокоричной кислоты [соединение (3а-6), i = 3, R1a = H]
21-1: Синтез соединения (3-6), i = 3, R1a = Boc
В 1 мл диоксана растворяют 88 мг (0.5 ммоля) трет.-бутоксикарбонилглицина и затем при охлаждении льдом последовательно добавляют 69.5 мкл (0.5 ммоля) триэтиламина и 1 мл раствора 64 мг (0.5 ммоля) диметилфосфинотиоилхлорида в диоксане. Полученную смесь перемешивают при комнатной температуре в течение 25 минут. Затем при охлаждении льдом добавляют 69.5 мкл (0.5 ммоля) триэтиламина в диоксане и смесь перемешивают при комнатной температуре в течение 1 часа. К полученной реакционной смеси добавляют 1 мл водного аммиака, а затем перемешивают в течение 20 минут. Раствор упаривают в вакууме и остаток разбавляют этилацетатом и последовательно промывают 2 порциями 5%-ного водного раствора лимонной кислоты, водой, 2 порциями 5%-ного водного раствора гидрокарбоната, водой и насыщенным водным раствором хлористого натрия. Органический слой сушат безводным сульфатом натрия. Сульфат натрия отфильтровывают и фильтрат упаривают в вакууме. Полученные белые кристаллы собирают и промывают эфиром, сушат в вакууме. Получают 153 кг (выход 89%) соединения (3-6).
21-2: Синтез хлоргидрата метилового эфира триглициламинокоричной кислоты [соединение (3а-6), i = 3, R1a = H]
К 137 мг (0.4 ммоля) соединения (3-6) при охлаждении льдом добавляют 3 мл 4 М раствора HCl/диоксан и полученную смесь перемешивают в течение 2 часов. К реакционной смеси добавляют этиловый эфир и отфильтровывают образующиеся кристаллы, промывают их эфиром, сушат в вакууме. Получают 110 мг (выход 98%) соединения (3а-6) в виде белых кристаллов, т.пл. 227.3 - 235.8oC.
Спектр ПМР (400 МГц, D2O, δ м.д.): 3.83 (3Н, с, -COOCH3), 3.94 (2Н, c, 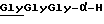 ), 4.12 (2Н, с,
), 4.12 (2Н, с, 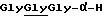 ), 4.4 (2Н, с,
), 4.4 (2Н, с, 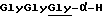 ), 6.54 (1Н, дд,
), 6.54 (1Н, дд, 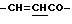 ), 7.55 (2Н, д, ароматические H в положениях 2, 6), 7.66 (2Н, д, ароматические H в положениях 3, 5), 7.72 (1H, дд,
), 7.55 (2Н, д, ароматические H в положениях 2, 6), 7.66 (2Н, д, ароматические H в положениях 3, 5), 7.72 (1H, дд, 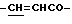 ).
).
[Синтез полимерных производных коричной кислоты и сшитых полимерных производных коричной кислоты]
Полимерное производное коричной кислоты до облучения УФ-светом называется фотоотверждаемой пленкой и сшитый полимер коричной кислоты после УФ-облучения называется отвержденной пленкой. Упоминаемый в примерах гелевый индекс рассчитывается по следующему уравнению: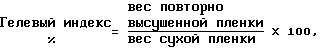
где вес повторно высушенной пленки = вес, найденный после погружения пленки в 10000 объемных частей воды на 24 часа при комнатной температуре, выделения пленки путем фильтрования, сушки в вакууме и взвешивания сухой пленки;
вес сухой пленки = вес пленки после сушки в вакууме до смачивания и последующей сушки.
Степень замещения производного коричной кислоты или CЗ (степень замещения) рассчитывается из мольного отношения производного коричной кислоты, введенной в дисахаридный фрагмент гиалуроновой кислоты или сульфата хондроитина на основе спектра ПМР или по данным поглощения в соответствии со следующим уравнением:
ПРИМЕРЫ 22-32. Производные коричная кислота - полимер формул (13) и соответствующие сшитые производные коричная кислота - полимер, в которых заместитель P1 представляет собой гиалуроновую кислоту.
Пример 22
22-1: Получение фотоотверждаемой пленки при введении соединения (1а-1) [соединения 1a-1-HA]
В 60 мл воды растворяют 400 мг (1.0 ммоля дисахаридных фрагментов) гиалуроновой кислоты со средним молекулярным весом 800000, а затем добавляют 30 мл 1,4-диоксана. При охлаждении льдом добавляют 300 мкл 0.2 М водного раствора N-гидроксисукцинимида и 300 мкм 0.1 М водного раствора водорастворимого карбодиимида и после перемешивания в течение 5 минут добавляют 300 мкл 0.1 М водного раствора соединения (1a-1). Полученную смесь перемешивают при комнатной температуре в течение 4 часов и по окончании этого времени добавляют 350 мл насыщенного раствора ацетата натрия в этаноле, при этом образуется осадок рассматриваемого соединения. Осадок собирают центрифугированием (2500 об/мин • 5 минут), промывают 3 порциями 80%-ного этанола и затем растворяют в 175 мл воды. Полученный раствор выливают в 2 кюветы с плоским дном размерами 90 мм х 62 мм и сушат в печи при 45oC. Получают образцы пленки. Выход составляет 350 мг. Пленка имеет степень замещения 0.58% (определяется по ее поглощению).
22-2: Получение отвержденной пленки при УФ-сшивке отверждаемой пленки [соединение 1a-1-HA]
Пленку, полученную в примере 22-1, укладывают между двумя стеклянными пластинами из пиростекла (Pуrex) толщиной 2.4 мм и облучают с каждой стороны ультрафиолетовым светом с помощью УФ-излучателя (источник света: галогеновая лампа на 3 КВт, расстояние 125 мм, скорость конвейера 1 мл/мин; аналогичные условия используются и в последующих примерах) в течение 4 минут с каждой стороны, всего 8 минут. Гелевый индекс 107%.
Примеры 23 - 28 и 30 - 32
Используя производные коричной кислоты, перечисленные в таблице 1, по методике примера 22 получают фотоотверждаемые пленки и отвержденные пленки.
Пример 29
29-1: Получение фотоотверждаемой пленки введением соединения (1а-8) [соединение 1a-1-HA]
В 50 мл воды растворяют 200 мг (0.5 ммоля дисахаридных фрагментов) гиалуроновой кислоты со средним молекулярным весом 800000, а затем добавляют 10 мл 1,4-диоксана. При охлаждении льдом добавляют 200 мкл 0.5 М раствора N-гидроксисукцинимида в диоксане и 200 мкм 0.25 M водного раствора карбодиимида. Полученную смесь перемешивают в течение 5 минут, добавляют 1 мл водного раствора 14 мг (0.05 ммоля) соединения (1а-8). Полученную смесь перемешивают при комнатной температуре в течение 2 ч и по окончании этого времени добавляют 350 мл насыщенного раствора ацетата натрия в этаноле, при этом образуется осадок рассматриваемого соединения. Осадок собирают центрифугированием (2500 об/мин х 5 минут), промывают 3 порциями водного этанола и затем растворяют в 80 мл воды. Полученный раствор выливают в кювету с плоским дном размерами 90 мм х 62 мм, сушат в печи и получают пленку. Выход составляет 201 мг. Пленка имеет степень замещения 0.70% (определяется по величине поглощения).
29-2: Получение отвержденной пленки при УФ-сшивке фотоотверждаемой пленки [соединение 1a-8-HAl
Пленку, полученную в примере 29-1, укладывают между двумя пластинами из пиростекла (Pyrex) толщиной 2.4 мм и облучают с каждой стороны ультрафиолетовым светом с помощью УФ-излучателя (источник света: галогеновая лампа на 3 КВт, расстояние 125 мм, скорость конвейера 1 мл/мин) в течение 4 минут для каждой стороны, всего 8 минут.
Гелевый индекс 94%.
ПРИМЕРЫ 33-36 При получении производных коричной кислоты и полимера формулы (14) и соответствующих сшитых производных коричной кислоты и полимера в качестве заместителя P2 используют хитозан, а фрагмент B-P2 образуется за счет амидной связи.
Пример 33
33-1: Получение фотоотверждаемой пленки [соединение (2-1-CHS)] при введении соединения (2-1)
В 1 мл диметилформамида (ДМФА) растворяют 44 мг (0.2 ммоля) соединения (2-1) и при охлаждении льдом добавляют 400 мкл 0.5 М раствора диметилфосфинотиоилхлорида в ДМФА и 28 мкл (0.2 ммоля) триэтиламина. Полученную смесь перемешивают при комнатной температуре в течение 10 минут и затем добавляют к раствору 290 мг (0.2 ммоля/GlcN) хитозана (фирмы Seikagaku Corporation) в смеси 50 мл 2%-ной уксусной кислоты и 50 мл метанола. Смесь перемешивают при комнатной температуре в течение 24 часов, после чего разбавляют 1 мл 1 М водного раствора гидроксида натрия и выливают в 250 мл этанола, а затем центрифугируют (2500 об/мин х 5 минут). Полученный осадок промывают 3 порциями 80%-ного этанола и растворяют в 150 мл воды. Полученный раствор выливают в кювету с плоским дном размерами 96 мм х 137 мм. Отливку сушат в печи при 45oC. Получают прозрачную пленку весом 320 мг.
33-2: Получение отвержденной пленки путем УФ-сшивки фотоотверждаемой пленки [соединение 2H-1-CHS]
Пленку, полученную в примере 33-1, размещают между двумя пластинами из пиростекла (Pуrex) толщиной 2.4 мм и облучают с каждой стороны ультрафиолетовым светом с помощью УФ-излучателя (источник света: галогеновая лампа на 3 КВт, расстояние 125 мм, скорость конвейера 1 мл/мин) в течение 4 минут для каждой стороны, всего 8 минут. Получают нерастворимую в воде пленку.
Примеры 34 - 36
Используя производные коричной кислоты, перечисленные в таблице 1, по методике примера 33 получают фотоотверждаемые пленки и отвержденные пленки.
ПРИМЕРЫ 37 - 42. Производные коричной кислоты и полимера формулы (15) и соответствующие сшитые производные коричная кислота - полимер, в которых заместитель P1 представляет собой гиалуроновую кислоту.
Пример 37
37-1: Получение фотоотверждаемой пленки введением соединения (3а-1) [соединение 3а-1-HA]
В 50 мл воды растворяют 200 мг (0.5 ммоля дисахаридных фрагментов) гиалуроновой кислоты со средним молекулярным весом 800000, а затем добавляют 10 мл 1,4-диоксана. При охлаждении льдом последовательно добавляют 200 мкл 0.5 М раствора N-гидроксисукцинимида в диоксане и 200 мкл 0.25 М водного раствора карбодиимида. После перемешивания в течение 2 минут добавляют 1 мл водного раствора 12 мг (0.05 ммоля) соединения (3а-1). Полученную смесь перемешивают при комнатной температуре в течение 3 часов и 40 минут, после чего добавляют 350 мл насыщенного раствора ацетата натрия в этаноле, при этом образуется осадок названного соединения. Осадок собирают центрифугированием (2500 об/мин х 5 минут), промывают 3 порциями водного этанола и затем растворяют в 40 мл воды. Полученный раствор выливают в кювету с плоским дном размерами 90 мм х 62 мм, сушат в печи при 45oC и получают пленку. Выход составляет 182 мг. Пленка имеет степень замещения 1.7% (определяется по величине поглощения).
37-2: Получение отвержденной пленки путем УФ-сшивки фотоотверждаемой пленки [соединение 3а-1-HA]
Пленку, полученную в Примере 37-1, размещают между двумя пластинами из пиростекла (Pyrex) толщиной 2.4 мм и облучают с каждой стороны ультрафиолетовым светом с помощью УФ-излучателя (источник света: галогеновая лампа на 3 КВт, расстояние 125 мм, скорость конвейера 1 мл/мин) в течение 2 минут для каждой стороны, всего 4 минуты.
Гелевый индекс 99%.
Примеры 38 - 42
Используя производные коричной кислоты, перечисленные в таблице 1, по методике примера 37 получают фотоотверждаемые пленки и отвержденные пленки.
Пример 43
При получении производного коричной кислоты и полимера формулы (13) и соответствующего сшитого производного коричной кислоты и полимера в качестве заместителя P1 используют сульфат хондроитина, а связь A-P1 представляет собой амидную связь, связывающую карбоксильную группу и сульфатный радикал P1.
43-1: Получение фотоотверждаемой пленки хондроитин-сульфата введением соединения (1d-4) [соединение (1a-4-CS)]
При использовании вместо гиалуроновой кислоты сульфата хондроитина по методике примера 25-1 получают названное соединение. CЗ = 0.79%.
43-2: Получение отвержденной пленки при УФ-сшивке фотоотверждаемой пленки [соединение (1a-4-CS)]
Пленку, полученную в примере 43-1, размещают между двумя пластинами из пиростекла (Pyrex) толщиной 2.4 мм и облучают с каждой стороны ультрафиолетовым светом с помощью УФ-излучателя (источник света: галогеновая лампа на 3 КВт, расстояние 125 мм, скорость конвейера 1 мл/мин) в течение 2 минут для каждой стороны, всего 4 минуты.
Пример 44
При получении производного коричной кислоты и полимера формулы (14) и соответствующего сшитого производного коричная кислота - полимер в качестве заместителя P2 используют сульфат хондроитина. При этом связь B-P2 представляет собой эфирную связь, включающую гидроксильную группу заместителя P2.
44-1: Получение фотоотверждаемой хондроитин-сульфатной пленки введением соединения (2-1) [соединение (1-1-CS)]
В этом примере соединение (2-1) вводится в гидроксильную функцию сульфата хондроитина (мол.вес 30000) за счет эфирной связи.
В 0.5 мл диметилформамида растворяют 13 мг (0.06 ммоля) соединения (2-1) и при охлаждении льдом добавляют 120 мкл 0.5 M раствора N-диметилфосфинотиоилхлорида в ДМФА и 10 мкл (0.06 ммоля) триэтиламина. Смесь перемешивают при комнатной температуре в течение 10 мин и затем добавляют отдельно приготовленный раствор 150 мг (0.3 ммоля) трибутиламинной соли хондроитин-сульфата в 17 мл ДМФА. Затем добавляют 7 мг (0.006 ммоля) 4-диметиламинопиридина и полученную смесь перемешивают при комнатной температуре в течение 24 часов. К полученной реакционной смеси добавляют 2 мл 5%-ного водного раствора гидрокарбоната натрия и смесь выливают в 150 мл насыщенного раствора ацетата натрия в этаноле, а затем центрифугируют (2500 х 5 минут). Полученный осадок промывают 3 порциями 80%-ного этанола и растворяют в 70 мл воды. Полученный раствор выливают в кювету с плоским дном размерами 35 мм х 65 мм. Отливку сушат в печи при 45oC. Получают прозрачную пленку весом 174 мг (CЗ = 18%).
44-2: Получение отвержденной пленки путем УФ-сшивки фотоотверждаемой пленки [соединение (2-1-CS)]
Пленку, полученную в примере 44-1, размещают между двумя пластинами из пиростекла (Pyrex) толщиной 2.4 мм и облучают с каждой стороны ультрафиолетовым светом с помощью УФ-излучателя (источник света: галогеновая лампа на 3 КВт, расстояние 125 мм, скорость конвейера 1 мл/мин) в течение 4 минут для каждой стороны, всего 8 минут. Получают нерастворимую в воде пленку.
Гелевый индекс 21%.
ПРИМЕРЫ 45 - 50 При получении производного коричной кислоты и полимера формулы (15) и соответствующего сшитого производного коричная кислота - полимер используют в качестве заместителя P1 хондроитин-сульфат. При этом связь C-P1 представляет собой амидную связь между карбоксильной группой и сульфатным радикалом P1.
Пример 45
45-1: Получение фотоотверждаемой хондроитин-сульфатной пленки введением соединения (3а-1) [соединение (3а-1-CS)]
Используя вместо натровой соли гиалуроновой кислоты хондроитин-сульфат, по методике примера 37-1 получают названное соединение (CЗ = 6%).
45-2: Получение отвержденной пленки путем УФ-сшивки фотоотверждаемой пленки [соединение (3а-1-CS)]
Пленку, полученную в примере 45-1, размещают между двумя пластинами из пиростекла (Pyrex) толщиной 2.4 мм и облучают с каждой стороны ультрафиолетовым светом с помощью УФ-излучателя (источник света: галогеновая лампа на 3 кВт, расстояние 125 мм, скорость конвейера 1 мл/мин) в течение 2 минут для каждой стороны, всего 4 минуты.
Гелевый индекс 73%.
Примеры 46-50
Используя производные коричной кислоты, перечисленные в таблице 1, по методике примера 45 получают фотоотверждаемые пленки и отвержденные пленки.
Результаты, полученные в примерах 22 - 50, представлены в таблицах 1 и 2.
Характеристики фотоотвержденных пленок на основе гиалуроновой кислоты в зависимости от сшивающей группы
В приведенных ниже примерах исследуются, главным образом, различия в свойствах пленок, которые обусловлены различиями в значениях n в приведенных выше структурных формулах производных гиалуроновой кислоты, содержащих производные коричной кислоты формулы
H2N-(CH2)n-OCOCH=CH-Ph.
Пример 51
В этом примере изучаются различия в реакционной способности по отношению гиалуроновой кислоты при введении производного коричной кислоты в зависимости от различий в значениях n в соединении (1-A) при идентичных условиях (фиг. 1). На фиг. 2 абсцисса представляет собой количество производного коричной кислоты, используемое из расчета на полисахаридный фрагмент гиалуроновой кислоты при приведенных ниже условиях, а ордината представляет собой степень замещения, CЗ.
[Условия реакции]
Соединение-хозяин: натриевая соль гиалуроновой кислоты (мол.вес 800000)
Растворитель: вода-диоксан (2:1)
Конденсирующий агент: N-гидроксисукцинимид, 2 мольных эквивалента / (1-A), водорастворимый карбодиимид, эквимольное количество / (1-а)
Температура реакции: комнатная температура
Время реакции: 24 часа.
Из фиг. 2 видно, что чем длиннее метиленовая цепочка, то есть, чем выше значение n, тем ниже реакционная способность. Следовательно, более высокое значение n приводит к увеличению, хотя и небольшому, гидрофильности самого соединения (1-A) и, соответственно, уменьшается сродство к растворителю или субстрату, следовательно, уменьшается реакционная способность.
Пример 52
В этом примере исследуются различия в скорости поглощения воды, которые обусловлены различиями в CЗ, сшитой под воздействием УФ-излучения в течение 4 мин пленки на основе гиалуроновой кислоты с введенными производными коричной кислоты, имеющими изменяющиеся значения n в формуле (1-A). Скорость поглощения воды рассчитывается с помощью следующего уравнения (фиг. 3):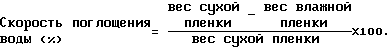
Вес сухой пленки: вес после сушки отвержденной пленки
Вес влажной пленки: вес после 1-часового вымачивания отвержденной пленки в воде.
По мере уменьшения CЗ и с достижением определенного уровня CЗ для всех проверенных отвержденных пленок скорость поглощения воды резко возрастает. Причина этого состоит в том, что поскольку уменьшение CЗ приводит к уменьшению плотности сшивки, сеточная структура становится грубой и может поглощать больше воды, но дальнейшее уменьшение плотности сшивки приводит к увеличению растворимости пленки. Анализ ответов, обусловленных различиями значений n, показывает, что чем выше значения n, тем больше график смещается по шкале CЗ в сторону более низких величин. Это означает, что более высокие значения n обеспечивают сеточную структуру, которая способна удержать больше влаги и может быть нерастворима при более низких значениях CЗ. Принимая во внимание сказанное выше, при создании сеточной структуры за счет реакции фотосшивки с использованием УФ-излучения можно, сохраняя CЗ на одном уровне, на основе фотореакционноспособного производного гиалуроновой кислоты, содержащего производное коричной кислоты с более высоким значением n, получать сеточную структуру с большей гибкостью. Это указывает на тот факт, что фотореакционная способность коричной кислоты имеет значительное влияние на характеристики отвержденной пленки.
Пример 53
В этом примере найдена зависимость между пределом прочности при растяжении и различными значениями CЗ сшитых пленок на основе гиалуроновой кислоты, полученных введением различных производных коричной кислоты, имеющих различные значения n в формуле (1-A), при воздействии УФ-излучения на пленку в течение 4 минут. Предел прочности при растяжении измеряют для погруженных в воду пленок с использованием реометра (фиг. 4).
Из фиг. 4 видно, что чем больше значение CЗ, тем выше плотность сшивки, следовательно, тем выше предел прочности при растяжении. Анализ зависимости между пределом прочности при растяжении и различными значениями n показывает, что чем выше n, тем больше график смещается по шкале CЗ в сторону меньших значений, показывая, что при сохранении значения CЗ на одном уровне более высокие значения n обеспечивают более высокую предельную прочность при растяжении.
Как показано в примере 52, при одинаковых значениях CЗ более высокие значения n приводят к большей эффективности реакции фотосшивки и получению пленки с более высокой плотностью сшивки. Так как предел прочности при растяжении считается пропорциональным значению n, более высокие значения n означают более высокий предел прочности при растяжении.
Пример 54
В этом примере изучается зависимость предела прочности при растяжении от скорости поглощения воды сшитыми пленками на основе гиалуроновой кислоты, которые получены введением различных производных коричной кислоты, имеющих различные значения n в соединении (1-A), при воздействии УФ-излучения на пленку в течение 4 минут (фиг. 5 и 6).
Фиг. 5 получают при нанесении величины поглощения воды по оси абсцисс и значений предела прочности при растяжении по оси ординат. Из фиг. 5 ясно видно, что независимо от значения n скорость поглощения воды обратно пропорциональна пределу прочности при растяжении. Фиг. 6 получают при нанесении обратных значений предела прочности при растяжении по оси ординат, при этом получают линейную зависимость.
Пример 55
В этом примере изучают зависимость критической точки перехода в нерастворимую форму сшитых пленок на основе гиалуроновой кислоты, полученных введением различных производных коричной кислоты, имеющих различные значения n в соединения (1-A), при воздействия УФ-излучения на пленку в течение 8 минут (фиг. 7). На оси абсцисс представлены значения n, на оси ординат - CЗ. Каждая нанесенная на графике точка представляет собой CЗ, соответствующую началу растворения, и каждые +/ точка соответствуют CЗ перехода нерастворимая форма - начало растворения, с критической точкой перехода в нерастворимую форму, находящейся между точкой и +. Критическая точка перехода в нерастворимую форму является также точкой перехода пленки в гель.
Пример 56
В этом примере исследуют влияние производных коричной кислоты, отличных от соединения (1-A), а именно производных, представленных формулами (7) и (9).
Относительная реакционная способность следующих сшиваемых соединений по отношению к натриевой соли гиалуроновой кислоты (молекулярный вес 800000) исследуется по методике примера 51. Эти производные коричной кислоты имеют одинаковое количество атомов в основной цепи между промежуточной аминогруппой и циннамоильной группой, но имеют различное строение спейсорной группы, то есть отличаются наличием эфирной связи, амидной связи или разветвленной цепи, помимо метиленовой
H2N-CH2CH2CH2CH2CH2-OCOCH=CH-Ph [соединение (1a-3)l;
H2N-CH2CH2-O-CH2CH2-OCOCH=CH-Ph [соединение (1а-7)1;
H2N-CH2-CONH-CH2CH2-OCOCH=CH-Ph [соединение (1a-9)];
H2N-CH(CH3)-CONH-CH2CH2-OCOCH=CH-Ph [соединение (1a-10);
H2N-CH[CH2CH(CH3)2]-CONH-CH2CH2- OCOCH=CH-Ph (соединение (1a-11)].
Полученные результаты показаны на фиг. 8, где на оси абсцисс представлено количество каждого производного коричной кислоты на дисахаридный фрагмент гиалуроновой кислоты, на оси ординат - степень замещения CЗ.
Соединения, имеющие в спейсере амидную связь, являются особенно реакционноспособными и среди них лучшую реакционную способность проявляют те, которые наименее разветвлены. Считается, что это является следствием гидрофильности спейсерной структуры.
Пример 57
Для пяти соединений, описанных в примере 56, по методике примера 52 изучена зависимость между CЗ и скоростью поглощения воды.
Результаты представлены на фиг. 9. Гидрофильные соединения (1a-9-HA) в (1a-10-HA), имеющие амидную связь и меньшую степень разветвления в спейсерной структуре, обладают более высокой скоростью поглощения при высоком по сравнению с другими соединениями уровне CЗ. На скорость поглощения воды заметно влияет плотность сшивки и рассматриваемые соединения с большой скоростью поглощения воды имеют более низкую плотность сшивки, чем другие соединения. Хотя сшитая структура образуется в результате фотореакции, описанной в примере 52, производное гиалуроновой кислоты, содержащее фотодимеризуемое соединение, содержащее высоко гидрофильный спейсер, как оказывается, является менее реакционноспособным, тогда как высоко гидрофобная структура имеет более высокую фотореакционную способность.
Хотя рассматриваемая фотореакция осуществляется отливанием водного раствора фотореакционноспособного производного гиалуроновой кислоты в пленку и облучением полученной пленки ультрафиолетовым светом, оказывается, что производное коричной кислоты, которое проявляет большую гидрофобность при образовании пленки, более склонно к объединению и поддается ориентации, обеспечивая таким образом лучшую среду для проведения фотореакции.
Гидрофобность вышеописанных соединений находится в следующем порядке:
соединение (1а-3) > соединение (1a-7) > соединение (1а-11) > соединение (1а-10) > соединение (1а-9).
Фотореакционная способность в фотореакции увеличивается при возрастании гидрофобности, а реакционная способность по отношению к гиалуроновой кислоте примера 56, наоборот, возрастает в порядке убывания гидрофобности.
Примеры 58 - 61
Способность к ферментативному разложению
Фотоотверждаемую пленку, приготовленную по описанию примера 25, облучают УФ-светом при условиях, приведенных в таблице 3, и определяют степень растяжения поверхности, гелевый индекс, степень ферментативного разложения (скорость разложения) отвержденной пленки.
Условия проведения ферментативного разложения описаны ниже.
Буфер; 0.2 М уксусная кислота - гидроксид натрия (pH 6)
Фермент: Гиалуронидаза (взята из яичка барана), 100 ед./мг
Температура: 37oC.
Способ оценки: Количество низкомолекулярной гиалуроновой кислоты, выделенное из отвержденной пленки при ферментативном разложении, определяют карбазольным методом и вычисляют степень разложения, сравнивая с начальным весом.

Как описано выше, создание производных коричной кислоты, содержащих спейсер, дает возможность получать производные коричной кислоты и полимера, в особенности производных коричной кислоты и гликозаминогликанов, которые обладают высокой чувствительностью и высокой эффективностью при проведении соответствующей реакции, обеспечивая таким образом получение сшитых производных коричной кислоты и глюкозаминогликанов, сохраняющих присущие последним положительные свойства, такие как биорезорбция, биосовместимость, нетоксичность, отсутствие антигенности и хорошее поглощение воды.
Хотя настоящее изобретение подробно описано с использованием конкретных примеров, квалифицированный в данной области специалист поймет, что в них могут быть сделаны различные изменения и модификации, которые не затрагивают сущности изобретения и его объема. Ыя
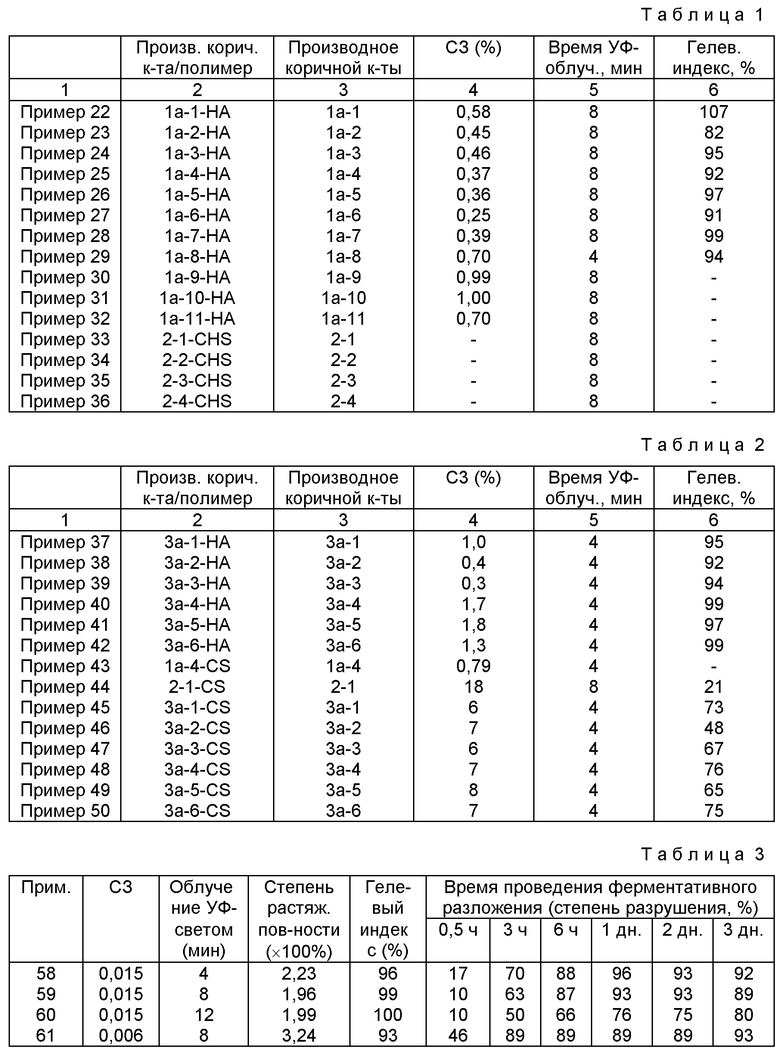
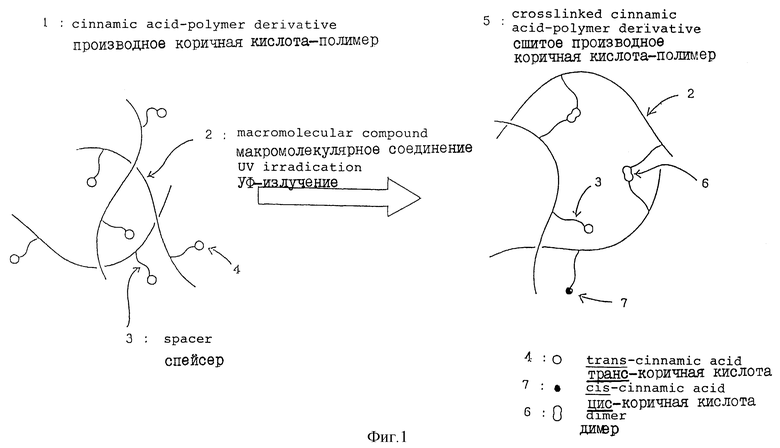
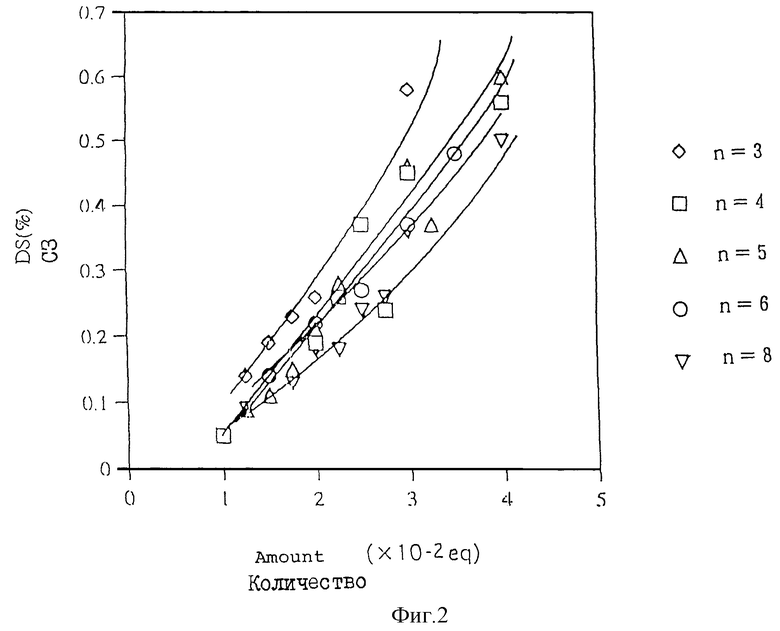
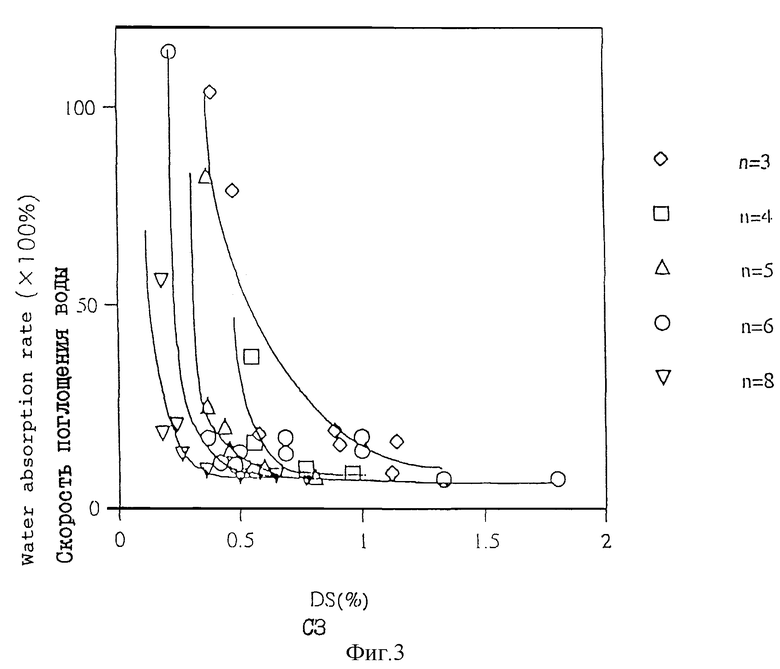
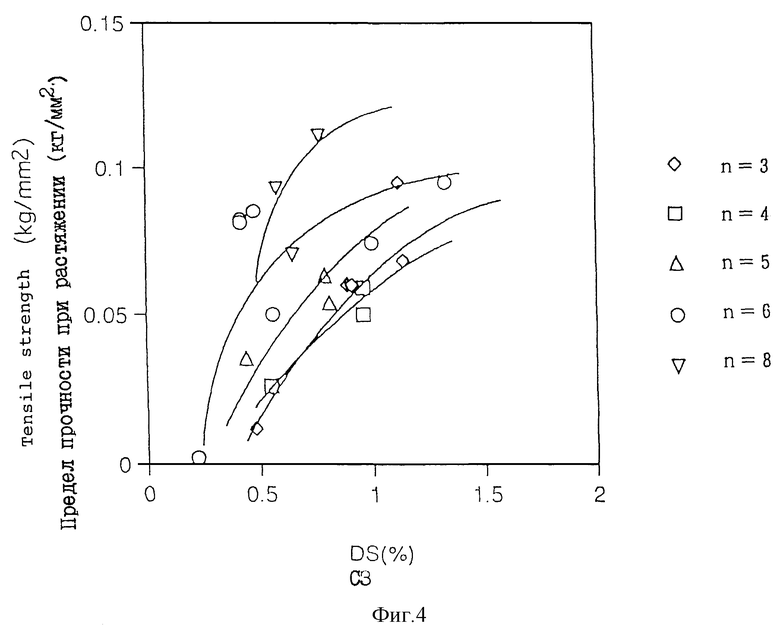
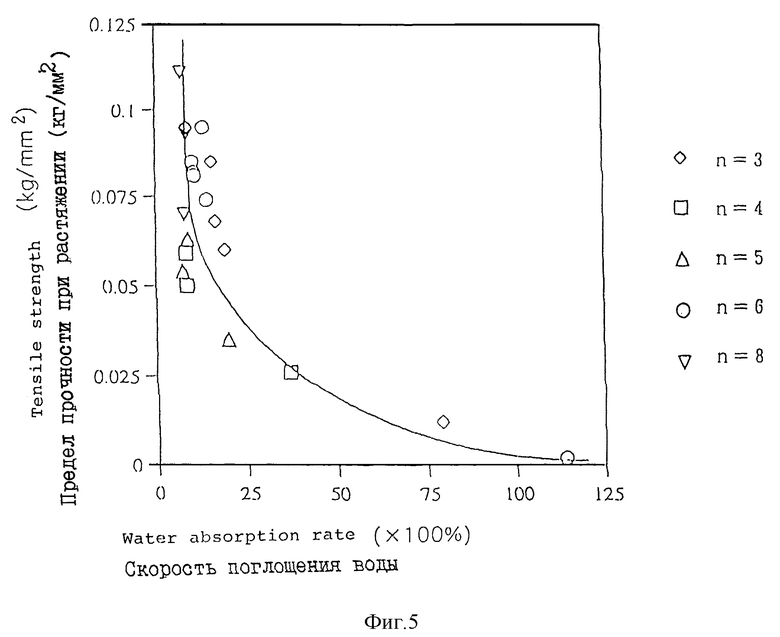
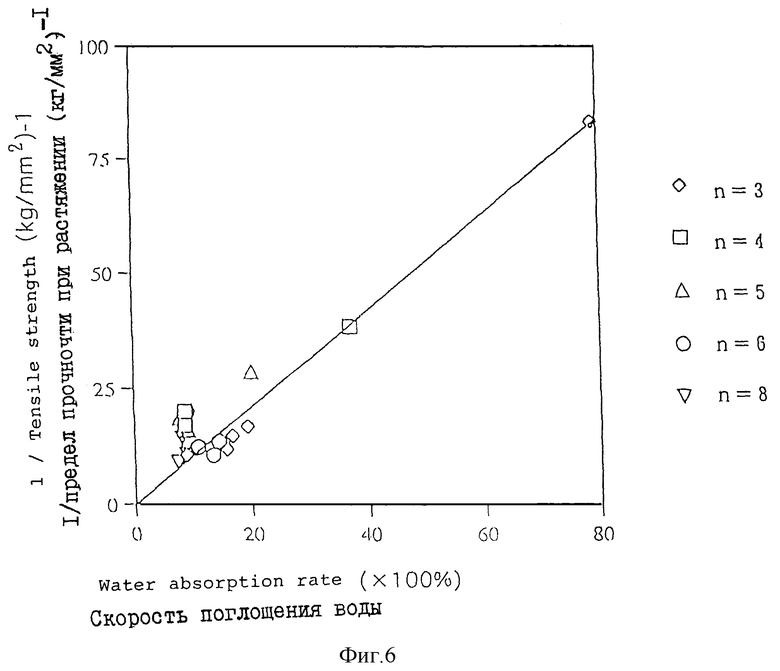
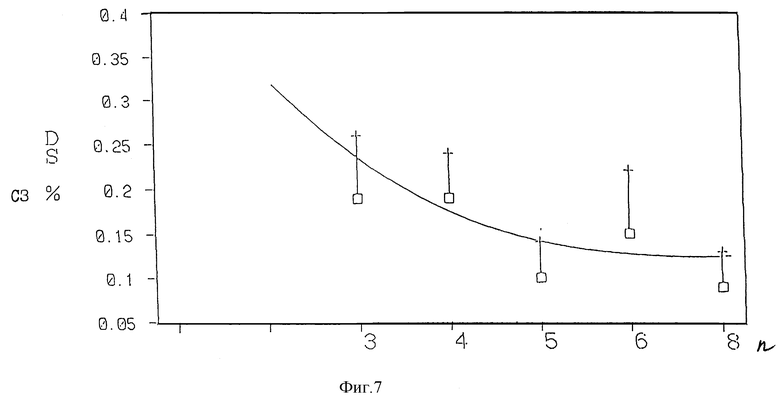
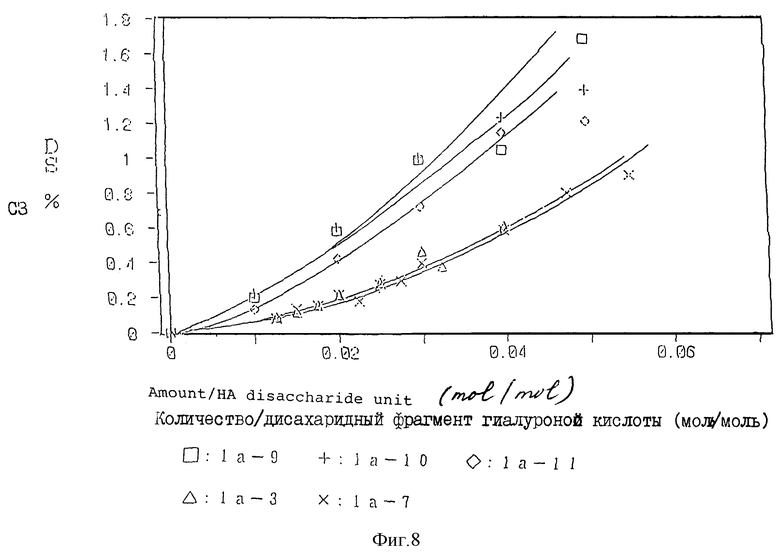
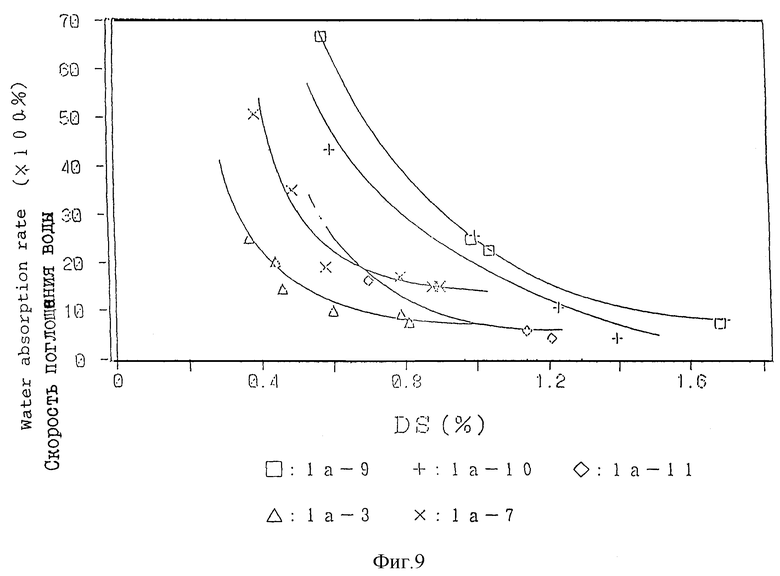
Описывается новое производное коричной кислоты, содержащее фотодимеризуемую сшивающую группу, представленное любой из формул (1) - (3), или его соль: R1 - A - H (1), R1 - В - ОН (2), R2 - С - H (3), где R1 представляет собой группу формулы (4), где R3 и R4 представляют собой водород; R2 представляет собой группу формулы (5), где R3 и R4 определены выше; R5 представляет собой низшую алкильную группу; фрагмент А-Н представляет собой внутримолекулярный остаток амино- и гидроксисодержащего соединения любой из формул (6) - (9): -O-(CH2)n-NH2 (6), где n обозначает целое число 3-18; -(O-CH2CH2)m-NH2 (7), где m обозначает целое число 2-10; -O-CHR6CH(COOR7)-NH2 (8), где R6 представляет собой водород; R7 представляет собой низший алкил; -O-(CH2)l-NHCO-CHR8-NH2 (9), где l обозначает целое число 2-18; R8 представляет собой боковую цепочку остатка о-аминокислоты, водород, низший алкил; фрагмент В-ОН представляет собой аминокислотный остаток формулы (10): -NH-(CH2)k-СООН (10), где k обозначает целое число 1-18; фрагмент С-Н представляет собой аминокислотный остаток формулы (11) или (12): -CO-(CH2)kNH2 (11), где k принимает значения, определенные выше; -(COCHR9NH)i-H (12), гдe i обозначает целое число 1-6; R9 представляет собой водород. Новые соединения могут быть использованы в качестве медицинского материала, обладающего биосовместимостью, биопоглощением и другими необходимыми свойствами. 7 с. и 19 з.п.ф-лы.
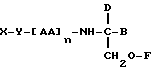
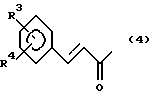
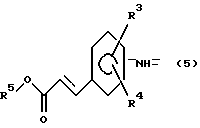
R1-А-Н (1),
R1-В-ОН (2),
R2-С-Н (3),
где R1 представляет собой группу формулы (4)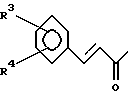
где R3 и R4 представляют собой водород;
R2 представляет собой группу формулы (5)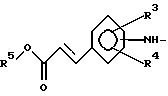
где R3 и R4 определены выше;
R5 представляет собой низшую алкильную группу;
фрагмент А-Н представляет собой внутримолекулярный остаток амино- и гидроксисодержащего соединения любой из формул (6) - (9):
-О-(СН2)n-NН2 (6),
где n обозначает целое число 3 - 18;
-(О-СН2СН2)m-NН2 (7),
где m обозначает целое число 2 - 10;
-О-СНR6СН(СООR7)-NН2 (8),
где R6 представляет собой водород;
R7 представляет собой низший алкил;
-О-(СН2)l-NНСО-СНR8-NН2 (9),
где l обозначает целое число 2 - 18;
R8 представляет собой боковую цепочку остатка α-аминокислоты, водород, низший алкил;
фрагмент В-ОН представляет собой аминокислотный остаток формулы (10)
-NН-(СН2)k-СООН (10),
где k обозначает целое число 1 - 18;
фрагмент С-Н представляет собой аминокислотный остаток формулы (11) или 12:
-СО-(СН2)k-NН2 (11),
где k принимает значения, определенные выше;
-(СОСНR9NН)i-Н (12),
где i обозначает целое число 1 - 6;
R9 представляет собой водород.
R1-А-Р1 (13),
R1-В-Р2 (14),
R2-С-Р1 (15),
где R1 представляет собой группу формулы (4)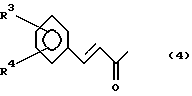
где R3 и R4 независимо друг от друга представляют собой водород;
R2 представляет собой группу формулы (5)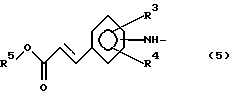
где R3 и R4 независимо друг от друга представляют собой водород;
R5 представляет собой низший алкил;
фрагмент А представляет собой остаток амино- и гидроксисодержащего соединения, представленный любой из формул (6') - (9'):
-О(СН2)n-NН- (6'),
где n обозначает целое число 3 - 18;
-(О-СН2СН2)m-NН- (7'),
где m обозначает целое число 2 - 10;
-О-СНR6СН(СООR7)-NН- (8'),
где R6 представляет собой водород;
R7 представляет собой низший алкил;
-О-(СН3)l-NНСО-СНR8-NН- (9'),
где l обозначает целое число 2 - 18;
R8 представляет собой боковую цепочку остатка α-аминокислоты, водород, низший алкил;
фрагмент В представляет собой аминокислотный остаток формулы (10')
-NН-(СН2)k-СО- (10'),
где k обозначает целое число 1 - 18;
фрагмент С представляет собой аминокислотный остаток формулы (11') или (12'):
-СО-(СН2)k-NН- (11'),
где k принимает значения, определенные выше;
-(СОСНR9NН)i (12'),
где i обозначает целое число 1 - 6;
R9 представляет собой водород;
Р1 представляет собой полисахаридный остаток, содержащий карбоксильную группу;
Р2 представляет собой полисахаридный остаток, содержащий амино- или гидроксигруппу;
связь А-Р1 представляет собой амидную связь, образованную между концевой аминогруппой формул (6'), (7'), (8') или (9') и карбоксильной группой заместителя Р1;
связь В-Р2 представляет собой амидную связь, образованную между концевой карбоксильной группой формулы (10') и аминогруппой заместителя Р2, или сложноэфирную связь, образованную между концевой карбоксильной группой формулы (10') и гидроксильной группой заместителя Р2;
связь С-Р1 представляет собой амидную связь, образованную концевой аминогруппой формулы (11') или (12') и карбоксильной группой заместителя Р1,
при условии, что когда производное коричной кислоты и полисахарида представлено формулой (13), фотодимеризуемая-сшивающая группа включена в состав производного коричной кислоты и полисахарида со степенью замещения 0,05 - 5,0% от содержания повторяющейся составляющей сахаридной единицы полисахарида.
R1-А-Р1 (13),
R2-С-Р1 (15),
где R1 представляет собой группу формулы (4)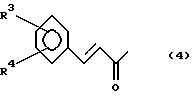
где R3 и R4 независимо друг от друга представляют собой водород;
R2 представляют собой группу формулы (5)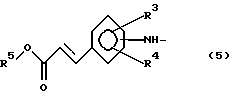
где R3 и R4 независимо друг от друга представляют водород;
R5 представляют собой низший алкил;
фрагмент А представляет собой остаток амино- и гидроксисодержащего соединения, представленный любой из формул (6') - (9'):
-О-(СН2)n-NН- (6'),
где n обозначает целое число 3 - 18;
-(О-СН2СН2)m-NН- (7'),
где m обозначает целое число 2 - 10;
-О-СНR6СН(СООR7)-NН- (8'),
где R6 представляет собой водород;
R7 представляет собой низший алкил;
-О-(СН2)l-NНСО-СНR8-NН- (9'),
где l обозначает целое число 2 - 18;
R8 представляет собой боковую цепочку остатка α-аминокислоты, водород, низший алкил;
фрагмент С представляет собой аминокислотный остаток формулы (11') или (12'):
-СО-(СН2)k-NН- (11'),
где k принимает значения, определенные выше;
-(СОСНR8NН)i (12'),
где i обозначает целое число 1 - 6;
R8 представляет собой водород;
Р1 представляет собой полисахаридный остаток, содержащий карбоксильную группу;
связь А-Р1 представляет собой амидную связь, образованную между концевой аминогруппой формул (6'), (7'), (8') или (9') и карбоксильной группой заместителя Р1;
связь С-Р1 представляет собой амидную связь, образованную концевой аминогруппой формулы (11') или (12') и карбоксильной группой заместителя Р1,
включающий стадии: (А) растворения полисахарида в воде или в воде, содержащей смешивающийся с водой органический растворитель и (В) взаимодействия карбоксильной группы полисахарида с аминогруппой производного коричной кислоты, содержащего фотодимеризуемую-сшивающую группу, представленного формулой (1) или (3):
R1-А-Н (1),
R2-С-Н (3),
где R1 представляет собой группу формулы (4)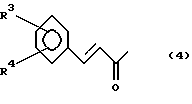
где R3 и R4 независимо друг от друга представляют собой водород;
R2 представляет собой группу формулы (5)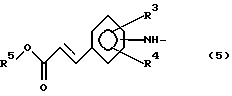
где R3 и R4 независимо друг от друга представляют собой водород;
R5 представляет собой низший алкил;
фрагмент А-Н представляет собой внутримолекулярный остаток амино- и гидроксисодержащего соединения, представленный любой из формул (6) - (9):
-О-(СН2)n-NН2 (6),
где n обозначает целое число 3 - 18;
-(О-СН2СН2)m-NН2 (7),
где m обозначает целое число 2 - 10;
-О-СНR6СН(СООR7)-NН2 (8),
где R6 представляет собой водород;
R7 представляет собой низший алкил;
-О-(СН2)l-NНСО-СНR8-NН2 (9),
где l обозначает целое число 2 - 18;
R8 представляет собой боковую цепочку остатка α-аминокислоты, водород, низший алкил;
фрагмент С-Н представляет собой аминокислотный остаток формулы (11) или (12):
-СО-(СН2)k-NН2 (11),
где k принимает значения, определенные выше;
-(СОСНR9NН)i-Н (12),
где i обозначает целое число 1 - 6;
R9 представляет собой водород,
в присутствии растворимого в воде карбодиимида и вспомогательного конденсирующего агента.
R1-В-Р2 (14),
где R1 представляет собой группу формулы (4)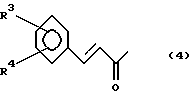
где R3 и R4 независимо друг от друга представляют собой водород;
фрагмент В представляет собой аминокислотный остаток формулы (10')
-NН-(СН2)k-СО- (10'),
где k обозначает целое число 1 - 18;
Р2 представляет собой полисахаридный остаток, содержащий амино- или гидроксигруппу;
связь В-Р2 представляет собой амидную связь, образованную между концевой карбоксильной группой формулы (10') и аминогруппой заместителя Р2, или сложноэфирную связь, образованную между концевой карбоксильной группой формулы (10') и гидроксильной группой заместителя Р2,
включающий стадии: (А) активации карбоксильной группы производного коричной кислоты и полисахарида, представленного формулой (2)
R1-В-ОН (2),
где R1 представляет собой группу формулы (4)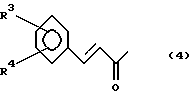
где R3 и R4 независимо друг от друга представляют собой водород;
фрагмент В-ОН представляет собой аминокислотный остаток формулы (10)
-NН-(СН2)k-СООН (10),
где k обозначает целое число 1 - 18, и (В) добавления активированного производного коричной кислоты к раствору амина или аммониевой соли гликозоаминогликана в органическом растворителе в присутствии основного катализатора.
R1-В-Р2 (14),
где R1 представляет собой группу формулы (4)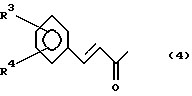
где R3 и R4 независимо друг от друга представляют собой водород;
фрагмент В представляет собой аминокислотный остаток формулы (10')
-NН-(СН2)k-СО (10'),
где k обозначает целое число 1 - 18;
Р2 представляет собой полисахаридный остаток, содержащий амино- или гидроксигруппу;
связь В-Р2 представляет собой амидную связь, образованную между концевой карбоксильной группой формулы (10') и аминогруппой заместителя Р2, или сложноэфирную связь, образованную между концевой карбоксильной группой формулы (10') и гидроксильной группой заместителя Р2,
включающий стадии: (А) активации карбоксильной группы производного коричной кислоты и полисахарида, представленного формулой (2)
R1-В-ОН (2),
где R1 представляет собой группу формулы (4)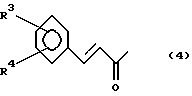
где R3 и R4 независимо друг от друга представляют собой водород;
фрагмент В-ОН представляет собой аминокислотный остаток формулы (10)
-NН-(СН2)k-СООН (10),
где k обозначает целое число 1 - 18,
и (В) добавления активированного производного коричной кислоты к раствору полиаминосахарида или его соли в органическом растворителе.
Приоритеты по пунктам:
17.11.94 - по пп.2, 3, 6, 7, 10, 12, 19, 21, 22 и 26;
20.09.95 - по пп.1, 4, 5, 8, 11, 20 и 23 - 25.
| СПОСОБ ПОЛУЧЕНИЯ ГЛЮКАН-ХИТОЗАНОВОГО КОМПЛЕКСА | 1992 |
|
RU2043995C1 |
| Способ получения бактериального препарата ацидофильных культур | 1983 |
|
SU1152105A1 |
Авторы
Даты
2001-06-20—Публикация
1995-11-16—Подача