Настоящее изобретение относится к противовоспалительному средству, противоаллергическому средству, иммуномодулятору, индуктору клеточной дифференцировки, индуктору апоптоза и кератансульфатолигосахариду, который может использоваться в качестве активного ингредиента в указанных фармацевтических препаратах.
Предпосылки создания изобретения
Кератансульфат представляет собой гликозаминогликан, содержащий N-ацетиллактозамин в качестве основной структуры, у которой в положении C-6N-ацетилглюкозаминового остатка имеется О-сульфатированная гидроксильная группа. В частности, известно, что высокосульфатированный кератансульфат, который кроме положения C-6N-ацетилглюкозаминового остатка содержит сульфатировнную гидроксильную группу в структурном дисахаридном звене, содержится в хрящевых рыбах, таких как акулы, и в хрящах, костях и роговице млекопитающих, таких как киты и жвачные животные. Сообщается о способе получения кератансульфатолигосахарида, являющегося продуктом расщепления кератансульфата, который включает воздействие расщепляющего кератансульфат фермента (кератаназа II); выложенная заявка на патент Японии N 2-57182), полученного из микроорганизмов, относящихся к Bacillus, на кератансульфат.
Кроме того, есть сообщение (Biochemistry, 33, 4836-4846 (1994)), в котором дается анализ 25 видов олигосахаридных фракций, полученных путем фракционирования продуктов расщепления после расщепления кератаназой II кератансульфата, полученного из коровьих хрящей, и предлагается структура тетрасульфатированного N-ацетиллактозаминатетрасахарида, представленного следующей формулой (I) (называемого здесь далее также "кератансульфаттетрасахаридом (I)"), трисульфатированного N-ацетиллактозаминопентасахарида, представленного следующей формулой (II) (называемого здесь далее также "кератансульфатпентасахаридом (II)"), дисульфатированного N-ацетиллактозаминодисахарида, представленного следующей формулой (III) (называемого здесь далее также "кератансульфатдисахаридом (III)"), и т.п.:
Gal(6S) β 1-4 GlcNAc(6S) β 1-3 Gal(6S) β 1-4 GlcNAc(6S).....(I)
NeuAc~Gal β 1-4 GlcNAc(6S) β 1-3 Gal(6S) β 1-4 GlcNAc(6S)...(II)
Gal(6S) β 1-4 GlcNAc(6S)... (III)
(В приведенных выше формулах Gal представляет галактозу, GlcN представляет глюкозамин, Neu представляет нейраминовую кислоту, Ac представляет ацетильную группу, и 6S представляет 6-O-сульфатный эфир. "~" представляет связь α 2, 3 или связь α 2, 6).
Однако до настоящего времени не было сообщений, относящихся к эффективному массовому получению чистого кератансульфатолигосахарида, в особенности кератансульфаттетрасахарида (I), кератансульфатпентасахарида (II) и кератансульфатдисахарида (III), без загрязнения примесями (например, эндотоксинами, нуклеиновыми кислотами, белками, протеазами, другими гликозаминогликанами, исключая кератансульфатолигосахарид и тому подобное). Загрязнение такими примесями рассматривается как серьезный недостаток, особенно в случае, когда кератансульфатолигосахариды используют в качестве фармацевтических препаратов. Кроме того, о фармакологическом действии кератансульфатолигосахаридов (в частности, противовоспалительном действии, противоаллергическом действии, иммуномодуляторном действии, индуцирующем клеточную дифференцировку действии и индуцирующем апоптоз действии) ничего не известно.
Описание изобретения
На основе вышеуказанного осуществляют настоящее изобретение и его целью является применение кератансульфатолигосахарида, по существу не содержащего примеси, в качестве противовоспалительного средства, противоаллергического средства, иммуномодулятора, индуктора клеточной дифференцировки (называемых здесь далее также "индукторами дифференцировки") или индуктора апоптоза.
Чтобы достичь указанной выше цели, заявители провели кропотливые исследования фармакологического действия олигосахарида, который содержит от двух до пяти сахаридных звеньев, в частности дисахарида, тетрасахарида или пентасахарида, полученного из продуктов расщепления, которые получаются при расщеплении высокосульфатированного кератансульфата расщепляющим кератансульфат ферментом, и в результате обнаружили, что описанный выше олигосахарид и его соли обладают превосходным противовоспалительным действием, противоаллергическим действием и иммуномодулирующим действием, индуцирующим клеточную дифференцировку действием и индуцирующим апоптоз действием. Таким образом осуществляют настоящее изобретение.
А именно противовоспалительное средство, противоаллергическое средство, иммуномодулятор, индуктор дифференцировки и индуктор апоптоза по настоящему изобретению (называемые здесь далее также обобщенно "фармацевтические препараты по настоящему изобретению") содержат кератансульфатолигосахарид и/или его фармацевтически приемлемую соль в качестве активного ингредиента. В настоящем описании "кератансульфатолигосахарид" означает продукт расщепления кератансульфата, который можно получить путем расщепления кератансульфата расщепляющим кератансульфат ферментом типа эндо- β -N-ацетилглюкозаминидазы.
Примерами кератансульфатолигосахаридов, используемых для фармацевтических препаратов по настоящему изобретению, являются кератансульфатолигосахарид, который содержит сульфатированное N-ацетиллактозаминовое звено, необязательно содержащее сиаловую кислоту и/или фукозу, кератансульфатолигосахарид, который содержит олигосахарид с двумя-пятью сахаридными звеньями и имеет сульфатированный N-ацетилгликозамин на своем редуцирующем конце, и в молекуле которых сульфатированы, по меньшей мере, две гидроксильные группы, и, в частности, кератансульфатолигосахарид, описанный выше, который содержит в качестве структурного компонента, по меньшей мере, дисахарид, представленный формулой Gal(6S)-GlcNAc(6S) (где Gal представляет галактозу, GlcN представляет глюкозамин. Ac представляет ацетильную группу и 6S представляет 6-O-сульфатный эфир). Более того, предпочтительным примером кератансульфатолигосахарида, описанного выше, является тетрасульфатированный N-ацетиллактозаминотетрасахарид, представленный следующей формулой (I), трисульфатированный N-ацетиллактозаминопентасахарид, представленный формулой (II), дисульфатированный N-ацетиллактозаминодисахарид, представленный формулой (III) и т. п.:
Gal(6S) β 1-4 GlcNAc(6S) β 1-3 Gal(6S) β 1-4 GlcNAc(6S)...(I)
NeuAc~Gal β 1-4 GlcNAc(6S) β 1-3 Gal(6S) β 1-4 GlcNAc(6S)...(II)
Gal(6S) β 1-4 GlcNAc(6S)... (III)
(В приведенных выше формулах Gal представляет галактозу, GlcN представляет глюкозамин, Neu представляет нейраминовую кислоту. Ac представляет ацетильную группу и 6S представляет 6-O-сульфатный эфир. И ~ представляет связь α 2, 3 или связь α 2, 6).
Настоящее изобретение также относится к фракции кератансульфатолигосахарида, содержащей не менее 99% кератансульфатолигосахарида, который содержит олигосахарид с двумя-пятью сахаридными звеньями и сульфатированный N-ацетилгликозамин на своем редуцирующем конце, в молекулах которых сульфатированы, по меньшей мере, две гидроксильные группы, и обладающие следующими свойствами:
(а) фракция по существу не содержит эндотоксин, а содержание нуклеиновых кислот, белков и протеаз во фракции меньше относительно пределов их обнаружения; и
(б) фракция по существу не содержит гиалуроновой кислоты, хондроитинсульфат, дерматансульфат, гепарансульфат и кератансульфат.
Настоящее изобретение также относится к фракции кератансульфатолигосахарида, содержащей не менее 99% кератансульфатолигосахарида, который содержит в качестве структурного компонента, по меньшей мере, дисахарид, представленный формулой Gal (6S)-GlcNAc (6S), и обладающий свойствами (а) и (б), описанными выше. Также предпочтительным примером кератансульфатолигосахарида, содержащегося в описанных выше олигосахаридных фракциях, является тетрасульфатированный N-ацетиллактозаминатетрасахарид, представленный формулой (I), трисульфатированный N-ацетиллактозаминопентасахарид, представленный формулой (II), дисульфатированный N-ацетиллактозаминодисахарид, представленный формулой (III), и т.п. Кроме того, кератансульфатолигосахарид включает кератансульфатолигосахарид, полученный путем фракционирования продуктов расщепления высокосульфатированного кератансульфата, получаемого из хрящевых рыб, расщепляющим кератансульфаты ферментом типа эндо- β -N-ацетилглюкозаминидазы.
Настоящее изобретение также относится к способу получения фракции кератансульфатолигосахарида, включающему стадии расщепления кератансульфата расщепляющим кератансульфаты ферментом, обладающим следующими физическими и химическими свойствами:
(1) действие:
расщепляющий фермент воздействует на кератансульфат и гидролизует его N-ацетилглюкозаминидную связь;
(2) специфичность к веществу:
расщепляющий фермент действует на кератансульфат I, кератансульфат II и кератанполисульфат и продуцирует сульфатированный кератансульфатдисахарид и сульфатированный кератансульфаттетрасахарид в качестве основных продуктов расщепления;
и предпочтительно обладающий физическими и химическими свойствами:
(3) оптимальный pH реакции:
расщепляющий фермент имеет оптимальный pH реакции от 4,5 до 6 в 0,1М ацетатном буфере или в 10 мМ трис-ацетатном буфере при 37oC;
(4) pH стабильность:
расщепляющий фермент обладает pH стабильностью от 6 до 7, когда расщепляющий фермент остается в 0,1М ацетатном буфере или в 10 мМ трис-ацетатном буфере при 37oC в течение часа;
(5) оптимальная температура реакции:
расщепляющий фермент имеет оптимальную температуру реакции от 50 до 60oC, когда расщепляющий фермент реагирует в 0,1М ацетатном буфере, pH 6,0, в течение 10 мин; и
(6) термоустойчивость:
расщепляющий фермент устойчив, по меньшей мере, при 45oC или ниже, когда расщепляющий фермент остается в 0,1М ацетатном буфере, pH 6,0, в течение часа;
и фракционирования из продуктов расщепления фракции кератансульфатолигосахарида, обладающей следующими свойствами:
(A) фракция содержит в качестве основного ингредиента кератансульфатолигосахарид, который содержит сульфатированный N-ацетиллактозамин в качестве основной структурной составляющей;
(Б) фракция по существу не содержит эндотоксин, и содержание нуклеиновой кислоты, белка и протеазы во фракции является следовым или меньше относительно пределов их обнаружения; и
(В) фракция по существу не содержит гиалуроновой кислоты, хондроитинсульфата, дерматансульфата, гепарансульфата и кератансульфата.
Кроме того, при способе получения фракции кератансульфатолигосахарида, описанной выше, например применение высокосульфатированного кератансульфата в качестве соединения кератансульфата дает кератансульфатолигосахарид, содержащий тетрасульфатированный N-ацетиллактозаминотетрасахарид, представленный формулой (I), описанной выше, трисульфатированный N-ацетиллактозаминопентасахарид, представленный формулой (II), дисульфатированный N-ацетиллактозаминодисахарид, представленный формулой (III), и т.п., в особенности кератансульфатолигосахариды, содержащие тетрасульфатированный N-ацетиллактозаминотетрасахарид, представленный формулой (I) и дисульфатированный N-ацетиллактозаминодисахарид, представленный формулой (III), в качестве основных ингредиентов.
В настоящем изобретении предпочтительным кератансульфатолигосахаридом, который содержит олигосахарид с двумя-пятью сахаридными звеньями, обычно является олигосахарид, который сульфатирован в двух-четырех позициях. Кроме того, предпочтительно, чтобы в кератансульфатолигосахариде, содержащем сиаловую кислоту, которая может использоваться по настоящему изобретению, сиаловая кислота включает N-ацетилнейраминовую кислоту и N-гликолилнейраминовую кислоту и N-ацетилнейраминовая кислота является предпочтительной. Кератансульфатолигосахарид, который может использоваться по настоящему изобретению, описанный выше, содержит олигосахариды, связывающие сиаловую кислоту по α 2,3 связи и по α 2,6 связи и, предпочтительно, связывающие сиаловую кислоту по α 2,3 связи.
Настоящее изобретение подробно описано далее.
(1) Кератансульфатолигосахарид и фракция кератансульфатолигосахарида, используемые в настоящем изобретении
Кератансульфат, который является исходным продуктом для кератансульфатолигосахарида, используемого по настоящему изобретению, содержит, главным образом, повторяющуюся структуру дисахарида галактозы или галактозо-6-сульфата и N-ацетилглюкозамино-6-сульфата, содержание сульфата в котором изменяется в зависимости от вида животного, ткани и т.д., и обычно добывается из такого сырья, как хрящи, кости и роговица хрящевых рыб, таких как акулы и млекопитающих, таких как киты и жвачные животные.
Используемый в качестве исходного вещества кератансульфат является обычно доступным материалом и не имеет особых ограничений, но предпочтителен высокосульфатированный кератансульфат (высокосульфатированный кератансульфат, содержащий от 1,5 до 2 молекул сульфатной группы на структурный дисахарид, упоминается здесь так же как кератанполисульфат), у которого сульфатирован входящий в структуру моносахарид, такой как галактозный остаток. Сульфатная группа, предпочтительно, располагается в положении 6 на галактозном остатке. Такой высокосульфатированный кератансульфат можно получить, например, из протеогликана хрящей хрящевых рыб, таких как акулы. Коммерчески доступный кератансульфат также можно использовать.
Кератансульфатолигосахарид по настоящему изобретению можно получить путем воздействия на кератансульфат расщепляющего кератансульфаты фермента типа эндо- β -N-ацетилглюкозаминидазы, например, кератаназы II, получаемой из микроорганизма, принадлежащего к роду Bacillus (выложенная заявка на патент Японии N 2-57182), или нового расщепляющего кератансульфаты фермента, обнаруженного авторами настоящего изобретения в микроорганизме, принадлежащем к роду Bacillus, в буферном растворе и расщепления его, и последующего фракционирования полученных продуктов расщепления. Такую реакцию расщепления проводят, например, в буферном растворе, содержащем кератансульфат в концентрациях от 1,0 до 100 мг/мл при pH от 6,0 до 7,0 при от 25 до 40oC в течение от 1 до 72 ч. При этой реакции концентрация буфера обычно находится в области от 0,01 до 0,2М. Вид буфера особенно не ограничивают, если его pH можно установить в указанных выше пределах, и к числу таких буферов относятся, например, ацетатный буфер, фосфатный буфер и трис-буфер. Количество фермента, используемого в реакции расщепления, находится, например, в интервале от 0,1 до 1,0 единицы на 1 г кератансульфата. Здесь одна единица означает количество фермента, которое продуцирует редуцирующий конец, соответствующий 1 мкмоль N-ацетилглюкозамина в минуту.
Новый, описанный выше расщепляющий кератансульфат фермент продуцируется микроорганизмом, принадлежащим Bacillus circulans, например Bacillus circulans KsT202, был выделен заявителями, и он обладает превосходной термоустойчивостью. Этот фермент получают путем культивирования Bacillus circulans KsT202 в подходящей среде и очистки фермента от среды и/или микробных клеток методами, принятыми для очистки ферментов. Bacillus circulans KsT202 депонирован в National Institute of Bioscience and Human-Technology of Agency of Industrial Science and Technology of Ministry of International Trade and Industry (1-3, Higashi 1-chome, Tsukuba-shi, Ibaraki-ken 305, Япония) 5 сентября 1994 г. под инвентарным номером FERM Р-14516 и затем передан для международного депонирования, согласно Будапештскому договору, 6 ноября 1995 г. , и депонирован под инвентарным номером FERM ВР-5285.
Физические и химические свойства нового расщепляющего кератансульфат фермента, описанного выше, описаны далее.
(1) Действие
Расщепляющий фермент действует на кератансульфат и гидролизует его N-ацетилглюкозаминидную связь.
(2) Специфичность к субстрату
Расщепляющий фермент действует на кератансульфат I, кератансульфат II и кератанполисульфат и продуцирует сульфатированный кератансульфатдисахарид и кератансульфаттетрасахарид в качестве основных продуктов расщепления. Подтверждено также, что расщепляющий фермент продуцирует сульфатированный кератансульфатпентасахарид.
(3) Оптимальный pH реакции:
Расщепляющий фермент имеет оптимальный pH реакции от 4,5 до 6 в 0,1М ацетатном буфере или в 10мМ трис-ацетатном буфере при 37oC.
(4) pH Стабильность:
Расщепляющий фермент обладает pH стабильностью от 6 до 7, когда расщепляющий фермент остается в 0,1М ацетатном буфере или в 10мМ трис-ацетатном буфере при 37oC в течение часа.
(5) Оптимальная температура реакции:
Расщепляющий фермент имеет оптимальную температуру реакции от 50 до 60oC, когда расщепляющий фермент реагирует в 0,1М ацетатном буфере, pH 6,0, в течение 10 мин.
(6) Термоустойчивость:
Расщепляющий фермент устойчив, по меньшей мере, при 45oC или ниже, когда расщепляющий фермент остается в 0,1М ацетатном буфере, pH 6,0, в течение часа.
Фракция кератансульфатолигосахарида по настоящему изобретению может быть получена также путем взаимодействия иммобилизованного фермента, расщепляющего кератансульфат, в том числе такого нового расщепляющего кератансульфат фермента и кератаназы II, указанных выше, которые иммобилизованы обычными способами.
В результате реакции расщепления ферментом, как описан выше, кератансульфат расщепляется до олигосахарида.
Затем полученный таким образом олигосахарид отделяют и очищают обычными способами, такими как осаждение этанолом и различные виды хроматографии, и можно получить нужный кератансульфатолигосахарид. Эта очистка будет подробно описана при описании очистки кератансульфатолигосахарида из дисахарида, тетрасахарида и пентасахарида. Описанный выше продукт расщепления обычно концентрируют сначала осаждением этанолом и гель-фильтрацией (интервал фракционированной молекулярной массы от 100 до 10000), чтобы грубо фракционировать сырой кератансульфатолигосахарид из дисахарида, тетрасахарида и пентасахарида. Затем грубые фракции разделяют и фракционируют анионообменной хроматографией соответственно с получением по существу чистых дисахарида, тетрасахарида и пентасахарида, которые по существу не содержат эндотоксина, а содержание нуклеиновых кислот, белков и протеаз в которых меньше пределов их обнаружения и которые по существу не содержат гиалуроновой кислоты, хондроитинсульфата, дерматансульфата, гепарансульфата и кератансульфата. В настоящем изобретении "по существу не содержат" означает такое содержание, которое может быть обнаружено чувствительными методами обнаружения, но не влияет на фармакологические функции кератансульфатолигосахарида, такие как противовоспалительная функция, противоаллергическая функция, иммуномодуляторная функция, функция индуцирования клеточной дифференцировки и функция индуцирования апоптоза.
Кератансульфатолигосахарид по настоящему изобретению получают из кератансульфата в качестве исходного продукта путем расщепления кератансульфата эндо- β -N-ацетилглюкозаминидазой и фракционирования олигосахарида из дисахаридных-пентасахаридных звеньев, который по существу не содержит кератансульфата и является для него исходным материалом.
Кератансульфатолигосахарид можно также получить из продуктов расщепления кератансульфата, расщепленного химическим способом, при котором предпочтительно или специфически разрушается связь между галактозой или галактозо-6-сульфатом и N-ацетилглюкозамин-6- сульфатом, которые составляют кератансульфат.
Кератансульфатолигосахарид, особенно тетрасульфатированный N-ацетиллактозаминатетрасахарид, представленный формулой (I), описанной выше, трисульфатированный N-ацетиллактозаминопентасахарид, представленный формулой (II), дисульфатированный N-ацетиллактозаминодисахарид, представленный формулой (III), и т.п., получают, как описано выше. В описанных далее примерах даны спектры ядерного магнитного резонанса (1H-ЯМР и 13C-ЯМР) и результаты масс-спектрометрического анализа при бомбардировке быстрыми атомами веществ, представленных формулами (I), (II) и (III).
Кератансульфатолигосахарид по настоящему изобретению также включает ионизованное вещество, протонированное вещество и фармацевтически приемлемую соль из числа солей с неорганическими основаниями, такими как щелочные металлы (натрий, калий, литий и т.п.), щелочноземельные металлы (кальций и т. п. ), аммоний и т. п., или солей с органическими основаниями, такие как соль диэтаноламина, соль циклогексиламина и соль аминокислоты.
Фармацевтическая композиция, содержащая кератансульфатолигосахарид и/или его соль, применяемые по настоящему изобретению, и носители, разбавители и другие добавки, обычно используемые в фармацевтических препаратах, также является новой и может вводиться с целью противовоспалительного, противоаллергического, иммуномодулирующего действия, с целью индуцирования клеточной дифференцировки, индуцирования апоптоза и т.п.
Фракция кератансульфатолигосахарида по настоящему изобретению содержит по меньшей мере 99% кератансульфатолигосахарида, который получают из продуктов ферментативного расщепления кератансульфата, удаляя из них эндотоксин, нуклеиновую кислоту, белок, протеазу и другие гликозаминогликаны, за исключением нужного кератансульфатолигосахарида, особенно из продуктов расщепления высокосульфатированного кератансульфата, следуя описанному выше способу.
(2) Фармацевтическая композиция по настоящему изобретению
Кератансульфатолигосахарид и/или его фармацевтически приемлемая соль, описанные выше, могут широко применяться в качестве противовоспалительного средства, противоаллергического средства, иммуномодулятора, индуктора клеточной дифференцировки, индуктора апоптоза и фармацевтических препаратов для другого применения.
Противовоспалительное средство по настоящему изобретению эффективно при многих заболеваниях, связанных с воспалением, и характерные показания для которого включают хронический ревматоидный артрит, системную красную волчанку, спондилитные изменения, остеоартрит, люмбаго, ремиссию воспаления и гипертрофию после операций и травм, периартериит лопатки, височно-нижечелюстной артроз, тендовагинит, обволакивающее воспаление сухожилий, воспаление мыщелока плечевой кости (теннисный локоть), миалгию, кератоконъюнктивит и подобные воспаления. Противовоспалительное средство настоящего изобретения обладает противовоспалительным действием, таким как аналгезирующее действие, противовоспалительное действие и жаропонижающее действие, при заболеваниях и симптомах, при которых действует кератансульфатолигосахарид и/или его фармацевтически приемлемая соль.
Противовоспалительное средство по настоящему изобретению эффективно при любом заболевании, связанном с аллергией, и конкретные показания для которого включают аллергический ринит, аллергический кератоконъюнктивит, весенний конъюнктивит, экзему, дерматит, крапивницу, атопический дерматит и подобные заболевания.
Иммуномодулятор по настоящему изобретению эффективен при любом заболевании, связанном с иммунным нарушением, и конкретными показаниями для которого являются аутоиммунный лимфопролиферативный синдром человека (Cell 81, 935-946 (1995), Science 268, 1347-1349 (1995)), лимфопролиферативное нарушение (Leukemia and Lymphoma 16, 363-368 (1995), ангиоиммунобластная лимфаденопатия (Blood 85(10), 2862-2869 (1995)), иммунобластная лимфаденопатия (The American Journal of Medicine 63, 849-851 (1977)), хронический ревматоидный артрит, системная красная волчанка, дискоидная красная волчанка, дерматомиозит (дерматомиома), склеродермия, смешанная диффузная болезнь соединительной ткани, хронический тиреоидит, первичная микседема, тиреотоксикоз, пернициозная анемия, сочетание пневмопатии с тяжелой анемией, острый прогрессирующий гломерулонефрит, миастения gravis, обыкновенная пузырчатка, буллезный пемфигоид, инсулиннезависимый сахарный диабет, ювенильный сахарный диабет, болезнь Адиссона, атрофический гастрит, мужская стерильность, климактерический прекокс (precox), факогенный увеит, симпатический ангиит, рассеянный склероз, прогрессирующий системный склероз, воспалительное заболевание кишечника (болезнь Крона, неспецифический язвенный колит и т.п.), первичный билиарный цирроз, хронический активный гепатит, аутоиммунная гемолитическая анемия, пароксизмальная гемоглобинурия, идиопатическая тромбоцитопеническая пурпура, синдром Шегрена, синдром антифосфолипидных антител и подобные заболевания.
Индуктор дифференцировки по настоящему изобретению эффективен при любом заболевании, вызванном недостаточностью физиологической клеточной дифференцировки, иммунным нарушением, злокачественной опухолью и т.п., и конкретными показаниями для которого являются аутоиммунный лимфопролиферативный синдром человека, лимфопролиферативное нарушение, ангиоиммунобластная лимфаденопатия, иммунобластная лимфаденопатия, хронический ревматоидный артрит, системная красная волчанка, воспалительное заболевание кишечника (болезнь Крона, неспецифический язвенный колит и т.п.), прогрессирующий системный склероз, дерматомиозит (дерматомиома), синдром Шегрена, карцинома, лейкоз, лимфома, задержка карциномного метастаза, предупреждение гиперплазии (лечение против псориаза и т.п.), заживление ран, синдром остеомиелофиброза, склеродермия и подобные заболевания.
Индуктор апоптоза по настоящему изобретению эффективен при любом заболевании, вызванном недостаточностью физиологического апоптоза, иммунным нарушением, злокачественной опухолью и т.п., и конкретными показаниями для которого являются аутоиммунный лимфопролиферативный синдром человека, лимфопролиферативное нарушение, ангиоиммунобластная лимфаденопатия, иммунобластная лимфаденопатия, хронический ревматоидный артрит, системная красная волчанка, неспецифический язвенный колит, прогрессирующий системный склероз, дерматомиозит (дерматомиома), синдром Шегрена, карцинома, лейкоз, лимфома, задержка карциномного метастаза, предупреждение гиперплазии (лечение против псориаза и т. п.), синдром остеомиелофиброза, склеродермия, апоптозное индуцирование аномальных мезангиальных клеток (лечение против гломерулонефрита) и подобные заболевания.
Эффекты снижения массы лимфатических узлов, индуцирования дифференцировки и индуцирования апоптоза наблюдали на мышах MRL-lpr/lpr. Патогенез аутоиммунного лимфопролиферативного синдрома человека считается таким же нарушением Fas-гена, как у мышей MRL-lpr/lpr, а патология синдрома имеет заметное сходство с патологией мышей MRL-lpr/lpr, как например, в отношении припухлости лимфоузлов. Мышей MRL-lpr/lpr можно принять в качестве подходящей модели аутоиммунного лимфопролиферативного синдрома человека. Следовательно, наиболее предпочтительным показанием применения фармацевтических препаратов в иммуномодуляторе, индукторе дифференцировки и индукторе апоптоза настоящего изобретения является аутоиммунный лимфопролиферативный синдром человека.
Фармацевтические препараты по настоящему изобретению могут быть изготовлены с учетом способа введения, таким как инъекция (внутримышечная, подкожная, интрадермальная, внутривенная, интраартикулярная, внутриглазная, внутрибрюшинная и т.д.), закапывание в глаза, инстилляция, чрезкожное введение, пероральное введение и ингаляция. Лекарственные формы включают формы для инъекции (растворы, суспензии, эмульсии, твердые препараты для инъекций, растворимые перед применением и т.п.), таблетки, капсулы, гранулы, порошки, растворы, липосомные включения, мази, гели, порошки для наружного применения, спреи, порошки для ингаляций, глазные капли, глазные мази и тому подобное. При получении фармацевтических препаратов можно применять ингредиенты, обычно используемые в лекарственных средствах, такие как традиционные носители, связующие, смазывающие вещества, красители и разрыхлители. В фармацевтических препаратах по настоящему изобретению кератансульфатолигосахарид может использоваться одновременно с другими противовоспалительными ингредиентами, противоаллергическими ингредиентами, иммуномодулирующими ингредиентами, ингредиентами, индуцирующими дифференцировку, ингредиентами, индуцирующими апоптоз и т.п.
В табл. 1 указаны предпочтительные способы введения и лекарственные формы противовоспалительного и противоаллергического средства. В табл. 2 указаны предпочтительные способы введения и лекарственные формы иммуномодулятора, индуктора клеточной дифференцировки и индуктора апоптоза.
Эффективная доза противовоспалительного средства и противоаллергического средства по настоящему изобретению составляет от 30 до 300 мг/пациент/сутки кератансульфатолигосахарида при введении в организм и от 1 до 10 мг/пациент/сутки при наружном введении. Эффективная доза иммуномодулятора, индуктора дифференцировки и индуктора апоптоза находится в интервале от 30 до 6000 мг/пациент/сутки кератансульфатолигосахарида.
На фиг. 1 представлена хроматограмма гель-фильтрации с помощью ВЭЖХ тетрасульфатированного N-ацетиллактозаминотетрасахарида (кератансульфаттетрасахарид (I)), полученного в примере 1.
На фиг. 2 представлена хроматограмма гель-фильтрации с помощью ВЭЖХ трисульфатированного N-ацетиллактозаминопентасахарида (кератансульфатпентасахарид (II)), полученного в примере 1.
На фиг. 3 представлена хроматограмма гель-фильтрации с помощью ВЭЖХ дисульфатированного N-ацетиллактозаминодисахарида (кератансульфатдисахарид (III), полученного в примере 1.
Фиг. 4 демонстрирует спектр 1H-ЯМР при 400 МГц кератансульфатпентасахарида (II), полученного в примере 1.
Фиг. 5 представляет диаграмму, показывающую объем синовиальной жидкости у кроликов в случае модели артрита, вызванного папаином, которым вводили кератансульфаттетрасахарид (I), кератансульфатпентасахарид (II) или кератан сульфатдисахарид (III).
Фиг. 6 представляет графики, показывающие изменение времени развития отека стоп у крыс, у которых вызвано воспаление, когда кератансульфаттетрасахарид (I) или различные испытываемые соединения вводят крысам за пять минут до индуцирования воспаления.
Фиг. 7 представляет графики, показывающие изменение времени развития отека стоп у крыс, у которых вызвано воспаление, когда кератансульфаттетрасахарид (I) или различные испытываемые соединения вводят крысам за три часа до индуцирования воспаления.
На фиг. 8 приведена диаграмма, показывающая объем плеврального выпота у крыс в случае модели каррагининового (carrageenin) плеврита, которым вводили кератансульфаттетрасахарид (I) или дексаметазонацетат.
На фиг. 9 дается диаграмма, показывающая число лейкоцитов в плевральном выпоте у крыс в случае модели каррагининового плеврита, которым вводили кератансульфаттетрасахарид (I) или дексаметазонацетат.
На фиг. 10 представлена диаграмма, показывающая ингибирующее действие на генерацию активного кислорода (O
На фиг. 11 дается диаграмма, показывающая оценку степени развития конъюнктивита в случае модели аллергического конъюнктивита у морских свинок, которым вводят или не вводят кератансульфаттетрасахарид (I).
Фиг. 12 представляет диаграмму, показывающую оценку степени развития конъюнктивита в случае модели аллергического конъюнктивита у морских свинок, которым вводят или соответственно не вводят кератансульфаттетрасахарид (I), кератансульфатпентасахарид (II) или кератансульфатдисахарид (III).
Фиг. 13 представляет диаграмму, показывающую оценку степени развития конъюнктивита в случае модели аллергического конъюнктивита у морских свинок, которым вводят кератансульфаттетрасахарид (I) в различных концентрациях.
На фиг. 14 приводится диаграмма, показывающая массу подчелюстных лимфатических узлов у мышей MRL, которые являются моделью аутоиммунного заболевания, которым в течение 28 дней повторно вводили различные дозы кератансульфатдисахарида (III).
На фиг. 15 приводится диаграмма, показывающая массу мезентериальных лимфатических узлов у мышей MRL, которым в течение 56 дней повторно вводили различные дозы кератансульфатдисахарида (III).
Фиг. 16 представляет диаграмму, показывающую массу подчелюстных лимфатических узлов у мышей MRL, которым в течение 56 дней повторно вводили различные дозы кератансульфатдисахарида (III).
Фиг. 17 является диаграммой, на которой даются результаты анализа концентраций окрашивания образцов срезов мезентериальных лимфатических узлов (НЕ-окрашивание) у мышей MRL, которым вводили различные дозы кератансульфатдисахарида (III).
Фиг. 18 является диаграммой, на которой даются результаты анализа концентраций окрашивания образцов срезов подчелюстных лимфатических узлов (Не - окрашивание) у мышей MRL, которым вводили различные дозы кератансульфатдисахарида (III).
Фиг. 19 является диаграммой, показывающей соотношение (%) CD3 и CD4 позитивных клеток для лимфоцитов у мышей MRL, которым вводили различные дозы кератансульфатдисахарида (III).
Фиг. 20 является диаграммой, показывающей соотношение (%) CD3 и CD8a позитивных клеток для лимфоцитов у мышей MRL, которым вводили различные дозы кератансульфатдисахарида (III).
Фиг. 21 является диаграммой, показывающей соотношение (%) CD3 и В220 позитивных клеток для лимфоцитов у мышей MRL, которым вводили различные дозы кератансульфатдисахарида (III).
Фиг. 22 является диаграммой, показывающей число апоптозных клеток в подчелюстных лимфатических узлах у мышей MRL, которым вводили различные дозы кератансульфатдисахарида (III).
Предпочтительные варианты осуществления изобретения
Настоящее изобретение подробно описано далее с помощью приведенных ниже примеров. В примере продуцирования описывается продуцирование нового расщепленного кератансульфат фермента, получаемого из микроорганизма, принадлежащего к роду Bacillus. В примере 1 описывается получение фракций кератансульфатолигосахаридов, а в примере 2 описывается острая токсичность и различные фармакологические свойства кератансульфатолигосахаридов. Кроме того, в примерах 3-6 даются примеры фармацевтических препаратов.
Пример продуцирования. Продуцирование фермента, расщепляющего кератансульфат
(1) Выделение Bacillus circulans KsT202
Небольшое количество почвы добавляют к 5 мл жидкой среды, содержащей источник азота, неорганические соли и кератансульфат и культивируют при встряхивании при 45oC в течение трех суток. После культивирования 10 мкл супернатанта культуральной среды капают на фильтровальную бумагу, и также таким же способом наносят на фильтровальную бумагу 10 мкл жидкой среды (контроль). После просушивания на воздухе фильтровальную бумагу смачивают в растворе толуидинового синего и соответственно промывают разбавленным раствором уксусной кислоты и окраску на стороне капли супернатанта культуральной среды сравнивают с окраской контрольного пятна. Так толуидиновый синий соединяется с кератансульфатом с образованием синего окрашивания, менее интенсивное окрашивание, чем в случае контрольного образца, подтверждает, что в образце находится усваивающий кератансульфат микроорганизм. Усваивающий кератансульфат микроорганизм выделяют в чистом виде из раствора культуры обычным способом с использованием пластинчатой среды (например, агара Heart infusion).
Выделенный вид микроорганизмов проверяют на усвоение кератансульфата с использованием жидкой среды так же, как описано выше, и получают нужный микроорганизм, усваивающий кератансульфат. В результате исследований морфологии, роста и физиологических свойств штамма, о котором идет речь, микроорганизм идентифицирован как Bacillus circulans. Указанный штамм является новым штаммом, который можно отличить от известных штаммов, так как он усваивает кератансульфат. KsT202 Bacillus circulans депонирован в National Institute of Bioscience and Human-Technology of Agency of Industrial Science and Technology 5 сентября 1994 г. под инвентарным номером FERM Р-14516, и он передан на международное депонирование, на основании Будапештского договора, 6 ноября 1995 г., и депонирован под инвентарным номером FERM ВР-5285.
(2) Получение фермента, расщепляющего кератансульфат
В ферментер емкостью 30 л загружают 20 л среды (pH 8,0), содержащей 1,5% пептона (Kyokuto Seiyaku Kogyo), 0,75% экстракта пивных дрожжей (Nippon Seiyaku), 0,75% кератанполисульфата, полученного из хрящей акулы (Seikagaku Corporation), 0,5% K2HPO4, 0,02% MgSO4•7H2O, 0,5% NaCl и 0,0015% противовспенивающего вещества Adekanol (торговое название, Asahi Denka Kogyo), автоклавируют при 121oC в течение 20 мин, инокулируют асептически 1 л (5%) раствора культуры штамма KsT202, который предварительно культивируют при встряхивании в такой же среде при 37oC в течение 16 ч, и культивируют при 45oC в течение 24 ч с одновременной аэрацией (1 о/ом (vvm)) и перемешиванием (300 об/мин). Обрабатывают 20 л раствора культуры на центрифуге непрерывного действия, чтобы удалить микробные клетки, и получают приблизительно 20 л внеклеточной жидкости.
К этой внеклеточной жидкости добавляют сульфат аммония до 70% насыщения и центрифугированием извлекают выпавший осадок, и растворяют его в 2,5 л 10 мМ трис-ацетатного буфера (pH 7,5). К этому раствору добавляют сульфат аммония до 35% насыщения, выпавший осадок извлекают центрифугированием, затем добавляют сульфат аммония до 55% насыщения, и выпавший осадок извлекают центрифугированием.
Осадок растворяют в 2,5 л 10 мМ трис-ацетатного буфера (pH 7,5) и пропускают через колонку (5,2 х 24 см) с DEAE-целлюлозой (DE52, Whatman Co.), которую предварительно уравновешивают тем же буфером, и дают возможность ферменту адсорбироваться. Затем колонку промывают 1,5 л того же буфера, и фермент элюируют при линейном возрастании концентрации хлорида натрия от нуля до 0,3 М в том же буфере.
Активные фракции собирают, добавляют сульфат аммония до 55% насыщения, и затем выпавший осадок извлекают центрифугированием и растворяют в небольшом количестве 10 мМ трис-ацетатного буфера (pH 7,5). Затем раствор загружают на колонку с сефакрилом S-300 (Pharmacia) (3,4 х 110 см), и подвергают гель-фильтрации с 50 мМ трис-ацетатного буфера (pH 7,5), содержащего 0,5 М хлорида натрия.
Активную фракцию концентрируют ультрафильтрацией с использованием мембраны UK-10 (Advantec Toyo) и диализуют против приблизительно 100-кратного количества 10 мМ трис-ацетатного буфера (pH 7,5). Диализованный внутренний раствор пропускают через колонку с DEAE-Toyopearl (Tosoh Corporation) (2,2 х 15 см), которую предварительно уравновешивают тем же буфером, и дают возможность ферменту адсорбироваться. Затем колонку промывают 150 мл того же буфера, содержащего 0,1 М хлорида натрия, и фермент элюируют при линейном возрастании концентрации хлорида натрия от 0,1 до 0,2 М в том же буфере.
Активную фракцию концентрируют ультрафильтрацией, загружают на колонку с сефакрилом S-300 (2,2 х 101 см), и подвергают гель-фильтрации.
После добавления к активной фракции хлорида натрия до концентрации 4 М раствор пропускают через колонку с фенилсефарозой (Pharmacia) (1,6 х 15 см), которую уравновешивают трис-ацетатным буфером (pH 7,5), содержащим 4 М хлорида натрия, и затем элюируют фермент при линейном снижении концентрации хлорида натрия от 4 М до нуля в том же буфере. Получают 29 единиц фермента, и его специфическая активность составляет 2,09 единиц/мг (вычислена на массу бычьего сывороточного альбумина). Очищенный фермент не содержит загрязняющих ферментов, таких как гликозидаза.
Полученный выше расщепляющий кератансульфат фермент имеет следующие свойства.
(1) Действие
Расщепляющий фермент воздействует на кератансульфат и гидролизует его N-ацетилглюкозаминидную связь.
(2) Субстратная специфичность
Расщепляющий фермент воздействует на кератансульфат I, кератансульфат II и кератанполисульфат и продуцирует сульфатированный кератансульфатдисахарид и сульфатированный кератансульфаттетрасахарид как основные продукты расщепления. Также подтверждено, что расщепляющий фермент продуцирует сульфатированный кератансульфатпентасахарид.
(3) Оптимальный pH реакции
Расщепляющий фермент имеет оптимальный pH реакции от 4,5 до 6 в 0,1М ацетатном буфере или в10мМ трис-ацетатном буфере при 37oC.
(4) Стабильность pH
Расщепляющий фермент обладает pH стабильностью от 6 до 7, когда расщепляющий фермент остается в 0,1М ацетатном буфере или в 10мМ трис-ацетатном буфере при 37oC в течение часа.
(5) Оптимальная температура реакции
Оптимальная температура реакции расщепляющего фермента составляет от 50 до 60oC, когда расщепляющий фермент реагирует в 0,1М ацетатном буфере, pH 6,0, в течение 10 мин.
(6) Термоустойчивость
Расщепляющий фермент устойчив, по меньшей мере, при 45oC или ниже, когда расщепляющий фермент остается в 0,1М ацетатном буфере, pH 6,0, в течение часа.
Расщепляющий кератансульфат фермент, полученный так, как описано выше, используют в приведенных ниже примерах. Однако настоящее изобретение не ограничивается этим ферментом, и в настоящем изобретении могут использоваться другие расщепляющие кератансульфаты ферменты типа эндо- β -N-ацетилглюкозаминидазы, например кератаназа II.
Пример 1
Растворяют 50 г высокосульфатированного кератансульфата, полученного из хрящей акулы, в 300 мл 0,1 М ацетатного буфера (pH 6,0). К этому раствору добавляют 25 единиц расщепляющего
кератансульфат фермента, описанного выше, и высокосульфатированный кератансульфат расщепляют при 37oC в течение 24 ч. После реакции расщепления к реакционной смеси добавляют двойное (по объему, также и далее) количество этанола и смесь перемешивают, и оставляют стоять в течение ночи при комнатной температуре. На следующий день смесь разделяют центрифугированием (4000 об/мин, 15 мин) на супернатант и осадок, и супернатант концентрируют при пониженном давлении, и получают концентрат (называемый здесь далее "супернатантом A"). С другой стороны, осадок растворяют в 300 мл дистиллированной воды, смешивают с тройным количеством этанола и перемешивают. Затем смесь оставляют на ночь при комнатной температуре. На следующий день смесь разделяют центрифугированием на супернатант и осадок и супернатант концентрируют при пониженном давлении, и получают концентрат (называемый здесь далее "супернатантом B").
Супернатант A растворяют в небольшом количестве дистиллированной воды, подвергают гель-хроматографии с использованием колонки с Bio-Gel Р-2 (Bio-Rad) (3,6 х 134 см) и дистиллированной воды в качестве растворителя, и затем подвергают ионообменной хроматографии, и получают фракции, содержащие кератансульфаттетрасахарид (I), кератансульфатпентасахарид (II) и кератансульфатдисахарид (III) соответственно. Каждую из фракций сушат вымораживанием.
Каждую из этих кератансульфатолигосахаридных фракций растворяют в небольшом количестве дистиллированной воды и дополнительно очищают анионообменной хроматографией с использованием колонки с Muromac (Muromachi Kagaku Kogyo) (4,3 x 35 см), которую предварительно уравновешивают дистиллированной водой. В качестве элюента используют физиологический раствор, содержащий линейно возрастающее количество хлорида натрия от нуля до концентрации 0,3 М, и элюируют кератансульфаттетрасахарид (I), кератансульфатпентасахарид (II) и кератансульфатдисахарид (III) соответственно.
Каждую из полученных фракций кератансульфаттетрасахарида (I), кератансульфатпентасахарида (II) и кератансульфатдисахарида (III) концентрируют при пониженном давлении, обессоливают гель-хроматографией с использованием колонки с целлулофином GCL-25 (Seikagaku Corporation) (3,2 x 125 см) и сушат вымораживанием.
Обрабатывают также супернатант B тем же способом, какой описан выше, и получают кератансульфаттетрасахарид (I), кератансульфатпентасахарид (II) и кератансульфатдисахарид (III).
Хроматограммы, полученные при гель-фильтрации с помощью ВЭЖХ (высокоэффективная жидкостная хроматография), кератансульфаттетрасахарида (I), кератансульфатпентасахарида (II) и кератансульфатдисахарида (III), полученных выше, приводятся на фиг. 1-3, соответственно.
Из 50 г кератансульфата получают 7,8 г (15,6%) кератансульфаттетрасахарида (I), 1,3 г (2,6%) кератансульфатпентасахарида (II) и 10,4 г (20,8%) кератансульфатдисахарида (III), и ни один из них не содержит эндотоксинов, нуклеиновых кислот, белков, протеаз и других гликозаминогликанов.
Спектры 1H-ЯМР и 13C-ЯМР кератансульфаттетрасахарида (I), кератансульфатпентасахарида (II) и кератансульфатдисахарида (III), полученных выше, определяют с помощью спектрометра JNM-EX400 (400 МГц, JEOL Ltd.) в случае спектров 1H-ЯМР и спектрометра JNM-EX400 (100 МГц, JEOL Ltd.) в случае спектров 13C-ЯМР, соответственно с натрий-3-(триметилсилил)пропионатом-D4 в качестве стандартного вещества. Химический сдвиг и константу взаимодействия представляют δ (м.д.) и Гц соответственно. Ниже приводятся результаты определения:
Кератансульфаттетрасахарид (I)
1H-ЯМР δ (D2O, 40oC): 4,757 (1H, д), 4,565 (1H, д), 4,561 (1H, д), 4,402 (1H, дд), 4,342 (2H, дд), 3,711 (1H, дд), 3,626 (1H, дд), 3,555 (1H, дд), 2,069 (3Н, с), 2,047 (3Н, с)
13C-ЯМР δ (D2O, 25oC): 177,81, 177,63, 177,30, 105,87, 105,69, 97,84, 93,34, 84,98, 82,41, 81,91, 81,25, 75,55, 75,44, 75,20, 75,13, 75,02, 73,70, 72,68, 72,07, 71,10, 71,01, 70,61, 69,82, 69,82, 69,59, 69,29, 58,92, 57,94, 56,42, 25,09, 24,76
Кератансульфатпентасахарид (II)
1H-ЯМР δ (D2O, 25oC): спектр приводится на фиг. 4
13C-ЯМР δ (D2O, 25oC): 177,80, 177,32, 176,86, 105,92, 105,78, 104,94, 102,60, 97,86, 93,32, 85,05, 82,55, 82,04, 79,75, 78,16, 77,93, 75,69, 75,59, 75,48, 75,24, 74,98, 74,36, 72,68, 72,33, 72,07, 71,38, 71,01, 70,65, 70,35, 69,62, 69,13, 65,38, 63,94, 58,92, 57,99, 56,42, 54,57, 42,47, 25,07, 24,93, 24,76
Кератансульфатдисахарид (III)
1H-ЯМР δ (D2O, 40oC): 5,235 (0,64H, д, J=1,46 Гц), 4,766 (0,41H, д, J= 4,88 Гц), 4,562 (1,15H, д, J=7,82 Гц), 4,44 (0,15H, ушир.), 4,42 (0,22H, ушир. ), 4,357 (1,30Н, д, J=3,42 Гц), 4,313 (0,22H, д, J=4,88 Гц), 4,286 (0,15H, д, J=3,90 Гц), 4,213 (2,37H, д, J=5,37 Гц), 4,183 (0,37H, т, J=3,42, 2,93 Гц), 4,01-3,97 (2,06H, м), 4,006 (д, J=2,44 Гц), 3,927 (1,27H, д, J= 5,37 Гц), 3,86-3,83 (0,37H, ушир.), 3,78-3,69 (2,78H, м), 3,59-3,56 (1,04H, м), 2,052 (3,00H, м)
13C-ЯМР δ (D2O, 25oC): 177,61, 177,30, 105,80, 105,63, 97,82, 93,38, 82,02, 81,55, 75,60, 75,47, 75,15, 75,09, 73,70, 72,04, 71,12, 71,07, 69,93, 69,51, 59,00, 56,44, 25,05, 24,76
Кератансульфаттетрасахарид (I), кератансульфатпентасахарид (II) и кератансульфатдисахарид (III), полученные выше, анализируют масс-спектрометрией с бомбардировкой быстрыми атомами (FABMS).
(1) Катионная FABMS (катионная масс-спектрометрия при бомбардировке быстрыми атомами)
Кератансульфаттетрасахарид (I), кератансульфатпентасахарид (II) и кератансульфатдисахарид (III) растворяют в воде и получают водные растворы с концентрациями 25, 40 и 50 нмоль/мкл соответственно, и каждые 0,1 мкл водных растворов смешивают с 1,0 мкл α -тиоглицерина (используемого в качестве матрицы) и используют для определения. Определения проводят с помощью трехфазного квадрупольного масс-спектрометра finnigan MAT TSQ700 с ксеноном (8 кВ) как источником бомбардирующих атомов. Результаты приводятся в табл. 3. Числа в скобках в таблице представляют относительную интенсивность пиков (%).
(2) Анионная FABMS (анионная масс-спектрометрия при бомбардировке быстрыми атомами)
Кератансульфаттетрасахарид (I), кератансульфатпентасахарид (II) и кератансульфатдисахарид (III) растворяют в воде и получают водные растворы с концентрациями 25, 40 и 50 нмоль/мкл соответственно, и 1,0, 1,0 и 0,5 мкл водного раствора кератансульфатолигосахарида, полученного как описано выше, соответственно смешивают с 1,0 мкл α -тиоглицерина (используемого в качестве матрицы) и используют для определения. Определения проводят с помощью трехфазного квадрупольного масс-спектрометра finnigan MAT TSQ700 с ксеноном (8 кВ) как источником бомбардирующих атомов. Результаты приводятся в табл. 4. Числа в скобках в таблице представляют относительную интенсивность пиков (%).
Кроме того, определяют содержание эндотоксинов, нуклеиновых кислот, белка и протеаз в очищенных кератансульфаттетрасахариде (I), кератансульфатпентасахариде (II) и кератансульфатдисахариде (III), которые получены так, как описано выше. Результаты приводятся в табл. 5.
Содержание гликозаминогликанов, таких как гиалуроновые кислоты, хондроитинсульфат, дерматансульфаты, гиперансульфаты, кератансульфаты и т.п., в очищенных кератансульфаттетрасахариде (I), кератансульфатпентасахариде (II) и кератансульфатдисахариде (III) определяют с помощью электрофореза с ацетатцеллюлозной мембраной (Cepallax, Fuji Photo Film) (буфер 0,1 М пиридинмуравьиная кислота; pH 3,0; ток 0,5 мА/см; время электрофореза 30 мин; краситель 0,5% раствор альцианового синего). В результате ни одно из указанных соединений не обнаружено ни в одном из кератансульфатолигосахаридов (меньше предела обнаружения).
Пример 2. Кератансульфаттетрасахарид (I), кератансульфатпентасахарид (II) и кератансульфатдисахарид (III), полученные как описано выше, испытывают на острую токсичность и подвергают различным фармакологическим испытаниям.
"Испытание на острую токсичность"
Очищенные кератансульфатолигосахариды, которые получают в примере 1, соответственно испытывают на острую токсичность на самцах и самках мышей ICR в возрасте пяти недель. Растворы кератансульфаттетрасахарида (I), кератансульфатпентасахарида (II) и кератансульфатдисахарида (III) соответственно, в ЗФР (забуференный фосфатом физиологический раствор) вводят внутривенно при дозе 1000 или 2000 мг/кг и затем наблюдают за общим внешним видом и смертностью, и в течение 14 дней измеряют массу тела подопытных мышей. После этого животных умерщвляют и вскрывают.
В результате обнаружено, что ни одно из животных не погибает и нет нарушений нормального внешнего вида, массы тела и при вскрытии.
На основании полученных результатов заключают, что минимальная летальная доза описанных выше кератансульфатолигосахаридов даже при внутривенном введении превышает 2000 мг/кг.
"Противовоспалительное испытание"
(1) Противовоспалительные испытания на кроличьей модели индуцированного папаином артрита
Противовоспалительное действие кератансульфатолигосахарида на кроличьей модели индуцированного папаином артрита проверяют, используя в качестве показателя объем синовиальной жидкости.
(1-1) Противовоспалительное действие кератансульфаттетрасахарида на модели билатерального артрита при интраартикулярном введении
В суставные полости обоих коленных суставов белых японских кроликов (самки) массой 3 кг инъецируют 150 мкл папаина (1%) в физиологическом растворе, и получают модель артрита. Через день после инъекции папаина в суставную полость левого колена инъецируют 150 мкл раствора очищенного кератансульфаттетрасахарида (I) в ЗФР (1% раствор; 1,5 мг/сустав), который получен в примере 1 (далее означает здесь "стопа, обработанная кератансульфаттетрасахаридом (I)"), а в первый сустав инъецируют 150 мкл ЗФР (далее означает здесь "стопа, необработанная кератансульфаттетрасахаридом (I)"). В дальнейшем здесь кролики, которым вводили кератансульфаттетрасахарид (I), называются "обработанной группой". Кроликов, которые получили только инъекцию папаина (называемые далее контрольной группой), и кроликов, которым не давали инъекции папаина (далее называемые нормальной группой), также проверяют тем же способом, который описан далее.
Через семь суток после инъекции из суставной артерии берут образец крови и отделяют плазму, содержащую гепарин. После отбора крови кроликов препарируют и отделяют оба коленных сустава. Суставную полость промывают 2 мл физиологического раствора три раза, чтобы извлечь синовиальную жидкость. Определяют содержание кальция в плазме и в извлеченной синовиальной жидкости, и вычисляют объем синовиальной жидкости по следующей формуле:
Объем синовиальной жидкости (мкл/сустав) = количество кальция в извлеч. синов.жидк. (мкг/сустав)/содержание кальция в плазме (мкг/мл)
Результаты, полученные при описанном выше испытании, приводятся в табл. 6. В таблице "n" показывает число кроликов в каждой группе, использованных при эксперименте.
Как видно из этих результатов, объем синовиальной жидкости в группе, обработанной кератансульфаттетрасахаридом (I) настоящего изобретения, значительно меньше, чем в контрольной группе, и, следовательно, подтверждается функция кератансульфаттетрасахарида (I) улучшать состояния при артрите.
(1-2) Противовоспалительное действие кератансульфаттетрасахарида на модели билатерального артрита при внутримышечном введении
Модель артрита получают по способу, описанному в (1-1), и через день после инъекции папаина в левую бедренную мышцу инъецируют 150 мкл раствора в ЗФР кератансульфаттетрасахарида (I) (1% раствор; 0,5 мг/кг массы), который получен в примере 1 (далее обозначается здесь как "группа, обработанная кератансульфаттетрасахаридом (I)"). В качестве контроля модели артрита инъецируют 150 мкл ЗФР вместо раствора кератансульфаттетрасахарида (I) в ЗФР, и таких кроликов далее называют контрольной группой. Кроликов, которым не давали инъекцию папаина (далее называемые нормальной группой), затем также проверяют тем же способом. Через семь суток после инъекции объем синовиальной жидкости определяют так же, как в разделе (1-1).
Как видно из этих результатов, объем синовиальной жидкости в группе, обработанной кератансульфаттетрасахаридом (I) настоящего изобретения, значительно меньше, чем в контрольной группе, и, следовательно, подтверждается функция кератансульфаттетрасахарида (I) улучшать состояния при артрите.
(1-3) Противовоспалительное действие кератансульфаттетрасахарида на модели одностороннего артрита при внутримышечном введении
В суставные полости левого сустава белых японских кроликов (самки) массой 3 кг инъецируют 150 мкл папаина (1%) в физиологическом растворе, а правый сустав не обрабатывают и получают модель одностороннего артрита. Через день после инъекции папаина в левую бедренную мышцу инъецируют 150 мкл раствора очищенного кератансульфаттетрасахарида (I) в ЗФР (2, 1 и 0,5% раствор; 1,0, 0,5 и 0,25 мг/кг соответственно), который получен в примере 1 (далее эта группа называется здесь "группой, обработанная кератансульфаттетрасахаридом (I)"). В качестве контроля модели артрита инъецируют 150 мкл ЗФР вместо раствора кератансульфаттетрасахарида (I) в ЗФР, (далее эта группа называется здесь "группой, необработанная кератансульфаттетрасахаридом (I)"). Кроликов, которым не давали инъекцию папаина (далее называемые нормальной группой), затем также проверяют тем же способом. Через семь суток после инъекции вычисляют объем синовиальной жидкости таким же способом, как в разделе (1-1).
Результаты, полученные при описанном выше испытании, приводятся в табл. 8. В таблице "n" показывает число кроликов, использованных при эксперименте в каждой группе.
Как видно из этих результатов, объем синовиальной жидкости в группе, обработанной кератансульфаттетрасахаридом (I) настоящего изобретения, значительно меньше, чем в контрольной группе, и, следовательно, подтверждается функция кератансульфаттетрасахарида (I) улучшать состояния при артрите.
(1-4) Противовоспалительное действие различных кератансульфатолигосахаридов на модели одностороннего артрита при внутримышечном введении
Проверку осуществляют таким же способом, как в (1-3), за исключением того, что используют по 150 мкл растворов очищенных кератансульфаттетрасахарида (I), кератансульфатпентасахарида (II) и кератансульфатдисахарида (III) (1% растворы; 0,5 мг/кг), полученных в примере 1, в ЗФР. Результаты показаны на фиг. 5. На этой фигуре *, ** и *** представляют, что имеется значимое различие с р<0,05, р<0,01 и р<0,001 соответственно. В каждой группе для проверки берут по 10 кроликов.
Согласно этим результатам, количество синовиальной жидкости в любой из групп, обрабатываемых кератансульфаттетрасахаридом (I), кератансульфатпентасахаридом (II) и кератансульфатдисахаридом (III), значительно меньше, чем в контрольной группе, и, следовательно, подтверждается функция улучшения состояния при артрите для каждого из описанных выше кератансульфатолигосахаридов.
(2) Противовоспалительные испытания с измененной пассивной реакцией Артюса отека стопы у крыс
Действие кератансульфатолигосахаридов проверяют по измененной пассивной реакции Артюса отека стопы у крыс, которая представляет собой модель аллергического воспаления типа III. Для этого кроличью антиовальбуминную сыворотку вводят подкожно в подошвы стоп крысам, которым предварительно вводят испытываемые вещества, затем вводят овальбумин посредством инъекции в каудальную вену, чтобы вызвать воспаление (отек), и проверяют ингибирующее действие на отек испытываемых веществ.
(Введение испытываемых веществ)
Самцов крыс Crj: SD в возрасте пяти недель выдерживают около 17 ч без пищи после недельного карантина и перед индуцированием воспаления вводят в качестве испытываемых веществ очищенный кератансульфаттетрасахарид (I), который получен в примере 1, индометацин (Sigma; серия N 19F0018) или дексаметазон (Banyu Pharmaceutical; инъекция Decadron; серия 8D307P), или физиологический раствор (Otsuka Pharmaceutical; серия N КЗН72) как негативный контроль. При применении кератансульфаттетрасахарид (I) и дексаметазон растворяют в физиологическом растворе соответственно, а индометацин растворяют в 0,5% натрийкарбоксиметилцеллюлозе (CMC-Na; Wako Pure Chemical Industries; серия N PTN1418). Объем дозы составляет 0,5 мл на 100 г массы при каждом испытании. Что касается способа введения, то кератансульфаттетрасахарид (I), физиологический раствор и дексаметазон вводят через каудальную вену, а индометацин вводят перорально. Вещества, за исключением индометацина, вводят скрытно (blind method).
Расписание введения каждого испытываемого вещества приводится ниже. Каждая группа состоит из пяти животных.
(I) Введение за пять минут до индуцирования воспаления
(1) Физиологический раствор (негативный контроль)
(2) Кератансульфаттетрасахарид (I) 1 мг/кг
(3) Кератансульфаттетрасахарид (I) 3 мг/кг
(4) Кератансульфаттетрасахарид (I) 10 мг/кг
(II) Введение за 30 мин до индуцирования воспаления
(5) Индометацин (положительный контроль) 5 мг/кг
(III) Введение за три часа до индуцирования воспаления
(6) Кератансульфаттетрасахарид (I) 1 мг/кг
(7) Кератансульфаттетрасахарид (I) 3 мг/кг
(8) Кератансульфаттетрасахарид (I) 10 мг/кг
(9) Дексаметазон (положительный контроль) 1 мг/кг
(Индукция воспаления)
Каждой из крыс, описанных выше, вводят подкожно в подошвы стоп кроличью антиовальбуминную сыворотку, а затем посредством инъекции в каудальную вену вводят овальбумин, чтобы вызвать воспалительный отек стоп. Применяемую антисыворотку получают следующим образом. Кроликам в участки на спине инъецируют интрадермально 1 мл смешанных в равных частях раствора (эмульсии) физиологического раствора, содержащего 2% овальбумина (10 мг на животное, яичный альбумин 5 х Cryst, серия Р93601; Seikagaku Corporation) и полного адъюванта Фрейнда (FCA) один раз в неделю всего три раза для их сенсибилизации. Через 34 дня после последней сенсибилизации отбирают кровь и получают антисыворотку. Титр антител полученной антисыворотки определяют методом двойного слоя. А именно определение осуществляют с использованием реакции "белой" преципитации и антисыворотки, разбавленной физиологическим раствором, и физиологического раствора, содержащего 0,1% овальбумина (1 мг/мл) в качестве индикатора. В результате полученный титр антител антисыворотки составляет х 27.
Через промежуток времени, который устанавливают для каждой группы, крысам, которым вводили каждое из испытуемых веществ, вводят в подошвы левых задних стоп по 0,1 мл разбавленной в шесть раз антисыворотки. Затем в каудальную вену для индуцирования воспаления вводят физиологический раствор, содержащий 0,5% овальбумина (25 мг/5 мл/кг). В каждой группе с помощью устройства для определения объема стопы (TK-101, Unicom) определяют объем обработанной стопы перед тем, как вызвать воспаление и через один, два, три и четыре часа после индуцирования воспаления, и по отличию от объема до индуцирования отека получают степень развития отека стопы, и вычисляют степень ингибирования развития отека в группах, которым вводили испытываемые вещества, относительно контрольной группы. При каждой полученной степени развития отека различие между средними величинами проверяют с помощью критерия минимальном значимом различии. Степень развития отека стопы и степень ингибирования развития отека в каждой обработанной группе показаны в табл. 9, и степень развития отека стопы в обработанных группах, которым вещество вводили за пять минут и за три часа до индуцирования воспаления, показаны на фиг. 6 и на фиг. 7 соответственно. На этих фигурах * и ** показывают, что имеется значимое различие с р<0,05 и р<0,001 соответственно.
Результаты показывают, что степень развития отека через час в группе, обработанной физиологическим раствором, которая является негативным контролем, составляет 40,9%, в то время как в группах, обработанных кератансульфаттетрасахаридом (I), при его введении за пять минут до индуцирования воспаления, этот показатель составляет от 29,1 до 34,4%, и наблюдают значимое различие от группы, которой вводили 1 мг/кг и группы, обработанной 10 мг/кг. Хотя зависимой от дозы реакции не наблюдают при и через час после индуцирования воспаления, степень развития отека стопы в группе, обработанной 3 мг/кг, и в группе, обработанной 10 мг/кг, составляет 37,2 и 35,4% соответственно, что достаточно мало даже через четыре часа. В группах, обработанных кератансульфаттетрасахаридом (I) за три часа до индуцирования воспаления, хотя значимого различия не наблюдают через час после индуцирования воспаления, существенно низкие значения наблюдают в группе, обработанной 3 мг/кг, через два часа, в группе, обработанной 10 мг/кг, через три часа и в группе, обработанной 1 мг/кг, через четыре часа, и эти величины составляют 35,3, 41,5 и 38% соответственно. В группе, обработанной индометацином, существенно низкие величины наблюдают через два часа и через четыре часа. В группе, обработанной дексаметазоном, существенно низкие величины наблюдают в любой точке определения между одним и четырьмя часами после индуцирования воспаления.
Степень ингибирования развития отека в группе, обработанной индометацином, составляет от 9 до 17,5% через один час и через четыре часа, в то время как вычислено, что в группах, обработанных кератансульфаттетрасахаридом (I) при введении с опережением на пять минут, эти показатели составляют от 8,6 до 36,5%. В группах, обработанных кератансульфаттетрасахаридом (I) при введении с опережением на три часа, степень ингибирования составляет от -8,1 до 24,4%. С другой стороны, в группе, обработанной дексаметазоном, степень ингибирования развития отека стопы достигает 31,7-58,1%.
(3) Противовоспалительный тест на модели с плевритом, вызванным у крыс каррагинином
Действие кератансульфатолигосахаридов проверяют на крысиной модели каррагининового плеврита, которую обычно используют для оценки противовоспалительных средств.
При этом испытании используют самок крыс S.D. (n=37) maccol 150-170 г. Растворяют λ каррагинин (Sigma) в физиологическом растворе до концентрации 2%, и раствор фильтруют через 0,8 мкм фильтр. Полученный раствор каррагинина вводят интраторакально в количестве 100 мкл/животное, и получают модель плеврита.
Крысам - моделям плеврита (n=19), описанным выше, вводят подкожно (s.c.) кератансульфаттетрасахарид (I), растворенный в ЗФР, при дозах 20 или 10 мг/кг. В качестве позитивного контроля восьми крысам, описанным выше, вводят подкожно стероид (дексаметазонацетат; Banyu Pharmaceutical) в количестве 150 мкг/кг, что составляет клиническую дозу. В качестве негативного контроля 10 крысам вводят подкожно ЗФР.
Каждое введение осуществляют сразу после введения каррагинина. Обработанные группы указываются в табл. 10.
Каждую крысу вскрывают через шесть часов после введения λ -каррагинина. Вскрывают полость грудной клетки у крыс и собирают сохранившийся плевральный выпот, используя 2-миллилитровый шприц с зондом. После этого внутреннюю часть полости грудной клетки обрабатывают 1 мл физиологического раствора и извлекают промывающий раствор. Определяют объем плеврального выпота, извлеченного шприцем, и с помощью автоматизированного цитометра определяют число лейкоцитов (число клеток) в плевральном выпоте. Результаты приводятся на фиг. 8 и фиг. 9 соответственно. На фигурах * и ** представляют, что имеется значимое различие с р<0,05 и р<0,01 соответственно (где "р" означает уровень значимости по критерию Дункана).
Как показано на фиг. 8, объем плеврального выпота в группе, обработанной 10 мг/кг кератансульфаттетрасахарида (I), значительно меньше, чем в группе негативного контроля, но почти такой же, как в группе, обработанной 20 мг/кг кератансульфаттетрасахарида (I) и, следовательно, не наблюдается зависимости от дозы. Количество плеврального выпота в группе, обработанной дексаметазонацетатом, значительно ниже количества в группе негативного контроля. Число лейкоцитов в плевральном выпоте в каждой из групп, обработанных 10 мг/кг и 20 мг/кг кератансульфаттетрасахарида (I), значительно меньше числа лейкоцитов в группе негативного контроля и наблюдается зависимое от дозы снижение числа лейкоцитов (см. фиг. 9). Число лейкоцитов в группе, обработанной дексаметазонацетатом, значительно ниже числа лейкоцитов в контрольной группе (см. фиг. 9).
Из описанных выше результатов следует, что подтверждается противовоспалительное действие кератансульфаттетрасахарида (I) в случае крысиной модели плеврита, вызванного каррагинином.
(4) Ингибирующее действие на генерацию активного кислорода (O2 -) в нейтрофилах морской свинки
Самкам морских свинок Hartley в возрасте пяти недель (приобретены у Japan SLC) вводят интраперитонеально 20 мл 0,2% водного раствора гликогена (тип II; Oyster; Sigma), растворенного в физиологическом растворе, который предварительно стерилизуют в автоклаве. Морских свинок умерщвляют посредством кровоизвлечения через 16 часов после обработки и впрыскивают в брюшную полость 20 мл физиологического раствора, содержащего гепарин при концентрации 10 Е/мл, чтобы извлечь перитонеальный эксудат. Все дальнейшие операции осуществляют при охлаждении смесью воды со льдом, за исключением инкубации. Извлеченный эксудат центрифугируют при 1000 об/мин в течение 10 мин, полученный осадок гемолизуют очищенной водой в течение 30 с и возвращают в изотоническое состояние раствором Хэнкса при двойной концентрации (не содержит фенолового красного Nissui Seiyaku), а затем центрифугируют при 1000 об/мин в течение 10 мин. Полученный осадок суспендируют в растворе Хэнкса и центрифугируют, и операции повторяют еще раз, чтобы получить нейтрофилы. Собранные нейтрофилы морских свинок суспендируют в растворе Хэнкса, определяют число лейкоцитов в суспензии с помощью цитометра (система К-2000; Toa lyo Denshi Co. ) и суспензию, разбавленную раствором Хэнкса до концентрации 2 х 106 клеток/мл, используют при определении в качестве суспензии клеток. После смешивания 1 мл суспензии клеток и 10 мкл очищенного кератансульфатолигосахарида (кератансульфаттетрасахарида (I), кератансульфатпентасахарида (II) или кератансульфатдисахарида (III)), полученного в описанном выше примере 1, смесь предварительно инкубируют при 37oC в течение часа. После этого к смеси добавляют 50 мкл 1,6 мМ цитохрома с (тип III; Horse Heart; Sigma) и 10 мкл 100 мкМ N-формил-Met-Leu-Phe (далее здесь иногда называемого "FMLP", Sigma) в указанном порядке и перемешивают. Затем смесь инкубируют при 37oC в течение 10 мин, охлаждают на льду, чтобы остановить реакцию, и центрифугируют при 3000 об/мин в течение пяти минут.
Супернатант, полученный при центрифугировании, отделяют и определяют его поглощение при 550 нм, и оценивают количество восстанавливающего цитохрома C на 2 х 106 клеток после инкубации в течение 10 мин. Количество восстанавливающего цитохрома C возрастает при генерации активного кислорода (O
Результаты показывают, что кератансульфаттетрасахарид (I) при концентрации 0,01, 0,1 и 1,0 мг/мл заметно ингибирует генерацию активного кислорода (O
(Противоаллергическая функция)
Различные кератансульфатолигосахариды закапывают в глаза морским свинкам, у которых вызван аллергический конъюнктивит, чтобы проверить их действие.
(1) Действие кератансульфаттетрасахарида (I) на аллергический конъюнктивит
Толуолдиизоцианат (называемый здесь далее TDI) растворяют в этилацетате до концентрации 10%. В билатеральные преддверия носа 10 самкам морских свинок Hartley, массой порядка 900-1000 г, подают один раз в сутки в течение пяти суток 10% TDI (10 мкл/животное), полученный как описано выше, и получают модели, сенсибилизированные TDI. Раствор в ЗФР кератансульфаттетрасахарида (I), полученного в примере 1 (100 мг/мл), закапывают сенсибилизированным TDI моделям в левый глаз, а в правый глаз закапывают ЗФР в качестве контроля. Доза закапывания составляет одну каплю (48±4,6 мкл (ст. откл., S. D.)) при каждом закапывании в глаза. Через 10 мин в оба глаза закапывают 6,5 мкл 10% TDI, чтобы вызвать конъюнктивит. После выдержки в течение пяти минут в левый глаз снова закапывают раствор в ЗФР кератансульфаттетрасахарида (I) (100 мг/мл), а в правый глаз закапывают ЗФР. Через 15 мин проверяют оба глаза. Оценивают степень развития конъюнктивита по трем показателям: гиперемия, отек и слезоотделение, четырьмя оценками - 0, +1, +2 и +3. В результате этой проверки получают средние оценки и стандартные отклонения, приведенные на фиг. 11. На этой фигуре * означает, что имеется значимое различие с р<0,05 (где "р" означает уровень значимости по критерию χ2).
Из результатов следует, что кератансульфаттетрасахарид (I) имеет свойство демонстрировать ингибирование всех трех явлений: гиперемии, отека и слезоотделения и в особенности существенно уменьшается отек по сравнению с контрольными животными.
(2) Действие различных кератансульфатолигосахаридов на аллергический конъюнктивит
Растворы в ЗФР, полученных в описанном выше примере 1, очищенных кератансульфатдисахарида (III), кератансульфаттетрасахарида (I) и кератансульфатпентасахарида (II) (6,0 мг/мл соответственно) как испытываемых веществ соответственно закапывают в левый глаз сенсибилизированных TDI моделей (по 10 животных в каждой группе), которые получают тем же способом, как описано выше в (1), а в правый глаз в качестве контроля закапывают ЗФР. Развитие конъюнктивита оценивают так же, как описано выше в (1). В результате этой проверки получают средние значения для точек и стандартные отклонения, показанные на фиг. 12. На этой фигуре * означает, что имеется значимое различие с р<0,05 (где "р" означает уровень значимости по критерию χ2).
В результате обнаруживается, что любое вещество из числа кератансульфатдисахарида (III), кератансульфаттетрасахарида (I) и кератансульфатпентасахарида (II) имеет свойство показывать ослабление всех проявлений гиперемии, отека и слезоотделения и в особенности подтверждено, что кератансульфаттетрасахарид (I) обнаруживает значительное ингибирующее действие на отек.
(3) Действие кератансульфаттетрасахарида (I) в различных концентрациях на аллергический конъюнктивит
Раствор в ЗФР, содержащий очищенный кератансульфаттетрасахарид (I), полученный в описанном выше примере 1, при различных концентрациях (6, 3, 1,5 или 0,75 мг/мл) закапывают сенсибилизированным TDI моделям по 10 животных в каждой группе, которых подготавливают таким же способом, как описано выше в (1) соответственно в левый глаз, а в правый глаз закапывают ЗФР в качестве контроля. Развитие конъюнктивита оценивают так же, как описано выше в (1). В результате этой проверки получают средние значения для точек и стандартные отклонения, показанные на фиг. 13. На этой фигуре * означает, что имеется значимое различие с р<0,05 (где "р" означает уровень значимости по критерию χ2).
В результате обнаруживается, что растворы кератансульфаттетрасахарида (I) в ЗФР при всех концентрациях имеют свойство обнаруживать ингибирование всех проявлений гиперемии, отека и слезоотделения и в особенности эти растворы при концентрации 6, 3 и 1,5 мг/мл обнаруживают ингибирующее действие на отек.
"Иммуномодулирующая функция, функция индуцирования клеточной дифференцировки и функция индуцирования апоптоза"
Действие кератансульфатолигосахаридов проверяют на мышах MRL, которые представляют мышиную модель аутоиммунного заболевания.
(1) Подавляющее действие на массу лимфоузлов
(1-1) Испытания при повторном внутримышечном введении кератансульфаттетрасахарида (I) мышам MRL в течение четырех недель
Раствор в ЗФР очищенного кератансульфаттетрасахарида (I) (100 мг/шт), который получен в описанном выше примере 1, при дозе 10 мг/кг массы (это называется здесь далее обработанной группой) и ЗФР в качестве контроля инъецируют внутримышечно, соответственно в область бедра мышам MRL-lpr/lpr пять раз в неделю в течение четырех недель. После этого мышей вскрывают и определяют массу селезенки и мезентериальных лимфатических узлов, и получают среднее значение массы. Результаты и стандартные отклонения приводятся в табл. 11. В этой таблице "n" показывает число использованных мышей.
В результате получают, что в группе, которой инъецировали кератансульфаттетрасахарид (I), наблюдается тенденция подавления возрастания селезенки и мезентериальных лимфатических узлов и, следовательно, это обстоятельство подтверждает иммуномодулирующую функцию кератансульфаттетрасахарида (I).
(1-2) Испытания при повторном внутримышечном введении кератансульфатдисахарида (III) мышам MRL в течение 28 сут.
Раствор в ЗФР очищенного кератансульфатдисахарида (III), который получен в описанном выше примере 1, при дозе 1, 5 или 25 мг/кг массы (что называется здесь далее группой, обработанной 1 мг/кг, группой, обработанной 5 мг/кг, и группой, обработанной 25 мг/кг соответственно) и ЗФР в качестве контроля инъецируют внутримышечно, соответственно в область бедра мышам MRL-lpr/lpr семь раз в неделю в течение четырех недель. После этого мышей вскрывают и определяют массу подчелюстных лимфатических узлов, и получают среднее значение массы. Результаты и стандартные отклонения приводятся на фиг. 14. В каждой группе используют по шесть мышей. Кроме того, на этой фигуре * показывает, что есть значимое различие с р<0,05 (где "р" означает уровень значимости по множественному сравнительному критерию Bonferroni).
В результате получают, что в группах, обработанных кератансульфатдисахаридом (III), наблюдается при сравнении с контрольной группой эффект подавления возрастания массы подчелюстных лимфатических узлов при любой дозе, особенно при вводимой дозе 5 мг/кг и, следовательно, это обстоятельство подтверждает иммуномодулирующую функцию кератансульфатдисахарида (III).
(1-3) Испытания при повторном внутримышечном введении кератансульфатдисахарида (III) мышам MRL в течение 56 сут.
Раствор в ЗФР очищенного кератансульфатдисахарида (III), который получен в описанном выше примере 1, при дозе 2,5, 5 или 10 мг/кг массы (что называется здесь далее группой, обработанной 2,5 мг/кг, группой, обработанной 5 мг/кг, и группой, обработанной 10 мг/кг соответственно) и ЗФР в качестве контроля (что иногда называется здесь контрольной группой) инъецируют внутримышечно, соответственно в область бедра мышам MRL-lpr/lpr семь раз в неделю в течение восьми недель. После этого мышей вскрывают и определяют массу мезентериальных лимфатических узлов и подчелюстных лимфатических узлов, и получают средние значения массы соответственно. Результаты, относящиеся к мезентериальным лимфатическим узлам и подчелюстным лимфатическим узлам, приводятся на фиг. 15 и 16 соответственно, вместе со стандартными отклонениями. В каждой группе используют по семь мышей.
В результате в группе, обработанной 2,5 мг/мл кератансульфатдисахарида (III), наблюдают эффект подавления возрастания массы мезентериальных лимфатических узлов, а в группе, обработанной 10 мг/кг, наблюдают подавление возрастания массы мезентериальных и подчелюстных лимфатических узлов и, следовательно, эти обстоятельства подтверждают иммуномодулирующую функцию кератансульфатдисахарида (III).
(2) Функция индуцирования клеточной дифференцировки
(2-1) Анализ индукции клеточной дифференцировки с использованием в качестве индикатора концентрации окрашивания клеток
Раствор в ЗФР очищенного кератансульфатдисахарида (III), который получен в описанном выше примере 1, при дозе 1, 5 или 25 мг/кг массы (что называется здесь далее группой, обработанной 1 мг/кг, группой, обработанной 5 мг/кг, и группой, обработанной 25 мг/кг соответственно) и ЗФР в качестве контроля (что иногда называется здесь контрольной группой) инъецируют внутримышечно, соответственно в область бедра мышам MRL-lpr/lpr семь раз в неделю в течение четырех недель. После этого мышей вскрывают и готовят образцы срезов (Не - окрашивание) мезентериальных лимфатических узлов и подчелюстных лимфатических узлов. Анализируют концентрации окрашивания на единицу площади образцов с помощью анализатора изображения (PIAS). В случае недифференцированных клеток концентрация окрашивания на единицу площади мала из-за высокой доли цитоплазмы и ядра окрашены плохо. В случае дифференцированных клеток концентрация на единицу площади высокая вследствие высокой доли ядер и окрашивание плотное.
Результаты анализа мезентериальных лимфатических узлов и подчелюстных лимфатических узлов приводятся на фиг. 17 и 18 соответственно. На этих фигурах ** означает, что имеется значимое различие с р<0,01 (где "р" означает уровень значимости по множественному сравнительному критерию Bonferroni). В каждой группе использовали шесть мышей.
В результате в группе, обработанной кератансульфатдисахаридом (III), наблюдают возрастание концентрации окрашивания на единицу площади (уменьшение относительной освещенности) при любой дозе, а в особенности в группе, обработанной 5 мг/кг, и в группе, обработанной 25 мг/кг, концентрации окрашивания существенно возрастают при сравнении с контрольной группой. Это обстоятельство указывает на увеличение количества дифференцированных клеток благодаря кератансульфатдисахариду (III), и предполагают у кератансульфатдисахарида (III) функцию индуцирования клеточной дифференцировки.
(2-2) Анализ индукции клеточной дифференцировки с использованием в качестве индикатора лимфоцитных поверхностных антигенов лимфатических узлов
Раствор в ЗФР очищенного кератансульфатдисахарида (III), который получен в описанном выше примере 1, при дозе 2,5, 5 или 10 мг/кг массы (что называется здесь далее группой, обработанной 2,5 мг/кг, группой, обработанной 5 мг/кг, и группой, обработанной 10 мг/кг соответственно) и ЗФР в качестве контроля (что иногда называется здесь контрольной группой) инъецируют внутримышечно, соответственно в область бедра мышам MRL-lpr/lpr семь раз в неделю в течение восьми недель. После этого мышей вскрывают и лимфатические узлы измельчают на клеточном фильтре (Falcon 2350), чтобы получить лимфоциты. Лимфоциты, полученные от каждой группы, подвергают двойной окраске иммунным методом антителом против CD3 (Seikagaku Corporation) и антителом против CD4 (Pharminjen), антителом против CD3 и антителом против CD8a (Pharminjen), и антителом против CD3 и антителом против В220 (Pharminjen) соответственно. Поверхностные антигены клеток CD3, CD4 и CD8a являются клеточными поверхностными антигенами, которые экспрессируются на Т-клетках, а В220 экспрессируются на В-клетках. Известно, что никакой экспрессии этих клеточных поверхностных антигенов не наблюдается на нуль-лимфоцитах.
Доля (%) позитивных клеток CD3 и CD4 (далее иногда обозначаемых как "CD3+CD4+клетки"; главным образом, хелперные Т-клетки) от всех лимфоцитов и стандартные отклонения показаны на фиг. 19, доля позитивных клеток CD3 и CD8a (далее иногда обозначаемых как "CD3+CD8a+клетки"; главным образом, супрессорные Т-клетки и цитотоксические Т-клетки) и стандартные отклонения показаны на фиг. 20, и доля позитивных клеток CD3 и В220 (далее иногда обозначаемых как "CD3+В220+клетки"; аномальные Т-клетки, имеющие поверхностные антигены В-клеток) и стандартные отклонения показаны на фиг. 21. На этих фигурах * показывает, что имеется значимое различие с р<0,05 (где "р" означает уровень значимости по множественному сравнительному критерию Ryan).
Как видно из фиг. 19, доля CD3+CD4+клеток в группе, обработанной 10 мг/кг кератансульфатдисахарид (III), существенно возрастает по отношению к контрольной группе, группе, обработанной 2,5 мг/кг и группе, обработанной 5 мг/кг. Это указывает на дифференцировку нуль-лимфоцитов в CD3+CD4+клетках при введении адекватного количества кератансульфатдисахарида (III).
Как видно из фиг. 20, доля CD3+CD8а+клеток в группе, обработанной 10 мг/кг кератансульфатдисахарида (III), возрастает по отношению к контрольной группе, группе, обработанной 2,5 мг/кг, и группе, обработанной 5 мг/кг. Это указывает на дифференцировку нуль-лимфоцитов в CD3+CD8a+клетках при введении адекватного количества кератансульфатдисахарида (III).
Как видно из фиг. 21, доля CD3+В220+клеток в группе, обработанной 10 мг/кг кератансульфатдисахарида (III), уменьшается по отношению к контрольной группе, группе, обработанной 2,5 мг/кг, и группе, обработанной 5 мг/кг. Это указывает на исчезновение CD3+В220+клеток, которые являются аномальными, при введении адекватного количества кератансульфатдисахарида (III) и подтверждает индукцию дифференцировки в нормальных лимфоцитах. Эти результаты предполагают функцию индуцирования клеточной дифференцировки у количества кератансульфатдисахарида (III).
(3) Функция индуцирования апоптоза
Раствор в ЗФР очищенного кератансульфатдисахарида (III), который получен в описанном выше примере 1, при дозе 1 мг/кг, 5 мг/кг или 25 мг/кг массы (что называется здесь далее группой, обработанной 1 мг/кг, группой, обработанной 5 мг/кг, и группой, обработанной 25 мг/кг соответственно) и ЗФР в качестве контроля (что иногда называется здесь контрольной группой) инъецируют внутримышечно, соответственно в область бедра мышам MRL-lpr/lpr семь раз в неделю в течение четырех недель. После этого мышей вскрывают и готовят образцы срезов подчелюстных лимфатических узлов, окрашенных по методу Gavrieli et al.,; Terminal deoxynucleotidyl transferase (TdT) - mediated nick end labeling method; (J. Cell Biol., 119, 493-501 (1992)). При этом методе окрашивания клетки с индуцированным апоптозом можно определить с помощью обнаружения концов фрагментированной ДНК. Полученные образцы наблюдают с помощью светового микроскопа и определяют число окрашенных клеток (клетки с клетки с индуцированным апоптозом; далее иногда называются здесь апоптозными клетками) на единицу площади. Результаты и стандартные отклонения приводятся на фиг. 22. На этих фигурах * и ** означают, что имеется значимое различие с р<0,05 и р<0,01 соответственно (где "р" означает уровень значимости по множественному сравнительному критерию Bonferroni). В каждой группе используют по шесть мышей.
В результате наблюдают возрастание числа апоптозных клеток в группах, обработанных кератансульфатдисахаридом (III), при любой дозе и в группе, обработанной 5 мг/кг, в особенности число апоптозных клеток возрастает существенно по сравнению с контрольной группой.
Кроме того, готовят образцы срезов (Не - окрашивание) подчелюстных лимфатических узлов мышей каждой группы и в световом микроскопе наблюдают наличие апоптозных тел в группах, обработанных кератансульфатдисахаридом (III), при любой дозе.
Эти результаты предполагают функцию индуцирования апоптоза у кератансульфатдисахарида (III).
Описанные выше результаты подтверждают иммуномодулирующую функцию, функцию индуцирования клеточной дифференцировки и функцию индуцирования апоптоза кератансульфатолигосахаридов.
Пример 3. Мази
Следуя традиционному методу, очищенный кератансульфаттетрасахарид (I), полученный в примере 1, растворяют в гидрофильной мази, фармакопея Японии, при концентрации 10 мг/мл и получают мазь. Эту мазь можно применять как в качестве противовоспалительного средства, так и в качестве противоаллергического средства.
Пример 4. Глазные капли
Следуя традиционному методу, очищенный кератансульфаттетрасахарид (I), полученный в примере 1, и гиалуронат натрия растворяют в физиологическом растворе с pH 6,8-7,6, установленным фосфатом при концентрациях 10 и 2 мг/мл соответственно, и получают глазные капли. Эти глазные капли можно применять в качестве противовоспалительного средства и противоаллергического средства.
Пример 5. Препарат с липосомным включением
Очищенный кератансульфаттетрасахарид (I), полученный в примере, растворяют при концентрации 10 мг/мл в липосомном включении (Aquasome LA; Nikko Chemicals), содержащем лецитин, и подвергают воздействию ультразвука, чтобы получить клатрат. Это липосомное включение можно применять в качестве любого средства из числа противовоспалительного средства, противоаллергического средства, иммуномодулятора, индуктора клеточной дифференцировки и индуктора апоптоза.
Пример 6
Инъекции
Следуя традиционному методу, очищенный кератансульфаттетрасахарид (I), полученный в примере 1, растворяют в физиологическом растворе с pH 6,8-7,6, установленным фосфатом, при концентрации 10 мг/мл и раствор фильтруют в асептических условиях через 0,22 мкм фильтр и получают раствор для инъекции. Этот раствор для инъекции можно применять в качестве любого из числа противовоспалительного средства, противоаллергического средства, иммуномодулятора, индуктора клеточной дифференцировки и индуктора апоптоза.
Промышленная применимость
Фракции очищенных высокосульфатированных кератансульфатолигосахаридов настоящего изобретения имеют высокую степень очистки и не содержат по существу эндотоксинов, нуклеиновых кислот, белка протеазы и других гликозаминогликанов, за исключением описанных выше олигосахаридов и, следовательно, могут использоваться в качестве фармацевтических препаратов, например, нового противовоспалительного средства.
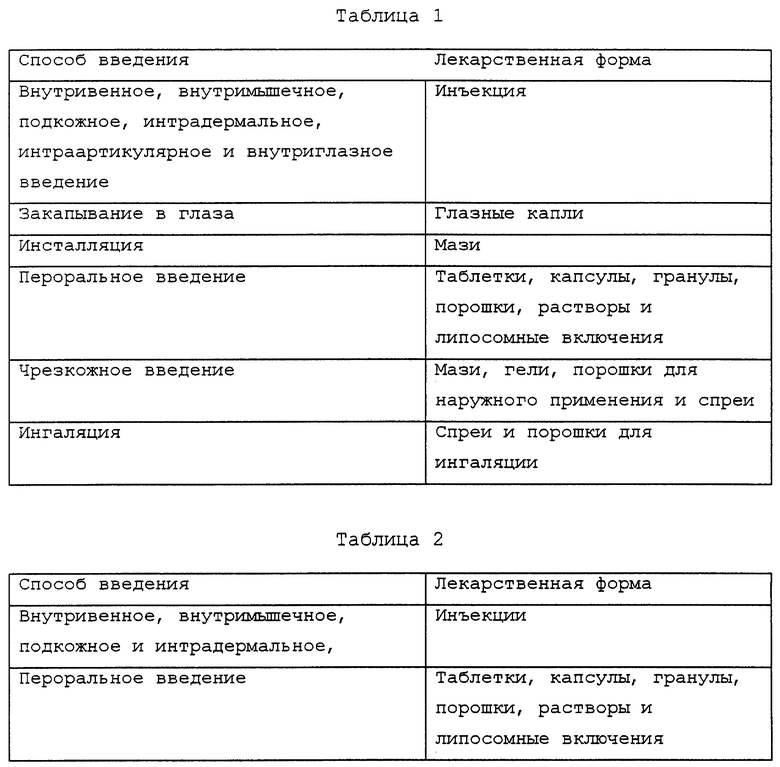
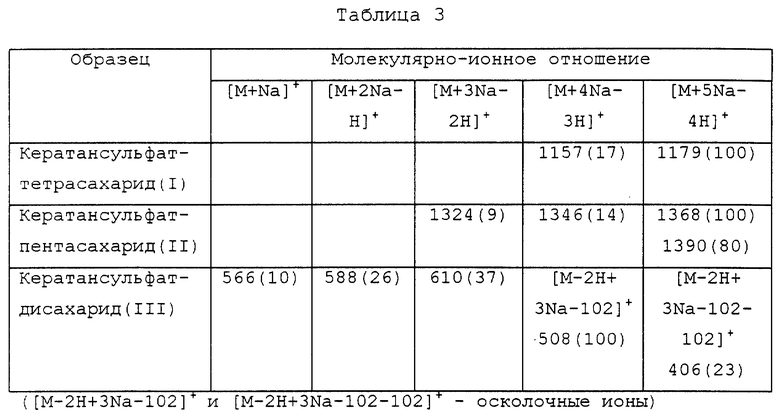
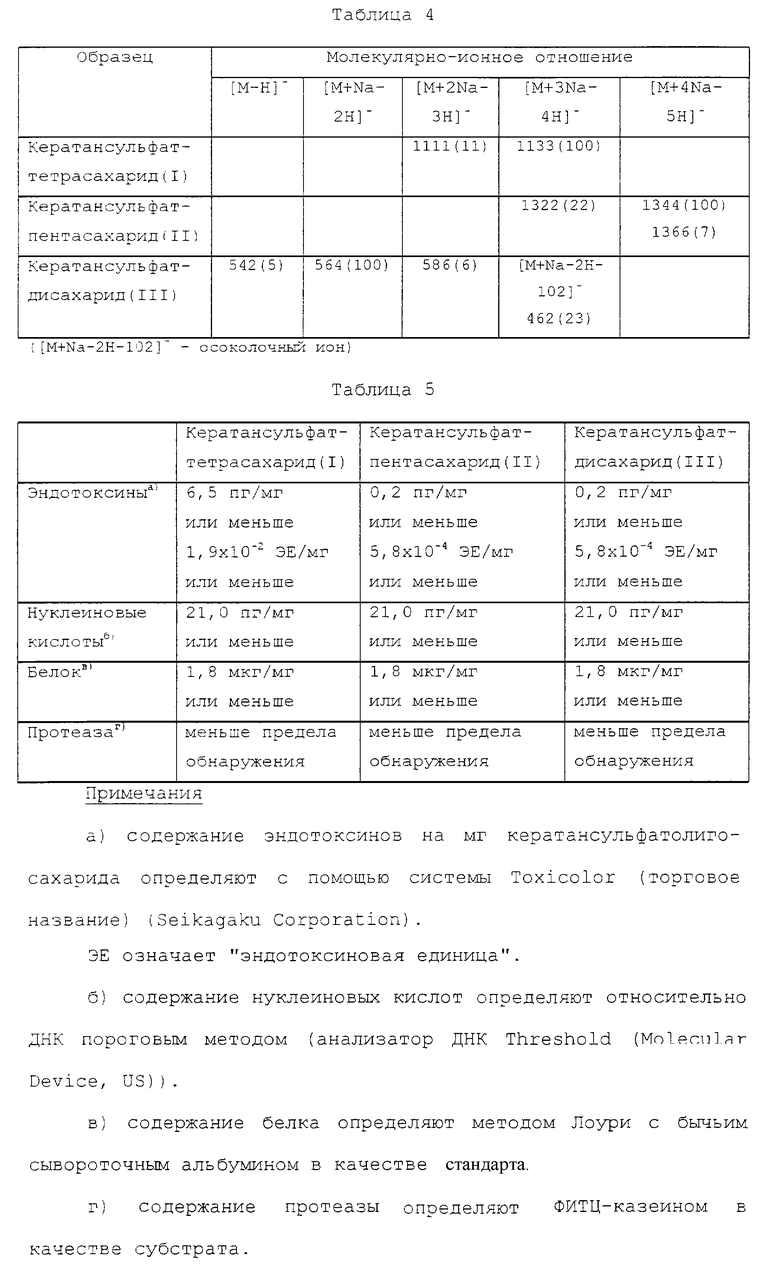
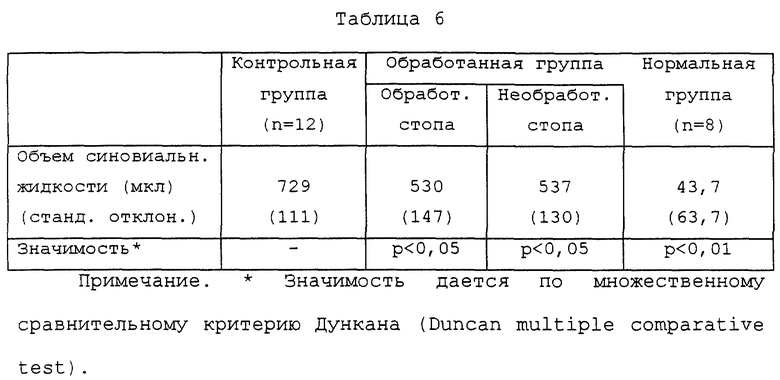
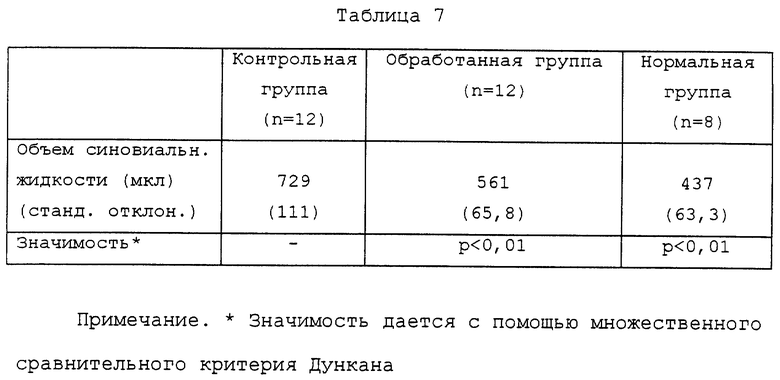
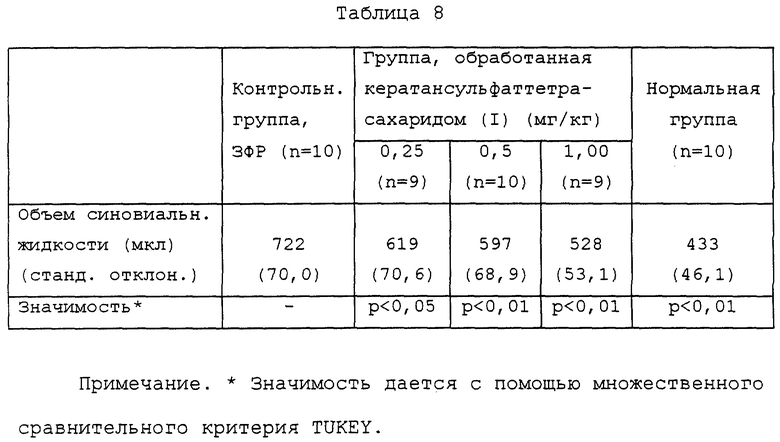
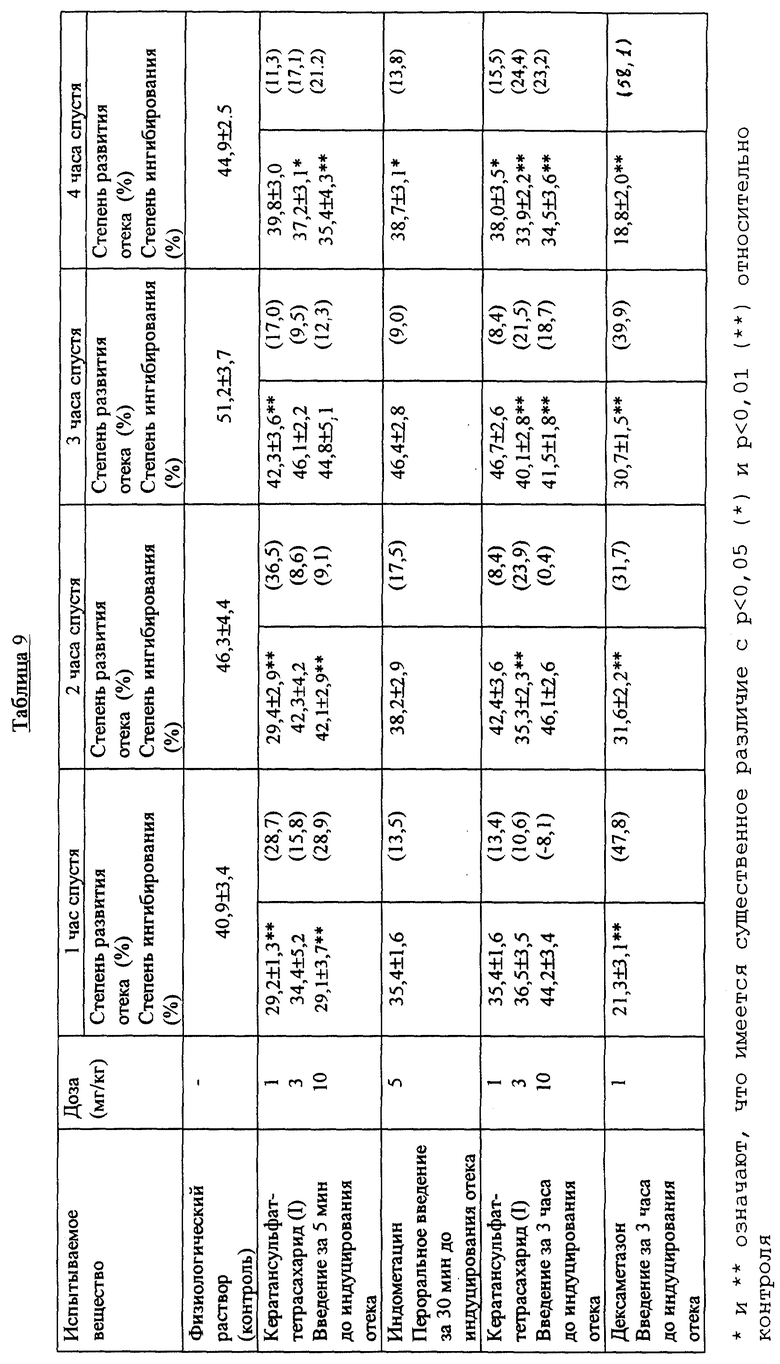
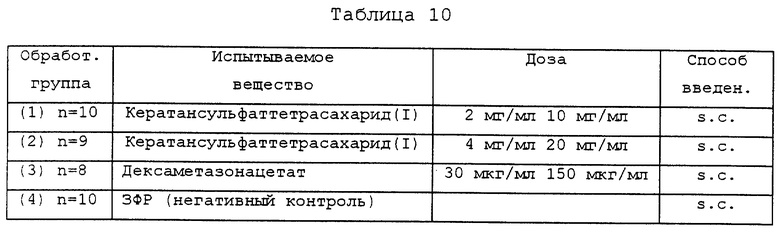

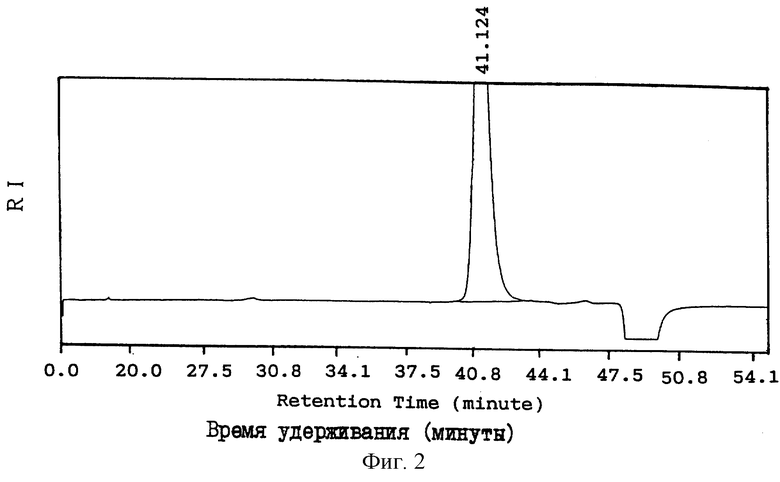
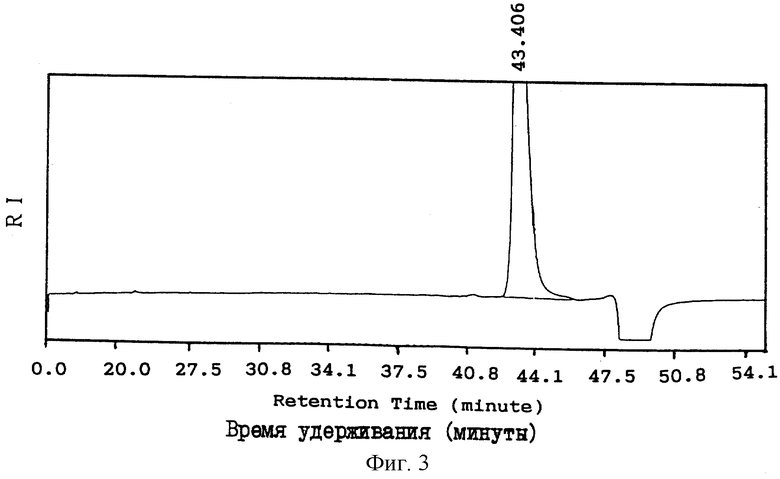
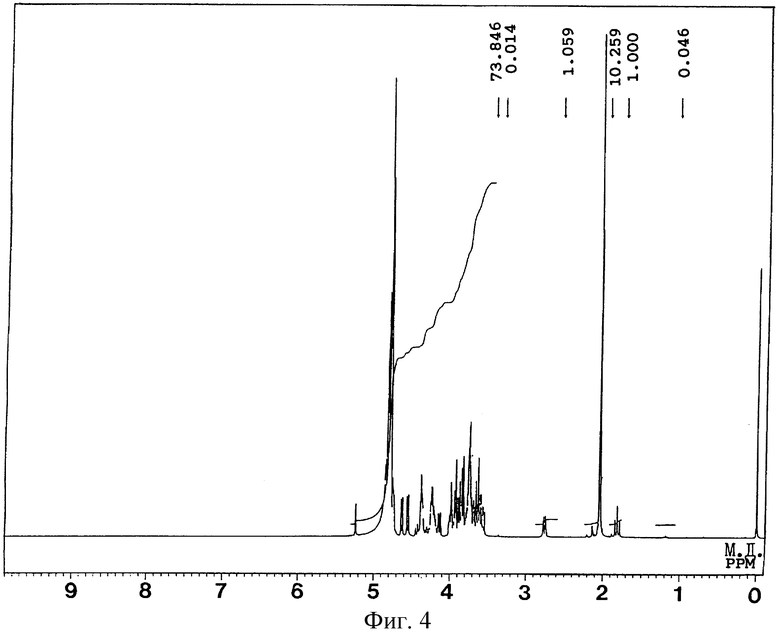
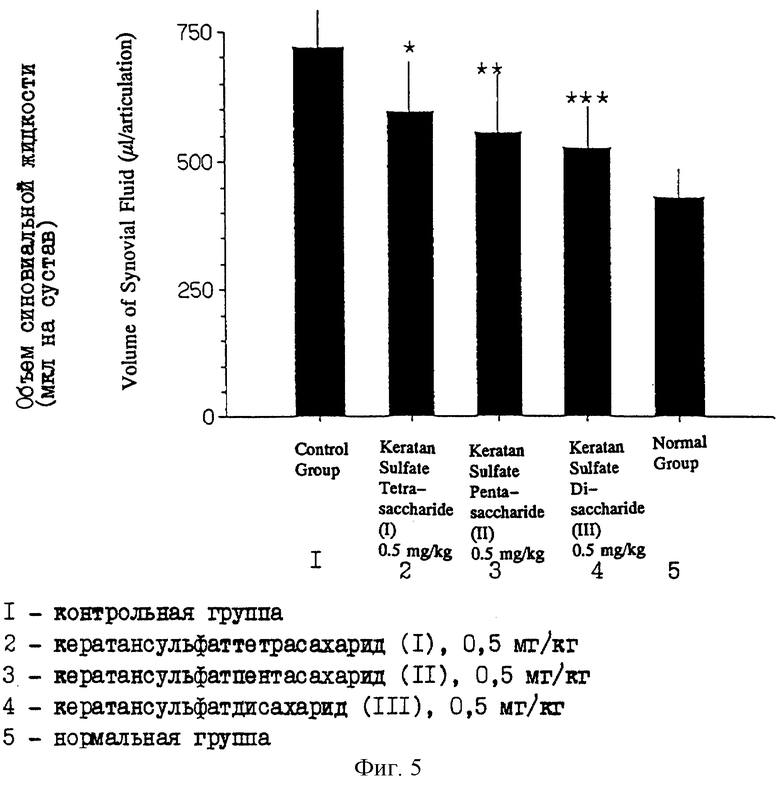
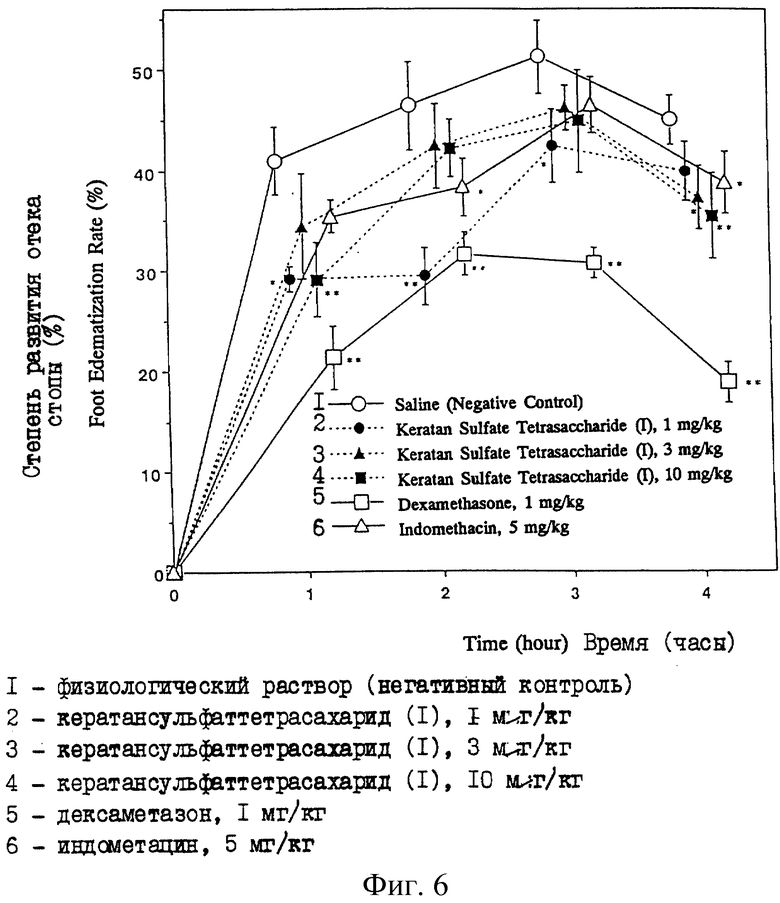
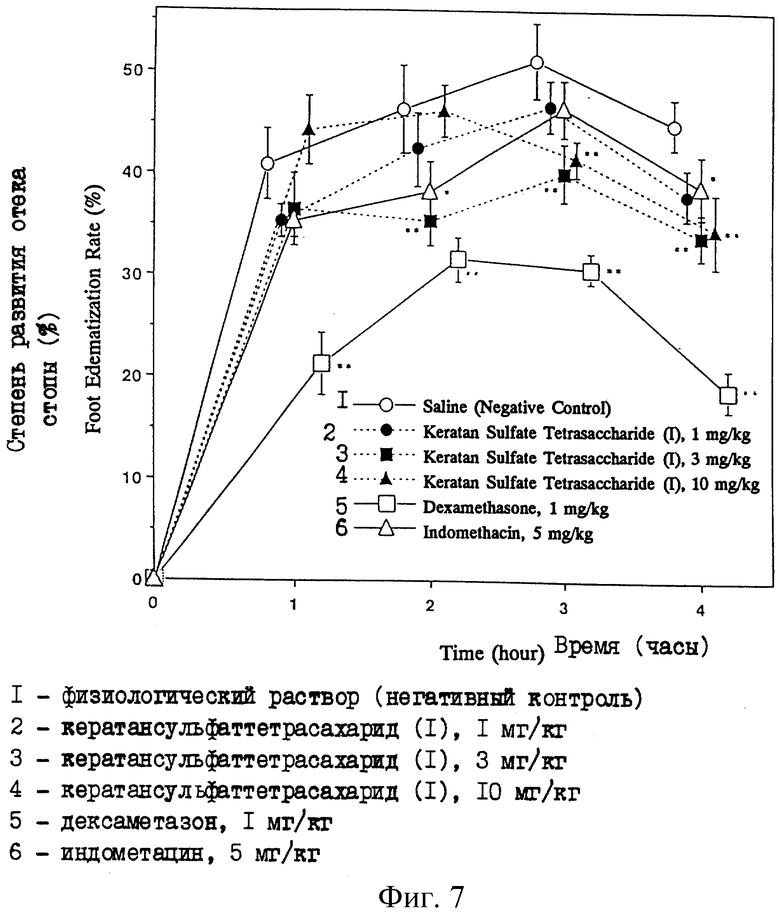
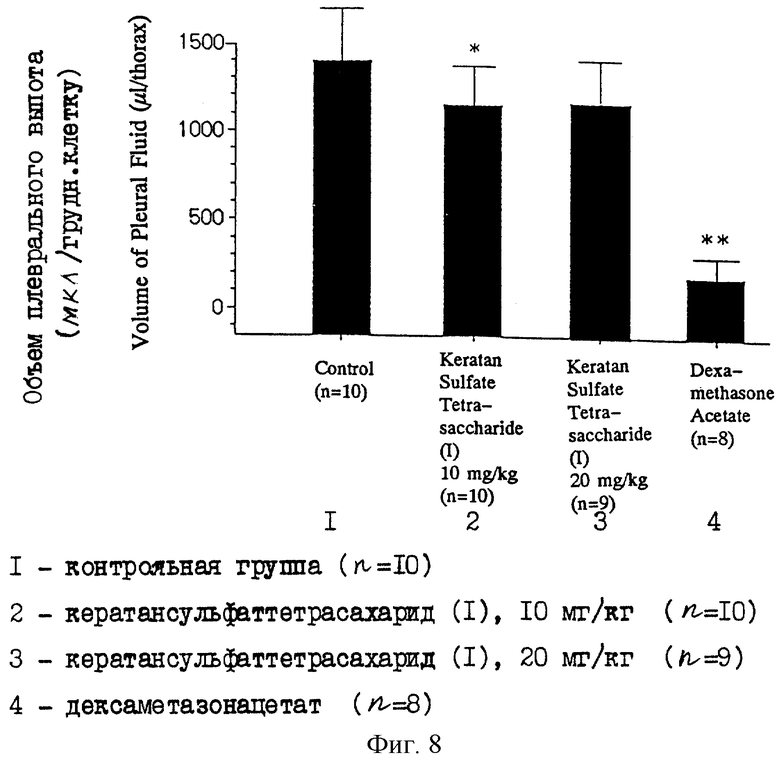
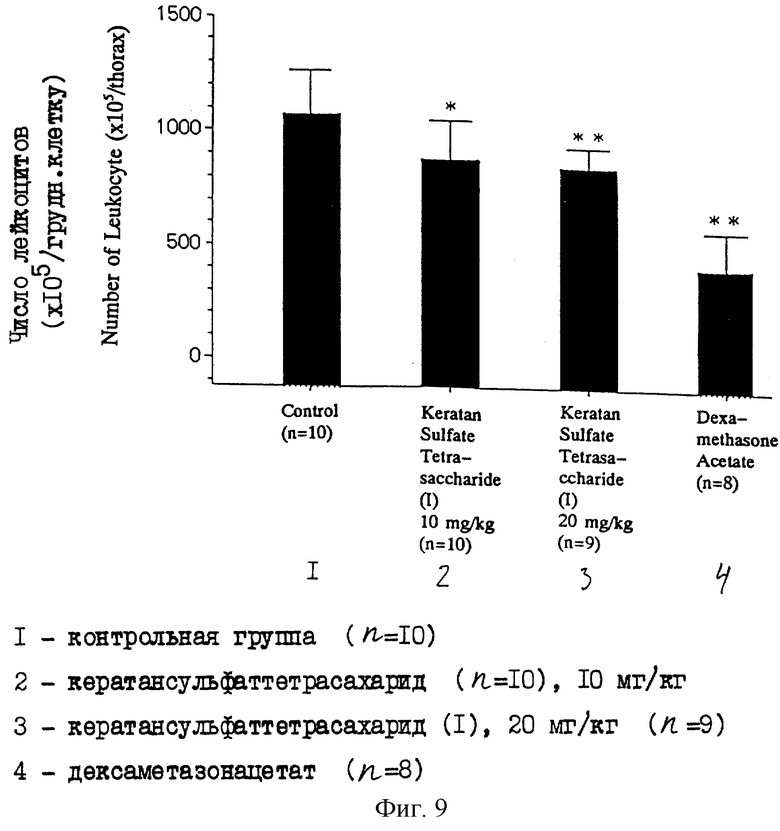
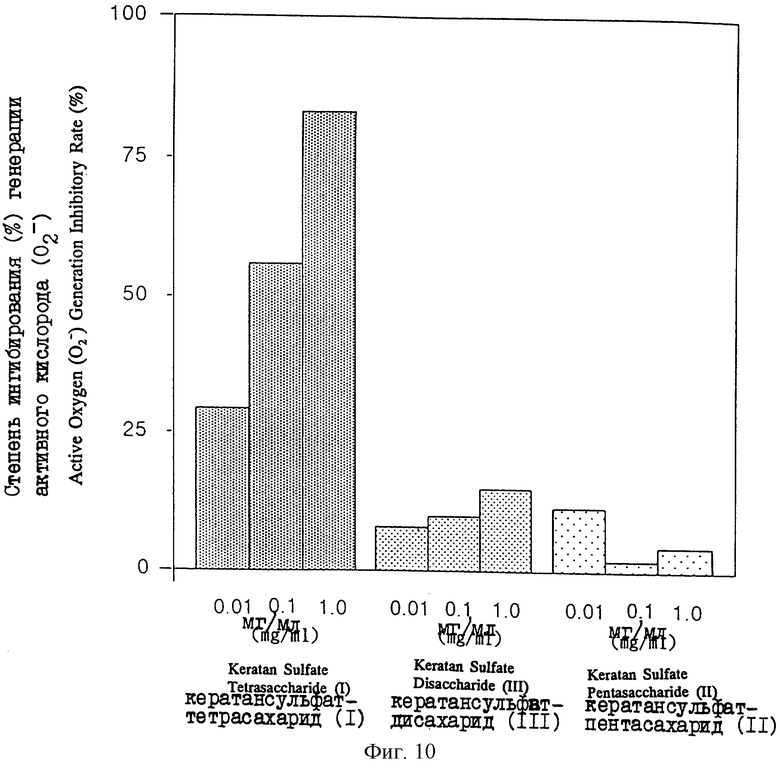
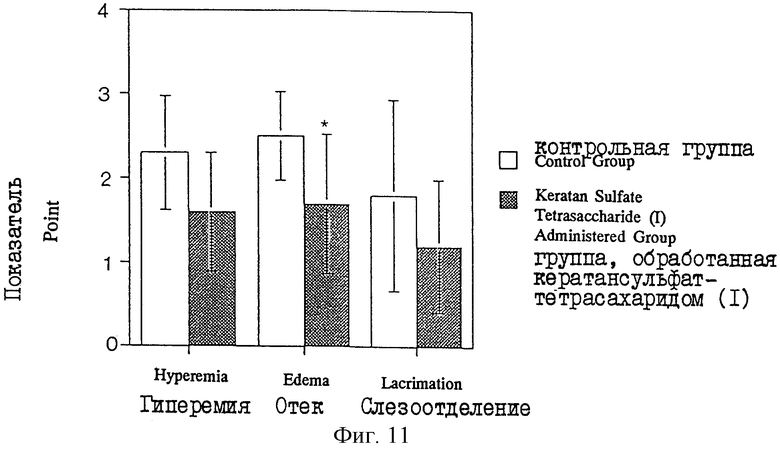
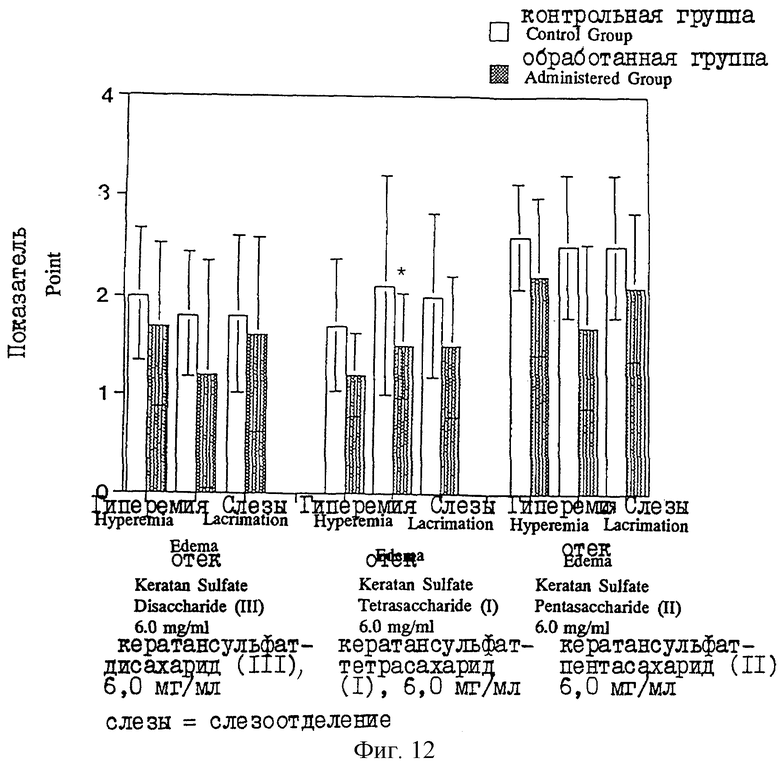
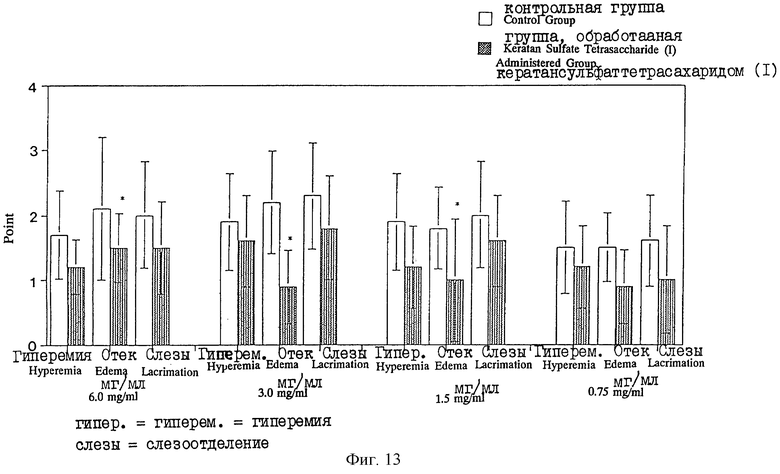
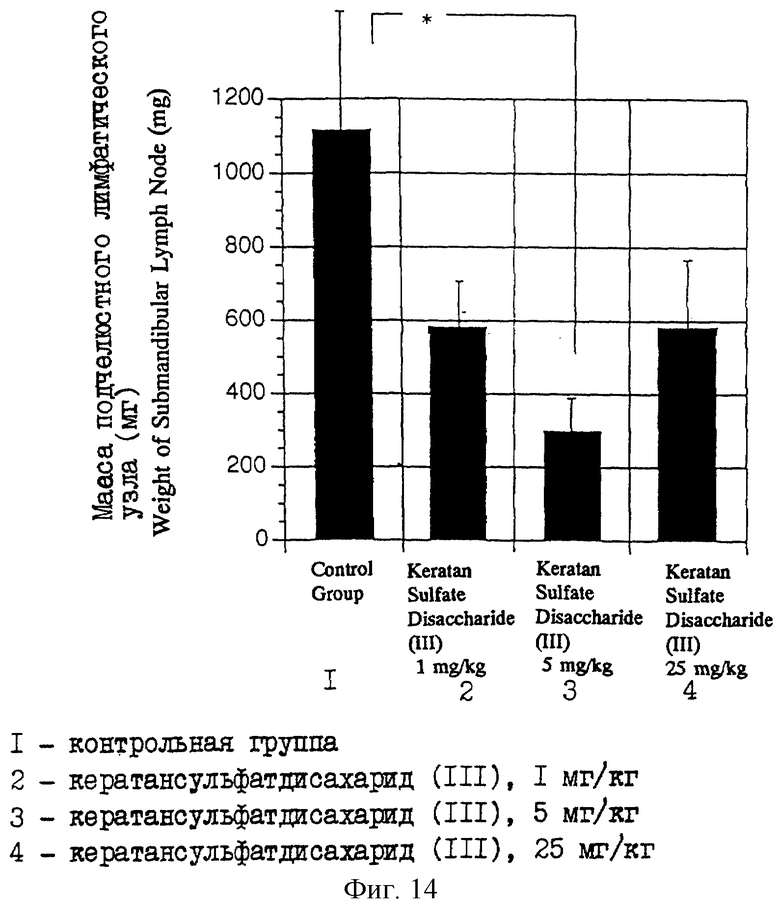
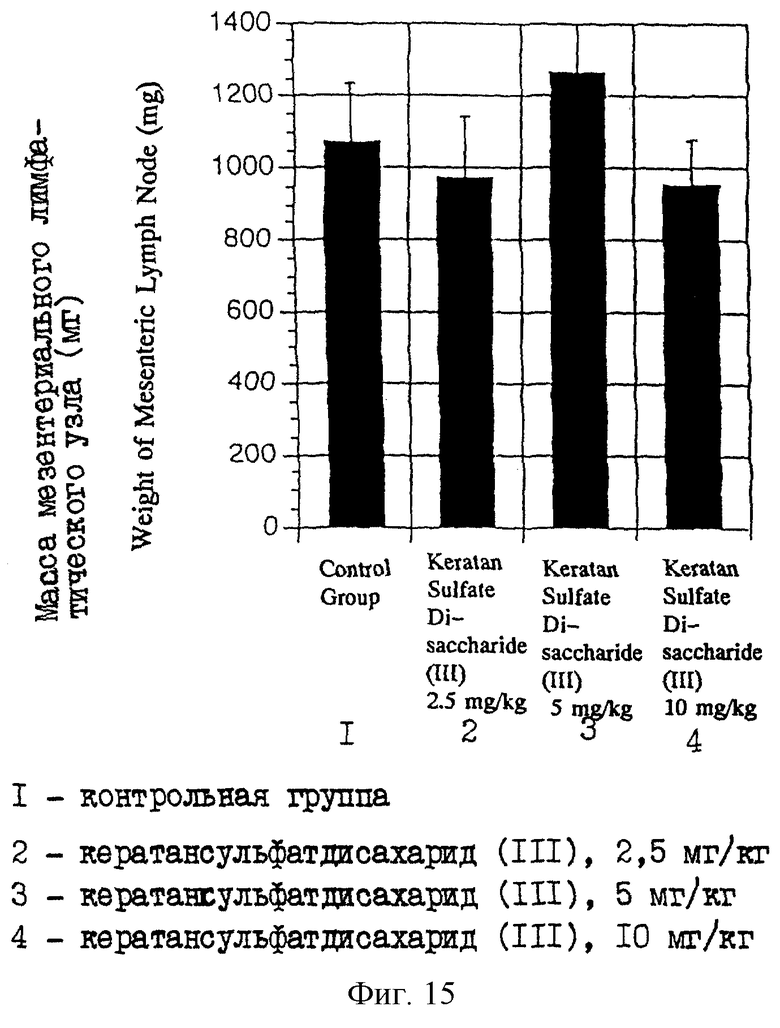
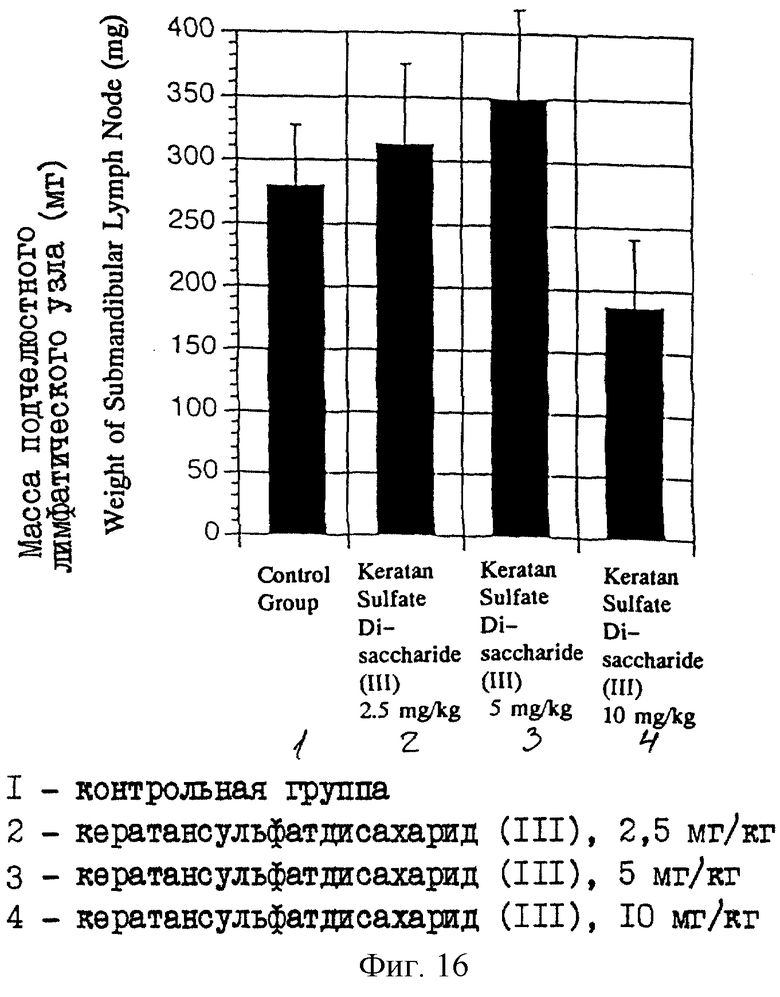
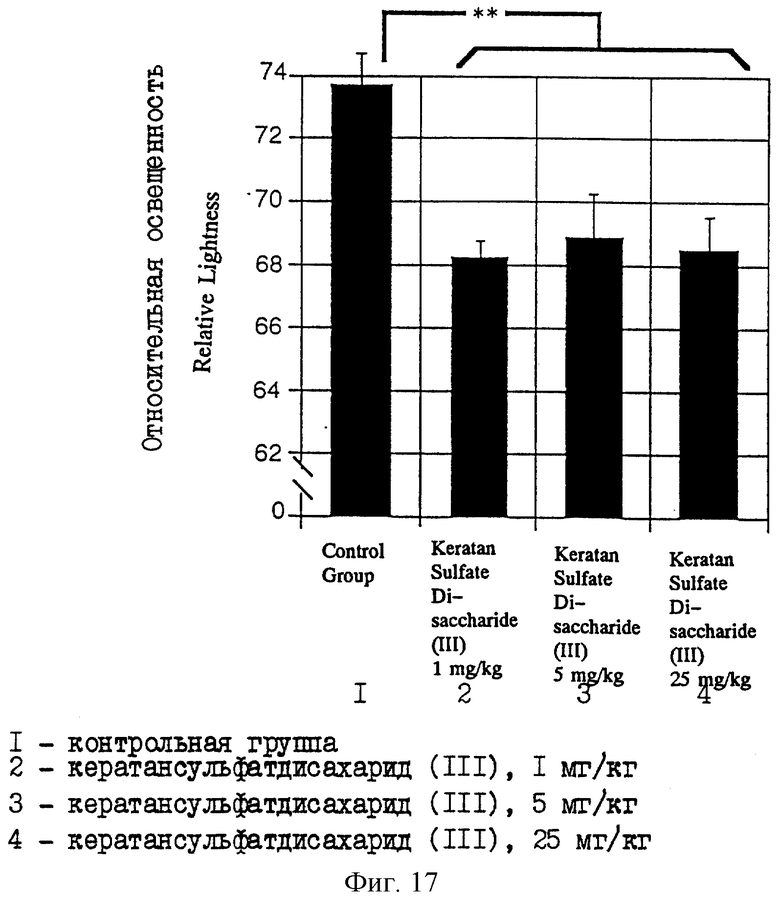
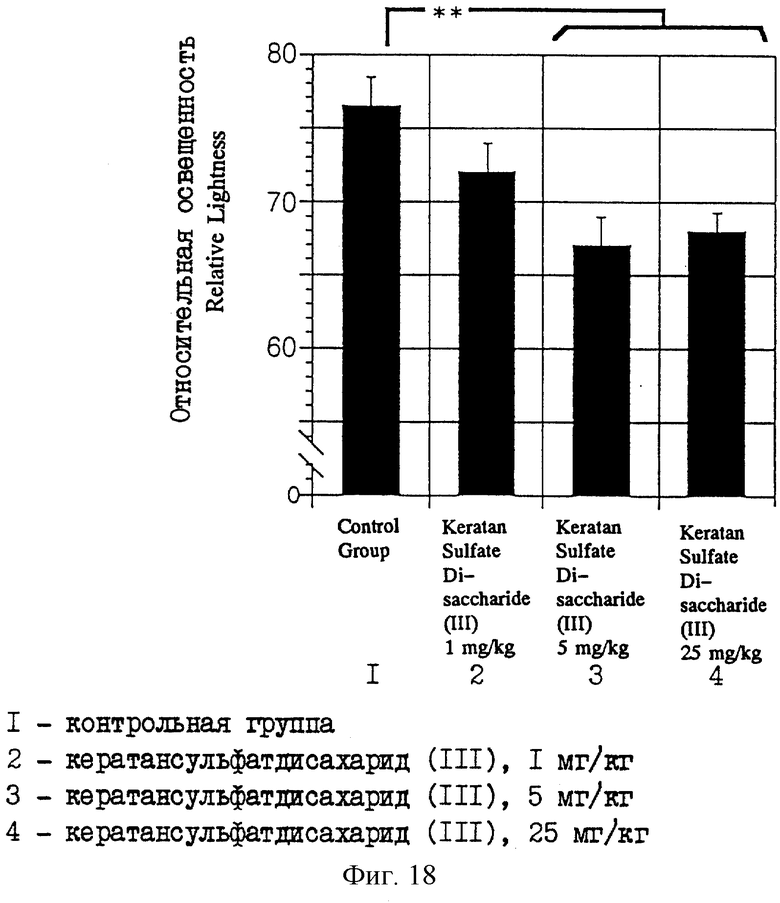
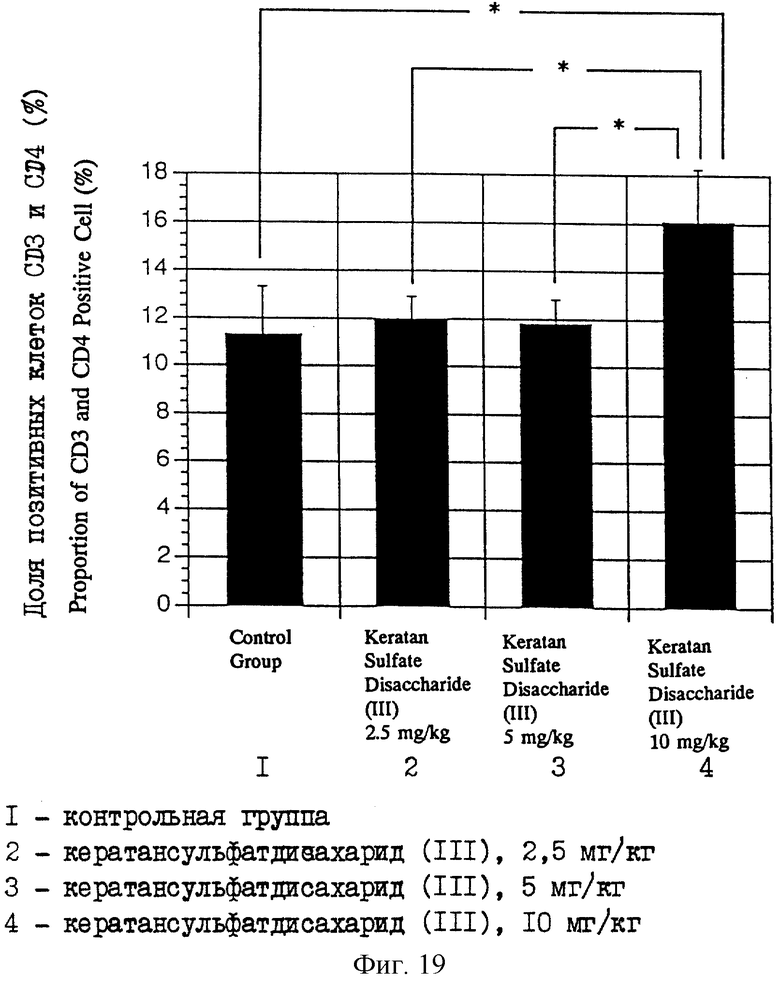
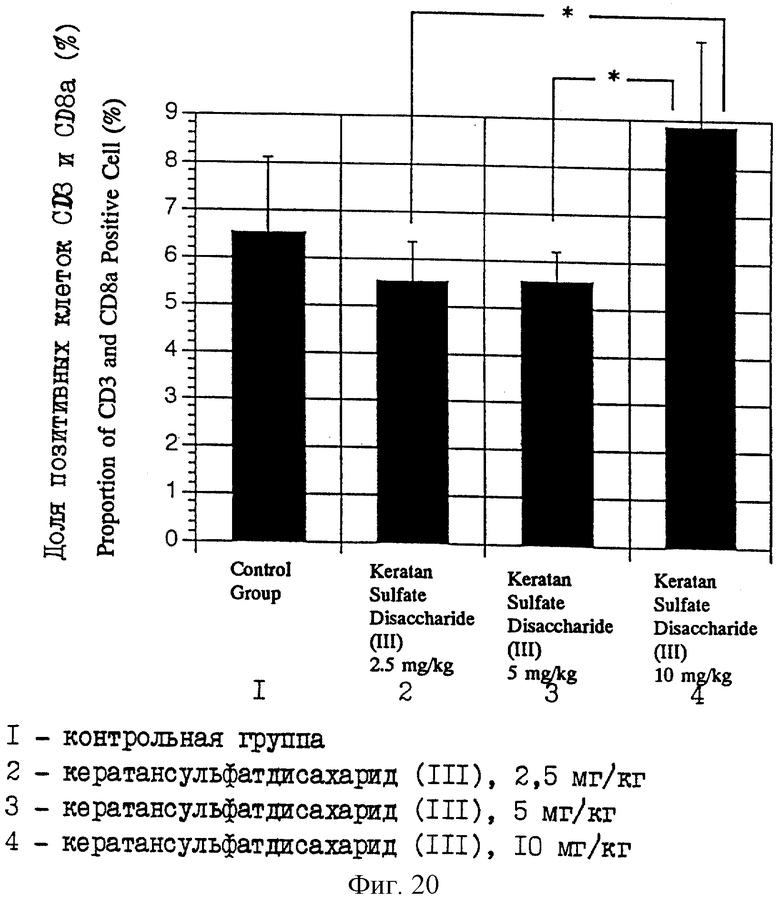
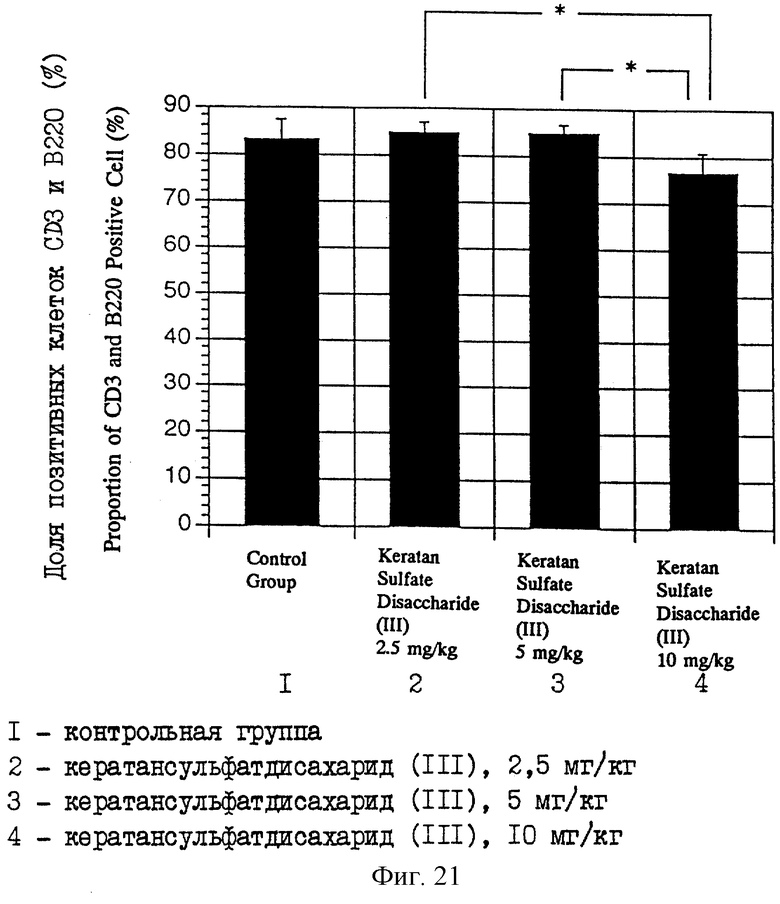
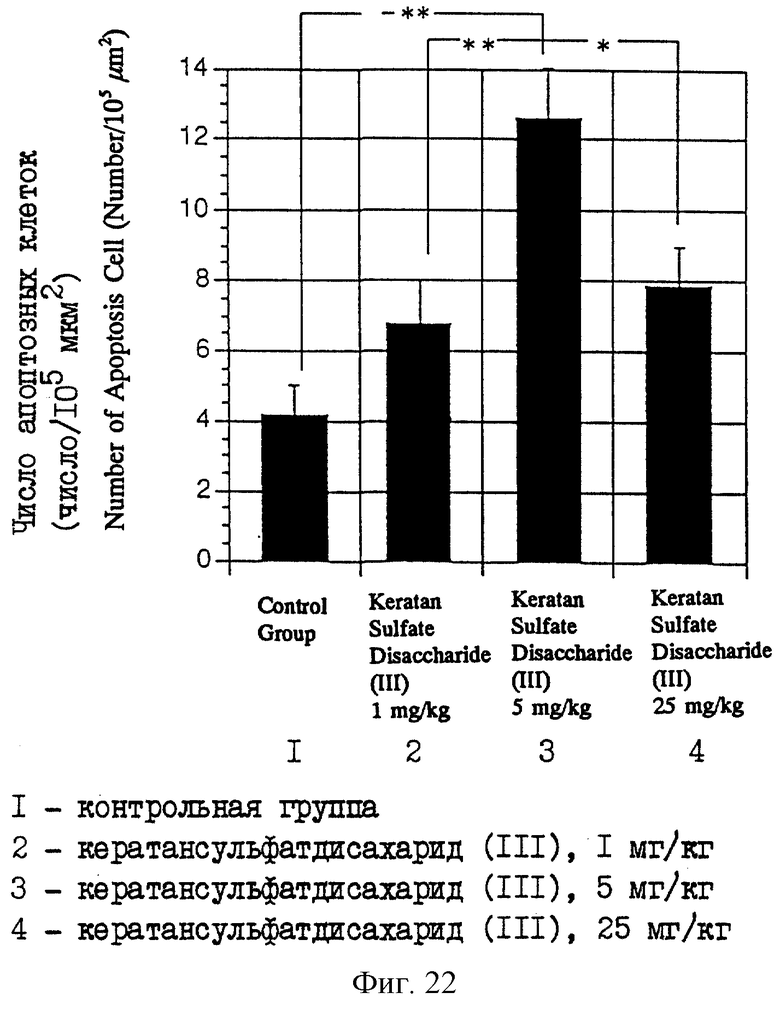
Фармацевтический препарат содержит фармацевтически приемлемый носитель или разбавитель и в качестве активного ингредиента - эффективное количество кератансульфатолигосахарида с двумя-пятью сахаридными звеньями, сульфатированными N-ацетилглюкозамином на своем редуцирующем конце, с сульфатированным N-ацетиллактозаминным звеном, необязательно содержащим сиаловую кислоту и/или фукозу, имеющего, по меньшей мере, две сульфатированных гидроксильных группы в молекуле, и/или его фармацевтически приемлемой соли. Предпочтительно кератансульфатолигосахарид содержит в качестве составного ингредиента, по меньшей мере, дисахарид формулы Gal(6S) - GlcNAc(6S), где Gal представляет галактозу, GlcN представляет глюкозамин, Ас представляет ацетильную группу и 6S представляет 6-О-сульфатный эфир. Фармацевтический препарат обладает противовоспалительным, противоаллергическим, иммуномодулирующим, индуцирующим апоптоз и клеточную дифференцировку действием. Технический результат заключается в реализации указанного назначения. 3 с. и 18 з.п.ф-лы, 11 табл., 22 ил.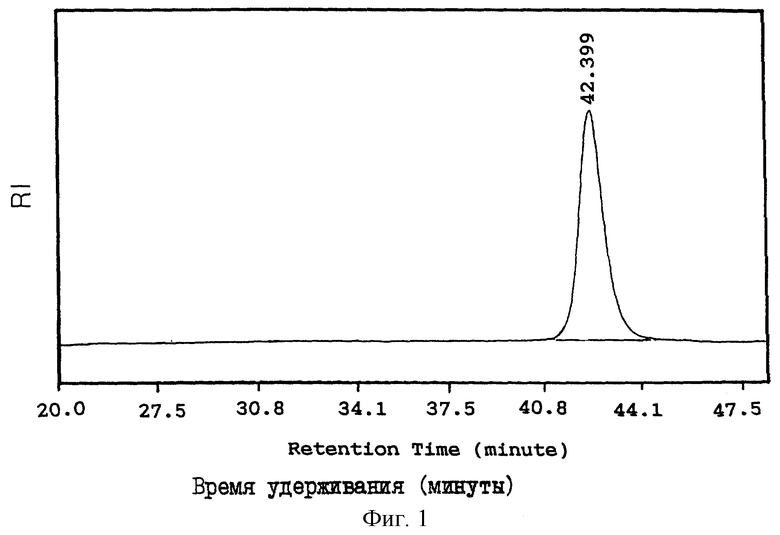
Gal(6S)-GlcNAc(6S),
где Gal представляет галактозу;
GlcN представляет глюкозамин;
Ac представляет ацетильную группу;
6S представляет 6-О-сульфатный эфир.
Gal(6S)β1-4GlcNAc(6S)βl-3Gal(6S)β1-4GlcNAc(6S) (I)
NeuAc~Galβ1-4GlcNAc(6S)βl-3Gal(6S)β1-4GlcNAc(6S) (II)
Gal(6S)β1-4GlcNAc(6S) (III),
где Gal представляет галактозу,
GlcN представляет глюкозамин,
Neu представляет нейраминовую кислоту,
Ас представляет ацетильную группу,
6S представляет 6-О-сульфатный эфир,
~ обозначает связь α2, 3 или связь α2,6.
Gal(6S)-GlcNAc(6S),
где Gal представляет галактозу;
GlcN представляет глюкозамин;
Ас представляет ацетильную группу;
6S представляет 6-О-сульфатный эфир.
Gal(6S)β1-4GlcNAс(6S)β1-3Gal(6S)β1-4GlcNAc(6S) (I)
NeuAc~Galβ1-4GlcNAc(6S)β1-3Gal(6S)β1-4GlcNAc(6S) (II)
Gal(6S)β1-4GlcNAc(6S) (III),
где Gal представляет галактозу,
GlcN представляет глюкозамин,
Neu представляет нейраминовую кислоту,
Ас представляет ацетильную группу,
6S представляет 6-О-сульфатный эфир,
~ обозначает связь α2, 3 или связь α2,6.
Gal(6S)-GlcNAc(6S),
где Gal представляет галактозу;
GlcN представляет глюкозамин;
Ас представляет ацетильную группу;
6S представляет 6-О-сульфатный эфир.
Gal(6S)β1-4GlcNAс(6S)β1-3Gal(6S)β1-4GlcNAc(6S) (I)
NeuAc~Galβ1-4GlcNAc(6S)β1-3Gal(6S)β1-4GlcNAc(6S) (II)
Gal(6S)β1-4GlcNAc(6S) (III),
где Gal представляет галактозу,
GlcN представляет глюкозамин,
Neu представляет нейраминовую кислоту,
Ас представляет ацетильную группу,
6S представляет 6-О-сульфатный эфир,
~ обозначает связь α2, 3 или связь α2,6.
Gal(6S)-GlcNAc(6S),
где Gal представляет галактозу;
GlcN представляет глюкозамин;
Ас представляет ацетильную группу;
6S представляет 6-О-сульфатный эфир.
Gal(6S)β1-4GlcNAс(6S)β1-3Gal(6S)β1-4GlcNAc(6S) (I)
NeuAc~Galβ1-4GlcNAc(6S)β1-3Gal(6S)β1-4GlcNAc(6S) (II)
Gal(6S)β1-4GlcNAc(6S) (III),
где Gal представляет галактозу,
GlcN представляет глюкозамин,
Neu представляет нейраминовую кислоту,
Ас представляет ацетильную группу,
6S представляет 6-О-сульфатный эфир,
~ обозначает связь α2, 3 или связь α2,6.
Gal(6S)-GlcNAc(6S),
где Gal представляет галактозу;
GlcN представляет глюкозамин;
Ас представляет ацетильную группу;
6S представляет 6-О-сульфатный эфир.
Gal(6S)β1-4GlcNAс(6S)β1-3Gal(6S)β1-4GlcNAc(6S) (I)
NeuAc~Galβ1-4GlcNAc(6S)β1-3Gal(6S)β1-4GlcNAc(6S) (II)
Gal(6S)β1-4GlcNAc(6S) (III),
где Gal представляет галактозу,
GlcN представляет глюкозамин,
Neu представляет нейраминовую кислоту,
Ас представляет ацетильную группу,
6S представляет 6-О-сульфатный эфир,
~ обозначает связь α2, 3 или связь α2,6.
где Gal представляет галактозу;
GlcN представляет глюкозамин;
Ас представляет ацетильную группу;
6S представляет 6-О-сульфатный эфир.
Gal(6S)β1-4GlcNAc(6S)β1-3Gal(6S)β1-4GlcNAc(6S) (I)
NeuAc~Galβ1-4GlcNAc(6S)β1-3Gal(6S)β1-4GlcNAc(6S) (II)
Gal(6S)β1-4GlcNAc(6S) (III),
где Gal представляет галактозу,
GlcN представляет глюкозамин,
Neu представляет нейраминовую кислоту,
Ас представляет ацетильную группу,
6S представляет 6-О-сульфатный эфир,
~ обозначает связь α2, 3 или связь α2,6.
Gal(6S)β1-4GlcNAc(6S)β1-3Gal(6S)β1-4GlcNAc(6S) (I)
NeuAc~Galβ1-4GlcNAc(6S)β1-3Gal(6S)β1-4GlcNAc(6S) (II)
Gal(6S)β1-4GlcNAc(6S) (III),
где Gal представляет галактозу,
GlcN представляет глюкозамин,
Neu представляет нейраминовую кислоту,
Ас представляет ацетильную группу,
6S представляет 6-О-сульфатный эфир,
~ обозначает связь α2, 3 или связь α2,6.
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| WO 9428889 A, 22.12.1994 | |||
| МАШКОВСКИЙ М.Д | |||
| Лекарственные средства | |||
| - М.: МЕДИЦИНА, 1986, ч.2, с.157 | |||
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ АРТРОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 1992 |
|
RU2021812C1 |
Авторы
Даты
2001-09-10—Публикация
1995-11-22—Подача