Изобретение относится к электротехнике, в частности - производству электрохимических конденсаторов с комбинированным механизмом накопления заряда и иных аналогичных перезаряжаемых накопителей энергии.
Электрохимические конденсаторы относятся к классу устройств, предназначенных для накопления-выделения электрической энергии. При этом, в отличие от аккумуляторов, в которых электрическая энергия (заряд) накапливается в форме внутренней энергии вещества активной массы электродов, электрохимические конденсаторы накапливают электрическую энергию в форме свободного или связанного заряда на поверхности раздела электрода (электронного проводника) и электролита (ионного проводника).
Среди электрохимических конденсаторов выделяются два основных типа - "двойнослойные" конденсаторы и "псевдоконденсаторы".
В двойнослойных электрохимических конденсаторах электрическая энергия (заряд) накапливается в форме свободного заряда двойного электрического слоя на границе "электрод-электролит".
В псевдоконденсаторах электрическая энергия (заряд) накапливается в форме связанного заряда в тонких адсорбционных моно- и полимолекулярных слоях (пленках) на границе "электрод-электролит". При зарядке псевдоконденсатора происходят электрохимические реакции образования (или преобразования) этих пленок, при разрядке эти же реакции идут в обратном направлении. В качестве материалов для электродов псевдоконденсаторов используются металлы, сплавы, органические и неорганические полупроводники, вступающие в электрохимические реакции с электролитом.
Каждому из указанных типов конденсаторов свойственны свои достоинства и недостатки, обусловленные достоинствами и недостатками используемых в них электродов и электролитов.
Так, электроды двойнослойного конденсатора, реализующие процесс накопления заряда в двойном электрическом слое на поверхности раздела (контакта) электрода и электролита, должны иметь очень высокоразвитую поверхность - порядка 1000 м2/г и выше, чтобы обеспечить приемлемую для практики удельную энергию. Реализация этого требования в настоящее время обеспечивается применением углеродных объемно-пористых материалов (активированного угля, углеродной ткани и т.д.). Однако электроды из углеродных материалов имеют высокое удельное электрическое сопротивление и высокое сопротивление электрических контактов с токоподводами. Кроме того, такие электроды при работе с водным электролитом имеют предел рабочего напряжения менее 1 В, так как при больших напряжениях возможно протекание необратимых электрохимических реакций, приводящих к разрушению тонкой структуры углеродных материалов и резкому уменьшению срока эксплуатации электродов. Переход к органическим и твердым электролитам позволяет повысить рабочее напряжение до 3 В, но ценой резкого уменьшения удельной проводимости электролита, и следовательно - повышения внутреннего сопротивления конденсаторов и соответствующего уменьшения удельной мощности.
Электроды псевдоконденсатора, реализующие процесс накопления заряда в тонких адсорбционных моно- и полимолекулярных слоях (пленках) на границе "электрод-электролит", могут иметь значительно меньшую удельную поверхность, так как протекание электрохимических реакций в указанных слоях обеспечивает накопление значительно больших зарядов на единицу истинной поверхности, чем при зарядке двойного электрического слоя на границе "электрод-электролит" в двойнослойных конденсаторах.
Например, электроды из благородных металлов (рутения, иридия) и их оксидов, предложенные для псевдоконденсаторов в [1], обеспечивают очень высокие значения удельного заряда и удельной энергии, позволяют применять высокопроводные водные кислые и щелочные электролиты. Это резко уменьшает внутреннее сопротивление и повышает удельную мощность псевдоконденсаторов, по сравнению с двойнослойными конденсаторами. Псевдоконденсаторы с такими электродами имеют некоторую узкую сферу применения, расширению которой препятствует очень высокая цена материалов электродов.
В качестве альтернативы использования благородных металлов для изготовления положительных электродов псевдоконденсаторов в [2] было предложено использовать никелевые сплавы, а в [3] - композит Ni/NiO. Такие электроды могут работать в водных щелочных растворах, в кислых растворах они химически и электрохимически не стойки. В качестве дешевого материала для отрицательных электродов псевдоконденсаторов в [4] предложены сплавы сурьмы (Sb) и висмута (Bi), но срок службы таких электродов невелик, так как сурьма и висмут недостаточно химически стойки в щелочных растворах. Поэтому это решение практически не может составить конкуренции и удовлетворительной замены дорогих отрицательных электродов из благородных металлов.
Попытки компромиссного решения задачи по созданию электрохимического конденсатора, характеризующегося, с одной стороны, приемлемыми для практики электрическими характеристиками, а с другой - возможностью использования в нем дешевых материалов для электродов, привели к необходимости разработок конденсаторов нового типа - электрохимических конденсаторов с комбинированным механизмом накопления заряда, сочетающих в себе принципы работы двойнослойных конденсаторов и псевдоконденсаторов.
Примером попытки создания такого конденсатора является конденсатор, описанный в [5] , в котором в качестве отрицательного электрода используется электрод из углеродного материала, а в качестве положительного электрода - окисно-никелевый электрод, аналогичный положительным электродам в щелочных аккумуляторах. По существу, в [5] описана конструкция накопителя энергии, один из электродов которого работает по принципу электрохимического конденсатора, а второй - по принципу аккумулятора, то есть накапливает энергию в форме внутренней энергии активной массы оксидно-никелевого электрода. Однако такое устройство, являясь некоторым гибридом электрохимического конденсатора и аккумулятора, обладает недостатками того и другого: относительно невысокой удельной энергией, свойственной двойнослойным электрохимическим конденсаторам, и невысокой удельной мощностью, свойственной аккумуляторам. Последнее обстоятельство обусловлено замедленностью процесса протекания окислительно-восстановительной реакции в твердой фазе - оксидах никеля, составляющих основную часть активной массы оксидно-никелевого электрода.
Наиболее близким к заявляемому электрохимическому конденсатору является электрохимический конденсатор с комбинированным механизмом накопления заряда, описанный в [6], в котором отрицательный электрод работает по принципу электрода в двойнослойном конденсаторе (т.е. по "двойнослойному принципу"), реализуя накопление энергии в форме электростатической энергии заряда двойного слоя, а положительный электрод работает по принципу электрода в псевдоконденсаторе (т. е. по "принципу псевдоконденсатора"), реализуя накопление энергии в форме внутренней энергии поверхностных соединений. Этот электрохимический конденсатор принят в качестве прототипа.
Электрохимический конденсатор с комбинированным механизмом накопления заряда, выбранный в качестве прототипа, содержит разделенные ионным проводником-электролитом электроды, реализующие отличающиеся механизмы накопления заряда. При этом отрицательный электрод, реализующий накопление заряда в двойном электрическом слое на поверхности контакта электрода и электролита, выполнен из углеродного материала с высокой удельной поверхностью, а положительный электрод, реализующий накопление заряда за счет обратимого протекания электрохимических реакций в моно- и полимолекулярных слоях продуктов взаимодействия материала электрода с электролитом, выполнен из неорганического окислительно-восстановительного материала, выбранного из группы материалов: рутений (Ru), родий (Rh), палладий (Pd), осмий (Os), иридий (Ir), кобальт (Со), никель (Ni), марганец (Mn), железо (Fe), платина (Pt), сплавы перечисленных металлов, оксиды перечисленных металлов и их комбинаций. В качестве электролита используются водные растворы КОН, NaOH, LiOH, NaClO4, H2SO4, HClO4 и их комбинации, а также различные органические электролиты.
В представленных в [6] примерах реализации рассмотрено электрохимическое поведение положительных электродов из кобальтовой фольги высокой чистоты и отрицательных электродов из углеродного материала, приведены циклические вольтамперограммы и оценена удельная емкость отрицательного электрода из углеродного материала - около 2,7 Ф/г, рассмотрена характеристика положительного кобальтового электрода, которая характеризуется двумя пиками тока окисления и восстановления, разделенными по шкале потенциалов промежутком в 400 мВ, из чего делается вывод, что данный положительный электрод имеет псевдоемкость, при этом количественной характеристики положительного электрода не приводится.
Оценивая предложенный в [6] список материалов для положительного электрода видно, что он представляет собой скорее список принципиально возможных материалов, чем реальных материалов, обеспечивающих реальные преимущества электрохимических конденсаторов с комбинированным механизмом накопления заряда перед известными двойнослойными конденсаторами и псевдоконденсаторами.
Объясняется это следующим. Очевидно, что для успешной конкуренции с двойнослойными конденсаторами и псевдоконденсаторами конденсаторы с комбинированным механизмом накопления заряда должны обладать удельной энергией и удельной мощностью не меньшей, чем у двойнослойных конденсаторов, а стоимость материалов при этом не должна превышать стоимость углеродных материалов. Исходя из этого, из списка материалов, представленного в [6], должны быть исключены дорогостоящие Ru, Rh, Pd, Os, Ir, Pt, их сплавы и оксиды. Из оставшихся в списке металлов марганец (Mn) и его оксиды электрохимически неустойчивы как в кислых, так и в щелочных водных растворах при высоких положительных потенциалах, при которых работает положительный электрод, поскольку переходят в раствор в форме манганатов и перманганатов. Железо (Fe), его сплавы и оксиды относительно устойчивы в щелочных растворах, но потенциалы окислительно-восстановительных реакций на железных и окисно- железных электродах лежат в области отрицательных потенциалов от минус 1,0 В до минус 0,3 В против нормального водородного электрода, поэтому в качестве материала положительного электрода выступать не могут.
Таким образом, из всего списка материалов, предложенных в [6] для положительного электрода, реально остаются только никель (Ni), кобальт (Co), их сплавы, оксиды и комбинации этих материалов.
Однако, чтобы выполнить требования по обеспечению приемлемой для практики удельной энергии в электрохимических конденсаторах с комбинированным механизмом накопления заряда и тем самым обеспечить техническую и экономическую целесообразность их применения, удельный заряд положительного электрода должен быть не меньше удельного заряда отрицательного электрода из углеродных материалов. Учитывая, что современные углеродные материалы имеют удельную поверхность до 2000 м2/г, что эквивалентно удельной емкости 400 Ф/г и удельному заряду 200 Кл/г, необходимо, чтобы удельный заряд материала положительного электрода был не ниже указанной величины. Это требование накладывает очень жесткие ограничения на выбор материала положительного электрода. Даже при использовании очень тонкого отрицательного электрода, например толщиной 0,1 мм, заряд на единицу видимой его поверхности составит 1 Кл/см2. Положительный электрод должен иметь не меньшее значение. Приведенный в [6, Fig. 5] в качестве примера положительного электрода кобальтовый электрод имеет заряд около 0,003 - 0,004 Кл/см2, что не отвечает указанным требованиям. Не удовлетворяют указанным требования и описанные в [7] электроды из никель-молибденовых и никель-молибден-хромовых сплавов, имеющие более высокий удельный заряд, достигающий 0,2 - 0,25 Кл/см2.
Таким образом, в конденсаторе-прототипе не решается задача по обеспечению приемлемых, с точки зрения целесообразности практического использования, характеристик как отдельного положительного электрода, так и конденсатора в целом.
Задачей, на решение которой направлено заявляемое изобретение, является создание электрохимического конденсатора с комбинированным механизмом накопления заряда, реализующего приемлемые для практики удельные характеристики, обеспечивающие техническую и экономическую целесообразность его использования.
Сущность изобретения состоит в том, что в электрохимическом конденсаторе с комбинированным механизмом накопления заряда, содержащем по крайней мере два разделенных ионным проводником-электролитом электрода, из которых первый - отрицательный электрод, реализующий накопление заряда в двойном электрическом слое на поверхности контакта электрода и электролита, выполнен из углеродного материала с высокой удельной поверхностью, а второй - положительный электрод, реализующий накопление заряда за счет обратимого протекания электрохимических реакций в моно- и полимолекулярных слоях продуктов взаимодействия материала электрода с электролитом, выполнен из материала, в состав которого входит металл из группы: никель (Ni), кобальт (Со), при этом положительный электрод выполнен в виде подложки из электронопроводящего, иононепроводящего, химически и электрохимически неактивного в электролите материала с расположенным на одной или обеих сторонах подложки поверхностным электрохимически активным слоем, полученным путем химической и/или электрохимической обработки в растворах кислот, солей или щелочей нанесенного на подложку покрытия из материала, состав которого удовлетворяет формуле
M1(1-Х)M2(Х),
где 0,4 ≤ X ≤ 0,97,
M1 - металл-разрыхлитель из группы: алюминий (Al), цинк (Zn), олово (Sn), щелочные и щелочноземельные металлы и их комбинации,
М2 - металл из группы: никель (Ni), кобальт (Со), серебро (Ag) или их сплав, или сплав по крайней мере одного из этих металлов с одним или несколькими металлами-модификаторами из группы: лантан (La) или лантаноиды, молибден (Mo), вольфрам (W), марганец (Mn), ванадий (V), титан (Ti), висмут (Bi), сурьма (SB), железо (Fe).
В заявляемом электрохимическом конденсаторе толщина подложки положительного электрода находится в пределах от 5 до 150 мкм, предпочтительно от 10 до 50 мкм, а толщина электрохимически активного слоя - в пределах от 5 до 100 мкм.
В заявляемом электрохимическом конденсаторе поверхностный электрохимически активный слой положительного электрода получен путем химической и/или электрохимической обработки покрытия подложки в водных растворах серной или фосфорной кислоты концентрации от 1 до 30 мас.%, или путем химической и/или электрохимической обработки покрытия подложки в водных растворах калиевых, натриевых или аммониевых солей органических и неорганических кислот, или путем химической и/или электрохимической обработки покрытия подложки в водных или смешанных водно-органических растворах щелочей концентрации от 1 до 70 мас.%.
Сущность заявляемого электрохимического конденсатора, возможность его осуществления и использования иллюстрируются фиг. 1 - 7 и пояснительными примерами.
На фиг. 1 представлено схематическое изображение двухэлектродного электрохимического конденсатора с комбинированным механизмом накопления энергии, модель которого использовалась при натурных исследованиях.
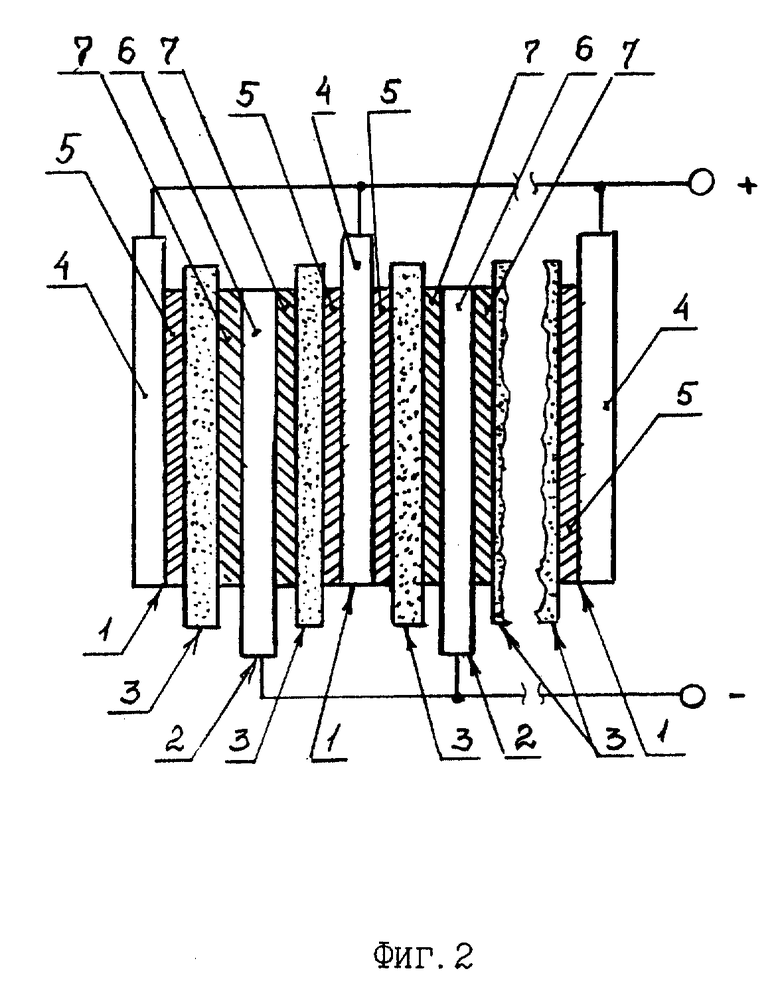
На фиг. 2 представлено схематическое изображение многоэлектродного конденсатора с параллельным соединением пар электродов.
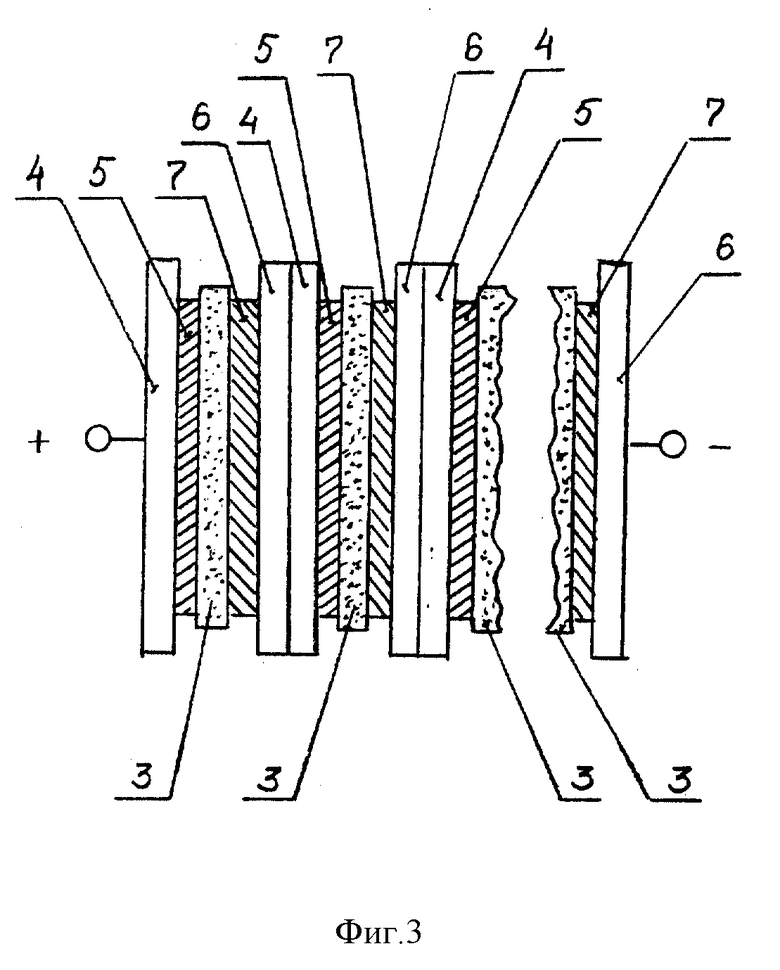
На фиг. 3 представлено схематическое изображение многоэлектродного конденсатора с последовательным соединением пар электродов.
На фиг. 4 представлены вольтамперограммы, соответствующие характеристикам положительного электрода по первому пояснительному примеру.
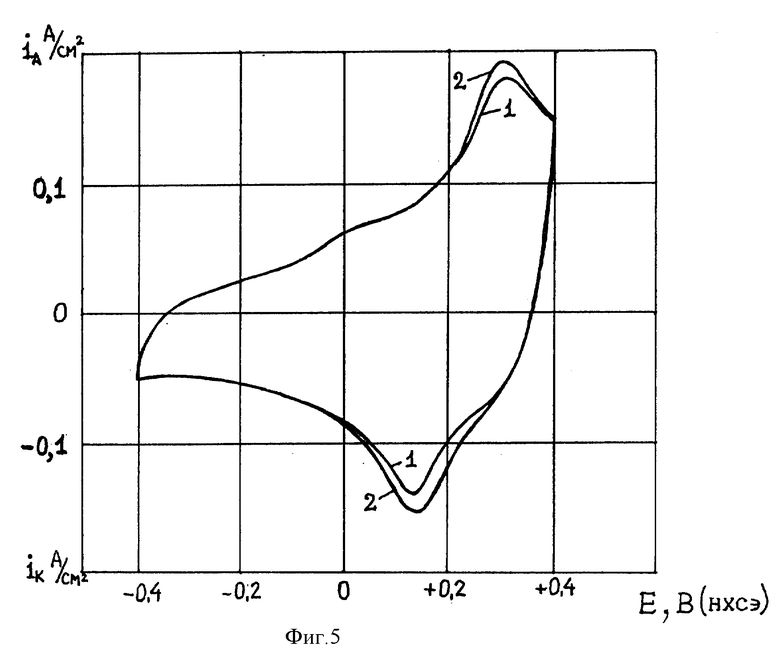
На фиг. 5 представлены вольтамперограммы, соответствующие характеристикам положительного электрода по второму пояснительному примеру.
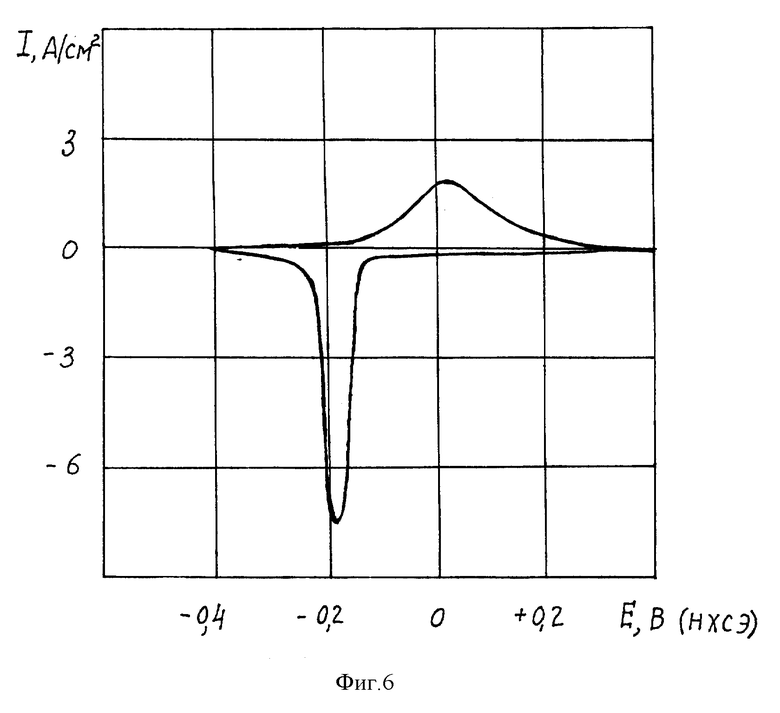
На фиг. 6 представлены вольтамперограммы, соответствующие характеристикам положительного электрода по четвертому пояснительному примеру.
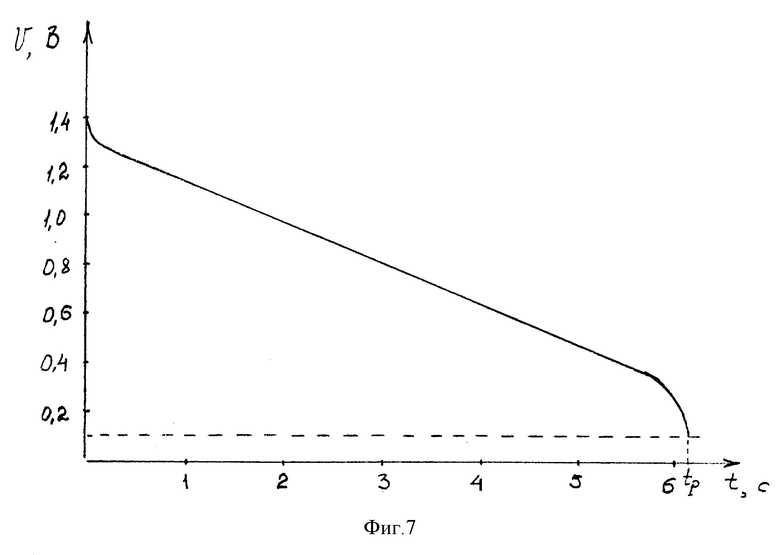
На фиг. 7 представлена разрядная характеристика модели двухэлектродного конденсатора по пятому пояснительному примеру.
Заявляемый электрохимический конденсатор содержит (фиг. 1 - 3) положительные 1 и отрицательные 2 электроды, разделенные сепараторным слоем 3, заключающем в себе электролит, являющийся ионным проводником. В качестве сепараторного слоя может использоваться, например, слой пористого полимера, в качестве электролита - водный раствор щелочи или соли.
Положительный электрод 1 в заявляемом конденсаторе выполнен в виде подложки 4 из электронопроводящего, но иононепроводящего материала с расположенным на одной (фиг. 1, 3) или обеих (фиг. 2) сторонах подложки 4 поверхностным электрохимически активным слоем 5.
Отрицательный электрод 2 в заявляемом конденсаторе выполнен в виде слоя 7 углеродного материала с высокоразвитой поверхностью, механически и электрически контактирующего с токоподводом 6 - электронным проводником, не имеющим ионной проводимости.
Подложка 4 положительного электрода 1 и токоподвод 6 отрицательного электрода 2 в заявляемом конденсаторе выполнены из химически и электрохимически неактивного в рабочем электролите материала, например из чистого никеля или коррозионно-стойких железо-никелевых сплавов, что обеспечивает надежный токоподвод в течение срока службы устройства. При последовательном соединении пар электродов (фиг.3) подложка 4 положительного электрода 1 и токоподвод 6 отрицательного электрода 2 механически и электрически контактируют друг с другом. При конструктивной необходимости функции подложки 4 положительного электрода 1 и токоподвода 6 отрицательного электрода 2 может выполнять один и тот же элемент конструкции.
Поверхностный электрохимически активный слой 5 положительного электрода 1 в заявляемом электрохимическом конденсаторе получен путем химической и/или электрохимической обработки в растворах кислот, солей или щелочей нанесенного на подложку 3 покрытия, выполненного из сплавов металлов-разрыхлителей с химически стойкими основными металлами и, при необходимости, с металлами-модификаторами.
В зависимости от природы используемого химически стойкого металла содержание металлов-разрыхлителей в составе покрытия может колебаться от 3 до 60% ат. При меньшем содержании эффект возрастания плотности тока, заряда и емкости недостаточен, при большем - материал положительного электрода 1 теряет свою механическую прочность после химической или электрохимической обработки и при эксплуатации.
Добавки металлов-модификаторов, изменяя структуру и состав поверхностного слоя 5 положительного электрода 1, могут привести к улучшению эксплуатационных характеристик как самого положительного электрода, так и конденсатора в целом: увеличению рабочего напряжения, ускорению окислительно-восстановительных реакций, протекающих при зарядке и разрядке, повышению механических свойств покрытия. Однако содержание металлов-модификаторов не должно превышать некоторого предела, выше которого падает химически стойкость сплава. Этот предел устанавливается в каждом конкретном случае экспериментально.
Повышает характеристики положительного электрода 1 и осуществляемая предварительно химическая и/или электрохимическая обработка в растворах кислот, солей или щелочей нанесенного на подложку 4 покрытия. При этом требуемые структура и состав электрохимически активного слоя 5, получаемые в результате химической и/или электрохимической обработки покрытия, обеспечиваются если исходный состав материала покрытия удовлетворяет формуле M1(1-Х)M2(Х), где 0,4 ≤ X ≤ 0,97, M1 - металл-разрыхлитель из группы: Al, Zn, Sn, щелочные и щелочноземельные металлы или комбинации этих металлов, M2 - металл из группы: Ni, Со, Ag или их сплав, или сплав хотя бы одного из этих металлов с одним или несколькими металлами-модификаторами, при этом в качестве металлов-модификаторов выбираются металлы из группы: La или лантаноиды, Mo, W, Mn, V, Ti, Bi, Sb, Fe.
Указанное покрытие наносят на одну или обе стороны подложки 4, например, путем электрохимического осаждения, плазменного напыления, термовакуумной конденсации или иным известным способом, применяемым в данной области техники. После этого подложку вместе с нанесенным покрытием подвергают указанной химической и/или электрохимической обработке в растворах кислот, солей или щелочей.
Толщина подложки 4 в конкретных вариантах реализации заявляемого электрохимического конденсатора может выбираться в пределах от 5 до 150 мкм, предпочтительно от 10 до 50 мкм, а толщина электрохимически активного слоя 5 - в пределах от 5 до 100 мкм.
Указанная химическая и/или электрохимическая обработка нанесенного на подложку 4 покрытия в конкретных вариантах реализации заявляемого электрохимического конденсатора может проводиться в водных растворах серной или фосфорной кислоты концентрации от 1 до 30 мас.%, в водных растворах калиевых, натриевых или аммониевых солей органических и неорганических кислот, например сульфатах, хлоридах, фторидах, фосфатах, дифосфатах, ацетатах, тартратах, формиатах щелочных металлов или аммония, а также в водных или водно-органических растворах щелочей концентрации от 1 до 70 мас.%.
Выполненные указанным образом положительные электроды 1 и отрицательные электроды 2, разделенные сепараторными слоями 3, несущими электролит, размещаются в корпусе электрохимического конденсатора (на фиг. 1 - 3 не показан) и, в случае необходимости, например при реализации параллельного соединения пар электродов (фиг. 2), соответствующим образом соединяются между собой внутренними электрическими проводниками, а также внешними токоподводами. При необходимости, в зависимости от условий эксплуатации, корпус конденсатора может быть загерметизирован.
Собранный таким образом электрохимический конденсатор готов к немедленной эксплуатации. При этом, в отличие от прототипа, электрохимический конденсатор реализует улучшенные удельных характеристики (плотность тока, удельную мощность, удельный заряд, плотность энергии) по сравнению с обычными электрохимическими конденсаторами с угольными электродами, работающими по двойнослойному механизму накопления заряда, при близкой стоимости материалов. Тем самым решается поставленная задача по созданию электрохимического конденсатора с комбинированным механизмом накопления заряда, реализующего приемлемые для практики удельные характеристики, обеспечивающие техническую и экономическую целесообразность его использования.
Возможность достижения указанного результата в заявляемом электрохимическом конденсаторе можно пояснить исходя из следующих теоретических соображений.
Первое требование, предъявляемое к конструкции устройств, использующих принцип работы псевдоконденсаторов, - реализация высокой химической и электрохимической стойкости электродов, в данном случае - положительных электродов, работающих по принципу псевдоемкости. Как уже отмечалось, в водных растворах кислот лишь благородные металлы стойки при высоких значениях электродных потенциалов, при которых работают положительные электроды, но эти металлы слишком дорогие. В щелочных растворах лишь пять металлов стойки в этих условиях: никель (Ni), кобальт (Со), серебро (Ag), кадмий (Cd), железо (Fe). Но последние два металла - Cd, Fe не имеют окислительно-восстановительных реакций в области высоких значений электродных потенциалов, поэтому не могут служить основой материала положительного электрода. Следовательно, лишь три металла: никель (Ni), кобальт (Со), серебро (Ag), - могут служить основой положительного электрода, работающего по механизму псевдоемкости.
Легирование этих металлов до определенного предела другими металлами не изменяет высокой химической стойкости сплавов и может использоваться для достижения определенных полезных свойств материала электрода. Наибольший интерес представляет свойство некоторых легирующих элементов вызывать увеличение плотности тока зарядки и разрядки, следовательно - удельного заряда и удельной энергии, отмеченное в [2], [4], [8]. Легированием достигаются и другие полезные результаты: повышение перенапряжения реакции окисления ОН- - ионов до кислорода и связанное с ним повышение рабочего напряжения и коэффициента использования энергии, обеспечение требуемых механических свойств и т.д.
Второе важное требование, предъявляемое к конструкции устройств, реализующих принцип работы псевдоконденсаторов, - протекание окислительно-восстановительных реакций в тонких поверхностных пленках на поверхности материалов электродов, в данном случае - положительных электродов, работающих по принципу псевдоконденсаторов, причем равновесный потенциал этих реакций должен быть как можно выше, но ниже верхней границы термодинамической устойчивости электролита. Например, для водных щелочных растворов верхняя граница термодинамической устойчивости электролита около 0,4 В против нормального водородного электрода. У всех трех металлов такие окислительно-восстановительные реакции, см. [9], есть: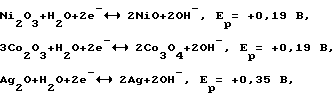
и равновесные потенциалы этих реакций в щелочных растворах (pH = 14) лежат именно в требуемой области потенциалов.
Принцип легирования металлов основной группы, реализованный в настоящем изобретении, можно пояснить, рассмотрев эффект возрастания емкости и удельного заряда в процессе циклирования электродов, описанный в [2] и [8]. Качественное объяснение этого эффекта дано в [10] и связывается по крайней мере со следующими факторами: увеличением ("развитием") поверхности, вызванным селективным вытравливанием в процессе циклирования более реакционноспособных компонентов сплавов, и увеличением числа реакционноспособных центров на поверхности, обусловленных изменением электронной структуры основного металла при легировании. Например, в [11] и [12] описаны приемы развития поверхности металлов путем их сплавления с более электроотрицательными металлами, такими как алюминий, цинк, щелочные и щелочноземельные металлы, с последующим химическим или электрохимическим вытравливанием большей части электроотрицательных металлов. В частности, так изготавливают "кислородные" и "водородные" электроды с высокоразвитой поверхностью, используемые для электролиза воды в устройствах получения кислорода и водорода [11], [12].
Аналогичное явление используется в заявляемом изобретении для придания нужных свойств положительному электроду, работающему по принципу псевдоконденсатора. Так, в заявляемом изобретении в результате использования в качестве материала положительного электрода материалов, полученных предложенным легированием основных металлов металлами-модификаторами, обеспечивается многократное повышение удельного заряда и псевдоемкости на единицу видимой поверхности, смещение потенциала окислительно-восстановительных реакций и ускорение их протекания, повышение рабочего напряжения конденсатора, обеспечение требуемых механических и химических свойств положительного электрода.
Основной идеей, реализованной в заявляемом изобретении, является разделение функций легирующих компонентов, используемых в сплавах для положительных электродов. Так, для развития поверхности электрода предложено вводить в состав сплавов металлы-разрыхлители, то есть электроотрицательные металлы (щелочные, щелочноземельные, алюминий, цинк, олово), легко выщелачивающиеся без заметного растворения основных металлов, а для целенаправленного улучшения химических, электрохимических и механических свойств электродов, подвергнутых обработке (травлению), - вводить в состав сплава металлы-модификаторы, которые полностью или частично остаются в структуре материала электрода после травления.
Предложенное разделение функций легирующих компонентов сплавов для положительных электродов позволяет достичь высоких удельных показателей (заряда, емкости) положительного электрода, а следовательно - важнейших технических характеристик конденсатора: удельной емкости, плотности заряда, удельной мощности.
Последнее замечание нуждается в пояснении. Емкость Cк простейшего конденсатора с двумя электродами определяется емкостью положительного С+ и отрицательного С- электродов: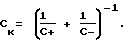
Энергия E заряженного до напряжения Uр конденсатора определяется формулой: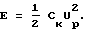
Если заменить положительный угольный электрод, имеющий приблизительно такую же емкость, как и отрицательный электрод, на положительный электрод с емкостью в пять раз большей, работающий по принципу псевдоконденсатора, то емкость конденсатора возрастет в 1,67 раз и во столько же раз увеличится его энергия.
Кроме того, как правило, замена положительного угольного электрода на положительный электрод, работающий по принципу псевдоконденсатора, приводит к повышению рабочего напряжения на 0,2 - 0,5 В, так что выигрыш в удельном заряде и удельной энергии еще выше. Однако эти преимущества достигаются лишь в том случае, если удельный заряд и удельные емкость положительного электрода, работающего по принципу псевдоконденсатора, выше, чем у положительного электрода из углеродного материала, накапливающего заряд по двойнослойному механизму, что имеет место в заявляемом электрохимическом конденсаторе.
Возможность решения заявляемым электрохимическим конденсатором поставленной задачи и получения требуемого технического результата иллюстрируется также следующими пояснительными примерами.
Пример 1
Положительный электрод изготовлен путем электрохимического осаждения покрытия толщиной 20 мкм из сплава Со 75% Zn 25% ат. на обе стороны подложки из чистого никеля Ni 99,9% толщиной 50 мкм.
Подложка с нанесенным на нее покрытием подвергалась электрохимической обработке в течение 2 часов в 10% растворе сульфата натрия при температуре 70oC при потенциале 0,2 В против насыщенного хлорсеребряного электрода (НХСЭ). Циклические вольтамперограммы (фиг. 4) такого электрода снимались в 25% водном растворе КОН при температуре 22oC, скорости развертки 100 мВ/с в диапазоне потенциалов от минус 1,0 В до 0,3 В против НХСЭ по стандартной методике, приведенной в [13]. Из кривой следует, что электрод имеет псевдоемкость порядка 2 Ф/см2 в интересующем диапазоне потенциалов от минус 0,2 В до 0,3 В при плотности тока около 0,2 А/см2 и удельном заряде около 1 Кл/см2.
Пример 2
Положительный электрод изготовлен путем термовакуумной конденсации покрытия толщиной 30 мкм из сплава Ni 75% Zn 15% Со 10% ат. на одну сторону подложки из чистого никеля толщиной 50 мкм при температуре подложки 300oC, продолжительности осаждения 110 мин. Последующая обработка покрытия проводилась в 3% растворе КОН при температуре 70oC, потенциале минус 0,2 В против НХСЭ в течение 2 час.
Циклические вольтамперограммы (фиг. 5, кривые 1, 2) такого электрода снимались в 25% растворе КОН при температуре 22oC, скорости развертки потенциала 100 мВ/с в диапазоне потенциалов от минус 0,4 В до 0,4 В против НХСЭ по той же стандартной методике, что и в примере 1. Заряд анодного (зарядного) и катодного (разрядного) тока определялся путем интегрирования кривых с помощью аналого-цифрового интегратора. Кривые вольтамперограмм через 10 циклов (кривая 1) и через 10000 циклов (кривая 2) практически совпадают. Удельный заряд зарядки и разрядки после 10 циклов составляют соответственно 0,45 Кл/см2 и 0,42 Кл/см2, после 10000 циклов они равны и составляют 0,5 Кл/см2.
Пример 3
Положительный электрод изготовлен путем одностороннего плакирования подложки - фольги из чистого никеля толщиной 40 мкм слоем алюминийжелезного сплава состава Al 80% Fe 20% толщиной 40 мкм с последующим диффузионным отжигом в инертной среде при температуре 620oC в течение 2 часов. Средний состав полученного таким образом покрытия толщиной 50 мкм - Ni 63% Al 30% Fe 7% ат. Последующая электрохимическая обработка покрытия проводилась в 25 % растворе КОН при температуре 60oC, плотности тока 20 мА/см2 в течение 45 мин. Измерение характеристик - как в примере 2. Максимальная плотность зарядного (анодного) тока 0,8 А/см2 разрядного (катодного) - 0,6 А/см2 заряды соответственно 2,8 Кл/см2 и 2,7 Кл/см2 после 10 циклов и 2,8 Кл/см2 и 2,8 Кл/см2 после 10000 циклов.
Пример 4
Положительный электрод изготовлен путем плакирования серебряной фольги толщиной 10 мкм слоем серебряно-литиевого сплава состава Ag 97% Li 3% ат. толщиной 15 мкм с последующим отжигом на воздухе при температуре 200oC в течение 3 часов. Электрохимическая обработка - в 10% растворе фосфата аммония, подкисленном до pH 3,5 раствором фосфорной кислоты, при температуре 90oC, плотности анодного тока 100 мА/см2 в течение 3 мин.
Циклическая вольтамперограмма после 50 циклов полученного таким образом электрода в 30% растворе КОН при температуре 22oC, скорости развертки потенциала 100 мВ/с в диапазоне потенциалов от минус 0,4 В до 0,4 В против НХСЭ приведена на фиг. 6. Из фиг. 6 следует, что электрод обеспечивает очень высокую плотность тока разрядки до 7 А/см2. Заряд зарядки и разрядки также очень высок и составляет 5 - 6 Кл/см2.
Пример 5
В двухэлектродном электрохимическом конденсаторе с комбинированным механизмом накопления заряда отрицательный электрод изготовлен из углеродистой ткани толщиной 0,4 мм, удельной массой в сухом состоянии 25 мг/см2, удельной емкостью 100 Ф/г. На одну сторону ткани магнетронным распылением наносился слой никеля толщиной 2 мкм, после чего точечной сваркой ткань приваривалась к токоподводу - фольге из чистого никеля толщиной 50 мкм. Положительный электрод изготовлен, как указано в примере 3. Положительный и отрицательный электроды диаметром 20 мм разделялись сепаратором из пористого полимерного материала толщиной 100 мкм, пропитанным электролитом - 30% водным раствором КОН. Конденсатор заряжался до рабочего напряжения Up = 1,4 В в течение 2 минут, после чего разряжался током Ip = 1 А до напряжения 0,1 В. Разрядная кривая представлена на фиг. 7. По первоначальному спаду потенциала ΔU определялось внутреннее сопротивление конденсатора по формуле:
Ri= ΔU/I.
Емкость конденсатора Cк определялась по наклону линейной части разрядной кривой:
Cк=I/(dU/dt),
где dU/dt - скорость уменьшения напряжения со временем на линейном участке разрядной характеристики.
Полная энергия, отдаваемая при разряде, определялась графическим интегрированием по времени напряжения и умножением этого интеграла на силу тока: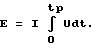
Максимальная мощность Wm рассчитывалась по формуле:
Wm=Up 2/4R1.
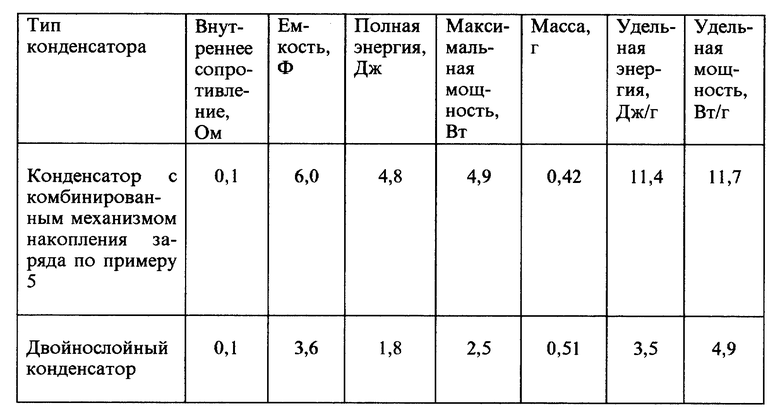
Для расчета удельных характеристик были взвешены оба электрода и пропитанный электролитом сепаратор. Их масса оказалась следующей: отрицательного электрода 0,225 г, положительного электрода 0,135 г, сепаратора 0,06 г. Суммарная масса 0,42 г.
Для оценки характеристик двухэлектродного электрохимического конденсатора с комбинированным механизмом накопления заряда, полученных в примере 5, был собран второй конденсатор, работающий по двойнослойному механизму, содержащий два одинаковых электрода, аналогичных отрицательному электроду первого конденсатора, и разделенных таким же сепаратором. Рабочее напряжение этого второго (двойнослойного) конденсатора - 1 В, остальные характеристики измерялись аналогично первому конденсатору по примеру 5.
Сравнение характеристик конденсатора по примеру 5, реализующего комбинированный механизм накопления заряда, и двойнослойного конденсатора, приведено в таблице.
Из таблицы следует, что изготовленный в соответствии с заявляемым изобретением электрохимический конденсатор, реализующий комбинированный механизм накопления заряда, превосходит по своим удельным характеристикам двойнослойный конденсатор.
Провести аналогичное сравнение конденсатора, изготовленного в соответствии с заявляемым изобретением, с конденсатором- прототипом не представляется возможным, так как в [6] характеристики прототипа не приведены. Единственная характеристика, которая может быть получена из примеров, приведенных в [6], - это заряд на единицу поверхности положительного электрода, составляющий величину около 0,003 - 0,004 Кл/см2. Эта характеристика на два-три порядка ниже, чем у положительных электродов в примерах 1 - 5.
Из рассмотренных примеров следует, что в заявляемом изобретении обеспечивается повышение удельных характеристик как отдельных (положительных) электродов, так и электрохимических конденсаторов с этими электродами, а также стабильность удельных характеристик электродов и конденсаторов в процессе их эксплуатации.
Из рассмотренных примеров также следует, что в заявляемом электрохимическом конденсаторе с комбинированным механизмом накопления заряда достигаются значения удельной энергии и мощности, в несколько раз более высокие, чем в двойнослойных электрохимических конденсаторах. Новые материалы положительного электрода и предложенная химическая и/или электрохимическая обработка позволяют получить положительные электроды с характеристиками достаточно высокими и стабильными при циклах зарядка-разрядка. Это свидетельствует о возможности решения поставленной задачи и достижения требуемых результатов при практической реализации заявляемого электрохимического конденсатора.
Таким образом, рассмотренные примеры, также как и приведенные теоретические пояснения подтверждают осуществимость заявляемого изобретения, его промышленную реализуемость и достижение требуемых технических результатов, которые обуславливают возможность создания электрохимического конденсатора с комбинированным механизмом накопления заряда, в котором реализуются приемлемые для практики удельные характеристики, обеспечивающие техническую и экономическую целесообразность его использования.
Источники информации
1. B.E.Conway. Transition from "Supercapacitor" to "Battery" behavior in electrochemical Energy Storage. J.Electrochem., Soc., 1991, v.138, N 6, p. 1539 - 1548.
2. Патент США N 5429895, кл. H 01 М 4/58, С 22 С 19/05, H 01 G 9/04, опубл. 04.07.95.
3. Kuo-Chuan Liu, Marc A.Anderson. Porous nickel oxide/nickel films for electrochemical capacitors. J. Electrochem. , Soc., 1996, v. 143, N 1, p. 124-130.
4. Международная заявка PCT (WO) N 96/19839, кл. H 01 М 4/58, 4/62, С 22 С 19/05, H 01 G 9/04, опубл. 27.06.96.
5. Патент РФ N 2058054, кл. H 01 G 9/04, опубл. 10.04.96.
6. Патент США N 5429893, кл. H 01 М 4/58, H 01 G 9/00, опубл. 04.07.95. (прототип).
7. Патент США N 5568353, кл. H 01 G 9/00, опубл. 22.10.96.
8. Международная заявка PCT (WO) N 96/07189, кл. H 01 G 9/00, 9/02, 9/04, 9/06, опубл. 07.03.96.
9. Справочник химика, т.3, "Химия", М.-Л., 1964.
10. Международная заявка РСТ (WO) N 96/122315, кл. H 01 М 4/58, C 22 С 19/05, H 01 G 9/04, опубл. 25.04.96.
11. Патент ФРГ N 3330961, кл. С 25 В 11/00, опубл. 07.03.85.
12. J.Balej, J.Divisek, H.Schmitz, J.Mergel. Preparation and properties of Raney nickel electrodes on nickel-zinc base for hydrogen and oxygen evolution from alkaline solution. Part I and II. J. Appl. Electrochem., 1992, v.22, N 8, p.705-716.
13. Методы измерений в электрохимии. Под ред. Э.Егер, А.Залкинд. М., Мир, 1977, Т.1, стр. 99-107, 158-165.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЭЛЕКТРОХИМИЧЕСКИЙ НАКОПИТЕЛЬ ЭНЕРГИИ | 1997 |
|
RU2121728C1 |
| ЭЛЕКТРОХИМИЧЕСКИЙ НАКОПИТЕЛЬ ЭНЕРГИИ ВЫСОКОЙ УДЕЛЬНОЙ МОЩНОСТИ И ЭЛЕКТРОД ДЛЯ НЕГО | 2000 |
|
RU2170468C1 |
| СПОСОБ ФОРМИРОВАНИЯ ОБЪЕМНО-ПОРИСТОГО СЛОЯ МЕТАЛЛА С ОТКРЫТОЙ ПОРИСТОСТЬЮ НА ЭЛЕКТРОПРОВОДНОЙ ПОДЛОЖКЕ | 1999 |
|
RU2150533C1 |
| СПОСОБ ЭЛЕКТРОХИМИЧЕСКОГО ПОЛИРОВАНИЯ МЕТАЛЛИЧЕСКИХ ИЗДЕЛИЙ | 1999 |
|
RU2168565C1 |
| Способ изготовления рисунка проводников | 1991 |
|
SU1812644A1 |
| МНОГОЭЛЕМЕНТНЫЙ ЭЛЕКТРОХИМИЧЕСКИЙ КОНДЕНСАТОР И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2010 |
|
RU2419907C1 |
| ГИБКИЙ ГИБРИДНЫЙ ЭЛЕКТРОД ДЛЯ СУПЕРКОНДЕНСАТОРА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2020 |
|
RU2748557C1 |
| НАНОКОМПОЗИТНЫЙ ЭЛЕКТРОХИМИЧЕСКИЙ КОНДЕНСАТОР И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2011 |
|
RU2518150C2 |
| КОНДЕНСАТОР С ДВОЙНЫМ ЭЛЕКТРИЧЕСКИМ СЛОЕМ | 1997 |
|
RU2180144C1 |
| СУПЕРКОНДЕНСАТОР И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2016 |
|
RU2668533C1 |

Изобретение относится к электротехнике, в частности к производству электрохимических конденсаторов с комбинированным механизмом накопления заряда. Техническим результатом изобретения является обеспечение приемлемых для практики удельных характеристик конденсатора, обуславливающих техническую и экономическую целесообразность его использования. Согласно изобретению электрохимический конденсатор с комбинированным механизмом накопления заряда содержит разделенные ионным проводником-электролитом электроды, из которых отрицательный электрод, реализующий накопление заряда в двойном электрическом слое на поверхности контакта электрода и электролита, выполнен из углеродного материала с высокой удельной поверхностью, а положительный электрод, реализующий накопление заряда за счет обратимого протекания электрохимических реакций в моно- и полимолекулярных слоях продуктов взаимодействия материала электрода с электролитом, выполнен в виде подложки из электропроводящего, иононепроводящего, химически и электрохимически неактивного в электролите материала с расположенным на одной или обеих сторонах подложки поверхностным электрохимически активным слоем, полученным путем обработки в растворах кислот, солей или щелочей нанесенного на подложку покрытия из материала, состав которого удовлетворяет формуле M1(1-Х) M2(Х), где 0,4 ≤ X ≤ 0,97 M1 - металл-разрыхлитель из группы: Аl, Zn, Sn, щелочные и щелочноземельные металлы и их комбинации, М2 - металл из группы: Ni, Со, Аg или их сплав, или сплав по крайней мере одного из этих металлов с одним или несколькими металлами-модификаторами из группы: а или лантаноиды, Мо, W, Мn, V, Тi, Вi, Sb, Fe. 4 з.п. ф-лы, 7 ил., 1 табл.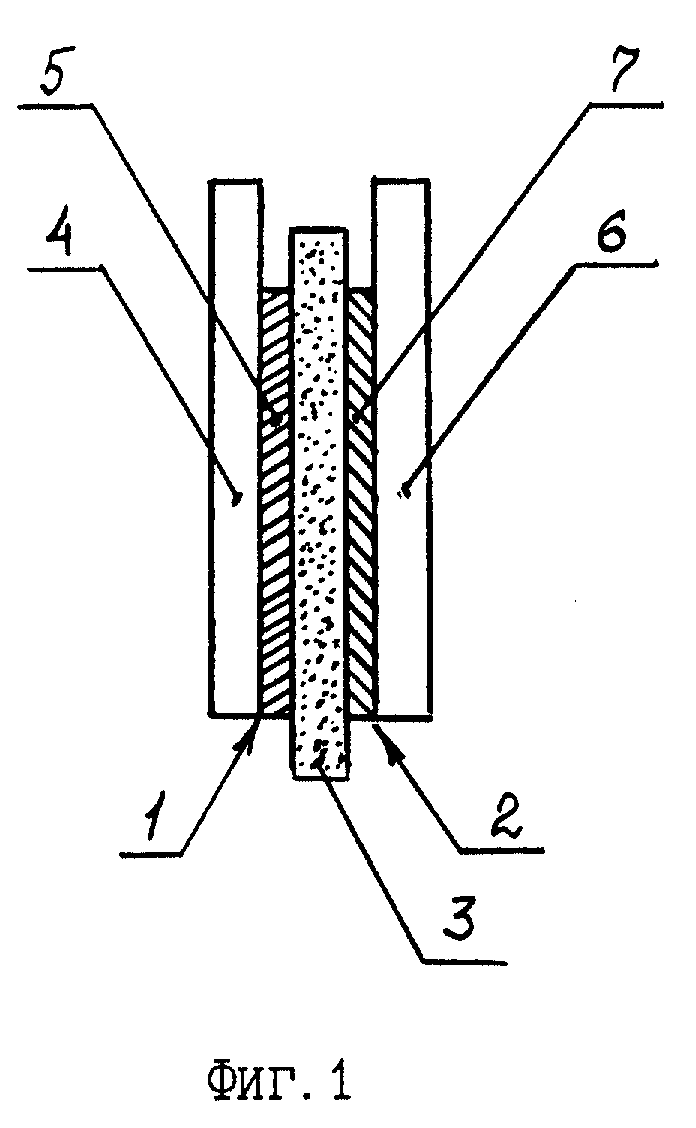
| US 5568353 A, 22.10.96 | |||
| Приспособление в пере для письма с целью увеличения на нем запаса чернил и уменьшения скорости их высыхания | 1917 |
|
SU96A1 |
| Конденсатор | 1989 |
|
SU1777183A1 |
Авторы
Даты
2000-01-27—Публикация
1998-07-03—Подача