Настоящее изобретение относится в основном к обработке живой биологической ткани оптическим излучением и конкретно к способу стимулирования мягкой, живой ткани лазерным излучением.
Различные нехирургические средства применяли для терапевтической обработки живой ткани. Такие приемы включали применение ультразвуковой энергии, электрическое стимулирование, высокочастотное стимулирование диатермическим воздействием, рентгеновских лучей (X-лучей) и микроволнового излучения. Приемы такие, как электрическое стимулирование, диатермическое воздействие, рентгеновские лучи, микроволновое излучение, оказывали некоторое благоприятное терапевтическое воздействие на мягкие ткани. Однако их использование было в некоторой степени ограничено потому, что вызывало повреждение ткани за счет интенсивных термических эффектов. Следовательно, уровни энергии, связанные с терапевтическими обработками, включающими диатермическое воздействие, рентгеновское излучение, микроволновое и электрическое стимулирование, были ограничены такими низкими уровнями, которые оказывали малое терапевтическое воздействие или не оказывали вовсе терапевтического воздействия. Кроме того, дозирование или выдерживание по отношению к микроволновому или рентгеновскому излучению должны быть осторожно контролируемыми для того, чтобы избежать облучения, связанного с проблемами здоровья. Энергия ультразвука не является предпочтительно поглощаемой и оказывает влияние на всю окружающую ткань.
Оптическая энергия, генерированная лазерами, применялась для различных медицинских и хирургических целей вследствие монохроматической и когерентной природы лазерного света, который может быть селективно поглощен живой тканью в зависимости от определенных характеристик длины волны света и свойств облучаемой ткани, включающих отражаемость, коэффициент поглощения, коэффициент пропускания, термическую проводимость и константу термической диффузии. Отражаемость, коэффициент поглощения и коэффициент пропускания зависят от длины волны оптического излучения. Известно, что коэффициент поглощения зависит от таких факторов, как переход между полосами поглощения свободного электрона, решеточное поглощение (фононное поглощение) и примесное поглощение, которое зависит от длины волны оптического излучения.
В живой ткани вода представляет преимущественный компонент, который содержит полосу поглощения, соответствующую колебаниям молекул воды в инфракрасной области. В видимой области существует поглощение, обусловленное присутствием гемоглобина. Кроме того, коэффициент пропускания в живой ткани является доминирующим фактором.
Таким образом, для данного типа ткани лазерный свет может распространяться через ткань, по существу, неослабленным или может быть почти полностью поглощенным. Уровень, до которого нагревается ткань и одновременно разрушается, зависит от уровня, до которого она поглощает оптическую энергию. Обычно предпочтительным является то, чтобы лазерный свет, по существу, пропускался в ткани, которые желательно не повреждались светом, и поглощался тканями, которые являются поврежденными. Например, когда применяют лазерное излучение в тканевой области, которая является влажной от крови или воды, желательно, чтобы оптическая энергия не поглощалась водой или кровью, тем самым позволяя лазерной энергии быть направленной специфично в ткань, которая обрабатывается. Другое преимущество лазерной обработки состоит в том, что оптическая энергия может быть доставлена к обрабатываемым тканям в точное, хорошо определенное местоположение и с предварительно определенными ограниченными уровнями энергии.
Известно, что рубиновый и аргоновый лазеры испускают оптическую энергию в видимой области электромагнитного спектра, и они успешно использовались в области офтальмологии для повторного присоединения сетчатки к нижележащей сосудистой оболочке глаза и для лечения глаукомы за счет перфорирования передних частей глаза для ослабления межсосудистого давления. Энергия рубинового лазера имеет длину волны 694 нм и находится в красной области видимого спектра. Аргоновый лазер испускает энергию при 488 и 515 нм и, таким образом, появляется в зелено-голубой области видимого спектра. Лучи рубинового и аргонового лазера минимально поглощаются водой, но интенсивно поглощаются гемоглобином хромогенов крови. Таким образом, энергия рубинового и аргонового лазеров слабо поглощается непигментированной тканью, такой как роговица, хрусталик, и жидкой частью стекловидного тела глаза, но предпочтительно поглощается пигментированной сетчаткой, где она может затем оказывать термический эффект.
Другой тип лазера, который был приспособлен для хирургического использования, представляет газовый лазер на двуокиси углерода (CO2), который испускает оптический пучок, который интенсивно поглощается водой. Длина волны CO2- лазера составляет 10,6 микрометров и поэтому лежит в невидимой, далекой инфракрасной области электромагнитного спектра и поглощается независимо от окраски ткани всеми мягкими тканями, имеющими высокое содержание воды. Таким образом, CO2-лазер становится превосходным хирургическим скальпелем и испарителем. Так как свет этого лазера является полностью поглощаемым, глубина его проникновения является неглубокой и может быть точно контролированной в отношении поверхности ткани, которая обрабатывается. CO2-лазер является, таким образом, хорошо адаптированным для использования в различных хирургических процедурах, в которых он является необходимым для испарения или коагулирования нейтральной ткани с минимальным термическим повреждением вблизи тканей.
Другой лазер, который получил широко распространенное использование, представляет неодимовый лазер с введенной иттрий-алюминий-гранатовой добавкой (Nd-YAG). Nd-YAG лазер имеет преобладающий режим работы при его вторичной длине волны 1320 нм в ближней инфракрасной области электромагнитного спектра. Nd-YAG оптическое излучение поглощается в большей степени кровью, чем водой, делая его полезным для коагулирования больших кровоточащих сосудов. Nd-YAG лазер при 1320 нм пропускался через эндоскоп для обработки различных гастроинтестинальных кровоточащих поражений, таких как варикозные расширения пищевода, пептические язвы и артериовенозные аномалии. Такие применения энергии лазера являются, таким образом, хорошо приспособленными там, где желательными являются высокоэнергетические термические эффекты, такие как испарение ткани, каутеризация ткани, коагуляция и в качестве хирургического скальпеля.
Следующие патенты США раскрывают устройства и способы для терапевтической обработки живых тканей с помощью лазерного излучения:
3456651 3720213 4141362
4144888 4367729 4561440
4573465 4589404 4601288
4604992 4672969 4692924
4705036 4931053 4966144
Три патента: Dew 4672969.00; L'Esperance, Jr. 4931053.00 от 5 июня 1990; и Rochkind, et.al., 4966144.00 от 30 октября 1990 лучше всего раскрывают ранее известный уровень техники. Этот ранее известный уровень техники рассматривает использование лазерной энергии в определенных, конкретных применениях. Dew обсуждает использование лазера, конкретно Nd-YAG лазера, работавшего при вторичной длине волны 1320 нм. Dew раскрывает тот факт, что Nd-YAG лазеры обычно работают при 1060 нм. Целью патента Dew является использование лазера для эффекта закрытия раны и реконструкции биологической ткани. Лазерная энергия превращается в тепло, которое одновременно разрывает ткань в коллагеновых элементах, которые выступают в качестве "биологического клея".
L'Esperance показывает применение лазерных лучей, используемых в видимой красной или ближней инфракрасной областях, и чрезвычайно низкомощных лазеров для облучения ткани. L'Esperance показывает использование либо гелий-неоновых, либо криптоновых лазеров. Длина волны, использованная L'Esperance, представляет 610-660 нм, дающая выход 0,15 мВт.
Rochkind 30 октября 1990 г. использовал либо когерентную, либо некогерентную продолжительность излучения, но описывает гелий-неоновый лазер, работающий при 632 нм с интенсивностью 16 мВт на см2, или лазер аргонового типа, генерирующий свет при 465 или 520 нм с интенсивностью света около 40 мВт на см2. Кроме того, Rochkind описывает двухстадийный процесс для достижения способов, рассматриваемых изобретением; первая обработка, в процессе которой ткань открывали и выдерживали в процессе операции, и вторая обработка после закрытия раны.
Была предпринята попытка применения обычных лазеров для целей стимулирования мягкой ткани, которые вызывают уменьшение боли и воспаления, при стимулировании микроциркуляция для уменьшения времени выздоровления при очень низких уровнях мощности, обычно при 100 мВт. Хотя было достигнуто некоторое полезное терапевтическое воздействие, время обработки было неприемлемо продолжительным.
Таким образом, целью настоящего изобретения является обеспечение способа для безопасного и эффективного применения реактивной энергии лазера к живой ткани для терапевтических целей, например для снижения боли, уменьшения воспаления при повышенных уровнях мощности и улучшения заживления ткани за счет стимуляции микроциркуляции, без воздействия на ткань повреждающих термических эффектов. Этот способ сокращает время обработки ниже времени, которое известно в настоящее время в этой области.
Способ использования реактивной лазерной системы с низким уровнем от 100 мВт до 800 мВт в импульсном или непрерывном режиме с оптической энергией, получаемой с помощью Nd-YAG лазера при фундаментальной длине волны 1,064 нм, как было найдено, уменьшает боль в мягких тканях, снижает воспаление и улучшает выздоровление ткани за счет стимулирования микроциркуляции без воздействия на ткань повреждающих термических эффектов. В альтернативном способе, оптическая энергия продуцируется неодимовым лазером с добавками иттрий-литий-фторида (Nd-YLF) при длине волны 1055 нм или каким-либо другим лазером в предпочтительной области длин волн от около 1000 до 1150 нм. Живая ткань облучается оптической энергией с длиной волны и при рассеивающем уровне мощности в ткань, которая дает количество энергии, поглощенной и превращенной в тепло, которая находится внутри области, связанной минимальной скоростью поглощения, достаточной для поднятия средней температуры облученной ткани до уровня выше базальной температуры тела, но которая ниже, чем скорость поглощения, при которой ткань превращается в коллагеновое вещество. Длина волны, размер пятна или пучка, мощность, время выдерживания осторожно контролируются с получением заметного эффекта потепления в облученной ткани, но который ограничивается для того, чтобы избежать повреждения ткани за счет термических эффектов.
Ни одно из известных ранее в этой области предложений не описывает настоящее изобретение. Как описано ранее в описании, Nd-YAG лазер работает в его первичной длине волны 1064 нм с мощностью 80-100 мВт или Nd-YLF лазер работает при длине волны 1055 нм с той же областью мощности. Ни L'Esperance, ни Rochkind не описывают применения Nd-YAG лазера в этой конкретной форме. Оба автора и L'Esperance и Rochkind детализируют предпочтительный способ работы, который составляет приблизительно половину длины волны настоящего изобретения. Фактически, L'Esperance использует скорее два пучка, чем один. Ни одно из известных ранее решений не раскрывает применение Nd-YAG лазера при его первичной длине волны 1064 нм.
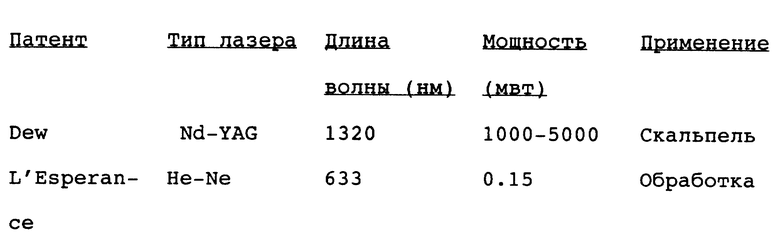
Таблица (см. в конце описания) сравнивает Dew, L'Esperance и Rochkind способы с настоящим изобретением.
В то время как L'Esperance может включить данные Rochkind, ни одно из ранее известных решений даже не намекает на то, что Nd-YAG лазер может быть использован в этом виде с такой малой мощностью и желаемыми результатами.
Согласно предпочтительному способу лазерная энергия продуцируется Nd-YAG лазером при фундаментальной длине волны 1064 нм при излучаемом уровне мощности от около 100 до 800 мВт. Оптическая лазерная энергия применяется к областям тела, которые требуют уменьшения мышечного спазма, увеличенной циркуляции, уменьшения боли или улучшения выздоровления ткани. Площадь поверхности разграничивается, и поверхность ткани облучается лазерным пучком в течение периода времени и интенсивности, необходимых для проявления желаемого терапевтического эффекта, с энергетической плотностью облученной ткани, которая ограничивается областью от около 1 Дж/см2 до около 15 Дж/см2. Интенсивность и продолжительность обработки определяются характером ткани, которая обрабатывается желаемой глубиной проникновения, остротой повреждения и состоянием пациента.
Терапевтическое лечение реактивными лазерными системами с низкими дозами было продемонстрировано для целей снижения боли, уменьшения воспаления и улучшения выздоровления ткани за счет стимулирования микроциркуляции, все успешно сопровождалось без проявления повреждающих термических эффектов в ткани. В качестве лазерного источника был использован резонатор Nd-YAG лазера. Его начальная длина волны составляла 1064 нм и имела энергетическое излучение пучка, контролируемое от 100 мВт до 800 мВт. Лазер был способен работать в импульсном или непрерывном режиме и его излучение контролировалось таймером в области 0,1-9,9 мин. Продолжительность импульса регулировалась от 0,1 до 9,9 с с 0,1 секундными интервалами. Частота импульса также контролировалось от 0,1 до 9,9 с с интервалами 0,1 с. Пучок Nd-YAG лазера работал в ближней инфракрасной области электромагнитного спектра при 1064 нм и, таким образом, был невидимым. Способ направления пучка к полю зрения, выступающему в качестве мишени, представлял гибкое кварцевое волокно и фокусировался вручную.
Nd-YAG лазерный пучок выходит из устройства на выходе лазерной головки и направляется парой расположенных на одной прямой клиньев до пропускания через циркулярно переменный, нейтральной плотности аттенюатор. Свет, прошедший через аттенюатор, фокусируется через пару линз с фокальной длиной 90 мм в дальний конец оптического волокнистого кабеля.
Аттенюатор основного пучка представляет прерыватель, помещенный снаружи лазерной головки между устройством на выходе лазера и зеркалом, направляющим пучок. Он включает четыре компонента: отражающую под 90o призму, шторный рычаг, шторную подъемную скобку и возбуждающий соленоид. Призма устанавливается на шторном рычаге таким образом, что в нормальном закрытом положении призма отсекает лазерный пучок и отражает его вниз в свинцовую плашку пучка в лазерной скамье. Соленоид снабжается энергией, когда выбирают канал на выходе и опускают ножную педаль, которая вызывает подъем шторного рычага и позволяет проходить пучку. Когда соленоидный рычаг обесточивается, шторка опускается в закрытое положение.
Оптическая энергия продуцируется с помощью когерентного источника света, предпочтительно лазера, имеющего длину волны 1064 нм в ближней инфракрасной области электромагнитного спектра. Лазер обеспечивается оптическим волокнистым проводником и устройством для направления пучка оптической энергии в тканевую поверхность. Энергия оптического излучения контролируется и подается для продуцирования минимальной скорости поглощения в облучаемой ткани, которая будет повышать среднюю температуру облучаемой ткани до уровня выше базальной температуры тела, но которая не превышает минимальную скорость поглощения, которая является достаточно большой для превращения облучаемой ткани в коллагеновое вещество.
С помощью расширенных испытаний было определено, что вышеуказанное условие удовлетворяется Nd-YAG лазером, работающим в его первой длине волны 1064 нм при уровне мощности на выходе от 100 до 800 мВт, с лазерным пучком, который является фокусированным для получения плотности энергии для отбрасываемого лазерного пучка в области от около 1,0 Дж/см2 до около 15 Дж/см2 на обрабатываемом участке.
Наблюдали определенные физиологические механизмы в ткани и на клеточном уровне, когда использовали указанный выше процесс. При оценке микроциркуляторной системы, например, было продемонстрировано, что стенки кровеносных сосудов обладают фоточувствительностью. Когда стенки кровеносных сосудов подвергают действию лазерного излучения, как продемонстрировано выше, ингибируется тонус в гладких миоцитах, увеличивая таким образом поток крови в капиллярах. Другие эффекты, которые наблюдали, заключаются в следующем: периферийной капиллярной неоваскуляризации, снижении агрегации тромбоцитов крови, восстановлении кислорода из триплетного в синглетное состояние, которое позволяет проводить большее насыщение кислородом ткани, восстановлении концентрации буферного вещества в крови, стабилизации индексов деформации эритроцитов, уменьшении продуктов перекисленных липидов окисления крови. Другие эффекты, которые наблюдали, заключаются в повышенных индексах антитромбиновой активности, стимулировании ферментов антиоксидантной системы, такой как супероксидная дисмутаза и каталаза. Наблюдали увеличение в венозных и лимфотических сосудах и в истечении облученных областей. Проницаемость ткани в облученной площади существенно увеличивалась. Это способствует немедленному уменьшению отека и количеству гематом в ткани. На клеточном уровне, также было замечено, что митохондрия образует повышенные количества ADP с последующим увеличением АТР. Очевидным также является то, что имеет место увеличенная стимуляция кальция и натрия, пропускаемых через мембрану ткани на клеточном уровне.
На нейронном уровне, наблюдали следующие эффекты в результате вышеупомянутого терапевтического лечения. Сначала, имело место повышенное действие потенциально разрушенных и интактных нервов. Кровяное снабжение и количество аксонов увеличивалось в облученной площади. Отмечалось ингибирование зарубцовывания ткани, когда ткань обрабатывалась. Имело место немедленное увеличение в мембранной проницаемости нерва. Продолжительные изменения в проницаемости ионов кальция и калия через нерв наблюдали по крайней мере 120 суток. Увеличивалось продуцирование РНК и последующее продуцирование ДНК. Образовывался синглетный O2, который является важным фактором в клеточной регенерации. Патологическая дегенерация с нервным повреждением изменяется на регенерацию. Стимулируются и астроциты и олигодедроциты, которые вызывают повешенное образование периферийных нервных аксонов и миелина.
Фагоцитоз клеток крови увеличивается, тем самым, по существу, снижая инфекцию. Очевидно также появление значительного противовоспалительного явления, которое обеспечивает снижение в воспалении сухожилий, нервов, синовиальных сумок в суставах, несмотря на то, что в то же самое время дает упрочнение коллагена. Происходит также влияние на значительное увеличение грануляции ткани в закрытии открытых ран при ограниченных условиях циркуляции.
Наблюдается инальгезия ткани вместе со сложным рядом действий на уровне ткани. На локальном уровне, имеет место уменьшение воспаления, вызывающее реабсорбцию эксудатов. Энкефалины и эндорфины восстанавливаются с модуляцией продуцирования боли и на уровне спинно-мозговой полости и в мозгу. Восстанавливается также серотоногенный путь. Несмотря на то что этот процесс является не полностью понятным, полагают, что облучение ткани вызывает возвращение баланса энергии на клеточный уровень, который является причиной для уменьшения боли.
В альтернативном способе, лазерная энергия продуцируется Nd-YLF лазером при длине волны 1055 нм. Могут быть использованы другие лазеры или усовершенствованы для работы в предпочтительной области от около 1000 до около 1150 нм при том же уровне мощности.
Хотя изобретение описывается со ссылкой на предпочтительный способ и со ссылкой на конкретные терапевтические применения, вышеуказанное описание не предназначено для того, чтобы быть составленным в ограниченном смысле. Модификации раскрытого варианта, а также альтернативные применения изобретения будут предполагаться специалистами в этой области вышеуказанным описанием. Поэтому предполагается, что прилагаемая формула изобретения будет включать любые такие модификации или варианты, которые входят в истинный объем изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ ГНОЙНО-ВОСПАЛИТЕЛЬНЫХ ПРОЦЕССОВ В МЯГКИХ ТКАНЯХ И ВНУТРЕННИХ ОРГАНАХ С ПОМОЩЬЮ ЛАЗЕРНОГО ИЗЛУЧЕНИЯ И УСТАНОВКА ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2003 |
|
RU2234349C1 |
| СПОСОБ УДАЛЕНИЯ ПОДКОЖНО-ЖИРОВОЙ ТКАНИ В ОБЛАСТИ ПЛЕЧА | 2019 |
|
RU2705625C1 |
| СПОСОБ ЛЕЧЕНИЯ РИНОФИМЫ В СОЧЕТАНИИ С БАЗАЛЬНОКЛЕТОЧНЫМ РАКОМ КОНЧИКА НОСА CT1N0M0 I ST | 2023 |
|
RU2802998C1 |
| СПОСОБ ЛАЗЕРНОЙ ГИПЕРТЕРМИИ ОПУХОЛЕЙ ПРИ ВВЕДЕНИИ ПЛАЗМОННО-РЕЗОНАНСНЫХ НАНОЧАСТИЦ С ПРИМЕНЕНИЕМ ТЕХНИКИ ИММЕРСИОННОГО ОПТИЧЕСКОГО ПРОСВЕТЛЕНИЯ | 2022 |
|
RU2800156C1 |
| Способ микроструктурирования поверхности прозрачных материалов | 2016 |
|
RU2635494C2 |
| СПОСОБ КОМБИНИРОВАННОГО ЛАЗЕРНОГО ЛЕЧЕНИЯ ЭПИТЕЛИАЛЬНОЙ КИСТЫ ЦИЛИАРНОГО ТЕЛА | 2012 |
|
RU2484799C1 |
| СПОСОБ ЛОКАЛЬНОЙ КРИСТАЛЛИЗАЦИИ СТЕКОЛ | 2015 |
|
RU2616958C1 |
| СПОСОБ ФОРМИРОВАНИЯ ПОЛИКРИСТАЛЛИЧЕСКОГО КРЕМНИЯ | 2023 |
|
RU2807779C1 |
| Комбинированный способ проведения лазерной иридэктомии с использованием диодного лазера и Nd: YAG лазера при темных радужках | 2022 |
|
RU2816806C1 |
| Способ лечения первичной открытоугольной глаукомы после ранее проведенной непроникающей глубокой склерэктомии | 2022 |
|
RU2801470C1 |

Изобретение относится к медицине. Способ состоит в том, что биологическая ткань живого субъекта облучается оптической энергией при длине волны и при мощности излучения на уровне рассеивания энергии, вызывающей количество оптической энергии, поглощаемой и превращаемой в тепло в ткани в пределах области, связанной минимальной скоростью поглощения, достаточной для повышения средней температуры облучаемой ткани до уровня выше базальной температуры тела, но которая является ниже, чем скорость поглощения, при которой ткань превращается в коллагеновое вещество. Согласно этому способу терапевтический согревающий эффект продуцируется внутри облученной ткани, но без того, чтобы вызвать эффект повреждения ткани за счет термического перегревания. Способ использования низкоуровневой лазерной системы от 100 до 800 мВт в импульсном или непрерывном режиме с оптической энергией, продуцируемой Nd-YAG лазером при фундаментальной длине 1064 нм, как было найдено, снижает боль в мягких тканях, снижает воспаление и усиливает вылечивание ткани за счет стимулирования микроциркулирования без того, чтобы подвергать живую ткань повреждающим термическим эффектам. 19 з.п. ф-лы, 1 табл.
| US 4672969 A, 16.06.87. |
Авторы
Даты
2000-02-27—Публикация
1995-03-31—Подача