Область техники, к которой относится изобретение
Изобретение относится к производным триазина, полезным в качестве лекарственных средств.
Предпосылки создания изобретения
Гепатит этиологически подразделяется на вирусный гепатит (гепатит A, B и C, множественный инфекционный гепатит и т.д.), токсический гепатит (например, вызванный лекарственными средствами) и аутоиммунный гепатит.
Среди этих видов гепатита есть гепатит, которому часто соответствует субхроническое-хроническое течение (острый гепатит C), и рефрактерный гепатит, характеризующийся повторяющимися эпизодами острого обострения и развитием, до цирроза (хронический гепатит B). Существует также гепатит, который протекает ускоренно, т.е. молниеносный гепатит.
Лечение гепатита включает, помимо общей терапии для стимулирования механизма лечения, основанного на отдыхе и режиме питания, противовирусное лечение, которое проводится для ингибирования роста болезнетворного вируса в случаях вирусного гепатита, и иммунотерапию для усиления поставленного под угрозу клеточного иммунитета хозяина. Доступными лекарственными средствами для лечения печени, среди прочих, являются печеночный гидролизат, глицирризин (qlycyrrhizin) восстановленный глутатион, тиопронин и полиенфосфатидилхолин. В качестве противовирусных средств применяются интерфероны, арабинозиладенин (Ara-A), арабинозиладенозинмонофосфат (Ara-AMP), ацикловир и т.п. В качестве иммунорегуляторов используются глюкокортикоиды, интерлейкин-2, пицибанил (ОК-432), цианиданол, левамизол и т.п. Интерфероны, кроме противовирусной активности, обладают иммунологическим действием. Известно, что простагландин E обладает цитозащитным действием, и ожидается, что он будет пригодным для защиты клеток печени. Известно, что помимо вышеупомянутых лекарственных средств, человеческий эпидермальный фактор роста (hEGF) и человеческий гепатоцитный фактор роста (hHGF) обладают активностью, усиливающей цитогенез, и полагают, что их клиническое применение в качестве факторов, усиливающих восстановление печени, является перспективным, но они еще находятся на стадии доклинических исследований.
В последнее время для лечения и предупреждения гепатита B рекомендуется вакцинная терапия.
Однако пока еще нет удовлетворительного доступного лекарственного средства для лечения гепатита, так же, как и существует постоянная необходимость в создании лекарственного средства, эффективного для предупреждения распространения некроза и усиления восстановления гепатоцитов.
Известно, что ильзогладинмалеат (малеат 2,4-диамино-6-(2,5-дихлорфенил)-1,3,5-триазина), который представляет собой производное бензогуанамина, по структуре аналогичное соединениям настоящего изобретения, и такое соединение, в котором положения 2 и 5 фенильной составляющей бензогуанамина замещены хлором, причем, вместе с тем, две аминогруппы являются незамещенными, обладает гепатоцит-защитным действием и пригоден для лечения гепатита (см. WO 91/01733, Japanese Kokai Tokkyo Koho S58-55423). Подобным образом, производные, также содержащие 2,5-дихлорфенильную группу, но имеющие пиперидино- или морфолиногруппу вместо одной из упомянутых аминогрупп, а именно 2-амино-4-(2,5-дихлорфенил)-6-пиперидино-1,3,5-триазин и 2-амино-4-(2,5-дихлорфенил)-6-морфолино-1,3,5-триазин, известны как промежуточные соединения для получения противоаллергических производных никотиноилбензогуанамина (Japanese Kokai Tokkyo Koho S57-203083 и S59-104320). Между тем, существует хозяин известных соединений, соответствующих бензогаунамину, фенильная группа которых является либо незамещенной, либо галогенированной, и одна из аминогрупп которых является замещенной. В качестве примера соединения, содержащего ациклическую группу, замещающую одну из указанных аминогрупп, можно упомянуть 2-амино-4-(2-гидроксиэтиламино)-6-фенил-1,3,5-триазин. Как сообщалось, это соединение пригодно в качестве исходного вещества для получения смол (CA 106:34062). Известно, что как соединение, содержащее циклическую аминогруппу, 2-амино-4-(4-метил-пиперазин-1-ил)-6-фенил-1,3,5-триазин обладает аналгезирующим действием (CA 84:135722). Однако соединения, соответствующие бензогуанамину, в котором как 2-, так и 5-положение его фенильной группы замещены хлором, а одна из аминогрупп является замещенной аминогруппой, неизвестны, за исключением упомянутых соединений, в которых одна из аминогрупп замещена либо пиперидино-, либо морфолиногруппой.
Описание изобретения
Настоящее изобретение имеет своей целью производное триазина, имеющее новое строение и низкую токсичность, демонстрирующее эффективность при гепатите, и пригодную лекарственную композицию, содержащую упомянутое производное в качестве активного ингредиента.
Для достижения вышеупомянутой цели авторы настоящего изобретения синтезировали и исследовали различные новые по строению соединения и обнаружили, что при сравнении с ильзогладинмалеатом, а именно с малеатом 2,4-диамино-[6-(2,5-дихлорфенил)-1,3,5-триазина] , который описан в Japanese Kokai Tokio Koho S58-55423 и в WO 91/01733, упомянутых выше, соединения приведенной ниже общей формулы [I] обнаруживают заметно превосходящую противогепатитную и ингибирующую печеночной онкогенез активность у млекопитающих животных при низкой токсичности и, следовательно, пригодны в качестве лечебного средства против гепатита. Настоящее изобретение выполнено на основе вышеупомянутых полученных сведений.
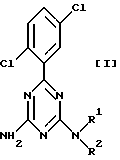
Настоящее изобретение относится, в своем первом аспекте, к лекарственной композиции, содержащей соединение вышеупомянутой общей формулы [I] или его сольват, или его соль, в качестве активного ингредиента, и, во втором аспекте, к упомянутому соединению общей формулы [I], его сольвату или соли.
В вышеупомянутой общей формуле R1 и R2 могут быть одинаковыми или различными, и каждый из них представляет собой водород, незамещенный или замещенный алкил, аралкил, аралкенил или арил, или R1 и R2, в совокупности и вместе с соседним атомом N, представляют собой 4-8-членную циклическую аминогруппу, такую как группа формулы NR1R2. Циклическая аминогруппа может содержать в качестве атома кольца, кроме вышеупомянутого атома N, азот, кислород или серу, и также может быть замещенной.
Структурной особенностью этого соединения является то, что как 2-, так и 5-положение фенильной группы бензогуанамина замещены хлором, и одна из аминогрупп гуанамина является свободной, а другая аминогруппа является замещенной.
Соединение вышеупомянутой общей формулы [I] является новым соединением, нигде ранее не описанным, за исключением соединений, в которых как R1, так и R2 являются водородом, и соединений, в которых NR1R2 представляют собой пиперидино- или мофролиногруппу. Такие соединения являются известными соединениями, и поэтому они не включаются в пункт формулы настоящего изобретения на соединение. Однако замечательная противогепатитная активность этих соединений впервые раскрыта авторами настоящего изобретения и поэтому включена в объем пунктов формулы настоящего изобретения на композицию.
Далее настоящее изобретение описывается подробно.
Алкил для R1 и R2 может являться линейным или разветвленным и состоять из 1-10 атомов углерода, как, например, метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, н-пентил, изопентил, н-гексил, изогексил, н-гептил, изогептил, н-октил, изооктил, н-нонил, изононил, н-децил и изодецил. Предпочтительными являются алкильные C1-4-группы. Алкил может быть замещен 1-3 заместителями, либо одинаковыми, либо разными, такими как группы, которые выбирают из группы, состоящей из гидроксигруппы, алкоксигруппы, аминогруппы, моноалкиламиногруппы, диалкиламиногруппы, ариламиногруппы, циклической аминогруппы, карбоксигруппы, карбамоилгруппы, арилоксигруппы и ароилоксигруппы. Особенно предпочтительной является гидроксильная группа. Когда заместитель имеет арильную группу, последняя может быть замещена C1-4-алкилом или алкоксигруппой.
Замещенный алкил включает, но не ограничивается перечисленным, следующие группы.
Примерами гидроксиалкила являются 2-гидроксиэтил, 3-гидроксипропил, 2-гидроксипропил, 4-гидроксибутил, 3-гидроксибутил, 5-гидроксипентил, 6-гидроксигексил, 7-гидроксигептил, 8-гидроксиоктил, 9-гидроксинонил, 10-гидроксидецил и подобные группы.
Алкоксигруппа алкоксиалкила может являться линейной или разветвленной и состоять из 1-4 атомов углерода, как, например, метоксигруппа, этоксигруппа, н-пропоксигруппа, изопропоксигруппа, н-бутоксигруппа, изобутоксигруппа, втор-бутоксигруппа, трет-бутоксигруппа, и т.д. Конкретно, алкоксиалкил представляет собой 2-метоксиэтил, 3-метоксипропил, 2-метоксипропил, 4-метоксибутил, 3-метоксибутил, 5-метоксипентил, 6-этоксигексил, 7-этоксигептил, 8-этоксиоктил, 9-пропоксинонил и 10-пропоксидецил.
Аминоалкил включает 2-аминоэтил, 3-аминопропил, 2-аминопропил, 4-аминобутил, 3-аминобутил, 5-аминопентил, 6-аминогексил, 7-аминогептил, 8-аминооктил, 9-аминононил и 10-аминодецил.
Моноалкиламиноалкил включает 2-метиламиноэтил, 3-метиламинопропил, 4-метиламинобутил, 3-этиламинопропил, 3-этиламинобутил, 5-этиламинопентил, 6-этиламиногексил, 7-пропиламиногептил, 8-пропиламинооктил, 9-бутиламинононил и 10-бутиламинодецил.
Диалкиламиноалкил включает 2-(N,N-диаметиламино)этил, 3-(N,N-диаметиламино)пропил, 4-(N,N-диаметиламино)бутил, 3-(N,N-диэтиламино)пропил, 3-(N,N-диэтиламино)бутил, 5-(N, N-диэтиламино)пентил, 6-(N,N-диэтиламино)гексил, 7-(N, N-дипропиламино)гекпил, 8-(N,N-дипропиламино)октил, 9-(N,N-дибутиламино)нонил и 10-(N,N-дибутиламино)децил.
Ариламинная группа ариламиноалкила включает, среди других, анилиногруппу и нафтиламиногруппу.
Циклическая аминогруппа циклического аминоалкила включает 4-8-членные циклические группы, упомянутые выше для NR1R2. Особенно предпочтительными являются пиперидиногруппа, пиперазинил и морфолиногруппа. Циклическая аминогруппа может быть замещена C7-13 аралкилом.
Карбоксиалкил включает 1-карбоксиметил, 2-карбоксиэтил, 3-карбоксипропил, 2-карбоксипропил, 4-карбоксибутил, 3-карбоксибутил, 5-карбоксипентил, 6-карбоксигексил, 7-карбоксигептил, 8-карбоксиоктил, 9-карбоксинонил и 10-карбоксидецил.
Карбамоилалкил включает 1-карбамоилметил, 2-карбамоилэтил, 3-карбамоилпропил, 2-карбамоилпропил, 4-карбамоилбутил, 3-карбамоилбутил, 5-карбамоилпентил, 6-карбамоилгексил, 7-карбамоилгептил, 8-карбамоилоктил, 9-карбамоилнонил и 10-карбамоилдецил.
Арильная группа арилоксиалкила включают C6-13-арильные группы, такие как фенил, 1-нафтил, 2-нафтил и бифенил. Особенно предпочтителен фенил.
Ароильная группа ароилоксиалкила включает C7-10-группы, такие как, среди других, бензоил и никотиноил. Особенно предпочтительным является бензоил.
Аралкил включает C7-14-группы, такие как бензил, фенетил, фенилпропил, фенилбутил и дифенилметил.
Аралкенил включает C7-10-группы, такие как, среди прочих, циннамил и 3-фенилаллил.
Арил включает группы, упомянутые в случае арильной группы арилоксигруппы. Особенно предпочтительным является фенил.
Что касается вышеупомянутых заместителей, содержащих арильную группу, то арильная группа может быть замещена 1-3-алкилами или алкоксигруппами, либо одинаковыми, либо разными, причем каждая содержит 1-4 атома углерода.
NR1R2 4-8-членная циклическая аминогруппа включает, среди прочих, азетидин-1-ил, пирролидин-1-ил, 3-пирролидин-1-ил, пиперидиногруппу, гексаметилениминогруппу, октагидроазоцин-1-ил, пиперазин-1-ил, гомопиперазин-1-ил, морфолиногруппу и тиоморфолиногруппу. Предпочтительными являются 5- или 6-членные циклические аминогруппы. Особенно предпочтительными являются пирролидин-1-ил, пиперидиногруппа или морфолиногруппа. Циклическая аминогруппа может быть замещена 1-4 заместителями, выбираемыми из группы, состоящей из гидроксила, оксогруппы, карбоксигруппы, алкила, гидроксиалкила, арилоксиалкила, аминоалкила, алкилсулфониламиноалкила, алкилсульфониламиногруппы, алксилсульфониларалкила, алкилсульфонила, арила, аралкила, 2-пиримидинила и циклической аминогруппы. Алкил в таком заместителе может представлять собой любую из вышеупомянутых линейных или разветвленных алкильных групп, содержащих 1-4 атома углерода. Арил в таком заместителе может представлять собой любую из C6-12-арильных групп, упомянутых ранее. Этот арил может быть замещен C1-4-алкилом или алкоксигруппой. Особенно предпочтительными заместителями для циклической аминогруппы NR1R2 являются гидроксильная групп, гидроксиалкил, оксогруппа, аминогруппа и алкил.
Соль соединения [I], которая охватывается объемом изобретения, включает соли с минеральными кислотами, такими как хлористоводородная кислота, серная кислота, азотная кислота, фосфорная кислота, фтористоводородная кислота и бромистоводородная кислота, и соли с органическими кислотами, такими как уксусная кислота, винная кислота, молочная кислота, лимонная кислота, фумаровая кислота, малеиновая кислота, янтарная кислота, метансульфоновая кислота, этансульфоновая кислота, бензолсульфоновая кислота, толуолсульфоновая кислота, нафталинсульфоновая кислота и камфорсульфоновая кислота.
Соединение [I] настоящего изобретения может быть получено, например, следующим способом.
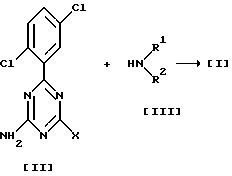
Так, соединение [I] может быть получено путем взаимодействия галогентриазинового производного [II] (где X представляет собой хлор или фтор) с амином [III] в присутствии основания, в инертном для реакции растворителе, при температуре 0-200oC, предпочтительно 25-100oC. Растворитель, который можно использовать при реакции, включает апротонные полярные растворители, такие как ацетонитрил, диметилсульфоксид и N,N-диаметилформамид (ДМФА), простые эфиры, такие как тетрагидрофуран, диметоксиэтан, диэтиловый эфир и диоксан, глимы, такие как метилцеллозольв и диметиловый эфир этиленгликоля, галогенированные углеводороды, такие как метиленхлорид и хлороформ, углеводороды, такие как бензол, толуол и ксилол, и смеси таких растворителей. Основание, которое можно использовать, представляет собой неорганические основания, такие как карбонаты щелочных металлов (например, карбонат калия, карбонат натрия), гидрокарбонаты щелочных металлов (например, гидрокарбонат калия, гидрокарбонат натрия) и гидроксиды щелочных металлов (например, гидроксид калия, гидроксид натрия), и органические основания, такие как триэтиламин и пиридин. Вместо основания может быть использован избыток амина (HNR1R2).
Время реакции зависит от вида исходных соединений, основания и применяемого растворителя, но, вообще, может изменяться от нескольких минут до 24 часов.
Количество используемого амина [III] является по меньшей мере эквимолярным, предпочтительно составляет 1-1,2 молярных эквивалента на каждый моль [II] . Количество используемого основания является по крайней мере эквимолярным, предпочтительно, составляет 1-2 молярных эквивалента на каждый моль [II].
Исходное соединение [II] может быть получено известным способом (Japanese Kokai Tokkyo Koho S51-70781). Соединение [III] может быть доступно коммерчески или его можно синтезировать обычным способом, как упоминается здесь в справочных примерах.
Кроме того, некоторые из соединений [I] содержат один или несколько асимметричных атомов углерода и, следовательно, могут существовать в виде оптически активных форм, и соответствующие изомеры и их производные смеси также включены в объем настоящего изобретения.
Упомянутые выше оптически активные соединения могут быть оптически отделены от смесей известными способами, например, с использованием хиральной колонки или с использованием хиральной кислоты (например, винной кислоты, дибензоилтартрата, миндальной кислоты, 10-камфорсульфоновой кислоты), пользуясь их основностью. С другой стороны, оптически активные соединения можно получить, используя в качестве исходного соединения предварительно полученное оптически активное соединение [III].
Соединение [I] настоящего изобретения может быть обработано непосредственно известным способом с образованием любой из вышеупомянутых солей. Например, гидрохлорид соединения [I] можно получить, растворяя соединение [I] в спиртовом растворе хлористого водорода.
Любое из различных соединений [I] по настоящему изобретению, содержащее карбоксильную группу, может быть превращено в соль известным способом. Соли, о которых здесь идет речь, включают соли щелочных металлов, такие как натриевые и калиевые соли, и соли щелочноземельных металлов, такие как кальциевые соли. Соли щелочных металлов соединений [I] могут быть получены при добавлении одного эквивалента гидроксида натрия, гидроксида калия или подобного гидроксида к содержащему карбоксильную группу соединению [I] изобретения, предпочтительно в спиртовом растворе. Соль щелочноземельного металла соединения [I] изобретения можно получить путем растворения вышеупомянутой соли щелочного металла в воде, метаноле, этаноле или в их смеси, например с последующим добавлением одного эквивалента, например хлорида кальция.
Сольват (в том числе, гидрад) соединения [I] или его соли, по настоящему изобретению, также включен в объем настоящего изобретения. Сольват, вообще, можно получить путем перекристаллизации соединения из соответствующего растворителя или подходящего смешанного растворителя, содержащего соответствующий растворитель. Например, гидрат соединения [I] настоящего изобретения может быть получен путем перекристаллизации соединения [I] из водного спирта.
Соединение [I] изобретения может демонстрировать кристаллический полиморфизм. Полиморфные модификации также включены в объем настоящего изобретения.
Полученное таким образом нужное соединение [I] может быть выделено и очищено, по сути, известными методами, такими как концентрирование, доведение pH, фазовый перенос, экстракция растворителем, кристаллизация, фракционная перегонка и хроматография.
Соединение настоящего изобретения пригодно в качестве лечебного лекарственного средства против гепатита.
Для применения в качестве лекарственного средства соединение настоящего изобретения вводят в том виде, в каком оно существует, или в форме фармацевтической композиции, содержащей, например, 0,1-99,5%, предпочтительно - 0,5-90%, соединения в фармацевтически приемлемом нетоксичном инертном носителе.
В качестве носителя может использоваться один или несколько твердых, полутвердых или жидких разбавителей, наполнителей и других вспомогательных компонентов составов. Фармацевтическую композицию вводят, предпочтительно, в виде стандартной лекарственной формы. Фармацевтическая композиция настоящего изобретения может вводиться перорально, парентерально, местно (например, трансдермально) или ректально. Конечно, должны выбираться лекарственные формы, подходящие для соответствующего способа введения. Особенно предпочтительным является пероральное введение.
Дозировку лекарственного средства при лечении гепатита устанавливают, предпочтительно, с учетом возраста, массы тела и других особенностей пациента, способа введения, природы и тяжести заболевания, и т.д. Как правило, однако, суточная пероральная дозировка для взрослых людей может составлять, вообще, от 100 мкг до 100 мг на пациента, предпочтительно - от 500 мкг до 30 мг на пациента. В ряде случаев удовлетворительными могут быть более низкие дозы, в то время как в других случаях могут потребоваться более высокие дозы. Вышеупомянутая дозировка может назначаться, при необходимости, в виде 2-3 раздельных доз.
Пероральный прием может осуществляться при использовании твердых или жидких лекарственных форм, таких как масс-порошки, порошки, таблетки, драже, капсулы, гранулы, суспензии, растворы, сиропы, капли и таблетки под язык.
Масс-порошки могут быть изготовлены посредством измельчения активного порошка до тонко раздробленной формы. Порошки могут быть изготовлены посредством измельчения активного вещества до тонко раздробленного состояния с последующим смешением его с измельченным до подобного состояния фармацевтическим носителем, например со съедобным углеводом, таким как крахмал или маннит. При необходимости также добавляются корригент, консервант, диспергатор, краситель, вкусовые добавки и т.п.
Капсулы могут быть изготовлены путем заполнения упомянутыми тонко измельченными масс-порошками, порошками или гранулами, описанными для случая таблеток, капсульных оболочек, таких как желатиновые капсульные оболочки. Перед операцией заполнения с порошками могут быть смешаны смазывающие или псевдоожижающие добавки, такие как коллоидный диоксид кремния, тальк, стеарат магния, стеарат кальция или твердый полиэтиленгликоль. Повышения эффективности лекарственного средства после приема можно достичь при добавлении дезинтегратора или солюбилизатора, такого как карбоксиметилцеллюлоза, кальцийкарбоксиметилцеллюлоза, гидроксипропилцеллюлоза с низкой степенью замещения, найтрийкроскармелоза (croscarmellose sodium), найтрикарбоксиметилкрахмал, карбонат кальция или карбонат натрия.
Мягкие капсулы можно изготовить путем суспендирования упомянутых тонко измельченных порошков в растительном масле, полиэтиленгликоле, глицерине или поверхностно-активном веществе и обертывания суспензии слоями желатина. Таблетки могут быть изготовлены посредством добавления эксципиента в упомянутые порошки, гранулирования или комкования смеси, добавления дезинтегратора или смазывающего агента и прессования всей композиции. Порошкообразная смесь может быть приготовлена смешением упомянутых тонко измельченных порошков с упомянутым разбавителем или основой. При необходимости можно добавить связующее (например, найтрикарбоксиметилцеллюлозу, метилцеллюлозу, гидроксипропилметилцеллюлозу, желатин, поливинилпирролидон, поливиниловый спирт и т. п. ), замедлитель растворения (например, парафин), реабсорбент (например, соли четвертичных оснований) и адсорбент (например, бентонит, каолин, дикальцийфосфат и т. п. ). Порошкообразная смесь может быть переработана в гранулы посредством смачивания ее связующим, например сиропом, крахмальным клейстером, аравийской камедью, раствором целлюлозы или раствором высокомолекулярного вещества, перемешивания смеси, ее высушивания и также распыления. Вместо гранулирования таких порошков можно прессовать порошки на таблетирующей машине и дробить получающийся кусок сырой формы. Получающиеся в результате гранулы могут быть защищены от слипания посредством добавления смазывающего вещества, такого как стеариновая кислота, соль стеариновой кислоты, минеральное масло или подобного вещества. Смазанную таким образом смесь затем прессуют. На получающиеся в результате таблетки без покрытия можно нанести покрытие из пленкообразующей композиции или из композиции, содержащей сахар.
Лекарственное средство может быть смешано со свободно текущим инертным носителем, и смесь можно прессовать непосредственно, не прибегая к вышеупомянутым процессам гранулирования или комкования. Также можно нанести прозрачное или просвечивающее защитное покрытие, состоящее, например, из герметичной пленки шеллака, пленки сахара или полимера, или гладкое покрытие из воска. Другие пероральные композиции, такие как раствор, сироп, эликсир, также могут быть получены в стандартных лекарственных формах, причем каждая содержит предварительно установленное количество лекарственного вещества. Сиропы могут быть получены путем растворения соединения в подходящих корригированных водных растворах, в то время как эликсиры можно изготовить, используя нетоксичные спиртовые носители. Суспензии могут быть составлены посредством диспергирования соединения в нетоксичных носителях. При необходимости также могут добавляться солюбилизаторы и эмульгаторы (например, этоксилированный изостеариловый спирт, сложный эфир полиоксиэтиленсорбита и т.п. ), консерванты и корригенты (например, мятное масло, сахарин и т.п.).
Когда это необходимо, стандартная лекарственная форма для перорального введения может быть микроинкапсулирована. Такой состав может быть покрыт или заключен в полимерную, восковую или иную матрицу, чтобы получить лекарственную форму с пролонгированным действием или лекарственную форму с отсроченным высвобождением.
Парентеральное введение может быть осуществлено с использованием жидких стандартных лекарственных форм для подкожной, внутримышечной или внутривенной инъекции, например, растворов и суспензий. Такие стандартные лекарственные формы могут быть изготовлены посредством суспендирования или растворения заранее установленного количества соединения в пригодном для инъекций нетоксичном жидком носителе, например в водном носителе или в масляном носителе, и стерилизации полученных в результате суспензии или раствора. Для придания изотоничности можно добавить нетоксичную соль или раствор соли. Кроме того, также могут быть добавлены стабилизаторы, консерванты, эмульгаторы и т.д.
Ректальное введение можно осуществить с применением суппозиториев, изготовленных посредством растворения или суспендирования соединения в низкоплавком водорастворимом или нерастворимом в воде твердом носителе, таком как полэитиленгликоль, масло какао, полусинтетическое масло (например, Witpsol®), высший сложный эфир (например, миристилпальмитат), или в их смесях.
Наилучший способ осуществления изобретения
Приведенные ниже примеры и тест-примеры, относящиеся к некоторым представителям соединений изобретения, предназначены для более подробного описания настоящего изобретения и не должны рассматриваться как определяющие объем изобретения.
Ссылочный пример 1
Синтез транс-4-гидрокси-L-пролинола
В 30 мл сухого ТГФ суспендируют 1,57 г алюмогидрида лития, и охлаждают раствор до -10oC. К этому раствору по каплям, при температуре в интервале от -10oC до -5oC, добавляют раствор метилового эфира транс-4-гидрокси-L-пролина (3,00 г) в ТГФ (10 мл). Смесь перемешивают при комнатной температуре в течение 2 часов и затем кипятят с обратным холодильником в течение 30 минут. К этой реакционной смеси добавляют этилацетат и водный ТГФ, и смесь фильтруют. Нерастворимое вещество промывают ТГФ, и фильтрат концентрируют при пониженном давлении, и получают 2,0 г желтого масла.
Ссылочный пример 2
Синтез 3-гидроксиметилазетидина
В редукционном аппарате среднего давления емкостью 300 мл суспензию 1-дифенилметил-3-гидроксиметилазетидина (8,00 г) и 5% Pd/C (2,50 г) в метаноле (80 мл) обрабатывают газообразным водородом при давлении 5,1 кг/см2 и 50oC в течение 15 часов. Эту реакционную смесь фильтруют, и отделившийся Pd/C тщательно промывают метанолом. Фильтрат и промывочный метанол объединяют и концентрируют при пониженном давлении. Остаток разбавляют 30 мл н-гексана и хорошенько перемешивают, декантируют супернатант, и получают 2,85 г сырого 3-гидроксиметилазетидина.
Подобным образом синтезируют 3,24 г 3-гидроксиазетидина, исходя из 10,11 г 1-дифенилметил-3-гидроксиазетидина.
Ссылочный пример 3
Синтез 3-метансульфониламинопирролидина
(Стадия 1)
К суспензии 3-амино-1-бензилпирролидина (7,00 г) и карбоната калия (6,04 г) в ТГФ (100 мл) при перемешивании при комнатной температуре постепенно, по каплям, добавляют раствор метансульфонилхлорида (5,00 г) в ТГФ (40 мл), и смесь перемешивают при комнатной температуре в течение 20 часов. Эту реакционную смесь концентрируют при пониженном давлении, и остаток суспендируют в этилацетате. Эту суспензию промывают водой и насыщенным водным раствором NaCl, обезвоживают над безводным сульфатом магния (MgSO4) и концентрируют. Оставшийся сырой продукт очищают колоночной хроматографией (C-200/товарный знак; CHCl3 ---> CHCl3:MeOH = 30:1), и получают 10,10 г 1-бензил-(3-метансульфониламино)пирролидина в виде светло-коричневого масла.
(Стадия 2)
В 300 мл редукционном аппарате среднего давления готовят суспензию, состоящую из 10,00 г вышеупомянутого соединения, 2,00 г 5% Pd/C, 50 мл метанола и 10 мл уксусной кислоты, и обрабатывают ее газообразным водородом при 5,1 кг/см3 и 40oC в течение 15 часов. Эту реакционную смесь далее обрабатывают, как в ссылочном примере 2, и получают 9,20 г 3-метансульфониламинопирролидина.
Пример 1
Синтез 2-амино-4-[N, N-бис(2-гидроксиэтил)амино]-6-(2,5- дихлорфенил)-1,3,5-триазина
К смеси диэтаноламина (9,2 г), N,N-диметилформамида (200 мл) и безводного карбоната калия (15 г) при перемешивании при комнатной температуре добавляют 20 г 2-амино-4-хлор-6-(2,5-дихлорфенил)-1,3,5-триазина, и смесь перемешивают при комнатной температуре в течение 7 часов. Эту реакционную смесь разбавляют 2 л (литрами) воды и перемешивают в течение 1 часа. Получающиеся в результате кристаллы собирают фильтрацией, промывают водой и сушат, получают 24 г белого кристаллического вещества. Эту порцию кристаллов перекристаллизовывают из метанола, собирают кристаллы фильтрацией и сушат, и получают 21 г названного в заголовке соединения в виде белого кристаллического вещества.
Т.пл. 199 - 200oC.
Элементный анализ для C13H15Cl2N5O2
Вычислено (%): C - 45,36; H - 4,39; N - 20,35
Найдено (%): C - 45,58; H - 4,33; N - 20,46.
Пример 2
2-Амино-4-(2,5-дихлорфенил)-6-метиламино-1,3,5-триазин
Используя метиламин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 205 - 206oC.
Элементный анализ для C10H9Cl2N5
Вычислено (%): C - 44,47; H - 3,36; N - 25,93.
Найдено (%): C - 44,24; H - 3,30; N - 25,70.
Пример 3
2-Амино-4-(2,5-дихлорфенил)-6-диметиламино-1,3,5-триазин
Используя диметиламин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 178 - 179oC.
Элементный анализ для C11H11Cl2N5
Вычислено (%): C - 46,50; H - 3,90; N - 24,65.
Найдено (%): C - 46,45; H - 3,73; N - 24,39.
Пример 4
2-Амино-4-(2,5-дихлорфенил)-6-(гидроксиэтиламино)- 1,3,5-триазин
Используя этаноламин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 198 - 199oC.
Элементный анализ для C11H11Cl2N5O
Вычислено (%): C - 44,02; H - 3,69; N - 23,33.
Найдено (%): C - 43,82; H - 3,46; N - 23,01.
Пример 5
2-Амино-4-(2,5-дихлорфенил)-6-[N-метил-N-(2-гидроксиэтил)-амино- 1,3,5-триазин
Используя N-метил-N-(2-гидроксиэтил)амин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 153 - 155oC.
Элементный анализ для C12H13Cl2N5O
Вычислено (%): C - 45,88; H - 4,17; N - 22,29.
Найдено (%): C - 45,60; H - 4,06; N - 22,25.
Пример 6
2-Амино-4-(2,5-дихлорфенил)-6-(2-метоксиэтиламино)- 1,3,5-триазин
Используя 2-метоксиэтиламин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 195 - 197oC.
Элементный анализ для C12H13Cl2N5O
Вычислено (%): C - 45,88; H - 4,17; N - 22,29.
Найдено (%): C - 45,72; H - 3,90; N - 22,12.
Пример 7
2-Амино-4-(2,5-дихлорфенил)-6-(8-диэтиламино-1-октиламино)- 1,3,5-триазин
Используя 8-диэтиламино-1-октиламино вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 101 - 102oC.
Элементный анализ для C21H32Cl2N6
Вычислено (%): C - 57,40; H - 7,34; N - 19,12.
Найдено (%): C - 57,16; H - 7,48; N - 18,92.
Пример 8
2-Амино-4-бензиламино-6-(2,5-дихлорфенил)-1,3,5-триазин
Используя бензиламин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 200 - 201oC.
Элементный анализ для C16H13Cl2N5
Вычислено (%): C - 55,51; H - 3,78; N - 20,23.
Найдено (%): C - 55,78; H - 3,66; N - 20,07.
Пример 9
2-Амино-4-(2,5-дихлорфенил)-6-[4-(2-пиримидил)-пиперазин-1-ил] - 1,3,5-триазин
Используя 4-(2-пиримидил)пиперазин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 224 - 225oC.
Элементный анализ для C17H16Cl2N8
Вычислено (%): C - 50,63; H - 4,00; N - 27,79.
Найдено (%): C - 50,48; H - 3,91; N - 27,92.
Пример 10
2-Амино-4-(N-бензил-N-метиламино)-6-(2,5-дихлорфенил)- 1,3,5-триазин
Используя N-метилбензиламин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 163 - 164oC.
Элементный анализ для C17H15Cl2N5
Вычислено (%): C - 56,68; H - 4,20; N - 19,44.
Найдено (%): C - 56,81; H - 4,20; N - 19,47.
Пример 11
2-Амино-4-(2,5-дихлорфенил)-6-[2-(диэтиламино)этиламино]- 1,3,5-триазин
Используя N, N-диэтилэтилендиамин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 141 - 142oC.
Элементный анализ для C15H20Cl2N6
Вычислено (%): C - 50,71; H - 5,67; N - 23,65.
Найдено (%): C - 50,63; H - 5,64; N - 23,50.
Пример 12
2-Амино-4-(2,5-дихлорфенил)-6-фенетиламино-1,3,5-триазин
Используя фенетиламин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 217 - 218oC.
Элементный анализ для C17H15Cl2N5
Вычислено (%): C - 56,68; H - 4,20; N - 19,44.
Найдено (%): C - 56,94; H - 4,16; N - 19,58.
Пример 13
2-Амино-4-(2,5-дихлорфенил)-6-(2-феноксиэтиламино)- 1,3,5-триазин
Используя 2-феноксиэтиламин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 172 - 173oC.
Элементный анализ для C17H15Cl2N5O
Вычислено (%): C - 54,27; H - 4,02; N - 18,61.
Найдено (%): C - 54,45; H - 3,80; N - 18,68.
Пример 14
2-Амино-4-анилино-6-(2,5-дихлорфенил)-1,3,5-триазин
Используя анилин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 180 - 181oC.
Элементный анализ для C15H11Cl2N5
Вычислено (%): C - 54,24; H - 3,34; N - 21,08.
Найдено (%): C - 54,36; H - 3,41; N - 21,15.
Пример 15
2-Амино-4-[(карбоксиметил)амино]-6-(2,5-дихлорфенил)-1,3,5- триазин
Используя глицин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 271 - 272oC (разл.).
Элементный анализ для C11H9Cl2N5O2
Вычислено (%): C - 42,06; H - 2,89; N - 22,29.
Найдено (%): C - 42,04; H - 2,96; N - 22,23.
Пример 16
2-Амино-4-циннамиламино-6-(2,5-дихлорфенил)-1,3,5-триазин
Используя циннамиламин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 198 - 199oC.
Элементный анализ для C18H15Cl2N5
Вычислено (%): C - 58,08; H - 4,06; N - 18,81.
Найдено (%): C - 58,21; H - 4,10; N - 18,90.
Пример 17
2-Амино-4-(2-аминоэтиламино)-6-(2,5-дихлорфенил)-1,3,5-триазин
Используя этилендиамин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 152 - 153oC.
Элементный анализ для C11H12Cl2N6
Вычислено (%): C - 44,16; H - 4,04; N - 28,09.
Найдено (%): C - 44,11; H - 3,93; N - 28,06.
Пример 18
Гидрохлорид 2-амино-4-(2-аминоэтиламино)-6-(2,5-дихлорфенил)-1,3,5-триазина
Используя соединение, синтезированное в примере 17, названное в заголовке соединение получают с помощью той же процедуры, которая описана ниже в примере 32 (стадия 2).
Т.пл. 267 - 268oC (разл.).
Элементный анализ для C11H12Cl2N6 • HCl
Вычислено (%): C - 39,36; H - 3,90; N - 25,04.
Найдено (%): C - 39,04; H - 4,15; N - 24,96.
Пример 19
2-Амино-4-(2,5-дихлорфенил)-6-[8-(3,4,5-триметоксибензоилокси) октил-1-амино]-1,3,5-триазин
Используя 8-(3,4,5-триметоксибензоилокси)октиламин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 72 - 73oC.
Элементный анализ для C27H33Cl2N5O5
Вычислено (%): C - 56,06; H - 5,75; N - 12,11.
Найдено (%): C - 56,09; H - 6,01; N - 12,01.
Пример 20
2-Амино-4-(2,5-дихлорфенил)-6-(2-пиперидиноэтиламино)- 1,3,5-триазин
Используя 2-пиперидиноэтиламино вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 179 - 181oC.
Элементный анализ для C16H20Cl2N6
Вычислено (%): C - 52,32; H - 5,49; N - 22,88.
Найдено (%): C - 52,12; H - 5,32; N - 22,79.
Пример 21
2-Амино-4-(2,5-дихлорфенил)-6-[4-[2-(4-метилфенокси)этил] - пиперазин-1-ил]-1,3,5-триазин
Используя N-[2-(4-метилфенокси)] этилпиперазин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 140 - 141oC.
Элементный анализ для C22H24Cl2N6O
Вычислено (%): C - 57,52; H - 5,27; N - 18,29.
Найдено (%): C - 57,59; H - 5,27; N - 18,42.
Пример 22
2-Амино-4-(2,5-дихлорфенил)-6-[2-(N-фениламино)этиламино]- 1,3,5-триазин
Используя N-фенилэтилендиамин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 139 - 141oC.
Элементный анализ для C17H16Cl2N6
Вычислено (%): C - 54,41; H - 4,30; N - 22,40.
Найдено (%): C - 54,43; H - 4,27; N - 22,55.
Пример 23
2-Амино-4-(2,5-дихлорфенил)-6-[4-[2-(2-гидроксиэтил)пиперазин- 1-ил] -1,3,5-триазин
Используя N-(2-гидроксиэтил)пиперазин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 185 - 187oC.
Элементный анализ для C15H18Cl2N6O
Вычислено (%): C - 48,79; H - 4,91; N - 22,76.
Найдено (%): C - 48,63; H - 4,85; N - 22,74.
Пример 24
2-Амино-4-(2,5-дихлорфенил)-6-(2-морфолиноэтиламино)- 1,3,5-триазин
Используя 2-(морфолино)этиламин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 159 - 161oC.
Элементный анализ для C15H18Cl2N6O
Вычислено (%): C - 48,79; H - 4,91; N - 22,76.
Найдено (%): C - 48,56; H - 4,87; N - 22,86.
Пример 25
2-Амино-4-(2,5-дихлорфенил)-6-[4-(дифенилметил)пиперазин- 1-ил]-1,3,5-триазин
Используя 1-дифенилметилпиперазаин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 217 - 218oC.
Элементный анализ для C26H24Cl2N6
Вычислено (%): C - 63,55; H - 4,92; N - 17,10.
Найдено (%): C - 63,68; H - 4,95; N - 17,24.
Пример 26
2-Амино-4-[2-(4-дифенилметилпиперазин-1-ил)этиламино] -6- (2,5-дихлорфенил)-1,3,5-триазин
Используя 2-(4-дифенилметилпиперазин-1-ил)этиламин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 192 - 193oC.
Элементный анализ для C28H29Cl2N7 • 1/2 H2O
Вычислено (%): C - 61,88; H - 5,56; N - 18,03.
Найдено (%): C - 61,87; H - 5,68; N - 18,07.
Пример 27
2-Амино-4-(2,5-дихлорфенил)-6-диэтиламино-1,3,5-триазин
Используя гидрохлорид диэтиламина вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 137 - 138oC.
Элементный анализ для C13H15Cl2N5
Вычислено (%): C - 50,01; H - 4,84; N - 22,43.
Найдено (%): C - 50,25; H - 4,75; N - 22,22.
Пример 28
2-Амино-4-(2,5-дихлорфенил)-6-диизопропиламино-1,3,5-триазин
Используя диизопропиламин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 158 - 159oC.
Элементный анализ для C15H19Cl2N5
Вычислено (%): C - 52,95; H - 5,63; N - 20,58.
Найдено (%): C - 53,04; H - 5,53; N - 20,71.
Пример 29
2-Амино-4-[(4-карбамоилметил)амино]-6-(2,5-дихлорфенил)- 1,3,5-триазин
Используя гидрохлорид глицинамида вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 260 - 261oC.
Элементный анализ для C11H10Cl2N6O • 1/4 H2O
Вычислено (%): C - 41,59; H - 3,33; N - 26,46.
Найдено (%): C - 41,98; H - 3,40; N - 25,74.
Пример 30
2-Амино-4-(2,5-дихлорфенил)-6-пирролидино-1,3,5-триазин
Используя пирролидин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 191 - 193oC.
Элементный анализ для C13H13Cl2N5
Вычислено (%): C - 50,34; H - 4,22; N - 22,58.
Найдено (%): C - 50,35; H - 4,11; N - 22,53.
Пример 31
Малеат 2-амино-4-(2,5-дихлорфенил)-6-(3-гидрокси-1- пирролидинил)-1,3,5-триазина
(Стадия 1). Используя 3-гидроксипирролидин вместо диэтиламина, осуществляют ту же процедуру, что в примере 1, и получают 7,3 г свободного основания названного в заголовке соединения.
(Стадия 2). В 100 мл метанола растворяют 7,1 г соединения, полученного на стадии 1, и 2,67 г малеиновой кислоты. Этот раствор концентрируют примерно до 1/5 его первоначального объема, и собирают фильтрацией образовавшиеся кристаллы. Получают 6,4 г названного в заголовке соединения в виде светло-желтых кристаллов.
Т.пл. 192 - 194oC.
Элементный анализ для C13H13Cl2N5O • C4H4O4
Вычислено (%): C - 47,17; H - 3,87; N - 15,84.
Найдено (%): C - 46,05; H - 3,84; N - 15,75.
Пример 32
Гидрохлорид (S)-2-амино-4-(2,5-дихлорфенил)-6-(2-гидрокси-1- метил-1-пирролидинил)-1,3,5-триазина
(Стадия 1). Используя (S)-2-гидроксиметилпирролидин вместо диэтиламина, осуществляют ту же процедуру, что в примере 1, и получают 6,2 г свободного основания названного в заголовке соединения.
(Стадия 2). В 50 мл метанола растворяют 5,1 г соединения, полученного на стадии 1, после чего, при охлаждении льдом, добавляют 6 мл 20% HCl-метанола. Смесь концентрируют примерно до 1/10 ее первоначального объема, и собирают фильтрацией образовавшиеся кристаллы. Получают 2,6 г названного в заголовке соединения в виде белых кристаллов.
Т.пл. 143 - 145oC.
Элементный анализ для C14H15Cl2N5O • HCl • H2O
Вычислено (%): C - 42,60; H - 4,60; N - 17,74.
Найдено (%): C - 42,34; H - 4,61; N - 17,79.
Пример 33
Гидрохлорид (R)-2-амино-4-(2,5-дихлорфенил)-6-(2- гидроксиметил-1-пирролидинил)-1,3,5-триазин
Используя (R)-2-гидроксиметилпирролидин вместо (S)-2-гидроксиметилпирролидина, осуществляют ту же процедуру, что в примере 32, и получают названное в заголовке соединение.
Т.пл. 140 - 143oC.
Элементный анализ для C14H15Cl2N5O • HCl • H2O
Вычислено (%): C - 42,60; H - 4,60; N - 17,74.
Найдено (%): C - 42,63; H - 4,59; N - 17,86.
Пример 34
2-Амино-4-(2,5-дихлорфенил)-6-пиперазино-1,3,5-триазин
Используя пиперазин вместо диэтиламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 163 - 165oC.
Элементный анализ для C13H14Cl2N6
Вычислено (%): C - 48,01; H - 4,34; N - 25,84.
Найдено (%): C - 47,89; H - 4,21; N - 25,81.
Пример 35
2-Амино-4-(2,5-дихлорфенил)-6-(4-фенил-1-пиперазин-1-ил)- 1,3,5-триазин
Используя N-фенилпиперазин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 203 - 206oC.
Элементный анализ для C19H18Cl2N6
Вычислено (%): C - 56,87; H - 4,52; N - 20,94.
Найдено (%): C - 56,77; H - 4,43; N - 20,85.
Пример 36
2-Амино-4-(2,5-дихлорфенил)-6-(4-гидрокси-1-пиперидинил)- 1,3,5-триазин
Используя 4-гидроксипиперидин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 222 - 224oC.
Элементный анализ для C14H15Cl2N5O
Вычислено (%): C - 49,43; H - 4,44; N - 20,59.
Найдено (%): C - 49,30; H - 4,53; N - 20,44.
Пример 37
2-Амино-4-(2,5-дихлорфенил)-6-(3-гидрокси-1-пиперидинил)- 1,3,5-триазин
Используя 3-гидроксипиперидин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 178 - 180oC.
Элементный анализ для C14H15Cl2N5O
Вычислено (%): C - 49,43; H - 4,44; N - 20,59.
Найдено (%): C - 49,37; H - 4,42; N - 20,57.
Пример 38
2-Амино-4-(2,5-дихлорфенил)-6-тиоморфолино-1,3,5-триазин
Используя тиоморфолин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 239 - 241oC.
Элементный анализ для C13H13Cl2N5S
Вычислено (%): C - 45,62; H - 3,83; N - 20,46.
Найдено (%): C - 45,45; H - 3,66; N - 20,49.
Пример 39
2-Амино-4-(2,5-дихлорфенил)-6-(2,6-диметил-4-морфолинил)- 1,3,5-триазин
Используя 2,6-диметилморфолин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 192 - 195oC.
Элементный анализ для C15H17Cl2N5O
Вычислено (%): C - 50,86; H - 4,84; N - 19,77.
Найдено (%): C - 50,62; H - 4,73; N - 19,99.
Пример 40
2-Амино-4-(2,5-дихлорфенил)-6-[4-[3-(4-метилфенокси)пропил] - 1-пиперазинил]-1,3,5-триазин
Используя N-[3-(4-метилфенокси)пропил] пиперазин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 148 - 150oC.
Элементный анализ для C23H26Cl2N6O
Вычислено (%): C - 58,36; H - 5,54; N - 17,75.
Найдено (%): C - 58,14; H - 5,43; N - 17,82.
Пример 41
2-Амино-4-(2,5-дихлорфенил)-6-(3-пирролин-1-ил)-1,3,5-триазин
Используя 3-пирролин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 205 - 206oC.
Элементный анализ для C13H11Cl2N5
Вычислено (%): C - 50,67; H - 3,60; N - 22,73.
Найдено (%): C - 50,61; H - 3,57; N - 22,69.
Пример 42
2-Амино-4-(2,5-дихлорфенил)-6-(3-оксо-1-пиперазинил)- 1,3,5-триазин
Используя 2-оксопиперазин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. > 275oC.
Элементный анализ для C13H12Cl2N6O
Вычислено (%): C - 46,04; H - 3,57; N - 24,78.
Найдено (%): C - 45,86; H - 3,73; N - 24,60.
H-ЯМР (ДМСО-d6) σ : 3,23 (2H, шс), 3,89 (2H, шс), 4,20 (2H, с), 7,20 (2H, шс), 7,56 (2H, с), 7,73 (1H, с), 8,11 (1H, с).
Пример 43
2-Амино-4-(4-бензил-1-пиперидинил)-6-(2,5-дихлорфенил)-1,3,5-триазин
Используя 4-бензилпиперидиин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 159 - 161oC.
Элементный анализ для C21H21Cl2N5
Вычислено (%): C - 60,88; H - 5,11; N - 16,90.
Найдено (%): C - 60,74; H - 5,09; N - 16,97.
Пример 44
2-Амино-4-(2,5-дихлорфенил)-6-(гексаметиленимин-1-ил)- 1,3,5-триазин
Используя гексаметиленимин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 155 - 156oC.
Элементный анализ для C15H17Cl2N5
Вычислено (%): C - 53,27; H - 5,07; N - 20,71.
Найдено (%): C - 53,17; H - 4,99; N - 20,66.
Пример 45
2-Амино-4-(2,5-дихлорфенил)-6-(2-метил-1-пиперидинил)- 1,3,5-триазин
Используя 2-метилпиперидин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 136 - 137oC.
Элементный анализ для C15H17Cl2N5
Вычислено (%): C - 53,27; H - 5,07; N - 20,71.
Найдено (%): C - 53,81; H - 4,90; N - 20,95.
Пример 46
2-Амино-4-(2-карбокси-4-гидрокси-1-пирролидинил)-6- (2,5-дихлорфенил)-1,3,5-триазин
Используя 4-гидроксипролин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 138 - 145oC.
Элементный анализ для C14H13Cl2N5O3 • H2O
Вычислено (%): C - 43,32; H - 3,89; N - 18,04.
Найдено (%): C - 43,63; H - 3,65; N - 18,17.
Пример 47
2-Амино-4-(2,5-дихлорфенил)-6-(2-гидроксиметил-4-гидркоси- 1-пирролидинил)-1,3,5-триазин
Используя 2-гидроксиметил-4-гидроксипирролидин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение в виде белого порошка.
Элементный анализ для C14H15Cl2N5O2 • 1/2 EtOH • 1/2H2O
Вычислено (%): C - 46,40; H - 4,93; N - 18,04.
Найдено (%): C - 46,36; H - 4,80; N - 18,24.
H-ЯМР (CDCl3) σ : 1,7 - 2,0 (1H, м), 2,1 - 2,25 (1H, м), 2,67 (1H, шс), 3,4 - 3,85 (3H, м), 3,95 - 4,25 (1H, м), 4,35 - 4,55 (2H, м), 5,53 (2H, д, J = 11 Гц), 7,25 - 7,4 (2H, м), 7,65 (1H, д, J = 19 Гц).
Пример 48
Гидрохлорид 2-амино-4-(2,5-дихлорфенил)-6- (3-гидроксиметил-1-пирролидинил)-1,3,5-триазин
Используя 3-гидроксиметилпирролидин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1. Используя получающееся в результате соединение, осуществляют такую же процедуру, как в примере 32 (стадия 2), и получают названное в заголовке соединение.
Т.пл. 241 - 243oC.
Элементный анализ для C14H15Cl2N5O • HCl
Вычислено (%): C - 44,64; H - 4,28; N - 18,59.
Найдено (%): C - 44,47; H - 4,34; N - 18,68.
Пример 49
2-Амино-4-(2,5-дихлорфенил)-6-(4-метансульфонил-1-пиперазинил)- 1,3,5-триазин
Используя 1-метансульфонилпиперазин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 184 - 186oC.
Элементный анализ для C14H16Cl2N6O2S
Вычислено (%): C - 41,70; H - 4,00; N - 20,84.
Найдено (%): C - 41,59; H - 3,85; N - 20,91.
Пример 50
(S)-2-Амино-4-(2-карбокси-1-пирролидини)-6- (2,5-дихлорфенил)-1,3,5-триазин
Используя (S)-пролин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 144 - 147oC.
Элементный анализ для C14H13Cl2N5O2
Вычислено (%): C - 47,47; H - 3,70; N - 19,77.
Найдено (%): C - 47,59; H - 3,88; N - 19,77.
Пример 51
2-Амино-4-(2,5-дихлорфенил)-6-(3-метансульфониламино-1- пирролидинил)-1,3,5-триазин
Используя 3-метансульфониламинопирролидин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 102 - 107oC.
Элементный анализ для C14H16Cl2N6O2S • 1/2CH3OH • 1/2CHCl3
Вычислено (%): C - 39,44; H - 3,98; N - 18,71.
Найдено (%): C - 39,77; H - 3,90; N - 18,77.
Пример 52
2-Амино-4-(2,5-дихлорфенил)-6-(3-гидрокси-1-азетидинил)- 1,3,5-триазин
Используя 3-гидроксиазетидин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 256 - 257oC.
Элементный анализ для C12H11Cl2N5O
Вычислено (%): C - 46,17; H - 3,55; N - 22,44.
Найдено (%): C - 45,93; H - 3,48; N - 22,03.
Пример 53
2-Амино-4-(2,5-дихлорфенил)-6-(3-гидроксиметил-1-азетидинил)- 1,3,5-триазин
Используя 3-гидроксиметилазетидин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 224 - 226oC.
Элементный анализ для C13H13Cl2N5O
Вычислено (%): C - 47,87; H - 4,02; N - 21,47.
Найдено (%): C - 47,67; H - 3,88; N - 21,15.
Пример 54
2-Амино-4-(2-карбокси-1-пиперидинил)-6-(2,5-дихлорфенил)- 1,3,5-триазин
Используя 2-карбоксипиперидин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 237 - 240oC.
Элементный анализ для C15H15Cl2N5O2
Вычислено (%): C - 48,93; H - 4,11; N - 19,02.
Найдено (%): C - 48,58; H - 4,19; N - 18,79.
Пример 55
2-Амино-4-(2,5-дихлорфенил)-6-(4-гидрокси-4-фенил-1- пиперидинил)-1,3,5-триазин
Используя 4-гидрокси-4-фенилпиперидин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 176 - 178oC.
Элементный анализ для C20H19Cl2N5O
Вычислено (%): C - 57,70; H - 4,60; N - 16,82.
Найдено (%): C - 57,54; H - 4,58; N - 16,76.
Пример 56
2-Амино-4-(2,5-дихлорфенил)-6-(4-оксо-1-пиперидинил)- 1,3,5-триазин
Используя 4-оксопиперидин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 223 - 225oC.
Пример 57
2-Амино-4-(2,5-дихлорфенил)-6-(4-гидроксиметил-1- пиперидинил)-1,3,5-триазин
Используя 4-гидроксиметилпиперидин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 173 - 175oC.
Элементный анализ для C15H17Cl2N5O
Вычислено (%): C - 50,86; H - 4,84; N - 19,77.
Найдено (%): C - 50,79; H - 4,80; N - 19,74.
Пример 58
2-Амино-4-(2,5-дихлорфенил)-6-(1-оксотиоморфолин-4-ил)- 1,3,5-триазин
В 150 мл уксусной кислоты растворяют 2,0 г соединения, синтезированного в примере 38. К этому раствору по каплям, при охлаждении льдом, добавляют 1,3 мл 30% водного раствора пероксида водорода, и смесь перемешивают при той же температуре в течение 3 часов. Избыток пероксида водорода разлагают водным раствором сульфита натрия, и смесь концентрируют. Выпавшие кристаллы собирают фильтрацией, промывают водой и сушат, получают 1,86 г названного в заголовке соединения в виде белых кристаллов.
Т.пл. 267 - 269oC.
Элементный анализ для C13H13Cl2N5OS
Вычислено (%): C - 43,58; H - 3,66; N - 19,55.
Найдено (%): C - 43,21; H - 3,58; N - 19,24.
Пример 59
2-Амино-4-(2,5-дихлорфенил)-6-(1,1-диоксотиоморфолин-4-ил)- 1,3,5-триазин
В 150 мл уксусной кислоты растворяют 2,0 г соединения, синтезированного в примере 38. К этому раствору по каплям, при охлаждении льдом, добавляют 2,5 мл 30% водного раствора пероксида водорода, и смесь перемешивают при 50oC в течение 6 часов. Выпавшие кристаллы собирают фильтрацией, промывают метанолом и сушат, получают 1,84 г названного в заголовке соединения в виде белых кристаллов.
Т.пл. > 275oC.
Элементный анализ для C13H13Cl2N5O2S
Вычислено (%): C - 41,72; H - 3,50; N - 18,71.
Найдено (%): C - 41,80; H - 3,50; N - 18,67.
H-ЯМР (ДМСО-d6) σ : 3,1 - 3,25 (2H, м), 4,1 - 4,25 (2H, м), 7,2 - 7,35 (2H, шс), 7,56 (2H, с), 7,73 - 7,75 (1H, м).
Пример 60
1,5-Дидезокси-1,5- [[2-амино-4-(2,5-дихлорфенил)-1,3,5-триазин-6-ил] имино-D-глюцит
Используя 1,5-дидезокси-1,5-имино-D-глюцит вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение в виде белого порошка.
Элементный анализ для C15H17Cl2N5O4 • 1/2C2H5OH • 3/10H2O
Вычислено (%): C - 44,62; H - 4,82; N - 16,26.
Найдено (%): C - 44,65; H - 4,99; N - 16,32.
H-ЯМР (ДМСО-d6) σ : 3,29 - 3,38 (1H, м), 3,49 - 3,54 (1H, м), 3,58 - 3,66 (2H, м), 3,74 - 3,82 (2H, м), 4,45 - 4,57 (2H, м), 4,67 (1H, т, J = 5 Гц), 4,89 - 4,96 (2H, м), 5,19 - 5,21 (1H, м), 6,85 - 7,05 (2H, шс), 7,53 - 7,58 (2H, м), 7,69 - 7,70 (1H, м).
Пример 61
2-Амино-4-(2,5-дихлорфенил)-6-(1-азетидинил)-1,3,5-триазин
Используя азетидинин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 207 - 208oC.
Элементный анализ для C12H11Cl2N5
Вычислено (%): C - 48,67; H - 3,74; N - 23,65.
Найдено (%): C - 48,58; H - 3,66; N - 23,63.
Пример 62
Дигидрохлорид 2-амино-4-(2,5-дихлорфенил)-6-(3-аминометил-1-пирролидинил)- 1,3,5-триазин
Используя 3-(трет-бутоксикарбониламинометил)пирролидин вместо диэтилоламина, осуществляют ту же процедуру, что в примере 1. Получающееся в результате соединение (6,3 г) растворяют в 60 мл метанола, и при перемешивании и охлаждении льдом добавляют 20 мл 30% HCl в CH3OH, и затем перемешивают смесь в течение 2 часов. Образовавшиеся кристаллы собирают фильтрацией, и получают 4,18 г названного в заголовке соединения.
Т.пл. > 275.
Элементный анализ для C14H16Cl2N6 • 2HCl • 2H2O
Вычислено (%): C - 37,52; H - 4,95; N - 18,75.
Найдено (%): C - 37,60; H - 4,96; N - 18,93.
H-ЯМР (ДМСО-d6) σ : 1,7 - 1,95 (1H, м), 2,05 - 2,3 (1H, м), 2,5 - 2,8 (1H, м), 2,92 (2H, шс), 3,25 - 3,45 (1H, м), 3,45 - 3,65 (1H, м), 3,65 - 4,0 (2H, м), 7,68 (2H, с), 7,83 (1H, с), 8,31 (3H, шс).
Пример 63
Гидрохлорид 2-амино-4-(2,5-дихлорфенил)-6-(3-метансульфонил- аминометил-1-пирролидин)-1,3,5-триазин
В 40 мл ТГФ растворяют 2,1 г свободного основания, полученного путем нейтрализации соединения примера 62, после чего добавляют 0,94 г карбоната калия и 0,78 г метансульфонилхлорида. Смесь реагирует при комнатной температуре в течение 20 часов. ТГФ удаляют посредством концентрирования, а остаток разбавляют водой и экстрагируют хлороформом. Экстракт промывают водой и сушат, и отгоняют хлороформ. Остаток очищают колоночной хроматографией на силикагеле (элюирование CHCl3: MeOH = 19:1), получающееся в результате масло обрабатывают таким же способом, как в примере 32 (стадия 2). Получают названное в заголовке соединение.
Т.пл. 220 - 230oC.
Элементный анализ для C15H18Cl2N6O2S • HCl • 1/2H2O
Вычислено (%): C - 38,93; H - 4,36; N - 18,16.
Найдено (%): C - 38,64; H - 4,13; N - 17,92.
Ссылочный пример 4
2-Амино-4-(2,5-дихлорфенил)-6-пиперидино-1,3,5-триазин
Используя пиперидин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 192 - 194oC.
Элементный анализ для C14H15Cl2N5
Вычислено (%): C - 51,87; H - 4,66; N - 21,60.
Найдено (%): C - 51,86; H - 4,65; N - 21,64.
Ссылочный пример 5
2-Амино-4-(2,5-дихлорфенил)-6-морфолино-1,3,5-триазин
Используя морфолин вместо диэтаноламина, осуществляют ту же процедуру, что в примере 1, и получают названное в заголовке соединение.
Т.пл. 189 - 191oC.
Элементный анализ для C13H13Cl2N5O
Вычислено (%): C - 47,87; H - 4,02; N - 21,47.
Найдено (%): C - 47,85; H - 3,92; N - 21,52.
Пример испытаний 1
Противогепатитное действие соединений изобретения можно подтвердить с помощью приведенного далее испытания на мышах. Этот тест является самым обычным испытанием на животных, проводимым для оценки противогепатитного действия лекарственны препаратов. Известно, что оценка противогепатитного действия с помощью этого метода испытаний хорошо коррелирует с клиническими результатами у людей (Kondo, Y., et al., Chem. Pharm. Bull., 38, 2887-2889, 1990).
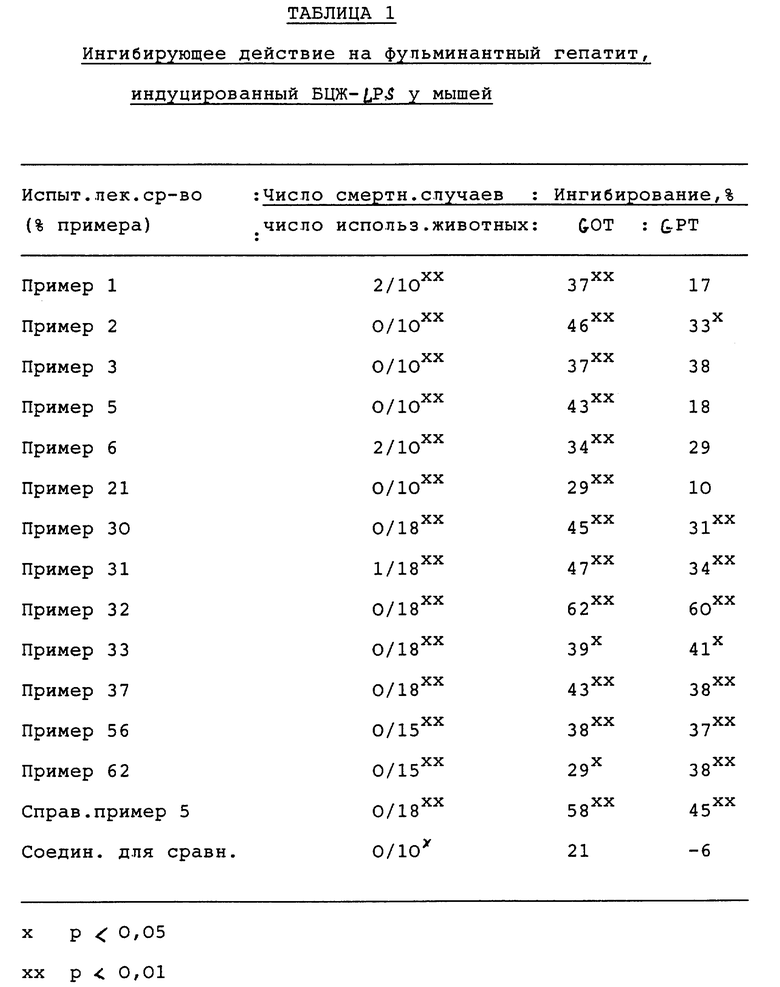
Способ. Самцам мышей BALB/C в возрасте 6 недель дают внутривенно дозу в 1 мг ВЦЖ, и через 2 недели вводят перорально 50 мг/кг испытываемого лекарственного средства. Затем, спустя 1 час, делают внутривенную инъекцию 2,5 мкг липополисахарида (ЛПС), чтобы индуцировать гепатит. Чтобы выявить летальность, связанную с ЛПС, через 48 часов определяют процент смертных случаев. Летальность в контрольной группе составляет 80-100%. Известно, что содержание трансаминаз [аспартатаминотрансферазы GOT), аламинаминотрансферазы (GPT)] в плазме начинает возрастать примерно через 8 часов после введения ЛПС, и 4 часов недостаточно для оценки. Однако, для сравнения, отбирают кровь из орбитальной вены через 4 часа, и определяют концентрацию трансаминаз (GOT, DTP) в плазме. В качестве соединения для сравнения используют 2,4-диамино-6-(2,5-дихлорфенил)-1,3,5-триазин. Результаты приводятся в табл. 1.
Соединения настоящего изобретения показывают, по существу, такое же препятствующее гибели действия, как соединение для сравнения, и ингибируют, в заметной степени, повышение уровня трансаминаз в сыворотке, который является индикатором нарушений в печени.
Таким образом, соединения настоящего изобретения обладают противогепатитной активностью и являются, следовательно, пригодными для лечения и профилактики гепатита.
Пример испытаний 2.
Ингибирующее действие на печеночный хемоонкогенез
Способ. На самцах крыс F344 (Slc) в возрасте 5 недель создают модель предрака, используя приведенную в конце текста схему, в соответствии со способом Solt и Faber (Nature, 263, 702 - 703, 1976).
Таким образом, за время эксперимента, которое установлено в 4 недели, сначала вводят внутрибрюшинно 200 мг/кг диэтилнитрозоамина (далее для кракности называемого DEN). Начиная со 2 недели, дают, неограниченно, питьевую воду, содержащую 0,02% 2-ацетиламинофлуорена (далее для кратности называемого AAF). В начале 3 недели выполняют 70% гепатэктомию. Проверяемое лекарственное средство подмешивают в пищу животных (F-2, Funabashi Farm) при концентрации 0,01%, и дают со 2 недели и до последнего дня эксперимента. В качестве проверяемого соединения используют соединение примера 1, а в качестве соединения (стандартного) используют 2,4-диамино-6-(2,5-дихлорфенил)-1,3,5-триазин.
В последний день эксперимента всех животных умерщвляют посредством цервикальной дисклокации под эфирным наркозом. Сразу же иссекают часть печени, быстро замораживают в ацетоне со льдом и хранят до использования. Препарируют из печени замороженные срезы толщиной 8 мкм, и используя набор вектастатина ABC (Funakoshi Yakuhin), окрашивают иммунно по методу ABC (метод с меченными ферментом антителами), используя антитело антиглутатион-S-трансферазной плацентарной формы (далее для кратности называемое DST-P) в качестве первичного антитела. Итак, срезы в отсутствие воды возвращают к условиям комнатной температуры и погружают в 10 мМ забуференный фосфатом физиологический раствор (далее для краткости называемый ЗФР), pH 7,2, на 15 минут. Затем на срез наносят сыворотку здоровой козы и первичное антитело (разведение 500, 20 мкл), и дают возможность реагировать в течение ночи. После реакции срез промывают ЗФР. Затем применяют антикроличье вторичное антитело, и осуществляют реакцию в течение 30 минут. После промывания ЗФР вводят авидин-биотиновый комплекс, и дают возможность реагировать в течение 30 минут. Срез промывают ЗФР и обрабатывают 0,1% диаминобензидином (DAB), содержащим 0,02% пероксида водорода, для проявления окрашивания, обезвоживают и закрывают.
Под оптическим микроскопом подсчитывают число позитивных к GST-P повреждений на см2 среза печеночной ткани, и измеряют площадь с помощью анализатора изображения (SPICCA-II, Japan Avionics). Удовлетворительная проверка средних значений осуществляется при обучении студентов, и результат оценивается при 5% уровне достоверности. Результаты приводятся в табл. 2.
Соединения настоящего изобретения, при концентрации 0,01%, снижает число и площадь GST-P-позитивных повреждений. Степень ингибирования составляет 28,9% и 48,6%, соответственно. С другой стороны, 0,01% стандартного соединения не показывает ингибирующего действия на число GST-P-позитивных повреждений или на площадь повреждений (степень ингибирования 7,7%).
Тест-пример 3
Острая токсичность
Используют крыс любого пола (линия SD, 280 - 360 мг) в группах по 5 особей. Накануне испытаний (за 16 - 18 часов) животных лишают пищи, и вводят перорально, посредством желудочного зонда, 1 г/кг соединения примера 1. Затем регистрируют смертные случаи в течение последующей одной недели. В результате не отмечается ни одного смертного случая.
Таким образом, токсичность соединения изобретения является очень низкой.
Тест-пример 4
Влияние на прибавление в весе
Соединение примера 1 ежедневно вводят крысам, чтобы исследовать его влияние на прибавление в весе. Даже при повторном введении 1000 мг/кг соединение настоящего изобретения не влияет на прибавление в весе.
Пример состава 1
Соединение примера 1 (2 г) тщательно смешивают с 70 г лактозы и 30 г кукурузного крахмала. После добавления 25 мл 16% раствора гидроксипропилцеллюлозы смесь перемешивают и гранулируют. Полученные таким образом гранулы сушат, просеивают, и смешивают с 2 г стеарата магния и 2 г талька, и всю композицию прессуют на роторной таблетирующей машине. Получают таблетки.
Состав: 110 мг на таблетку
Соединение примера 1 - 2 мг
Лактоза - 70 мг
Кукурузный крахмал - 30 мг
Гидроксипропилцеллюлоза - 4 мг
Стеарат магния - 2 мг
Тальк - 2 мг
Пример состава 2
К 4 мг соединения примера 1 добавляют 996 мг лактозы, и смесь равномерно перемешивают, чтобы получить порошок.
Промышленное применение
Соединения настоящего изобретения обладают сильной противогепатитной активностью, так же, как и активностью ингибирования печеночного онкогенеза, которая не обнаруживается в стандартном лекарственном средстве ильзогладинмалеате, и являются безопасными соединениями с низким потенциалом токсичности. Следовательно, соединения являются пригодными в качестве лекарственных средств для лечения и профилактики гепатита у млекопитающих, включая человека.


Изобретение относится к лекарственным композициям, содержащим в качестве активного ингредиента производное триазина следующей общей формулы I или его сольват, или его соль, и производным триазина. В вышеупомянутой формуле R1 и R2 могут быть одинаковыми или различными, и каждый из них представляет собой водород, незамещенный или замещенный алкил, аралкил, или алкенил, или вместе, в сочетании с соседним атомом азота, представляют собой циклическую аминогруппу NR1R2. Циклическая аминогруппа может содержать в качестве атома кольца, кроме соседнего атома N, азот, кислород или серу, и также может быть замещенной. Исключается случай, когда NR1R2 представляет собой NH2. Соединения изобретения пригодны в качестве лекарственных средств против гепатита, расширяют арсенал лекарственных средств против гепатита и обладает низкой токсичностью для теплокровных. 2 с. и 5 з.п. ф-лы, 1 ил., 2 табл.
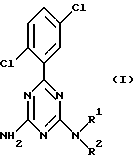

где R1 и R2 могут быть одинаковыми или различными, и каждый из них представляет водород, незамещенный или замещенный алкил, аралкил, аралкенил или арил, или R1 и R2 вместе с соседним атомом N представляют собой 4 - 8-членную циклическую аминогруппу формулы NR1R2, циклическая аминогруппа может содержать в качестве атома кольца, кроме вышеупомянутого атома N, азот, кислород или серу, а также может быть замещенной при условии, что исключают случай, когда как R1, так и R2 представляют собой водород, его соль или его сольват в качестве активного ингредиента в эффективном количестве.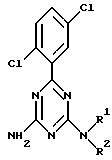
где R1 и R2 могут быть одинаковыми или различными, и каждый из них представляет водород, незамещенный или замещенный алкил, аралалкил, аралкенил или арил, или R1 и R2 вместе с соседним атомом N, представляют собой 4 - 8-членную циклическую аминогруппу формулы NR1R2, циклическая аминогруппа может содержать в качестве атома кольца, кроме вышеупомянутого атома N, азот, кислород или серу, а также может быть замещенной, при условии, что исключают случай, когда как R1, так и R2 представляют собой водород, и случай, когда NR1R2 представляют незамещенную пиперидино или морфолино группу, его соль или сольват.
| Огнетушитель | 0 |
|
SU91A1 |
| US 4333933 A, 08.06.82 | |||
| US 4554275 A, 19.11.85 | |||
| Машковский М.Д | |||
| "Лекарственные средства", М., Медицина, 1986, с.46. | |||
Авторы
Даты
2000-04-10—Публикация
1995-08-08—Подача