Настоящее изобретение относится к новым гетероциклическим соединениям или их солям, которые могут применяться в качестве лекарственного средства.
Предпосылки создания изобретения
Известно, что в качестве противоракового агента могут применяться гетероциклические соединения приведенной ниже формулы (WО 95/027699):
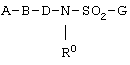
где А обозначает необязательно замещенный гетероарил или его оксид, В обозначает необязательно замещенный этенилен, D обозначает необязательно замещенный фенилен, G обозначает необязательно замещенный фенил, a R0 обозначает водород, ацетил, необязательно замещенный алкил или необязательно замещенный алкенил.
Известно также, что 1-оксид (Е)-4-(2-(2-(N-(4-метоксибензолсульфонил)амино)фенил)этенил)пиридина (далее упоминаемый как соединение А) обладает мощной активностью, направленной на ингибирование роста раковых клеток, и что 1-оксид (Е)-4-(2-(2-(N-(4-ацетил-N-(4-метоксибензолсульфонил) амино)фенил)этенил)пиридина (далее упоминаемый как соединение В) обладает противораковой активностью при низкой токсичности. Соответственно предполагалось, что соединения А и В являются многообещающими лекарственными средствами для перорального введения при лечении различных злокачественных опухолей, таких, как рак легких, рак молочной железы, рак желудочно-кишечного тракта, рак простаты, рак крови и т.п.
Хотя соединения А и В являются подходящими для перорального введения, они вряд ли могут использоваться для внутривенной инъекции или т.п. из-за крайне низкой растворимости в растворах для инъекций.
Абсорбция противораковых агентов при пероральном введении иногда варьируется в зависимости от субъекта; и, следовательно, с точки зрения надежности, точности и безопасности, для лечения рака в основном применяется внутривенное введение. Внутривенная инъекция является подходящей, если для пациента нельзя применять пероральное введение. В свете вышесказанного в области клинической медицины существует потребность в противораковых агентах, которые можно применять в виде инъекции.
Описание изобретения
Целью настоящего изобретения являются новые соединения, обладающие мощной противораковой активностью, которые являются водорастворимыми и пригодными для инъекций.
Авторы настоящего изобретения синтезировали и исследовали различные соединения, в процессе чего они обнаружили, что среди них соединения формулы [I], приведенной ниже, являются водорастворимыми и обладают крайне высокой противораковой активностью, и, таким образом, осуществили настоящее изобретение.
Настоящее изобретение относится к нижеследующим пунктам (1)-(10).
(1) Соединение формулы [I] или его соль
A-B-D-E [1]
где
А обозначает необязательно замещенный гетероарил или его оксид;
В обозначает необязательно замещенный этенилен;
D обозначает необязательно замещенный фенилен; и
Е обозначает группу формулы
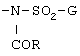
где G обозначает необязательно замещенный фенил; и R обозначает необязательно замещенный гетероарил или гетероарилметил, или группу формулы
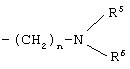
где n представляет собой целое число от 1 до 5; R5 и R6 являются одинаковыми или разными и независимо выбраны из группы, состоящей из водорода, C1-С6 алкила, гидроксиалкила, аминоалкила; или R5 и R6, взятые вместе с соседним атомом азота, могут образовывать 5-7-членную циклическую аминогруппу –NR5(R6), которая может быть необязательно замещена и кроме атома азота может необязательно включать атом кислорода, серы или азота в качестве образующего цикл члена.
(2) Соединение формулы [I], упомянутое в приведенном выше пункте (1), или его соль, где А обозначает 4-пиридил или 1-оксидо-4-пиридил; В обозначает этенилен; D обозначает необязательно замещенный фенилен; и Е обозначает группу формулы
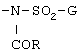
где R и G являются такими, как определено в пункте 1.
(3) Соединение формулы [I], упомянутое в приведенном выше пункте (1), или его соль, где А обозначает 4-пиридил или 1-оксидо-4-пиридил; В обозначает этенилен; D обозначает необязательно замещенный фенилен; и Е обозначает группу формулы
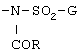
где G обозначает необязательно замещенный фенил, а R обозначает группу формулы
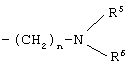
где n, R5 и R6 являются такими, как определено в пункте 1.
(4) Соединение, упомянутое в приведенном выше пункте (3), или его соль, где R5 и R6 являются одинаковыми или разными и независимо выбраны из группы, состоящей из водорода, C1-С6 алкила; или R5 и R6, взятые вместе с соседним атомом азота, могут образовывать необязательно замещенную 5-6-членную циклическую аминогруппу -NR5(R6).
(5) Соединение формулы [I], упомянутое в приведенном выше пункте (1), или его соль, где А обозначает 4-пиридил или 1-оксидо-4-пиридил; В обозначает этенилен; D обозначает фенилен; и Е обозначает группу формулы
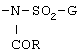
где G обозначает необязательно замещенный фенил; а R обозначает необязательно замещенный 5-6-членный гетероарил или гетероарилметил.
(6) Соль, упомянутая в приведенном выше пункте (1), где солью является гидрохлорид.
(7) Фармацевтическая композиция, включающая в качестве активного ингредиента соединение формулы [I], упомянутое выше в пункте (1), или его соль.
(8) Фармацевтическая композиция по упомянутому выше пункту (7), которая находится в виде инъекционной формы.
(9) Противораковый агент, включающий в качестве активного ингредиента соединение формулы [I], упомянутое выше в пункте (1), или его соль.
(10) Противораковый агент по упомянутому выше пункту (9), который находится в виде инъекционной формы.
Структурной особенностью соединения настоящего изобретения является то, что фенил в стилбазольном ядре несет аминоациламиногруппу, или гетероароиламиногруппу, или гетероароиламинометильную группу, содержащую атом азота.
Соединение, имеющее указанную выше структурную особенность, является новым соединением, никогда ранее не описанным. Соединение настоящего изобретения имеет превосходную противораковую активность и низкую токсичность.
Далее настоящее изобретение будет описано подробно.
Термины, используемые в данном описании для обозначения различных заместителей, определены ниже.
Примеры "фениленовой" группы включают 1,2-фенилен, 1,3-фенилен и 1,4-фенилен. Фениленовая группа может иметь один или два заместителя в произвольных положениях, примеры которых включают гидрокси, галоген, амино, C1-C6 алкил и C1-С6 алкокси. Среди прочих предпочтительным является необязательно замещенный 1,2-фенилен, особенно незамещенный 1,2-фенилен.
Этениленовая группа может иметь заместитель(и) при каждом атоме углерода, примеры которого включают циано, бром и C1-С6 алкил. Среди прочих предпочтительным является необязательно замещенный этенилен, особенно незамещенный этенилен.
Термин "гетероарил" относится к 5-6-членной гетероарильной группе, имеющей от одного до двух атомов азота в качестве образующих цикл членов. Гетероарильная группа необязательно имеет один или два заместителя в произвольных положениях, примеры которых включают галоген, C1-С6 алкил, C1-С6 алкокси, гидрокси и C1-С6 аминоалкил. Гетероарил для А включает 6-членный гетероарил, например 2-пиридил, 3-пиридил, 4-пиридил, 2-пиримидинил, 4-пиримидинил, 5-пиримидинил, 3-пиридазинил, 4-пиридазинил и пиразинил. Среди прочих предпочтительным является незамещенный 4-пиридил. Гетероарил для R включает 5-6-членный гетероарил, например 2-пиридил, 3-пиридил, 4-пиридил, 2-пиримидинил, 4-пиримидинил, 5-пиримидинил, 3-пиридазинил, 4-пиридазинил, 1-имидазолил, 2-имидазолил и 4-имидазолил.
Термин "алкил" относится к линейной или разветвленной алкильной группе из 1-6 атомов углерода и включает, например, метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, н-пентил, изопентил, н-гексил, изогексил и т.п. Среди прочих предпочтительным является C1-С3 алкил, особенно метил.
Алкильный фрагмент "гидроксиалкила" и "аминоалкила" является таким, как определено выше.
Примеры "циклической аминогруппы" включают, например, пирролидин-1-ил, пиперидино, гексаметиленимино, тетрагидропиридин-1-ил, октагидроазозин-1-ил, пиперазин-1-ил, гомопиперазин-1-ил, морфолино и тиоморфолино. Циклическая аминогруппа может иметь один или два заместителя, выбранных из группы, состоящей из алкила, алкенила, алкинила, арила, аралкила и гетероциклической группы, имеющей атом азота в любом положении. Среди прочих предпочтительными являются незамещенный пирролидин-1-ил, пиперидино, морфолино, а также пиперазин-1-ил, замещенный пиридилом.
Примеры "галогена" включают фтор, хлор, бром, иод.
"Фенильная" группа может иметь один или два заместителя, например гидрокси или C1-C6 алкокси. Среди прочих предпочтительным является фенил, замещенный алкокси, особенно 4-метоксифенил.
Алкилен, представленный "-(CH2)n-", может иметь заместитель, выбранный из группы, состоящей из амино или C1-С6 алкила, в любом положении.
Термин "алкокси" относится к линейной или разветвленной алкоксильной группе из 1-6 атомов углерода и включает, например, метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси, втор-бутокси, трет-бутокси, н-пентилокси, изопентилокси, н-гексилокси, изогексилокси и т.п. Среди прочих предпочтительным является C1-С3 алкокси, особенно метокси.
Термин "алкенил" относится к линейной или разветвленной алкенильной группе из 2-6 атомов углерода и включает, например, винил, 1-пропенил, 2-пропенил, изопропенил, 2-бутенил, 3-бутенил, изобутенил, металил, пренил, изопренил, 1,1-диметилаллил и т.п. Особенно предпочтительным является С2-С4 алкенил.
Термин "алкинил" относится к линейной или разветвленной алкинильной группе из 2-6 атомов углерода и включает, например, этинил, 1-пропинил, 2-пропинил, 2-бутинил, 3-бутинил, 3-метил-2-бутинил и т.п. Особенно предпочтительным является С2-С4 алкинил.
Термин "арил" относится к арилу из 6-10 атомов углерода, например фенилу, 1-нафтилу и 2-нафтилу.
Термин "аралкил" относится к аралкилу из 7-8 атомов углерода, например, бензилу и фенетилу.
Термин "гетероцикл, имеющий атом азота", относится к вышеупомянутым циклической аминогруппе или гетероарилу. Такой гетероцикл может иметь один или два заместителя, выбранных из группы, состоящей из алкила, амино, гидрокси и оксо.
Соли соединения [1], которые попадают в объем данного изобретения, включают фармацевтически приемлемые соли, образованные неорганическими кислотами, такими, как хлористоводородная кислота, серная кислота, азотная кислота, фосфорная кислота, фтористоводородная кислота и бромисто-водородная кислота; органическими кислотами, такими, как уксусная кислота, винная кислота, молочная кислота, лимонная кислота, фумаровая кислота, малеиновая кислота, янтарная кислота, метансульфоновая кислота, этансульфоновая кислота, бензолсульфоновая кислота, толуолсульфоновая кислота, нафталинсульфоновая кислота и камфорсульфоновая кислота.
Соединение настоящего изобретения может существовать в цис- (Z) и транс- (Е) формах. Соответствующие изомеры и их смеси также попадают в объем настоящего изобретения. Среди прочих предпочтительной является Е-форма.
Среди соединений данного изобретения формулы [I] предпочтительными являются соединения, в которых А обозначает необязательно замещенный пиридил или 1-оксидопиридил, особенно незамещенный 4-пиридил или 1-оксидо-4-пиридил; В обозначает этенилен в транс-форме, особенно незамещенный этенилен в транс-форме; D обозначает незамещенный 1,2-фенилен; и Е обозначает 4-замещенный фенил, причем предпочтение отдается 4-алкоксифенилу, особенно 4-алкоксифенилу.
Для настоящего изобретения предпочтительными являются гидрохлорид 1-оксида (Е)-4-(2-(2-(N-(4-метоксибензолсульфонил)-N-пиперидиноацетиламино)фенил)этенил)пиридина (соединение примера 5), гидрохлорид 1-оксида (Е)-4-(2-(2-(N-(N,N-диметилглицил)-N-(4-метоксибензолсульфонил)амино)-фенил)этенил)пиридина (соединение примера 8), дигидрохлорид 1-оксида (Е)-4-(2-(2-(N-(4-метоксибензолсульфонил)-N-(4-(2-пиридил)пиперазино)ацетиламино)фенил)этенил)пиридина (соединение примера 9), гидрохлорид 1-оксида (Е)-4-(2-(2-(N-(4-метоксибензолсульфонил)-N-морфолиноацетиламино)фенил)-этенил)пиридина (соединение примера 13) и гидрохлорид 1-оксида (Е)-4-(2-(2-(N-(4-метоксибензолсульфонил)-N-пирролидиноацетиламино)фенил)этенил)пиридина (соединение примера 14).
Соединение настоящего изобретения может быть синтезировано в соответствии со способами, иллюстрируемыми ниже.
Способ 1
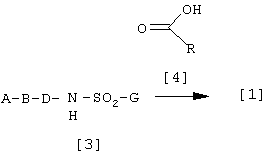
где А, В, D, G и R такие, как определены выше.
Соединение [3] и карбоновую кислоту [4] подвергают реакции прямой конденсации, используя конденсирующий агент в соответствии с известным per se способом, получая соединение [1]. Реакция может быть проведена в присутствии такого конденсирующего агента, как N,N-дициклогексилкарбодиимид (DCC), карбонилдиимидазол или дифенилфосфорилазид (DPPA), в подходящем растворителе (например, в галогенированных углеводородах, таких как метиленхлорид и хлороформ; в простых эфирах, таких как тетрагидрофуран и диоксан; ацетонитриле; N,N-диметилформамиде (DMF) или т.п.), при температуре приблизительно от -30 до 180°С. При необходимости в качестве катализатора можно использовать 4-диметиламинопиридин (DMAP) или 4-пирролидинопиридин (4-PPY). При использовании 1 моль соединения [3] можно использовать эквимолярное количество или небольшой избыток соединения [4] и конденсирующего агента (например, DCC). Если используют катализатор, его количество может составлять от 0,1 до 1 моль на один моль соединения [3]. Время реакции зависит от природы веществ, растворителя, температуры реакции и т.п., применяемых в реакции, но обычно составляет приблизительно от 5 минут до 70 часов.
Альтернативно, соединение [1] может быть получено взаимодействием соединения [3] с реакционноспособным производным карбоновой кислоты [4] в соответствующем растворителе. Растворителем, используемым для реакции, может быть растворитель любого вида, который не препятствует протеканию реакции, например простые эфиры, такие как тетрагидрофуран, диоксан и диэтиловый эфир; углеводороды, такие, как бензол и толуол; галогенированные углеводороды, такие, как метиленхлорид и хлороформ; кетоны, такие, как ацетон и метилэтилкетон; апротонные растворители, такие, как N,N-диметилформамид (DMF), N,N-диметилацетамид, пиридин или ацетонитрил, или различные смеси таких растворителей. Реакционноспособное производное карбоновой кислоты включает традиционно используемые производные, такие, как ацилгалогениды, ангидриды карбоновых кислот, активированные амиды и активированные эфиры. В основном, предпочтительными являются ацилгалогениды. Такие ацилгалогениды включают ацилхлориды и ацилбромиды. Ангидриды кислот включают смешанные ангидриды, полученные из моноалкилугольных кислот, и смешанные ангидриды, полученные из алифатических карбоновых кислот (например, уксусной кислоты, трет-бутилкарбоновой, триметилуксусной кислоты, валериановой кислоты, изовалериановой кислоты, трифторуксусной кислоты и др.), а также симметричные ангидриды.
Активированные амиды включают такие амиды кислот, как имидазол, пиразол, 4-замещенный имидазол, диметилпиразол, триазол, тетразол и бензотиазол. Активированные эфиры включают такие сложные эфиры, как метиловый эфир, метоксиметиловый эфир, пропаргиловый эфир, 4-нитрофениловый эфир, 2,4-динитрофениловый эфир, трихлорфениловый эфир, метансульфониловый эфир, N-гидроксисукцинимид и N-гидроксифталимид.
Если в способе настоящего изобретения используют ацилгалогенид, предпочтительно реакцию проводят в присутствии подходящего основания. Примеры такого основания включают соединения щелочных металлов, такие, как карбонат калия, гидроксид натрия, гидроксид калия, гидрид натрия и метилат натрия, а также органические третичные амины, такие, как пиридин, триэтиламин и триэтилендиамин. Во многих случаях реакция может протекать при комнатной температуре, но при необходимости она может проводиться при охлаждении или нагревании, в температурном интервале от -78 до 150°С, предпочтительно, от 0 до 120°С. Количество соединения [4] на 1 моль соединения [3] составляет предпочтительно от 1 до 10 молярных эквивалентов и более предпочтительно от 1 до 3 молярных эквивалентов. Время реакции зависит от применяемых исходных соединений, растворителя, температуры реакции и т.п., но обычно оно составляет приблизительно от 5 минут до 70 часов. Соединение [1] также может быть получено по реакции Митсунобу (Mitsunobu) (см. Synthesis 981,1).
Способ 2
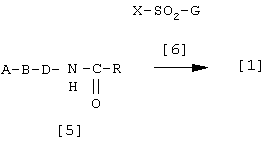
где А, В, D, R и G такие, как определены выше, и Х представляет галоген.
Соединение [1] настоящего изобретения может быть получено взаимодействием соединения [5] с соединением [6] в соответствующем растворителе. Реакция может быть проведена по существу способом, используемым для проведения реакции между реакционноспособным производным карбоновой кислоты и соединением [3] в способе 1, описанном выше.
Полученное таким образом соединение [1] может быть выделено и очищено известными per se методами, такими, как концентрирование, регулирование рН, перераспределение, экстракция растворителем, кристаллизация, перекристаллизация, фракционная перегонка и хроматография.
Исходное соединение [3] может быть получено в соответствии с известным способом (WO 95/27699).
Исходное соединение формулы [4], в котором R обозначает -(CH2)n-NR5R6 (соединение [4а]), в числе прочих может быть получено по реакционной схеме, приведенной ниже, как описано далее в данном документе в справочном примере.
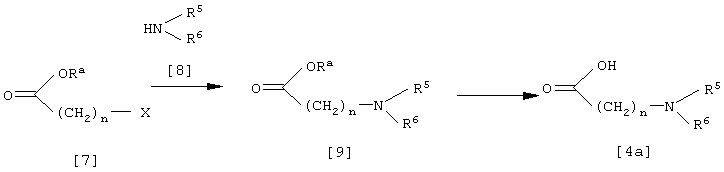
где R5, R6, n и X такие, как определены выше, a Ra обозначает защитную группу для гидроксильной группы.
Что касается исходных соединений формулы [4], в которых R обозначает гетероарил или гетероарилметил, в числе прочих коммерчески доступными могут быть гетероарильные карбоновые кислоты или гетероарильные уксусные кислоты, или их производные, или те, которые могут быть получены из существующих соединений в соответствии с известным per se способом.
Исходные соединения [5] могут быть получены в соответствии с нижеследующей схемой реакции.
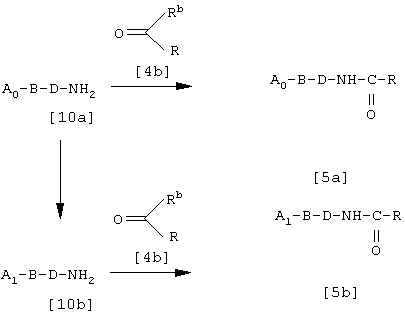
где В, D и R такие, как определены выше; A0 обозначает гетероарил, соответствующий A; A1 обозначает оксид А0; а Rb обозначает уходящую группу.
Примеры уходящих групп включают хлор, бром, иод, гидроксильную группу, алкоксикарбонилоксильную группу и т.п.
Соединение [10а] взаимодействует с соединением [4b] в соответствующем растворителе с получением соединения [5а], соответствующего соединению формулы [5], в котором А обозначает гетероарил. По существу реакция может быть проведена способом, используемым в описанном выше способе 1. Соединение [10а] может быть превращено в оксид [10b] взаимодействием с органическим пероксидом способом, известным из литературы (Jikken Kagaku Koza 21, Yukikagobutsu-no-Gosei III (Part 2), p.295, 1958), после чего его подвергают взаимодействию с соединением [4b], в результате получают соединение [5b], соответствующее соединению формулы [5], в котором А обозначает оксид или гетероарил.
Соединения, в которых R обозначает -(СН2)n-NR5R6, также могут быть получены в соответствии со следующей схемой реакции:
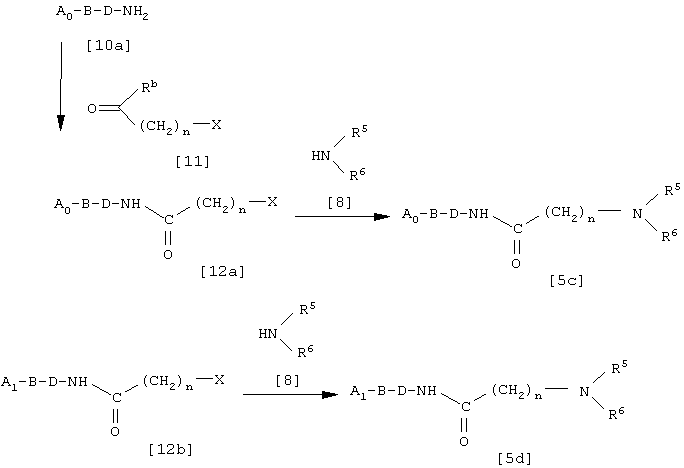
где A0, A1, В, D, R5, R6, n, Х и R13 такие, как определены выше.
Соединение [12а] может быть получено взаимодействием соединения [10а] с соединением [11] в соответствующем растворителе способом 1; однако, если соединение [11] является реакционноспособным производным карбоновой кислоты, требуется присутствие основания. Соединение [12а] взаимодействует с амином [8] в соответствующем растворителе, необязательно в присутствии основания, при температуре от 0 до 160°С, предпочтительно от 10 до 120°С, с получением соединения [5с], соответствующего соединению формулы [5], в котором R обозначает -(СН2)n-NR5R6 и А обозначает гетероарил. При желании соединение [12а] может быть подвергнуто взаимодействию с органическим пероксидом способом, описанным в литературе (Jikken Kagaku Koza 21, Yukikagobutsu-no-Gosei III (Part 2), p.295, 1958), с получением оксида [12b], который в свою очередь взаимодействует с соединением [8] способом, используемым для проведения реакции между соединением [8] и соединением [12а] с получением соединения [5d], соответствующего соединению формулы [5], в котором R обозначает -(CH2)n-NR5R6 и А обозначает оксид гетероарила.
Соединение [5d] может быть также получено в соответствии с нижеследующей схемой реакции.
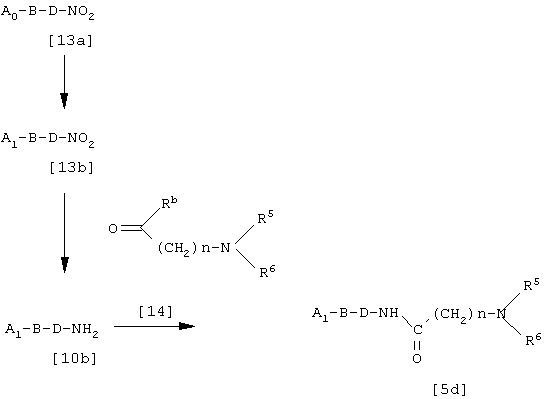
где A0, A1, В, D, R5, R6, n и R13 такие, как определены выше.
Соединение [13а] превращают в соединение [13b] способом, используемым для превращения соединения [12а] в соединение [12b]. Затем соединение [13b] восстанавливают способом, известным из литературы (Shin-Jikken Kagaku Koza 14, Yukikagobutsu-no-Gosei, (Part 3), p.1333, 1978), получая соединение [10b]. Соединение [10b] и соединение [14] взаимодействуют способом, используемым для проведения реакции между соединением [10b] и [4b], с получением соединения [5d].
Исходные соединения [4b] и [11] либо являются коммерчески доступными, либо их получают способом из справочного примера.
Исходные соединения [6], [7] и [8] являются коммерчески доступными.
Исходное соединение [10a] может быть получено способом, описанным в WO 95/27699.
В описанных выше способах перед вступлением соединений в реакцию аминогруппа или гидроксильная группа может быть необязательно защищена традиционной защитной группой. Удаление защитной группы может проводиться на соответствующей стадии с помощью известного per se способа, такого, как обработка кислотой, обработка щелочью или каталитическое восстановление.
Примеры аминозащитных групп включают бензил, бензилоксикарбонил и трифторацетил. Примеры гидроксизащитных групп включают метоксиметил. 2-метоксиэтоксиметил, метилтиометил, тетрагидропиранил, трет-бутил, бензил, триметилсилил и трет-бутилдиметилсилил.
Соли соединений [1] настоящего изобретения могут быть получены известным per se способом. Например, гидрохлориды соединений [1] настоящего изобретения могут быть получены обработкой соединения [1] раствором хлористого водорода в спирте или этиловом эфире и выделением кристаллических осадков фильтрацией. В случае небольшого количества кристаллических осадков или их отсутствия раствор можно концентрировать и выпавшие кристаллы отфильтровать.
Если соединение настоящего изобретения вводят в качестве лекарственного средства, оно может быть непосредственно введено млекопитающим, включая человека, или в виде фармацевтической композиции, содержащей соединение в фармацевтически приемлемом нетоксичном и инертном носителе в концентрации, составляющей, например, от 0,1 до 99,5%, предпочтительно от 0,5 до 90%.
Примеры применяемых носителей включают твердые, полутвердые или жидкие разбавители, наполнители, а также другие вспомогательные средства для композиций, причем применяется по меньшей мере один из них. Фармацевтическую композицию предпочтительно вводят в дозированной лекарственной форме. Соединение настоящего изобретения является водорастворимым и может использоваться в виде растворов (например, раствора для инъекций для внутривенного введения или введения внутрь мочевого пузыря, или сиропа для перорального введения), а также в твердой форме. Фармацевтическая композиция настоящего изобретения может быть введена в ткани (далее в данном описании упоминается как "парентеральное введение"), перорально, местно (например, чрескожно) или ректально. Конечно, применяется дозированная форма, подходящая для каждого способа введения. Например, внутривенное введение является особенно предпочтительным.
Дозу соединения как противоракового средства предпочтительно следует определять в зависимости от таких параметров пациента, как возраст, масса тела, природа и тяжесть заболевания, а также от способа введения; однако ежедневная доза соединения настоящего изобретения как активного ингредиента при внутривенном введении для взрослых, как правило, может составлять 0,1 - 1000 мг, предпочтительно, 1 - 500 мг. Приведенный выше интервал дозы не является обязательным, и в некоторых случаях может быть достаточен более низкий уровень дозы, тогда как в других случаях может потребоваться доза, превышающая верхний предел указанного интервала. Ежедневную дозу, как правило, предпочтительно вводят в один прием. Композицию настоящего изобретения также можно вводить непрерывно или периодически.
Парентеральное введение можно осуществлять с использованием жидкой дозированной лекарственной формы, такой, как раствор для подкожного, внутримышечного или внутривенного введения. Такая дозированная форма может быть получена путем растворения предварительно определенного количества соединения в нетоксичной жидкой среде для инъекции, такой, как водная или масляная среда, и стерилизации раствора. Альтернативно, она может быть получена путем помещения предварительно определенного количества соединения в каждый флакон, стерилизации флакона и содержимого и герметизации флакона. Для растворения или смешивания для немедленного приема порошкообразное или лиофилизированное активное соединение может поставляться вместе с дополнительным флаконом и средой. Для получения изотонического раствора для инъекции может быть добавлена нетоксичная соль или солевой раствор. Кроме того, вместе с соединением могут также использоваться стабилизаторы, консерванты, эмульгаторы и другие добавки.
Пероральное введение можно осуществлять с использованием твердой или жидкой дозированной лекарственной формы, такой, как нерасфасованные порошки, порошки, таблетки, драже, капсулы, гранулы, суспензии, растворы, сиропы, капли, подъязычные таблетки, свечи и другие формы. Нерасфасованные порошки получают измельчением активного вещества до получения частиц подходящего размера. Порошки получают измельчением активного вещества до получения частиц подходящего размера и смешиванием полученного порошка с подобным образом измельченными фармацевтическими носителями, такими, как пищевые углеводы, например крахмал, маннит и т.п., и с другими веществами, если требуется их присутствие. При необходимости могут быть добавлены ароматизаторы, консерванты, диспергирующие средства, красители, отдушки и др.
Капсулы получают в промышленности путем заключения измельченных нерасфасованных частиц, порошков или гранул, полученных способом, описанным ниже для таблеток, в желатиновые или другие капсульные оболочки. К порошкообразным веществам перед капсулированием могут быть добавлены смазывающее средство или разрыхляющий агент например, коллоидный оксид кремния, тальк, стеарат магния, стеарат кальция, твердый полиэтиленгликоль и т.п. Медицинская эффективность капсулы после проглатывания может быть улучшена добавлением дезинтегрирующего или солюбилизирующего средства, например карбоксиметилцеллюлозы, кальциевой соли карбоксиметилцеллюлозы, гидроксипропилцеллюлозы с низкой степенью замещения, натриевой соли кроскармелозы, натриевой соли карбоксикрахмала, карбоната кальция и карбоната натрия.
Мелкоизмельченный порошок можно суспендировать и диспергировать в растительном масле, полиэтиленгликоле, глицерине или поверхностно-активном веществе и упаковывать в желатиновую оболочку с получением мягких капсул. Таблетки могут быть получены гранулированием и формованием порошкообразной композиции, добавлением к ней дезинтегрирующего или смазывающего агента и прессованием смеси. Порошкообразная композиция может быть получена смешиванием подходящим образом измельченного вещества с разбавителем или основой, упомянутыми выше, которые могут дополнительно содержать при необходимости связующее средство (например, натриевую соль карбоксиметилцеллюлозы, гидроксипропилцеллюлозу, метилцеллюлозу, гидроксипропилметилцеллюлозу, желатин, поливинилпирролидон, поливиниловый спирт и др.), замедлитель растворения (например, парафин, воск, гидрированное касторовое масло и др.), стимулятор реабсорбции (например, четвертичные соли) и адсорбент (например, бентонит, каолин, дикальцийфосфат и др.). Порошкообразную композицию можно гранулировать увлажнением вещества связующим агентом, например сиропом, крахмальной пастой, раствором гуммиарабика или целлюлозы, или раствором полимера, и затем пропусканием влажной массы через сито под давлением. Негранулированный порошок можно прессовать с помощью устройства для таблетирования с получением комков грубой формы, которые затем дробят, получая гранулы.
Полученные таким образом гранулы могут быть защищены от слипания добавлением смазывающего агента, такого, как стеариновая кислота, соль стеариновой кислоты, тальк или минеральное масло. Смазанные гранулы затем прессуют в таблетки.
Полученные таблетки без оболочки могут быть покрыты оболочкой или сахаром.
Лекарственное средство, не подвергавшееся описанному выше процессу гранулирования или формования, можно непосредственно прессовать после смешивания с сыпучим инертным носителем. Может также применяться прозрачное или полупрозрачное защитное покрытие, включающее герметичную шеллаковую пленку, сахарное или полимерное покрытие или покрытие из восковой глазури.
Другие лекарственные формы для перорального применения, такие, как растворы, сиропы и эликсиры, могут также формулироваться в дозированных формах, каждая из которых содержит предварительно определенное количество лекарственного средства. Сироп может быть получен растворением соединения в подходящей водной среде с приятным ароматом, тогда как эликсир может быть получен при использовании нетоксичной спиртовой среды.
При необходимости разовая доза композиции для перорального введения может быть заключена в микрокапсулу. Данная разовая доза также может быть покрыта полимером, воском или т.п. или погружена в полимер, воск или т.п. для обеспечения пролонгированного действия или замедленного высвобождения активного ингредиента.
Ректальное введение может проводиться с применением свечей, которые могут быть получены смешиванием соединения с водорастворимой или водонерастворимой твердой основой с низкой температурой плавления, такой, как полиэтиленгликоль, масло какао или высшие сложные эфиры (например, миристилпальмитат), или их смесью.
Наилучший способ осуществления изобретения
Нижеследующие примеры получения исходных соединений (справочные примеры) и соединений настоящего изобретения (примеры), а также примеры составов и примеры анализов представлены для более подробной дополнительной иллюстрации настоящего изобретения и никоим образом не являются ограничивающими объем настоящего изобретения. Удельное вращение измеряют при 20°С.
Справочный пример 1
Синтез 4-метилпиперазин-1-илуксусной кислоты
[Способ 1]
Синтез бензил 4-метилпиперазин-1-илацетата
N-Метилпиперазин (2,29 г) растворяют в DMF (20 мл). К раствору добавляют карбонат калия (2,76 г) и бензил-бромацетат (1,20 г) и смесь нагревают при 80°С в течение 1 часа. Реакционную смесь концентрируют при пониженном давлении. Остаток объединяют с водой со льдом и экстрагируют хлороформом. Экстракт сушат над сульфатом магния и растворитель отгоняют при пониженном давлении. Полученный остаток очищают колоночной хроматографией на силикагеле (элюент: СН2Сl2/СН3ОН/NН3 (28% водн.) = 90/10/1), получая целевое соединение (2,0 г, бесцветное масло).
Нижеследующие соединения получают описанным выше способом.
Бензил 4-пиперидинопиперидиноацетат
Бензил 4-(3-пиридил)пиперазин-1-илацетат
Бензил 4-(2-пиридил)пиперазин-1-илацетат
Бензил 4-пирролидинопиперидиноацетат
Бензилпиперидиноацетат
Этил 4-(4-пиперидинопиперидино)бутират
Этил 3-(4-пиперидинопиперидино)пропионат
Бензилморфолиноацетат
Бензилпирролидиноацетат
Этил 2-пиперидинопропионат
[Способ 2]
Синтез 4-метилпиперазин-1-илуксусной кислоты
Бензил-4-метилпиперазин-1-илацетат (1,98 г), полученный в описанном выше способе 1, растворяют в метаноле (20 мл) и подвергают гидрогенолизу при комнатной температуре при обычном давлении в течение 4 часов в присутствии 10% палладия на угле. Реакционный раствор фильтруют и фильтрат концентрируют при пониженном давлении, получая целевое соединение (1,11 г, бесцветные кристаллы).
Нижеследующие соединения получают описанным выше способом.
4-Пиперидинопиперидиноуксусная кислота
4-(3-Пиридил)пиперазин-1-илуксусная кислота
4-(2-Пиридил)пиперазин-1-илуксусная кислота
4-Пирролидинопиперидиноуксусная кислота
Пиперидиноуксусная кислота
Морфолиноуксусная кислота
Пирролидиноуксусная кислота
Справочный пример 2
Синтез гидрохлорида 4-(4-пиперидинопиперидино)масляной кислоты
Этил-4-(4-пиперидинопиперидино)бутират (2,20 г), полученный способом справочного примера 1 (способ 1), растворяют в этаноле (20 мл). После добавления 1N водного раствора гидроксида натрия (11,7 мл) смесь кипятят с обратным холодильником в течение 4 часов при перемешивании. Реакционную смесь концентрируют досуха. Остаток осаждают разбавлением этанолом с последующим добавлением 1N хлористоводородной кислоты при охлаждении льдом. Кристаллический осадок отфильтровывают и используют в качестве исходного вещества без дополнительной очистки.
Нижеследующие соединения получают описанным выше способом.
Гидрохлорид 3-(4-пиперидинопиперидино)пропионовой кислоты
Гидрохлорид 3-пиперидинопропионовой кислоты
Пример 1
Гидрохлорид 1-оксида (Е)-4-(2-(2-(N-глицил-Н-(4-метокси-бензолсульфонил)амино)фенил)этенил)пиридина
1-Оксид (Е)-4-(2-(2-(N-(4-метоксибензолсульфонил)амино)-фенил)этенил)пиридина (1,15 г) растворяют в метиленхлориде (25 мл) и добавляют к нему N-(трет-бутоксикарбонил)глицин (1,31 г) и 4-пирролидинопиридин (44 мг). К смеси добавляют по каплям N,N'-дициклогексилкарбодиимид (1,55 г), растворенный в метиленхлориде (15 мл), и смесь перемешивают в течение ночи при комнатной температуре. Реакционный раствор фильтруют и фильтрат концентрируют. Полученный остаток растворяют в этилацетате и промывают водой. Органический слой сушат над сульфатом магния и растворитель отгоняют при пониженном давлении. Остаток очищают колоночной хроматографией на силикагеле (элюент: СНСl3/СН3ОН=30/1), получая бесцветное порошкообразное соединение (2,10 г). Полученный продукт растворяют в этаноле (20 мл) и кипятят с обратным холодильником в течение ночи после добавления 1N хлористоводородной кислоты (20 мл). Реакционный раствор концентрируют и осажденные кристаллы промывают теплой смесью хлороформа и метанола, получая целевое соединение (0,70 г, бесцветный порошок). Т.пл. 235-237°С.
Элементный анализ для С22Н21N3O5S·НСl·2,5Н2О:
Вычислено (%): С, 50,67; Н, 4,64; N, 8,06;
Найдено (%): С, 50,69; Н, 4,62; N, 8,01.
Пример 2
Гидрохлорид 1-оксида (Е)-4-(2-(2-(N-(4-метилпиперазин-1-ил)ацетил-N-(4-метоксибензолсульфонил)амино)фенил)этенил)-пиридина
1-Оксид (E)-4-(2-(2-(N-(4-метоксибензолсульфонил)амино)-фенил)этенил)пиридина (0,96 г) растворяют в метиленхлориде (25 мл) и добавляют к нему 4-метилпиперазин-1-илуксусную кислоту (0,99 г), полученную в справочном примере 1, и 4-пирролидинопиридин (37 мг). К смеси добавляют по каплям N,N'-дициклогексилкарбодиимид (1,29 г), растворенный в метиленхлориде (13 мл), и смесь перемешивают в течение ночи при комнатной температуре. Реакционный раствор фильтруют и фильтрат концентрируют. Полученный остаток подвергают колоночной хроматографии на силикагеле (элюент: СНСl3/СН3ОН = от 100/1 до 10/1), получая фракции. К каждой фракции добавляют раствор хлористоводородной кислоты в эфире, после чего концентрируют. Остаток разбавляют водой, фильтруют через мембранный фильтр и лиофилизируют, получая целевое соединение (1,25 г, бесцветный порошок).
МС (m/е): 523 (М+)
1H-ЯМР (DMSO-d6): δ: 2,69 (3Н, с), 3,18-3,52 (9Н, м), 3,76 (1Н, д), 3,82 (3Н, д), 7,08-7,23 (3Н, м), 7,43-7,72 (6Н, м), 7,88-8,05 (3Н, м), 8,54 (2Н, д), 11,25 (1Н, уш.)
Пример 3
Дигидрохлорид 1-оксида (Е)-4-(2-(2-(N-(4-пиперидино-пиперидино)ацетил-N-(4-метоксибензолсульфонил)амино)фенил)-этенил)пиридина
4-Пиперидинопиперидиноуксусную кислоту (1,70 г), полученную способом справочного примера 1, подвергают взаимодействию и последующей обработке способом примера 2, получая целевое соединение (1,28 г, бледно-желтый порошок).
МС (m/е): 591 (M+)
Элементный анализ для C32H38N4O5S·2HCl·8H2O:
Вычислено (%): С, 47,58; Н, 6,99; N, 6,94;
Найдено (%): С, 46,95; Н, 6,72; N, 6,80.
1H-ЯМР (DMSO-d6): δ: 1,38-2,21 (12H, м), 2,86-3,36 (8Н, м), 3,80 (3Н, с), 3,89 (1Н, д), 6,99-7,12 (3Н, м), 7,35-7,69 (6Н, м), 7,93-8,04 (3Н, м), 8,38 (2Н, д), 10,45 (1Н, уш. ) 11,15 (1Н, уш.)
Пример 4
Дигидрохлорид 1-оксида (Е)-4-(2-(2-(N-(4-пирролидинопиперидино)ацетил-N-(4-метоксибензолсульфонил)амино)фенил)этенил)пиридина
4-Пирролидинопиперидиноуксусную кислоту (1,59 г), полученную способом справочного примера 1, подвергают взаимодействию и последующей обработке способом примера 2, получая целевое соединение (0,50 г, бледно-желтый порошок).
МС (m/е): 577 (М+)
Элементный анализ для C31H36N4O5S·2HCl·7H2O:
Вычислено (%): С, 48,00; Н, 6,76; N, 7,22;
Найдено (%): С, 47,87; Н, 6,76; N, 7,10.
1H ЯМР (DMSO-d6): δ: 1,91-2,17 (7Н, м), 3,00-3,89 (14Н, м), 4,24 (1Н, д), 6,97-7,14 (3Н, м), 7,32-7,69 (6Н, м), 7,90-8,05 (3Н, м), 8,38 (2Н, д), 10,25 (1Н, уш.), 10,60 (1Н, уш.).
Пример 5
Гидрохлорид 1-оксида (Е)-4-(2-(2-(N-(4-метоксибензолсульфонил)-N-пиперидиноацетиламино)фенил)этенил)пиридина
Пиперидиноуксусную кислоту (0,89 г), полученную способом справочного примера 1, подвергают взаимодействию и последующей обработке способом примера 2, получая целевое соединение (0,85 г, бесцветный порошок).
МС (m/е): 508 (М+)
1H-ЯМР (DMSO-d3): δ: 1,67 (6Н, уш.), 2,87 (2Н, уш. ), 3,35 (2Н, уш.), 3,62 (3Н, с), 3,73 (1Н, д), 4,19 (1Н, д), 7,06-7,14 (3Н, м), 7,41-7,71 (6Н, м), 7,90-8,07 (3Н, м), 8,48 (2Н, м), 9,99 (1Н, уш.).
Пример 6
Дигидрохлорид 1-оксида (Е)-4-(2-(2-(N-изоникотиноил-N-(4-метоксибензолсульфонил)амино)фенил)этенил)пиридина
Изоникотиновую кислоту (0,20 г) подвергают взаимодействию и последующей обработке способом примера 2, получая целевое соединение (0,25 г, бледно-желтый порошок).
Т.пл. 198-200°С.
Элементный анализ для С26Н21N3O5S·2НСl·0,5Н2O:
Вычислено (%): С, 54,84; Н, 4,24; N, 7,37;
Найдено (%): С, 54,98; Н, 4,41; N, 7,39.
Пример 7
Дигидрохлорид 1-оксида (Е)-4-(2-(2-(N-никотиноил-N-(4-метоксибензолсульфонил)амино)фенил)этенил)пиридина
Никотиновую кислоту (0,20 г) подвергают взаимодействию и последующей обработке способом примера 2, получая целевое соединение (0,24 г, бледно-желтый порошок). Т.пл. 187-189°С.
Элементный анализ для С26Н21N3O5S·2НСl:
Вычислено (%): С, 55,72; Н, 4,14; N, 7,50;
Найдено (%): С, 55,45; Н, 4,30; N, 7,38.
Пример 8
Гидрохлорид 1-оксида (Е)-4-(2-(2-(N-(N,N-диметилглицил)-N-(4-метоксибензолсульфонил)амино)фенил)этенил)пиридина
N,N-Диметилглицин (0,65 г) подвергают взаимодействию способом примера 2. Реакционный раствор фильтруют и фильтрат концентрируют. Остаток разбавляют толуолом и изопропиловым эфиром и перемешивают. Осажденные кристаллы отфильтровывают, промывают водой, сушат и перекристаллизовывают из ацетонитрила. Полученные белые кристаллы суспендируют в воде, после чего добавляют IN водный раствор соляной кислоты и перемешивают. Смесь фильтруют через мембранный фильтр и лиофилизируют, получая целевое соединение (0,62 г, бесцветный порошок). Т.пл. 158-162°С.
МС (m/е): 468 (М+)
Элементный анализ для C24H25N3O5S·HCl·4H2O:
Вычислено (%): С, 50,04; Н, 5,95; N, 7,29;
Найдено (%): С, 49,73; Н, 5,67; N, 7,37.
1H ЯМР (DMSO-d6): δ: 2,70 (6Н, с), 3,75-4,18 (2Н, м), 3,84 (3Н, с), 6,95-7,15 (3Н, м), 7,36-7,70 (6Н, м), 7,91-8,05 (3Н, м), 8,26 (2Н, д), 9,87 (1Н, уш.).
Пример 9
Дигидрохлорид 1-оксида (Е)-4-(2-(2-(N-(4-метоксибензолсульфонил)-N-(4-(2-пиридил)пиперазино)ацетиламино)фенил)этенил)пиридина
4-(2-Пиридил)пиперазин-1-илуксусную кислоту (1,10 г), полученную способом справочного примера 1, подвергают взаимодействию способом примера 2. Затем реакционный раствор обрабатывают способом примера 8, получая целевое соединение (0,67 г, бесцветный порошок). Т.пл. 167°С (разложение).
МС (m/е): 586 (М+)
Элементный анализ для C31H31N5O5S·2HCl·4H2O:
Вычислено (%): С, 50,96; Н, 5,66; N, 9,58;
Найдено (%): С, 51,40; Н, 6,00; N, 9,46.
1H-ЯМР (DMSO-d6): δ: 3,0-4,0 (12H, м), 4,19 (1Н, д), 6,82-7,15 (5Н, м), 7,37-7,82 (7Н, м), 7,94 (2Н, д), 8,02-8,10 (2Н, м), 8,33 (2Н, д).
Пример 10
Дигидрохлорид 1-оксида (Е)-4-(2-(2-(N-(4-(3-пиридил)пиперазино)ацетил-N-(4-метоксибензолсульфонил)амино)фенил)этенил)пиридина
4-(3-Пиридил)пиперазин-1-илуксусную кислоту (1,39 г), полученную способом справочного примера 1, подвергают взаимодействию и последующей обработке способом примера 2, получая целевое соединение (1,30 г, бледно-желтый порошок). Т.пл. 167°С (разложение).
МС (m/е): 586 (М+)
Элементный анализ для C31H31N5O5S·2HCl·4H2O:
Вычислено (%): С, 50,96; Н, 5,66; N, 9,58;
Найдено (%): С, 51,31; Н, 6,00; N, 9,40.
1H ЯМР (DMSO-d6): δ: 3,0-4,0 (12Н, м), 4,22 (1Н, д), 6,98-7,14 (3Н, м), 7,36-7,69 (6Н, м), 7,80-8,05 (5Н, м), 8,23-8,50 (4Н, м).
Пример 11
Дигидрохлорид 1-оксида (Е)-4-(2-(2-(N-(3-(4-пиперидино-пиперидино)пропионил)-N-(4-метоксибензолсульфонил)амино)фенил)этенил)пиридина
Гидрохлорид 3-(4-пиперидинопиперидино)пропионовой кислоты, полученный способом справочного примера 2, и триэтиламин подвергают взаимодействию и последующей обработке способом примера 2, получая целевое соединение (0,13 г, бледно-желтый порошок).
МС (m/е): 605 (М+)
Элементный анализ для C33H40N4O5S·2HCl·4H2O:
Вычислено (%): С, 52,87; Н, 6,72; N, 7,47;
Найдено (%): С, 52,13; Н, 7,24; N, 7,47.
1H ЯМР (DMSO-d6): δ; 1,10-2,40 (10Н, м), 2,6-3,05 (6Н, м), 3,06-3,80 (7Н, м), 3,84 (3Н, С), 6,88-7,21 (3Н, м), 7,38-7,64 (6Н, м), 7,89-8,04 (3Н, м), 8,34 (2Н, д), 10,5 (1Н, уш.), 10,7 (1Н, уш.).
Пример 12
Дигидрохлорид 1-оксида (Е)-4-(2-(2-(N-(4-(4-пиперидинопиперидино)бутирил)-N-(4-метоксибензолсульфонил)амино)фенил)этенил)пиридина
Гидрохлорид 3-(4-пиперидинопиперидино)масляной кислоты, полученный способом справочного примера 2, и триэтиламин подвергают взаимодействию и последующей обработке способом примера 2, получая целевое соединение (0,88 г, бледно-желтый порошок).
МС (m/е): 619 (М+)
Элементный анализ для C34H42N4O5S·2HCl·8H2O:
Вычислено (%): С, 48,86; Н, 7,24; N, 6,70;
Найдено (%): С, 48,54; Н, 6,60; N, 6,61.
1H ЯМР (DMSO-d6): δ: 1,64-2,26 (15Н, м), 2,85 (6Н, уш. ), 3,30-3,63 (4Н, м), 3,83 (3Н, с), 7,05-7,13 (3н, м), 7,36-7,61 (6Н, м), 7,88-8,03 (3Н, м), 8,30 (2Н, д), 10,84 (2Н, уш.).
Пример 13
Гидрохлорид 1-оксида (Е)-4-(2-(2-(N-(4-метоксибензолсульфонил) -N-морфолинацетиламино)фенил)этенил)пиридина
Указанное в заголовке соединение получают способом примера 2, используя морфолинуксусную кислоту, полученную способом справочного примера 1.
МС (m/е): 510 (М+)
1H ЯМР (DMSO-d6): δ: 2,80-3,30 (4Н, м), 3,55-4,20 (9Н, м), 6,95 (1Н, д), 7,09-7,15 (2Н, м), 7,36-7,96 (6Н, м), 7,89-8,05 (3Н, м), 8,24 (2Н, д), 10,40 (1Н, уш.).
Пример 14
Гидрохлорид 1-оксида (Е)-4-(2-(2-(N-(4-метоксибензолсульфонил)-N-пирролидинацетиламино)фенил)этенил)пиридина
Указанное в заголовке соединение получают способом примера 2, используя пирролидинуксусную кислоту, полученную способом справочного примера 1.
МС (m/е): 494 (М+)
1H ЯМР (DMSO-d6): δ: 1,65-2,00 (4Н, м), 2,80-3,10 (2Н, м), 3,20-3,60 (2Н, м), 3,80 (3Н, с), 3,84-3,93 (1Н, м), 4,19-4,28 (1Н, м), 7,04 (1Н, д), 7,10-7,16 (2Н, м), 7,34-7,69 (6Н, м), 7,88-8,04 (3Н, м), 8,25 (2Н, д), 10,11 (1Н, уш.).
Пример 15
Гидрохлорид 1-оксида (Е)-4-(2-(2-(N-(3-пиридилацетил)-N-(4-метоксибензолсульфонил)амино)фенил)этенил)пиридина
Гидрохлорид 3-пиридилуксусной кислоты и триэтиламин подвергают взаимодействию и последующей обработке способом примера 2, получая целевое соединение (1,06 г).
МС (m/е): 502 (М+)
1H ЯМР (DMSO-d6): δ: 3,59 (1H, д), 3,84 (3Н, с), 3,85 (1H, д), 7,01 (2Н, д), 7,35-8,10 (11Н, м), 8,40 (1H, д), 8,54 (2Н, д), 8,77 (1H, с), 8,82 ИН, д), 9,90 (1H, уш).
Пример 16
Дигидрохлорид 1-оксида (Е)-4-(2-(2-(N-(3-морфолин-пропионил)-N-(4-метоксибензолсульфонил)амино)фенил)этенил)пиридина
Гидрохлорид 3-морфолинпропионовой кислоты, полученный способом справочного примера 2, и триэтиламин подвергают взаимодействию и последующей обработке способом примера 2, получая целевое соединение (1,08 г).
МС (m/е): 524 (М+)
1H ЯМР (DMSO-d6): δ; 2,57-3,92 (15Н, м), 7,12 (2Н, д), 7,25 (1H, д), 7,42-7,67 (6Н, м), 7,91 (2Н, д), 8,02 (1H, д), 8,45 (2Н, д), 11,04 (1H, уш.).
Пример 17 (другой способ получения)
Гидрохлорид 1-оксида (Е)-4-(2-(2-(N-морфолинацетил-N-(4-метоксибензолсульфонил)амино)фенил)этенил)-пиридина
Морфолинуксусную кислоту (5,18 г), полученную способом справочного примера 1, растворяют в метиленхлориде (230 мл) и добавляют триэтиламин (4,86 г). К смеси при охлаждении льдом по каплям добавляют хлоркарбонат (5,21 г) и смесь перемешивают тридцать минут при комнатной температуре. К смеси добавляют 1 оксид (Е)-4-(2-(2-(N-(4-метоксибензолсульфонил)амино)фенил)этенил)пиридина (7,65 г) и смесь перемешивают еще три часа при комнатной температуре. Реакционный раствор промывают водой, сушат над сульфатом магния и концентрируют. Полученный остаток растворяют в ацетонитриле. К раствору добавляют раствор хлористого водорода в метаноле и смесь перемешивают в течение ночи при комнатной температуре. Осажденные кристаллы отфильтровывают, промывают ацетонитрилом и еще дополнительной порцией эфира и получают неочищенные кристаллы. Перекристаллизация из метанола дает целевое соединение (8,16 г).
Пример 18
Гидрохлорид 1-оксида (Е)-4-(2-(2-(N-(N',N'-диметиламино-пропионил)-N-(4-метоксибензолсульфонил)амино)фенил)этенил)-пиридина
Гидрохлорид N,N-диметиламинопропионовой кислоты и триэтиламин подвергают взаимодействию и последующей обработке способом примера 2, получая целевое соединение.
Пример тестирования 1
Растворимость в воде
Водорастворимость соединения настоящего изобретения измеряют при 25°С. В качестве контрольных соединений используют 1-оксид (Е)-4-(2-(2-(N-(4-метоксибензолсульфонил)-амино)фенил)этенил)пиридина (соединение А) и 1-оксид (Е)-4-(2-(2-(N-ацетил-N-(4-метоксибензолсульфонил)амино)фенил)этенил)пиридина (соединение В). Обнаружено, что растворимость соединений настоящего изобретения, т.е. соединений, полученных в примерах 1-16, превышает 10 мг/мл, тогда как растворимость соединения А и соединения В составляет 29 и 18 мкг/мл соответственно.
Пример тестирования 2
Противораковая активность против клеток Colon-26 (рака ободочной кишки мыши), трансплантированных мышам
Клетки Colon-26, культивированные in vitro, трансплантируют подкожно с помощью инъекционного шприца в правую подмышечную область самцов мышей Balb/c возрастом 5 недель (5×105 клеток/животное). Когда объем опухоли достигает приблизительно 120 мм3 (эксперимент 1) или приблизительно 100 мм3 (эксперимент 2), мышей делят на группы по 6 животных в каждой. Тестируемое лекарственное средство, растворенное в 5% растворе глюкозы, вводят внутривенно всего 5 раз, один раз в день с интервалами в 4 дня. Мышей контрольной группы обрабатывают таким же образом 5% раствором глюкозы. Объем опухоли рассчитывают по уравнению 1, приведенному ниже, на основе большой и малой осей опухоли, измеренных с заданными интервалами штангенциркулями.
Уравнение 1
Объем опухоли = 1/2ґ(большая ось)ґ(малая ось)2
Затем по уравнению 2 на основе объема опухоли рассчитывают интенсивность роста, которую затем используют в уравнении 3 для расчета степени ингибирования роста в группе, обработанной лекарственным средством, по сравнению с контрольной группой.
Уравнение 2
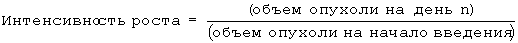
Уравнение 3

Степень ингибирования роста опухоли и количество выживших животных на 21 день после начала введения показаны в таблице 1.
Соединения настоящего изобретения проявляют предельно высокую активность в отношении ингибирования опухолевого роста.
Пример композиции 1
Композиция для инъекции (в 1 мл)
Соединение примера 9 10 мг
Маннит 50 мг
Вода для инъекции количество, необходимое для получения 1 мл раствора
Способ получения
Соединение настоящего изобретения и маннит растворяют в воде для инъекции, фильтруют через мембранный фильтр (0,22 мкм) в стерильных условиях, вносят во флакон и лиофилизируют, получая композицию для инъекции, предназначенную для растворения непосредственно перед применением.
Пример композиции 2
Композиция для инъекции (в 1 мл)
Соединение примера 9 10 мг
Мальтоза 100 мг
Вода для инъекции количество, необходимое для получения 1 мл раствора
Способ получения
Соединение настоящего изобретения и мальтозу растворяют в воде для инъекции, фильтруют через мембранный фильтр (0,22 мкм) в стерильных условиях, вносят во флакон и лиофилизируют, получая композицию для инъекции, предназначенную для растворения непосредственно перед применением.
Промышленная применимость
Соединение настоящего изобретения является водорастворимым и обладает мощной противораковой активностью и низкой токсичностью. Соответственно оно может применяться в качестве активного ингредиента фармацевтических композиций в виде растворов, особенно растворов для инъекций, которые в течение длительного периода могут безопасно применяться для лечения у пациентов, не способных перорально принимать лекарственное средство, различных злокачественных опухолей, таких, как рак легких, рак молочной железы, рак желудочно-кишечного тракта, рак простаты, рак крови и т.п.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ХРОНИЧЕСКОГО СУСТАВНОГО РЕВМАТИЗМА | 2002 |
|
RU2282446C2 |
| ПРОИЗВОДНОЕ 1,3,5-ТРИАЗИНА И СПОСОБ ЕГО ПРИМЕНЕНИЯ | 2016 |
|
RU2724333C2 |
| КОНДЕНСИРОВАННЫЕ БИЦИКЛИЧЕСКИЕ ГЕТЕРОАРОМАТИЧЕСКИЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ МОДУЛЯТОРОВ АКТИВНОСТИ TNF | 2014 |
|
RU2685234C1 |
| КОНДЕНСИРОВАННЫЕ ПРОИЗВОДНЫЕ ИМИДАЗОЛА И ПИРАЗОЛА В КАЧЕСТВЕ МОДУЛЯТОРОВ АКТИВНОСТИ TNF | 2014 |
|
RU2686117C1 |
| ЗАМЕЩЕННЫЕ ФЕНОКСИУКСУСНЫЕ КИСЛОТЫ, ИХ ЭФИРЫ И АМИДЫ, ВКЛЮЧАЮЩИЕ 2,6-ДИОКСО-2,3,6,7-ТЕТРАГИДРО-1Н-ПУРИН-8-ИЛОВЫЙ ФРАГМЕНТ, - АНТАГОНИСТЫ АДЕНОЗИНОВОГО A РЕЦЕПТОРА И ИХ ПРИМЕНЕНИЕ | 2011 |
|
RU2477726C1 |
| ПРОИЗВОДНЫЕ ПИРАЗОЛА, ПОЛЕЗНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОТЕИНКИНАЗЫ | 2001 |
|
RU2332415C2 |
| ИНГИБИТОР, ПРЕДСТАВЛЯЮЩИЙ СОБОЙ ПРОИЗВОДНОЕ ПИРИДАЗИНА, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2807611C2 |
| (ГЕТЕРО)АРИЛЦИКЛОПРОПИЛАМИНЫ В КАЧЕСТВЕ ИНГИБИТОРОВ LSD1 | 2012 |
|
RU2668952C2 |
| (АЗА)ИНДОЛ-, БЕНЗОТИОФЕН- И БЕНЗОФУРАН-3-СУЛЬФОНАМИДЫ | 2017 |
|
RU2767904C2 |
| СОЕДИНЕННЫЕ МОСТИКОВОЙ СВЯЗЬЮ N-ЦИКЛИЧЕСКИЕ СУЛЬФОНАМИДО-ИНГИБИТОРЫ ГАММА-СЕКРЕТАЗЫ | 2006 |
|
RU2422443C2 |
Изобретение относится к азотсодержащим гетероциклическим производным формулы (I)
A-B-D-E (I), где А означает 5- или 6-членный гетероарил, содержащий в цикле один или два атома азота; В означает этенилен; D означает фенилен; Е означает группу -N(COR)-SO2-G, где G означает фенил; R означает 5- или 6-членный гетероарил или гетероарилметил, содержащие в цикле один или два атома азота, или группу -(CH2)n-N(R5)R6, где n означает целое число от 1 до 5; R5 и R6 одинаковые или разные: водород, С1-С6алкил, гидроксиалкил, аминоалкил, или R5 и R6 вместе с атомом азота могут образовывать 5-7-членную циклическую аминогруппу – N(R5)R6, которая кроме атома азота может включать атом кислорода, серы или азота в качестве образующего цикл члена, или их N-оксидам. Соединения формулы (I) обладают противораковой активностью и могут найти применение в медицине. 3 с. и 7 з.п. ф-лы, 1 табл.
A-B-D-E [1]
где
А обозначает необязательно замещенный 5- или 6-членный гетероарил, содержащий в цикле один или два атома азота, или его оксид;
В обозначает необязательно замещенный этенилен;
D обозначает необязательно замещенный фенилен; и Е обозначает группу формулы:
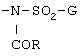
где G обозначает необязательно замещенный фенил;
и R обозначает необязательно замещенный 5- или 6-членный гетероарил, содержащий в цикле один или два атома азота, или 5- или 6-членный гетероарилметил, содержащий в цикле один или два атома азота, или группу формулы:
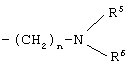
где n представляет собой целое число от 1 до 5; R5 и R6 являются одинаковыми или разными, и независимо выбраны из группы, состоящей из водорода, C1-С6 алкила, гидроксиалкила, аминоалкила; или R5 и R6, взятые вместе с соседним атомом азота, могут образовывать 5-7-членную циклическую аминогруппу –NR5(R6), которая может быть необязательно замещена, и, кроме атома азота, может необязательно включать атом кислорода, серы или азота, в качестве образующего цикл члена.
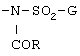
где R и G являются такими, как определено в п.1.
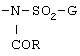
где G обозначает необязательно замещенный фенил, а R обозначает группу формулы:
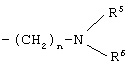
где n, R5 и R6 являются такими, как определено в п.1.
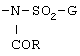
где G обозначает необязательно замещенный фенил; a R обозначает необязательно замещенный 5-6-членный гетероарил, содержащий в цикле один или два атома азота, или 5-6-членный гетероарилметил, содержащий в цикле один или два атома азота.
Приоритет по признакам:
А обозначает 4-пиридил или 1-оксидо-4-пиридил;
В обозначает этенилен;
D обозначает необязательно замещенный фенилен; и Е обозначает группу формулы:
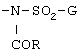 ,
,
где G обозначает необязательно замещенный фенил; и R обозначает необязательно замещенный 5- или 6-членный гетероарил, содержащий в цикле один или два атома азота, или 5- или 6-членный гетероарилметил, содержащий в цикле один или два атома азота, или группу формулы:
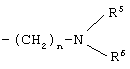 ,
,
где n представляет собой целое число от 1 до 5;
R5 и R6 являются одинаковыми или разными, и независимо выбраны из группы, состоящей из водорода, C1-С6 алкила, гидроксиалкила, аминоалкила; или R5 и R6, взятые вместе с соседним атомом азота, могут образовывать 5-7-членную циклическую аминогруппу –NR5(R6), которая может быть необязательно замещена, и, кроме атома азота, может необязательно включать атом кислорода, серы или азота, в качестве образующего цикл члена, установлен приоритет от 14.12.1999, по остальным признакам установлен приоритет от 04.07.2000.
| ЦИКЛИЧЕСКОЕ АМИНОСОЕДИНЕНИЕ ИЛИ ЕГО ФИЗИОЛОГИЧЕСКИ ПРИЕМЛЕМАЯ АДДИТИВНАЯ СОЛЬ КИСЛОТЫ | 1990 |
|
RU2021989C1 |
| Прибор для очистки паром от сажи дымогарных трубок в паровозных котлах | 1913 |
|
SU95A1 |
| US 5529999 A, 25.06.1996 | |||
| US 5721246 A, 24.02.1998. | |||
Авторы
Даты
2005-03-27—Публикация
2000-12-13—Подача