Настоящее изобретение относится к производным пиразола, обладающим антипаразитическими свойствами.
Некоторые антипаразитические производные пиразола уже известны. Они включают в себя фипронил (5-амино-3-циано-1-(2,6-дихлор-4- трифторметилфенил)-4-трифторметилсульфинилпиразол) и некоторые его аналоги, упомянутые в International Patent Application WO 87/03781.
В EP 0 658 047 A1 раскрыт ряд 4-алкенил и 4-алкинил пиразолов с H и алкилом в 1 - положении и карбаматной группой в положении 5 пиразола, в качестве антигрибковых агентов.
Теперь найдена новая группа антипаразитических производных пиразола. Так, согласно настоящему изобретению, обеспечено соединение формулы I:
где R1 является CN, C1-6 алкоксикарбонилом, NO2, CHO, C1-6 алканоилом, фенилом, необязательно (произвольно) замещенным одним или более атомами галогена, или C1-6 алкилом, необязательно замещенным одним или более атомами галогена;
R2 является группой формулы II, III или IV: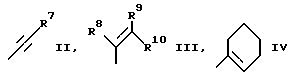
в которой
R7 является H, галогеном, карбамоилом, циано, три (C1-6 алкил) силилом, C1-6 алкилом (необязательно замещенным одним или более атомами галогена, ОН или C1-6 алкоксигруппой), C1-6 алкоксикарбонилом, фенильной группой или 5- или 6-членным циклическим гетероциклом, который насыщен или частично или полностью ненасыщен и содержит вплоть до 4 гетероатомов, независимо выбранных из вплоть до 4 N атомов, до 2 О атомов и до 2 S атомов и который присоединен к алкинильному звену при помощи подходящего атома C, S, или N, где позволяет валентность;
и R8, R9 и R10 каждый является независимо H, галогеном, фенилом, необязательно замещенным одним или более атомами галогена, CN или C1-6 алкильной группой, необязательно замещенной одним или более атомами галогена;
R3 представляет H, C1-6 алкил, галоген, NH2, NH (C1-6 алканоил), NH (C1-6 алкоксикарбонил), N (C1-6 алкоксикарбонил)2, NH (C1-6 алкил), N (C1-6 алкил)2, NHCONH (C1-6 алкил), N-пирролил, NHCONH (фенил, необязательно замещенный одним или более атомами галогена), N = CH (фенил), ОН, C1-6 алкокси, SH или S (О)n (C1-6 алкил, необязательно замещенный одним или более атомами галогена), где n равно 0, 1 или 2; и R4, R5 и R6 каждый является независимо H, галогеном, C1-6 алкилом, необязательно замещенным одним или более атомами галогена, C1-6 алкоксигруппой, необязательно замещенной одним или более атомами галогена, S (О)n (C1-6 алкилом, необязательно замещенным одним или более атомами галогена), где n равно 0, 1 или 2, или CH3CO, CN, CONH2, CSNH2, OCF3, SCF3, или SF5, или его фармацевтически или ветеринарно пригодные соли (в дальнейшем называемые совместно "соединениями изобретения").
Алкильные группы могут быть прямыми, циклическими или разветвленными, где позволяет число атомов углерода. Галоген означает фтор, хлор, бром или йод.
Фармацевтически и ветеринарно пригодные соли хорошо известны тем, кто имеет опыт в данной области техники, и включают в себя, например, те, которые упомянуты Berge et al в J:.Pharm. Sci 66, 1-19 (1997).
R1 предпочтительно является CN, необязательно замещенным фенилом, необязательно замещенной C1-6 алкильной группой или C1-6 алкоксикарбонильной группой.
R1 более предпочтительно является CN, Ph, CO2C2H5, CH3, CF3 или CO2CH3.
R2 предпочтительно является группой формулы II, где R7 является H, три (C1-6 алкил) силильной группой, C1-6 алкильной группой, необязательно замещенной одним или более атомами галогена, ОН или C1-6 алкоксигруппой, или R7 является C1-6 алкоксикарбонильной, фенильной группой или 5- или 6-членным циклическим гетероциклом, как определено выше, галогеном,
или группой формулы III, в которой каждый из R8, R9 и R10 является H, или группой формулы III, в которой два из R8, R9 и R10 являются галогенами, а другой является H, CN, фенилом, необязательно замещенным одним или более атомами галогена, или C1-6 алкилом, необязательно замещенным одним или более атомами галогена, или группой формулы III, в которой R8, R9 и R10 являются каждый независимо F, Cl, Br или 1,
или группой формулы III, в которой R8 является H или C1-6 алкилом, необязательно замещенным одним или более атомами галогена, OH или C1-6 алкоксигруппой, a R9 и R10 оба являются галогеном, или группой формулы III, в которой R8 является H и один из R9 и R10 является галогеном, а другой является C1-6 алкилом, необязательно замещенным одним или более атомами галогена, OH или C1-6 алкоксигруппой, или группой формулы III, в которой R8 является H и один из R9 и R10 является H, а другой является CN или C1-6 алкилом, необязательно замещенным одним или более атомами галогена, OH или C1-6 алкоксигруппой,
или группой формулы III, в которой R8 является H и один из R9 и R10 является C1-6 алкилами, необязательно замещенными одним или более атомами галогена, OH или C1-6 алкоксигруппами,
или группой формулы III, в которой R8 является C1-6 алкилом, необязательно замещенным одним или более атомами галогена, OH или C1-6 алкоксигруппой, a R9 и R10 оба являются H,
или группой формулы IV.
Более предпочтительно R2 является группой формулы II, в которой R7 является Si(CH3)3, H, CH3, CH(CH3)2, CH2OH, (CH2)2OH, CO2CH3, Ph, тиен-2-ил, CH2OCH3, Br, Cl или CF3,
или группой формулы III, в которой R8, R9 и R10 каждый является H, или группой формулы III, в которой R8, R9 и R10 каждый является Cl,
или группой формулы III, в которой R8 и R9 являются Br, a R10 является H,
или группой формулы III, в которой R8 и R10 являются Br, a R9 является H,
или группой формулы III, в которой R8 и R9 являются Br, a R10 является CH3,
или группой формулы III, в которой R8 и R10 являются Br, a R9 является CH3,
или группой формулы III, в которой R8 и R10 являются Br, a R9 является Ph,
или группой формулы III, в которой R8 и R9 являются Br, a R10 является Ph,
или группой формулы III, в которой R8 и R10 являются Cl, a R9 является Ph,
или группой формулы III, в которой R8 и R9 являются Cl, a R10 является Ph,
или группой формулы III, в которой R8 и R10 являются Cl, a R9 является Br,
или группой формулы III, в которой R8 и R9 являются Cl, a R10 является Br,
или группой формулы III, в которой R8 является H, R9 и R10 являются Br,
или группой формулы III, в которой R8 является H, a R10 и R9 являются Cl,
или группой формулы III, в которой R8 является H, a R10 и R9 являются F,
или группой формулы III, в которой R8 является H, a R10 является CF3, и R9 является Cl,
или группой формулы III, в которой R8 является H, a R9 является CF3, и R10 является Cl,
или группой формулы III, в которой R8 является H, a R10 является CF3, и R9 является Br,
или группой формулы III, в которой R8 является H, a R9 является CF3, и R10 является Br,
или группой формулы III, в которой R8 является H, a R10 является CF3, и R9 является F,
или группой формулы III, в которой R8 является H, a R9 является CF3, и R10 является F,
или группой формулы III, в которой R8 и R10 являются H, a R9 является CN,
или группой формулы III, в которой R8 и R9 являются Br, a R10 является CF3,
или группой формулы III, в которой R8 и R10 являются Br, а R9 является CF3,
или группой формулы III, в которой R8 является Br, R9 является Br и R10 является Cl,
или группой формулы III, в которой R8 является Br, R10 является Br и R9 является Cl,
или группой формулы III, в которой R8 является CH3, R9 и R10 являются Br,
или группой формулы III, в которой R8 является CH3, R9 и R10 являются F,
или группой формулы III, в которой R8 является CH3, R9 и R10 являются H,
или группой формулы III, в которой R8 является H, R9 и R10 являются CH3,
или группой формулы III, в которой R8, R9 и R10 являются каждый Br,
или группой формулы IV.
R3 предпочтительно представляет H, C1-16алкил, NH2, NH (C1-6 алканоил), NH (C1-6 алкоксикарбонил), N (C1-6 алкоксикарбонил)2, NH (C1-6алкил)2, N-пирролил, галоген, или S(О)n (C1-6 алкил, необязательно замещенный одним или более атомами галогена), где n равно 0, 1 или 2.
R3 более предпочтительно представляет H, CH3, NH2, N-пирролил, N(CH3)2, NH(CO2(трет-бутил)), N(CO2 (трет-бутил))2, NHCOCH3, Br, Cl, SCH3 или SCF3.
R4 и R6 предпочтительно являются галогенами.
R4 и R6 более предпочтительно являются Cl.
R5 предпочтительно является C1-6 алкилом, необязательно замещенным одним или более атомами галогена, C1-6 алкоксилом, необязательно замещенным одним или более атомами галогена, C1-6 алкилтиогруппой, необязательно замещенной одним или более атомами галогена, SF5 или галогеном.
R5 более предпочтительно является CF3, OCF3, SCF3 или SF5.
Наиболее предпочтительными являются следующие соединения (и их соли):
3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-этинилпиразол;
3-циано-1-(2,6-дихлор-4-трифторметоксифенил)-4-этинилпиразол;
3-циано-1-(2,6-дихлор-4-трифторметилсульфенилфенил)-4-этинилпиразол;
4-(2-бром-1,2 -дихлорэтенил-3-циано-1-(2,6-дихлор-4-трифторметоксифенил) пиразол:
3-циано-1-(2,6-дихлор-4-трифторметоксифенил)-4-трибромэтенилпиразол;
4-(2,2-дибромэтенил)-3- циано-1-(2,6-дихлор-4-трифторметилфенил) пиразол;
3-циано-4-(2,2-дихлорэтенил)-1-(2,6-дихлор-4-трифторметилфенил) пиразол;
3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4(2,2-дифторэтенил) пиразол;
3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-трибромэтенилпиразол;
3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-трихлорэтенилпиразол;
4-(2-бром-1,2-дихлорэтенил)-3-циано-1-(2,6-дихлор-4-трифторметилфенил) пиразол;
4-(2-хлор-1,2-дибромэтенил)-3-циано-1-(2,6-дихлор-4- трифторметилфенил) пиразол;
3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-(1-метил-2,2-дибромэтенил) пиразол;
3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-(1-метил-2,2-дифторэтенил) пиразол;
1-(2,6-дихлор-4-трифторметилфенил)-4-этинил-3-трифторметилпиразол;
4-(2-бром -1,2-дихлорэтенил)-1-(2,6-дихлор-4-трифторметилфенил)- 3-трифторметилпиразол;
1-(2,6-дихлор-4-трифторметилфенил)-4-этинил-3-метилпиразол.
Соединения формулы (I) обладают одним или более асимметрическими центрами и таким образом могут существовать в двух или более стереоизомерных формах. Настоящее изобретение включает в себя все индивидуальные стереоизомеры соединений формулы (I) и их смеси.
Разделение диастереоизомеров может быть достигнуто обычными методами, например, дробной кристаллизацией, хроматографией или ВЭЖХ стереоизомерной смеси соединения формулы (I) или его подходящей соли или производного. Индивидуальный энантиомер соединения формулы (I) можно также получить из соответствующего оптически чистого интермедиата или при разделении, таком, как при ВЭЖХ, соответствующего рацемата с использованием подходящей хиральной подложки, или дробной кристаллизацией диастереомерных солей, образованных при взаимодействии соответствующего рацемата с подходящей оптически активной кислотой или основанием.
Далее настоящее изобретение обеспечивает методы получения соединений изобретения, которые описаны ниже и проиллюстрированы Примерами.
Метод 1
Получение соединения формулы (I), в которой R2 является группой формулы II (C  CR7), реакцией соединения формулы V:
CR7), реакцией соединения формулы V:
в котором R1 и R3-6 определены выше, a R2A является 1, Br или трифторметилсульфонатом, с соединением формулы HC  CR7, где R7 определен выше. Реакция предпочтительно проводится в присутствии палладиевого катализатора, например бис(трифенилфосфин) палладий (II) хлорида [PdCl2(PPh3)2] и йодида меди. Альтернативно, соответствующие алкилкупратные соединения, полученные из HC
CR7, где R7 определен выше. Реакция предпочтительно проводится в присутствии палладиевого катализатора, например бис(трифенилфосфин) палладий (II) хлорида [PdCl2(PPh3)2] и йодида меди. Альтернативно, соответствующие алкилкупратные соединения, полученные из HC  CR7, могут быть получены заранее и введены в реакцию с соединением формулы V, как определено выше.
CR7, могут быть получены заранее и введены в реакцию с соединением формулы V, как определено выше.
Реакция предпочтительно проводится в растворителе, который не оказывает неблагоприятного влияния на реакцию (например, в триэтиламине и/или диметилформамиде (ДМФА)).
Соединения формулы 1, в котором R2 является HC  CR7, могут быть превращены друг в друга с использованием обычных методов: например, соединения, в которых R7 является C1-6 триалкилсинильной группой, можно превратить в соединения, в которых R7 является H при действии основания, такого как карбонат калия, в растворителе, таком как метанол.
CR7, могут быть превращены друг в друга с использованием обычных методов: например, соединения, в которых R7 является C1-6 триалкилсинильной группой, можно превратить в соединения, в которых R7 является H при действии основания, такого как карбонат калия, в растворителе, таком как метанол.
Соединения формулы V, в которой R2A является 1 или Br, можно получить из соответствующего соединения формулы V, в котором R2A является H, при взаимодействии с йодирующим или бромирующим агентом, таким как N - (йод или бром) сукцинимид.
Соединения формулы V, в которых R2A является H, доступны коммерчески или доступны при помощи обычных методов, или методов, описанных здесь и их подходящих приложений.
Метод 2
Получение соединения формулы I, в котором R2 является группой формулы III, взаимодействием соединения формулы V, в которых R2A является 1, с подходящими винильными соединениями, такими как соединения винил (триалкил) олова, необязательно в присутствии каталитического количества соединения Pd, и затем, при необходимости, галоидированием полученного соединения. Реакцию предпочтительно проводят в присутствии палладиевого катализатора, например, тетракис (трифенил-фосфин) палладий (O) или ацетата палладия. Реакцию предпочтительно проводят в растворителе, который не оказывает неблагоприятного воздействия на реакцию (например, в триэтиламине или ДМФА), при или около 75oC. Галоидирование проводят с использованием обычных методов.
Метод 3
Получение соединения формулы I, в котором R2 является группой формулы IV, взаимодействием соединения формулы V, определенного выше, в котором R2A является H, с циклогексаноном. Реакцию предпочтительно проводят в органической кислоте (например, в уксусной кислоте) при или около 120oC.
Соединения формулы V, в которых R1 является CN, NO2, CHO, C1-6 алканоильной или C1-6 алкильной группой, произвольно замещенной одним или более атомами галогена; R2A является H, R3 является NH2, OH, C1-6 алкоксильной группой или S(О)n (C1-6 алкильной группой, произвольно замещенной одним или более атомами галогена); а R4-6 определен выше, либо известны, либо доступны с использованием известных методов.
Метод 4
Получение соединения формулы I, в котором R1 является C1-6 алкоксикарбонилом, обработкой соответствующего соединения формулы 1, в котором R1 является CN, основанием в присутствии соответствующего спирта. Подходящие основания включают в себя карбонат калия и гидроокись калия. Эту реакцию можно проводить при комнатной температуре или близкой к ней.
Метод 5
Получение соединения формулы I, в котором R3 является галогеном, при обработке соответствующего соединения формулы I, в котором R3 является NH2, алкил нитритом, таким как н-бутил нитрит, и подходящим источником галогена. Подходящий источник галогена включает в себя бромоформ. Реакцию предпочтительно проводят в растворителе, который не оказывает неблагоприятного воздействия на реакцию (например, в ацетонитриле), при или около 70oC.
Метод 6
Получение соединения формулы I, в котором R3 является H, обработкой соответствующего соединения формулы I, в котором R3 является NH2, алкил нитритом, таким как н-бутил нитрит. Реакцию предпочтительно проводят в растворителе, который не оказывает неблагоприятного воздействия на реакцию (например, в тетрагидрофуране), при температуре кипения растворителя с обратным холодильником.
Метод 7
Получение соединения формулы I, в котором R3 является N-пирролилом, обработкой соответствующего соединения формулы I, в котором R3 является NH2, 2,5-диалкокситетрагидрофураном, таким как 2,5-диметокситетрагидрофуран, в присутствии кислоты. Реакцию предпочтительно проводят, используя органическую кислоту, такую как уксусная кислота, при повышенной температуре, такой как температура кипения с обратным холодильником уксусной кислоты.
Метод 8
Получение соединения формулы I, в котором R3 является S(О)n (C1-6 алкильной группой, произвольно замещенной одним или более атомами галогена), обработкой соответствующего соединения формулы I, в котором R3 является NH2, алкилнитритом, таким как н-бутилнитрит, и ди (C1-6 алкил, произвольно замещенного одним или более атомами галогена) дисульфидом, и при необходимости, окислением соединения формулы I, в котором R3 является S(C1-6 алкилом, произвольно замещенным одним или более атомами галогена). Соединение формулы I, в котором R3 является S(О)n (C1-6 алкил, произвольно замещенный одним или более атомами галогена), а n равно 1 или 2, можно получить окислением соединения формулы I, в котором R3 является S(О)n (C1-6 алкилом, произвольно замещенным одним или более атомами галогена), а n равно 0 или 1. Эту реакцию предпочтительно проводят, нагревая соединение формулы I, в котором R3 является NH2, с дисульфидным соединением в подходящем растворителе, который не оказывает неблагоприятного влияния на реакцию (например, в ацетонитриле), при повышенных температурах, с последующим прибавлением алкилнитрита и дальнейшем нагревании. Окисление сульфида (или сульфоксида) можно осуществить с использованием обычных методов, например, при использовании пертрифторуксусной кислоты.
Метод 3
Получение соединения формулы I, в котором R2 является группой формулы III, в которой каждый из R9-10 является галогеном, взаимодействием соединения формулы V, в котором R1 и R3-6 определены выше, a R2A является COR8, с три (алкил или арил) - замещенным фосфином и тетрагалогенидом углерода. Тризамещенным фосфином предпочтительно является трифенилфосфин.
Соединения формулы V, в которых R2A является CO(C1-6 алкил, произвольно замещенный одним или более атомами галогена) можно получить из соответствующего соединения формулы I, в котором R2 является C (C1-6 алкил, произвольно замещенный одним или/ более атомами галогена) = CH2 при взаимодействии с окислительной системой, такой как N-метилморфолин оксид/тетроксид осмия (кат. ) /метаперйодат натрия. Альтернативно соединения формулы V, в которых R2A является CO(CH2 (C1-5 алкил, произвольно замещенный одним или более атомами галогена), можно получить из соответствующего соединения формулы I, в котором R2 является группой формулы II, где R7 является (C1-5 алкил, произвольно замещенный одним или более атомами галогена), при гидратации, например, при взаимодействии с полугидратом толуолсульфоновой кислоты в сыром ацетонитриле.
Метод 10
Получение соединения формулы I, в котором R2 является группой формулы III, в которой R8 является H и один из R9 и R10 является галогеном, а другой CF3 взаимодействием соединения формулы V, в котором R1 и R3-6 определены выше, a R2A является CHO, с соединением формулы (галоген)3CCF3 в присутствии галогенида цинка, такого как хлорид цинка, и галогенида меди, такого как хлорид меди. Реакцию предпочтительно проводят в присутствии полярного растворителя, такого как N,N-диметилформамид.
Получение соединения формулы I, в котором R2 является группой формулы III, в которой R8 является H и один из R9 и R10 является Cl, Br или 1, а другой C (Cl, Br или l)3 доступно аналогичным способом с использованием реагентов формулы (Cl, Br или l)3CC (Cl, Br или l)3. Менее реакционноспособная связь C - галоген не разрывается, и C (Cl, Br или l)3 группа, содержащая эту связь, переносится так же, как случае переноса упомянутой выше CF3 группы.
Соединения формулы V, в которых R2A является CHO можно получить из соответствующего соединения формулы I, где R2 является этенилом, при взаимодействии с окислительной системой, такой как N-метилморфолин оксид / тетроксид осмия (кат.) / метаперйодат натрия.
Метод 11
Получение соединения формулы I, в котором R2 является группой формулы II, взаимодействием соединения формулы V, в котором R2A является I, с соединением R7-C  C-Sn, таким как соединение R7-C
C-Sn, таким как соединение R7-C  C-Sn(алкил)3. Реакцию предпочтительно проводят в присутствии палладиевого катализатора, например тетракис (трифенилфосфин) палладия (O). Реакцию предпочтительно проводят в растворителе, который не оказывает неблагоприятного влияния на реакцию (например, в диметилформамиде), при или около 75oC.
C-Sn(алкил)3. Реакцию предпочтительно проводят в присутствии палладиевого катализатора, например тетракис (трифенилфосфин) палладия (O). Реакцию предпочтительно проводят в растворителе, который не оказывает неблагоприятного влияния на реакцию (например, в диметилформамиде), при или около 75oC.
Метод 12
Получение соединения формулы I, в котором R2 является группой формулы II, a R7 не является H, взаимодействием соединения формулы I, в котором R2 является группой формулы II и R7 является H, с реагентом, способным реагировать как (R7)+ синтон, таким как R7Z, где Z является подходящей удаляемой группой, такой как хлор, бром, йод, или алкильной или сульфонатной группой, необязательно в присутствии основания. Реакцию проводить с соединением R7l, например, в присутствии йодида меди и соединения PdII, такого как бис (трифенилфосфин) палладий (II) хлорида и основания, такого как триэтиламин.
Метод 13
Получение соединения формулы I, в котором R2 является группой формулы II, a R7 является C1-6 алкоксикарбонилом, взаимодействием соединения формулы I, в котором R2 является группой формулы II и R7 является CN, с C1-6 спиртом, необязательно в присутствии основания. Подходящие основания включают в себя карбонат калия и гидроксид калия. Реакцию можно проводить при или около комнатной температуры.
Метод 14
Получение соединения формулы I, в котором R2 является группой формулы II, a R7 является C1-6 алкоксикарбонилом, при окислении соединения формулы I, в котором R2 является группой формулы II и R7 является CH2OH, образованием соответствующей кислоты, с последующей этерификацией C1-6 спиртом. Этот процесс обычно проводят с использованием двуокиси марганца/цианида калия в спирте.
Метод 15
Получение соединения формулы I, в котором R3 является NH (C1-6 алканоилом), взаимодействием соединения формулы I, в котором R3 является NH2, с ацилирующим агентом, таким C1-6 аканоил (хлорид, бромид или йодид). Этот процесс предпочтительно проводят с хлорангидридом кислоты и акцептором кислоты, таким как пиридин.
Метод 16
Получение соединения формулы I, в котором R3 представляет N (C1-6алкоксикарбонил)2, взаимодействием соединения формулы I, в котором R3 является NH2, с ди(C1-6 алкил) дикарбонатом. Этот процесс предпочтительно проводят, используя основную систему, такую как триэтиламин / 4-диметиламинопиридин (ДМАП) в растворителе, таком как ДМФА.
Метод 17
Получение соединения формулы I, в котором R3 представляет NH (C1-6 алкоксикарбонил), взаимодействием соединения формулы I, в котором R3 представляет N (C1-6алкоксикарбонил)2, с кислотой. Этот процесс предпочтительно проводят с использованием трифторуксусной кислоты (ТФУ) в растворителе, таком как хлористый метилен.
Метод 18
Получение соединения формулы I, в котором R3 представляет N (C1-6алкил)2, взаимодействием соединения формулы 1, в котором R3 является NH2 с C1-6 алкилирующим агентом, таким как алкил (хлорид, бромид или йодид). Предпочтительно реакцию проводят с использованием алкилйодида. Предпочтительно реакцию проводят в присутствии основания, такого как NaH. Предпочтительно реакцию проводят в подходящем растворителе, таком как ТГФ.
Соединения формулы I, в которых R3 является амино производным, можно получить из соединений формулы I, в которых R3 является NH2, используя обычные методы, такие, как приведенные выше.
Метод 19
Получение соединения формулы I, в котором R2 является группой формулы III, в которой некоторые или все из R8, R9 и R10 являются галогенами, взаимодействием соединения формулы I, где R2 представляет группу формулы II с галогеном, необязательно в присутствии основания. Примером является взаимодействие алкина, в котором R7 является H, с бутиллитием, затем с источником галогена, предпочтительно в эфирном растворителе, с образованием соединений, где R8, R9 и R10 все являются галогенами. Взаимодействие алкина с любой R7 группой с источником галогена (таким, как Cl, Br2 или I2) приводит к 1,2-дигалогензамещенным соединениям.
Метод 20
Получение соединения формулы I, в котором R2 является группой формулы II, взаимодействием соединения формулы V, в котором R2A является I, с соединением формулы HC  CR7 в присутствии бутиллития, хлорида цинка и соединения палладия. Реакцию предпочтительно проводят в присутствии подходящего основания, такого как триэтиламин, и в подходящем растворителе, таком как ДМФА.
CR7 в присутствии бутиллития, хлорида цинка и соединения палладия. Реакцию предпочтительно проводят в присутствии подходящего основания, такого как триэтиламин, и в подходящем растворителе, таком как ДМФА.
Предпочтительно алкин растворяют в подходящем растворителе, таком как ТГФ, обрабатывают бутиллитием при пониженной температуре, затем добавляют хлорид цинка в растворителе и доводят температуру до окружающей. Предпочтительно смесь вновь охлаждают и прибавляют соединение палладия, такое как бис (трифенилфосфин) палладий хлорид, вместе с соединением формулы V, в котором R2A является I. Предпочтительно температуру реакции затем повышают, например, до температуры кипения растворителя с обратным холодильником.
Метод 21
Получение соединения формулы I, в котором R2 является группой формулы II, где R7 является галогеном, взаимодействием соединения формулы I, в котором R2 является группой формулы III, в которой R является H, a R9 и R10 являются галогенами, с основанием, таким как 1,8-диазабицикло[5.4.0]ундец-7-ен (ДБУ).
Метод 22
Получение соединения формулы I, в котором R2 является группой формулы III, где R8 является H, фенилом или алкилом, взаимодействием соединения формулы V, в котором R2A является COR8, с соединением R9R10C = Ti. Примером соединения R9R10C = Ti является μ -хлор - μ -метилен-[бис (циклопентадиенил)титаний]диметилалюминий ("реагент Теббе"). Предпочтительно соединение формулы V, в котором R2A является COR8, растворяют в инертном растворителе, таком как тетрагидрофуран (ТГФ), охлаждают в инертной атмосфере, затем прибавляют соединение карбена титана и оставляют смесь нагреваться.
Метод 23
Получение соединения формулы I, в котором R2 является группой формулы III, где R8 является H, при взаимодействии соединения формулы V, в котором R2A является CHO, с соединением R9R10CH- фосфония (реакция Виттига), R9R10CH - силильным соединением (олефинирование по Петерсену) или R9R10CH-фосфатным соединением (реакция Хорнера - Эммонса или реакция Водсворта - Эммонса) в присутствии основания. Подобные реагенты доступны коммерчески или через обычные методы.
Метод 24
Получение соединения формулы I, в котором R2 является группой формулы III, взаимодействием соединения формулы V, в котором R2A является H, с соединением формулы R8COCHR9R10. Реакцию предпочтительно проводят в органической кислоте (например, в уксусной кислоте), предпочтительно при повышенных температурах, таких как около 120oC.
Метод 25
При желании или необходимости превращают соединение формулы I в его фармацевтически или ветеринарно пригодную соль. Фармацевтически или ветеринарно пригодную соль соединения формулы (I) легко получить смешиванием вместе растворов соединения формулы (I) и желательной кислоты или основания соответственно. Эту соль можно высадить из раствора и отделить фильтрованием или выделить другими способами, такими как упариванием растворителя.
Соединения изобретения доступны либо при помощи методов, описанных здесь в Методах и Примерах, или обычных методов, известных специалистам в данной области техники, или их подходящих приложений с использованием методов, известных в данной области техники.
Соединения изобретения можно выделить и очистить обычными методами. Имеющим опыт в данной области техники очевидно, что для чувствительных функциональных групп необходима защита и снятие защиты во время синтеза соединения изобретения. Этого можно достичь с помощью обычных методов, описанных, например, в издании "Защитные группы в органическом синтезе" Т. V. Green and P.G.M. Wuts, John Wiley and Sons Inc., 1991.
Соединения изобретения полезны, поскольку они обладают антипаразитической активностью в организмах человека, животных и растений. Они особенно полезны для обработки эктопаразитов.
Обращаясь прежде всего к использованию соединений изобретения для человека, обеспечиваются:
а) фармацевтические составы, включающие соединения изобретения в смеси с фармацевтически пригодным вспомогательным лекарственным веществом, разбавителем или носителем, которые пригодны для местного введения;
b) соединение изобретения, для использования в качестве лекарства;
с) использование соединения изобретения в производстве антипаразитических лекарств; и
d) способ лечения паразитического заражения у пациента, включающий введение эффективного количества соединения изобретения пациенту.
Что касается использования соединений изобретения для животных, то эти соединения можно вводить сами по себе или в составе, подходящем для рассматриваемого специального использования и для определенных видов животного - хозяина, которого лечат, и участвующего паразита. Способы, которыми можно вводить соединения, включают в себя оральный в виде капсулы, пилюли, таблетки или вливания лекарства, или наливаемые или наносимые составы, или, альтернативно, их можно вводить путем инъекции (например, подкожно, внутримышечно или внутривенно) или в виде имплантанта, или в виде раствора или спрея, или при использовании распылителя или шампуня.
Подобные составы готовят обычным способом в соответствии со стандартной фармацевтической и ветеринарной практикой. Эти капсулы, пилюли или таблетки готовят, смешивая активный ингредиент с подходящим тонко измельченным разбавителем или носителем, содержащим дополнительно разрыхляющий агент и/или связывающее вещество, такое как крахмал, лактоза, тальк или стеарат магния. Оральные дозы готовят путем растворения или суспендирования активного ингредиента в подходящей среде. Составы, вводимые путем инъекции, готовят в виде стерильного раствора, который может содержать другие вещества, например достаточное количество солей или глюкозы для того, чтобы сделать этот раствор изотоническим крови. Приемлемые жидкие носители включают в себя растительные масла, такие как кунжутное масло и т. п., глицериды, такие как триацетин и т. п., эфиры, такие как бензил, бензоат, изопропил мюристат и производные жирных кислот пропиленгликоля и т. п., а также органические растворители, такие как пирролидон, глицерин- формаль и т. п. Жидкие составы готовят путем растворения или суспендирования активного ингредиента в жидком носителе таким образом, чтобы конечный состав содержал от 0,5 до 60% по весу активного ингредиента. Твердые составы готовят способами, хорошо известными в данной области техники.
Эти составы будут различаться в том, что касается веса активного соединения, который зависит от вида животного - хозяина, которого лечат, тяжести и типа инфекции и веса тела хозяина. Для парэнтерального, местного и орального введения типичные пределы доз активного ингредиента составляют 0,1-50 мг на кг веса тела животного, предпочтительно в пределах 1- 5 мг на кг.
В качестве альтернативы соединения можно вводить с кормом животных и для этой цели можно приготовить концентрированную пищевую добавку или премикс для смешения с обычным кормом животного.
Соединение настоящего изобретения используются для борьбы с артроподами, растительными нематодами, глистами или простейшими паразитами. В частности, соединения настоящего изобретения можно использовать в области ветеринарии и домашнего скота в сельском хозяйстве и для защиты общественного здоровья от артроподов, глистов или простейших, которые паразитируют внутри или снаружи на позвоночных, в частности на теплокровных позвоночных, например на человеке и домашних животных, например на крупном рогатом скоте, овцах, козах, лошадях, свиньях, домашней птице, собаках, кошках и рыбах, например Acarina, включая клещей (например, виды lxodes, виды Boophilus, например Boophilus microplus, виды Amblyomma, виды Hyalomma, виды Rhipicephalus, например Rhipicephalus appendiculatus, виды Haemaphysalis, виды Dermacentor, виды Opnithodorus (например, Opnithodorus moubata и клещи (например, виды Damalinia, Dermahyssus gallinae, виды Sarcoptes, например Sarcoptes scabiei, виды Psoroptes, виды Chorioptes, виды Demodex, виды Eutrombicula) Diptera (например, виды Aedes, виды Anopheles, виды Musca, виды Hypoderma, виды Gastrophilus, виды Simulium); Hemiptera (например, виды Triatoma); Phthiraptera (например, виды Damalinia, виды Linognathus) Siphonaptera (например, виды Ctenocephalides); Dictyoptera (например, виды Periplaneta, виды Blatella); Htmenoptera, например Monomorium pharaonis), например, против инфекций желудочно-кишечного тракта, вызванных паразитическими круглыми червями, например членами семейства Trichostrongylidae, Nippostronylus brasiliensis, Trichinella spiralis, Haemonchus contortus, Trichostronylus colubriformis, Nematodirus battus, Ostertagia circumcincta, Trichostrongylus axei, видами Cooperia и Hymenolepis папа, против и при лечении протозойных заболеваний, вызванных, например, видами Eimeria, например Eimeria tenella, Eimeria acervulina, Eimeria brunetti, Eimeria maxima, Eimeria necatrix, Eimeria bovis, Eimeria zuerni и Eimeria ovinoidalis; Trypanosoma cruzi, видами Leishmania, видами Plasmodium, видами Babesia, видами Trichomonadidae, видами Histomonas, видами Giardia, видами Toxoplasma, Entamoeba histolytica и видами Theileria; для защиты хранящихся продуктов, например хлебных злаков, включающих зерно и крупчатку, арахис, корм животных, лесоматериалы и домашние продукты, например ковры и ткани, от артроподов, точнее жуков, включая долгоносиков, моль и клещей, например виды Ephestia (огневка мельничная), виды Anthrenus (кожееды), виды Tribolium (хрущак малый мучной), Sitophilus (долгоносик зерновой), виды Acarus (клещи), для борьбы с тараканами, муравьями и термитами и похожими членистоногими вредителями в зараженных домашних и производственных помещениях и для борьбы с личинками москитов в водных путях, колодцах, резервуарах или прочей протекающей или стоячей воде; для обработки фундаментов, сооружений и почвы для предотвращения атаки на здания термитов, например, видов Reticu-litermes, видов Heterotermes, видов Coptoterms, в сельском хозяйстве, против взрослых особей, личинок и яиц Lepidoptera (бабочки и моли), например, видов Heliothis, таких как Heliothis virescens (совка), Heliothis armioera и Heliothis zea, видов Spodoptera, таких как S. exempta, S. littoralis (египетская гусеница совки хлопковой), S. eridania (южный походный червь), Mamestra configurata (берта походный червь); видов Earias, например Е. insulana (египетский коробочный червь), видов Pectinophora, например Pectinophora gossypiela (розовый коробочный червь), видов Ostrinia, например О. nubilalis (европейский мотылек кукурузный), Trichoplusia ni (совка капустная), видов Pieris (мермитиды), видов Laphyqma (походные черви), видов Agrotis и Amantes (подгрызающая совка), видов Wiseana (порина моль), видов Chilo (точильщик стеблей риса), видов Tryporyza и видов Diatraea (огневка сахарного тростника и рисовый точильщик), Sparganothis pilleriana (листовертка виноградная), Cydia pomonella (плодожорка яблонная), видов Archips (листовертка), Plutella xylos-tella (моль капустная); против взрослых особей и личинок Coleoptera (жуки), например Hypothenemus hampei (точильщик жостера калифорнийского), видов Hylesinus (короеды), Anthonomus grandis (долгоносик хлопковый), видов Acalymma (листоеды), видов Lema, видов Psylliodes, Leptinotarsa decemlineata (колорадский жук), видов Diabrotica (блошки длинноусые), видов Gonocephalum (ложные проволочники), видов Agriotes (проволочники), видов Dermolepida и Heteronychus (личинки хруща), Phaedon cochleariae (горчичный жук), Lissorhoptrus oryzophilus (долгоносик рисовый водяной), Melioethes (пыльцовый жук), видов Ceutorhynchus, видов Rhynchophorus и Cosmopolites (корневые долгоносики), против Hemiptera, например, видов Psylla, видов Bemisia, видов Trialeurodes, видов Aphis, видов Myzuz, Megoura viciae, видов Phylloxera, видов Adelges, Phorodon humuli (тля хлопковая), видов Aeneolamia, видов Nephotettix (толстоголовка амброзии трехраздельной), видов Empoasca, видов Nilaparvata, видов Perkinsiella, видов Pyrilla, видов Aonidiella (щитовки красные померанцевые), видов Coccus, видов Pseudococcus, видов Helopeltis (москиты), видов Lygus, видов Dysdercus, видов Oxycarenus, видов Nezara; Nymenoptera, например видов Athalia и видов Cephus (пилильщики), видов Atta (муравьи листорезы); Diptera, например, видов Hylemyia (корневые мухи), видов Atherigona и видов Chlorops (мухи), видов Phytomyza (моли - минеры), видов Ceratitis (дрозофилы); Thysanoptera, таких как Thrips tabaci: Orthoptera, таких как Locusta и видов Schistocerca (саранча) и бескрылых, например, видов Gryllus и видов Acheta; Collembola, например, видов Sminthurus и видов Onychiurus (ногохвостки), Ioptera, например, видов Odontoterms (термиты), Dermaptera, например, видов Forficula (уховертки), а также прочих артроподов сельскохозяйственного значения, таких как Acari (клещи), например, видов Tetranychus, видов Panonychus и видов Bryobia (клещики паутинные), видов Eriophyes (галлообразующие клещи), видов Polypha-cotarsonemus; видов Bianiulus (двупарноногие), видов Scutigerella (симфилии), видов Oniscus (мокрицы) и видов Triops (ракообразные); нематоды, поражающие растения и деревья, важные для сельского хозяйства, лесоводства и садоводства либо непосредственно, либо путем распространения бактериальных, вирусных, микоплазматических или грибковых заболеваний растений, нематоды корневых наростов, такие как виды Meliodogyne (например, М. incognita); пузыревидные нематоды, такие как виды Globodera (например, G. rostochiensis), виды Heterodera (например, H. avenae); виды Radopholus (например, R. Similis); пораженные нематоды, такие как виды Pratylenchus (например, P. pratensis); виды Belonoliamus (например, В. gracilis); виды Tylenchulus (например, T. semipene - trans); виды Rotylenchius (например, R. reniformis); виды Rotylenchus (например, R. robustus); виды Helicotylenchus (например, H. multicinctus), виды Hemicycliophora (например, H. gracilis); виды Criconemoides (например, С. similis); виды Trichodorus (например, Т. primitivus); нематоды совки, такие как виды Xiphinema (например, X. diversicaudatum); виды Longidorus (например, L. elongatus); виды Hoplolaimus (например, H. coronatus); виды Aphelenchoides (например, A. ritzemabosi, A. besseyi); стеблевые и луковичные нематоды, такие как виды Ditylenchus (например, D. dipsaci).
Соединения настоящего изобретения также полезны для борьбы с членистоногими или нематодными вредителями растений. Активное соединение применяют обычно к очагу, в котором собираются бороться с артроподным или нематодным заражением, в количестве от 0,1 кг до около 25 кг активного соединения на гектар обрабатываемого очага. В идеальных условиях, в зависимости от вредителя, с которым борются, достаточную защиту может оказать и меньшее количество. С другой стороны, неблагоприятные погодные условия, сопротивление вредителя и прочие факторы могут потребовать использование активного ингредиента в более высоких пропорциях. Для некорневой подкормки можно использовать количество от 1 г до 1000 г/га.
В случае, когда вредитель рождается в земле, составы, содержащие активный компонент, равномерно распространяют на обрабатываемую площадь любым подходящим способом. При желании, их можно применить в общем на поле или площадь, на которой растет урожай, или в непосредственной близости к семени или растению, которое необходимо защитить от поражения. Активный компонент можно внести в почву при распылении с водой на этой площади, или представить его естественному действию дождя. При желании, во время или после применения, состав можно распространять в почву механически, например, при вспахивании или дисковании. Применять можно до посадки, при посадке, после посадки, но до того, как начнется прорастание или после прорастания.
Соединения изобретения можно применять к почве в твердых или жидких составах в основном для борьбы с теми нематодами, которые там обитают, но также и к листве, в основном для борьбы с теми нематодами, которые поражают надземные части растений (например, указанные выше виды Aphelenchoides и виды Ditylenchus).
Соединения изобретения полезны для борьбы с вредителями, которые кормятся частями растения, удаленными от точки применения, например, поедающих листья насекомых уничтожают соединения, примененные к корням. В дополнение, эти соединения способны уменьшать нападения на растение при помощи антипитающего и отпугивающего эффектов. Соединения изобретения особенно полезны
для защиты поля, фуража, плантации, теплицы, фруктового сада и виноградника или декоративных культур и плантационных и лесных деревьев, например зерновых (таких, как маис, пшеница, рис, сорго), хлопка, табака, овощей и салатов (таких, как бобы, капустные культуры, curcurbits, латука, лука, помидоров и перцев), полевых урожаев (таких, как картофель, сахарная свекла, арахис, соевые бобы, масличная капуста), сахарного тростника, пастбищ и фуража (такого, как маис, сорго, люцерна посевная), плантаций (таких, как чая, кофе, какао, бананов, пряностей), фруктовых садов и рощ (таких, как косточковых плодов и односемянных плодов, цитрусовых, киви, авокадо, манго, маслин и орехов), виноградников, декоративных растений, цветов и кустарников в парниках и в садах, и парках, лесных деревьев (как опадающих, так и вечнозеленых) в лесах, на плантациях и питомниках.
Также они полезны для защиты древесины (стоящей, срубленной, превращенной, хранящейся или строительной) от поражения пилильщиками (например, Urocerus) или жуками (например, scolytids, platypodids, lyctids, bostrychids, cerambycids, anobiids), или термитами, например, видов Reticulitemnes, видов Heterotermes, видов Coptotermes.
Они применимы для защиты хранящихся продуктов, таких как зерно, фрукты, орехи, специи и табак, вне зависимости от того, целые ли они, молотые или составляют продукты, от поражения молью, жуками и клещами. Защищенными от поражения молью и жуками являются также животные продукты, такие как кожа, волос, шерсть и перо в естественном или превращенном виде (например, ковры или ткани); кроме этого, хранящееся мясо и рыба от поражения жуками, клещами и мухами.
Соединения изобретения полезны при борьбе с артроподами, глистами или простейшими, которые вредны или распространяют, или выступают в качестве переносчиков заболеваний человека и домашних животных, например, упомянутых ранее, и в особенности при борьбе с клещами, вшами, блохами, галлицами и кусающими, надоедными и myiasis мухами. Соединения изобретения полезны при борьбе с артроподами, глистами или простейшими, которые находятся в домашних животных, или которые питаются внутри или на коже, или сосут кровь животного, в целях которой их можно вводить орально, парэнтерально, подкожно или местно.
Кокцидиоз, заболевание, вызываемое инфекциями простейших паразитов рода Eimeria, является важной потенциальной причиной экономической потери домашних животных и птиц, в особенности тех, которые выросли или содержатся в интенсивных условиях. Например, могут быть поражены крупный рогатый скот, овцы, свиньи и кролики, однако болезнь особенно значительна для домашней птицы, в частности для цыплят.
Заболевание домашней птицы обычно передается птицами, подхватившими инфекционный организм из помета на зараженной подстилке или земле, или при кормлении, или питье воды. Заболевание проявляется путем кровотечения, накопления крови в слепой кишке, появления крови в помете, слабости и расстройствах пищеварения. Это заболевание обычно заканчивается смертью животного, но рыночная стоимость домашней птицы, пережившей тяжелые инфекции, значительно снижается в результате этой инфекции.
Введение небольшого количества соединения изобретения предпочтительно в сочетании с птичьим кормом эффективно для предотвращения или значительного уменьшения случаев кокцидиоза. Эти соединения эффективны как против формы слепой кишки (вызванной Е. tenella), так и против кишечной формы (вызванной главным образом Е. acervulina, Е. brunetti, Е. maxima и Е. necatrix).
Соединения изобретения оказывают также ингибирующий эффект по отношению к ооцистам, значительно снижая число и/или споруляцию возникших ооцист.
Поэтому, согласно дальнейшему аспекту изобретения, в нем обеспечиваются ветеринарные антипаразитические составы, включающие соединение изобретения в смеси с совместимым вспомогательным лекарственным веществом, разбавителем или носителем. Состав предпочтительно применим для местного введения.
Кроме этого, изобретение обеспечивает соединение изобретения для использования в качестве антипаразитического; и способ лечения очага паразитического заражения, который включает в себя обработку этого очага эффективным количеством соединения изобретения. Предпочтительно очагом является шкура, или мех животного, или растение, или семя, или область, окружающая растение или семя.
Кроме этого, изобретение обеспечивает способ обезвреживания или уничтожения паразита, включающий введение упомянутому паразиту или в его очаг эффективного количества соединения формулы (I), или его соли или состава, как описано ранее.
Следует понять, что упоминание о лечении включает в себя профилактику, а также облегчение установленных симптомов паразитического заражения.
Тест на инсектицидную активность
Взрослых мух (Stomoxys calcitrans) собрали и усыпили, используя CO2 1 μ I раствора ацетона, содержащего тестовое соединение, ввели непосредственно в грудную клетку мухи. После этого мух осторожно поместили в 50 мл пробирку, накрытую влажной марлей, чтобы они пришли в себя после CO2. Контрольными опытами было введение в них 1 μ I ацетона. Смертность оценивали спустя 24 часа после введения дозы.
Изобретение иллюстрировано следующими примерами, в которых точки плавления были определены с использованием аппаратуры для плавления Gallenkamp и неточны; данные ядерного магнитного резонанса были получены с использованием Bruker AC300 или AM300; масс-спектрометрические данные были получены на Finnigan Mat. TSQ 7000 Fisons Instruments Trio 1000 - расчетные и наблюдаемые приведенные ионы относятся к изотопному составу самой низкой массы.
Примеры
Пример A1 (иллюстративный)
5-Амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-йодпиразол
К раствору 5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил) пиразола (5.0 г, соединение из Ссылки Примера 1 из ЕР 295,117 A1) в ацетонитриле (60 мл) при перемешивании при комнатной температуре, порциями в течение 5 минут прибавляли N-йодсукцинимид (3,52 г). Перемешивание продолжали в течение 1 часа, после чего смесь упарили досуха, получив при этом сырой продукт (8.2 г), все еще содержащий сукцинимид. Его можно использовать без дальнейшей очистки или, при желании, очистить распределением между хлористым метиленом и водой, отделить, высушить (MgSO4) и упарить органический слой, получив желтый твердый остаток. При растирании с гексаном целевое соединение получают в виде белых кристаллов, Т. пл. 213oC (разл.).
Пример A2
5-Амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- триметилсилилэтинилпиразол
К раствору 5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4 йодпиразола (6.96 г, сырой продукт из Примера 1) в триэтиламине (30 мл) и диметилформамиде (6 мл) при перемешивании при комнатной температуре прибавили триметилсилилацетилен (3 мл), йодид меди (150 г) и бис (трифенилфосфин) палладий (II) хлорид (300 мг). Смесь нагревали при 50 - 60oC в течение одного часа, затем добавили триметилсилилацетилен (0.3 мл) и продолжали перемешивание и нагревание еще в течение 30 минут. Охлажденную реакционную смесь разбавили водой (250 мл) и экстрагировали эфиром (250 мл). Органический слой разделили (при помощи прибавления рассола). Водный слой повторно экстрагировали эфиром (250 мл). Объединенные органические экстракты высушили (MgSO4) и упарили, получив сырой продукт в виде смолы (4,67 г), при очистке колоночной хроматографией на силикагеле с элюированием хлористым метиленом:гексаном (1: 1) с последующей перекристаллизацией из смеси эфир/гексан целевой продукт был получен в виде белых кристаллов с Т. пл. 181-2oC.
ПМР (CDCl3) δ: 0.2 (с, 9H), 4.1 (ушир. с, 2H), 7.7 (с, 2H)
MS (термораспыление): М/Z [М+NH4] 434.2; C16H13Cl2F3N4Si + NH4 составляет 434.0
Пример A3
5-Аминo-3-цианo-1-(2,6-дихлор-4-трифторметилфенил)-4-этинилпиразол
К раствору 5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4 триметилсилилэтинилпиразола (2.0 г, сырой продукт из Примера А2) в метаноле (30 мл) при перемешивании прибавили карбонат калия (1 г). Спустя 10 минут при комнатной температуре реакционную смесь распределили между эфиром (100 мл) и водой (100 мл). Органический слой отделили, промыли рассолом (100 мл), высушили (MgSO4) и упарили. При очистке остатка колоночной хроматографией на силикагеле с элюированием хлористым метиленом:гексаном с последующей перекристаллизацией из эфира целевой продукт был получен в виде белых кристаллов с Т.пл. 215-216oC.
ПМР (CDCl3) δ: 3.49 (с. 1H), 4.2 (ушир. с, 2H), 7.8 (с. 2H)
MS (термораспыление): М/Z [М+ NH4] 362.4; C13H5Cl2F3N4 + NH4 составляет 362.0.
Пример A4
5-Амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-(проп-1-инил) пиразол
К раствору 5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- йодпиразола (0.904 г, соединение из Примера A1) в диметилформамиде (2 мл) и триэтиламине (10 мл), находившемуся в автоклаве из нержавеющей стали, при перемешивании прибавили йодид меди (60 мг) и бис (трифенилфосфин) палладий (II) хлорид (120 мг). Реакционный сосуд охладили до - 70oC и сконденсировали в него пропин (2 г). Сосуд герметично закрыли и нагревали при 79oC в течение 18 часов, а затем оставили его при комнатной температуре на два дня. Реакционную смесь распределили между эфиром и водой. Органический слой отделили, промыли рассолом, высушили (MgSO4) и упарили. При очистке остатка колоночной хроматографией на силикагеле с элюированием хлористым метиленом:гексаном (1: 1) целевой продукт был получен в виде белых кристаллов с Т. пл. 226 - 8oC.
ПМР (CDCl3) δ: 2.2 (с, 3H), 4.19 (ушир. с, 2H), 7,78 (с, 2H)
MS (термораспыление): M/Z [М+H] 358.9; C14H7Cl2F3N4 + H составляет 359.0
Пример A5
5-Амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-(3-метилбутил-1- инил)пиразол
К раствору 5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- йодпиразола (447 мг, соединение из Примера A1) в триэтиламине (10 мл) при перемешивании при комнатной температуре прибавили 3-метилбут-1-ин (0.5 мл), йодид меди (15 мг) и бис(трифенилфосфин)палладий (II) хлорид (30 мг). Реакционную смесь нагревали при 70oC в течение двух часов. Реакционную смесь разделили между эфиром (100 мл) и водой (100 мл). Органический слой отделили, промыли рассолом, высушили (MgSO4) и упарили. При очистке остатка колоночной хроматографией на силикагеле с элюированием хлористым метиленом:гексаном (1: 1) целевой продукт был получен в виде бледно-желтых кристаллов с Т.пл. 210-2oC.
ПМР (CDCl3) δ: 1.3 (д, 6H), 2.83 (г, 1H), 4,0 (ушир. с, 2H), 7.78 (с, 2H).
MS (термораспыление): M/Z [М+H] 387.0; C16H11Cl3F3N4 + H составляет 387.
Пример A6
5-Амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-(3-гидроксипроп- 1-инил)пиразол
К раствору 5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- йодпиразола (200 мг, соединение из Примера A1) в триэтиламине (2 мл) и диметилформамиде (1 мл) при перемешивании при комнатной температуре прибавили пропаргиловый спирт (0.2 мл), йодид меди (10 мг) и бис(трифенилфосфин) палладий (II) хлорид (20 мг). Реакционную смесь нагревали при 70oC в течение двух часов. Реакционную смесь разделили между эфиром (10 мл) и водой (10 мл). Органический слой отделили, промыли рассолом, высушили (MgSO4) и упарили. При очистке остатка колоночной хроматографией на силикагеле с элюированием эфиром: хлористым метиленом (10:1) целевой продукт был получен в виде бледно-желтых кристаллов с Т. пл. 237 - 9oC.
ПМР (d6-DMSO) δ: 4.32 (д, 2H), 5.3 (т, 1H), 6.58 (ушир. с, 1H), 8.28 (с, 2H)
MS (термораспыление): М/Z [М+ NH4] 391.8; C14H7Cl2F3N4O + NH4 составляет 392.0.
Пример A7
5-Амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- (4-гидроксибут-1-инил)пиразол
К раствору 5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- йодпиразола (447 мг, соединение из Примера A1) в триэтиламине (20 мл) и диметилформамиде (2 мл) при перемешивании при комнатной температуре прибавили 3-бутин-1-ол (0.5 мл), йодид меди (15 мг) и бис(трифенилфосфин)палладий (II) хлорид (30 мг). Реакционную смесь нагревали при 70oC в течение двух часов. Реакционную смесь распределили между эфиром (10 мл) и водой (10 мл). Органический слой отделили, промыли рассолом, высушили (MgSO4) и упарили. При очистке остатка колоночной хроматографией на силикагеле с элюированием эфиром целевой продукт был получен в виде светло-коричневых кристаллов с Т.пл. 215-6oC.
ПМР (CDCl3) δ: 2.72 (т, 2H), 3.49 (м, 1H), 3.87 (м, 2H), 4.1 (ушир. с, 1H), 7.8 (с, 2H)
MS (термораспыление): М/Z [М+ NH4] 406.4; C15H9Cl2F3N4O + NH4 составляет 406.0
Пример A8
5-Амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- метоксикарбонилэтинилпиразол
К раствору 5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- (3-гидроксипроп-1-инил)пиразола (250 мг, соединение из Примера A6) в эфире (10 мл) при перемешивании прибавили двуокись марганца (1 г) и перемешивали смесь при комнатной температуре в течение двух часов. После этого добавили метанол (2 мл) и цианид калия (250 мг) и продолжили перемешивание в течение 15 минут. Реакционную смесь отфильтровали и упарили досуха. Остаток очистили хроматографией на силикагеле с элюированием хлористым метиленом. При объединении и упаривании соответствующих фракций целевое соединение было получено в виде светло-коричневых кристаллов с Т. пл. 201 - 2oC.
ПМР (CDCl3) δ: 3.82 (с, 3H), 4.6 (ушир. с, 2H), 7.81 (с, 2H)
MS (термораспыление): М/Z [М+ NH4] 420.5; C15H7Cl2F3N4O2 + NH4 составляет 420.0
Пример A9
5-Амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-фенилэтил)пиразол
К раствору 5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- йодпиразола (250 мг, соединение из Примера A1) в диметилформамиде (2 мл) при перемешивании при комнатной температуре прибавили 2-фенилэтинилтри-н- бутилолово (0.6 мл) и тетракис (трифенилфосфин) палладий (0) (30 мг). Реакционную смесь нагревали при 75oC в течение двух часов и затем оставили на ночь при комнатной температуре. Реакционную смесь распределили между эфиром и водой. Органический слой отделили, промыли рассолом, высушили (MgSO4) и упарили. При очистке остатка колоночной хроматографией на силикагеле с элюированием сперва гексаном: хлористым метиленом (1: 1), а затем хлористым метиленом, целевой продукт был получен в виде светло - желтых кристаллов с Т. пл. 265 - 267oC;
ПМР (CDCl3) δ: 4.21 (ушир. с, 2H), 7.38 (м, 3H), 7,54 (м, 2H), 7.8 (с, 2H).
MS (термораспыление): M/Z [М+H] 420.8; C19H9Cl2F3N4 + H составляет 421.0
Пример A10
5-Амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- (тиен-2-илэтинил)пиразол
К раствору 5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- этинилпиразола (200 мг, соединение из Примера A3) в триэтиламине (4 мл) и диметилформамиде (1 мл) при перемешивании при комнатной температуре прибавили 2-йодтиофен (0.5 мл), йодид меди (15 мг) и бис (трифенилфосфин) палладий (II) хлорид (30 мг). Реакционную смесь нагревали при 60oC в течение одного часа. Реакционную смесь распределили между эфиром (100 мл) и водой (100 мл). Органический слой отделили, промыли рассолом, высушили (MgSO4) и упарили. При очистке остатка колоночной хроматографией на силикагеле с элюированием гексаном: хлористым метиленом (1: 1) целевой продукт был получен в виде светло-коричневых кристаллов с Т. пл. 262oC разл.
ПМР (CDCl3) δ: 4.23 (ушир. с, 1H), 7.05 (м, 1H), 7.45 (м, 2H), 7.8 (с, 2H)
MS (термораспыление): M/Z [М+H] 426.6; C17H7Cl2F3N4S + H составляет 427.0
Пример A11
5-Амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-(метоксипроп-1-инил) пиразол
К раствору 5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- йодпиразола (200 мг, соединение из Примера A1) в триэтиламине (2 мл) и диметилформамиде (1 мл) при перемешивании при комнатной температуре прибавили метилпропаргиловый эфир (0.5 мл), йодид меди (15 мг) и бис (трифенилфосфин) палладий (II) хлорид (30 мг). Реакционную смесь нагревали при 70oC в течение двух часов. Реакционную смесь распределили между эфиром (50 мл) и водным раствором лимонной кислоты (50 мл, 20 %). Органический слой отделили, промыли водой, высушили (MgSO4) и упарили. При очистке остатка колоночной хроматографией на силикагеле с элюированием хлористым метиленом целевой продукт был получен в виде бледно-желтых кристаллов с Т.пл. 210oC разл.
ПМР (CDCl3) δ: 3.48 (с, 3H), 4,2 (ушир. с, 2H), 4.89 (с, 2H), 7.8 (с, 2H)
MS (термораспыление): М/Z [М+ NH4] 406.0; C15H9Cl2F3N4O + NH4 составляет 406.0
Пример A12
5-Амино-1-(2,6-дихлор-4-трифторметилфенил)-3-этоксикарбонил-4- этинилпиразол
К раствору гидроксида калия (0.25 г) в этаноле (3 мл) прибавили 5-амино- 3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-триметилсилилэтинилпиразол (0.21 г). После выдерживания при 30oC в течение 30 минут реакционную смесь вылили в смесь воды (10 мл) и льда (10 г). Добавили эфира (30 л). Органический слой отделили. Водный слой экстрагировали эфиром (30 мл, х 2). Объединенные органические слои высушили (MgSO4) и упарили. Остаток очистили колоночной хроматографией на силикагеле (4 г) при элюировании хлористым метиленом. При объединении и упаривании соответствующих фракций с последующей кристаллизацией из смеси эфир/гексан целевое соединение было получено в виде светло-оранжевых кристаллов с Т. пл. 152- 154oC.
ПМР (CDCl3) δ: 1.42 (т, 3H), 3.49 (с, 1H), 4.11 (ушир. с, 2H), 4.43 (кв, 2H), 7.78 (с, 2H)
MS (термораспыление): М/Z [М] 391.3; C15H10Cl2F3N3O2 составляет 391.01
Пример A13
5-Амино-1-(2,6-дихлор-4-трифторметилфенил)-4-этинил-3-метоксикарбонилпиразол
К суспензии карбоната калия (0.03 г) в метаноле (2 мл) прибавили 5-амино- 3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-триметилсилилэтинилпиразол (0.03 г). После выдерживания при 25oC в течение 40 часов реакционную смесь вылили в воду (10 мл и экстрагировали эфиром (20 мл, x 2). Объединенные органические слои высушили (MgSO4) и упарили. Целевое соединение было получено при очистке остатка перекристаллизацией из смеси эфир/гексан.
ПМР (CDCl3) δ: 3.51 (с, 1H), 3.97 (с, 3H), 4.13 (ушир. с, 2H), 7.78 (с, 2H)
MS (термораспыление): М/Z [М] 377.0; C14H8Cl2F3N3O2 составляет 376.99
Пример B1 (иллюстрированный)
5-Ацетамидо-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-йодпиразол
К раствору 5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- йодпиразола (447 мг, соединение из Примера A1) в пиридине (5 мл) при перемешивании прибавили по каплям хлористый ацетил (0.5 мл). Реакционную смесь перемешивали при комнатной температуре в течение двух дней, а затем нагревали 4 часа при 50oC. Реакционную смесь распределили между эфиром (50 мл) и водой (50 мл), органический слой отделили, высушили (MgSO4) и упарили. Сырой продукт очистили колоночной хроматографией на силикагеле (40 г) при элюировании смесью эфир: гексан (10:1), получив при этом целевое соединение в виде белых кристаллов.
MS (термораспыление): М/Z [М+ NH4] 505.4; C13H6Cl2F3lN4O + NH4 составляет 505.9
Пример B2
5-Ацетамидо-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- триметилсилилэтинилпиразол
К раствору 5-ацетамидо-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- йодпиразола (80 мг, соединение из Примера B1) в триэтиламине (5 мл) при перемешивании добавили триметилсилилацетилен (0.1 мл), йодид меди (4 мг) и бис (трифенилфосфин) палладий (II) хлорид (8 мг). Реакционную смесь нагревали при 60oC в течение 1 часа, а затем вылили в воду (20 мл) и эфир (20 мл). Органический слой отделили, высушили (MgSO4) и упарили. Сырой продукт очистили колоночной хроматографией на силикагеле при элюировании смесью эфир: гексан (10:1), получив при этом целевое соединение в виде белых кристаллов.
MS (термораспыление): М/Z [М+NH4] 475.7; C18H15Cl2F3N4OSi + NH4 составляет 476.1
Пример B3
5-Ацетамидо-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-этинилпиразол
К раствору 5-ацетамидо-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- триметилсилилэтинилпиразола (20 мг, соединение из Примера B2) в метаноле (1 мл) добавили карбонат калия (20 мг). Реакционную смесь перемешивали при комнатной температуре в течение 40 минут, а затем вылили в воду (20 мл) и эфир (20 мл). Органический слой отделили, высушили (MgSO4) и упарили. Сырой продукт очистили колоночной хроматографией на силикагеле при элюировании эфиром, получив при этом целевое соединение в виде белых кристаллов.
ПМР (CDCl3) δ: 2.1 (с, 3H), 3.51 (с, 1H), 7.78 (с, 2H)
MS (термораспыление): M/Z [М+ NH4] 403.9; C15H7Cl2F3N4O + NH4 составляет 404.0
Пример B4
3-Циано-5-ди-(трет-бутоксикарбонил)аминo-1-(2,6-дихлор-4-трифторметилфенил)- 4-этинилпиразол
К раствору 5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- этинилпиразола (1.3 г, соединение из Примера A3) в диметилформамиде (4 мл) и триэтиламине (20 мл) прибавили ди-трет-бутилкарбонат (0.9 г) и 4-диметиламинопиридин (5 мг). И перемешивали смесь при комнатной температуре в течение шестнадцати часов. Затем добавили ди-трет-бутилкарбонат (0.45 г) и продолжали перемешивание в течение двух часов. После этого реакционную смесь вылили в эфир (200 мл) и водный раствор лимонной кислоты (200 мл, 20 %). Органический слой отделили, высушили (MgSO4) и упарили. Сырой продукт очистили колоночной хроматографией на силикагеле при элюировании смесью хлористый метилен:гексан (1:1), получив при этом целевое соединение в виде бледно-желтых кристаллов с Т. пл. 227 - 8oC.
ПМР (CDCl3) δ: 1.41 (с, 18H), 3.48 (с, 1H), 7.75 (с, 2H)
Элементный анализ - найдено: C, 50.66, H, 3.88, N, 10.27 %;
для C23H21Cl2F3N4O4 C, 50.34, H, 3.80, N, 10.04 %.
Пример B5
3-Циано-5-ди-(трет-бутоксикарбонил)-амино-1-(2,6-дихлор-4- тpифтоpмeтилфeнил)-4-бpoмэтинилпиpaзoл
К раствору 3-циано-5-ди-(трет-бутоксикарбонил)амино-1- (2,6-дихлор-4-трифторметилфенил)-4-этинилпиразола (100 мг, соединение из Примера B4) в ацетоне (10 мл) добавили нитрат серебра (5 мг) и N- бромсукцинимид (80 мг). Реакционную смесь перемешивали при комнатной температуре в течение одного часа, а затем вылили в эфир (100 мл) и воду (100 мл). Органический слой отделили, высушили (MgSO4) и упарили. Сырой продукт очистили колоночной хроматографией на силикагеле при элюировании хлористым метиленом, получив при этом целевое соединение в виде бледно-желтых кристаллов с Т. пл. 130-1oC.
ПМР (CDCl3) δ: 1.41 (с,18H), 7.75 (с, 1H)
MS (термораспыление): М/Z [М+ Na] 645.0; C23H20BrCl2F3N4O4 + Na составляет 645.0
Пример B6
5-Трет-бутоксикарбониламино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)- 4-бромэтинилпиразол
К раствору 3-циано-5-ди-(трет-бутоксикарбонил)амино-1-(2,6-дихлор-4- трифторметилфенил)-4-бромэтинилпиразола (200 мг, соединение из Примера B5) в безводном хлористом метилене (2 мл) прибавили по каплям трифторуксусную кислоту (0.2 мл). Спустя 30 минут реакционную смесь обработали эфиром (10 мл) и насыщенным водным раствором гидрокарбоната натрия (10 мл). Органический слой отделили, высушили (MgSO4) и упарили, получив при этом целевое соединение в виде белых кристаллов с Т. пл. 168- 70oC.
ПМР (CDCl3) δ: 1.38 (с, 9H), 6.23 (с, 1H), 7.75 (с, 2H)
MS (термораспыление): M/Z [М+ NH4] 539.6; C18H12BrCl2F3N4O4 + NH4 составляет 540.0
Пример B7 (иллюстративный)
5-Циано-1-(2,6-дихлор-4-трифторметилфенил)-4-йод-5-(N-пирролил)пиразол
Смесь 5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-йодпиразола (0.5 г) и 2,5-диметокситетрагидрофурана (1 мл) в уксусной кислоте (5 мл) кипятили 1 час. Реакционную смесь вылили в диэтиловый эфир (100 мл) и воду (100 мл). Органический слой промыли насыщенным водным раствором гидрокарбоната калия (50 мл) и высушили над MgSO4. При упаривании растворителя было получено целевое соединение.
ПМР (CDCl3) δ: 6.38 (с, 2H), 6.7 (с, 2H), 7.7 (с, 2H)
MS (термораспыление): М/Z [М+ NH4] 513.6; C15H6Cl2F3lN4 + NH4 составляет 513.9
Пример B8
3-Циано-1-(2,6-дихлор-4-трифторметилфенил)-5-(N-пирролил)- 4-триметилсилилэтинилпиразол
К раствору 3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-йод- 5-(N-пирролил) пиразола (0.55 г) в триэтиламине (1 мл) и диметилформамиде (10 мл) при перемешивании прибавили триметилсилилацетилен (1 мл) йодид меди (15 мг) и бис (трифенилфосфин) палладий (II) хлорид (30 мг). Реакционную смесь нагревали при 70oC в течение 24 часов, затем вылили в воду (100 мл) и диэтиловый эфир (100 мл). Органический слой высушили над MgSO4 и упарили растворитель. Сырой продукт очистили хроматографией на силикагеле (50 г) при элюировании смесью хлористый метилен:гексан 1:1, получив при этом целевое соединение в виде бледно-коричневых кристаллов.
Пример B9
3-Циано-1-(2,6-дихлор-4-трифторметилфенил)-4-этинил-5-(N-пирролил) пиразол
К раствору 3-циано-1-(2,6-дихлор-4-трифторметилфенил)-5-(N-пирролил- 4-триметилсилилэтинилпиразола (0.045 г) в хлористом метилене (5 мл) прибавили по каплям в течение 5 минут тетра-н-бутиламмоний фторид (0.1 мл, 1М в тетрагидрофуране). Реакционную смесь перемешивали 5 минут, а затем упарили, получив масло, которое хроматографировали на силикагеле (5 г) при элюировании хлористым метиленом. Целевое соединение было получено в виде бледно-коричневых кристаллов, Т. пл. 161 - 3oC.
ПМР (CDCl3) δ: 3.44 (с, 1H), 6.3 (м, 1H), 6.77 (м, 2H), 7.74 (с, 2H)
MS (термораспыление): M/Z [М+H] 394.9; C17H7Cl2F3N4 + H составляет 395.0
Пример B10
3-Циано-1-(2,6-дихлор-4-трифторметилфенил)-5-диметиламино-4-этинилпиразол
К раствору 5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- триметилсилилэтинилпиразола (0.417 г) в тетрагидрофуране (20 мл) при перемешивании порциями прибавили в течение 5 минут гидрид натрия (0.1 г, 60% дисперсии в масле). По каплям в течение 2 минут прибавили йодистый метил (0.156 мл). Через 5 минут добавили гидрид натрия (0.05 г) и йодистый метил (0.050 мл) и продолжили перемешивание еще в течение 5 минут. Реакционную смесь вылили в воду/диэтиловый эфир. Органический слой высушили над MgSO4 и упарили, получив при этом целевое соединение в виде бледно-коричневых кристаллов.
ПМР (CDCl3) δ : 2.83 (с, 6H), 3.42 (с, 1H), 7.78 (с, 2H)
MS (термораспыление): M/Z [М+H] 373.2; C15H9Cl2F3N4 + H составляет 373.02
Пример C1
5-Бром-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-триметилсилилэтинилпиразол
К раствору 5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- триметилсилилэтинилпиразола (30 мг, соединение из Примера A2) в ацетонитриле (0.5 мл) и бромоформа (0.5 мл) при перемешивании прибавили по каплям н-бутил нитрит (0.025 мл) в течение 5 минут. Смесь нагревали при 70oC в течение 30 минут, затем охладили и упарили. Остаток очистили колоночной хроматографией на силикагеле (40 г) при элюировании хлористым метиленом:гексаном (1:4), получив при этом целевое соединение в виде белых кристаллов с Т.пл. 130oC (разл).
ПМР (CDCl3) δ : 0.2 (с, 9H), 7.78 (с, 2H)
MS (термораспыление): М/Z [М+ NH4] 497.0, C16H11BrCl2F3N3Si + NH4 составляет 497.0
Пример C2
5-Бpoм-3-циaнo-1-(2,6-диxлop-4-тpифтормeтилфeнил)-4-этинилпиразол
К раствору 5-бром-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- триметилсилилэтинилпиразола (43 мг, соединение из Примера C1) в хлористом метилене (1 мл) при перемешивании прибавили по каплям в течение 5 минут тетра- н-бутиламмоний фторид (0.098 мл). Перемешивание продолжали при комнатной температуре в течение 30 минут. Затем реакционную смесь вылили в хлористый метилен (10 мл) и воду (10 мл). Органический слой отделили, высушили (MgSO4) и упарили. Остаток очистили колоночной хроматографией на силикагеле (10 г) при элюировании смесью хлористый метилен:гексан (1: 2), получив при этом целевое соединение в виде бледно-желтых кристаллов с Т.пл. 134-5oC.
ПМР (CDCl3) δ: 3.55 (с, 1H), 7.8 (с, 2H)
MS (термораспыление): М/Z [М+ NH4] 425.0; C13H3BrCl2F3N3 + NH4 составляет 424.9
Пример C3
5-Бром-1-(2,6-дихлор-4-трифторметилфенил)-4-этинил-3-метоксикарбонилпиразол
К раствору 5-бром-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- триметилсилилэтинилпиразола (100 мг, соединение из Примера C1) в метаноле (1 мл) при перемешивании прибавили карбонат калия (2.9 мг). Перемешивание продолжали при комнатной температуре в течение 2 часов, а затем добавили карбонат калия (3.0 мг). Перемешивание продолжали еще в течение 4 часов. Затем реакционную смесь вылили в эфир (10 мл) и воду (10 мл). Органический слой отделили, высушили (MgSO4) и упарили, получив при этом целевое соединение в виде белых кристаллов с Т. пл. 198oC
ПМР (CDCl3) δ : 3.6 (с, 1H), 4.09 (с, 3H), 7.79 (с, 2H)
MS (термораспыление): М/Z [М +H] 441.0; C14H6BrCl2F2N2O2 + H составляет 440.9
Пример C4
3-Циано-1-(2,6-дихлор-4-трифторметилфенил)-4-триметилсилилэтинилпиразол
К раствору 5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- триметилсилилэтинилпиразола (30 мг, соединение из Примера C1) в тетрагидрофуране (10 мл) при перемешивании прибавили по каплям н-бутил нитрит (0.025 мл) в течение 5 минут. Смесь кипятили в течение 30 минут, затем охладили и упарили. Остаток очистили колоночной хроматографией на силикагеле (50 г) при элюировании хлористым метиленом: гексаном (1:4), получив при этом целевое соединение в виде белых кристаллов с Т. пл. 128-9oC.
ПМР (CDCl3) δ: 0.3 (с, 9H), 7.72 (с, 2H); 7.78 (с, 2H)
MS (термораспыление): М/Z [М+ NH4] 419.0; C16H12Cl2F3N3Si + NH4 составляет 419.0
Пример C5
3-Циано-1-(2,6-диxлop-4-тpифтopмeтилфeнил)-4-этинилпиразол
К раствору 3-циано-1-(2,6-дихлор-4-трифторметилфенил)- 4-триметилсилилэтинилпиразола (201 мг, соединение из Примера C4) в хлористом метилене (5 мл) при перемешивании прибавили по каплям в течение 5 минут тетра-н-бутиламмоний фторид (0.55 мл). Перемешивание продолжали при комнатной температуре в течение 30 минут. Затем реакционную смесь вылили в хлористый метилен (10 мл) и воду (10 мл). Органический слой отделили, высушили (MgSO4) и упарили. Остаток очистили колоночной хроматографией на силикагеле при элюировании смесью хлористый метилен:гексан (1:4), получив при этом целевое соединение в виде бледно-желтых кристаллов с Т.пл. 130-2oC.
ПМР (CDCl3) δ : 3.4 (с, 1H), 7.79 (с, 1H + 2H)
MS (термораспыление): М/Z [М+ NH4] 347.0; C13H4Cl2F3N3 + NH4 составляет 347.0
Пример C6
5-Бромоэтинил-3-циано-1-(2,6-дихлор-4-трифторметилфен)-пиразол
К раствору 3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- этинилпиразола (100 мг, соединение из Примера C5) в ацетоне (5 мл) при перемешивании добавили N-бромсукцинимид (54.9 мг) и нитрат серебра (5 мг). Перемешивание продолжали при комнатной температуре в течение 60 минут. Затем реакционную смесь вылили в эфир (10 мл) и воду (10 мл). Органический слой отделили, высушили (MgSO4) и упарили. Остаток очистили колоночной хроматографией на силикагеле при элюировании смесью хлористый метилен:гексан (2:1), получив при этом целевое соединение в виде белых кристаллов с Т. пл. 166-8oC.
ПМР (CDCl3) δ : 7.78 (с, 1 H), 7.79 (с, 2H)
MS (термораспыление): М/Z [М+ NH4] 425.0; C13H3BrCl2F3N3 + NH4 составляет 424.9
Примеру C7
4-Хлорэтинил-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-пиразол
К раствору 3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- этинилпиразола (2 г) в ацетонитриле (50 мл) при перемешивании прибавили N- хлорсукцинимид (4 г) и кипятили смесь, нагревали при температуре кипения с обратным холодильником 1 час, после чего оставили ее на ночь при комнатной температуре. Добавили N-хлорсукцинимида (1.2 г) и смесь кипятили с обратным холодильником 2 часа. Добавили N-хлорсукцинимид (4 г) и смесь нагревали при температуре кипения с обратным холодильником 4 часа. Упарили реакционную смесь в вакууме и хроматографировали остаток на силикагеле при элюировании смесью хлористый метилен: гексан (5:1). Соответствующие фракции объединили и упарили, а полученный при этом твердый продукт очищали далее ВЭЖХ на колонке 21 х 250 мм DynamaxTM 0,005 мм ODS с обращенной фазой, при элюировании смесью ацетонитрил: 0.005М водная гептансульфоновая кислота:метанол (5:4:1) со скоростью 10 мл/минуту. При объединении соответствующих фракций и упаривании их неводных компонентов, с последующим распределением между диэтиловым эфиром и насыщенным водным раствором гидрокарбоната натрия, высушивании органического слоя и упаривания растворителя, целевое соединение было получено в виде белых кристаллов с Т.пл. 132-4oC.
ПМР (CDCl3) δ : 7.75 (с, 1H), 7.78 (с, 2H)
MS (термораспыление): М/Z [М+ NH4] 380.9; C13H3Cl3F3N3 + NH4 составляет 380.97
Пример C8
3-Циано-1-(2,6-дихлор-4-трифторметилфенил)-4-этинил-5-метилтиопиразол
К раствору 5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- триметилсилилэтинилпиразола (0.46 г) в ацетонитриле (20 мл) при перемешивании прибавили диметил дисульфид (0.108 мл) и нагрели смесь до 50oC. Прибавили н-бутил нитрит (0.401 мл) и нагрели реакционную смесь до 70oC за 30 минут. После охлаждения до комнатной температуры добавили тетра-н- бутиламмоний фторид (1.2 мл, 1М в гексане). Через 10 минут реакционную смесь вылили в диэтиловый эфир (50 мл) и воду (50 мл). Органический слой высушили (MgSO4) и удалили растворитель в вакууме. Остаток хроматографировали на силикагеле (50 г) при элюировании смесью хлористый метилен:гексан (2:1). При объединении и упаривании подходящих фракций были получены кристаллы, которые промыли гексаном. Гексановые смывы упарили и остаток далее хроматографировали на силикагеле (20 г) при элюировании смесью диэтиловый эфир:гексан (1:10). При объединении и упаривании подходящих фракций были получены белые кристаллы с Т. пл. 85 - 6oC
ПМР (CDCl3) δ : 2.56 (с, 3H), 3.51 (с, 1H); 7.79 (с, 2H)
MS (термораспыление): M/Z [M+H] 376; C14H6Cl2F3N3S + H составляет 375.97
Пример D1
5-Амино-3-циано-1-(2,6-дихлор-4-трифторметоксифенил)-4-йодпиразол
К раствору 5-амино-3-циано-1-(2,6-дихлор-4-трифторметоксифенил)пиразола (4.1716 г) в ацетонитриле (20 мл) при перемешивании при комнатной температуре прибавили N-йодсукцинимид (2.79 г). Спустя 15 минут смесь упарили до сухого остатка и растворили оставшийся оранжевый твердый осадок в хлористом метилене. Этот раствор промыли водой, затем рассолом, высушили (Na2SO4) и упарили, получив при этом целевое соединение в виде бледно-оранжевых кристаллов с Т.пл. 149.5-150.0oC.
ПМР (CDCl3) δ : 3.95 (ушир. с, 2H), 7.41 (с, 2H)
MS (термораспыление): M/Z [M+H] 463.1; C11H4Cl2F3IN4O + H составляет 462.88
Пример D2
5-Амино-3-циано-1-(2,6-дихлор-4-трифторметоксифенил)-4- триметилсилилэтинилпиразол
К раствору 5-амино-3-циано-1-(2,6-дихлор-4-трифторметоксифенил)-4- йодпиразола (5.489 г) в диметилформамиде (4 мл) при перемешивании при комнатной температуре прибавили триметилсилилацетилен (3.35 мл), йодид меди (0.116 г), бис(трифенилфосфин) палладий (II) хлорид (0.228 г) и триэтиламин (1 мл). Смесь нагревали при 60oC в течение 2.5 часов. Затем добавили триметилсилилацетилена (1.675 мл), йодида меди (0.058 г) и бис(трифенилфосфин)палладий (II) хлорида (0.114 г) и продолжили перемешивание и нагревание в течение одного часа. Охлажденную реакционную смесь разбавили водой и экстрагировали эфиром. Эфирный экстракт высушили (MgSO4) и упарили, получив сырой продукт, который очистили колоночной хроматографией на силикагеле при элюировании смесью хлористый метилен/гексан. При объединении и упаривании соответствующих фракций с последующей перекристаллизацией их остатка из смеси хлористый метилен/гексан было получено соединение в виде светло-желтых кристаллов с Т. пл. 151.5-152.1oC.
ПМР (CDCl3) δ : 0.26 (с, 9H), 4.15 (ушир. с, 2H); 7.42 (с, 2H)
MS (термораспыление): M/Z [М+H] 433.7; C16H13Cl2F3N4OSi + H составляет 433.03
Пример D3
5-Амино-3-циано-1-(2,6-дихлор-4-трифторметоксифенил)-4-этинилпиразол
К раствору 5-амино-3-циано-1-(2,6-дихлор-4-трифторметоксифенил)-4- триметилсилилэтинилпиразола (0.4657 г) в хлористом метилене (5 мл) при перемешивании и охлаждении в водно-ледяной бане медленно прибавили тетра-н-бутиламмоний фторид (1.07 г 1М раствора в тетрагидрофуране). Через пять минут водно-ледяную баню убрали. В течение десяти минут продолжали перемешивание, затем реакционную смесь промыли водой. Водный слой промыли хлористым метиленом. Объединенные органические слои промыли раствором соли, высушили (Na2SO4) и упарили, получив при этом целевое соединение в виде маслянистых кристаллов, которые закристаллизовывались при высушивании в печи в белые кристаллы с Т. пл. 175.7-176.1oC.
ПМР (CDCl3) δ : 3.48 (с, 1H), 4.2 (ушир. с, 2H), 7.42 (с, 2H)
MS (термораспыление): М/Z [М+ NH4] 377.9; C13H5Cl2F3N4O + NH4 составляет 378.01
Пример D4
3-Циано-1-(2,6-дихлор-4-трифторметоксифенил)-4-триметилсилилэтинилпиразол
К раствору 5-амино-3-циано-1-(2,6-дихлор-4-трифторметоксифенил)-4- триметилсилилэтинилпиразола (4.0 г) в тетрагидрофуране (50 мл) при перемешивании прибавили по каплям н-бутил нитрит (3.29 мл). Смесь кипятили с обратным холодильником в течение 3 часов, а затем упарили досуха. Остаток очистили колоночной хроматографией на силикагеле при элюировании хлористым метиленом: гексаном (3: 1). При объединении и упаривании соответствующих фракций с последующей перекристаллизацией их остатка из гексана получили при этом целевое соединение в виде белых кристаллов с Т. пл. 142.3-142.9oC.
ПМР (CDCl3) δ : 0.3 (с, 9H), 7.39 (с, 2H), 7.70 (с, 1H)
MS (термораспыление): М/Z [М+H] 418.1; C16H12Cl2F3N3OSi + H составляет 418.02
Пример D5
3-Циано-1-(2,6-дихлор-4-трифторметоксифенил)-4-этинилпиразол
К раствору 3-циано-1-(2,6-дихлор-4-трифторметоксифенил)-4- триметилсилилэтинилпиразола (2.691 г) в хлористом метилене (25 мл) при перемешивании прибавили тетра-н-бутиламмоний фторид (6.45 мл 1М раствора в тетрагидрофуране). Перемешивание продолжали в течение 30 минут, затем реакционную смесь распределили между водой и хлористым метиленом. Водный слой отделили и дважды экстрагировали хлористым метиленом. Объединенные органические слои промыли раствором соли, высушили (Na2SO4) и упарили. Остаток очистили колоночной хроматографией на силикагеле при элюировании хлористым метиленом:гексаном (1:1). При объединении и упаривании подходящих фракций было получено целевое соединение в виде белых кристаллов с Т. пл. 95.2 - 96.0oC.
ПМР (CDCl3) δ : 3.39 (с, 1H), 7.40 (с, 2H), 7.77 (с, 1H)
MS (термораспыление): М/Z [М+ NH4] 363.1; C13H4Cl2F3N3O + NH4 составляет 363.0
Пример D6
4-Бромэтинил-3-циано-1-(2,6-дихлор-4-трифторметоксифенил)-пиразол
К раствору 3-циано-1-(2,6-дихлор-4-трифторметоксифенил)-4-этинилпиразола (0.5 г) в ацетоне (5 мл) прибавили N-бромсукцинимид (0.258 г), после чего прибавили нитрат серебра (0.024 г). Перемешивание продолжали в течение одного часа, затем реакционную смесь упарили досуха. Остаток распределили между эфиром и водой. Водный слой отделили и экстрагировали эфиром. Объединенные органические слои промыли рассолом, высушили (Na2SO4) и упарили. Остаток очистили колоночной хроматографией на силикагеле при элюировании хлористым метиленом:гексаном (1:1). При объединении и упаривании соответствующих фракций с последующей перекристаллизацией из гексана было получено целевое соединение в виде белых кристаллов с Т.пл. 123.0-123.8oC.
ПМР (CDCl3) δ: 7.40 (с, 2H), 7.72 (с, 1H)
MS (термораспыление): М/Z [М+ NH4] 440.9; C13H3BrCl2F3N3O + NH4 составляет 440.91
Пример D7 (иллюстративный)
5-Амино-3-циано-1-(2,6-дихлор-4-трифторметилсульфенилфенил)-4-йодпиразол
К раствору 5-амино-3-циано-1-(2,6-дихлор-4-трифторметилсульфенилфенил) пиразола (10 г) в ацетонитриле (50 мл) при перемешивании при комнатной температуре прибавили N-йодсукцинимид (6.4 г) в ацетонитриле (25 мл). Спустя 15 минут смесь упарили до сухого остатка и растворили оставшийся желто-коричневый твердый осадок в хлористом метилене (300 мл). Этот раствор промыли водой (75 мл, 3), затем рассолом (50 мл), затем высушили (MgSO4) и упарили. При растирании с гексаном (100 мл, х 2) было получено целевое соединение в виде желто-коричневых кристаллов с Т.пл. 172-174oC.
ПМР (CDCl3) δ : 3.96 (ушир. с, 2H), 7.81 (с, 2H)
Пример D8
5-Амино-3-циано-1-(2,6-дихлор-4-трифторметилсульфенилфенил)-4 триметилсилилэтинилпиразол
К раствору 5-амино-3-циано-1-(2,6-дихлор-4-трифторметилсульфенилфенил)-4- йодпиразола (10 г) в диметилформамиде (45 мл) при перемешивании при комнатной температуре прибавили триэтиламин (34 мл), триметилсилилацетилен (6 мл), йодид меди (0.4 г) и бис (трифенилфосфин) палладий (II) хлорид (0.4 г). Смесь нагревали при 75oC в течение 6 часов. Охлажденную реакционную смесь упарили досуха и распределили остаток между водой и хлористым метиленом. Органический слой отделили и промыли водой, затем раствором соли, а затем высушили (Na2SO4) и упарили, получив сырой продукт, который очистили колоночной хроматографией на силикагеле (400 г) при элюировании хлористым метиленом. При объединении и упаривании соответствующих фракций был получен маслянистый осадок, который далее очистили колоночной хроматографией на силикагеле (400 г) при элюировании смесью хлористый метилен/гексан. При объединении и упаривании соответствующих фракций с последующей перекристаллизацией из смеси хлористый метилен/гексан было получено целевое соединение в виде желто-коричневых кристаллов с Т. пл. 165-169oC.
ПМР (CDCl3) δ : 0,28 (с, 9H), 4.16 (ушир. с, 2H); 7.8 (с, 2H)
MS (термораспыление): M/Z [М+H] 448.9; C16H13Cl2F3N4SSi + H составляет 449.0
Пример D9
Циано-1-(2,6-дихлор-4-трифторметилсульфенилфенил)-4- триметилсилилэтинилпиразол
К раствору 5-амино-3-циано-1-(2,6-дихлор-4-трифторметилсульфенилфенил)- 4-триметилсилилэтинилпиразола (3.0 г) в тетрагидрофуране (18 мл) при кипении с обратным холодильником прибавили при перемешивании по каплям раствор н-бутил нитрита (2.4 мл) в тетрагидрофуране (7 мл). По окончании прибавления смесь кипятили с обратным холодильником в течение 1 часа, а затем оставили охлаждаться до комнатной температуры. После стояния при комнатной температуре в течение ночи смесь упарили досуха. Остаток очистили колоночной хроматографией на силикагеле (100 г) при элюировании хлористым метиленом. При объединении и упаривании соответствующих фракций с последующей перекристаллизацией остатка из гексана было получено целевое соединение в виде бледно-желтых кристаллов с Т.пл. 129-133oC.
ПМР (CDCl3) δ : 0.29 (с, 9H), 7.72 (с, 1H), 7.8 (с, 2H)
MS (термораспыление): M/Z [М+H] 434.0; C16H12Cl2F3N3SSi + H составляет 433.99
Пример D10
3-Циано-1-(2,6-дихлор-4-трифторметилсульфенилфенил)-4-этинилпиразол
К раствору 3-циано-1-(2,6-дихлор-4-трифторметилсульфенилфенил)-4- триметилсилилэтинилпиразола (2.2 г) в хлористом метилене (40 мл) при перемешивании при комнатной температуре прибавили тетра-н-бутиламмоний фторид (6 мл 1М раствора в тетрагидрофуране). Перемешивание продолжали в течение 30 минут, затем реакционную смесь сконцентрировали до малого объема и затем распределили между хлористым метиленом (50 мл) и водой (20 мл). Органический слой отделили и промыли водой (20 мл), рассолом (10 мл), высушили (Na2SO4) и упарили. Остаток очистили колоночной хроматографией на силикагеле (60 г) при элюировании хлористым метиленом. При объединении и упаривании соответствующих фракций было получено целевое соединение в виде грязно-белых стекловидных кристаллов с Т.пл. 118-119oC.
ПМР (CDCl3) δ : 3.39 (с, 1H), 7.80 (с + с, 1H + 2H)
MS (термораспыление): М/Z [М+ NH4] 379.0; C13H14Cl2F3N3O + NH4 составляет 378.98
Пример D11 (иллюстративный)
5-Амино-3-циано-1-(2,6-дихлор-4-серапентафторфенил)-4-йодпиразол
К раствору 5-амино-3-циано-1-(2,6-дихлор-4-серапентафторфенил) пиразола (18.95 г) в ацетонитриле (100 мл) при перемешивании при комнатной температуре прибавили N-йодсукцинимид (11.5 г) четырьмя порциями в течение пяти минут. Спустя 15 минут смесь упарили до сухого остатка и обработали оставшийся твердый осадок хлористым метиленом и водой. Нерастворившееся вещество отфильтровали и растворили в этилацетате. Раствор высушили (Na2SO4) и упарили, получив при этом целевое соединение в виде желто-коричневых кристаллов с Т. пл. 253oC.
ПМР (CDCl3) δ : 3.94 (ушир. с, 2H), 7.92 (с, 2H)
MS (термораспыление): М/Z [М+ NH4] 521.9; C10H4Cl2F5lN4S + NH4 составляет 521.88
Пример D12
5-Амино-3-циано-1-(2,6-дихлор-4-серапентафторфенил)-4-триметилсилилэтинилпиразол
К раствору 5-амино-3-циано-1-(2,6-дихлор-4-серапентафторфенил)-4- йодпиразола (5.05 г) в диметилформамиде (5 мл) при перемешивании при комнатной температуре прибавили йодид меди (0.1 г), бис(трифенилфосфин)палладий (II) хлорид (0.2 г), триметилсилилацетилен (2.9 мл) и триэтиламин (1 мл). Смесь нагревали при 70oC в течение 5 часов. Охлажденную реакционную смесь оставили стоять на ночь при комнатной температуре и затем вылили в воду. Осадок отфильтровали и растворили в хлористом метилене (50 мл). После добавления гексана (100 мл) отделилось масло. Отстоявшийся раствор упарили, получив сырой продукт, который очистили колоночной хроматографией на силикагеле (80 г) при элюировании смесью хлористый метилен:гексан (1:9, затем 2:8). При объединении и упаривании соответствующих фракций с последующей перекристаллизацией остатка из смеси диизопропиловый эфир/гексан было получено целевое соединение в виде белых микрокристаллических кристаллов с Т. пл. 175oC.
(ПМР (CDCl3) δ : 0.29 (с, 9H), 4.16 (ушир. с, 2H); 7.94 (с, 2H).)
MS (термораспыление): М/Z [М+ NH4] 492.1; C15H13Cl2F5N4SSi + NH4 составляет 492.02
Пример D13
5-Амино-3-циано-1-(2,6-дихлор-4-серапентафторфенил)-4-этинилпиразол
К раствору 5-амино-3-циано-1-(2,6-дихлор-4-серапентафторфенил)- 4-триметилсилилэтинилпиразола (0.4 г) в хлористом метилене (5 мл) при перемешивании прибавили тетра-н-бутиламмоний фторид (1.5 мл 1М раствора в тетрагидрофуране). Через один час добавили тетра-н-бутиламмоний фторида (0.5 мл 1М раствора в тетрагидрофуране). Через три часа реакционную смесь упарили досуха. Остаток очистили колоночной хроматографией на силикагеле (6.6 г) при элюировании смесью гексан: этилацетат (9: 1, затем 4:1, затем 2:1), а затем этилацетатом. При объединении и упаривании соответствующих фракций с последующей перекристаллизацией остатка из смеси этилацетат/гексан было получено целевое соединение в виде желтых микрокристаллических кристаллов с Т. пл. 251oC.
ПМР (d6-DMSO) δ : 3.31 (с, 1 H), 6.88 (ушир. C, 2H), 8.47 (с, 2H)
MS (термораспыление): M/Z [М+H] 403.0; C12H5Cl2F5N4S + H составляет 402.96
Пример E1
5-Амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-этенилпиразол
К раствору 5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- йодпиразола (2 г, соединение из Примера A1) в диметилформамиде (10 мл) при перемешивании при комнатной температуре прибавили винилтри-н-бутил олово (4.25 г) и тетракис(фенилфосфин)палладий (O) (300 мг). Смесь нагревали при 75oC 1 час, а затем охладили и оставили при комнатной температуре на 60 часов. Реакционную смесь разбавили водой и экстрагировали эфиром. Органический слой отделили, промыли рассолом, высушили (MgSO4) и упарили, получив сырой продукт в виде черного масла (6 г), которое очистили колоночной хроматографией на силикагеле (200 г) при элюировании смесью хлористый метилен:гексан (1:1). При объединении и упаривании соответствующих фракций было получено целевое соединение в виде желто-коричневых кристаллов с Т. пл. 186 - 7oC.
ПМР (CDCl3) δ : 3.85 (с, 2H), 5.41 (д, 1H), 5.7 (д, 1H), 6,52 (дд, 1H), 7.8(с, 2H)
MS (термораспыление): M/Z [М+H] 347.0; C13H7Cl2F3N4 + H составляет 347.0
Примеру E2
5-Амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-трибромэтенилпиразол
К раствору 5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- этенилпиразола (1035.3 мг соединение из Примера A3) в эфире (20 мл), охлажденному до - 20oC, при перемешивании прибавили по каплям н-бутиллитий (2.52 мл, 2.5М в гексане) в течение пяти минут. После этого реакционную смесь охладили до - 78oC и прибавили бром (0.487 мл) в течение двух минут. Прекратили охлаждение и оставили реакционную смесь нагреваться до комнатной температуры в течение часа. Реакционную смесь вылили в эфир (100 мл) и воду (100 мл). Органический слой отделили, высушили (MgSO4) и упарили, получив сырой продукт, который очистили колоночной хроматографией на силикагеле при элюировании смесью хлористый метилен: гексан (1:1). При объединении и упаривании соответствующих фракций было получено целевое соединение в виде белых кристаллов с Т.пл. 187oC разл).
ПМР (CDCl3) δ : 4.04 (с, 2H), 7.8 (с, 2H)
Элементарный анализ - найдено: C, 26.95, H, 0.62, N 9.55 % для C13H4Br3Cl2F3N4 C, 26.75, H, 0.69, N, 9.60 %
Примеры E3a и E3b
5-Амино-3-циано-4-(Е-1,2-дибромэтенил-1-(2,6-дихлор- 4-трифторметилфенил)пиразол и
5-Амино-3-циано-4-(Z-1,2-дибромэтенил-1-(2,6-дихлор-4-трифторметилфенил) пиразол
К раствору 5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- этинилпиразола (100 мг, соединения из Примера A3) в эфире (1 мл) при осторожном встряхивании по каплям, в течение минуты по каплям прибавили бром (0.019 мл). После этого реакционную смесь упарили и очистили продукт колоночной хроматографией на силикагеле (10 г) при элюировании смесью хлористый метилен:гексан (2:1). При объединении и упаривании соответствующих фракций получили смесь целевых соединений в соотношении приблизительно 60:40 в виде белых кристаллов с Т. пл. 138-141oC, которую далее очистили ВЭЖХ на колонке 21 х 250 мм Dynamax 0.005 мм ODS с обращенной фазой при элюировании смесью ацетонитрил: 0.005 водная гептансульфоновая кислота:метанол (5:4:1) со скоростью 10 мл/минуту. Соответствующие фракции объединили и обработали упариванием неводных компонентов с последующим распределением между этиловым эфиром и насыщенным водным раствором гидрокарбоната натрия. Органический слой высушили и упарили, получив i) Z-изомер целевого соединения в виде желто-коричневых кристаллов, Т.пл. 175-6oC
{ ПМР (CDCl3) δ : 4.04 (ушир. с, 2H), 6.92 (с, 1H), 7.82 (с, 2H)} и (ii) E-изомер целевого соединения в виде желто-коричневых кристаллов, Т.пл. 169-170oC
{ПМР (CDCl3) δ : 3.98 (ушир. с, 2H), 7.26 (с, 1H), 7.8 (с, 2H)}
MS (термораспыление): M/Z [М+H] 502.0 C13H5Br2Cl2F3N4 + NH4 составляет 502.8
Пример E4
5-Амино-3-циано-4-(циклогекс-1-енил)-1-(2,6-дихлор-4-трифторметилфенил) пиразол
Раствор 5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил) пиразола (1 г, соединение из Ссылки Примера 1 из EP 295, 117) и циклогексонона (1.6 мл) в уксусной кислоте (5 мл) перемешивали и нагревали при 120oC в атмосфере азота в течение ночи. Охлажденную реакционную смесь разбавили водой и экстрагировали этилацетатом и затем эфиром. Объединенные органические экстракты промыли насыщенным водным раствором гидрокарбоната натрия, затем водой. После высушивания (MgSO4) при упаривании получили сырой продукт, который очистили колоночной хроматографией на силикагеле (50 г) при элюировании смесью хлористый метилен:гексан (1:2), затем смесью хлористый метилен: гексан (1:1). При объединении и упаривании соответствующих фракций было получено целевое соединение в виде белых кристаллов с Т.пл. 175-7oC.
ПМР (CDCl3) δ : 1.7 (м, 2H), 1.8 (м, 2H), 2.2 (м, 2H), 2,45 (м, 2H), 3.74 (с, 2H), 5.9 (с, 1 H), 7.78 (с, 2H)
Элементный анализ - найдено: C, 50.75, H, 3.07, N 13.68 % для C17H13Cl2F3N4 C, 50.89, H, 3.27, N, 13.69%
Пример E5
5-Амино-3-циано-4-(E-1,2-дибромпропен-1-ил)-1-(2,6-дихлор-4-трифторметилфенил) пиразол
К раствору 5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)пиразола (0.045 r) в эфире (2 мл) при перемешивании прибавили по каплям раствор брома (0.02 г) в хлористом метилене (1.5 мл). После выдерживания в течение пяти минут при комнатной температуре реакционную смесь упарили и очистили колоночной хроматографией на силикагеле (5 г) при элюировании смесью хлористый метилен: гексан (3:7). При объединении и упаривании соответствующих фракций получили целевое соединение в виде белых кристаллов.
ПМР (CDCl3) δ : 2.63 (с, 3H), 3.94 (ушир. с, 2H), 7.8 (с, 2H)
MS (термораспыление): M/Z [М+H] 516.2; C14H7Br2Cl2F3N4 + H составляет 516.84
Пример E6
5-Амино-3-циано-4-(1,2-дибром-2-фенилэтенил)-1-(2,6-дихлор-4- трифторметилфенил)пиразол
К раствору 5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- фенэтинилпиразола (0.15 г) в хлористом метилене (4 мл) при перемешивании прибавили по каплям раствор брома (0.057 r) в хлористом метилене (0.25 мл). После выдерживания в течение 20 минут при комнатной температуре реакционную смесь упарили и очистили остаток колоночной хроматографией на силикагеле (10 г) при элюировании гексаном, а затем гексаном, содержащим возрастающие количества хлористого метилена. При объединении и упаривании соответствующих фракций получили целевое соединение в виде желтых кристаллов, Т.пл. 211oC.
ПМР (CDCl3) δ : 4.1 (ушир. с, 2H), 7.28 (м, 1H), 7.42 (м, 2H), 7.52 (м, 2H), 7.82 (с, 2H)
MS (термораспыление): M/Z [М+H] 578.7; C19H9Br2Cl2F3N4 + H составляет 578.86
Пример E7
5-Амино-3-циано-4-(1,2-дихлор-2-фенилэтенил)-1-(2,6-дихлор-4 -трифторметилфенил)пиразол
К раствору 5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- фенэтинилпиразола (0.5 г) в хлористом метилене (20 мл) при перемешивании прибавили по каплям раствор хлора (0.085 г) в хлористом метилене (5 мл). После выдерживания в течение 30 минут при комнатной температуре реакционную смесь упарили и очистили остаток колоночной хроматографией на силикагеле (30 г) при элюировании гексаном, а затем гексаном, содержащим возрастающие количества хлористого метилена. При объединении и упаривании соответствующих фракций получили целевое соединение в виде оранжевых кристаллов, Т.пл. 168-172oC.
ПМР (CDCl3) δ : 3.7 (ушир. с, 2H), 7.3 (м, 2H), 7.4 (м, 2H), 7.47 (м, 1H), 7.74 (с, 2H)
MS (термораспыление): M/Z [М+H] 490.8; C19H9Cl4F3N4 + H составляет 490.96.
Пример E8
4-(2-бром-1,2-дихлорэтенил)-3-циано-1-(2,6-дихлор-4-трифторметоксифенил) пиразол
К раствору 4-бромэтенил-3-циано-1-(2,6-дихлор-4-трифторметоксифенил) пиразола (0.4 г) в хлористом метилене (10 мл), охлажденному до - 78oC, прибавили при перемешивании раствор хлора (0.133 г) в хлористом метилене (5 мл). Перемешивание при - 78oC продолжали в течение двух часов, после чего реакционную смесь оставили нагреваться до комнатной температуры. Перемешивание продолжали в течение ночи, затем реакционную смесь упарили досуха. Остаток очистили колоночной хроматографией на силикагеле при элюировании смесью хлористый метилен:гексан (1:1). При объединении и упаривании соответствующих фракций с последующей перекристаллизацией из циклогексана получили целевое соединение в виде белых кристаллов, Т.пл. 143.4-143.8oC.
ПМР (CDCl3) δ : 7.40 (с, 2H), 7.72 (с, 1 H)
MS (термораспыление): M/Z [М+H] 494.0; C13H3BrCl4F3N3O + H составляет 493.82
Пример E9
3-Циано-1-(2,6-дихлор-4-триформетоксифенил)-4-трибромэтенилпиразол
К раствору 3-циано-1-(2,6-дихлор-4-трифторметоксифенил)-4- этинилпиразола (0.5 г) в тетрагидрофуране (20 мл), охлажденному до -45oC, прибавили при перемешивании н-бутиллитий (0.876 мл 2.5 М раствора в гексане) с такой скоростью, чтобы температура держалась ниже -40oC. После охлаждения до -78oC перемешивание продолжали в течение двадцати минут, затем по каплям прибавили бром (0.187 мл). Перемешивание продолжали в течение 15 минут, затем реакционную смесь оставили нагреваться до комнатной температуры и продолжили перемешивание еще в течение 15 минут. После чего реакционную смесь распределили между эфиром и водой. Водный слой отделили и дважды экстрагировали эфиром. Объединенные органические слои промыли рассолом, высушили (Na2SO4) и упарили. Остаток очистили колоночной хроматографией на силикагеле при элюировании смесью хлористый метилен:гексан (1:2). При объединении и упаривании соответствующих фракций с последующей перекристаллизацией из гексана было получено целевое соединение в виде белых кристаллов, Т.пл. 155.9-156.2oC.
ПМР (CDCl3) δ : 7.42 (с, 2H), 7.82 (с, 1H)
MS (термораспыление): М/Z [М+ NH4] 598.7; C13H3BrCl2F3N3O + NH4 составляет 598.75
Пример E10
5-Амино-3-циано-1-(2,6-дихлор-4-серапентафторфенил)-4-этенилпиразол
К дегазированному раствору 5-амино-3-циано-1-(2,6-дихлор-4- серапентафторфенил)-4-йодпиразола (5.05 г) и тетракис (трифенилфосфин) палладия (O) (0.175 г) в диметилформамиде (32 мл) при перемешивании прибавили при комнатной температуре винилтри-н-бутил олово (4.5 мл). Смесь нагрели до 70oC за 30 минут и затем выдержали при 70oC в течение одного часа. Добавили тетракис (трифенилфосфин) палладия (O) (0.175 г) и винилтри-н- бутил олова (4.5 мл) и продолжили нагревание еще в течение часа. Реакционную смесь упарили и распределили остаток между водой и эфиром. Водный слой экстрагировали эфиром. Объединенные органические слои промыли рассолом, высушили (MgSO4) и упарили, получив при этом сырой продукт в виде коричневой пасты. При растирании с гексаном получили коричневые кристаллы, которые растворили в этилацетате и профильтровали. Фильтрат упарили и перекристаллизовали его остаток из толуола, получив целевое соединение в виде желто-коричневых кристаллов с Т. пл. 227-228oC.
ПМР (CDCl3) δ : 3.86 (с, 2H), 5.41 (д, 1H), 6.5 (д, 1H), 6.5 (дд, 1H), 7.92 (с, 2H)
MS (термораспыление): M/Z [М+H] 405.1; C12H7Cl2F5N4S + H составляет 404.98
Пример E11 (Иллюстративный)
3-Циано-1-(2,6-дихлор-4-серапентафторфенил)-4-йодпиразол
К нагретому до кипения раствору 3-циано-1-(2,6-дихлор-4- серапентафторфенил)-4-йодпиразола (1.23 г) в тетрагидрофуране (35 мл) в течение тридцати минут прибавили по каплям при перемешивании раствор трет-бутил нитрита (3.1 г) в тетрагидрофуране (15 мл). После этого реакционную смесь упарили и перекристаллизовали остаток из изопропанола, получив целевое соединение в виде розоватых кристаллов с Т.пл. 179-180oC.
ПМР (CDCl3) δ : 7.66 (с, 1H), 7.9 (с, 2H)
MS (термораспыление): М/Z [М+ NH4] 506.4; C10H3Cl2F5lN3S + NH4 составляет 506.87
Пример E12
3-Циано-1-(2,6-дихлор-4-серапентафторфенил)-4-этенилпиразол
К дегазированному раствору 5-амино-3-циано-1-(2,6-дихлор- 4-серапентафторфенил)-4-йодпиразола (1.23 г) и тетракис (трифенилфосфин) палладия (O) (0.09 г) в диметилформамиде (32 мл) при перемешивании прибавили при комнатной температуре винилтри-н-бутил олово (4.2 мл). Реакционную смесь нагревали при 70oC в течение 1,5 часов. Реакционную смесь упарили и растерли остаток с гексаном. Полученные кристаллы растворили в хлористом метаноле и поместили в колонку с силикагелем (60 г). При элюировании гексаном и затем гексаном:хлористым метиленом (4: 1) после объединения и упаривания соответствующих фракций было получено целевое соединение в виде белых кристаллов с Т. пл. 156oC.
ПМР (CDCl3) δ : 5.5 (д, 1H), 5.95 (д, 1H), 6.63 (дд, 1H), 7.77 (с, 1H), 7.92 (с, 2H)
MS (термораспыление): М/Z [М+ NH4] 406.8; C12H6Cl2F5N3S + NH4 составляет 406.99
Пример F1 (Иллюстративный)
3-Циано-1-(2,6-дихлор-4-трифторметилфенил)-4-йодпиразол
К нагретому до 65oC раствору 5-амино-3-циано-1-(2,6-дихлор-4- трифторметилфенил)-4-йодпиразола (90 г) в тетрагидрофуране (720 мл) при перемешивании в течение 0.5 часа прибавили трет-бутил нитрит (144 мл). Перемешивание и нагревание продолжали в течение 3 часов. Охлажденную реакционную смесь упарили и перекристаллизовали остаток из н-пропанола, получив целевое соединение в виде белых кристаллов с Т. пл. 83-4oC.
ПМР (CDCl3) δ : 7.7 (с, 1H), 7.79(с, 2H)
MS (термораспыление): М/Z [М+ NH4] 448.8; C11H3Cl2F3N3l + NH4 составляет 448.9
Пример E2
3-Циано-1-(2,6-дихлор-4-трифторметилфенил)-4-этенилпиразол
Раствор 3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-йодпиразола (58 г) в диметилформамиде (350 мл), содержащий винилтри-н-бутил олово (116 мл) и тетракис(трифенилфосфин)палладий (О) (3.5 г), перемешивали при 75oC в течение 3 часов. Реакционную смесь вылили в воду (600 мл) и эфир (600 мл). Органический слой промыли водой (5 раз), рассолом (700 мл) и высушили над сульфатом натрия. При удалении растворителя в вакууме с последующей кристаллизацией остатка из пропан-2-ола получили целевое соединение в виде бледно-коричневых кристаллов с Т. пл. 75 - 6oC.
ПМР (CDCl3) δ : 5.5 (д, 1H), 5.94 (д, 1H), 6.64 (дд, 1H), 7.64 (с, 1H), 7.77 (с, 2H)
MS (термораспыление): М/Z [М+ NH4] 349.5; C13H6Cl2F3N3 + NH4 составляет 349.02
Пример F3 (Иллюстративный)
3-Циано-1-(2,6-дихлор-4-трифторметилфенил)-4-формилпиразол
Раствор 3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-этенилпиразола (0.1 г), N-метилморфолин оксида (0.005 г), тетроксида осмия (0.05 мл 2.5% раствора в трет-бутаноле) в воде (5 мл) и ацетоне (45 мл) перемешивали при комнатной температуре в течение 16 часов. Добавили метапериодат натрия (0.005 г) и продолжали перемешивание в течение 16 часов. Реакционную смесь упарили в вакууме и распределили остаток между диэтиловым эфиром и водным раствором гидрокарбоната натрия. Водный слой отделили и экстрагировали диэтиловым эфиром. Объединенные водные экстракты высушили над сульфатом натрия и упарили. Остаток очистили колоночной хроматографией на силикагеле (5 г) при элюировании хлористым метиленом, получив при этом целевое соединение в виде бежевых кристаллов, Т.пл. 167.5-168.5oC.
ПМР (CDCl3) δ : 7.8 (с, 2H), 8.18 (с, 1H), 10.08 (с, 1H)
MS (термораспыление): М/Z [М+ NH4] 351.3; C12H4Cl2F3N3O + NH4 составляет 351.0
Пример F4
4-(2,2-Дибромэтил)-3-циано-1-(2,6-дихлор- 4-трифторметилфенил)пиразол
К раствору трифенилфосфина (0.983 r) в сухом хлористом метилене (50 мл) при 0oC прибавили при перемешивании четырехбромистый углерод (0.497 г). Смесь перемешивали в течение 5 минут и затем прибавили 3-циано-1- (2,6-дихлор-4-трифторметилфенил)-4-формилпиразола (0.25 г). Реакционной смеси давали нагреться до комнатной температуры и перемешивание продолжали в течение 1 часа. Реакционную смесь упарили и очистили остаток колоночной хроматографией на силикагеле при элюировании хлористым метиленом, получив при этом целевое соединение в виде белых кристаллов, Т.пл. 109-110oC.
ПМР (CDCl3) δ : 7.48 (с, 1H), 7.76 (с, 2H), 8.34 (с, 1H)
MS (термораспыление): M/Z [М+H] 487.2; C13H4Br2Cl2F3N3 + H составляет 487.8
Пример F5a и F5b
4-(Z-1,2-Дибромэтенил)-3-циано-1-(2,6-дихлор-4-трифторметилфенил)пиразол
4-(E-1,2-Дибромэтенил)-3-циано-1-(2,6-дихлор-4-трифторметилфенил)пиразол
К раствору 5-амино-4-дибромэтенил-3-циано-1-(2,6-дихлор-4-трифторметилфенил) пиразола (смесь E/Z) (0.3 г) в тетрагидрофуране (2 мл) при перемешивании прибавили трет-бутил нитрит (0.21 мл) и нагревали эту смесь при 65oC в течение 1 часа. Реакционную смесь упарили и очистили остаток колоночной хроматографией на силикагеле (20 г) при элюировании гексаном и затем гексаном:хлористым метиленом (1:3). Соответствующие фракции объединили и упарили в вакууме и далее очистили ВЭЖХ на колонке 21 х 250 мм DynamaxTM 0.005 мм ODS с обращенной фазой при элюировании смесью ацетонитрил:вода (3:2) со скоростью 11 мл/минуту, получив
(i) 4-(Z-1,2-дибромэтенил)-3-циано-1-(2,6-дихлор-4-трифторметилфенил) пиразол в виде белых кристаллов, Т. пл. 88-90oC,
{ПМР (CDCl3) δ : 7.7 (с, 1H), 7.8 (с, 2H), 7.87 (с, 1H)
MS (термораспыление): М/Z [М+ NH4] 504.0; C13H4Br2Cl2F3N3 + NH4 составляет 504.8}.
и
(ii) 4-(E-1,2-дибромэтенил)-3-циано-1-(2.6-дихлор-4-трифторметилфенил) пиразол в виде белых кристаллов, Т. пл. 119oC,
{ПМР (CDCl3) δ : 7.0 (с, 1H), 7.8 (с, 2H), 7.98 (с, 1 H)
MS (термораспыление): М/Z [М+ NH4] 504.3; C13H4Br2Cl2F3N3 + NH4 составляет 504.8}.
Пример F6
3-Циано-4-(2,2-дихлорэтенил)-1-(2,6-дихлор-4-трифторметилфенил)пиразол
Раствор трифенилфосфина (0.983 г) и четыреххлористого углерода (0.145 г) в безводном хлористом метилене (5 мл) перемешивали в течение 5 минут при 0oC. Затем прибавили 3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- формилпиразол (0.25 г) и кипятили с обратным холодильником реакционную смесь в течение 5 часов и после этого упарили. Остаток очистили колоночной хроматографией на силикагеле при элюировании хлористым метиленом. При объединении и упаривании соответствующих фракций было получено целевое соединение в виде белых кристаллов, Т.пл. 99-101oC.
ПМР (CDCl3) δ : 6.9 (с, 1H), 7.8 (с, 2H), 8.2 (с, 1H)
MS (термораспыление): М/Z [М+ NH4] 417.0; C13H4Cl4F3N3 + NH4 составляет 416.95
Пример F7
3-Циано-1-(2,6-дихлор-4-трифторметилфенил)-4-(2,2-дифторэтенил)пиразол
3-циано-1-(2,6-дихлор-4 -трифторметилфенил)-4-формил-пиразол (1.3 г), трифенилфосфина (5.1 г), дибромдифторметан (2 г) и дихлорметан (50 мл) поместили в стальной автоклав из нержавеющей стали и нагревали при перемешивании при 70oC с течение 3 часов. Реакционную смесь упарили и очистили остаток колоночной хроматографией на силикагеле при элюировании хлористым метиленом: гексаном (9: 1). При объединении и упаривании соответствующих фракций было получено целевое соединение в виде белых кристаллов с Т.пл. 75- 77oC.
ПМР (CDCl3) δ : 5.43 (д, 1H), 7.7 (с, 1H), 7.79 (с, 2H)
MS (термораспыление): М/Z [М+ NH4] 368.0; C13H4Cl2F5N3 + NH4 составляет 368.0.
Примеры F8a и F8b
4-(E-2-Хлор-3,3,3-трифторпропенил)-3-циано-1-(2,6-дихлор-4- трифторметилфенил)пиразол
4-(Z-2-Хлор-3,3,3-трифтопропенил)-3-циано-1-(2,6-дихлор-4-трифторметилфенил) пиразол
Раствор 3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-формилпиразола (0.75 г), 1,1,1-трихлор-2,2,2-трифторэтана (0.54 мл), уксусного ангидрида (0.32 мл) в диметилформамиде (2 мл), содержащий порошок цинка (0.734 г), нагревали при 50oC при перемешивании в течение 3 часов. Охлажденную реакционную смесь разбавили водой (20 мл) и экстрагировали эфиром (50 мл, х 3). Объединенные органические слои высушили и упарили. Остаток очистили колоночной хроматографией на силикагеле при элюировании хлористым метиленом. Соответствующие фракции объединили и упарили и далее очистили обращенно-фазовой хроматографией на двуокиси кремния C18 при элюировании смесью метанол: ацетонитрил: PIC B7 буфер (10:65:35). Соответствующие фракции объединили, частично упарили и распределили между эфиром и водой. Органический слой отделили, высушили и упарили, получив:
4-(E-2-Хлор-3,3,3-трифторпропенил)-3-циано-1-(2,6-дихлор-4- трифторметилфенил) пиразол в виде белых кристаллов, Т.пл. 108-110oC.
ПМР (CDCl3) δ : 7.1 (с, 1H), 7.8 (с, 2H), 7.83 (с, 1H).
MS (термораспыление): M/Z [М+H] 434.0; C14H4Cl3F6N3 + H составляет 433.94;
и
4-(Z-2-Хлор-3,3,3-трифторпропенил)-3-циано-1-(2,6-дихлор-4- трифторметилфенил) пиразол в виде белых кристаллов, Т.пл. 125- 126oC,
ПМР (CDCl3) δ : 7.36 (с, 1H), 7.8 (с, 2H), 8.42 (с, 1H).
MS (термораспыление): М/Z [М+ NH4] 434; C14H4Cl3F6N3 + H составляет 433.94.
Примеры F9a и F9b
4-(E-2-Бром-3,3,3-трифторпропенил)-3-циано-1-(2,6-дихлор-4-трифторметилфенил) пиразол
4-(Z-2-Бром-3,3,3-трифторпропенил)-3-циано-1-(2,6-дихлор-4- трифторметилфенил)пиразол
Раствор 3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-формилпиразола (0.5 г), 1,1,1-трибром-2,2,2-трифторэтана (0.96 мл), уксусного ангидрида (0.3 мл) в диметилформамиде (2 мл), содержащий порошок цинка (0.49 г), нагревали при 50oС при перемешивании в течение 12 часов. Охлажденную реакционную смесь разбавили хлористым метиленом (20 мл) и дважды промыли водой (10 мл). Органическую фазу высушили и упарили. Остаток очистили колоночной хроматографией на силикагеле при элюировании хлористым метиленом. При объединении и упаривании соответствующих фракций получили:
4-(E-2-Бром-3,3,3-трифторпропенил)-3-циано-1-(2,6-дихлор-4- трифторметилфенил)пиразол в виде белых кристаллов.
ПМР (CDCl3) δ : 6.58 (с, 1H), 7.8 (с, 2H), 7.97 (с, 1H).
и
4-(Z-2-Бром-3,3,3-трифторпропенил)-3-циано-1-(2,6-дихлор-4- трифторметилфенил)пиразол в виде белых кристаллов, Т.пл. 125-126oC,
ПМР (CDCl3) δ : 7.68 (с, 1H), 7.8 (с, 2H), 8.62 (с, 1H).
MS (термораспыление): М/Z [М+ NH4] 494.6; C14H4BrCl2F5N3 + NH4 составляет 494.92.
Пример F10
3-Циано-1-(2,6-дихлор-4-трифторметилфенил)-4-(Z-2-фтор-3,3,3-трифторпропен- 1-ил)пиразол
3-Циано-1-(2,6-дихлор-4-трифторметилфенил)-4-формилпиразол (1.25 г), уксусный ангидрид (0.5 мл), диметилформамид (50 мл) и порошок цинка (1.2 г) поместили в стальной автоклав из нержавеющей стали и охладили до -40oC. Добавили 1,1-дихлор-1,2,2,2-тетрафторэтан (1.6 г) и затем содержимое герметизированного автоклава нагревали и перемешивали при 70oC в течение 6 часов. Реакционную смесь распределили между эфиром и водой. Органическую фазу отделили, высушили и упарили. Остаток очистили колоночной хроматографией на силикагеле при элюировании хлористым метиленом. При объединении и упаривании получили целевое соединение в виде белых кристаллов.
ПМР (CDCl3) δ : 6.57 (д, 1H), 7.8 (с, 2H), 8.05 (с, 1 H)
Пример F11
3-Циано-4-(транс-2-цианоэтенил)-1-(2,6-дихлор-4-трифторметилфенил)пиразол
Смесь 3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-йодпиразола (0.864 г), акрилонитрила (0.264 г), триэтиламина (0.4 мл), ацетата палладия (0.04 г) и диметилформамида (10 мл) перемешивали в атмосфере азота при 70oC в течение 6 часов. Реакционную смесь упарили и распределили между водой и хлористым метиленом. Органическую фазу отделили, промыли водой, рассолом, высушили (Na2SO4) и упарили. Остаток очистили колоночной хроматографией на силикагеле (40 г) при элюировании хлористым метиленом. При объединении и упаривании получили целевое соединение в виде белых кристаллов, Т.пл. 144-145oC.
ПМР (CDCl3) δ: 6.19 (д, 1H), 7.34 (д, 1H), 7.8 (с, 2H), 7.81 (с, 1H)
MS (термораспыление): М/Z [М+ NH4] 373.8; C14H5Cl2F3N4 + NH4 составляет 374.02
Пример F12
3-Циано-1-(2,6-дихлор-4-трифторметилфенил)-4-трифторметилэтинилпиразол
К раствору трифторпропина (0.66 г) в безводном тетрагидрофуране (10 мл) при -78oC прибавили при перемешивании н-бутиллитий (3.125 мл 2.5М раствора в гексане), удерживая температуру ниже -78oC. Через 30 минут прибавили хлорид цинка (44 мл 0.5М раствора в тетрагидрофуране) и оставили реакционную смесь нагреваться до комнатной температуры в течение трех часов. После охлаждения до 0oC прибавили бис(трифенилфосфин)палладий хлорид (0.12 г) и 3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-йодпиразол (1.5 г) и смесь кипятили с обратным холодильником в течение 6 часов. Затем охлажденную смесь распределили между эфиром и водой. Органическую фазу отделили, высушили и упарили. Остаток очистили колоночной хроматографией на силикагеле при элюировании хлористым метиленом:гексаном (3:7). При объединении и упаривании получили целевое соединение в виде бледно-желтых кристаллов, Т.пл. 121-123oC.
ПМР (CDCl3) δ: 7.8 (с, 2H), 7.94 (с, 1H)
MS (термораспыление): М/Z [М+ NH4] 419.9; C14H3Cl2F8N3 + NH4 составляет 414.80
Пример F13
4-(1,2-Дибром-3,3,3-трифторпропенил)-3-циано-1-(2,6-дихлор-4-трифторметилфенил) пиразол
К раствору 3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- трифторметилэтинилпиразола (0.11 г) в эфире (1 мл) при перемешивании прибавили бром (0.015 г). Спустя 24 часа смесь распределили между эфиром (10 мл) и водой (10 мл). Органическую фазу отделили, высушили и упарили, получив целевое соединение (в виде изомерной смеси) в виде грязно-белых кристаллов, Т.пл. 119 - 121oC.
ПМР (CDCl3) δ : 7.8 (с, 2H), 7.9 & 7.94 (с&с, 1H)
MS (термораспыление): М/Z [М+ NH4] 556.00; C14H3Br2Cl2F6N3 + NH4 составляет 555.8.
Примеры F14a и F14b
3-Циано-1-(2,6-дихлор-4-трифторметилфенил)-4-трибромэтенилпиразол
5-Бром-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-трибромэтенилпиразол
К раствору 3-циано-1-(2,6-дихлор-4-трифторметилфенил)- 4-этинилпиразола (0.25 г) в тетрагидрофуране (10 мл) при - 20oC прибавили при перемешивании н-бутиллитий (0.455 мл 2.5М раствора в гексане). Через 5 минут смесь охладили до -78oC и по каплям прибавили бром (0.0975 мл). Смесь оставили нагреваться до комнатной температуры в течение 10 минут и после этого вылили в воду (20 мл) и эфир (10 мл). Органический слой отделили, высушили и упарили. Остаток очистили колоночной хроматографией на силикагеле (10 г) при элюировании гексаном, а затем гексаном: хлористым метиленом (2:3). При объединении и упаривании получили целевые соединения в виде белых кристаллов, Т. пл. 163-163.5oC и 136 - 139oC соответственно
ПМР (CDCl3) δ: 7.8 (с, 2H), 7.85 (с, 1H)
MS (термораспыление): М/Z [М + NH4] 582.4; C13H3Br3Cl2F3N3 + NH4 составляет 582.72
ПМР (CDCl3) δ : 7.8 (с, 2H)
MS (термораспыление): М/Z [М+NH4] 660.7; C13H2Br4Cl2F3N3 + NH4 составляет 660.67
Пример F15
3-Циано-1-(2,6-дихлор-4-трифторметилфенил)-4-трихлорэтенилпиразол
К раствору 3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- трихлорэтинилпиразола (0.25 г) в хлористом метилене (10 мл) при перемешивании прибавили хлор (0.049 г) и оставили на ночь. Добавили хлора (0.049 г) и опять оставили смесь на ночь. Смесь упарили и очистили остаток колоночной хроматографией на силикагеле (50 г) при элюировании смесью гексан : эфир: хлористый метилен (8:1:1). При объединении и упаривании получили целевое соединение в виде белых кристаллов, Т.пл. 122-124oC.
ПМР (CDCl3) δ : 7.79 (с, 2H), 7.93 (с, 1H)
MS (термораспыление); М/Z [М+ NH4] 450.8; C13H3Cl5F3N3 + NH4 составляет 450.91
Пример F16
3-Циано-4-(E-1,2-дибромпропенил)-1-(2,6-дихлор-4-трифторметилфенил)пиразол
К раствору 5-амино-4-(Е-1,2-дибромпропенил)-3-циано-1-(2,6-дихлор-4- трифторметилфенил) пиразола (0.06 г) в тетрагидрофуране (1.5 мл) при перемешивании прибавили трет-бутил нитрит (0.05 мл). Реакционную смесь нагревали при 60oC в течение двух часов. Затем реакционную смесь упарили, очистили остаток колоночной хроматографией на силикагеле (5 г) при элюировании гексаном: хлористым метиленом (от 100:0 до 20:7). При объединении и упаривании получили целевое соединение в виде белых кристаллов, Т.пл. 134-135oC.
ПМР (CDCl3) δ : 2.64 (с, 1H), 7.78 (с, 1H), 7.79 (с, 2H)
MS (термораспыление): М/Z [М+ NH4] 518.6: C14H6Br2Cl2F3N3 + NH4 составляет 518.86.
Пример F17
4-(2-Бром-1,2-дихлорэтенил)-3-циано-1-(2,6-дихлор-4-трифторметилфенил) пиразол
К раствору 4-бромэтинил-3-циано-1-(2,6-дихлор-4-трифторметилфенил) пиразола (0.2 г) в хлористом метилене (5 мл), охлажденному до -78oC, при перемешивании прибавили хлор (2.17 мл 0.255М раствора в хлористом метилене). Реакционную смесь оставили нагреваться до комнатной температуры. Через два часа добавили хлора (2.17 мл 0.255М раствора в хлористом метилене) и продолжали перемешивание в течение двух дней, после чего смесь упарили досуха, получив при этом целевое соединение в виде белых кристаллов, Т.пл. 128-131oC.
ПМР (CDCl3) δ : 7.80 (с, 2H), 7.92 (с, 1H)
MS (термораспыление): М/Z [М+ NH4] 495.1; C13H3BrCl4F3N3 + NH4 составляет 494.86
Пример F18
4-12-Хлор-1,2-дибромэтенил)-3-циано-1-(2,6-дихлор-4-трифторметилфенил)пиразол
К раствору 4-хлорэтинил-3-циано-1-(2,6-дихлор-4-трифторметилфенил) пиразола (0.1203 г) в безводном хлористом метилене (3 мл) при перемешивании прибавили бром (0.017 мл). Перемешивание продолжали в течение ночи, после чего смесь упарили досуха, получив после перекристаллизации из гексана целевое соединение в виде белых кристаллов, Т.пл. 135-138oC.
ПМР (CDCl3) δ: 7.80 (с, 2H), 7.83 (с, 1H)
MS (термораспыление): М/Z [М+ NH4] 538.8; C13H3Br2Cl3F3N3 + NH4 составляет 538.81
Пример F19 (Иллюстративный)
4-Ацетил-5-амино-3-циано-1-(2,6-дихлор 4-трифторметилфенил)пиразол
К раствору 5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- этинилпиразола (0.345 r) в ацетонитриле (5 мл) прибавили n-толуолсульфоновую кислоту (0.5 г) и перемешивали смесь в течение 2 часов при комнатной температуре, а затем вылили в воду (100 мл) и эфир (100 мл). Органический слой отделили, промыли насыщенным водным раствором гидрокарбоната натрия (50 мл), рассолом (50 мл), высушили (Na2SO4) и упарили. Остаток очистили колоночной хроматографией на силикагеле (40 г) при элюировании хлористым метиленом:гексаном (10: 1). При объединении и упаривании получили целевое соединение в виде белых кристаллов, Т. пл. 200-201oC.
ПМР (CDCl3) δ : 2.65 (с, 3H), 5.83 (ушир. с, 2H), 7.82 (с, 2H)
MS (термораспыление): М/Z [М+NH4] 380.4; C13H7Cl2F3N3O + NH4 составляет 380.03
Пример F20 (Иллюстративный)
4-Ацетил-3-циано-1-(2,6-дихлор-4-трифторметилфенил)пиразол
К раствору 4-ацетил-5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил) пиразола (0.4 r) в тетрагидрофуране (2 мл) прибавили по каплям трет-бутил нитрит (0.0262 г). Смесь кипятили с обратным холодильником в течение 30 минут. Реакционную смесь поместили в колонку с силикагелем (1 г) и элюировали тетрагидрофураном, получив целевое соединение в виде белых кристаллов, Т. пл. 166- 168oC.
ПМР (CDCl3) δ : 2.67 (с, 3H), 7.8 (с, 2H), 8.12 (с, 1H)
MS (термораспыление): M/Z [М+ NH4] 365.0; C13H6Cl2F3N3O + NH4 составляет 365.02
Пример F21
3-Циано-1-(2,6-дихлор-4-трифторметилфенил)-4-(1-метил-2,2-дибромэтенил) пиразол
Раствор трифенилфосфина (0.94 г) и четырехбромистого углерода (0.6 г) в безводном хлористом метилене (30 мл) перемешивали при 0oC в течение 5 минут. Затем прибавили 4-ацетил-3-циано-1-(2,6- дихлор-4-трифторметилфенил) пиразол (0.25 г) и смесь кипятили с обратным холодильником в течение 6 часов и после этого упарили. Остаток очистили колоночной хроматографией на силикагеле при элюировании хлористым метиленом. При объединении и упаривании соответствующих фракций было получено целевое соединение в виде бледно-розовых кристаллов с Т.пл. 119-122oC.
ПМР (CDCl3) δ : 2.35 (с, 3H), 7.79 (c + c, 1H + 2H)
MS (термораспыление): М/Z [М+ NH4] 518.7; C14H6Br2Cl2F3N3 + NH4 составляет 518.86
Пример F22
3-Циано-1-(2,6-дихлор-4-трифторметилфенил)-4-(1-метил-2,2- дифторэтенил)пиразол
4-Ацетил-3-циано-1-(2,6-дихлор-4-трифторметилфенил)пиразол (0.5 г), трифенилфосфин (1.884 г), дибромдифторметан (0.33 мл) и дихлорметан (50 мл) поместили в стальной автоклав из нержавеющей стали, нагревали и перемешивали при 90oC в течение 12 часов. Реакционную смесь упарили и очистили остаток колоночной хроматографией на силикагеле при элюировании хлористым метиленом. При объединении и упаривании соответствующих фракций было получено целевое соединение в виде белых кристаллов с Т. пл. 66-68oC.
ПМР (CDCl3) δ : 2.15 (м, 3H), 7.68 (с, 1H), 7.8 (с, 2H)
MS (термораспыление): М/Z [М + NH4] 398.9; C14H6Cl2F5N3 + NH4 составляет 399.02.
Пример F23 (Иллюстративный)
5-Хлор-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-йодпиразол
К раствору 5 амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- йодпиразола (1 г) в ацетонитриле (15 мл) при перемешивании при 0oC прибавили по каплям хлористый нитрозил (2.7 мл ~ 1М раствора в хлористом метилене). Реакционную смесь кипятили с обратным холодильником в течение 10 минут. Затем реакционную смесь упарили и очистили остаток колоночной хроматографией на силикагеле при элюировании гексаном:толуолом (2:1), а затем толуолом. При объединении и упаривании соответствующих фракций было получено целевое соединение в виде бледно-оранжевых кристаллов с Т. пл. 115.7-116.3oC.
ПМР (CDCl3) δ : 7.8 (с, 2H)
MS (термораспыление): M/Z [М+H] 466.0; C11H2Cl3F3IN3 + NH4 составляет 465.84.
Пример F24
5-Хлор-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-
4-этенилпиразол
К перемешиваемому раствору 5-хлор-3-циано-1-(2,6-дихлор-4- трифторметилфенил)-4-йодпиразола (6 г) в диметилформамиде (75 мл) при комнатной температуре прибавили тетракис(трифенилфосфин) палладий (O) (0.448 г). Через 5 минут по каплям прибавили винил-три-н-бутил олово (11.3 мл) и смесь нагревали при 70oC в течение ночи. Реакционную смесь упарили и распределили между эфиром и водой. Органический слой отделили, высушили и упарили. Остаток очистили колоночной хроматографией на силикагеле при элюировании гексаном, а затем гексаном:хлористым метиленом (2:1). При объединении и упаривании соответствующих фракций с последующей перекристаллизацией из гексана получили целевое соединение в виде белых кристаллов, Т. пл. 69.8-70.4oC.
ПМР (CDCl3) δ : 5.61 (д, 1H), 6.2 (д, 1H), 6.56 (дд, 1H), 7.8 (с, 2H)
MS (термораспыление): М/Z [М+ NH4] 383.1; C13H5Cl3F3N3 + NH4 составляет 382.98.
Пример F25 (Иллюстративный)
5-Хлор-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-формилпиразол 4-формилпиразол
К раствору 5-хлор-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- этенилпиразола (0.6352 г) в ацетоне (18 мл) прибавили воду (2 мл), тетроксид осмия (0.57 мл 2.5% раствора в трет-бутаноле) и метапериодат натрия (0.749 г). После перемешивания при комнатной температуре в течение 1 часа добавили метапериодата натрия (0.749 г) и продолжали перемешивание в течение 1 часа. Реакционную смесь упарили и обработали остаток этилацетатом (20 мл) и водным раствором гидрокарбоната калия (3 мл). После перемешивания в течение 20 минут слои разделили. Водный слой экстрагировали этилацетатом. Объединенные этилацетатные экстракты промыли водным раствором гидрокарбоната калия, затем рассолом, высушили (Na2SO4) и упарили. Остаток очистили колоночной хроматографией на силикагеле при элюировании гексаном:хлористым метиленом (2:1). При объединении и упаривании соответствующих фракций с последующей перекристаллизацией из гексана получили целевое соединение в виде белых кристаллов, Т.пл. 145.2-145.9oС.
ПМР (CDCl3) δ : 7.84 (с, 2H), 10.04 (с, 1H)
MS (термораспыление): М/Z [М+ NH4] 385.3; C12H3Cl3F3N3O + NH4 составляет 384.96.
Пример F26
5-Хлор-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-(2,2-дибромэтенил) пиразол
К раствору трифенилфосфина (0.709 г) в сухом хлористом метилене (2 мл) при перемешивании при 0oC в атмосфере сухого азота прибавили четырехбромистый углерод (0.358 г) в сухом хлористом метилене (2 мл) в течение 5 минут, после чего прибавили 5-хлор-3-циано-1-(2,6-дихлор- 4-трифторметилфенил)-4-формилпиразол (0.2 г) в сухом хлористом метилене (3 мл). Смесь оставили нагреваться до комнатной температуры и продолжали перемешивание в течение ночи. Реакционную смесь промыли водой. Водный слой дважды экстрагировали хлористым метиленом. Объединенные органические слои промыли рассолом, высушили (Na2SO4) и упарили. Остаток очистили колоночной хроматографией на силикагеле при элюировании гексаном:хлористым метиленом (1:1). При объединении и упаривании соответствующих фракций с последующей перекристаллизацией из гексана получили целевое соединение в виде белых кристаллов, Т.пл. 119.1-119.5oC.
ПМР (CDCl3) δ : 7.24 (с, 1H), 7.81 (с, 2H)
MS (термораспыление): М/Z [М+ NH4] 538.8; C13H3Br2Cl3F3N3 + NH4 составляет 538.81.
Пример F27
5-Хлор-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-этинилпиразол
К раствору 5-хлор-3-циано-4-(2,2-дибромэтенил)-1-(2,6-дихлор-4- трифторметилфенил) пиразола (2.12 г) в диметилсульфоксиде (8 мл) при 15oC прибавили по каплям при перемешивании раствор 1,8-диазабицикло [5.4.0] ундец-7-ена (1.21 мл) в диметилсульфоксиде (7.9 мл). Через 2 часа реакционную смесь нейтрализовали 0.5 N соляной кислотой и распределили между водой и хлористым метиленом. Водный слой трижды экстрагировали хлористым метиленом. Объединенные органические слои промыли рассолом, высушили (Na2SO4) и упарили. Остаток очистили колоночной хроматографией на силикагеле при элюировании гексаном: хлористым метиленом (1:1). При объединении и упаривании соответствующих фракций с последующей перекристаллизацией из гексана получили целевое соединение в виде светло-розовых кристаллов, Т.пл. 109.1 -109.9oC.
ПМР (CDCl3) δ : 3.54 (с, 1H), 7.84 (с, 2H)
MS (термораспыление): М/Z [М+NH4] 380.7; C13H3Cl3F3N3 + NH4 составляет 380.97.
Пример F28
4-Бромэтинил-5-хлор-3-циано-1-(2,6-дихлор-4-трифторметилфенил)пиразол
К раствору 5-хлор-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- этинилпиразола (0.499 г) в ацетоне (5 мл) прибавили при перемешивании N- бромсукцинимид (0.244 г), а затем нитрат серебра (0.023 г). Перемешивание продолжали один час, затем реакционную смесь упарили досуха. Остаток распределили между эфиром и водой. Водный слой отделили и экстрагировали эфиром. Объединенные органические слои промыли рассолом, высушили (Na2SO4) и упарили. Остаток очистили колоночной хроматографией на силикагеле при элюировании хлористым метиленом: гексаном (1: 1). При объединении и упаривании соответствующих фракций с последующей перекристаллизацией из гексана получили целевое соединение в виде белых кристаллов, Т.пл. 152.9-153.4oC.
ПМР (CDCl3) δ : 7.80 (с, 2H)
MS (термораспыление): М/Z [М+NH4] 459.0; C13H2BrCl3F3N3 + NH4 составляет 458.88.
Пример F29
4-(2-бром-1,2-дихлорэтенил)-5-хлор-3-циано-1-(2,6-дихлор-4- трифторметилфенил)пиразол
К раствору 4-бромэтинил-5-хлор-3-циано-1-(2,6-дихлор- 4-трифторметилфенил) пиразола (0.42 г) в хлористом метилене (10 мл), охлажденному до -78oC, при перемешивании прибавили раствор хлора (0.134 г) в хлористом метилене (5 мл). Перемешивание продолжали при -78oC два часа и затем реакционную смесь оставили нагреваться до комнатной температуры. Перемешивание продолжали в течение ночи и затем смесь упарили досуха. Остаток очистили колоночной хроматографией на силикагеле при элюировании хлористым метиленом: гексаном (1:1). При объединении и упаривании соответствующих фракций с последующей перекристаллизацией из гексана получили целевое соединение в виде белых кристаллов, Т.пл. 91.1-91.9oC.
ПМР (CDCl3) δ : 7.80 (с, 2H)
MS (термораспыление): М/Z [М+NH4] 528.9; C13H2BrCl5F3N3 + NH4 составляет 528.81.
Пример F30
3-Циано-1-(2,6-дихлор-4-трифторметилфенил)-4-(1-метил-этен-1-ил) пиразол
К раствору 4-ацетил-3-циано-1-(2,6-дихлор-4-трифторметилфенил) пиразола (0.75 г) в тетрагидрофуране (5 мл), охлажденному до -40oC в атмосфере азота, прибавили μ -хлор- μ -метилен-[бис(циклопентадиенил)титан] диметилалюминий (5.18 мл 0.5 М раствора в толуоле) и перемешивали смесь в течение 15 минут, а затем оставили нагреваться до комнатной температуры. После выдерживания при комнатной температуре в течение 2 часов прибавляли по каплям 0.1 М водный раствор сульфата натрия, пока не прекратилось кипение. Реакционную смесь разбавили эфиром (50 мл), промыли водным раствором сульфата натрия, высушили и упарили. Остаток очистили колоночной хроматографией на силикагеле при элюировании хлористым метиленом: гексаном (1: 1). При объединении и упаривании соответствующих фракций получили целевое соединение в виде рыжевато-коричневых кристаллов, Т. пл. 63-64oC.
ПМР (CDCl3) δ : 2.63 (с, 3H), 5.19 (м, 1H), 5.32 (м, 1H), 7.49 (с, 1H), 7.87 (с, 2H)
MS (термораспыление): М/Z [М+NH4] 363.0; C14H8Cl2F3N3 + NH4 составляет 363.04.
Пример F31
3-Циано-1-(2,6-дихлор-4-трифторметилфенил)-4-(2-метилпроп-1-енил)пиразол
Изопропилтрифенилфосфоний йодид (0.97 г) в безводном эфире (10 мл) при комнатной температуре обработали н-бутиллитием (0.9 мл 2.5 М раствора в гексанах). К полученному темно-красному раствору прибавили 3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4- формилпиразол (0.6 г) в эфире (20 мл) и перемешивали смесь в течение 2 часов. Этот раствор промыли водой (20 мл) и отделенный органический слой высушили (MgSO4) и упарили. Остаток очистили колоночной хроматографией на силикагеле при элюировании хлористым метиленом. При объединении и упаривании соответствующих фракций получили целевое соединение в виде светлых рыжевато-коричневых кристаллов, Т. пл. 72-74oC.
ПМР (CDCl3) δ : 1.9 (с, 3H), 1.99 (с, 3H), 6.17 (с, 1H), 7.6 (с, 1H), 7.77 (с, 2H)
MS (термораспыление): М / Z [М+ NH4] 360.2: C15H10Cl2F3N3 + NH4 составляет 360.03.
Пример G1 (Иллюстративный)
5-Амино-1-(2,6-дихлор-4-трифторметилсульфенилфенил)-4-йод-3- трифторметилпиразол
К раствору 5-амино-1-(2,6-дихлор-4-трифторметилсульфенилфенил)-3- трифторметилпиразола (0.182 г) в ацетонитриле (3 мл) при перемешивании при комнатной температуре прибавили N-йодсукцинимид (0.113 г). Спустя 20 минут смесь упарили до сухого остатка и растворили остаток в хлористом метилене (20 мл). После промывания водой (20 мл, х 2), рассолом и высушивания (MgSO4) раствор упарили. Остаток растерли с гексаном, а отстой упарили, получив целевое соединение в виде беловатых кристаллов, Т. пл. 126oC.
ПМР (CDCl3) δ : 3.9 (ушир. с, 2H), 7.80 (с, 2H)
MS (термораспыление): M/Z [М+H] 490.2; C11H4Cl2F6IN3 + H составляет 489.88.
Пример G2 (Иллюстративный)
1-(2,6-Дихлор-4-трифторметилфенил)-4-йод-3-трифторметилпиразол
К раствору 5-амино-1-(2,6-дихлор-4-трифторметилфенил)-4-йод-3- трифторметилпиразола (3.3 г) в тетрагидрофуране (25 мл) при перемешивании при 65oC прибавили по каплям трет-бутил-нитрит (4.22 г) в тетрагидрофуране (5 мл) в течение 30 минут и продолжали нагревание в течение 3 часов. Реакционную смесь упарили в масло, которое затвердело при стоянии. При кристаллизации из пропан-2-ола целевое соединение было получено в виде желтых кристаллов, Т. пл. 109-112oC.
ПМР (CDCl3) δ : 7.7 (с, 1H), 7.77 (с, 2H)
Элементный анализ - найдено: C, 27.87, H, 0.69, N? 6/15%; для C11H4Cl2F6IN3 C, 27.82, H, 0.64, N, 5.90%.
Пример G3
1-(2,6-Диxлop-4-тpифтopмeтилфeнил)-4-этенил-3-трифторметилпиразол
Раствор 1-(2,6-дихлор-4-трифторметилфенил)-4-йод-3-трифторметилпиразола (1 г) в диметилформамиде (5 мл), содержащий винилтри-н-бутил олово (2 мл) и тетракис(трифенилфосфин)палладий (O) (0.1 г), перемешивали при 75oC в течение 3 часов. Реакционную смесь упарили и распределили затем между водой и эфиром. Органический слой отделили, промыли водой (х 5), высушили (Na2SO4) и упарили. Остаток кристаллизовали из гексана и далее очистили колоночной хроматографией на силикагеле при элюировании эфиром. При объединении и упаривании соответствующих фракций получили желтый остаток, который далее очистили высокоэффективной хроматографией с обращенной фазой на двуокиси кремния C18 при элюировании смесью ацетонитрил: метанол:вода (40:20:50). При объединении и упаривании соответствующих фракций с последующей перекристаллизацией из пропан-2-ола получили целевое соединение в виде светло-желтых кристаллов, Т. пл. 95-98oC.
ПМР (CDCl3) δ : 5.39 (д, 1H), 5.65 (д, 1H), 6.69 (дд, 1H), 7.8 (с, 1H), 7.81 (с, 2H)
MS (термораспыление): М/Z [М+ NH4] 391.9; C13H6Cl2F6N2 + NH4 составляет 392.02.
Пример G4
5-Амино-1-(2,6-дихлор-4-трифторметилфенил)-3-трифторметил-4- триметсилилэтинилпиразол
К раствору 5-амино-1-(2,6-дихлор-4-трифторметилфенил)-4-йод- 3-трифторметилпиразола (28 г) в триэтиламине (120 мл) и диметилформамиде (24 мл) при перемешивании при комнатной температуре прибавили триметилсилилацетилен (12 мл), йодид меди (0.6 г) и бис(трифенилфосфин)палладий (II) хлорид (1.2 г). Смесь кипятили с обратным холодильником в течение 4 часов и затем оставили при комнатной температуре на ночь. Реакционную смесь разбавили водой (500 мл) и эфиром (500 мл) и профильтровали. Органический слой фильтрата отделили, высушили (MgSO4) и упарили, получив сырой продукт в виде масла, которое очистили колоночной хроматографией на силикагеле при элюировании хлористым метиленом: гексаном (1: 1). При объединении и упаривании соответствующих фракций с последующей перекристаллизацией из гексана получили целевое соединение в виде желто-коричневых кристаллов. Т. пл. 120-123oC.
ПМР (CDCl3) δ : 0.28 (с, 9H), 4.12 (ушир. с, 2H), 7.75 (с, 2H)
MS (термораспыление): M/Z [М+H] 459.9; C16H13Cl2F6N3Si + H составляет 460.02.
Пример G5
1-(2,6-Дихлор-4-трифторметилфенил)-3-трифторметил-4- триметсилилэтинилпиразол
К раствору 5-амино-1-(2,6-дихлор-4-трифторметилфенил)-3-трифторметил-4- триметилсилилэтинилпиразола (6.39 г) в тетрагидрофуране (50 мл) при перемешивании при 65oC прибавили по каплям трет-бутил нитрит (7.15 г) в тетрагидрофуране (10 мл) в течение одного часа. Нагревание продолжали в течение 2 часов, затем смесь оставили на ночь при комнатной температуре. После упаривания остаток растворили в гексане и декантировали с нерастворившихся веществ. Этот раствор упарили и очистили колоночной хроматографией на силикагеле при элюировании хлористым метиленом:гексаном (1:1). При объединении и упаривании соответствующих фракций с последующей перекристаллизацией из гексана получили целевое соединение в виде бледно-желтых кристаллов, Т.пл. 105-108oC.
ПМР (CDCl3) δ : 0.28 (с, 9H), 7.74 (с, 1H), 7.75 (с, 2H)
MS (термораспыление): М/Z [М+NH4] 461.8; C16H12Cl2F6N2Si + NH4 составляет 462.04.
Пример G6
1-(2,6-Дихлор-4-трифторметилфенил)-4-этинил-3-трифторметилпиразол
К раствору 1-(2,6-дихлор-4-трифторметилфенил)-3-трифторметил-4- триметилсилилэтинилпиразола (4.6 г) в метаноле (75 мл) прибавили при перемешивании карбонат калия (2.5 г). После выдерживании при комнатной температуре в течение 3 часов реакционную смесь сконцентрировали и затем распределили между эфиром (250 мл) и водой (250 мл). Органический слой отделили, промыли рассолом, высушили и упарили, получив масло, которое кристаллизовали гексаном, получив целевое соединение в виде бледно-желтых кристаллов, Т. пл. 95-98oC.
ПМР (CDCl3) δ : 3.27 (с, 1H), 7.75 (с, 2H), 7.79 (с, 1H)
MS (термораспыление): М/Z [М + NH4] 390.2; C13H4Cl2F6N2 + NH4 составляет 390.0
Пример G7
4-Бромэтинил-1-(2,6-дихлор-4-трифторметилфенил)-3-трифторметилпиразол
К раствору 1-(2,6-дихлор-4-трифторметилфенил)-4-этинил-3- трифторметилпиразола (3.1 г) в ацетоне (25 мл) при перемешивании добавили N-бромсукцинимид (1.4 г) и нитрат серебра (0.14 г). Перемешивание продолжали при комнатной температуре в течение 2 часов. Реакционную смесь упарили и распределили остаток между эфиром и водой. Органический слой отделили, промыли раствором соли, высушили и упарили. Остаток очистили колоночной хроматографией на силикагеле (10 г) при элюировании гексаном, а затем хлористым метиленом: гексаном (1:1). При объединении и упаривании соответствующих фракций с последующей перекристаллизацией из гексана получили целевое соединение в виде белых кристаллов, Т. пл. 92-94oC.
ПМР (CDCl3) δ : 7.77 (с, 1H), 7.78 (с,2H).
MS (термораспыление): М/Z [М + NH4] 468.6; C13H3BrCl2F6N2 + NH4 составляет 468.91.
Пример G8
4-(2-Бром-1,2-дихлорэтенил)-1-(2,6-дихлор-4-трифторметилфенил)-3- трифторметилпиразол
К раствору 4-бромэтинил-1-(2,6-дихлор-4-трифторметилфенил)-3- трифторметилпиразола (0.45 г) в хлористом метилене (10 мл), охлажденному до -78oC, при перемешивании прибавили по каплям раствор хлора (0,142 г) в хлористом метилене (5 мл). Перемешивание продолжали при -78oC в течение 2-х часов и затем реакционную смесь оставили нагреваться до комнатной температуры в течение ночи. Смесь упарили и очистили колоночной хроматографией на силикагеле (10 г) при элюировании гексаном и затем хлористым метиленом:гексаном (1: 1). При объединении и упаривании соответствующих фракций с последующей перекристаллизацией из гексана получили целевое соединение в виде светло-желтых кристаллов, Т. пл. 57-59oC.
ПМР (CDCl3)δ : 7.77 (с, 1H), 7.79 (с, 2H)
Элементный анализ - найдено: C, 30.14, H, 0.55, N, 6.67%; для C13H3BrCl4F6N2 C, 29.86, H, 0.58, N, 5.36%.
Пример G9 (Иллюстративный)
1-(2,6-Дихлор-4-трифторметилфенил)-3,5-диметил-4-йодпиразол
К раствору 1-(2,6-дихлор-4-трифторметилфенил)-3,5-диметилпиразола (0.218 г) в ацетонитриле (3 мл) при перемешивании при комнатной температуре прибавили раствор N-йодсукцинимида (0.158 г) в ацетонитриле (2 мл). Через 27 часов смесь упарили досуха и очистили остаток колоночной хроматографией на силикагеле (5 г) при элюировании хлористым метиленом. При объединении и упаривании соответствующих фракций с последующей перекристаллизацией из гексана получили целевое соединение в виде желтого масла.
ПМР (CDCl3) δ : 2.11 (с, 3H), 2.32 (с, 3H), 7.73 (с, 2H)
MS (термораспыление): M/Z [М+H] 435.0; C12H8Cl2F3IN2 + H составляет 434.91.
Пример G10
1-(2,6-Дихлор-4-трифторметилфенил)-3,5-диметил-4-этенилпиразол
Раствор 1-(2,6-дихлор-4-трифторметилфенил)-3,5-диметил-4-йодпиразола (1 г) в диметилформамиде (10 мл), содержащий винилтри-н-бутил олово (2 мл) и тетракис(трифенилфосфин)палладий (О) (0.1 г), перемешивали при 75oC в течение 2 часов, после чего оставили на ночь при комнатной температуре. Смесь опять нагревали при 75oC в течение 2 часов, затем добавили винилтри-н-бутил олово (2 мл) и нагревали смесь при 75oC в течение 2 часов. Добавили тетракис(трифенилфосфин)палладий (O) (0.1 г) и продолжали перемешивать еще в течение 2 часов. Реакционную смесь упарили и распределили затем между водой и хлористым метиленом. Органический слой отделили, промыли водой (х 5), рассолом, высушили (Na2SO4) и упарили. Остаток адсорбировали на силикагель (20 г) и очистили колоночной хроматографией на силикагеле (150 г) при элюировании гексаном, затем гексаном с возрастающими количествами хлористого метилена и наконец хлористым метиленом. При объединении и упаривании соответствующих фракций с последующей перекристаллизацией из гексана получили целевое соединение в виде желтого масла.
ПМР (CDCl3) δ : 2.11 (с, 3H), 2.4 (с, 3H), 5.23 (д, 1H), 5.41 (д, 1H), 6.59 (дд, 1H), 7,71 (с, 2H)
MS (термораспыление): M/Z [М+H] 335.1; C14H11Cl2F3N2 + H составляет 335.03
Пример G11 (Иллюстративный)
5-Амино-1-(2,6-дихлор-4-трифторметилфенил)-4-йод-3-метилпиразол
К раствору 5-амино-1-(2,6-дихлор-4-трифторметилфенил)-3-метилпиразола (9 г) в ацетонитриле (200 мл) при перемешивании при комнатной температуре прибавили N-йодсукцинимид (5.5 г). Смесь кипятили с обратным холодильником один час и затем оставили на ночь при комнатной температуре. Смесь упарили и растерли остаток с горячим гексаном. Выпавший при остывании осадок отфильтровали и высушили, получив целевое соединение в виде беловатых кристаллов, Т. пл. 116-118oC.
ПМР (CDCl3) δ : 2.24 (с, 3H), 3.68 (ушир. с, 2H), 7.74 (с, 2H)
MS (термораспыление): M/Z [М+H] 435.8; C11H7Cl2F3IN3 + H составляет 435.91.
Пример G12 (Иллюстративный)
1-(2,6-Дихлор-4-трифторметилфенил)-4-йод-3-метилпиразол
К раствору 5-амино-1-(2,6-дихлор-4-трифторметилфенил)- 4-йод-3-триметилпиразола (2.85 г) в тетрагидрофуране (35 мл) при 0oC по каплям при перемешивании прибавили трет-бутил нитрит (2.33 мл). Реакционной смеси дали нагреться до комнатной температуры, а затем кипятили с обратным холодильником 1.5 часа. Реакционную смесь упарили и очистили остаток колоночной хроматографией на силикагеле при элюировании хлористым метиленом:гексаном (1: 1). При объединении и упаривании соответствующих фракций получили желтое масло, которое очистили далее колоночной хроматографией на силикагеле при элюировании хлористым метиленом:гексаном (1:2). При объединении и упаривании соответствующих фракций получили целевое соединение в виде белых кристаллов, Т. пл. 118.5-119.4oC.
ПМР (CDCl3) δ : 2.18 (с, 3H), 7.54 (с, 1H), 7.7 (с, 2H)
MS (термораспыление): M/Z [М+H] 420.5; C11H6Cl2F3IH2 + H составляет 419.89.
Пример G13
1-(2,6-Дихлор-4-трифторметилфенил)-4-этенил-3-метилпиразол
К раствору 1-(2,6-дихлор-4-трифторметилфенил)-4-йод-3- метилпиразола (2.06 г) в диметилформамиде (25 мл) прибавили тетракис (трифенилфосфин) палладий (O) (0.1 г) и винилтри-н-бутил олово (2 мл). Смесь нагревали при 70oC в течение 2 часов. Смесь упарили и распределили между водой и эфиром. Водный слой отделили и дважды экстрагировали эфиром. Объединенные органические слои промыли рассолом, высушили (Na2SO4) и упарили. Остаток очистили колоночной хроматографией на силикагеле при элюировании смесью гексан:эфир (9:1). При объединении и упаривании соответствующих фракций получили желтый осадок, который очистили далее высокоэффективной хроматографией с обращенной фазой на двуокиси кремния C18 при элюировании смесью ацетонитрил:метанол:вода (40: 10: 50). При объединении и упаривании соответствующих фракций с последующей перекристаллизацией из пропан-2-ола получили целевое соединение в виде белых кристаллов, Т. пл. 68.1 - 68.7oC.
ПМР (CDCl3) δ : 2.44 (с, 3H), 5.24 (д, 1H), 5.5 (д, 1H), 6.62 (дд, 1H), 7.57 (с, 1H), 7,74 (с, 2H)
MS (термораспыление): М/Z [М+H] 321.1; C13H9Cl2F3N2 + H составляет 321.02.
Пример G14
5-Амино-1-(2,6-дихлор-4-трифторметилфенил)-3-метил-4- триметсилилэтинилпиразол
К раствору 5-амино-1-(2,6-дихлор-4-трифторметилфенил)-4-йод-3- метилпиразола (9.1 г) в триэтиламине (45 мл) и диметилформамиде (9 мл) при перемешивании при комнатной температуре прибавили триметилсилилацетилен (4.5 мл), йодид меди (0.225 г) и бис (трифенилфосфин) палладий (II) хлорид (0.45 г). Смесь кипятили с обратным холодильником в течение 4 часов и оставили при комнатной температуре на ночь. Реакционную смесь упарили, получив сырой продукт в виде масла, которое очистили колоночной хроматографией на силикагеле при элюировании смесью хлористый метилен:гексан (1:1). При объединении и упаривании соответствующих фракций с последующей перекристаллизацией из гексана получили целевое соединение в виде желто-коричневых кристаллов, Т. пл. 121 -123oC.
ПМР (CDCl3) δ : 0.28 (с, 9H), 2.3 (с, 3H), 3.92 (ушир. с, 2H), 7.82 (с, 2H)
MS (термораспыление): M/Z [М+H] 406.0; C16H16Cl2F3N3Si + H составляет 406.05.
Пример G15
1-(2,6-Дихлор-4-трифторметилфенил)-3-метил-4-триметсилилэтинилпиразол
К раствору 5-амино-1-(2,6-дихлор-4-трифторметилфенил)-3-метил-4- триметилсилилэтинилпиразола (1.3 г) в тетрагидрофуране (15 мл) при 65oC по каплям при перемешивании прибавили в течение 15 минут трет-бутил нитрит (1.65 г) в тетрагидрофуране (5 мл) и продолжали нагревание в течение 3 часов. Реакционную смесь оставили стоять при комнатной температуре на ночь, затем ее упарили, получив сырой продукт в виде смолы, которую очистили колоночной хроматографией на силикагеле при элюировании смесью хлористый метилен:гексан (1:1). При объединении и упаривании соответствующих фракций получили целевое соединение в виде светло-желтых кристаллов, Т. пл. 76-78oC.
ПМР (CDCl3) δ : 0.28 (с, 9H), 2.43 (с, 3H), 7.62 (с, 1H), 7.72 (с, 2H)
MS (термораспыление): М/Z [М +H] 391.0; C16H15Cl2F3N2Si + H составляет 391.04.
Пример G16
1-(2,6-Дихлор-4-трифторметилфенил)-4-этинил-3-метилпиразол
К раствору 1-(2,6-дихлор-4-трифторметилфенил)-3-метил-4- триметилсилилэтинилпиразола (0.82 г) в метаноле (15 мл) прибавили при перемешивании карбонат калия (0.75 г). После выдерживания при комнатной температуре в течение 3 часов реакционную смесь вылили в воду (100 мл) и экстрагировали эфиром (50 мл х 2). Объединенные органические слои промыли рассолом, высушили и упарили, получив целевое соединение в виде светло-бежевой смолы.
ПМР (CDCl3) δ : 2.45 (с, 3H), 3.21 (с, 1 H), 7.64 (с, 1H), 7.81 (с, 2H)
MS (термораспыление): M/Z [М+H] 319.0; C13H7Cl2F3N2 + H составляет 319.0
Пример G17
4-Бромэтинил-1-(2,6-дихлор-4-трифторметилфенил)-3-метилпиразол
К раствору 1-(2,6-дихлор-4-трифторметилфенил)-4-этинил-3-метилпиразола (0.53 г) в ацетоне (5 мл) при перемешивании при комнатной температуре прибавили N-бромсукцинимид (0.295 г) и нитрат серебра (0.028 г). Перемешивание продолжили при комнатной температуре в течение 1 часа. Реакционную смесь упарили, а остаток растворили в эфире и промыли водой. Органический слой отделили, высушили и упарили. Остаток очистили колоночной хроматографией на силикагеле (10 г) при элюировании гексаном, а затем смесью хлористый метилен: гексан (1: 1). При объединении и упаривании соответствующих фракций с последующей перекристаллизацией из гексана получили целевое соединение в виде очень бледно-желтых кристаллов, Т. пл. 86-89oC.
ПМР (CDCl3) δ: 2.42 (с, 3H), 7.62 (с, 1H), 7.81 (с, 2H)
Элементный анализ - найдено: C, 39.20, H, 1.52, N, 6.94 %; для C13H6BrCl4F3N2 C, 39.23, H, 1.52, N, 7.04%.
Пример G18 (Иллюстративный)
5-Амино-1-(2,6-дихлор-4-трифторметилфенил)-3-фенилпиразол
Раствор 2,6-дихлор-4-трифторметилфенилгидразина (0.245 г) в этаноле (2 мл) прибавили к бензоилацетонитрилу (0.145г) в этаноле (8 мл) и нагревали этот раствор при 80oC в течение 6 часов. Прибавили ледяную уксусную кислоту (1 мл) и нагревали смесь при 80oC в течение 4 часов, а затем при 90oC в течение 2 часов. Реакционную смесь упарили, а остаток очистили колоночной хроматографией на силикагеле (10 г) при элюировании хлористым метиленом. После объединения и упаривания соответствующих фракций последовала дальнейшая очистка их остатка высокоэффективной жидкостной хроматографией с обращенной фазой на двуокиси кремния C18 при элюировании смесью метанол: ацетонитрил: вода (1: 5: 4). При объединении и упаривании соответствующих фракций получили целевое соединение в виде белых кристаллов, Т. пл. 141.5-142.5oC.
ПМР (CDCl3) δ : 3.60 (ушир. с, 2H), 6.08 (с, 1H). 7.3-7.45 (м, 3H), 7.80 (с, 2H), 7.8-7.85 (м, 2H)
MS (термораспыление): M/Z [М+H] 372.1; C16H10Cl2F3N2 + H составляет 372.03.
Пример G19 (Иллюстративный)
5-Амино-1-(2,6-дихлор-4-трифторметилфенил)-4-йод-3-фенилпиразол
Раствор 5-амино-1-(2,6-дихлор-4-трифторметилфенил)-3-фенилпиразола (0.12 г) и N-йодсукцинимида (0.08 г) в ацетонитриле (5 мл) оставили на ночь при перемешивании при комнатной температуре. Смесь упарили досуха и распределили остаток между хлористым метиленом (15 мл) и водой (15 мл). Органический слой отделили и промыли водой (20 мл х 2), рассолом (15 мл) и высушили (MgSO4) и упарили. Остаток растерли с гексаном, получив целевое соединение в виде желтых кристаллов, Т.пл. 162-164oC.
ПМР (CDCl3) δ: 3.8 (ушир. с, 2H), 7.35 (м, 3H), 7.78 (с, 2H), 7,95 (м, 2H)
MS (термораспыление): M/Z [М+H] 498.1; C16H9Cl2F3IN3 + H составляет 497.93.
Пример G20 (Иллюстративный)
1-(2,6-Дихлор-4-трифторметилфенил)-4-йод-3-фенилпиразол
К раствору 5-амино-1-(2,6-дихлор-4-трифторметилфенил)-4-йод-3- фенилпиразола (2.5 г) в тетрагидрофуране (50 мл) при 65oC при перемешивании прибавили по каплям в течение 30 минут трет-бутил нитрит (3 г) в тетрагидрофуране (20 мл) и продолжали нагревание в течение 3 часов, после чего смесь оставили стоять при комнатной температуре на ночь. Реакционную смесь упарили до состояния масла, которое очистили колоночной хроматографией на силикагеле при элюировании хлористым метиленом. После объединения и упаривания соответствующих фракций провели дальнейшую колоночную хроматографию на силикагеле при элюировании гексаном, затем гексаном, содержащим 5% этилацетата, и наконец гексаном, содержащим 10% этилацетата. При объединении и упаривании соответствующих фракций получили целевое соединение в виде кремовых кристаллов, Т. пл. 88-89oC.
ПМР (CDCl3) δ : 7.45 (м, 3H), 7.7 (с, 1H), 7.72 (с, 2H), 7.95 (м, 2H)
MS (термораспыление): M/Z [М+H] 482.8; C16H8Cl2F3IN2 + H составляет 482.91.
Пример G21
1-(2,6-Дихлор-4-трифторметилфенил)-4-этенил-3-фенил-пиразол
К раствору 1-(2,6-дихлор-4-трифторметилфенил)-4-йод-3-фенилпиразола (1 г) в диметилформамиде (12 мл) прибавили тетракис(трифенилфосфин)палладий (O) (0.07 г) и перемешивали смесь при комнатной температуре в течение 10 минут. Добавили винилтри-н-бутил олово (1.8 мл) и нагревали смесь при 70oC в течение 6 часов, а затем оставили на ночь при комнатной температуре. Реакционную смесь упарили и распределили между водой (50 мл) и хлористым метиленом (50 мл). Органический слой отделили и дважды экстрагировали эфиром. Объединенные органические слои промыли рассолом, высушили (MgSO4) и упарили. Остаток очистили колоночной хроматографией на силикагеле при элюировании гексаном, содержащим возрастающие количества этилацетата. Соответствующие фракции объединили и упарили, а их остаток далее очистили колоночной хроматографией на силикагеле при элюировании гексаном, содержащим возрастающие количества эфира. При объединении и упаривании соответствующих фракций получили целевое соединение в виде желтого масла.
ПМР (CDCl3) δ : 5.25 (д, 1 H), 5.65 (д, 1 H), 6.80 (дд, 1 H), 7.45 (м, 5H), 7.75 (м, 5H)
MS (термораспыление): M/Z [М+H] 383.3: C18H11Cl2F3N2 + H составляет 383.00
Приготовления
Приготовление 1: 5-Амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил) пиразол, использованный в примере A1, получали, как описано в ЕР-295,117.
Приготовление 2: 5-Амино-3-циано-1-(2,6-дихлор-4-трифторметоксифенил) пиразол, использованный в примере D1, получали, как описано в ЕР-295,117.
Приготовление 3: 5-Амино-3-циано-1-(2,6-дихлор-4- трифторметилсульфенилфенил)пиразол, использованный в примере D7, получали при использовании метода, упомянутого выше для Приготовления 2.
Приготовление 4: 5-Амино-3-циано-1-(2,6-дихлор-4-ceрапентафторфенил) пиразол, использованный в примере D11, получали, как описано в WO 93/06089.
Приготовление 5: 5-Амино-1-(2,6-дихлор-4-трифторметилфенил)-3- трифторметилпиразол, использованный в примере G1, получали, как описано в WO 87/03781.
Приготовление 6: 1-(2,6-дихлор-4-трифторметилфенил)-3,5-диметилпиразол, использованный в примере G9, получали, как описано в Can. J, Chem., 1979, 57,904.
Приготовление 7: 5-Амино-1-(2,6-дихлор-4-трифторметилфенил)-3- метилпиразол, использованный в примере G11, получали при использовании метода, описанного в DE 4414333 для получения 5-амино -1-[(3- хлор-5-трифторметил)-2 - пиридил]-3-метилпиразола.
Результат биологического теста
Найдено, что соединение Примера A3 вызывает 100% смертность в пределах дозировки 0.005-100 μг на муху при использовании описанного выше способа.
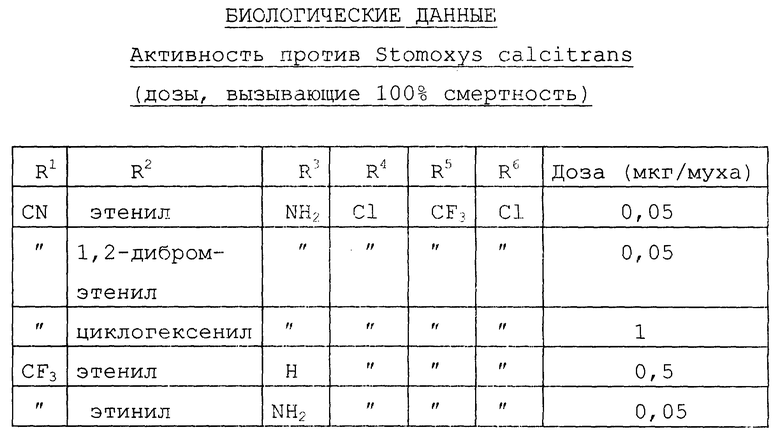

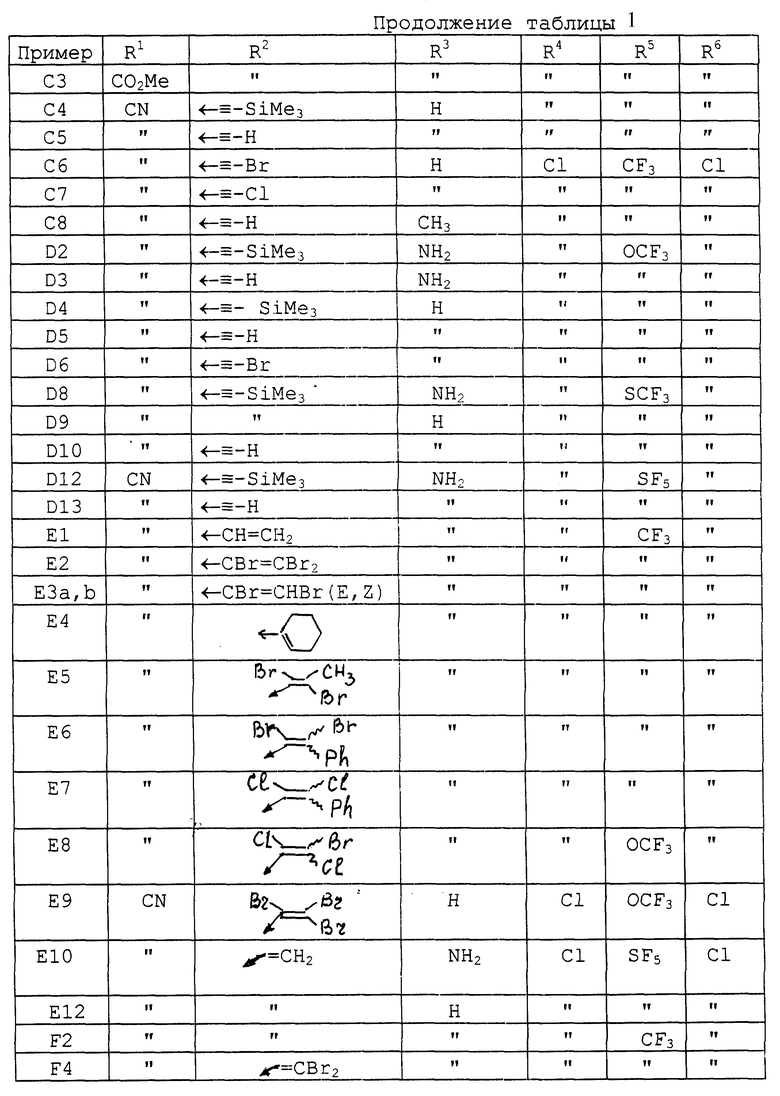
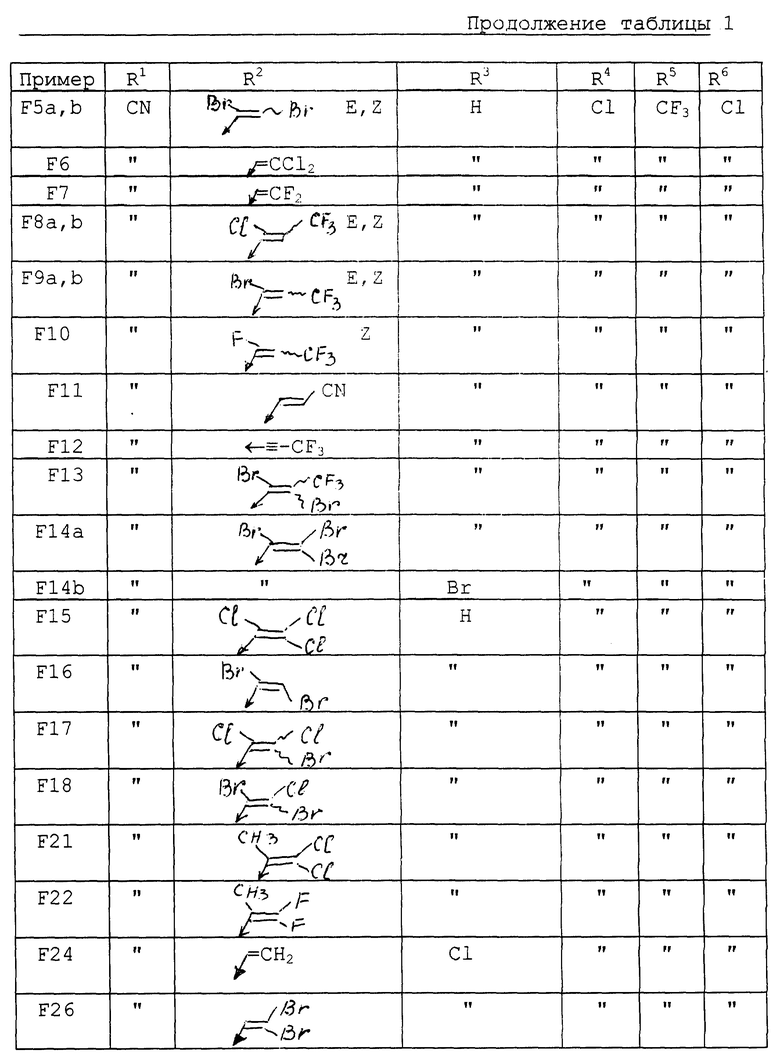

Описываются новые производные пиразола формулы (I), где R1 является CN, C1-6 алкоксикарбонилом, фенилом или C1-6 алкилом, необязательно замещенным одним или более атомами галогена; R2 является группой формулы II, III или IV, в которой R7 является H, галогеном, три(C1-6алкил)силилом, C1-6алкилом (необязательно замещенным одним или более атомами галогена, OH или C1-6алкоксигруппой), C1-6алкоксикарбонилом, фенильной группой или 5- или 6-членным циклическим гетероциклом, который насыщен или частично или полностью ненасыщен и содержит вплоть до 4 гетероатомов, независимо выбранных из вплоть до 4 N атомов, до 2 O атомов и до 2 S атомов, и который присоединен к алкильному звену при помощи подходящего атома С, S или N, где позволяет валентность; и R8, R9 и R10 каждый является независимо H, галогеном, фенилом, необязательно замещенным одним или более атомами галогена, CN или C1-6алкильной группой, необязательно замещенной одним или более атомами галогена; R3 представляет H, C1-6алкил, галоген, NH2, NH(С1-6алканоил), NH(C1-6алкоксикарбонил), N(C1-6 алкоксикарбонил)2, NH(C1-6алкил), N(C1-6алкил)2, NHCONH(C1-6 алкил), N-пирролил, SH или S (O)n (C1-6алкил), где n равно 0, 1 или 2; и R4, R5 и R6 каждый является независимо галогеном, C1-6алкилом, замещенным одним или более атомами галогена, C1-6алкоксигруппой, замещенной одним или более атомами галогена, S(O)n (C1-6алкилом, необязательно замещенным одним или более атомами галогена), где n равно 0, 1 или 2, или SF5, или их фармацевтически или ветеринарно приемлемые соли. Указанные соединения обладают антипаразитическими свойствами. Описывается также способ лечения паразитического заражения и способ повреждения или уничтожения паразитов. 3 с. и 13 з.п.ф-лы, 1 табл.



где R1 является CN С1-6алкоксикарбонилом, фенилом или С1-6алкилом, необязательно замещенным одним или более атомами галогена;
R2 является группой формулы II, III или IV

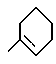
в которой R7 является Н, галогеном, три(С1-6алкил)силилом, С1-6 (необязательно замещенным одним или более атомами галогена, ОН или С1-6алкоксигруппой), С1-6алкоксикарбонилом, фенильной группой или 5- или 6-членным циклическим гетероциклом, который насыщен или частично или полностью ненасыщен и содержит вплоть до 4 гетероатомов, независимо выбранных из вплоть до 4 N атомов, до 2 О атомов и до 2 S атомов и который присоединен к алкинильному звену при помощи подходящего атома С, S, или N, где позволяет валентность;
R8, R9 и R10 каждый является независимо Н, галогеном, фенилом, необязательно замещенным одним или более атомами галогена, CN или С1-6алкильной группой, необязательно замещенной одним или более атомами галогена;
R3 представляет Н, С1-6алкил, галоген, NH2, NH(С1-6алканоил), NH(С1-6алкоксикарбонил), N(С1-6алкоксикарбонил)2, N(С1-6алкил)2, NHCONH(C1-6алкил), N-пирролил, SH или S(О)n(С1-6алкил), где n равно 0,1 или 2;
R4, R5 и R6 каждый является независимо галогеном, C1-6алкилом, замещенным одним или более атомами галогена, C1-6алкоксигруппой, замещенной одним или более атомами галогена, S(O)n(C1-6алкилом, необязательно замещенным одним или более атомами галогена), где n равно 0, 1 или 2, или SF5,
или их фармацевтически или ветеринарно приемлемые соли.
Приоритет по пунктам признакам:
11.08.95 по пп.1 - 16, вариации радикалов R1 - R10;
19.01.96 по пп.1 - 16, вариации радикалов R1 - R10.
| Способ получения производных @ -фенилпиразола | 1983 |
|
SU1309909A3 |
| US 5091378 A, 25.02.1992 | |||
| Торфодобывающая машина с вращающимся измельчающим орудием | 1922 |
|
SU87A1 |
| CHEMICAL ABSTRACTS, т.116, N 25, abstr | |||
| no | |||
| УСТРОЙСТВО ДЛЯ ПРОИЗВОДСТВА РАБОТ В АТМОСФЕРЕ, ОЧИЩЕННОЙ ОТ ПЫЛИ | 0 |
|
SU255528A1 |
Авторы
Даты
2000-06-27—Публикация
1996-08-05—Подача