Изобретение относится к области гальваностегии, в частности к электролитическому нанесению покрытий на основе хрома, а именно сплава хром-цинк, и может найти применение для защиты изделий из металла от коррозии и механического износа.
Известен электролит для нанесения коррозионностойких хромовых покрытий, содержащий хромовый ангидрид (М.К. Шлугер "Гальванические покрытия в машиностроении", 1985 г., с. 125).
Недостатком известного электролита является то, что получение покрытия с удовлетворительной коррозионной стойкостью возможно лишь при высоких температурах электролита и высоких плотностях тока. Кроме того, присутствие серной кислоты в электролите повышает его агрессивность.
Наиболее близким по технической сущности и достигаемому результату к заявляемому изобретению является электролит для нанесения коррозионностойких покрытий сплавом хром-цинк, содержащий хромовый ангидрид и сернокислый цинк, гидрат (патент ГДР N 109032, C 23 B 5/32, 1974 г., опубл. РЖ "Химия", N 4, реф. 4Л 32111, 1976 - прототип).
Недостатками указанного электролита являются низкий выход сплава хром-цинк по току и низкая коррозионная стойкость из-за высоких внутренних напряжений.
Задачей заявляемого изобретения является повышение выхода сплава хром-цинк по току и его коррозионной стойкости, снижение внутренних напряжений.
Решение поставленной задачи достигается тем, что электролит для нанесения коррозионностойких покрытий сплавом хром-цинк, содержащий хромовый ангидрид и сернокислый цинк, гидрат, дополнительно содержит фолиевую кислоту формулы
при следующем соотношении компонентов, г/л:
Хромовый ангидрид - 200 - 300
Сернокислый цинк, гидрат - 70 - 90
Фолиевая кислота - 4 - 6
Молекулы фолиевой кислоты взаимодействуют с ионами хрома (VI), а именно, группа NH2 в мета-положении с группой OH, при этом NH2 окисляется до NO2, а две группы COOH образуют с восстановленными ионами хрома (VI) до хрома (III) и ионами цинка электроактивный адсорбционный комплекс, который является основной (75-80%) составной частью "катодной" пленки. Адсорбционные комплексы проницаемы для протонов, в результате чего концентрация протонов в прикатодном пространстве резко снижается, что приводит к уменьшению наводороживания, уменьшению гидридов хрома и, как следствие, снижению внутренних напряжений в образующихся осадках и повышению их коррозионной стойкости. В присутствии фолиевой кислоты реакция неполного восстановления хрома (VI) до хрома (III) замедляется, а реакция восстановления хрома (III) и цинка до металлического ускоряется, что приводит к увеличению скорости осаждения и содержания цинка в сплаве, получению осадков более измельченной структуры и уменьшению внутренних напряжений в них, что снижает степень трещиноватости.
Таким образом, использование фолиевой кислоты в качестве органической добавки в составе электролита способствует формированию покрытия, обладающего высоким процентом химической и физической однородности, что является новым техническим свойством предлагаемого электролита.
Электролит готовят следующим образом:
в воде растворяют необходимое количество хромового ангидрида и сернокислого цинка, вводят органическую добавку - фолиевую кислоту и доводят раствор водой до требуемого объема.
Процесс электроосаждения проводят при 20-25oC, плотности тока 15-50 А/дм2.
Готовили несколько составов электролитов, отличающихся друг от друга содержанием хромового ангидрида, сернокислого цинка и фолиевой кислоты соответственно, г/л: 200, 250, 300; 70, 80, 90; 4, 5, 6.
Процесс электроосаждения проводили при 20oC и катодной плотности тока 25 А/дм2.
Для сравнения готовили электролит по прототипу при следующем соотношении компонентов, г/л:
Хромовый ангидрид - 270
Сернокислый цинк, гидрат - 100
Серная кислота - 3
Для оценки влияния фолиевой кислоты на процесс осаждения сплава хром-цинк на потенциостате ПИ-50-1 при скорости развертки потенциала 1 мВ/с исследовались потенциодинамические поляризационные кривые с использованием платинового электрода. Эффективную энергию активации определяли температурно-кинетическим методом на основе парциальных кривых.
Коррозионная стойкость хром-цинковых покрытий определялась методом И.Л. Розенфельда и Л.В. Фроловой прибором "Измеритель скорости коррозии Р-5035". Коррозионной средой служит 0,1 н. раствор NaCl.
Внутренние напряжения покрытий определялись методом сжатия-растяжения проволочного катода.
Морфология покрытия изучалась электронно-микроскопически на микроскопе УЭЗМ-100к методом угольных реплик.
Катодный выход сплава по току определяли с помощью медного кулонометра, предварительно определив фотокалориметрически процентный состав покрытия.
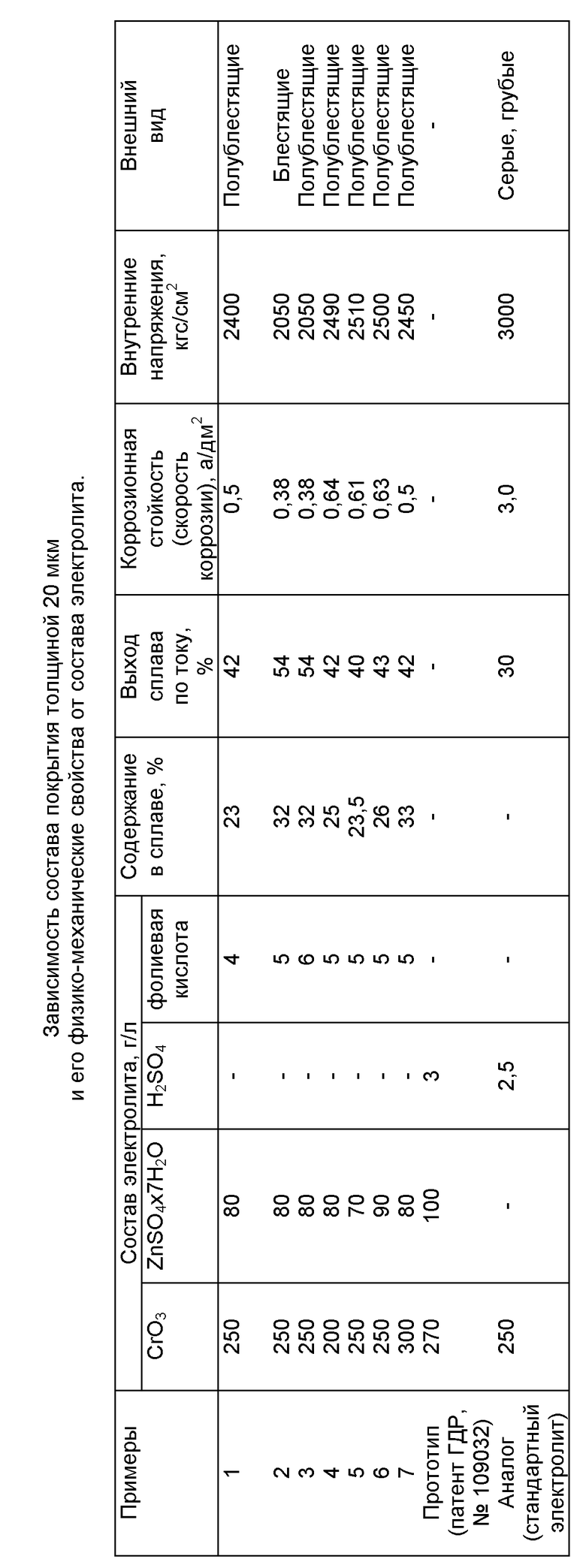
В таблице представлена зависимость состава покрытия толщиной 20 мкм и его физико-механических свойств от состава электролита.
Из анализа представленных данных видно, что при 20oC, плотности тока 25 А/дм2, концентрации фолиевой кислоты в электролите 5 г/л, выход сплава по току составляет 54%, коррозионная стойкость - 0,38 а/дм2, содержание цинка в сплаве - 32%, внутренние напряжения - 2050 кгс/см2, внешний вид осадков удовлетворительный.
По сравнению с прототипом применение предлагаемого электролита при прочих равных условиях (рабочей температуре электроосаждения и катодной плотности тока) позволяет повысить коррозионную стойкость покрытия за счет образования сплава хром-цинк с низкими внутренними напряжениями и увеличить выход сплава хром-цинк по току при удовлетворительном качестве покрытий.
Электролит стабилен в работе. Фолиевая кислота в процессе электролиза не разрушается. Фолиевая кислота обладает высокой биологической активностью, является основной частью ферментных систем, служащих катализаторами жизненных процессов, и выполняет важную функцию защиты организма человека от неблагоприятного воздействия среды, поэтому присутствие ее в водных стоках не опасно.
Фолиевая кислота - доступное и дешевое сырье, необходимое количество ее в электролите 4-6 г/л содержится в 360-500 г зеленых листьев тополя, дуба, акации и др. деревьев, кроме хвойных и фруктовых пород. Корректировку электролита по его составляющим проводят согласно данным анализа раствора.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЭЛЕКТРОЛИТ ДЛЯ НАНЕСЕНИЯ КОРРОЗИОННОСТОЙКИХ ПОКРЫТИЙ СПЛАВОМ ХРОМ - ЦИНК | 1996 |
|
RU2103423C1 |
| ЭЛЕКТРОЛИТ ДЛЯ НАНЕСЕНИЯ МИКРОТВЕРДЫХ ПОКРЫТИЙ НА ОСНОВЕ ХРОМА | 1996 |
|
RU2103421C1 |
| ЭЛЕКТРОЛИТ ДЛЯ НАНЕСЕНИЯ ИЗНОСОСТОЙКИХ ПОКРЫТИЙ СПЛАВОМ НА ОСНОВЕ ХРОМА | 1996 |
|
RU2103422C1 |
| ЭЛЕКТРОЛИТ ДЛЯ НАНЕСЕНИЯ ХРОМОВЫХ ПОКРЫТИЙ | 1995 |
|
RU2092624C1 |
| ЭЛЕКТРОЛИТ ДЛЯ ПОЛУЧЕНИЯ ПОКРЫТИЯ СПЛАВОМ ХРОМ-МОЛИБДЕН | 1995 |
|
RU2092625C1 |
| ЭЛЕКТРОЛИТ ДЛЯ НАНЕСЕНИЯ ХРОМОВЫХ ПОКРЫТИЙ | 1999 |
|
RU2151826C1 |
| ЭЛЕКТРОЛИТ ДЛЯ ПОЛУЧЕНИЯ ХРОМОВЫХ ПОКРЫТИЙ | 1995 |
|
RU2087599C1 |
| ЭЛЕКТРОЛИТ ДЛЯ НАНЕСЕНИЯ ХРОМОВЫХ ПОКРЫТИЙ | 2000 |
|
RU2187586C1 |
| СПОСОБ ОЧИСТКИ ЭЛЕКТРОЛИТА ХРОМИРОВАНИЯ | 1993 |
|
RU2083268C1 |
| СПОСОБ НАНЕСЕНИЯ ЭЛЕКТРОЛИТИЧЕСКИХ ПОКРЫТИЙ НА ОСНОВЕ ХРОМА | 2011 |
|
RU2457288C1 |
Изобретение относится к области гальваностегии, в частности к электролитическому нанесению покрытий на основе хрома, а именно сплава хром-цинк, и может найти применение для защиты изделий из металла от коррозии и механического износа. Сущность изобретения: электролит содержит, г/л: хромовый ангидрид 200 - 300; сернокислый цинк, гидрат 70 - 90 и фолиевую кислоту 4 - 6. Техническим результатом изобретения является повышение выхода сплава хром-цинк по току и его коррозионной стойкости, снижение внутренних напряжений. 1 табл.
Электролит для нанесения коррозионно-стойких покрытий сплавом хром-цинк, содержащий хромовый ангидрид и серно-кислый цинк, гидрат, отличающийся тем, что он дополнительно содержит фолиевую кислоту формулы
при следующем соотношении компонентов, г/л:
Хромовый ангидрид - 200 - 300
Сернокислый цинк, гидрат - 70 - 90
Фолиевая кислота - 4 - 6
| Способ разливки металлов и сплавов в атмосфере защитного газа | 1955 |
|
SU109032A1 |
| US 5616232 A, 26.09.1995 | |||
| Экономайзер | 0 |
|
SU94A1 |
| Теплообменная труба | 1974 |
|
SU566121A1 |
| EP 0607452 A1, 27.07.1994 | |||
| Способ лечения больных ограниченным нейродермитом | 1977 |
|
SU643157A1 |
| ЭЛЕКТРОЛИТ ДЛЯ НАНЕСЕНИЯ КОРРОЗИОННОСТОЙКИХ ПОКРЫТИЙ СПЛАВОМ ХРОМ - ЦИНК | 1996 |
|
RU2103423C1 |
Авторы
Даты
2000-06-27—Публикация
1998-02-03—Подача