Изобретение относится к синтезу кислородсодержащих продуктов из метана, конкретнее, к двухстадийному процессу, на первой стадии которого окислительной каталитической димеризацией метана синтезируют этилен, после чего полученный этилен окисляют на втором реакторе, где образуется окись этилена, легко выделяемая из газовой смеси, например, методом абсорбции.
Известные способы синтеза этилена окислительной димеризацией метана [Мхитарова Д. А. , Потемкина Э.Д., Шепелева Е.А., Ахапкина О.В. Прогностическое исследование в области технологии одностадийного превращения метансодержащего сырья. Москва, ЦНИИТЭнефтехим, 1990. - 109 с.] характеризуются общим недостатком - низкой (1,0-3,0 об.%) концентрацией этилена в реакционных газах, что значительно увеличивает затраты на выделение конечного продукта - этилена.
Наиболее близким к предлагаемому изобретению является способ олигомеризации метана в высшие углеводороды, осуществляемый по двухреакторной схеме: в первом реакторе осуществляется сочетание метана в этилен, во втором этилен на катализаторе цеолите типа ZSM превращается в бензиновую фракцию углеводородов C5-C8 [патент USA N 4849571, МКИ C 07 C 2/04 - 18.07.1989.] (прототип). Но используемые в этом способе катализаторы обладают низкой селективностью. При использовании известного способа, помимо этана и этилена, образуются в заметных количествах C3-C4-углеводороды, присутствие которых в реакторе синтеза этиленоксида нежелательно из-за зауглероживания катализатора и снижения выхода окиси этилена. Кроме того, специфика современных химических производств переработки этилена такова, что только для ограниченного круга синтезов требуется этилен высокой чистоты, например, для производства полимеров. Для других производств в исходный этилен, согласно технологии, целесообразно вводить различные компоненты для дальнейшего синтеза.
Цель изобретения - улучшение существующих способов переработки метана и увеличение продуктивности процесса синтеза окиси этилена.
Указанная цель достигается использованием двухстадийного синтеза этиленоксида, в котором на стадии окислительной димеризации метана исключена фаза выделение этилена из реакционных газов. На первой стадии используется новый катализатор на основе диоксида олова, промотированный оксидами щелочных или щелочноземельных металлов состава x Me2O•(1 - x)SnO2 или xMeO•(1 - x)SnO2, где Me - Li, Na или Ca; x = 0,05 - 0,15. Синтез этилена из метана проводят в проточном режиме при атмосферном давлении при температуре 760 - 820oC и времени контакта 0,5 - 1 с. Содержание метана, кислорода и азота в исходной смеси задают 38-65 об. %, 12-20 об.% и 20-50 об.% соответственно. К смеси газов добавляется дихлорэтан в количестве 12 ppm. Введение малых количеств хлорорганики способствует росту селективности по целевым продуктам как при окислительной димеризации метана, так и в синтезе этиленоксида [патент Франции N 1113310 - 28.03.1956; S. Ahmed et all. Promotion by I Tetrachlormethane of the Oxidative Coupling of Methane on Silica-Supported Alkaline Earth Oxides //J. Catal., 1990, 121, N 2. - p. 408-421].
Проведение реакции предложенным способом позволяет на первой стадии получать смесь реакционных газов с концентрацией этилена 2,75 - 8,0 об.%. Реакционные газы, полученные на первой стадии синтеза, осушают и корректируют кислородом до соотношения C2H4:O2 = 1:1,2-3,5. Затем газы направляют в реактор второй стадии, где при использовании катализаторов состава 30% Ag/α-Al2O3 или 30% Ag/α-Al2O3 с добавкой 5 мас.% BaO получают окись этилена. Процесс проводят при температуре 245 - 290oC и времени контакта τ = 1,5 - 4 с. Конверсия этилена при этом составляет 60 - 98%, селективность образования окиси этилена 45 - 77%, что превышает известные аналоги.
Предложенный способ реализован в лабораторных условиях.
Катализаторы для первой стадии синтеза приготавливали введением в водную эмульсию Sn(OH)2 расчетных количеств гидрооксидов щелочных или щелочноземельных металлов. Эмульсию гидрооксидов металлов упаривали при перемешивании, затем сушили в течение 2 часов при T = 200oC, после чего прокаливали в течение 10 часов при T = 900oC. Катализаторы для второй стадии приготавливали пропиткой α-Al2O3 азотно-кислыми солями серебра и бария с последующей прокалкой в течение 10 часов при 550oC.
Проведение процесса предлагаемым способом обеспечивает выход кислородсодержащих продуктов до 6,5 - 11,2% мольных в расчете на пропущенный метан и позволяет получить легко выделяемый абсорбцией из газовой фазы целевой продукт - оксид этилена. Анализ исходной смеси и продуктов реакции проводился хроматографически. Предлагаемые катализаторы характеризуются высокой стабильностью. Сущность изобретения иллюстрируется примерами.
Пример 1. Первая стадия: в трубчатый алундовый реакторе внутренним диаметром 6,5 см помещают 0,5 см3 катализатора состава 0,05 Li2O•0,95 SnO2. Реакционную смесь состава 43,0 об.% CH4; 15,0 об.% O2; 42,0 об.% N2 с добавкой дихлорэтана в количестве 12 ppm пропускают через катализатор при температуре 780oC и времени контакта τ = 1,0 с. Вторая стадия: газовую этиленсодержащую смесь, выходящую из первого реактора с концентрацией этилена 3.4 об.%, осушают конденсацией водяных паров, корректируют добавлением кислорода до соотношения C2H4: O2 = 1:3,5 и направляют в трубчатый кварцевый реактор диаметром 0,8 см, где находится 1,5 см3 катализатора состава 30% Ag/α-Al2O3, при температуре 280oC. Конверсия этилена составляет 91,8%, выход оксида этилена - 6,6% мольных.
Пример 2 аналогичен примеру 1, но состав катализатора первой стадии изменен на 0,05 CaO•0,95 SnO2, температура реакции составляет 780oC, время контакта τ = 0,5 с. Реакционная смесь состава (об.%) 50,0 CH4; 12,0 O2; 38,0 N2. Температура во втором реакторе 260oC, соотношение C2H4:O2 = 1:1,8.
Пример 3 аналогичен примеру 1, но состав катализатора 0,1 Li2O•0,9 SnO2, температура 800oC, τ = 1,0 с. Используется реакционная смесь состава (об.%) 60,0 CH4; 18,0 O2; 22,0 N2. Соотношение C2H4:O2 = 1:1,7 перед входом во второй реактор, температура 270oC, объем катализатора 30% Ag/α-Al2O3 - 1,2 см3.
Пример 4 аналогичен примеру 3, но состав катализатора первой стадии 0,15 Li2O•0,85 SnO2, температура реакции 800oC, τ = 0,7 с. Используется реакционная смесь состава (об.%) 60,0 CH4; 20,0 O2; 20,0 N2.
Пример 5 аналогичен примеру 3, но состав катализатора первой стадии 0,1 Na2O•0,9 SnO2, температура реакции 760oC, τ = 1,0 с. Используется реакционная смесь состава (об.%) 65,0 CH4; 15,0 O2; 20,0 N2. Объем катализатора 30% Ag/α-Al2O3 во втором реакторе составляет 1,1 см3, соотношение C2H4:O2 = 1: 2,0, температура 275oC.
Пример 6 аналогичен примеру 3, используется реакционная смесь состава (об. %) 60,0 CH4; 18,0 O2; 22,0 N2, состав катализатора 0,1 CaO•0,9 SnO2, температура реакции 820oC, τ = 1,0 с. Температура в реакторе окисления этилена 280oC, соотношение C2H4:O2 = 1:1,5.
Пример 7 аналогичен примеру 5, но на первой стадии используется катализатор состава 0,15 Na2O•0,85 SnO2, подается смесь состава (об.%) 40,0 CH4; 12,5 O2; 47,5 N2, температура реакции 800oC, τ = 1.0 с. Соотношение C2H4:O2 = 1:1,6 перед входом во второй реактор, температура 276oC, а в качестве катализатора использован 5% BaO - 30% Ag/α-Al2O3 в количестве 1,2 см3.
Пример 8 аналогичен примеру 7, но использован катализатор состава 0,15 CaO•0,85 SnO2, температура реакции 760oC и τ = 1,0 с. Используется смесь состава (об.%) 38,0 CH4; 14,0 O2; 48,0 N2.
Пример 9. Используется катализатор, аналогичный примеру 3, но температура 760oC, τ = 1,0 с, используется смесь состава (об.%) 38,0 CH4; 12,0 O2; 50,0 N2. Соотношение C2H4:O2 = 1:3,5, температура в реакторе второй стадии 245oC, объем катализатора 5% BaO - 30% Ag/α-Al2O3 - 2,3 см3.
Пример 10 аналогичен примеру 5, используется состав катализатора той же формулы, но температура 780oC, контактируется смесь состава (об.%) 43,0 CH4; 13,0 O2; 44,0 N2. Соотношение C2H4:O2 = 1:1,8, объем катализатора 5% BaO - 30% Ag/α-Al2O3 - 1,2 см3, температура в реакторе второй стадии 290oC.
Пример 11 аналогичен примеру 8, используется состав катализатора той же формулы, но температура 800oC, контактируется смесь состава (об.%) 54,0 CH4; 16,0 O2; 30,0 N2, время контакта τ = 0,5 с. Температура во втором реакторе 290oC, в качестве катализатора использован 5% BaO - 30% Ag/αAl2O3 в количестве 1,2 см3, соотношение C2H4:O2 = 1:1,2.
Пример 12 аналогичен примеру 9, используется состав катализатора той же формулы, но температура в первом реакторе 740oC, время контакта τ = 1,0 с.
Пример 13 аналогичен примеру 9, используется состав катализатора той же формулы, но температура в первом реакторе 760oC, время контакта τ = 0,25 с.
Пример 14 аналогичен примеру 9, используется состав катализатора той же формулы, температура в первом реакторе составляет 760oC, время контакта τ = 1,0 с, контактирует смесь того же состава (38,0 CH4; 12,0 O2; 50,0 N2), но температура во втором реакторе 310oC.
Пример 15 аналогичен примеру 14, но температура в реакторе второй стадии 205oC.
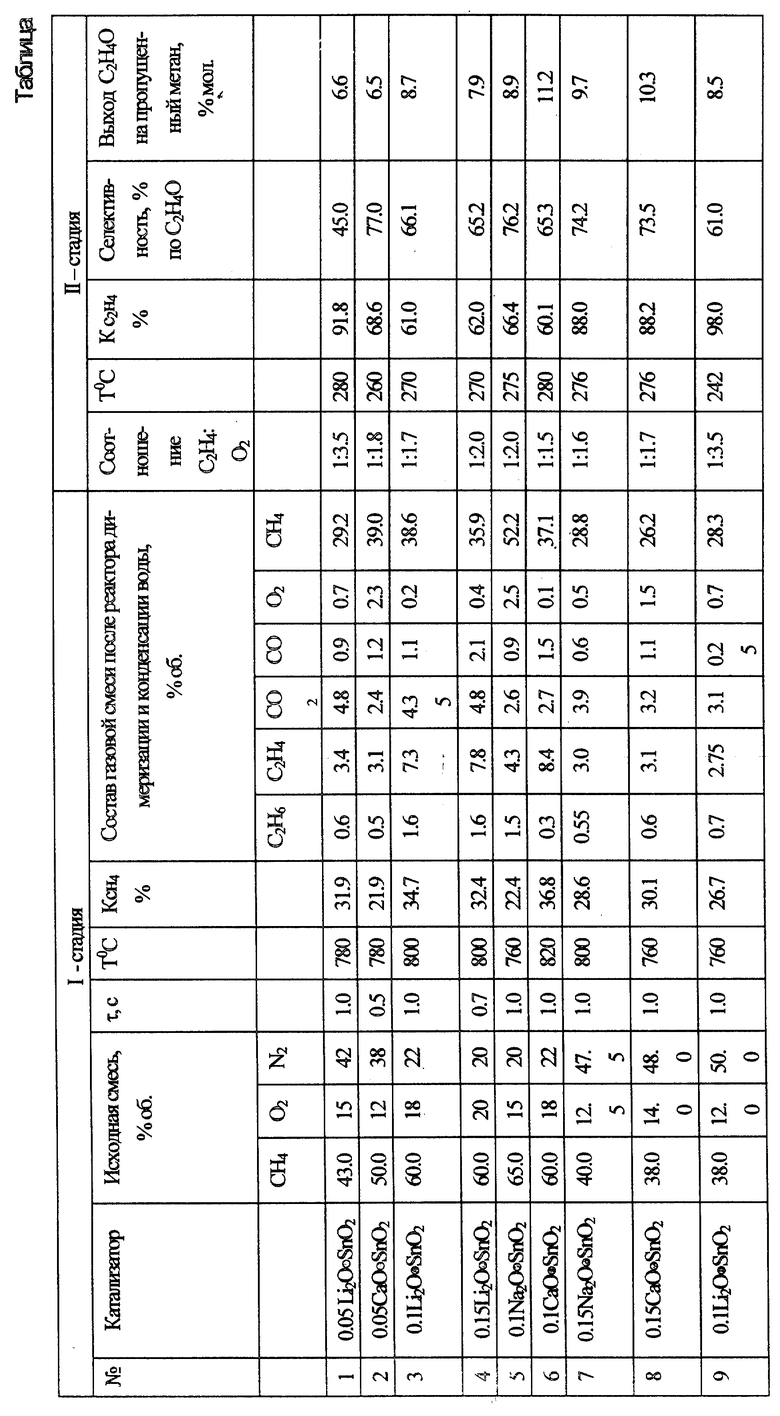
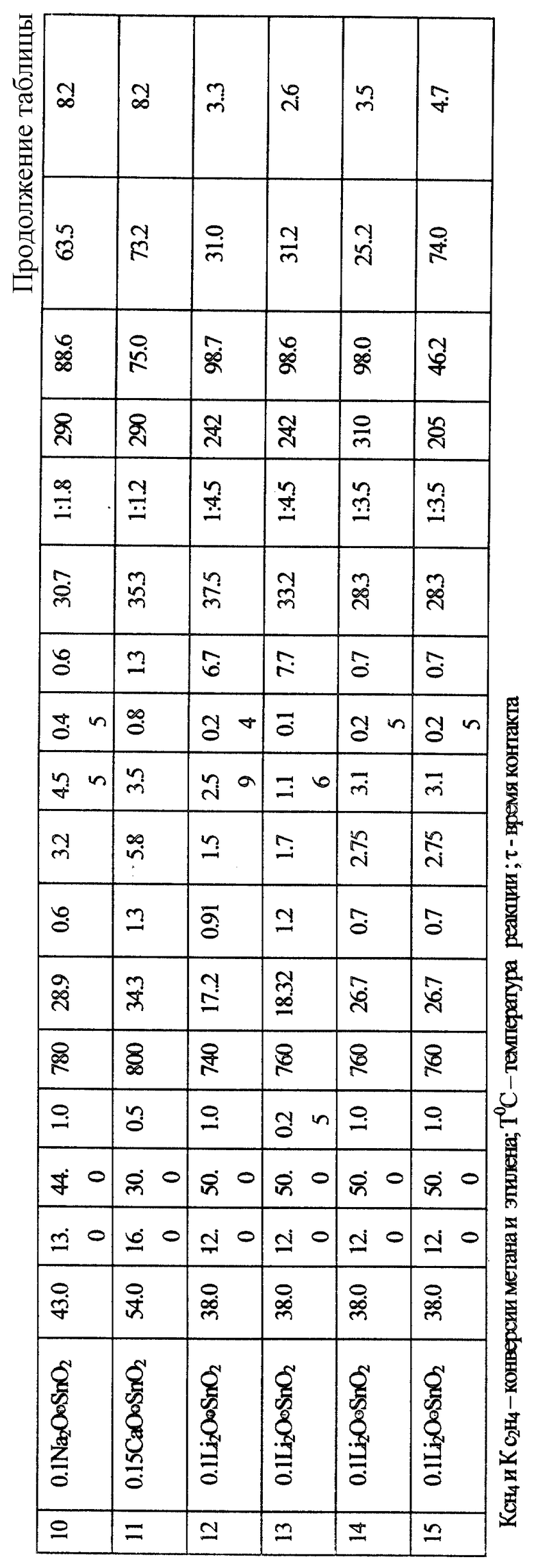
Количественные данные по примерам реализации предлагаемого способа N 1-15 приведены в таблице. Режимы заявляемого способа определены по оптимальному выходу конечного продукта на пропущенный метан, превышающему известные аналоги.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ЭТИЛЕНА | 1994 |
|
RU2065429C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭТИЛЕНА | 2013 |
|
RU2528829C1 |
| СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРА НА ОСНОВЕ CeO-SnО НА СТЕКЛОТКАННОМ НОСИТЕЛЕ | 2014 |
|
RU2554943C1 |
| СПОСОБ ГЛУБОКОГО ОКИСЛЕНИЯ МЕТАНА | 2010 |
|
RU2440926C1 |
| СПОСОБ ХИМИЧЕСКОЙ ПЕРЕРАБОТКИ МЕТАНА | 2000 |
|
RU2172731C1 |
| ИНТЕГРАЦИЯ ОКИСЛИТЕЛЬНОГО СОЧЕТАНИЯ В МЕТАНОВЫЕ УСТАНОВКИ | 2018 |
|
RU2764097C2 |
| СПОСОБ ПОЛУЧЕНИЯ C-УГЛЕВОДОРОДОВ | 1992 |
|
RU2008303C1 |
| СПОСОБ ПРЕВРАЩЕНИЯ МЕТАНА В ЭТИЛЕН И ЭТАН В ПРОЦЕССЕ ЕГО ОКИСЛИТЕЛЬНОГО ПРЕВРАЩЕНИЯ С ИСПОЛЬЗОВАНИЕМ ФТАЛОЦИАНИНОВЫХ КОМПЛЕКСОВ В КАЧЕСТВЕ ВЫСОКОЭФФЕКТИВНЫХ КАТАЛИЗАТОРОВ | 2008 |
|
RU2412143C2 |
| СПОСОБ СИНТЕЗА АЦЕТОНИТРИЛА | 2000 |
|
RU2214396C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЭТИЛЕНА | 2001 |
|
RU2224734C2 |
Описывается способ получения окиси этилена из метана, при котором смесь метана и кислорода разбавляют азотом, добавляют хлорорганическое соединение, проводят реакцию димеризации метана в присутствии катализатора, после чего проводят каталитическую реакцию окисления этилена и выделяют из полученной смеси окись этилена. Способ отличается тем, что исходную смесь выбирают из соотношения: 38-65 об. % метана, 12-20 об. % кислорода и 20-50 об. % азота, в качестве катализатора на стадии димеризации используют состав х Ме2O•(1-х)SnO2 или х МеO•(1-х)SnO2, где Ме - Li, Na или Са, х = 0,05 - 0,15, реакцию проводят при температуре 760 - 820oС и времени контакта 0,5-1,0 с, после чего, минуя стадию газоразделения, корректируют соотношение этилен : кислород в реакционных газах кислородом до величины 1 : 1,2-3,5 и проводят вторую стадию на катализаторе состава 30% Ag/α-Al2O3 или 5% ВаO-30% Ag/α-Al2O3 при температуре реакции 245-290oС. Технический результат - улучшение известных способов переработки метана и увеличение продуктивности процесса синтеза окиси этилена. 2 з.п. ф-лы, 1 табл.
| US 4849571 A, 18.07.1989 | |||
| GB 1545840 A, 16.05.1979 | |||
| СПОСОБ ПОЛУЧЕНИЯ ОКСИДА ЭТИЛЕНА | 1992 |
|
RU2054424C1 |
Авторы
Даты
2000-09-20—Публикация
1999-08-09—Подача