Настоящее изобретение включает соединение формулы I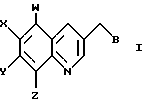
где W, X, Y и Z независимо представляют собой водород, галоген, NO2, NH2 -О-алкил с прямым или разветвленным C1-C6; В представляет собой хлор, бром или четвертичный галогенид аммония, или В может представлять собой -О-алкил с прямым или разветвленным C1-C6, при условии, что W, X, Y не являются водородом, и Z не является ОН или -О-алкилом; Z может представлять собой ОН, при условии, что W, X, Y не являются водородом, и В не является -O- алкилом; а также способ получения соединения формулы I
где W, X, Y и Z независимо представляют собой водород, галоген, NO2, NH2, ОН или -О-алкил с прямым или разветвленным C1-C6, который предусматривает взаимодействие соединения формулы II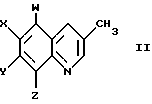
где W, X, Y и Z независимо представляют собой водород, галоген, NО2 или -О-алкил с прямым или разветвленным C1-C6, с радикальным галогенирующим агентом, где галоген представляет собой бром или хлор, получая соединение формулы III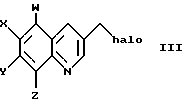
взаимодействие соединения III с третичным амином, получая соединение формулы IV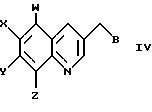
взаимодействие соединения IV с алкоксидом металла ROM, где R представляет собой прямой или разветвленный C1-C6 алкил и М представляет собой Na, Li или K, получая 3-алкоксизамещенные производные хинолина формулы I.
3-алкоксизамещенные хинолины, заявленные в настоящем изобретении, представляют собой гербицидные промежуточные соединения, используемые в синтезе замещенных полупродуктов производства хинолиновых гербицидов, которые в свою очередь являются промежуточными соединениями в синтезе гербицидного полупродукта 5-метоксиметил-2,3-пиридиндикарбоновой кислоты для получения гербицида 2-(4-изопропил-4-метил-5-оксо-2-имидазолидинил) -5-метоксиметилникотиновой кислоты из патента CША 5334576.
Изобретение дополнительно иллюстрируется примерами, которые не следует рассматривать в качестве ограничения настоящего изобретения.
ПРИМЕР 1
Получение 3-(бромметил)-8-нитрохинолина
Смесь из 3-метил-8-нитрохинолина (9,5 г, 0,05 моль) в хлорбензоле (75 мл) нагревают при перемешивании до температуры 80oC в токе азота. К реакционной смеси прибавляют смесь N- бромсукцинимида (9,0 г, 0,05 моль) и 2,2'-азобисизобутиронитрила (0,5 г, 0,003 моль) и выдерживают при температуре 80-90oC в течение 1 часа. Смесь промывают водой (100 мл) при температуре 60- 80oC, охлаждают до комнатной температуры и фильтруют. Полученный твердый остаток промывают хлорбензолом и сушат под вакуумом, получая целевое соединение в виде твердого вещества светло-желтого цвета (3,9 г, т.пл. 121-124oC), которое идентифицируют с помощью спектроскопии ЯМР на ядрах 1H и 13C.
ПРИМЕР 2
Получение бромида (8-нитро-3-хинолил)-метилтриметиламмония
Смесь из 3-метил-8-нитрохинолина (75 г, 0,40 моль) в хлорбензоле (1000 мл) нагревают при перемешивании до температуры 80oC в токе азота. К реакционной смеси прибавляют смесь N-бромсукцинимида (75 г, 0,42 моль) и 2,2'-азобисизобутиронитрила (4 г, 0,024 моль) при температуре 80-90oC в течение 30 минут. По окончании добавления реагента смесь выдерживают при температуре 80-90oC в течение 4 часов. После этого ее промывают водой (400 мл) при 60-80oC и органическую массу разбавляют ацетоном (300 мл). Полученную смесь охлаждают до 10oC и прибавляют безводный триэтиламин (49 г, 0,83 моль). Смесь оставляют до утра при перемешивании при температуре 10-30oC и фильтруют. Полученный твердый остаток промывают ацетоном и сушат под вакуумом, получая целевое соединение в виде твердого вещества светло-желтого цвета (74 г), которое идентифицируют с помощью спектроскопии ЯМР на ядрах 1H и 13C.
ПРИМЕР 3
Получение 3-(метоксиметил)-8-нитрохинолина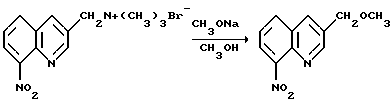
Смесь из 25%-ного метоксида натрия (88 г, 0,19 моль) в метаноле (600 мл) и бромида (8-нитро-3-хинолил)- метилтриметиламмония (63 г, 0,19 моль) нагревают в токе азота при температуре перегонки в течение 2 часов, а затем охлаждают до комнатной температуры. Полученную смесь разбавляют смесью воды со льдом (600 мл) и фильтруют. Полученный твердый остаток промывают водой и сушат под вакуумом, получая целевое соединение в виде твердого вещества беловатого цвета (32,2 г, т.пл. 69-71oC), которое идентифицируют с помощью спектроскопии ЯМР на ядрах 1H и 13C.
ПРИМЕР 4
Получение 3-(метоксиметил)-8-аминохинолина
Смесь из 3-(метоксиметил)-8-нитрохинопина (5,64 г, 0,026 моль), 5% палладия на углероде Pd/C (0,32 г) и метанола (70 мл) нагревают в автоклаве до 45oC. Смесь обрабатывают водородом, находящимся под давлением около 2,1 кг/см2 (30 фунт/кв. дюйм), в течение 4 часов при 45oC и затем охлаждают до комнатной температуры.
Смесь фильтруют для удаления Pd/C и осадок промывают метанолом. Фильтрат и промывную воду объединяют и концентрируют в вакууме с получением целевого продукта в виде прозрачной жидкости (4,7 г), которую идентифицируют с помощью спектроскопии ЯМР на ядрах 1H и 13C.
ПРИМЕР 5
Получение 3-(бромметил)-8-хлорхинолина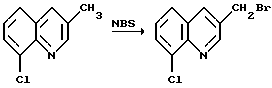
Смесь из 3-метил-8-хлорхинолина (9 г, 0,05 моль) в хлорбензоле (75 мл) нагревают при перемешивании до 80oC в токе азота. К полученной реакционной смеси прибавляют смесь N-бромсукцинимида (9 г, 0,05 моль) и 2,2'-азобисизобутиронитрила (0,5 г, 0,003 моль) и выдерживают при температуре 80-90oC в течение 1 часа. Смесь дважды промывают водой (50 мл) при 60-80oC, охлаждают до комнатной температуры, разбавляют гептаном (75 мл) и фильтруют, получая твердый остаток, который промывают сначала хлорбензолом, а затем гептаном. Остаток сушат в вакууме и получают целевое соединение в виде твердого вещества беловатого цвета (6,2 г, т.пл. 125-129oC), которое идентифицируют с помощью спектроскопии ЯМР на ядрах 1H и 13C.
ПРИМЕР 6
Получение бромида (8-хлор-3-хинолил)-метилтриметиламмония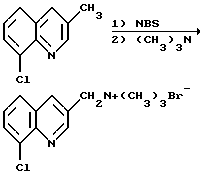
Смесь из 3-метил-8-хлорхинолина (71,2 г, 0,4 моль) в хлорбензоле (700 мл) нагревают при перемешивании до температуры 80oC в токе азота. К реакционной смеси прибавляют смесь N- бромсукцинимида (71,2 г, 0,4 моль) и 2,2'-азобисизобутиронитрила (4 г, 0,024 моль) при температуре 80-90oC в течение 30 минут. По окончании добавления реагента смесь выдерживают при температуре 80-90oC в течение 1,5 часов. После этого ее дважды промывают водой (300 мл) при 60-80oC и органическую массу разбавляют ацетоном (250 мл). Полученную смесь охлаждают до 10oC и прибавляют безводный триэтиламин (29,5 г, 0,5 моль). Смесь перемешивают при температуре 10-30oC и фильтруют. Полученный твердый остаток промывают ацетоном и сушат под вакуумом, получая целевое соединение в виде твердого вещества нестандартного белого цвета (69,4 г), которое идентифицируют с помощью спектроскопии ЯМР на ядрах 1H и 13C.
ПРИМЕР 7
Получение 3-(метоксиметил)-8-хлорхинолина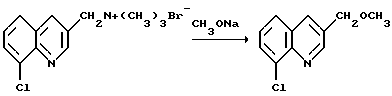
Смесь из 25%-ного метоксида натрия (66 г, 0,3 моль) в метаноле (600 мл) и бромида (8-хлор-3-хинолил)- метилтриметиламмония (66 г, 0,21 моль) нагревают в токе азота при температуре перегонки в течение 3 часов, а затем охлаждают до комнатной температуры. Полученную смесь разбавляют смесью воды со льдом (500 мл) и фильтруют. Полученный твердый остаток промывают водой и дважды экстрагируют метиленхлоридом. Экстракты объединяют, промывают водой и концентрируют в вакууме, получая целевое соединение в виде прозрачной жидкости (39,4 г), которое идентифицируют с помощью спектроскопии ЯМР на ядрах 1H и 13C.
ПРИМЕР 8
Получение 3-(метоксиметил)-5-нитро-8-хлорхинолина
3-(метоксиметил)-8-хлорхинолин (10,3 г, 0,05 моль) прибавляют к 96%-ной серной кислоте (40 г, 0,39 моль) при 10-30oC, а затем в течение 15 минут к смеси прибавляют 70%-ную азотную кислоту. Реакционную смесь перемешивают при комнатной температуре в течение 14 часов, разбавляют смесью воды со льдом (150 мл) и фильтруют. Полученный твердый остаток промывают водой и сушат под вакуумом, получая целевое соединение в виде твердого вещества желтого цвета (9,4 г, т.пл. 83-86oC), которое идентифицируют с помощью спектроскопии ЯМР на ядрах 1H и 13C.
ПРИМЕР 9
Получение бромида (7,8-дихлор-3-хинолил)-метилтриметиламмония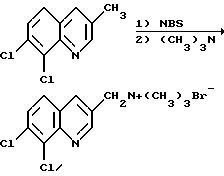
Смесь из 3-метил-7,8-дихлорхинолина (106 г, 0,5 моль) в хлорбензоле (1000 мл) нагревают при перемешивании до температуры 80oC в токе азота. К реакционной смеси прибавляют смесь N-бромсукцинимида (89 г, 0,5 моль) и 2,2'-азобисизобутиронитрила (3 г, 0,02 моль) при температуре 80-90oC в течение 30 минут. По окончании добавления реагента смесь выдерживают при температуре 80-90oC в течение 2 часов. После этого ее промывают водой (400 мл) при 60-80oC и органическую массу разбавляют ацетоном (300 мл). Полученную смесь охлаждают до 10oC и прибавляют безводный триэтиламин (49 г, 0,83 моль). Смесь оставляют до утра при перемешивании при температуре 10-30oC и фильтруют. Полученный твердый остаток промывают ацетоном и сушат под вакуумом, получая целевое соединение в виде твердого вещества белого цвета (129 г), которое идентифицируют с помощью спектроскопии ЯМР на ядрах 1H и 13C.
ПРИМЕР 10
Получение 3-(метоксиметил)-7,8-дихлорхинолина
Смесь из 25%-ного метоксида натрия (100 г, 0,46 моль) в метаноле (800 мл) и бромида (7,8-дихлор-3-хинолил)- метилтриметиламмония (110 г, 0,31 моль) нагревают в токе азота при температуре перегонки в течение 2 часов, а затем охлаждают до комнатной температуры. Полученную смесь разбавляют смесью воды со льдом (800 мл) и фильтруют. Полученный твердый остаток промывают водой и сушат в вакууме, получая целевое соединение в виде твердого вещества нестандартного белого цвета (64,30 г), которое идентифицируют с помощью спектроскопии ЯМР на ядрах 1H и 13C.
ПРИМЕР 11
Получение бромида (5,8-дихлор-3-хинолил)-метилтриметиламмония
Смесь из 3-метил-5,8-дихлорхинолина (143 г, 0,67 моль) в хлорбензоле (1000 мл) нагревают при перемешивании до температуры 80oC в токе азота. К реакционной смеси прибавляют смесь N-бромсукцинимида (120 г, 0,67 моль) и 2,2'-азобисизобутиронитрила (5 г, 0,03 моль) при температуре 80-90oC в течение 30 минут. По окончании добавления реагента смесь выдерживают при температуре 80-90oC в течение 3 часов. После этого смесь промывают водой (600 мл) при 60-80oC, и органическую массу разбавляют ацетоном (200 мл) Полученную смесь охлаждают до 10oC и прибавляют безводный триэтиламин (65 г, 1,1 моль). Смесь оставляют до утра при перемешивании при температуре 10-30oC и фильтруют. Полученный твердый остаток промывают ацетоном и сушат под вакуумом, получая целевое соединение в виде твердого вещества белого цвета (174,6 г), которое идентифицируют с помощью спектроскопии ЯМР на ядрах 1H и 13C.
ПРИМЕР 12
Получение 3-(метоксиметил)-5,8-дихлорхинолина
Смесь из 25%-ного метоксида натрия (130 г, 0,6 моль) в метаноле (800 мл) и бромида (5,8-дихлор-3-хинолил)- метилтриметиламмония (146 г, 0,41 моль) нагревают в токе азота при температуре перегонки в течение 2 часов, а затем охлаждают до комнатной температуры. Полученную смесь разбавляют смесью воды со льдом (1200 мл) и фильтруют. Полученный твердый остаток промывают водой и сушат в вакууме, получая целевое соединение в виде твердого вещества светло-коричневого цвета (91 г), которое идентифицируют с помощью спектроскопии ЯМР на ядрах 1H и 13C.
ПРИМЕР 13
Получение бромида (8-хлор-3-хинолил)-метилтриметиламмония с помощью 1,3-дибром-5,5-диметилгидантоина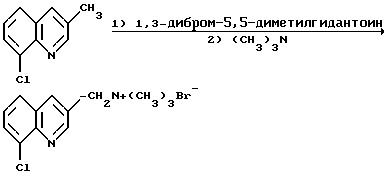
Смесь из 3-метил-8-хлорхинолина (71,2 г, 0,4 моль) в хлорбензоле (700 мл) нагревают при перемешивании до температуры 80oC в токе азота. К реакционной смеси прибавляют смесь 1,3- дибром-5,5-диметилгидантоина (57 г, 0,02 моль) и 2,2'-азобисизобутиронитрила (4 г, 0,024 моль) при температуре 80-90oC в течение 30 минут. По окончании добавления реагента смесь выдерживают при температуре 80-90oC в течение 1,5 часов. После этого ее дважды промывают водой (300 мл) при 60-80oC и органическую массу разбавляют ацетоном (250 мл). Полученную смесь охлаждают до 10oC и прибавляют безводный триэтиламин (36 г, 0,6 моль). Смесь перемешивают при температуре 10-30oC в течение 3 часов и фильтруют. Полученный твердый остаток промывают ацетоном и сушат под вакуумом, получая целевое соединение в виде твердого вещества нестандартного белого цвета (34,1 г), которое идентифицируют с помощью спектроскопии ЯМР на ядрах 1H и 13C.
Изобретение включает гербицидные 3-замещенные промежуточные хинолины общей формулы I, где W, X, Y, Z и B имеют указанные в формуле изобретения значения, и способ получения 3-алкоксиметилзамещенных хинолинов, являющихся полупродуктами для производства гербицидов. 2 с. и 9 з.п. ф-лы. 

где W, X, Y и Z независимо представляют собой водород, галоген, NO2, NH2 или -O-алкил с прямым или разветвленным С1-С6;
В представляет собой хлор, бром или четвертичный галогенид аммония или В представляет собой -O-алкил с прямым или разветвленным С1-С6, при условии, что W, X, Y не являются водородом, и Z не является ОН или -O-алкилом, или Z представляет собой ОН, при условии, что W, X, Y не являются водородом и В не является -O-алкилом.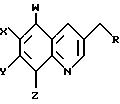
где W, X, Y и Z независимо представляют собой водород, галоген, NO2, NH2, OH или -O-алкил с прямым или разветвленным С1-С6;
R представляет собой -O-алкил с прямым или разветвленным С1-С6,
который включает следующие стадии: взаимодействие соединения формулы II
где W, X, Y и Z независимо представляют собой водород, галоген, NO2 или -O-алкил с прямым или разветвленным С1-С6,
с радикальным галогенирующим агентом, где галоген представляет собой бром или хлор, получая соединение формулы III
взаимодействие соединения III с третичным амином, получая соединение формулы IV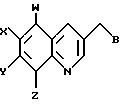
где В представляет собой третичный галогенид аммония;
и взаимодействие соединения IV с алкоксидом металла ROM,
где R представляет собой прямой или разветвленный С1-С6 алкил;
М представляет собой Na, Li или К,
с получением соединения формулы I.
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ХЛОРМЕТИЛХИНОЛИНА | 1987 |
|
RU2012560C1 |
| Домовый номерной фонарь, служащий одновременно для указания названия улицы и номера дома и для освещения прилежащего участка улицы | 1917 |
|
SU93A1 |
| Способ автоматического управления процессом гипохлоритной отбелки целлюлозы | 1976 |
|
SU675111A1 |
Авторы
Даты
2001-01-10—Публикация
1996-06-04—Подача