Изобретение относится к фармацевтической химии и представляет собой способ очистки и выделения 2'-дезокси-2',2,'-дифторнуклеозидов.
Предпосылки создания изобретения
Постоянный интерес к синтезу 2'-дезоксинуклеозидов и их аналогам отражается в их удачном использовании в качестве терапевтических средств при лечении вирусных заболеваний и злокачественных опухолей. Определяющей стадией в общем синтезе 2'-дезоксинуклеозидов является очистка и выделение целевой бета-аномерной формы нуклеозида, поскольку синтез 2'-дезоксинуклеозидов обычно не является стереоспецифическим и приводит к образованию смеси альфа- и бета-нуклеозидов.
Vorbruggn, et al., J. Org. Chem., 41, 2084 (1976), М. Hofer, Chem. Ber, 93, 2777 (I960), Walker, et al., Nucleic Acid Research, 12, 6827 (1984), R. P. Nodge, et al. , J. Org. Chem., 56, 1553 (1991), Tann, et al., J. Org. Chem., 50, 3644 (1985), Howell, et al., J. Org. Chem., 53, 85 (1988) и патент США 4965374, Chou, et al., все описывают различные синтезы смеси альфа- и бета-аномерных дезоксинуклеозилов.
Несмотря на успехи, достигнутые на стадии переработки в синтезе нуклеозидов, остается потребность в способе, способном эффективно очищать и выделять обогащенные бета-аномером 2'-дезокси-2',2'-дифторнуклеозиды с повышенным выходом, где дифторнуклеозиды были синтезированы в отсутствие катализатора.
В соответствии с этим цель данного изобретения состоит в разработке способа эффективной очистки и выделения обогащенных бета-аномером 2'-дезокси-2',2'-дифторнуклеозидов.
Другие цели и преимущества данного изобретения станут очевидными из последующего описания.
Описание изобретения
Данное изобретение представляет собой способ очистки и выделения обогащенных бета-аномером нуклеозидов, содержащий
a) предоставление смеси, содержащей R'' и обогащенный бета- аномером нуклеозид формулы
где каждый X независимо выбирают из гидроксизащитных групп, и R' представляет нуклеиновое основание формулы
где W представляет аминозащитную группу; и
R'' представляет нуклеиновое основание формулы
где W' представляет аминозащитную группу или водород;
в высококипящем растворителе;
b) разбавление смеси органическим растворителем, выбранным из группы, состоящей из простых эфиров, сложных эфиров и нитрилов;
c) добавление разбавленной реакционной смеси в водную кислоту; и
d) выдерживание полученной таким образом кислотной смеси при температуре от 70oC до 100oC до тех пор, пока не осадится продукт формулы IB, где W представляет теперь W'.
Наилучший способ осуществления изобретения
На всем протяжении этого документа все температуры приводятся в градусах Цельсия, все отношения, проценты и подобные приводятся в массовых долях, а отдельные соединения и все смеси приводятся в объемных единицах, за исключением случаев, где указано иначе. Аномерные смеси выражают как отношение масса/масса или в виде процента. Термин "алкил", один или в комбинации, относится к алифатическим углеводородным группам с нормальной, циклической и разветвленной цепью, которые предпочтительно содержат вплоть до 7 атомов углерода, например, метильной, этильной, н-пропильной, изопропильной, н-бутильной, трет-бутильной, н-пентильной, н-гексильной, 3-метилпентильной группам и подобным или замещенным алифатическим углеводородам с нормальной, циклической и разветвленной цепью, например, хлорэтилу, 1,2-дихлорэтилу и тому подобным. Термин "замещенный", один или в комбинации, относится к замещению одной или несколькими группами, выбранными из циано, галогена, карбоалкокси, толуоила, нитро, алкокси, алкила и диалкиламино. Фраза "обогащенный аномером", одна или в комбинации, относится к аномерной смеси, где отношение конкретного аномера выше чем 1:1, и включает практически чистый аномер.
Гидроксизащитные группы (X) относятся к гидроксизащитным группам, известным в данной области, как описано в главе 3 Protective Groups in Organic Chemistry, McOmie Ed., Plenum Press, New York (1973), и в главе 2 Protective Group in Organic Synthesis, Green, John, J. Wiley and Sons, New York (1981). Предпочтительными гидроксизащитными группами являются образующие сложный эфир группы, например, формил, ацетил, замещенный ацетил, пропионил, бутинил, пивалоил, 2-хлорацетил, бензоил, замещенный бензоил, феноксикарбонил, метоксиацетил; карбонатные производные, например, феноксикарбонил, этоксикарбонил, трет-бутоксикарбонил, винилоксикарбонил, 2,2,2-трихлорэтоксикарбонил и бензилоксикарбонил; группы, образующие алкиловый простой эфир, например, бензил, дифенилметил, трифенилметил, трет-бутил, метоксиметил, тетрагидропиранил, аллил, тетрагидротиенил, 2-метоксиэтоксиметил; карбаматы, например, N-фенилкарбамат и N-имидазоилкарбамат; более предпочтительными являются бензоил, монозамещенный бензоил и дизамещенный бензоил, ацетил, пивалоил, трифенилметиловые простые эфиры, и наиболее предпочтительным является бензоил.
Аминозащитные группы (W) выбирают из группы, состоящей из групп, образующих силиламины, например, триалкилсилила, включая триметилсилил; изопропилдиалкилсилила, алкил-диизопропилсилила, триизопропилсилила, 1,1,3,3-тетраизопропилдисилоксанила, трет-бутилдиалкилсилила и трет-бутилдиарилсилила; карбаматов, например, трет-бутоксикарбонила, бензилоксикарбонила, 4-метоксибензилоксикарбонила и 4-нитробензилоксикарбонила; формила, ацетила, бензоила и пиваламидо; групп, образующих простой эфир, например, метокси-метила, трет-бутила, бензила, аллила и тетрагидропиранила; предпочтительной аминозащитной группой является триметилсилил.
Первой стадией в способе заявленного изобретения является обеспечение смеси, содержащей R'', и обогащенный бета-аномером нуклеозид формулы IB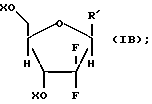
где каждый X независимо выбирают из гидроксизащитных групп, и R' представляет нуклеиновое основание формулы
где W представляет аминозащитную группу, и R'' представляет нуклеиновое основание формулы
где W' представляет аминозащитную группу или водород; в высококипящем растворителе.
Такую смесь можно получить многими различными способами. Способы синтеза такой смеси описаны в заявке на Европейский Патент N 93304817.5. Некоторыми способами (в частности, без использования катализатора; с использованием избытка R''-нуклеинового основания, с.9, EP 93304817.5; и с использованием высококипящего растворителя, с. 10, строки 13-17), описанными в Европейской заявке N 93304817.5, можно получить обогащенные бета-аномером нуклеозиды с отношением альфа- и бета-аномеров между собой, равным от более чем 1:1 до менее или равным 1:9. Для достижения таких соотношений необходимо использовать большой избыток R'' продукта, который отделяют от целевого продукта заявленным способом.
Высококипящий растворитель представляет растворитель, который имеет точку кипения выше 70oC. Высококипящий растворитель является умеренно полярным, стабильным в кислой среде и имеет ненуклеофильный характер. Типичные высококипящие растворители включают ароматические галогеналкил-, алкокси- и галогензамещенные ароматические растворители и их смеси. К предпочтительным высококипящим растворителям относятся 1,2-дихлорэтан, 1,1,2-трихлорэтан, глим, диглим, толуол, ксилолы, анизол, дихлорбромметан, хлорбензол, дибромхлорметан, трибромметан, дибромметан, ацетонитрил, пропионитрил, диоксан и их смеси, тогда как более предпочтителен анизол.
Как только получают смесь, содержащую R'' и описанный обогащенный бета-аномером нуклеозид, заявленный способ идет по следующему пути. Сначала реакционную смесь разбавляют органическим растворителем с точкой кипения выше 60oC. Приемлемые растворители относятся к классам простых эфиров, сложных эфиров и нитрилов; предпочтительными примерами их являются ацетонитрил, этилацетат и тетрагидрофуран. Разбавление проводят при повышенной температуре, которая может быть температурой реакции. Органический растворитель нужно нагревать до повышенной температуры, кроме того, температура как реакционной смеси, так и растворителя должна быть в диапазоне от 70oC до 110oC. Наиболее предпочтительным растворителем является ацетонитрил.
Количество добавленного органического растворителя находится в диапазоне от 1 мл до 5 мл на 1 грамм используемого R'' (защищенный или незащищенный цитозин). После разбавления реакционной смеси не требуется особого периода выдерживания; разбавленную смесь можно сразу вводить в следующую стадию. Разбавленную реакционную смесь добавляют в большое количество водной кислоты при повышенной температуре. Назначением водной кислоты является растворение избытка R'' (защищенный или незащищенный цитозин), который использовали в реакции гликозилирования, описанной на странице 9 описания к EP N 93304817.5. Следовательно, количество и величина кислотности водной кислоты зависит от избыточного количества R'' (защищенный или незащищенный цитозин), используемого в самой реакции. Кроме того, количество водной кислоты зависит также от выбора кислотного вещества, используемого при получении водной кислоты.
Наиболее предпочтительной кислотой является соляная кислота, используемая в концентрации от 1 н. до 6 н., наиболее предпочтительно при 4 н. При использовании такой кислоты и 5-20- кратного избытка R'' (защищенного или незащищенного цитозина), объем водной соляной кислоты составляет от 3 мл до 5 мл на 1 грамм используемого R'' (защищенного или незащищенного цитозина).
Тем не менее, возможно предпочтительное использование других водных минеральных кислот и условий реакции. Например, при необходимости оператор использует такие минеральные кислоты, как серная, сернистая, фосфорная, азотная и фосфоновая кислоты. Концентрацию кислоты меняют в довольно широких пределах, приблизительно в обратной пропорции по отношению к приемлемому объему из общей стадии выделения. Как правило, используют водную кислоту с концентрацией от 1 н. до 10%. Объем ее определяют методом оптимизации эксперимента с целью определения количества индивидуальной кислоты в реакционной смеси. Необходимые эксперименты просты; от оператора требуется проведение только последовательной корректировки концентрации кислоты и ее объема относительно используемой конкретной реакционной смеси и слежения за растворимостью продукта R'' (защищенного или незащищенного цитозина) в каждом случае.
Водная кислота не должна быть горячей при ее объединении с реакционной смесью, а иметь комнатную температуру, поскольку всю смесь нагревают до температуры от 70oC до 100oC. Теплота реакции может быть достаточной для доведения смеси до такой температуры или в некоторых случаях необходимо нагреть смесь посредством наружного нагрева. В некоторых случаях теплота реакции выше 100oC, поэтому реакционную смесь охлаждают, чтобы она оставалась ниже 100oC. Это следует принимать во внимание также и потому, чтобы повышение температуры водной кислоты не приводило к преждевременному отщеплению на этой стадии защитных групп. Когда в качестве органического растворителя используют ацетонитрил, наиболее предпочтительная температура составляет от 70oC до 80oC.
Кислую смесь, образуемую в результате добавления разбавленной реакционной смеси в водную кислоту, выдерживают, предпочтительно при умеренном перемешивании, в течение некоторого времени. Физическими изменениями, которые имеют место во время этого периода выдерживания, являются растворение избытка R'' (защищенного или незащищенного цитозина) в водном кислом слое и осаждение целевого бета-нуклеозида. Осаждение селективное, и нежелательный альфа-нуклеозид остается в большей части растворенным в органическом слое. Таким образом, кислую смесь выдерживают при постоянной температуре до тех пор, пока не имеют место эти два физических изменения. Как правило, для этого достаточно от 10 минут до 1 часа.
После достаточного периода выдерживания осажденный бета-нуклеозид отделяют от двух жидких фаз фильтрацией или центрифугированием и дополнительно промывают водной кислотой. Фильтрацию или центрифугирование проводят при постоянной температуре для предотвращения осаждения из раствора растворенного в нем защищенного или незащищенного цитозина R''.
Бета-нуклеозид, выделенный и очищенный таким образом, может все же иметь присутствующую аминозащитную группу (W), или эта аминозащитная группа (W) может быть отщеплена и замещена на атом водорода. Бета-нуклеозид, выделенный и очищенный указанным выше способом, является продуктом высокой чистоты по отношению к альфа-нуклеозиду, R'' (защищенному или незащищенному цитозину) и другим примесям; кроме того, установлено, что целевой продукт получают с превосходным выходом.
Когда кислую смесь фильтруют или центрифугируют для удаления твердого продукта, органический и водный слои разделяются. Избыток продукта R'' (защищенного или незащищенного цитозина) находится в водном слое, откуда его можно удалить и рециркулировать обратно в процесс. Защищенный или незащищенный цитозин R'' можно также выделить простым охлаждением водного слоя и фильтрацией осажденного продукта R'' или путем придания водному слою щелочных свойств, охлаждения щелочного раствора и последующего фильтрования для сбора осажденного защищенного или незащищенного цитозина R''. Выделенный цитозин по описанному выше способу по обычной процедуре рециркулируют в процесс получения смеси так, как описано в EP N 93304817.5. Таким образом, заявленный способ обеспечивает экономичную рециркуляцию защищенного или незащищенного цитозина R'', что является полезным достижением заявленного способа.
Конечной фазой процесса является удаление защитных групп X и любой оставшейся W из защищенного, очищенного твердого нуклеозида формулы IB. Удалением защитных групп получают то же самое аномерное отношение незащищенного нуклеозида.
Большинство силиламинозащитных групп легко отщепляют с помощью протонного растворителя, такого как вода или спирт. Большинство силиламинозащитных групп уязвимы к отщеплению во время контактирования с минеральной кислотой. Ацильные защитные группы, например бензоил, и ациламинозащитные группы, удаляют гидролизом с помощью сильного основания при температуре от 0oC до 100oC. Сильные или умеренно сильные основания, подходящие для использования в этой реакции, имеют pKa (при 25oC) от 8,5 до 20,0. Такие основания включают гидроокиси щелочных металлов, например гидроокись натрия или калия; алкоксиды щелочных металлов, например метоксид натрия или трет-бутоксид калия; амиды щелочных металлов; амины, например диэтиламин, гидроксиламин, аммиак и подобные; и другие основания, например гидразин и подобные. Для каждой защитной группы необходимо использование по меньшей мере одного эквивалента основания.
Ацильные защитные группы можно также удалить с помощью кислых катализаторов, например метансульфокислоты, соляной кислоты, бромистоводородной кислотой, серной кислотой или кислыми ионообменными смолами. Такой гидролиз предпочтительно проводят при относительно высокой температуре, например, температуре флегмы данной смеси, однако при использовании сильных кислот процесс ведут при комнатной температуре. Следует принимать меры предосторожности, чтобы ацильные защитные группы преждевременно не отщеплялись на более ранних стадиях заявленного способа.
Удаление простых эфирных защитных групп проводят известными способами, например с помощью этантиола и хлорида алюминия.
трет-Бутилдиметилсилильная защитная группа требует для ее удаления кислых условий, например, контактирования с газообразным галогеноводородом.
Удаление защитных групп можно удобно проводить в спиртовых растворителях, особенно водных алканолах, например метаноле. Тем не менее реакцию деблокирования (удаления защитной группы) можно также проводить в любом удобном растворителе, таком как полиолы, включая этиленгликоль, простые эфиры, например тетрагидрофуран, кетоны, например ацетон и метилэтилкетон, или диметилсульфоксид.
В предпочтительном примере осуществления изобретения в реакции удаления защитной группы используют аммиак для удаления бензоильной гидроксизащитной группы при температуре 10oC. Тем не менее, предпочтительно использование в этой реакции избытка основания, хотя количество используемого избыточного основания не является критическим параметром.
Получаемый бета-обогащенный нуклеозид
или его органическую или неорганическую кислотно-аддитивную соль можно экстрагировать и/или выделить из реакционной смеси способом, описанным в Патенте США 4965374.
Следующий пример иллюстрирует характерные особенности данного изобретения и не предназначен для какого-либо ограничения его объема.
Пример 1
Получение, очистка и выделение обогащенного бета-аномером 1- (2'-деокси-2', 2'-дифтор-3',5'-ди-O-бензоил-D-рибофуранозил)-4- аминопиримидин-2-она с 22.5 эквивалентами бис-три-метилсилилцитозина
В трехгорлую колбу на 250 мл добавляют 30 г цитозина, 25 мг сульфата аммония и 150 мл гексаметилдисилазана и смесь нагревают до 125oC и выдерживают в течение 30 минут после растворения всех твердых соединений. Затем температуру поднимают до 145oC, выдерживают до остановки кипения и затем выдерживают при температуре до 120oC в вакууме до начала образования твердых продуктов выше уровня жидкости в колбе. Затем смесь охлаждают до 105oC и добавляют 25 мл анизола.
В другой колбе на 125 мл смешивают 10 мл анизола и 5,75 г 2-деэокси-2,2-дифтор-3,5-дибензоил-D-рибофуранозил- 1- α -метансульфоната и смесь нагревают до образования гомогенной жидкости. Эту жидкость добавляют при постоянной температуре в смесь цитозина и объединенную смесь выдерживают при 100oC в течение 24 часов.
133 мл часть 4 н. соляной кислоты помещают в колбе на 500 мл. 31,3 мл часть ацетонитрила добавляют в реакционную смесь и разбавленную реакционную смесь затем выливают на кислоту при постоянном перемешивании, в то время как для колбы на 500 мл применяют охлаждающую баню. Объединенную смесь перемешивают при 70oC в течение 10 минут и затем фильтруют при постоянной температуре. Влажный осадок на фильтре суспендируют в течение 10 минут при 70oC в 25 мл 4 н. хлористоводородной кислоты и снова фильтруют. Полученную лепешку суспендируют в течение 10 минут при 70oC в 25 мл деионизированной воды, фильтруют и влажный осадок на фильтре снова суспендируют при 70oC в 50 мл деионизированной воды. pH водной суспензии поднимают до 7 с помощью бикарбоната натрия и смесь перемешивают в течение 10 минут при 50oC или выше и снова фильтруют. Осадок на фильтре суспендируют еще раз в 50 мл деионизированной воды при 70oC в течение 10 минут, фильтруют, остаток сушат и анализируют. 3,98 г полученного продукта соответствует выходу в 61% и содержит менее 1% нежелательного альфа-аномера.
Данное изобретение описано достаточно подробно, включая и предпочтительные примеры его осуществления. Тем не менее следует признать, что специалисты в данной области при рассмотрении настоящего изобретения могут произвести некоторые изменения или усовершенствования, которые не выходят за пределы объема и сущности изобретения, изложенного в следующей формуле.
Описывается способ очистки и выделения обогащенного бета-аномером нуклеозида, содержащий а) предоставление смеси, содержащей R'', и обогащенный бета-аномером гликозид формулы IB, где каждый X независимо выбирают из гидроксизащитных групп, и R' представляет нуклеиновое основание формулы II, где W представляет аминозащитную группу; R'' представляет нуклеиновое основание формулы III, где W' представляет аминозащитную группу или водород; в высококипящем растворителе; b) разбавление смеси органическим растворителем, выбранным из группы, состоящей из простых эфиров, сложных эфиров и нитрилов; с) добавление разбавленной реакционной смеси в водную кислоту; d) выдерживание полученной таким образом кислотной смеси при температуре 70 - 100oC до тех пор, пока не осадится продукт формулы IB, где W представляет теперь W'. Технический результат - упрощение процесса и повышение выхода целевого продукта. 4 з.п. ф-лы.



а) получение смеси, содержащей R'', и обогащенный бета-аномером нуклеозид формулы IВ
где каждый Х независимо выбирают из гидроксизащитных групп;
R' представляет нуклеиновое основание формулы
где W представляет аминозащитную группу;
R'' представляет нуклеиновое основание формулы
где W' представляет аминозащитную группу или водород,
в высококипящем растворителе,
b) разбавление смеси органическим растворителем, выбранным из группы, состоящей из простых эфиров, сложных эфиров и нитрилов,
с) добавление разбавленной реакционной смеси в водную неорганическую кислоту,
d) выдерживание полученной кислой смеси при температуре 70 - 100oC до тех пор, пока не осадится продукт формулы IВ, где W представляет собой теперь W'.
| US 5223608 А, 29.06.1993 | |||
| Способ получения нуклеозида или его фармацевтически приемлемых солей | 1984 |
|
SU1442076A3 |
| US 5015743 А, 14.05.1991 | |||
| US 4965374 А, 23.10.1990. | |||
Авторы
Даты
2001-01-10—Публикация
1995-11-01—Подача