Изобретение относится к области синтеза производных адамантана, а именно к способу получения 1-адамантилальдегида, который может быть использован в качестве полупродуктов для синтеза функциональных адамантанов, а также биологически активных веществ.
Известен способ получения 1-адамантилальдегида восстановлением хлорангидрида 1-адамантанкарбоновой кислоты алюмогидридом лития в присутствии азиридина с выходом 24%. В основном получается полимерный продукт. (Патент Нидерланды N 6613232, 1967 г., Chem. Abst.68, N 68538, 1968 г.).
Известен также способ получения 1-адамантилальдегида из 1-адамантилметанола окислением тетраацетатом свинца с выходом 52%. (Н.Л.Довгань, Ф.Н.Степанов "Тезисы докладов 10-й Украинской республиканской конференции по органической химии". Киев: Наукова Думка, 1969 г., с.79).
1-Адамантилальдегид получают также при сухой перегонке смеси Ca-соли 1-адамантанкарбоновой кислоты с большим избытком муравьино-кислого кальция. Выход сырого продукта - 70%. Полученный альдегид очищают через бисульфитное производное (Ф.Н.Степанов, Н.Л.Довгань, ЖОХ N 4, 277, 1968 г.).
(AdCOO)2Ca + (HCOO)2Ca ---> 1-Ad-CHO
Общим недостатком рассмотренных способов получения 1-адамантилальдегида является недостаточно высокий выход конечного продукта, большая часть продуктов реакции представляет собой продукт полимеризации 1-адамантилальдегида. Эти факторы снижают эффективность способов получения 1-адамантилальдегида.
Наиболее близким решением к заявляемому по технической сущности является способ получения 1-адамантилальдегида (Авторское свидетельство СССР N 438249 МКИ C 07 C 47/44, 1977 г.) взаимодействием адамантана с окисью углерода в хлористом метилене в присутствии хлористого алюминия при ступенчатом подъеме температуры реакционной смеси от -10oC до 25oC в течение двух часов. В середине процесса перед пропусканием окиси углерода к реакционной смеси добавляют пентан. Альдегид выделяется стандартными приемами ступенчатой экстракции. Выход 1-AdCHO-75%.
Описанный процесс имеет следующие недостатки: сложный состав реагентов, необходимость осуществления программного режима по температуре, сложное выделение продуктов реакции, большая часть продуктов реакции представляет собой продукт полимеризации 1-адамантилальдегида, недостаточно высокий выход целевого продукта.
Задачей предлагаемого изобретения является создание эффективного способа синтеза 1-адамантилальдегида.
Техническим результатом предлагаемого изобретения является улучшение технологичности процесса, повышения выхода, отсутствие полимера в продуктах реакции.
Представленный технический результат достигается тем, что при получении 1-адамантилальдегида в качестве функционального производного используют нитрил 1-адамантанкарбоновой кислоты, который восстанавливают продуктом взаимодействия хлорида олова (II) с хлористым водородом в присутствии диэтилового эфира с получением гексахлороловянной соли 1-адамантилальдегимина, которую обрабатывают избытком воды с получением 1-адамантилальдегида при мольном соотношении нитрила 1-адамантанкарбоновой кислоты, хлорида олова, диэтилового эфира 1:1,5-2,0:6,2-7,0.
SnCl2 + 2HCl ---> H2SnCl4.
2AdCN + 2H2SnCl4 + 2HCl ---> [AdCH = NH2]2 · SnCl6 + SnCl4.
[AdCH = NH2]2 · SnCl6 + 2H2O ---> 2AdCHO + SnCl4 + 2NH4Cl.
Использование нитрила 1-адамантанкарбоновой кислоты, обладающего высокой реакционной способностью позволяет восстанавливать его продуктом взаимодействия хлорида олова (II) с хлористым водородом с получением гексахлороловянной соли 1-адамантилальдимина, не склонной к полимеризации в присутствии органического растворителя, что повышает выход и чистоту конечного продукта. 1-Адамантилальдегид выделяют в водной среде, что позволяет избежать быстрой полимеризации 1-адамантилальдегида, вследствие этого полимер отсутствует в продуктах реакции.
Разработанный способ позволяет получать 1-адамантилальдегид с высоким выходом 93-95%.
Выбор указанных соотношений реагентов обусловлен следующим:
- уменьшение концентрации хлорида олова ниже указанных интервалов приводит к снижению выхода целевого продукта за счет снижения конверсии нитрила адамантанкарбоновой кислоты, а повышение концентрации хлорида олова приводит к неоправданному перерасходу этого реагента, не приводя к увеличению выхода 1-адамантилальдегида;
- уменьшение концентрации диэтилового эфира приводит к уменьшению выхода 1-адамантилальдегида, а увеличение концентрации диэтилового эфира приводит к увеличению продолжительности реакции.
Проведенный заявителем анализ уровня техники, включающий поиск по патентным и научным источникам информации, и выявление источников, содержащих сведения об аналогах заявленного изобретения, позволили установить, что заявителем не обнаружен аналог, характеризующийся признаками, идентичными всем существенным признакам заявленного изобретения, изложенным в формуле изобретения.
Следовательно, заявленное изобретение соответствует требованию "новизна" по действующему законодательству.
Для проверки соответствия заявленного изобретения требованию "изобретательского уровня" заявитель провел дополнительный поиск известных решений с целью выявления признаков, совпадающих с отличительными от прототипа признаками заявленного изобретения, результаты которого показывают, что заявленное изобретение не следует явным образом из известного уровня техники, определенного заявителем, не выявлено влияние предусматриваемых существенными признаками заявленного изобретения преобразования на достижение технического результата.
Следовательно, заявленное изобретение соответствует требованию "изобретательский уровень" по действующему законодательству.
Способ осуществляется следующим образом: в реактор последовательно загружают абсолютный диэтиловый эфир и хлорид олова (II). При перемешивании суспензию охлаждают до 0-5oC и при этой температуре насыщают хлористым водородом до образования истинного раствора. Не прекращая перемешивания, порциями вносят нитрил 1-адамантанкарбоновой кислоты, следя за тем, чтобы температура реакционной массы не превышала 5oC. После прибавления всего количества нитрила реакционную массу перемешивают при температуре 0-5oC 2 часа, затем выдерживают без перемешивания 20 часов при температуре 20-25oC. За это время выпадает в осадок гексахлороловяннокислый 1-адамантилальдимин. Соль альдимина отфильтровывают и обрабатывают избытком воды при температуре 60oC. При этом 1-адамантилальдимин полностью гидролизуется до 1-адамантилальдегида. Суспензию альдегида в воде охлаждают до 20-25oC, отфильтровывают осадок, промывают водой и сушат.
Способ апробирован в лабораторных условиях, ниже приведены конкретные примеры осуществления способа.
Пример 1.
В четырехгорлый реактор, снабженный мешалкой, термометром, барботером и обратным холодильником с хлоркальцевой трубкой, последовательно загружают 40 мл (0,385 моль) абсолютного диэтилового эфира, 17,6 г (0,093 моль) хлорида олова (II). При перемешивании суспензию охлаждают до 0 - 5oC и при этой температуре насыщают хлористым водородом до образования истинного раствора. Не прекращая перемешивания, порциями вносят 10 г (0,062 моль) нитрила адамантанкарбоновой кислоты, следя за тем чтобы температура реакционной массы не превышала 5oC. После прибавления всего количества нитрила реакционную массу перемешивают при температуре 0-5oC 2 часа, затем выдерживают без перемешивания 20 часов при температуре 20-25oC. За это время выпадает в осадок гексахлороловяннокислый 1-адамантилальдимин. Соль альдимина отфильтровывают и переносят в стакан с 200 мл воды. При перемешивании суспензию нагревают до 60oC. При этом 1-адамантилальдимин полностью гидролизуется до 1-адамантилальдегида. Суспензию альдегида в воде охлаждают до 20 - 25oC, отфильтровывают осадок и промывают дважды по 20 мл воды, сушат. Мольное соотношение 1-AdCN: SnCl2: (C2H5)2O = 1:1,5:6,2. Выход 1-адамантилальдегида 9,5 г (93%). Tпл = 139-141oC. Найдено, %: C 80,21; H 9,83; C11H16O. Вычислено, %: C 80,48; H 9,75; C11H16O. ИК-спектр (в вазелиновом масле), см-1: 1728 (C=O), 1376 (CH).
Пример 2.
В четырехгорлый реактор, снабженный мешалкой, термометром, барботером и обратным холодильником с хлоркальциевой трубкой, последовательно загружают 40 мл (0,385 моль) абсолютного диэтилового эфира, 18,8 г (0,099 моль) хлорида олова (II). При перемешивании суспензию охлаждают до 0-5oC и при этой температуре насыщают хлористым водородом до образования истинного раствора. Не прекращая перемешивания порциями вносят 10 г (0,062 моль) нитрила адамантанкарбоновой кислоты, следя за тем, чтобы температура реакционной массы не превышала 5oC. После прибавления всего количества нитрила реакционную массу перемешивают при температуре 0-5oC 2 часа, затем выдерживают без перемешивания 20 часов при температуре 20-25oC. За это время выпадает в осадок гексахлороловяннокислый 1-адамантилальдимин. Соль альдимина отфильтровывают и переносят в стакан с 200 мл воды. При перемешивании суспензию нагревают до 60oC. При этом 1-адамантилальдимин полностью гидролизуется до 1-адамантилальдегида. Суспензию альдегида в воде охлаждают до 20-25oC, отфильтровывают осадок и промывают дважды по 20 мл воды, сушат. Мольное соотношение 1-AdCN: SnCl2: (C2H5)2O = 1:1,6:6,2. Выход 1-адамантилальдегида 9,6 г (94%).
Пример 3.
В четырехгорлый реактор, снабженный мешалкой, термометром, барботером и обратным холодильником с хлоркальциевой трубкой, последовательно загружают 40 мл (0,385 моль) абсолютного диэтилового эфира 20,0 г (0,105 моль) хлорида олова (II). При перемешивании суспензию охлаждают до 0-5oC и при этой температуре насыщают хлористым водородом до образования истинного раствора. Не прекращая перемешивания порциями вносят 10 г (0,062 моль) нитрила адамантанкарбоновой кислоты, следя за тем, чтобы температура реакционной массы не превышала 5oC. После прибавления всего количества нитрила реакционную массу перемешивают при температуре 0-5oC 2 часа, затем выдерживают без перемешивания 20 часов при температуре 20-25oC. За это время выпадает в осадок гексахлороловяннокислый 1-адамантилальдимин. Соль альдимина отфильтровывают и переносят в стакан с 200 мл воды. При перемешивании суспензию нагревают до 60oC. При этом 1-адамантилальдимин полностью гидролизуется до 1-адамантилальдегида. Суспензию альдегида в воде охлаждают до 20-25oC, отфильтровывают осадок и промывают дважды по 20 мл воды, сушат. Мольное соотношение 1-AdCN: SnCl2:(C2H5)2O = 1:1,7:6,2. Выход 1-адамантилальдегида 9,6 г (94%).
Пример 4.
В четырехгорлый реактор, снабженный мешалкой, термометром, барботером и обратным холодильником с хлоркальциевой трубкой, последовательно загружают 40 мл (0,385 моль) абсолютного диэтилового эфира 21,2 г (0,112 моль) хлорида олова (II). При перемешивании суспензию охлаждают до 0-5oC и при этой температуре насыщают хлористым водородом до образования истинного раствора. Не прекращая перемешивания порциями вносят 10 г (0,062 моль) нитрила адамантанкарбоновой кислоты, следя за тем, чтобы температура реакционной массы не превышала 5oC. После прибавления всего количества нитрила реакционную массу перемешивают при температуре 0-5oC 2 часа, затем выдерживают без перемешивания 20 часов при температуре 20-25oC. За это время выпадает в осадок гексахлороловяннокислый 1-адамантилальдимин. Соль альдимина отфильтровывают и переносят в стакан с 200 мл воды. При перемешивании суспензию нагревают до 60oC. При этом 1-адамантилальдимин полностью гидролизуется до 1-адамантилальдегида. Суспензию альдегида в воде охлаждают до 20-25oC, отфильтровывают осадок и промывают дважды по 20 мл воды, сушат. Мольное соотношение 1-AdCN: SnCl2:(C2H5)2O = 1:1,9:6,2. Выход 1-адамантилальдегида 9,7 г (95%).
Пример 5.
В четырехгорлый реактор, снабженный мешалкой, термометром, барботером и обратным холодильником с хлоркальциевой трубкой, последовательно загружают 40 мл (0,385 моль) абсолютного диэтилового эфира, 22,3 г (0,118 моль) хлорида олова (II). При перемешивании суспензию охлаждают до 0-5oC и при этой температуре насыщают хлористым водородом до образования истинного раствора. Не прекращая перемешивания порциями вносят 10 г (0,062 моль) нитрила адамантанкарбоновой кислоты, следя за тем, чтобы температура реакционной массы не превышала 5oC. После прибавления всего количества нитрила реакционную массу перемешивают при температуре 0-5oC 2 часа, затем выдерживают без перемешивания 20 часов при температуре 20-25oC. За это время выпадает в осадок гексахлороловяннокислый 1-адамантилальдимин. Соль альдимина отфильтровывают и переносят в стакан с 200 мл воды. При перемешивании суспензию нагревают до 60oC. При этом 1-адамантилальдимин полностью гидролизуется до 1-адамантилальдегида. Суспензию альдегида в воде охлаждают до 20-25oC, отфильтровывают осадок и промывают дважды по 20 мл воды, сушат. Мольное соотношение 1-AdCN: SnCl2:(C2H5)2O = 1:1,9:6,2. Выход 1-адамантилальдегида 9,7 г (95%).
Пример 6.
В четырехгорлый реактор, снабженный мешалкой, термометром, барботером и обратным холодильником с хлоркальциевой трубкой, последовательно загружают 40 мл (0,385 моль) абсолютного диэтилового эфира, 23,5 г (0,124 моль) хлорида олова (II). При перемешивании суспензию охлаждают до 0-5oC и при этой температуре насыщают хлористым водородом до образования истинного раствора. Не прекращая перемешивания порциями вносят 10 г (0,062 моль) нитрила адамантанкарбоновой кислоты, следя за тем, чтобы температура реакционной массы не превышала 5oC. После прибавления всего количества нитрила реакционную массу перемешивают при температуре 0-5oC 2 часа, затем выдерживают без перемешивания 20 часов при температуре 20-25oC. За это время выпадает в осадок гексахлороловяннокислый 1-адамантилальдимин. Соль альдимина отфильтровывают и переносят в стакан с 200 мл воды. При перемешивании суспензию нагревают до 60oC. При этом 1-адамантилальдимин полностью гидролизуется до 1-адамантилальдегида. Суспензию альдегида в воде охлаждают до 20-25oC, отфильтровывают осадок и промывают дважды по 20 мл воды, сушат. Мольное соотношение 1-AdCN: SnCl2:(C2H5)2O = 1:2,0:6,2. Выход 1-адамантилальдегида 9,7 г (95%).
Пример 7.
В четырехгорлый реактор, снабженный мешалкой, термометром, барботером и обратным холодильником с хлоркальциевой трубкой, последовательно загружают 42,5 мл (0,410 моль) абсолютного диэтилового эфира, 22,3 г (0,118 моль) хлорида олова (II). При перемешивании суспензию охлаждают до 0-5oC и при этой температуре насыщают хлористым водородом до образования истинного раствора. Не прекращая перемешивания порциями вносят 10 г (0,062 моль) нитрила адамантанкарбоновой кислоты, следя за тем, чтобы температура реакционной массы не превышала 5oC. После прибавления всего количества нитрила реакционную массу перемешивают при температуре 0-5oC 2 часа, затем выдерживают без перемешивания 20 часов при температуре 20-25oC. За это время выпадает в осадок гексахлороловяннокислый 1-адамантилальдимин. Соль альдимина отфильтровывают и переносят в стакан с 200 мл воды. При перемешивании суспензию нагревают до 60oC. При этом 1-адамантилальдимин полностью гидролизуется до 1-адамантилальдегида. Суспензию альдегида в воде охлаждают до 20-25oC, отфильтровывают осадок и промывают дважды по 20 мл воды, сушат. Мольное соотношение 1-AdCN:SnCl2:(C2H5)2O = 1:1,9:6,6. Выход 1-адамантилальдегида 9,7 г (95%).
Пример 8.
В четырехгорлый реактор, снабженный мешалкой, термометром, барботером и обратным холодильником с хлоркальциевой трубкой, последовательно загружают 45,0 мл (0,434 моль) абсолютного диэтилового эфира, 22,3 г (0,118 моль) хлорида олова (II). При перемешивании суспензию охлаждают до 0-5oC и при этой температуре насыщают хлористым водородом до образования истинного раствора. Не прекращая перемешивания порциями вносят 10 г (0,062 моль) нитрила адамантанкарбоновой кислоты, следя за тем, чтобы температура реакционной массы не превышала 5oC. После прибавления всего количества нитрила реакционную массу перемешивают при температуре 0-5oC 2 часа, затем выдерживают без перемешивания 20 часов при температуре 20-25oC. За это время выпадает в осадок гексахлороловяннокислый 1-адамантилальдимин. Соль альдимина отфильтровывают и переносят в стакан с 200 мл воды. При перемешивании суспензию нагревают до 60oC. При этом 1-адамантилальдимин полностью гидролизуется до 1-адамантилальдегида. Суспензию альдегида в воде охлаждают до 20-25oC, отфильтровывают осадок и промывают дважды по 20 мл воды, сушат. Мольное соотношение 1-AdCN: SnCl2:(C2H5)2O = 1:1,9:7,0. Выход 1-адамантилальдегида 9,7 г (95%).
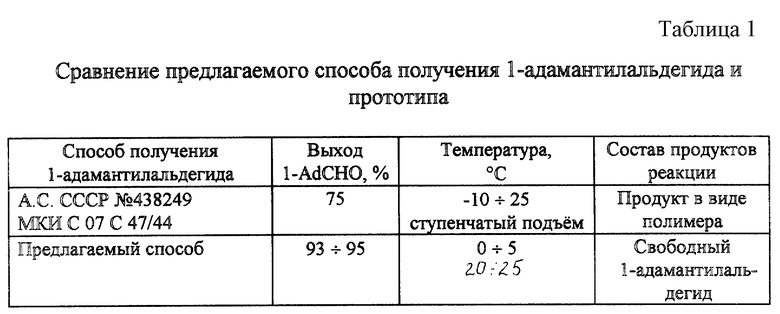
Сравнительные характеристики предлагаемого и известных способов получения 1-адамантилальдегида приведены в таблице 1.
Как следует из данных таблицы, предлагаемый способ обладает существенными преимуществами перед прототипом: более высокую технологичность, более высокий выход, более простые способы выделения конечного продукта, отсутствие полимера в продуктах реакции.
Таким образом, вышеизложенные сведения свидетельствуют о выполнении при использовании заявленного изобретения следующей совокупности условий:
- средство, воплощающее изобретение при его осуществлении, предназначено для использования в различных отраслях химической и фармацевтической промышленности;
- для заявленного изобретения в том виде, как оно охарактеризовано в формуле изобретения, подтверждена возможность его осуществления с помощью вышеописанных в заявке или известных до даты приоритета средств и методов:
- средство, воплощающее заявленное изобретение при его осуществлении, способно обеспечить достижение технического результата.
Следовательно, заявленное изобретение соответствует требованию промышленная применимость.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ АЛЬФА-АДАМАНТИЛСОДЕРЖАЩИХ АЛЬДЕГИДОВ | 2003 |
|
RU2240303C1 |
| СПОСОБ ПОЛУЧЕНИЯ 4-БРОМ-5-НИТРОФТАЛОНИТРИЛА | 1999 |
|
RU2167855C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-(АДАМАНТ-1-ИЛ)ЭТИЛАМИНА И ЕГО ГОМОЛОГОВ | 1998 |
|
RU2152924C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-ЗАМЕЩЕННЫХ АЛКИЛ-(2-ДИАЛКОКСИФОСФОРИЛ)АЛКИЛИМИДАТОВ | 2001 |
|
RU2203284C1 |
| МНОГОЯДЕРНЫЕ БИСАЗИДЫ | 1994 |
|
RU2067572C1 |
| СПОСОБ ПОЛУЧЕНИЯ АДАМАНТИЛСОДЕРЖАЩИХ НИТРИЛОВ | 2003 |
|
RU2240310C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОХЛОРИДОВ АМИНОПРОИЗВОДНЫХ АДАМАНТАНА | 2010 |
|
RU2440971C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-(2-АЛКИЛ(ДИАЛКИЛ)АМИНО)АДАМАНТИЛАЛКИЛ(АРИЛ)КЕТОНОВ | 2009 |
|
RU2408570C1 |
| СПОСОБ ПОЛУЧЕНИЯ α-АДАМАНТИЛСОДЕРЖАЩИХ АЛИФАТИЧЕСКИХ И ЖИРНОАРОМАТИЧЕСКИХ КЕТОНОВ | 2000 |
|
RU2186760C2 |
| СПОСОБ ПОЛУЧЕНИЯ N-ЗАМЕЩЁННЫХ ЭТИЛ-(2-ДИАЛКОКСИФОСФОРИЛ-4ЦИАНО)-БУТАНИМИДАТОВ | 2003 |
|
RU2236414C1 |
Изобретение относится к синтезу производных адамантана, а именно к способу получения 1-адамантилальдегида, который может быть использован в качестве полупродукта для синтеза функциональных адамантанов, а также биологически активных веществ. Техническим результатом является упрощение процесса, повышение выхода, отсутствие полимера в продуктах реакции. Технический результат достигается тем, что в качестве функционального производного используют нитрит 1-адамантанкарбоновой кислоты, который восстанавливают продуктом взаимодействия хлорида олова (II) с хлористым водородом в присутствии диэтилового эфира с получением гексахлороловянной соли 1-адамантилальдимина, которую обрабатывают избытком воды с получением 1-адамантилальдегида при мольном соотношении нитрила 1-адамантанкарбоновой кислоты, хлорида олова, диэтилового эфира 1 : 1,5 - 2,0 : 6,2 - 7,0. 1 табл.
Способ получения 1-адамантилальдегида из функциональных производных адамантана, отличающийся тем, что в качестве функционального производного используют нитрил 1-адамантанкарбоновой кислоты, который восстанавливают продуктом взаимодействия хлорида олова II с хлористым водородом в присутствии диэтилового эфира с получением гексахлороловянной соли 1-адамантилальдимина, которую обрабатывают избытком воды с получением 1-адамантилальдегида при мольном соотношении нитрила 1-адамантанкарбоновой кислоты, хлорида олова, диэтилового эфира 1 : 1.5 - 2.0 : 6.2 - 7.0.
| Способ получения адамантил-1-альдегида | 1972 |
|
SU438249A1 |
| GB 811527 A, 08.04.1959 | |||
| US 2904594 A, 15.09.1959 | |||
| Химическая энциклопедия | |||
| - М.: Большая Российская энциклопедия, 1992, т.3, стр.262 | |||
| Цифровой измеритель средней частоты | 1978 |
|
SU765742A1 |
| ДОВГАНЬ Н.Л., СТЕПАНОВ Ф.Н | |||
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| - Киев: Наукова Думка, 1969, стр.79 | |||
| СТЕПАНОВ Ф.Н., ДОВГАНЬ Н.Л | |||
| - ЖОХ, 1968, № 4, стр.277. | |||
Авторы
Даты
2001-02-27—Публикация
1999-04-06—Подача