Изобретение относится к способу получения 4-бром-5-нитрофталонитрила (БНФН), который является полупродуктом в синтезе мономеров для термостойких полимерных материалов и биологически активных веществ.
Известен способ получения 4-нитрофталонитрила (НФН), заключающийся в последовательном проведении амидизации 4-нитрофталимида (I) и дегидратации 4-нитрофталимида (II) (Griffith J.R., O'Rear J.G. Copoliymers, Polyblends and Compos. Symp. , Los Angeles, Calif., 1976, Washington, D.C., 1976, p. 458-464):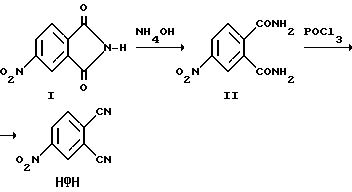
Амидизацию I проводят в 30%-ном водном растворе гидроксида аммония при мольном соотношении NH4OH : I = 20 и температуре 45oC в течение 1 часа. Синтез II в данных условиях сопровождается значительным вспениванием реакционной массы. Образующийся осадок - целевой продукт отфильтровывают, промывают водой и сушат. Выход II - 80% от теории. Дегидратацию II проводят путем обработки его суспензии в пиридине хлорокисью фосфора при мольном соотношении II : POCl3 : пиридин = 1 : 2,3 : 8,8 и температуре 65...70oC в течение 1,5 часа. Выделение и очистка целевого НФН заключается в последовательном проведении нейтрализации реакционной массы водным раствором соляной кислоты, выделения и сушки осадка, его экстрагирования этилацетатом, обесцвечивания и упаривания экстракта. Выход НФН составляет 50% от теории в расчете на II. Таким образом, суммарный выход НФН в расчете на исходный I составляет 40,5% от теории.
Недостатком данного способа являются значительное вспенивание реакционной массы на стадии амидизации, в результате чего возникает необходимость снижения интенсивности перемешивания, а следовательно, скорости амидизации, использование токсичного пиридина в качестве растворителя на стадии дегидратации, необходимость проведения дополнительной очистки - экстракции с использованием этилацетата по окончании дегидратации, низкий выход продукта в расчете на исходный 4-нитрофталимид.
Наиболее близким к предлагаемому является способ получения БНФН (Галогенонитрофталимиды и фталодинитрилы на их основе. Шишкина О.В., Майзлиш B. Е. , Шапошников Г.П. и др. //Ж. Общ. Хим. -1997, т. 67, вып. 5, с. 842-845), включающий нитрование 4-бpoмфтaлимидa (III), амидизацию 4-бpoм-5-нитрофталимида (IV) и дегидратацию 4-бром-5-нитрофталамида (V) по схеме: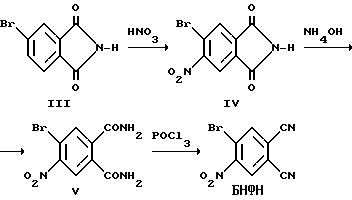
Нитрование III проводят 100%-ной азотной кислотой в растворе концентрированной серной кислоты. Количество азотной кислоты, берущейся на нитрование, составляет 14% нитрующей смеси, мольное соотношение HNO3 : III = 4, начальная концентрация III в серной кислоте 0,8 моль/л. Температура реакции 20oC, время 5 часов. По окончании нитрования реакционную массу выливают в воду со льдом, осадок отфильтровывают, промывают водой до нейтральной среды фильтрата, сушат. Выход IV составляет 79% от теории. Амидизацию IV проводят в 25%-ном водном растворе гидроксида аммония при температуре 20oC в течение 2 суток. Выход V составляет около 80%. Дегидратацию V проводят путем обработки его 50%-ного раствора в ДМФА тионилхлоридом при температуре 20...25oC и мольном соотношении SOCl2 : V = 3,7 в течение 4 часов. По окончании дегидратации реакционную массу выливают на лед, осадок отфильтровывают, промывают водой до нейтральной среды фильтрата, сушат. Выход БНФН составляет 86% от теории в расчете на V. Таким образом, выход БНФН в расчете на исходный III составляет 54%.
Недостатками данного способа являются чрезвычайно большое время амидизации, значительный избыток дегидратирующего агента на стадии дегидратации и азотной кислоты на стадии нитрования, низкий выход целевого БНФН в расчете на исходный 4-бромфталимид.
Цель изобретения - сокращение времени амидизации, снижение расходных коэффициентов на стадиях нитрования и дегидратации, повышение чистоты и выхода целевого продукта.
Поставленная цель достигается тем, что нитрование III проводят 100%-ной азотной кислотой в растворе концентрированной серной кислоты при мольном соотношении азотная кислота : III = 1,2...1,4 начальной концентрации III в серной кислоте 2,6...2,7 моль/л и температуре 45...50oC в течение 5...6 ч, амидизацию IV проводят в водном растворе гидроксида аммония с содержанием аммиака не менее 25 мас.% в присутствии хлористого аммония при температуре 35. . .40oC и мольном соотношении IV : NH4OH : NH4Cl = 1 : 30...32 : 2...4 в течение 1,5. ..2 часов, а дегидратацию V проводят хлорокисью фосфора в ДМФА при температуре 30...35oC и мольном соотношении V : POCl3 : ДМФА = 1 : 1,2.. .1,3 : 8...10 в течение 1,5...2 часов.
Нитрование III проводят в колбе, снабженной мешалкой, обратным холодильником, термометром и капельной воронкой.
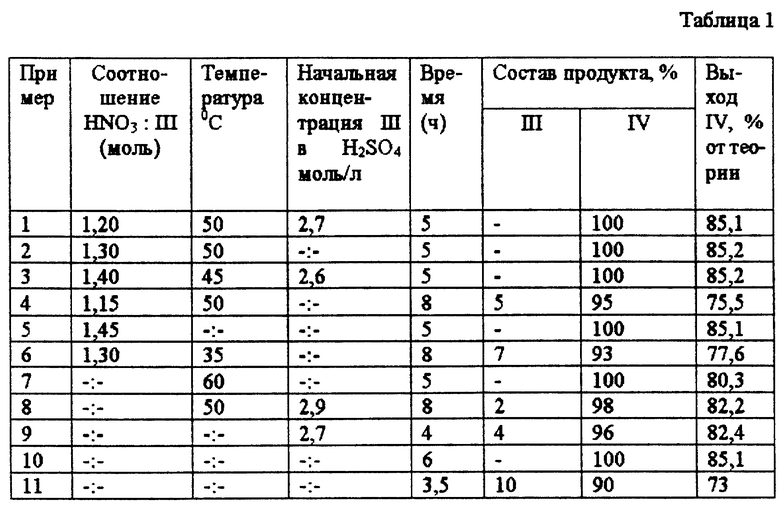
Зависимость расходных коэффициентов реагентов, чистоты и выхода целевого продукта от условий нитрования представлены в таблице 1.
Из таблицы 1 видно, что соотношение азотная кислота : III = 1,2...1,4 : 1 (моль) позволяет достигать максимальной степени чистоты и выхода целевого продукта (примеры 1-3). Если соотношение азотная кислота : III меньше 1,2, то полная конверсия III не достигается даже за 8 ч в указанных условиях (пример 4). Соотношения HNO3 : III > 1,4 (моль) не приводит к увеличению выхода IV (пример 5).
Другим важным фактором является температура нитрования. В выбранных условиях максимальный выход достигается при температуре 45...50oC (примеры 1-3,5). При температуре ниже 45oC наблюдается снижение скорости нитрования, в результате чего не достигается полная конверсия III (пример 6). При температуре выше 50oC имеет место снижение выхода IV, по-видимому, из-за протекания побочных реакций (пример 7).
Начальная концентрация III в серной кислоте влияет на чистоту целевого продукта и величину расходных коэффициентов реагентов на стадии нитрования. Установлено, что начальная концентрация III в серной кислоте, равная 2,6... 2,7 моль/л, позволяет осуществлять реакцию с максимальным выходом (пример 1 - 3, 5, 9). Если концентрация III в серной кислоте больше 2,7 моль/л, имеет место неполная конверсия III (пример 8). При концентрации III меньше 2,6 моль/л чистота и выход целевого продукта максимальны, однако снижается съем продукта с единицы реакционного объема.
Время реакции определяет глубину превращения реагентов. В выбранных условиях полная конверсия III достигается за 5...5,5 ч, максимальный выход IV составляет 85,2% на исходный III (примеры 1 - 3, 5, 10).
Амидизацию IV проводят в колбе, снабженной мешалкой, обратным холодильником и термометром. Выделение V проводят путем охлаждения реакционной смеси до 5oC с последующей фильтрацией целевого продукта.
Зависимость времени реакции и выхода целевого V от условий реакции представлены в таблице 2.
Из таблицы 2 видно, что наибольший выход V получается при использовании водного раствора аммиака с концентрацией не менее 25% (примеры 12, 13, 16, 17, 20). При меньших концентрациях выход V снижается (пример 14).
Температура также оказывает влияние на выход V. В выбранных условиях максимальный выход V можно получить при температуре 35...40oC (примеры 12, 13, 16, 17, 20). Дальнейшее повышение температуры невозможно по причине сильного вскипания реакционной массы. При снижении температуры выход целевого продукта уменьшается (пример 15).
Соотношения реагентов так же влияют на результаты амидизации. При мольном соотношении IV : NH4Cl : NH4OH = 1 : 2...4 : 30...32 выход V максимален (примеры 12, 13, 16, 17). При дальнейшем увеличении количеств аммиака и хлорида аммония не происходит увеличения выхода целевого V (пример 20). Уменьшение количеств аммиака и хлорида аммония вызывает уменьшение выхода V (пример 18). Проведение амидизации без хлорида аммония приводит к вскипанию и значительному вспениванию реакционной массы при более низкой температуре, к снижению выхода V (пример 19). Максимальный выход V составляет 98,2% на исходный IV.
Дегидратацию V проводят в колбе, снабженной мешалкой, обратным холодильником, термометром и капельной воронкой.
Зависимость чистоты и выхода целевого продукта на стадии дегидратации от условий реакции представлены в таблице 3.
Из таблицы 3 видно, что при соотношении V : POCl3 : ДМФА = 1 : 1,2...1,3 : 8. . . 10 (моль) чистота и выход БНФН максимальны (примеры 21, 22). Дальнейшее увеличение количеств POCl3 и ДМФА не приводит к увеличению выхода БНФН (пример 23). Снижение количества POCl3 приводит к неполной конверсии V и снижению выхода целевого БНФН (пример 24). При уменьшении количества ДМФА выход БНФН уменьшается по причине плохой растворимости исходных реагентов (пример 25).
Другим важным фактором, оказывающим влияние на протекание реакции, является температура. Установлено, что в выбранных условиях наилучших результатов удается добиться в интервале 30...35oC (примеры 21-23). При температуре ниже 30oC наблюдается снижение скорости дегидратации и, следовательно, выхода БНФН (пример 26). При температуре выше 35oC выход и качество БНФН снижаются из-за протекания побочных реакций (пример 27).
Время реакции определяет глубину превращения реагентов. В выбранных условиях полная конверсия достигается за 1,5...2 ч, максимальный выход БНФН составляет 85,2% на исходный V (примеры 21 - 23, 27).
Таким образом, суммарный выход БНФН при последовательном проведении нитрования, амидизации и дегидратации составляет 71,2% в расчете на исходный III.
Строение и чистоту промежуточных соединений и целевого БНФН анализировали методами ПМР, определением температуры плавления и элементного состава.
Изобретение иллюстрируется следующими примерами.
Пример 1. В колбу, снабженную мешалкой, обратным холодильником, термометром и капельной воронкой, загружают 50 г (0,22 моль) III, 80 мл концентрированной серной кислоты, поднимают температуру до 50oC, при интенсивном перемешивании в течение 1 мин прибавляют 11 мл (0,264 моль) 100% азотной кислоты. Реакцию ведут при 50oC в течение 5 часов, после чего реакционную смесь охлаждают, выливают в 300 мл ледяной воды, выпавший осадок отфильтровывают, промывают водой (2 раза по 30 мл), сушат. Получают 51 г (85% от теории) IV - белый порошок, т.пл. 216-218oC.
Найдено, %: C 35,67; H 1,10; N 10,07.
Вычислено, %: C 35,45; H 1,12; N 10,34.
Примеры 2-10. Нитрование III проводят аналогично примеру 1. Условия и результаты приведены в таблице 1.
Пример 11. В колбу, снабженную мешалкой, обратным холодильником, термометром, загружают 563 мл (7,5 моль) 25%-ного раствора аммиака, 26,5 г (0,5 моль) хлорида аммония. После полного растворения соли прибавляют 68 г (0,25 моль) IV и поднимают температуру до 40oC. Реакцию ведут при 40oC в течение 1,5 часов, после чего реакционную смесь охлаждают до 5oC, осадок отфильтровывают, промывают водой (2 раза по 200 мл), сушат. Получают 68,5 г (95% от теории) V - белый порошок, т.пл. 216-218oC.
Найдено, %: C 33,54; H 2,14; N 14,21.
Вычислено, %: C 33,35; H 2,10; N 14,59.
Примеры 12-20. Амидизацию IV проводят аналогично примеру 11. Условия и результаты приведены в таблице 2.
Пример 21. В колбу, снабженную мешалкой, обратным холодильником, термометром и капельной воронкой, загружают 302 г (1,05 моль) V и 560 мл (8,4 моль) ДМФА. При интенсивном перемешивании из капельной воронки вводят в течение 0,5 мин 115 мл (193,1 г, 1,26 моль) POCl3. Температура реакционной массы поднимается до 35oC, массу перемешивают при 35oC в течение 1,5 ч до растворения осадка, медленно охлаждают до комнатной температуры за 1 ч, выливают в 3 л ледяной воды. Выпавший осадок отфильтровывают, промывают 300 мл воды и сушат. Получают 225 г (85% от теории) БНФН - белый порошок, т.пл. 160-161oC.
Найдено, %: C 38,25; H 0,76; N 16,42.
Вычислено, %: C 38,12; H 0,80; N 16,68.
1H NMR (DMSO - d6) δ, мд: 8.82 (s, 1H, H-1), 8.80 (s, 1H, H-2).
Примеры 22 - 27. Дегидратацию V проводят аналогично примеру 21. Условия и результаты приведены в таблице 3.
| название | год | авторы | номер документа |
|---|---|---|---|
| 4-ТРЕТ-БУТИЛ-5-НИТРОФТАЛОНИТРИЛ | 2012 |
|
RU2495025C1 |
| МЕТАЛЛОКОМПЛЕКСЫ ТЕТРА-(4-ТРЕТ-БУТИЛ-5-НИТРО)ФТАЛОЦИАНИНА | 2012 |
|
RU2507229C1 |
| СПОСОБ ПОЛУЧЕНИЯ 3,4-(3'-АМИНОФЕНОКСИ)ФТАЛЕВОЙ КИСЛОТЫ | 1994 |
|
RU2089540C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,5-БИФЕНИЛДИКАРБОНОВОЙ КИСЛОТЫ | 1994 |
|
RU2078100C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-МЕТИЛ-2-(2'-ОКСОПРОПИЛ)-1,3-ДИОКСОЛАН-4-ИЛМЕТИЛМЕТАКРИЛАТА | 2000 |
|
RU2174515C1 |
| 4'-АМИНО-3,4-БИФЕНИЛДИКАРБОНОВАЯ КИСЛОТА | 1999 |
|
RU2151141C1 |
| СПОСОБ ПОЛУЧЕНИЯ СЛОЖНЫХ ЭФИРОВ 4-(3,4-ДИАМИНОФЕНОКСИ)БЕНЗОЙНОЙ КИСЛОТЫ | 2009 |
|
RU2409555C1 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ О-ДИКАРБОНИТРИЛЫ | 2000 |
|
RU2165929C1 |
| СПОСОБ ПОЛУЧЕНИЯ СУЛЬФОХЛОРИДОВ РЯДА 6-АРИЛПИРИДАЗИН-3(2Н)-ОНОВ | 2011 |
|
RU2455004C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГАЛОГЕН- И/ИЛИ АЛКИЛЗАМЕЩЕННЫХ ДИАРИЛСУЛЬФОНОВ | 1998 |
|
RU2131870C1 |


Изобретение относится к способу получения 4-бром-5-нитрофталонитрила, который может быть использован в качестве полупродукта в синтезе мономеров для термостойких полимерных материалов и биологически активных веществ. Способ включает нитрование 4-бромфталимида азотной кислотой в растворе концентрированной серной кислоты, амидизацию 4-бром-5-нитрофталимида водным аммиаком и дегидратацию 4-бром-5-нитрофталимида в растворе диметилформамида, отличающийся тем, что нитрование проводят при 45 - 50oC с начальной концентрацией 4-бромфталимида в серной кислоте 2,6 - 2,7 моль/л и мольном соотношении азотная кислота : 4-бромфталимид, равном 1,2 - 1,4, в течение 5 - 6 ч, амидизацию проводят в присутствии хлористого аммония при концентрации аммиака в растворе не менее 25 мас.%, температуре 35 - 40oC и мольном соотношении 4-бром-5-нитрофталимид : NH4OH : NH4Cl, равном 1 : 30-32 : 2-4, в течение 1,5 - 2 ч, а дегидратацию 4-бром-5-нитрофталимида проводят хлорокисью фосфора при температуре 30 - 35oC и мольном соотношении 4-бром-5-нитрофталамид : POCl3 : ДМФА, равном 1 : 1,2-1,3 : 8-10, в течение 1,5 - 2 ч. Технический результат - сокращение времени амидизации, снижение расходных коэффициентов на стадиях нитрования и дегидратации, повышение чистоты и выхода целевого продукта. 3 табл.
Способ получения 4-бром-5-нитрофталонитрила, включающий нитрование 4-бромфталимида азотной кислотой в растворе концентрированной серной кислоты, амидизацию 4-бром-5-нитрофталимида водным аммиаком и дегидратацию 4-бром-5-нитрофталимида в растворе диметилформамида, отличающийся тем, что нитрование проводят при 45-50°С с начальной концентрацией 4-бромфталимида в серной кислоте 2,6-2,7 моль/л и мольном соотношении азотная кислота : 4-бромфталимид, равном 1,2-1,4, в течение 5-6 ч, амидизацию проводят в присутствии хлористого аммония при концентрации аммиака в растворе не менее 25 мас. %, температуре 35-40°С и мольном соотношении 4-бром-5-нитрофталимид : NH40H : NH4Cl, равном 1 : 30-32 : 2-4, в течение 1,5-2 ч, а дегидратацию 4-бром-5-нитрофталимида проводят хлорокисью фосфора при температуре 30-35oС и мольном соотношении 4-бром-5-нитрофталамид : РОСl3 : ДМФА, равном 1 : 1,2-1,3 : 8-10, в течение 1,5-2 ч.
| ШИШКИНА О.В | |||
| и ДР | |||
| Галогенонитрофталимиды и фталодинитрилы на их основе | |||
| - Общая химия, 1997, т.67, вып.5, с.842-845 | |||
| US 5202455 С, 06.09.91 | |||
| Способ охлаждения элементов ватержакетных, мартеновских, доменных и других печей | 1949 |
|
SU85986A1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИНИТРИЛОВ АЛКИЛЗАМЕЩЕННЫХ 0-ФТАЛЕВЫХ КИСЛОТ | 0 |
|
SU382612A1 |
Авторы
Даты
2001-05-27—Публикация
1999-07-30—Подача