Изобретение относится к аддитивной композиции для использования в корме для жвачных млекопитающих. Конкретнее, оно относится к аддитивной композиции для использования в порошковом или однородно гранулированном корме для жвачных млекопитающих, которая устойчива в первом отделе желудка, т.е. рубце, жвачного млекопитающего и способна высвобождать основную аминокислоту в четвертом отделе желудка, т.е. сычуге, и последующих органах пищеварения жвачного млекопитающего.
Когда такие биологически активные вещества, как аминокислоты и витамины, вводятся жвачным животным, таким как коровы и овцы, прямым пероральным путем они в основном гидролизуются микроорганизмами, находящимися в рубце, что не позволяет иx эффективно использовать. Следовательно, такой препарат для жвачных млекопитающих, который способен защитить биологически активное вещество от гидролиза микроорганизмами в рубце и дать ему возможность быть усвоенным и поглощенным в сычуге и других органах пищеварения, является важным в области кормов, кормовых агентов и лекарств для жвачных млекопитающих.
В настоящее время для приготовления кормовых добавок, содержащих биологически активные вещества, предложены способы, заключающиеся в диспергировании биологически активного вещества в матриксе, образованном из такого защитного вещества, как гидрофобное вещество типа масла или жира или основное макромолекулярное вещество, и гранулировании полученного композиционного материала, либо способы, заключающиеся в покрытии кристаллов, содержащих биологически активное вещество, таким чувствительным к кислотам веществом, как гидрофобное вещество типа масла, жира или основное макромолекулярное вещество.
В качестве одного из способов, предполагающего диспергирование биологически активного вещества в защитном веществе, по JP-A-60-168,351 предложен, например, способ, основанный на включении в биологически активное вещество не менее 20 мас.% карбоната кальция и не менее 10 мас.% алифатической монокарбоновой кислоты, имеющей 14 или более атомов углерода, отвержденного масла или жира и т.п., а также гранулирование полученной смеси. В JP-B-59-10,780 предложен другой способ, который предусматривает диспергирование от 30 до 50 мас. % биологически активного вещества в защитном веществе, состоящем из от 10 до 35 мас.% соли алифатической монокарбоновой кислоты, имеющей от 14 до 22 атомов углерода, или рицинолеиновой кислоты и остальной части, которая состоит из алифатической монокарбоновой кислоты, имеющей от 14 до 22 атомов углерода, рицинолеиновой кислоты, отвержденного масла или жира и т.д.
В качестве одного из способов покрытия биологически активного вещества гидрофобным защитным веществом в JP-A-63-317,053 предложен, например, способ, включающий покрытие биологически активного вещества защитным агентом, состоящим из алифатической монокарбоновой кислоты, имеющей 12-24 атомов углерода, отвержденного масла или жира, лецитина и сложного алифатического эфира глицерина.
В качестве способов, предусматривающих покрытие биологически активного вещества защитным веществом, чувствительным к кислоте, JP-A-54-46,823 предлагает, например, способ, который выполняет покрытие композицией, содержащей основное макромолекулярное вещество, образующее пленку, и в JP-A-04-217,625 предложен способ, заключающийся в нанесении распылением зеина в форме водной эмульсии или водной дисперсии.
Однако способы, включающие диспергирование биологически активного вещества в защитном веществе, требуют, чтобы содержание биологически активного вещества было значительно понижено с учетом способности защиты, поскольку биологически активное вещество находится близко к поверхности частиц. Учитывая то, что биологически активное вещество при растворении в воде имеет время удерживания в рубце от 10 ч до нескольких дней, эти способы не могут обеспечить необходимую защиту.
Был предложен также способ, заключающийся в покрытии кристаллов, содержащих биологически активное вещество, макромолекулярным веществом, чувствительным к кислоте, или гидрофобным защитным веществом. Однако, с точки зрения производства комплексного корма, который в последние годы популярен, продукт этого способа не может называться аддитивной композицией общего назначения для корма, поскольку гранулы и/или их покрытия подвергаются разрыву при механическом воздействии в процессе смешивания кристаллов с другой кормовой композицией и грануляции полученной смеси, в результате чего нарушается стабильность удерживания в рубце жвачного животного.
Для того чтобы кормовая добавка могла выдержать такое смешивание с другой кормовой композицией или упомянутое выше гранулирование, она должна быть в форме порошка или однородных гранул, обладающих свойством, препятствующим высвобождению биологически активного вещества в рубце и в то же время допускающим выделение растворением биологически активного вещества в сычуге и последующих пищеварительных органах. Однако при применении основной аминокислоты с целью улучшения питательных свойств корма, кроме фосфовольфраматов (солей фосфорно-вольфрамовой кислоты), не было найдено ни одного вещества, содержащего основную аминокислоту в виде порошка или однородных гранул, демонстрирующего нейтральность, нерастворимость и растворимость в кислотах.
В JP-A-63-98,357 описана аддитивная композиция, которая покрыта солью основной аминокислоты и кислого фосфата и применяется в корме для жвачных млекопитающих. Соль основной аминокислоты, которая представляет собой кислую соль щелочноземельного металла фосфорной кислоты по изобретению указанной патентной публикации, является веществом, аналогичным комплексной соли фосфорной кислоты - аминокислоты данного изобретения. В этой соли основной аминокислоты с кислой солью щелочноземельного металла фосфорной кислоты по указанному изобретению молярное соотношение фосфорной кислоты, щелочноземельного металла и основной аминокислоты составляет 1:0,5:1:2. Таким образом, эта соль отличается от комплексной соли фосфорной кислоты, соли щелочноземельного металла и основной аминокислоты, которая является предметом настоящего изобретения. Соль основной аминокислоты с солью щелочноземельного металла кислой фосфорной кислоты согласно вышеуказанному изобретению с течением времени подвергается разложению в воде и дает вторичный кислый фосфат щелочноземельного металла и первичный кислый фосфат основной аминокислоты или вторичный кислый фосфат основной аминокислоты. Поскольку фосфат основной аминокислоты проявляет чрезвычайно высокую растворимость в воде, он фактически нейтрален и растворим в воде, с точки зрения растворимости основной аминокислоты.
Фосфорная кислота образует различные соли с щелочноземельными металлами. Некоторые из этих солей нерастворимы в нейтральной и щелочной воде и растворимы в подкисленной воде. Например, известно, что вторичный кислый фосфат кальция, третичный фосфат магния и другие соли обладают способностью осаждаться в виде "накипи" и вызывать механические неисправности в устройствах оборудования ферментационной промышленности, которая в изобилии использует фосфорную кислоту. Фосфорнокислая соль магния и аммония обладает такой же склонностью. Комплексная соль, которая состоит из 1 моль фосфорной кислоты, 1 моль щелочноземельного металла и 1 моль основной аминокислоты вследствие замещения иона аммония как основного иона эквивалентной основной аминокислотой и третичной фосфорной кислотой и/или вторичным кислым фосфатом, состоящая из 1-1.45 моль щелочноземельного металла и 1-0.05 моль основной аминокислоты на 1 моль фосфорной кислоты, до сих пор не была известна. Комплексная соль фосфорной кислоты - аминокислоты, которая представляет собой соль щелочноземельного металла конденсированной фосфорной кислоты и метафосфорной кислоты, содержащая основную аминокислоту и щелочноземельный металл в соотношении 0,02-0,3:0,7-0,98, до настоящего времени была не известна.
Задача, которую ставит изобретение, заключается в разработке композиции, содержащей основную аминокислоту с учетом экономии и безопасности, которая не растворяется в первом отделе желудка, композиции, из которой растворяется основная аминокислота в четвертом отделе желудка жвачного млекопитающего и последующих органах пищеварительной системы, и позволяющая эффективное переваривание и всасывание отделенной основной аминокислоты, причем эта композиция находится в форме порошка или однородных гранул.
Описание изобретения
Авторы данного изобретения после интенсивных поисков с целью выполнения указанной выше задачи выявили, что комплексная соль, состоящая из основной аминокислоты, щелочноземельного металла и фосфорной кислоты, допускает форму порошка, не растворимого в нейтральной и щелочной воде и растворимого в кислой воде, и соединяет в себе свойства нерастворимости в рубце жвачного животного и отличной растворимости в сычуге и последующих органах пищеварения. Результатом этого явилось настоящее изобретение.
Более конкретно, изобретение касается разработки комплексной соли фосфорной кислоты - аминокислоты, состоящей из основной аминокислоты, щелочноземельного металла и ортофосфорной кислоты, представленной следующей общей формулой (1):
RaMbHcPO4 · nH2O, (1)
(где R обозначает катион водорода основной аминокислоты, М - щелочноземельный металл, a - цифровую величину в пределах от 0,05 до 1, b - цифровую величину в пределах от 1 до 1,47, c - цифровую величину в пределах от 0 до 0,3, при условии, что a, b и c вместе соответствуют выражению a + (2 х b) + c = 3 и n соответствует цифровой величине в пределах от 0 до 10),
состоящей из основной аминокислоты, щелочноземельного металла и конденсированной фосфорной кислоты, как представлено следующей общей формулой (2):
RaMbHcPO4(PO3) · nH2O, (2)
(где R обозначает катион водорода основной аминокислоты, M - щелочноземельный металл, a - цифровую величину в пределах от 0,02 х (m + 3) до 0,3 х (m + 3), b - цифровую величину в пределах от 0,35 х (m + 3) до 0,49 х (m + 3), c - цифровую величину от 0 до 0,2 х (m + 3), при условии, что a, b и c вместе соответствуют выражению a + (2 х b) + c = m + 3, m соответствует целому числу в пределах от 0 до 10), или
состоящей из основной аминокислоты, щелочноземельного металла и метафосфорной кислоты, как представлено следующей общей формулой (3):
RaMbHc(PO3) · nH2O, (3)
(где R обозначает катион водорода основной аминокислоты, М - щелочноземельный металл, a - цифровую величину в пределах от 0,02 х m до 0,3 х m, b - цифровую величину в пределах от 0,35 х m до 0,49 х m, c - цифровую величину в пределах от 0 до 0,2 х m, при условии, что a, b и c вместе соответствуют выражению a + (2 х b) + c = m, m - соответствует целому числу в пределах от 3 до 50 и n соответствует целому числу в пределах от 0 до 20), т.е. комплексной соли фосфорной кислоты - аминокислоты, не растворимой в нейтральном или щелочном водном растворе и растворимой в кислом (подкисленном) водном растворе, аддитивной композиции для применения в корме жвачных млекопитающих, отличающейся тем, что она содержит комплексную соль фосфорной кислоты - аминокислоты и обладает способностью образовывать однородные гранулы, а также способа получения аддитивной композиции.
Далее предлагается подробное описание изобретения.
Краткое описание чертежей
Фиг. 1 показывает рентгеновскую порошковую дифрактограмму нового комплексного соединения фосфорной кислоты аминокислоты по изобретению, полученного по примеру 1.
Фиг. 2 представляет собой рентгеновскую порошковую дифрактограмму нового комплексного соединения фосфорной кислоты - аминокислоты по изобретению, полученного по примеру 3.
Фиг. 3 представляет собой рентгеновскую порошковую дифрактограмму нового комплексного соединения фосфорной кислоты - аминокислоты по изобретению, полученного по примеру 13.
Фиг. 4 представляет собой рентгеновскую порошковую дифрактограмму нового комплексного соединения фосфорной кислоты - аминокислоты по изобретению, полученного по примеру 14.
Фиг. 5 представляет собой рентгеновскую порошковую дифрактограмму нового комплексного соединения фосфорной кислоты - аминокислоты по изобретению, полученного по примеру 17.
Подробное описание изобретения
В качестве конкретных примеров фосфорной кислоты, используемой в этом изобретении, кроме ортофосфорной кислоты можно указать конденсированные фосфорные кислоты, такие, как дифосфорная (пирофосфорная) кислота, триполифосфорная кислота, тетраполифосфорная кислоты и другие полифосфорные кислоты, триметафосфорная кислота, тетраметафосфорная кислота, гексаметафосфорная кислота и другие метафосфорные кислоты и крепкая фосфорная кислота. Соли ортофосфорной кислоты, пирофосфорной кислоты, триполифосфорной, тетраполифосфорной, триметафосфорной, гексаметафосфорной и других метафосфорных кислот хороши с точки зрения растворимости и особенно удобны в применении.
Основные аминокислоты, которые применимы в этом изобретении, включают природные основные аминокислоты, такие, как лизин, аргинин и орнитин и их основные производные, а также, например, основные производные нейтральных аминокислот. Можно использовать один член или смесь двух или нескольких членов, выбранных из группы основных аминокислот, перечисленных выше. Более конкретно, для использования здесь пригодны природные основные аминокислоты, такие, как лизин, аргинин и орнитин, амиды и эфиры аминокислот, такие, как метионин, триптофан и треонин, и основные производные, такие, как содержащие основные аминокислоты пептиды.
Щелочноземельные металлы, которые используют в этом изобретении, включают магний, кальций, стронций и барий. С точки зрения биологической безопасности и приемлемости предпочтительны соли магния и кальция.
Комплексная соль фосфорной кислоты - аминокислоты по настоящему изобретению представляет собой комплексную соль, которую получают в виде осажденных кристаллов, когда основную аминокислоту, щелочноземельный металл и фосфорную кислоту заставляют сосуществовать в относительно высоких концентрациях в водном растворе в условиях от нейтральных до щелочных. Соль можно грубо разделить на четыре типа комплексной соли фосфорной кислоты - аминокислоты, в зависимости от наличия или отсутствия конденсации фосфорной кислоты, вида конденсации и в случае ортофосфорной кислоты от соотношения эквивалентных масс основной аминокислоты и щелочноземельного металла.
Первый тип комплексной соли представляет собой аминокислотную комплексную соль, которая состоит из трех эквивалентных масс фосфорной кислоты, которая является ортофосфорной кислотой, одной эквивалентной массы основной аминокислоты и двух эквивалентных масс щелочноземельного металла. Второй тип комплексной соли - это комплексная соль фосфорной кислоты - аминокислоты, которая состоит из 3,0 эквивалентных масс ортофосфорной кислоты, 0,05-0,8 эквивалентной массы основной аминокислоты, 2,2-2,94 эквивалентной массы щелочноземельного металла и 0-0,3 эквивалентной массы радикала водорода. В качестве щелочноземельного металла для первого и второго типов комплексной соли фосфорной кислоты - аминокислоты наилучшим выбором является соль, целиком состоящая из соли магния, и смешанная соль магния и кальция, хотя отдельные соли магния и кальция также подходят. Третий тип комплексной соли фосфорной кислоты - аминокислоты представляет собой комплекс, который использует конденсированную фосфорную кислоту в качестве фосфорной кислоты, и состоит из конденсированной фосфорной кислоты, основной аминокислоты, щелочноземельного металла и иона водорода в соотношении эквивалентных масс 100:2-30:70-98:0-20. Четвертый тип комплексной соли фосфорной кислоты - аминокислоты - это комплексная соль, в которой используется в качестве фосфорной кислоты метафосфорная кислота, и состоит она из метофосфорной кислоты, основной аминокислоты, щелочноземельного металла и иона водорода в соотношении эквивалентных масс 100:2-30:70-98:0-20. В качестве щелочноземельного металла для третьего и четвертого типов комплексной соли фосфорной кислоты - аминокислоты наилучшим выбором является соль, целиком состоящая из соли кальция, и смешанная соль магния и кальция, хотя отдельные соли магния и кальция также подходят.
Способ получения комплексной соли первого и второго типов с использованием ортофосфорной кислоты не является решающим, если продукты не растворимы в нейтральном или щелочном водном растворах и растворимы в кислом водном растворе. Для получения предлагаются следующие четыре способа.
По первому способу предлагается получение диспергированием вторичного кислого фосфата щелочноземельного металла в основном водном растворе избыточного количества основной аминокислоты, нагреванием полученной дисперсии и промыванием осадка, образованного в результате в дисперсии. В качестве конкретного примера этого способа можно предложить способ, который предусматривает добавление такого вторичного кислого фосфата щелочноземельного металла в виде димагнийфосфата к избытку основного концентрированного водного раствора основной аминокислоты, подготовленного обработкой ионообменной смолой, и нагревание и перемешивание их до образования нужной смеси. Вторичный кислый фосфат щелочноземельного металла в смешанном растворе постепенно гасят, и комплексная соль фосфорной кислоты - аминокислоты образуется в виде осадка. После выделения осадка отделением твердой фазы от жидкой, промывания водой для удаления избытка основной аминокислоты и последующего высушивания получают аминокислотную комплексную соль, которая состоит из трех эквивалентных масс ортофосфорной кислоты, одной эквивалентной массы основной аминокислоты и двух эквивалентных масс щелочноземельного металла по вышеупомянутой общей формуле (1), или композицию комплексной соли фосфорной кислоты - аминокислоты с такой комплексной солью в качестве основного ее компонента. Диапазон гидратной воды может быть широким от ангидрида до декагидрата. При нормальных условиях продукт получают в виде моногидрата или дигидрата.
По второму способу предлагается получать смешиванием нейтрального водного раствора щелочноземельного металла и либо ортофосфорной кислоты, либо соли щелочного металла ортофосфорной кислоты в соотношении при эквивалентных масс 2,9-2,0:3,0 в основном водном растворе избытка основной аминокислоты и промыванием образованного в результате осадка. В качестве конкретного примера этого способа можно привести способ, который предусматривает добавление трех эквивалентных масс ортофосфорной кислоты и/или соли щелочного металла ортофосфорной кислоты не менее чем к трем эквивалентным массам основного концентрированного водного раствора основной аминокислоты с образованием высококонцентрированного раствора третичного фосфата, затем добавление 2,9-2,0 эквивалентных масс концентрированного водного раствора такой нейтральной соли щелочноземельного металла, как хлорид магния или сульфат магния, перемешивание до образования нужной смеси, выделение образованного осадка отделением твердожидким от жидкой фазы и промывание выделенного осадка водой для удаления избыточной основной аминокислоты, а затем высушивание этого осадка. Этот способ дает получение комплексной соли фосфорной кислоты - аминокислоты, представленной вышеупомянутой общей формулой (1). По этому способу в зависимости от соотношения эквивалентных масс соли щелочноземельного металла и фосфорной кислоты, скорости добавления и вида затравочных кристаллов в ходе добавления получают композиции комплексной соли фосфорной кислоты - аминокислоты с первым и вторым типами комплексной соли, упомянутыми выше в качестве основных компонентов.
Композицию комплексной соли фосфорной кислоты аминокислоты с первым типом комплексной соли в качестве основного компонента получают, если добавляемое количество нейтрального раствора соли щелочноземельного металла близко к двум эквивалентным массам при трех эквивалентных массах ортофосфорной кислоты и/или соли щелочного металла ортофосфорной кислоты, и нейтральный солевой раствор щелочноземельного металла постепенно добавляют в присутствии первого типа комплексной соли в виде затравочных кристаллов. И, наоборот, второй тип комплексной соли или композицию комплексной соли фосфорной кислоты - аминокислоты с такой комплексной солью в качестве основного ее компонента получают, если добавляемое количество нейтрального раствора соли щелочноземельного металла близко к 2,8 эквивалентным массам при 3,0 эквивалентных массах ортофосфорной кислоты, и добавление производят быстро. Альтернативно получение можно провести с количеством щелочноземельного металла в пределах от 2,94 до 2,0 эквивалентных масс. Этим способом можно получить комплексные соли фосфорной кислоты - аминокислоты вышеуказанной общей формулы (1) с вариацией a) в пределах 0,05-1, вариацией b) в пределах 1-1,47, вариацией c) в пределах 0-0,3 и вариацией n) от 0 до 10.
Третий способ предусматривает получение добавлением 2,9-2,0 эквивалентных масс гидроксида щелочноземельного металла и/или оксида щелочноземельного металла к раствору первичного кислого фосфата основной аминокислоты, смешиванием их и промыванием образованного таким образом осадка. В качестве конкретного примера этого способа можно привести способ, который включает в себя смешивание 0,7-1,4 эквивалентных масс основного концентрированного водного раствора основной аминокислоты и трех эквивалентных масс ортофосфорной кислоты до нужной нейтрализации с образованием концентрированного водного раствора с первичным кислым фосфатом основной аминокислоты в качестве его основного компонента, добавление к этому раствору 2,9-2,0 эквивалентных масс такого гидроксида щелочноземельного металла, как гидроксид магния или гидроксид кальция, и/или такого оксида щелочноземельного металла, как оксид магния или оксид кальция в форме водной дисперсии, и их смешивание. Добавленный гидроксид щелочноземельного металла и/или оксид щелочноземельного металла подвергают постепенному гашению, и в виде осадка образуется комплексная соль фосфорной кислоты - аминокислоты. В конечном итоге эту комплексную соль фосфорной кислоты - аминокислоты получают выделением этого осадка путем отделения твердой фазы от жидкой, промыванием выделенного осадка водой до удаления избытка основной аминокислоты и высушиванием остатка после промывания. Этим способом получают комплексную соль фосфорной кислоты - аминокислоты, представленную общей формулой (1). По этому способу в зависимости от соотношения эквивалентных масс соли щелочноземельного металла и фосфорной кислоты и вида затравочных кристаллов во время добавления получают композиции комплексной соли фосфорной кислоты - аминокислоты с первым и вторым типами комплексной соли, указанными выше, в качестве основных компонентов.
Аналогичным образом по третьему способу первый тип комплексной соли или композицию комплексной соли фосфорной кислоты - аминокислоты с такой комплексной солью в качестве основного компонента получают, если количество гидроксида щелочноземельного металла и/или оксида щелочноземельного металла близко к двум эквивалентным массам при трех эквивалентных массах ортофосфорной кислоты, и нейтральный солевой раствор щелочноземельного металла добавляют постепенно в присутствии первого типа комплексной соли в виде затравочных кристаллов. И, наоборот, второй тип комплексной соли или композиции комплексной соли фосфорной кислоты - аминокислоты с такой комплексной солью в качестве ее основного компонента получают, если количество добавляемого нейтрального солевого раствора щелочноземельного металла близко к 2,8 эквивалентной массы при 3,0 эквивалентных массах ортофосфорной кислоты, и добавление делается в присутствии второго типа комплексной соли в качестве затравочных кристаллов. Добавлением к водному раствору первичного кислого фосфата основной аминокислоты 2,94-2,0 эквивалентных масс гидроксида щелочноземельного металла и/или оксида щелочноземельного металла при 3,0 эквивалентных массах ортофосфорной кислоты, смешиванием их и промыванием образованного осадка можно получить комплексные соли фосфорной кислоты - аминокислоты вышеупомянутой общей формулы (1) с вариацией a) в пределах от 0,05 до 1, вариацией b) в пределах от 1 до 1,47, вариацией c) в пределах от 0 до 0,3 и вариацией n) от 0 до 10.
По четвертому способу осуществляют получение путем смешивания основного водного раствора основной аминокислоты и ортофосфорной кислоты с соотношением эквивалентных масс от 0,05 до 0,8:3,0 с образованием нейтрализованного раствора, добавлением к нейтрализованному раствору 2,94-2,2 эквивалентной массы гидроксида щелочноземельного металла, смешиванием их и нагреванием и высушиванием полученной смеси. В качестве конкретного примера этого способа можно привести способ, предусматривающий смешивание 0,05-0,8 эквивалентной массы основного концентрированного водного раствора основной аминокислоты и 3,0 эквивалентных масс ортофосфорной кислоты до нейтрализации с образованием смешанного концентрированного водного раствора первичного кислого фосфата и ортофосфорной кислоты, добавление к этому раствору 2,94-2,2 эквивалентной массы такого гидроксида щелочноземельного металла, как гидроксид магния или гидроксид кальция, в форме водной дисперсии и смешивание их. Добавленный гидроксид щелочноземельного металла претерпевает постепенное погашение, и в виде осадка образуется комплексная соль фосфорной кислоты - аминокислоты. Комплексную соль фосфорной кислоты аминокислоты, представленную вышеупомянутой общей формулой (1), получают высушиванием осадка в его неизмененной форме. Этим способом получают второй тип комплексной соли или композицию комплексной соли фосфорной кислоты - аминокислоты с такой комплексной солью в качестве основного компонента. Смешиванием трех эквивалентных масс ортофосфорной кислоты с 0,05-0,8 эквивалентной массы основной аминокислоты в виде основного водного раствора и 2,94-2,2 эквивалентной массы гидроксида щелочноземельного металла и/или оксида щелочноземельного металла с последующим нагреванием и высушиванием полученной смеси можно получить комплексные соли фосфорной кислоты - аминокислоты вышеупомянутой общей формулы (1) с вариацией a) в пределах от 0,05 до 0,8, вариацией b) в пределах от 1,1 до 1,47, вариацией c) в пределах от 0 до 0,3 и вариацией n) в пределах от 0 до 10.
Эти четыре способа обладают тем общим признаком, что основной концентрированный водный раствор основной аминокислоты используют в качестве исходного материала и комплексная соль аминокислоты образуется вследствие реакции, использующей основную аминокислоту в относительно высокой концентрации. В этом изобретении нужная концентрация основной аминокислоты находится в пределах от 10 до 60 массовых частей на 100 массовых частей общего количества воды, присутствующей в реакционной системе в случае второго способа, по которому выбирают наивысшую концентрацию, и в пределах от 3 до 20 массовых частей на 100 массовых частей общего количества воды в случае четвертого способа, по которому выбирают наименьшую концентрацию.
Эти четыре способа можно использовать в подходящем сочетании. В качестве конкретных примеров сочетания можно привести способ, включающий добавление концентрированного водного раствора нейтральной соли ортофосфорной кислоты и/или соли щелочного металла ортофосфорной кислоты в подходящем количестве к реакционному раствору с комплексной солью фосфорной кислоты - аминокислоты, образованной в виде осадка первым способом, описанным выше, перемешивание их для получения нужной смеси, и нагревание полученной смеси, что вынуждает нейтральную соль реагировать с избыточным количеством основной аминокислоты, все еще остающейся в реакционном растворе, и способ, включающий добавление гидроксида щелочноземельного металла в подходящем количестве к реакционному раствору с комплексной солью фосфорной кислоты - аминокислоты, образованной в виде осадка вторым способом, описанным выше, что вынуждает, таким образом, гидроксид реагировать с избыточными количествами основной аминокислоты и фосфорной кислоты, все еще остающимися в реакционном растворе. Комплексные соли фосфорной кислоты - аминокислоты, которые получают этими способами, представляют собой смеси первого типа комплексной соли второго типа комплексной соли, упомянутых выше. Эти способы получения и условия реакции влияют на соотношение сочетания таких смесей.
Способ получения комплексной соли фосфорной кислоты - аминокислоты третьего и четвертого типов с использованием конденсированной фосфорной кислоты и метафосфорной кислоты отдельно в качестве фосфорной кислоты не является решающим, если продукты не растворимы в нейтральном или щелочном водном растворе и растворимы в кислотном водном растворе. Способ почти тот же, что и способ получения комплексной соли с использованием ортофосфорной кислоты, за исключением того, что в качестве фосфорной кислоты соответственно применяются конденсированная фосфорная кислота и метафосфорная кислота. Следующие три способа предлагают нужный выбор.
Первый способ получения осуществляют путем добавления к основному водному раствору (полученному в результате добавления фосфорной кислоты и/или соли щелочного металла фосфорной кислоты к основному водному раствору избыточного количества основной аминокислота) 70-130 эквивалентных масс (на 100 эквивалентных масс фосфорной кислоты) нейтрального водного раствора соли щелочноземельного металла, промыванием образованного осадка, и высушиванием промытого осадка. Конкретным примером этого способа является способ, включающий добавление 70-130 эквивалентных масс нейтрального водного раствора такого щелочноземельного металла, как хлорид магния, сульфат магния или хлорид кальция к 100 эквивалентным массам фосфорной кислоты, выбранной из дифосфорной (пирофосфорной) кислоты, триполифосфорной кислоты, тетраполифосфорной кислоты и других полифосфорных кислот, триметафосфорной кислоты, тетраметафосфорной кислоты, гексаметафосфорной кислоты и других метафосфорных кислот, и/или соли щелочного металла фосфорной кислоты в основном водном растворе избыточного количества основной аминокислоты, полученной обработкой ионообменной смолой, затем выдерживание реакционной смеси для протекания взаимодействия и образования осадка, промывание этого осадка большим количеством воды и высушивание промытого осадка. Этим способом получают комплексную соль фосфорной кислоты - аминокислоты, представленную общей формулой (2) или общей формулой (3), приведенными выше, или композицию комплексной соли, содержащую комплексную соль в качестве основного компонента.
Второй способ получения комплексной соли осуществляют путем смешивания 100 эквивалентных масс фосфорной кислоты с 2-50 эквивалентными массами основной аминокислоты в виде основного водного раствора и 70-130 эквивалентными массами гидроксида щелочноземельного металла и/или оксида щелочноземельного металла, что приводит к образованию осадка, и промыванием осадка. Конкретным примером этого способа является способ, включающий смешивание 2-50 эквивалентных масс основного водного раствора избыточного количества основной аминокислоты, полученной обработкой ионообменной смолой, со 100 эквивалентными массами фосфорной кислоты, выбранной из пирофосфорной кислоты, триполифосфорной, тетраполифосфорной, и других полифосфорных кислот, триметафосфорной кислоты, тетраметафосфорной, гексаметафосфорной и других метафосфорных кислот, и со 70-130 эквивалентными массами гидроксида и/или оксида такого щелочноземельного металла, таких как гидроксид кальция, гидроксид магния, оксид кальция или оксид магния, затем выдерживание реакционной смеси для протекания взаимодействия и образования осадка, промывание и высушивание. Этим способом получают комплексную соль фосфорной кислоты - аминокислоты, представленную общей формулой (2) или общей формулой (3), или композицию комплексной соли, содержащую комплексную соль в качестве основного компонента.
Третий способ получения комплексной соли осуществляют путем смешивания 100 эквивалентных масс фосфорной кислоты с 2-30 эквивалентными массами основной аминокислоты в виде основного водного раствора и 70-130 эквивалентными массами оксида щелочноземельного металла и/или гидроксида щелочноземельного металла с последующим нагреванием и высушиванием полученной смеси. Конкретным примером этого способа является способ, включающий смешивание 2-50 эквивалентных масс основного водного раствора избыточного количества основной аминокислоты, полученной обработкой ионообменной смолой, со 100 эквивалентными массами фосфорной кислоты, выбранной из дифосфорной (пирофосфорной) кислоты, триполифосфорной, тетраполифосфорной и других полифосфорных кислот, триметафосфорной кислоты, тетраметафосфорной, гексаметафосфорной и других метафосфорных кислот, и 70-130 эквивалентными массами гидроксида и/или оксида щелочноземельного металла, такого как гидроксид кальция, гидроксид магния, оксид кальция или оксид магния, и нагревание и смешивание полученной смеси. Этим способом получают комплексную соль - фосфорной кислоты - аминокислоты, представленную общей формулой (2) или общей формулой (3), приведенными выше, или композицию комплексной соли с такой комплексной солью в качестве основного компонента. Смешиванием 100 эквивалентных масс по меньшей мере одного вещества, выбранного из конденсированной фосфорной кислоты, метафосфорной кислоты, солей щелочных металлов конденсированной фосфорной кислоты и солей щелочных металлов метафосфорной кислоты, со 70-130 эквивалентными массами нейтрального водного раствора щелочноземельного металла в основном водном растворе избыточного количества основной аминокислоты и затем промыванием образованного осадка можно получить комплексные соли фосфорной кислоты - аминокислоты вышеприведенной общей формулы (2) или (3) с вариацией a), b) и c) в соответствующих пределах от 0,02 до 0,3, от 0,35 до 0,49 и от 0 до 0,2 и с вариацией n) от 0 до 20.
Третий тип и четвертый типы комплексной соли по этому изобретению можно получить независимо один от другого. Способ, с помощью которого получают смешанную композицию третьего и четвертого типов комплексной соли с применением конденсированной фосфорной кислоты и метафосфорной кислоты в качестве исходных материалов либо одновременно, либо смешанных заранее, может быть выбран как подходящий способ. Смешиванием 100 эквивалентных масс конденсированной фосфорной кислоты и/или метафосфорной кислоты с 2-50 эквивалентными массами основной аминокислоты в виде основного водного раствора и 70-130 эквивалентными массами гидроксида щелочноземельного металла и/или оксида щелочноземельного металла и затем промыванием образованного осадка можно получить комплексные соли фосфорной кислоты - аминокислоты вышеприведенной общей формулы (2) или (3) с разными величинами a), b) и c) в соответствующих пределах от 0,02 до 0,3, от 0,35 до 0,49 и от 0 до 0,2 и величинами n) от 0 до 20.
Кроме способа получения комплексной соли первого типов и второго типа и комплексной соли третьего типа и четвертого типа, независимо друг от друга, можно выбрать способ получения смешанной композиции первого-четвертого типов комплексной соли, с использованием соответствующих видов фосфорной кислоты в качестве исходных материалов либо одновременно, либо приготовленных в смеси заранее. В качестве приемлемых способов можно указать способ, по которому образуется третий тип и/или четвертый тип комплексной соли путем получения реакционного раствора, содержащего первый тип и второй тип комплексной соли, предварительно образованной, и добавления конденсированной фосфорной кислоты и/или метафосфорной кислоты и щелочноземельного металла к реакционному раствору, и способ, по которому получают смешанную композицию первого-четвертого типов комплексной соли путем получения реакционного раствора, содержащего композицию комплексной соли третьего и четвертого типа, полученных заранее, и добавлением ортофосфорной кислоты и щелочноземельного металла к реакционному раствору с образованием первого типа и/или второго типа комплексной соли, более конкретно, комплексные соли фосфорной кислоты - аминокислоты вышеприведенной общей формулы (2) или (3) при различных значениях a), b) и c) в пределах от 0,02 до 0,3, от 0,35 до 0,49 и от 0 до 0,2, соответственно и значениях n) в пределах от 0 до 20.
Можно получить смешиванием 100 эквивалентных масс конденсированной фосфорной кислоты и/или метафосфорной кислоты с 2-30 эквивалентными массами основной аминокислоты в виде основного водного раствора с получением раствора, смешиванием этого раствора с 70-130 эквивалентными массами гидроксида щелочноземельного металла и/или оксида щелочноземельного металла с последующим нагреванием и высушиванием полученной смеси.
Четыре вида комплексной соли, указанные выше, можно четко отличить один от другого по степени конденсации фосфорной кислоты, соотношению сочетания основной аминокислоты и щелочноземельного металла и при помощи анализа рентгеновской порошковой дифракции. В спектре рентгеновской порошковой дифракции с применением Cu K-α-излучения первый тип комплексной соли показывает основные пики каждый с 2 θ при приблизительно 3,7o, приблизительно 7,4o, приблизительно 18,5o, приблизительно 18,8o, приблизительно 20,7o, приблизительно 22,2o, приблизительно 29,7o и приблизительно 32,3o, и второй тип комплексной соли показывает основные пики при приблизительно 6,0-6,5o, приблизительно 7,4-7,7o, приблизительно 15,6o, приблизительно 28,2o и приблизительно 32,5o. Третий тип и четвертый тип комплексной соли не показывают четкого пика. Они показывают небольшой подъем или очень небольшой пик на линии фона 2 θ в диапазоне приблизительно 25-35o.
Из четырех типов комплексной соли, указанных выше, первый тип комплексной соли при использовании лизина в качестве основной аминокислоты и магния в качестве щелочноземельного металла показывает очень острые пики в рентгеновской порошковой дифракции, упомянутой выше. Этот факт указывает на то, что это комплексная соль, обладающая высоко удовлетворительной кристалличностью. Анализ состава выявил, что эта комплексная соль состоит из 1 моль ортофосфорной кислоты, 1 моль лизина и 1 моль магния и 2 моль гидратной воды в нормальных сухих условиях, хотя количество гидратной воды различно в зависимости от состояния сухости. Комплексная соль такого состава до сих пор была неизвестна.
Из четырех видов комплексной соли, упомянутых выше, у второго типа комплексной соли, использующей лизин в качестве основной аминокислоты и магний в качестве щелочноземельного металла, впервые было выявлено наличие самой стабильной кристаллической композиции. По наблюдениям, при тепловой обработке второго типа соли в течение длительного времени в основном водном растворе, содержащем лизин в относительно высокой концентрации, рентгеновская порошковая дифракция термообработанной комплексной соли показывает особенно острые пики в сравнении с пиками комплексной соли до термообработки. Кроме того, было отмечено, что упомянутая термообработка дает тот же результат с несколькими образцами второго типа комплексной соли, содержащей лизин, фосфорную кислоту и магний в различных концентрациях, и что термообработанные образцы содержат лизин, фосфорную кислоту и магний в неизмененных концентрациях. Этот факт указывает на наличие самой стабильной кристаллической композиции во втором типе комплексной соли. В кристаллическую композицию входят лизин в качестве основной аминокислоты, магний в качестве щелочноземельного металла и ортофосфорная кислота в качестве фосфорной кислоты, она содержит катион водорода лизина в концентрации порядка 0,21-0,25 моль, магний в концентрации порядка 1,325-1,395 моль, ион водорода от 0 до 0,1 моль на 1 моль ортофосфорной кислоты и гидратную воду от 0 до 5 моль. Также было выявлено, что гидратная вода легко меняет свое содержание в зависимости от условия сухости. Комплексная соль с таким составом до сих пор была неизвестна.
Хотя четыре вида комплексной соли показывают нерастворимость в нейтральной и щелочной воде, компоненты их основной аминокислоты отличаются друг от друга характеристикой растворимости. А именно, первый тип комплексной соли при дисперсии в нейтральной воде обеспечивает полное постепенное растворение компонента основной аминокислоты, в то время как второй - четвертый типы соли очень редко дают растворение в нейтральной воде основных аминокислотных компонентов.
В случае второго, третьего и четвертого типов комплексных солей или композиций комплексных солей фосфорной кислоты - аминокислоты, в состав которых входят эти комплексные соли в качестве главных компонентов, полученные в конечном итоге кристаллические порошки композиций комплексной соли, даже при применении в немодифицированной форме, обладают нерастворимостью в нейтральной - щелочной воде и растворимостью в кислой воде, и могут применяться в качестве аддитивных композиций в порошковых кормах для жвачных млекопитающих, композиций, которые стабильны в рубце, но способны выделять основную аминокислоту в четвертом отделе желудка и последующих органах пищеварения.
И, наоборот, в случае первого типа комплексной соли, указанного выше, или композиции комплексной соли фосфорной кислоты - аминокислоты, в состава которой входит эта комплексная соль в качестве главного компонента, удобнее формовать комплексную соль или композицию в виде гранул с нужным диаметром частиц и снижать таким образом растворимость компонента основной аминокислоты в нейтральной или щелочной воде, чем применять комплексную соль или композицию в ее немодифицированной форме. Даже в этом случае, поскольку комплексная соль фосфорной кислоты - аминокислоты по этому изобретению обладает свойством растворимости в кислой воде, а ее гранулированный продукт свойством растворимости в четвертом отделе желудочка, независимо от ее состава, ее можно применять в качестве аддитивной композиции в порошковом корме для жвачных млекопитающих, поскольку она устойчива в рубце и может выделять основную аминокислоту в четвертом отделе желудка и последующих органах пищеварения.
В этом изобретении гранулы комплексной соли фосфорной кислоты - аминокислоты можно применять наиболее выгодно, если они имеют однородную гранулированную структуру. Выражение "однородные гранулы" здесь означает такие гранулы, фрагменты, которых при образовании гранул диаметром приблизительно 1-2 мм, сохраняют неизменно свой состав. Минимальные диаметры частиц, на которые разламываются гранулы при жевании жвачными, составляют около 1-2 мм. Если фрагменты гранул с размером частиц диаметром 1-2 мм имеют однородный состав, следовательно, гранулы, которые проходят процесс жевания, также должны иметь однородный состав. Если гранулы смешивают с другими кормовыми компонентами и затем таблетируют, на способность гранул растворять компонент основной аминокислоты не влияет каким-либо заметным образом такое динамическое воздействие.
Гранулирование комплексной соли фосфорной кислоты - аминокислоты по этому изобретению может осуществляться любым известным способом гранулирования без каких-либо ограничений с условием сохранения однородности, упомянутой выше. В качестве конкретных примеров способа, применение которого предпочтительно можно привести способ, включающий смешивание комплексной соли с приемлемым связующим веществом, и затем гранулирование полученной смеси такими методами, как методы экструзионной грануляции, прокатки, прессования или метод распыления расплава, который включает превращение комплексной соли в суспензию и сушку суспензии распылением, и метод, предусматривающий превращение комплексной соли в порошок, смешивание этого порошка со связующим веществом и гранулирование полученной смеси методом псевдоожиженного слоя или перемешиванием.
В качестве связующего вещества в случае композиций комплексной соли фосфорной кислоты - аминокислоты, имеющих второй - четвертый типы комплексной соли в качестве главных компонентов, можно применять любые общепринятые связующие вещества без особых ограничений. В качестве конкретных примеров можно указать водорастворимые связующие вещества, включающие водорастворимые полисахариды, такие, как крахмал, соли карбоксиметилцеллюлозы, альгинаты, метилцеллюлозу, этилцеллюлозу, гидроксипропилцеллюлозу, и соли крахмалгликолевой кислоты, водорастворимые белки, такие, как натриевая соль казеина, желатин и соевый белок, сахариды, такие, как мелассы, молочный сахар и декстрин, и синтетические макромолекулы, такие как полиметакрилаты, поливиниловые спирты и поливинилпирролидон, и гидрофобные связующие вещества, включающие натуральные воски, такие, как шеллак, канифоль, пчелиный воск, парафиновые воски, высшие жирные кислоты, такие, как цетанол и стеариновая кислота, масляные и жирные производные, такие, как соли металлов высших жирных кислот, животные и растительные масла и жиры, и отвержденные животные и растительные масла и жиры, неионные ПАВ, такие, как моностеарат глицерина, полусинтетические смолы и синтетические макромолекулы, такие, как ацетилцеллюлоза, поливинилацетат, эфирные смолы и кумароновая смолы. В случае комплексной соли фосфорной кислоты - аминокислоты первого типа соли в качестве главного компонента можно использовать любое из указанных здесь связующих веществ гидрофобного характера. Наиболее подходящий выбор составляют натуральные воски и относящиеся к маслам и жирам вещества, указанные выше.
Соотношение сочетания комплексной соли и связующего вещества в образовании гранул различно в зависимости от конкретного применяемого связующего вещества. В случае комплексной соли с первым типом соли в качестве главного компонента подходящим является соотношение порядка 30-350 массовых частей связующего агента на 100 массовых частей комплексной соли фосфорной кислоты - аминокислоты. В случае комплексной соли со вторым, третьим и четвертым типами комплексной соли в качестве главного компонента подходящим соотношением будет 0,1-50 массовых частей связующего агента на 100 массовых частей комплексной соли.
Диаметр частиц гранул, содержащих комплексную соль фосфорной кислоты - аминокислоты изобретения, особого значения не имеет. Средний диаметр частиц гранул не более 5 мм вполне достаточен и при этом качество корма значительно не страдает, а гранулы со средним размером частиц 2-0,2 мм наиболее приемлемы, поскольку они облегчают работу по смешиванию гранул с другими компонентами корма.
Гранулы, содержащие комплексную соль фосфорной кислоты - аминокислоты изобретения, могут включать другие добавки, кроме аминокислотной комплексной соли и связующего агента, которые вводят в процессе получения с целью регулировки удельного веса, повышения их прочности, улучшения растворимости в четвертом отделе желудка и улучшения способности обработки в процессе производства. Эти добавки выбираются из порошковых или восковых веществ. В качестве конкретных примеров добавок, которые используют для этого, можно привести такие неорганические вещества, как карбонаты, фосфаты и гидроксиды щелочноземельных металлов, тальк, бентонит, глина, мелко измельченный диоксид кремния и органические вещества, такие, как парафиновые воски, полиэтиленовый порошок, порошок жома, целлюлозный порошок и хитозан.
В гранулы, содержащие комплексную соль фосфорной кислоты - аминокислоты по данному изобретению, в ходе получения можно ввести другие биологически активные вещества, однородно распределенные в них, при условии, что их наличие не ухудшит устойчивости комплексной соли в рубце и растворимости в четвертом отделе желудка. Биологически активные вещества такого назначения включают различные хорошо известные питательные вещества и лекарства, такие, как, например, аминокислоты и их производные, гидрокси-гомологичные производные аминокислот, витамины и лекарства для животных. Приемлемо использование одного элемента или смеси из двух или нескольких элементов, выбранных из группы веществ, указанных выше.
В качестве конкретных примеров биологически активных веществ можно привести аминокислоты, такие, как метионин, триптофан и треонин, производные аминокислот, такие, как кальциевые соли N-ациламнокислоты и N-гидроксиметилметионина, гидрокси-гомологичные производные аминокислот, такие, как 2-гидрокси-4-метилмеркаптомасляная кислота и ее соли, крахмал, жирные кислоты и соли металлов жирных кислот в качестве источника калорий, витамины и вещества с функцией аналогичной витаминам, такие, как витамин A, ацетат витамина A, пальмитат витамина A, ряд витамина B, тиамин, тиамина гидрохлорид, рибофлавин, никотиновая кислота, амид никотиновой кислоты, пантотенат кальция, гидрохлорид пиридоксина, хлорид холина, цианокобаламин, биотин, фолиевая кислота, п-аминобензойная кислота, витамин D2, витамин D3 и витамин E, антибиотики типа тетрациклина, типа аминогликозида, типа макролида и полиэфирного типа, противопаразитарные средства, такие, как негфон, вермициды, такие, как пиперазин, и гормоны, такие, как эстроген, стилбестрол, гексестрол, гонтроген и гормон роста.
Примеры
Далее изобретение будет описано более конкретно со ссылкой на рабочие примеры и сравнительные эксперименты. Объем изобретения не ограничивается этими рабочими примерами.
Количество аминокислоты, содержащейся в качестве биологически активного вещества, и ее растворенное количество определяли жидкостной хроматографией, содержание воды методом весовых потерь путем высушивания (выдерживанием в вакууме в течение 3 ч при 120oC), и содержание кальция, магния и фосфора эмиссионным спектральным анализом 1PC (индуктивного сопряжения плазмы).
Растворимость в чистой воде
В колбу Эрленмейера объемом 200 мл помещали 1,00 г подготовленного образца и добавляли 100 мл очищенной воды. Полученный водный раствор подвергали ультразвуковой обработке при нормальной комнатной температуре в течение 10 мин. Раствор анализировали на основную аминокислоту, чтобы определить растворимость образца в очищенной воде.
Устойчивость по отношению к желудочному соку в первом отделе желудка
В колбу Эрленмейера объемом 300 мл помещали около 0,5 г подготовленного образца, к образцу добавляли 200 мл буферного раствора МакДугаллa* (буферный раствор, в состав которого входят следующие реагенты, растворенные в 1000 мл воды), эквивалентного желудочной жидкости в первом отделе желудка, и полученную смесь встряхивали при 39oC 24 ч. После завершения встряхивания смесь анализировали на основную аминокислоту, растворенную в ней, для определения путем расчета ее устойчивости по отношению к желудочному соку в первом отделе желудка.
*Бикарбонат натрия - 7,43 г
Додекагидрат динатрийфосфата - 7,00 г
Хлорид натрия - 0,34 г
Хлорид калия - 0,43 г
Гексагидрат хлорида магния - 0,10 г
Хлорид кальция - 0,05 г
Растворимость в растворе, эквивалентном желудочному соку в четвертом отделе желудка
В колбу Эрленмейера объемом 300 мл помещали около 0,5 г подготовленного образца, к этому образцу добавляли 200 мл буферного раствора* уксусной кислоты - фосфорной кислоты, эквивалентного желудочной жидкости в четвертом отделе желудка, и полученную смесь встряхивали при 39oC 1 ч. После встряхивания образец анализировали на основную аминокислоту, растворенную в жидкости, чтобы определить растворимость образца в растворе, эквивалентном желудочной жидкости в четвертом отделе желудка.
Буферный раствор* уксусной кислоты - фосфорной кислоты. Буферный раствор получали растворением следующих реагентов в 1000 мл воды и нейтрализацией полученного водного раствора соляной кислотой до pH 2,2.
Дигидрат динатрийфосфата - 1,95 г
Тригидрат ацетата натрия - 3,40 г
Пример 1
К 1300 г водного основного раствора L-лизина (концентрация 45 мас.%) добавляли 174,3 тригидрата вторичного фосфата магния. Смесь нагревали и перемешивали при 80oC 3 ч, гранулированные кристаллы тригидрата вторичного фосфата магния исчезали и в больших количествах появлялись мелкие кристаллы. Полученные таким образом кристаллы отделяли фильтрованием, промывали 1000 мл воды и затем высушивали при 60oC при пониженном давлении с получением 285 г белого кристаллического порошка. При помещении 1 г белого порошка в 100 мл очищенной воды и буферного раствора, эквивалентного желудочному соку в первом отделе желудка, и перемешивании он не проявлял никаких признаков растворения в этом растворе. Хотя белый порошок имел одну молекулу гидратной воды, ее содержание могло различаться в пределах от 0 до 10 молекул в зависимости от условий высушивания. При нормальных условиях сушки гидратная вода составляет одну или две молекулы. В следующих рабочих примерах рассматриваемые комплексные соли получают с таким же большим диапазоном гидратирования, как в настоящем примере.
Пример 2
К жидкости, полученной смешиванием 4386 г водного основного раствора L-лизина (концентрация 20 мас. %) с 231 г фосфорной кислоты (концентрация 85%) до нейтрализации, сразу добавляли раствор 493 г гептагидрата сульфата магния в 1000 мл воды. Образовавшийся гелевый осадок отделяли фильтрованием, промывали 12000 мл воды и затем высушивали при 60oC при пониженном давлении с получением 280 г белого порошка. При помещении 1 г белого порошка в 100 мл очищенной воды и буферного раствора, эквивалентного желудочной жидкости в первом отделе желудка, и перемешивании он не проявлял никаких признаков растворения.
Пример 3
Когда раствор, полученный диспергированием 291,7 г гидроксида магния в 1000 мл воды добавляли к жидкости, полученной смешиванием 650 г водного основного раствора L-лизина (концентрация 45 мас.%) с 461,2 г фосфорной кислоты (85% концентрации) и смешивали с ней до нейтрализации, происходила экзотермическая реакция с образованием твердого вещества белого цвета. Это твердое вещество нагревали при 95oC 3 ч и затем помещали в 3000 мл воды и тщательно размешивали. Образованную твердую фазу отделяли фильтрованием, промывали 3000 мл воды и затем высушивали при 60oC при пониженном давлении с получением 750 г белого порошка. При помещении 1 г белого порошка в 100 мл очищенной воды и буферного раствора, эквивалентного желудочной жидкости в первом отделе желудка, и перемешивании он не проявлял признаков растворения.
Пример 4
Когда жидкость, полученную смешиванием 311 г водного основного раствора L-лизина (47 мас.% концентрации) с 461,2 г фосфорной кислоты (85% концентрации) до нейтрализации, и раствор, полученный диспергированием 291,7 г гидроксида магния с 700 мл воды, до гомогенности, происходила экзотермическая реакция с образованием твердого вещества белого цвета. Это твердое вещество белого цвета нагревали при 90oC 3 ч, затем измельчали и высушивали при 60o при пониженном давлении с получением 750 г белого порошка. При помещении 1 г белого порошка в 100 мл очищенной воды и буферного раствора, эквивалентного желудочному соку в первом отделе желудка, и перемешивании он не проявлял признаков растворения.
Пример 5
Когда 20 г белого кристаллического порошка, полученного в примере 1, добавляли к жидкости, полученной смешиванием 4386 г водного основного раствора L-лизина (20 мас.% концентрации) с 231 г фосфорной кислоты (85% концентрации) до нейтрализации, и к ней медленно по частям добавляли раствор 407 г гексагидрата хлорида магния в 500 мл воды, появлялись мелкие кристаллы. Полученные таким образом кристаллы отделяли фильтрованием, промывали 3000 мл воды и затем высушивали при 60oC при пониженном давлении с получением 573 г белого кристаллического порошка. При помещении 1 г белого порошка в 100 мл очищенной воды и буферного раствора, эквивалентного желудочному соку в первом отделе желудка, и перемешивании признаков растворения порошка не появилось.
Пример 6
При добавлении 87,2 г тригидрата вторичного фосфата магния к 730 г водного основного раствора L-лизина (40 мас.% концентрации) и нагревании и перемешивании при 80oC в течение 3 ч, гранулированные кристаллы тригидрата вторичного фосфата магния исчезали и появлялись мелкие кристаллы. Далее 46,1 г фосфорной кислоты (85% концентрации) медленно в охлажденном виде добавляли к полученному смешанному раствору, а затем сразу добавляли и раствор 98,6 г гептагидрата сульфата магния в 150 мл воды, полученный смешанный раствор превращался в вязкую кристаллическую суспензию. Полученные таким образом кристаллы отделяли фильтрованием, промывали 1300 мл воды и высушивали при 60oC при пониженном давлении с получением 198 г белого кристаллического порошка. При помещении 1 г белого порошка в 100 мл очищенной воды и буферного раствора, эквивалентного желудочному соку в первом отделе желудка, он не показал признаков растворения в этом растворе.
Пример 7
Раствор 610 г гексагидрата хлорида магния в 1000 мл воды сразу добавляли к жидкости, полученной смешиванием 4873 г водного основного раствора L-лизина (30 мас.% концентрации) с 461 г фосфорной кислоты (85% концентрации) до нейтрализации. Вязкую смесь, которая впоследствии образовалась, и раствор с 93,3 г гидроксида магния, тщательно диспергированного в 700 мл воды, гомогенно смешивали и полученную гомогенную смесь оставляли на всю ночь, в результате чего образовывался белый осадок. Этот осадок отделяли фильтрованием, промывали 7000 мл воды, и затем высушивали при 60oC при пониженном давлении с получением 980 г белого порошка. При помещении 1 г белого порошка в 100 мл очищенной воды и буферного раствора, эквивалентного желудочной жидкости в первом отделе желудка, и перемешиванием он не показал никаких признаков растворения.
Пример 8
Кристаллические порошки и белые порошки, полученные в примерах 1-7, исследовали на содержание воды и содержание лизина по методу Карла Фишера и потерю веса при сушке (выдерживанием в вакууме при 120oC в течение 3 ч) и на содержание Mg и содержание фосфора методом эмиссионного спектрального анализа индуктивного сопряжения плазмы (1PC). Результаты приведены в табл. 1. Содержание лизина в данном образце определяли растворением образца в разбавленной соляной кислоте и анализом полученного раствора жидкостной хроматографией. Данные по коэффициенту растворения в очищенной воде, защищенности против буферного раствора, эквивалентного желудочной жидкости в первом отделе желудка, и растворимости в буферном растворе, эквивалентном желудочной жидкости в четвертом отделе желудка, приведены дополнительно в табл. 1.
Пример 9
При гомогенном смешивании жидкости, полученной смешиванием 650 г водного основного раствора L-лизина (45 мас.% концентрации) с 461,2 г фосфорной кислоты (85% концентрации) до нейтрализации, и раствора с 201,5 г оксида магния, диспергированного в 600 мл воды, происходила экзотермическая реакция с образованием твердого вещества белого цвета. Это твердое белое вещество измельчали в порошок, промывали 12000 мл воды и затем высушивали при 60oC при пониженном давлении с получением 650 г белого порошка. При помещении 1 г белого порошка в 100 мл очищенной воды и буферного раствора, эквивалентных желудочному соку в первом отделе желудка, и перемешивании он не показал никаких признаков растворения в этом растворе. Когда 1,00 г этого белого порошка растворяли в 100 мл разбавленной соляной кислоты и полученный раствор исследовали на концентрацию L-лизина, концентрация составляла 112 мг/дл, указывая на то, что содержание L-лизина было 11,2%. Когда 1,00 г этого белого порошка смешивали со 100 мл очищенной воды, полученную смесь подвергали ультразвуковой обработке в течение 5 мин и образованный надосадочный слой исследовали на концентрацию L-лизина, эта концентрация составила 12 мг/дл. Результаты показывают, что коэффициент растворения L-лизина в очищенной воде составил 10,7%. При изучении этого белого порошка на защищенность против буферного раствора, эквивалентного желудочному соку в первом отделе желудка, и при определении коэффициента растворения в буферном растворе, эквивалентном желудочному соку в четвертом отделе желудка, коэффициент защищенности составил 85%, а коэффициент растворения - 100% соответственно.
Пример 10
При гомогенном смешивании, полученной смешиванием 311 г водного основного раствора L-лизина (47 мас.% концентрации) с 461,2 г фосфорной кислоты (85% концентрации) до нейтрализации, и раствора с 233,3 г гидроксида магния и 74,1 г гидроксида кальция, диспергированного в 700 мл воды, происходила экзотермическая реакция с образованием твердого вещества белого цвета. Это твердое белое вещество измельчали в порошок, промывали 10000 мл воды и затем высушивали при 60oC при пониженном давлении с получением 600 г белого порошка. При помещении 1 г белого порошка в 100 мл очищенной воды и буферного раствора, эквивалентного желудочному соку в первом отделе желудка, и перемешивании он не показал никаких признаков растворения в этом растворе. При растворении 1,00 г этого белого порошка в 100 мл разбавленной соляной кислоты и тестировании полученного раствора на концентрацию L-лизина эта концентрация составила 65 мг/дл, указывая на то, что содержание L-лизина было 6,5%. 1,00 г этого белого порошка смешивают со 100 мл очищенной воды, полученную смесь подвергают ультразвуковой обработке в течение 5 мин и образовавшийся надосадочный слой исследуют на концентрацию L-лизина. Эта концентрация составила 24 мг/дл. Результаты показывают, что коэффициент растворения L-лизина в очищенной воде составил 36,9%. При изучении этого белого порошка на защищенность против буферного раствора, эквивалентного желудочному соку в первом отделе желудка, и на коэффициент растворения в буферном растворе, эквивалентном желудочной жидкости в четвертом отделе желудка, коэффициент защищенности составил 61% и коэффициент растворения - 100% соответственно.
Пример 11
Раствор 294,4 г дигидрата хлорида кальция в 300 мл воды добавляли к жидкости, полученной смешиванием 4386 г водного основного раствора L-лизина (20 мас. % концентрации) с 203,9 г гексаметафосфата натрия. Гелевый осадок, который впоследствии образовался, отделяли фильтрованием, промывали 12000 мл воды и затем высушивали при 60oC при пониженном давлении с получением 238 г белого порошка. При помещении 1 г белого порошка в 100 мл очищенной воды и буферного раствора, эквивалентного желудочному соку в первом отделе желудка, и перемешивании он не показал признаков растворимости. Когда 1,00 г этого белого порошка растворяли в 100 мл разбавленной соляной кислоты и полученный раствор исследовали на концентрацию L-лизина, концентрация составила 125 мг/дл, указывая на то, что содержание L-лизина было 12,5%. Когда 1,00 г этого белого порошка смешивали со 100 мл очищенной воды, полученную смесь подвергали ультразвуковой обработке в течение 5 мин и образованный надосадочный слой исследовали на концентрацию L-лизина, эта концентрация составила 7 мг/дл. Результаты показывают, что коэффициент растворения L-лизина в очищенной воде составил 5,6%. При исследовании этого белого порошка на защищенность против буферного раствора, эквивалентного желудочному соку в первом отделе желудка, и на коэффициент растворения в буферном растворе, эквивалентном желудочной жидкости в четвертом отделе желудка, коэффициент защищенности составил 92% и коэффициент растворения - 100% соответственно.
Пример 12
К раствору 466,6 г водного основного раствора L-лизина (47 мас.% концентрации) и 183,9 г триполифосфата натрия в 1000 мл воды добавляли раствор, содержащий 9,26 г гидроксида кальция и 147,2 г дигидрата хлорида кальция, растворенных и диспергированных в 300 мл воды. Образовавшийся в результате гелевый осадок отделяли фильтрованием, промывали 12000 мл воды и высушивали при 60oC при пониженном давлении с получением 180 г белого порошка. При помещении 1 г белого порошка в 100 мл очищенной воды и буферного раствора, эквивалентного желудочному соку в первом отделе желудка, и перемешивании он не показал признаков растворения. Когда 1,00 г этого белого порошка растворяли в 100 мл разбавленной соляной кислоты и полученный раствор исследовали на концентрацию L-лизина, концентрация составила 98 мг/дл, указывая на то, что содержание L-лизина было 9,8%. После смешивания 1,00 г этого белого порошка со 100 мл очищенной воды, полученную смесь подвергали ультразвуковой обработке в течение 5 мин и образовавшийся надосадочный слой исследовали на концентрацию L-лизина, эта концентрация составила 8 мг/дл. Результаты показывают, что коэффициент растворения L-лизина в очищенной воде был 8,1%. При исследовании этого белого порошка на защищенность против буферного раствора, эквивалентного желудочному соку в первом отделе желудка, и на коэффициент растворения в буферном растворе, эквивалентном желудочной жидкости в четвертом отделе желудка, коэффициент защищенности составил 89% и коэффициент растворения - 100% соответственно.
Пример 13
Раствор 259,3 г гидроксида кальция в 500 мл воды добавляли к жидкости, полученной смешиванием 609 г водного основного раствора L-лизина (30 мас.% концентрации) с 337,9 г охлажденной полифосфорной кислоты до нейтрализации. Полученная смесь реагировала с выделением тепла и постепенно затвердевала полностью. Полученное таким образом твердое вещество измельчали в порошок, промывали 12000 мл воды и затем высушивали при 60oC при пониженном давлении с получением 505,9 г белого порошка. При помещении 1 г белого порошка в 100 мл очищенной воды и буферного раствора, эквивалентного желудочному соку в первом отделе желудка, и перемешивании он не показал никаких признаков растворения. Затем 1,00 г этого белого порошка растворяли в 100 мл разбавленной соляной кислоты и полученный раствор исследовали на концентрацию L-лизина, концентрация составила 165 мг/дл, указывая на то, что содержание L-лизина было 16,5%. Когда 1,00 г этого белого порошка смешивали со 100 мл очищенной воды, полученную смесь подвергали ультразвуковой обработке в течение 5 мин и образованный надосадочный слой исследовали на концентрацию L-лизина, эта концентрация составила 10 мг/дл. Результаты показывают, что коэффициент растворения L-лизина в очищенной воде был 11%. При исследовании этого белого порошка на защищенность против буферного раствора, эквивалентного желудочной жидкости в первом отделе желудка, и на коэффициент растворения в буферном растворе, эквивалентном желудочной жидкости в четвертом отделе желудка, коэффициент защищенности составил 85% и коэффициент растворения - 100% соответственно.
Пример 14
487 г водного основного раствора L-лизина (30 мас.% концентрации) смешивали с 51,9 г гидроксида кальция и 216 г вторичного пирофосфата кальция (CaH2P2O7) и полученную смесь перемешивали и нагревали до 90oC, полученная смесь постепенно полностью затвердевала. Полученное твердое вещество измельчали в порошок, промывали 10000 мл воды и затем высушивали при 60oC при пониженном давлении с получением 356 г белого порошка. При помещении 1 г белого порошка в 100 мл очищенной воды и буферного раствора, эквивалентного желудочной жидкости в первом отделе желудка, и перемешивании он не показал признаков растворения. Затем 1,00 г этого белого порошка растворяли в 100 мл разбавленной соляной кислоты и полученный раствор исследовали на концентрацию L-лизина, концентрация составила 116 мг/дл, указывая на то, что содержание L-лизина было 11,6%. Далее 1,00 г этого белого порошка смешивали со 100 мл очищенной воды, полученную смесь подвергали ультразвуковой обработке в течение 5 мин и образованный надосадочный слой исследовали на концентрацию L-лизина, эта концентрация составила 27 мл/дл. Результаты показывают, что коэффициент растворения L-лизина в очищенной воде был 23%. При исследовании этого белого порошка на защищенность против буферного раствора, эквивалентного желудочному соку в первом отделе желудка, и на коэффициент растворения в буферном растворе, эквивалентном желудочному соку в четвертом отделе желудка, коэффициент защищенности составил 75% и коэффициент растворения - 100% соответственно.
Пример 15
Раствор, содержащий 259,3 г гидроксида кальция, диспергированного в 400 мл воды, добавляли к жидкости, полученной смешиванием 292 г водного основного раствора L-лизина (50 мас.% концентрации) с 337,9 г полифосфорной кислоты (H6P4O13) и 150 г охлажденной воды, до нейтрализации. Полученная смесь реагировала с выделением тепла и постепенно полностью отвердевала. Твердое вещество, полученное таким образом, измельчали и высушивали при 60oC при пониженном давлении с получением 690 г белого порошка. При помещении 1 г белого порошка в 100 мл очищенной воды и буферного раствора, эквивалентного желудочной жидкости в первом отделе желудка, и перемешивании он не показал признаков растворения. 1,00 г этого белого порошка растворяли в 100 мл разбавленной соляной кислоты и полученный раствор исследовали на концентрацию L-лизина, концентрация составила 212 мг/дл, указывая на то, что содержание L-лизина было 21,2%. Затем 1,00 г этого белого порошка смешивали со 100 мл очищенной воды, полученную смесь подвергали ультразвуковой обработке в течение 5 мин и образованный надосадочный слой исследовали на концентрацию L-лизина, эта концентрация составила 76 мг/дл. Результаты показали, что коэффициент растворения L-лизина в очищенной воде составил 36%. При исследовании этого белого порошка на защищенность против буферного раствора, эквивалентного желудочной жидкости в первом отделе желудка, и коэффициент растворения в буферном растворе, эквивалентном желудочной жидкости в четвертом отделе желудка, коэффициент защищенности составил 59% и коэффициент растворения - 100% соответственно.
Пример 16
Раствор, содержащий 185,2 г гидроксида кальция и 58,1 г гидроксида магния, диспергированных в 350 мл воды, добавляли к жидкости, полученной смешиванием 363 г водного основного раствора L-лизина (50 мас.% концентрации) с 337,9 г полифосфорной кислоты (H6P4O13) и 260 мл очищенной охлажденной воды, до нейтрализации. Полученная смесь выделяла тепло и постепенно полностью отвердевала. Полученное твердое вещество измельчали, промывали 12000 мл воды и высушивали при 60oC при пониженном давлении с получением 165 г белого порошка. При помещении 1 г белого порошка в 100 мл очищенной воды и буферного раствора, эквивалентного желудочному соку в первом отделе желудка и перемешивании он не показал признаков растворения. Затем 1,00 г этого белого порошка растворяли в 100 мл разбавленной соляной кислоты и полученный раствор исследовали на концентрацию L-лизина, она составила 126 мг/дл, указывая, что содержание L-лизина было 12,6%. 1,00 г этого белого порошка смешивали со 100 мл очищенной воды, полученную смесь подвергали ультразвуковой обработке в течение 5 мин и образовавшийся надосадочный слой исследовали на концентрацию L-лизина, эта концентрация составила 2,6 мг/дл. Результаты показали, что коэффициент растворения L-лизина в очищенной воде составил 2,1%. Когда этот белый порошок исследовали на защищенность против буферного раствора, эквивалентного желудочному соку в первом отделе желудка, и на коэффициент растворения в буферном растворе, эквивалентном желудочному соку в четвертом отделе желудка, коэффициент защищенности составил 97% и коэффициент растворения - 100% соответственно.
Пример 17
Раствор, содержащий 166,7 г гидроксида кальция, диспергированного в 300 мл воды, добавляли к жидкости, полученной смешиванием 363 г водного основного раствора L-лизина (50 мас.% концентрации) с 467 г метафосфорной кислоты (HPO3) и 200 мл очищенной охлажденной воды до нейтрализации. Эта полученная смесь выделяла тепло и постепенно полностью отвердевала. Полученное твердое вещество измельчали, промывали 12000 мл воды и затем высушивали при 60oC при пониженном давлении с получением 295 г белого порошка. При помещении 1 г белого порошка в 100 мл очищенной воды и буферного раствора, эквивалентного желудочной жидкости в первом отделе желудка, и перемешивании, он не проявлял никаких признаков растворения. Затем 1,00 г этого белого порошка растворяли в 100 мл разбавленной хлористоводородной кислоты и полученный раствор исследовали на концентрацию L-лизина, концентрация составила 99 мг/дл, указывая на то, что содержание L-лизина было 9.9%. Когда 1,00 г этого белого порошка смешивали со 100 мл очищенной воды, полученную смесь подвергали ультразвуковой обработке в течение 5 мин и образованный надосадочной слой исследовали на концентрацию L-лизина, эта концентрация составила 2,4 мг/дл. Результаты показывают, что коэффициент растворения L-лизина в очищенной воде был 2,4%. При тестировании этого белого порошка на защищенность против буферного раствора, эквивалентного желудочному соку в первом отделе желудка, и на коэффициент растворения в буферном растворе, эквивалентном желудочному соку в четвертом отделе желудка, коэффициент защищенности составил 96% и коэффициент растворения - 100% соответственно.
Пример 18
Белые порошки, полученные в примерах 11-17, были подвергнуты анализу. Результаты анализа показаны в табл. 2. Содержание лизина данного образца определяли растворением образца в разбавленной соляной кислоте и анализом полученного раствора жидкостной хроматографией. Данные по коэффициенту растворения в очищенной воде, защищенности против буферного раствора, эквивалентного желудочной жидкости в первом отделе желудка, и растворимости в буферном растворе, эквивалентном желудочной жидкости в четвертом отделе желудка, дополнительно показаны в табл. 1. Белые порошки, полученные в примере 1, примере 3, примере 13, примере 14 и примере 17, каждый, изучали с помощью спектра рентгеновской порошковой дифракции с применением Cu K-α-излучения. Полученные спектральные графики показаны на фиг. 1-5. Углы дифракции (2 θ) и относительные коэффициенты интенсивности основных пиков, выявленных на графиках, показаны в сводной табл. 3. Выявленные основные пики постоянно не совпадали с пиками рентгеновской порошковой дифракции, полученными для соответствующих исходных материалов и гомологичных фосфатов, не содержащих основной аминокислоты.
Пример 19
Когда раствор с 72,9 г гидроксида магния, тщательно диспергированного в 200 мл воды, смешивали с раствором 174,2 г L-аргинина и 98,0 г фосфорной кислоты (85% концентрации) в 300 мл воды, происходила экзотермическая реакция с образованием белого твердого вещества. Это твердое белое вещество нагревали при 95oC 3 ч и затем тщательно размешивали в 1000 мл очищенной воды. Образованную твердую фазу отделяли фильтрованием, промывали 1000 мл воды и затем высушивали при 60oC при пониженном давлении с получением 235 г белого порошка. Затем 1 г этого белого порошка помещали в 100 мл очищенной воды и буферного раствора, эквивалентного желудочному соку в первом отделе желудка, и перемешивали, он не проявил никаких признаков растворения. Когда 1,00 г этого белого порошка растворяли в 100 мл разбавленной соляной кислоты и полученный раствор тестировали на концентрацию L-лизина, концентрация составила 370 мг/дл, указывая на то, что содержание L-лизина было 37,0%. Когда 1,00 г этого белого порошка смешивали со 100 мл очищенной воды, полученную смесь подвергали ультразвуковой обработке в течение 5 мин, и образовавшийся надосадочный слой исследовали на концентрацию L-лизина, эта концентрация составила 100 мг/дл. Результаты показывают, что коэффициент растворения L-лизина в очищенной воде был 27,0%. При исследовании этого белого порошка на защищенность против буферного раствора, эквивалентного желудочному соку в первом отделе желудка, и на коэффициент растворения в буферном растворе, эквивалентном желудочной жидкости в четвертом отделе желудка, коэффициент защищенности составил 30% и коэффициент растворения - 100% соответственно.
Пример 20
Гранулы диаметром около 1 мм получали смешиванием 200 г белого кристаллического порошка, полученного в примере 1, со 150 г отвержденного соевого масла, экструдированием полученной смеси через головку экструдера диаметром в 1 мм при 65oC с использованием устройства горячей экструзии и нагреванием экструдированной нити смеси на части длиной около 1 мм. Когда полученные таким образом гранулы исследовали на защищенность против буферного раствора, эквивалентного желудочному соку в первом отделе желудка, и на коэффициент растворения в буферном растворе, эквивалентном желудочному соку в четвертом отделе желудка, коэффициент защищенности был 35% и коэффициент растворения - 95% соответственно.
Пример 21
Гранулы диаметром около 2 мм получали смешиванием 300 г белого порошка, полученного в примере 3, с 20 г порошка метионина, 50 г карбоната кальция, 30 г натриевой соли казеина и 5 г крахмал-гликолата натрия, перемешиванием полученной смеси со 100 мл воды, экструдированием полученного теста через дисковый гранулятор с диаметром отверстий 2 мм, нарезанием экструдированной нити теста на части длиной около 2 мм и высушиванием нарезанных гранул. Полученные гранулы разрезали ножом на небольшие кусочки диаметром около 0,5 мм. Пять из этих небольших кусочков нагревали по отдельности и экстрагировали разбавленной соляной кислотой и исследовали на содержание аминокислоты. Никакой разницы в содержании аминокислоты среди этих пяти небольших кусочков найдено не было. При тестировании гранул, полученных, как описано выше, на защищенность против буферного раствора, эквивалентного желудочному соку в первом отделе желудка, и на коэффициент растворения в буферном растворе, эквивалентном желудочному соку в четвертом отделе желудка, коэффициент защищенности по отношению к лизину составил 97 и 64% по отношению к метионину, и коэффициент растворения лизина и метионина был 95%. Когда небольшие кусочки диаметром около 0,5 мм тестировали аналогичным образом на защищенность против буферного раствора, эквивалентного желудочному соку в первом отделе желудка, и на коэффициент растворения в буферном растворе, эквивалентном желудочному соку в четвертом отделе желудка, коэффициент защищенности составил 95% по отношению к лизину и 62% по отношению к метионину и коэффициент растворения лизина и метионина составил 98%.
Положительный эффект изобретения
Благодаря получению комплексной соли, которая состоит из основной аминокислоты, щелочноземельного металла и фосфорной кислоты и демонстрирует нерастворимость в водном растворе от нейтрального до щелочного и растворимость в кислом водном растворе, как описано выше, становится возможным получение аддитивной композиции для применения в корме для жвачных млекопитающих, содержащем такие основные аминокислоты, как лизин, т.е. вещества, часто отсутствующие в обычном корме жвачных животных, и отличающейся превосходными качествами защиты в первом отделе желудка и растворимостью в четвертом отделе желудочка. Гомогенные гранулы согласно этому изобретению обладают прочностью к разрушению при жевании жвачными или при смешивании с другими кормовыми компонентами. Данное изобретение предлагает получение аддитивной композиции для применения в корме для жвачных млекопитающих, которая отлично защищена в первом отделе желудка и растворима в четвертом отделе желудка по сравнению с аддитивной композицией, получаемой общепринятой технологией. Таким образом, это изобретение предлагает кормовую добавку, которая делает возможным эффективное всасывание биологически активного вещества жвачными животными и вносит очень существенный вклад в экономику.
| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО И ПРОДУКТ ПИТАНИЯ ДЛЯ ПРОФИЛАКТИКИ/УМЕНЬШЕНИЯ ПРОЯВЛЕНИЙ ФУНКЦИОНАЛЬНОГО РАССТРОЙСТВА ПИЩЕВАРЕНИЯ | 2005 |
|
RU2407524C2 |
| СПОСОБ ПОЛУЧЕНИЯ КРИСТАЛЛОВ ГИДРОХЛОРИДА ОСНОВНОЙ АМИНОКИСЛОТЫ | 2007 |
|
RU2460799C2 |
| СПОСОБ ПОЛУЧЕНИЯ L-АМИНОКИСЛОТЫ | 2009 |
|
RU2518677C2 |
| Способ определения активности х-пролилдипептидиламинопептидазы | 1976 |
|
SU786853A3 |
| СПОСОБ ПОЛУЧЕНИЯ ОСНОВНОГО ВЕЩЕСТВА | 2005 |
|
RU2350655C2 |
| АГЕНТ ДЛЯ ПРИДАНИЯ КОКУМИ | 2010 |
|
RU2532834C2 |
| ФРАГМЕНТ ДНК, КОДИРУЮЩИЙ АСПАРТОКИНАЗУ III, СПОСОБ ПОЛУЧЕНИЯ L-ТРЕОНИНА | 1993 |
|
RU2113484C1 |
| БАКТЕРИЯ РОДА BACILLUS, ПРОДУЦИРУЮЩАЯ L-АМИНОКИСЛОТУ, И СПОСОБ ПОЛУЧЕНИЯ L-АМИНОКИСЛОТЫ | 2002 |
|
RU2299907C2 |
| СПОСОБ ПОЛУЧЕНИЯ L-ГЛУТАМИНОВОЙ КИСЛОТЫ | 2002 |
|
RU2288271C2 |
| ПИТАТЕЛЬНАЯ КОМПОЗИЦИЯ | 2006 |
|
RU2390272C2 |


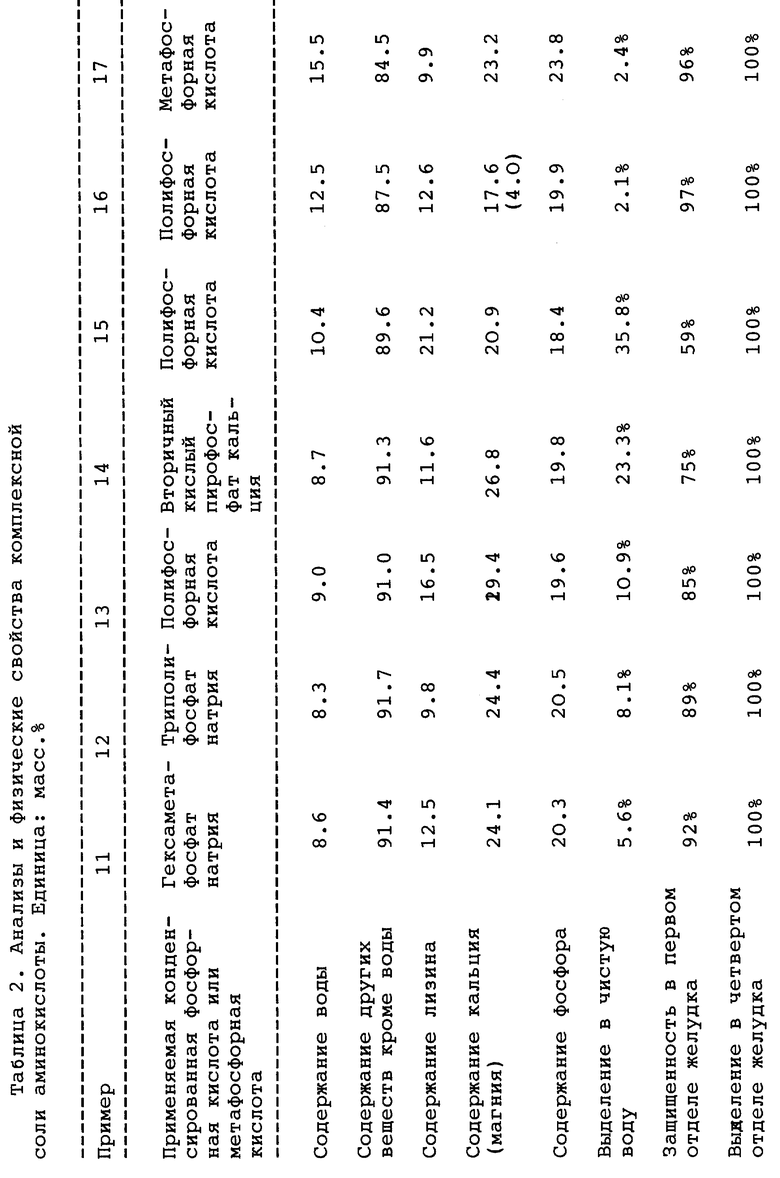

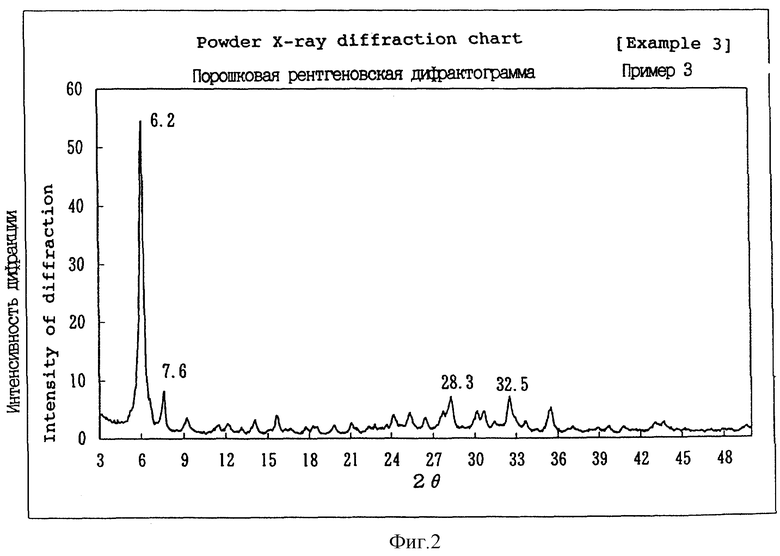
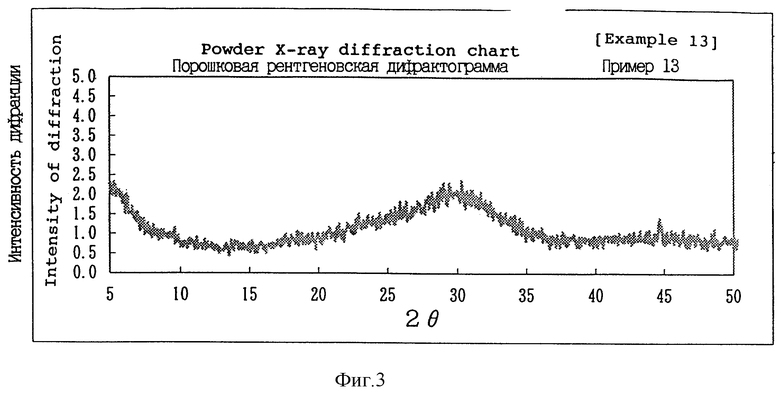
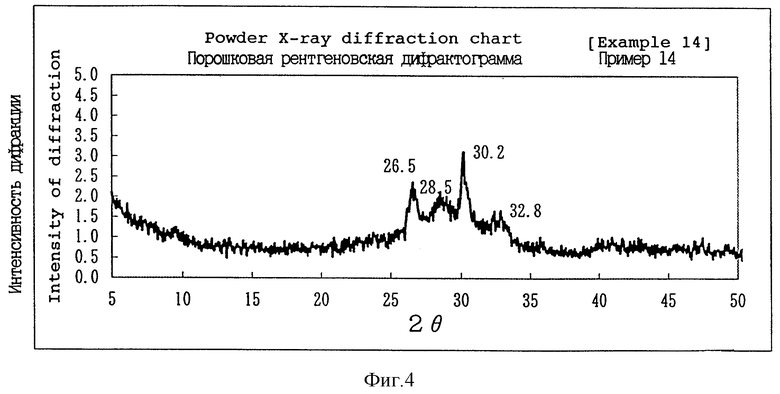
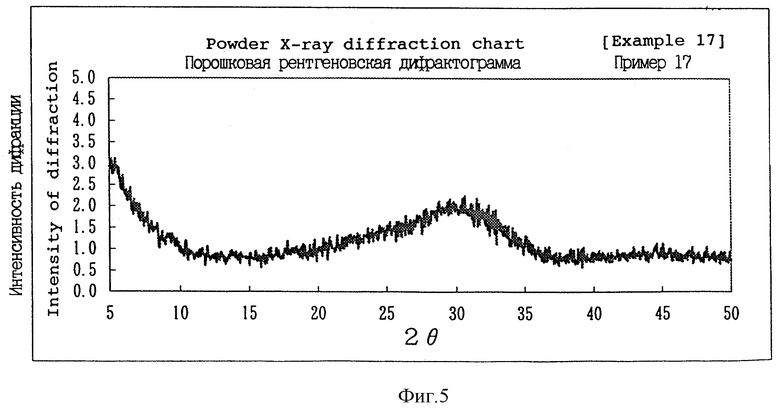
Описывается новая комплексная соль, представленная следующей общей формулой: RaMbHcPO4 · nH2O, где R обозначает катионный лизин, М представляет ион магния, а - цифровую величину 0,05-1, b - цифровую величину в пределах 1-1,47, с - цифровую величину 0-0,3, при условии, что а, b и с вместе соответствуют выражению а + (2 · b) + с = 3 и n соответствует числу в пределах 0-10. Описывается также аддитивная композиция, содержащая эту соль и применимая для использования в корме для жвачных млекопитающих. Эта аддитивная композиция улучшает питательную ценность корма благодаря присутствию в ней такой основной аминокислоты, как лизин - вещества, которое часто отсутствует в корме жвачных млекопитающих. 2 c. и 8 з.п. ф-лы, 5 ил., 3 табл.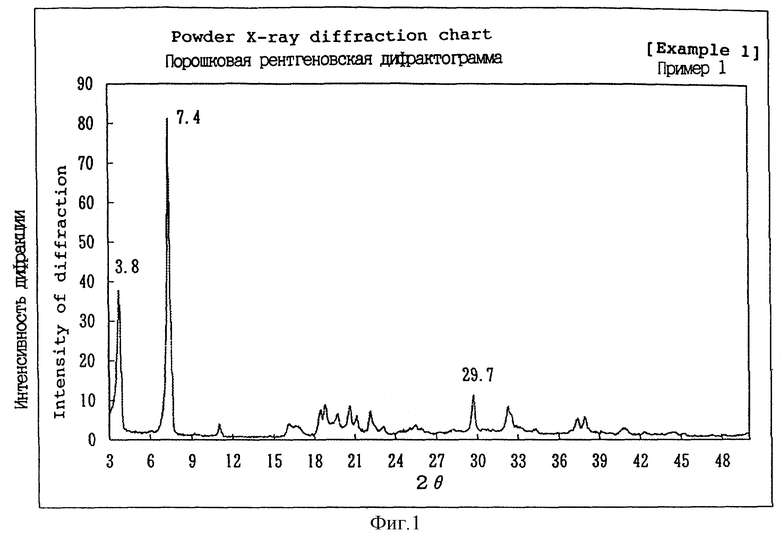
RaMbHcPO4 · nH2O,
где R обозначает катионный лизин;
M - ион магния;
а - цифровая величина в пределах 0,05 - 1;
b - цифровая величина в пределах 1 - 1,47;
с - цифровая величина 0 - 0,3,
при условии, что а, b и с вместе соответствуют выражению а + (2 x b) + c = 3 и n соответствует числу в пределах 0 - 10.
| Способ приготовления сернистого красителя защитного цвета | 1915 |
|
SU63A1 |
| Способ приготовления сернистого красителя защитного цвета | 1915 |
|
SU63A1 |
| УСТРОЙСТВО для ИССЛЕДОВАНИЯ ФУНКЦИЙ ДВИГАТЕЛЬНОГО АНАЛИЗАТОРА | 0 |
|
SU198508A1 |
| СПОСОБ ПОЛУЧЕНИЯ ФОСФОРНЫХ ЭФИРОВ ТИАМИНА | 1992 |
|
RU2041229C1 |
| Способ приготовления сернистого красителя защитного цвета | 1915 |
|
SU63A1 |
Авторы
Даты
2001-02-27—Публикация
1996-06-07—Подача