Область техники, к которой относится изобретение
Настоящее изобретение относится к способу промышленного применения микроорганизмов, в частности к способу получения основного вещества ферментацией. В качестве основных веществ, получаемых ферментацией, можно указать, например, L-лизин, используемый в виде добавки в корм для животных, L-аргинин и L-гистидин, используемые для приготовления фармацевтических препаратов, таких как препараты для инфузий.
Уровень техники
Способы получения основных веществ ферментацией предполагают культивирование микроорганизмов, обладающих способностью продуцировать и аккумулировать основное вещество в среде, из которой указанное основное вещество затем собирают. При осуществлении таких способов культивирование выполняют в виде периодического культивирования, культивирования с подпиткой или непрерывного культивирования.
В процессе получения основных веществ ферментацией в среду обычно добавляют ионы сульфата или хлорида в качестве противоанионов для целевого вещества, которые диссоциируют в среде в катионы для сохранения рН среды на нейтральном уровне (выложенные патенты Японии (Kokai) № 5-30985 и 5-244969).
Во многих случаях, когда необходимо произвести очистку вещества, основные вещества собирают из среды путем ионного обмена. Например, при получении L-лизина ферментационный бульон слегка подкисляют, L-лизин адсорбируют на ионообменной смоле и элюируют из смолы при помощи ионов аммония. Элюированный L-лизин используют в виде основного лизина или кристаллизуют хлористоводородной кислотой с образованием гидрохлорида L-лизина.
При введении в среду ионов хлорида в качестве противоанионов вышеуказанную очистку L-лизина или гидрохлорида L-лизина можно производить путем концентрирования среды. Однако, поскольку ионы хлорида вызывают коррозию металлических ферментеров и другого оборудования, в процессе производства нежелательно использовать высококонцентрированные среды.
С другой стороны, в тех случаях, когда основное вещество не подвергают очистке, ферментационный бульон концентрируют в том виде, как есть, или слегка подкисляют хлористоводородной или серной кислотой и затем гранулируют распылением. В данном случае остаточные компоненты содержат противоанионы, добавленные в среду, вследствие чего сокращается количество основного вещества в полученном продукте ферментации.
В выложенном патенте Японии № 2002-65287 (заявка на патент США № 2002/025564) описан способ применения в процессе ферментации основной аминокислоты ионов карбоната и бикарбоната в качестве противоанионов основной аминокислоты для замены части ионов сульфата или хлорида. Ионы карбоната или бикарбоната можно сравнительно легко удалить из культуральной среды, делая показатель рН среды кислым или концентрируя среду либо тем и другим способами вместе. В вышеуказанной публикации описан способ создания положительного внутреннего давления в ферментере во время ферментации или введения в среду газообразного диоксида углерода или газовой смеси, содержащей диоксид углерода, для добавления в среду ионов карбоната и бикарбоната. Однако в стандартных условиях культивирования при нейтральном показателе рН в среде растворяется лишь небольшое количество доксида углерода, если такое растворение вообще имеет место. Поэтому для введения в культуральную среду ионов бикарбоната и карбоната и уменьшения концентрации ионов сульфата или хлорида культивирование необходимо производить при щелочном показателе рН. Однако при высоком значении рН скорость роста бактерий и продуцирование целевого вещества обычно уменьшаются.
Описание изобретения
Объектом настоящего изобретения является способ уменьшения ионов сульфата и хлорида, эффективного продуцирования целевого вещества путем ферментации с использованием микроорганизма, обладающего способностью продуцировать целевое основное вещество, и использования ионов карбоната и бикарбоната в качестве противоанионов основного вещества без снижения скорости роста микроорганизма или уменьшения продуцирования целевого вещества.
При использовании коринеформных бактерий или бактерий Escherichia для получения основных веществ ферментацией скорость роста бактерий или продуцирование целевого вещества обычно уменьшаются при слишком высоком значении рН. Авторы настоящего изобретения обнаружили, что основным фактором, вызывающим данное явление, является аммиак, который добавляют в среду в качестве источника азота для продуцирования основного вещества, роста бактерий или в качестве источника противоионов основного вещества, причем скорость роста микроорганизма или продуцирование целевого вещества в условиях высокого значения рН можно сохранить на должном уровне, контролируя концентрацию общего аммиака при выполнении ферментации в пределах приемлемого диапазона концентраций.
Настоящее изобретение создано на основе вышеуказанных открытий.
Таким образом, предметом настоящего изобретения являются нижеследующие способы.
(1) Способ продуцирования основного вещества ферментацией, который включает культивирование микроорганизма, обладающего способностью продуцировать данное основное вещество в жидкой среде, находящейся в ферментере, и аккумулировать основное вещество в среде, при этом количество ионов сульфата и/или хлорида, используемых в качестве противоионов основного вещества, уменьшают, регулируя концентрацию общего аммиака в среде в определенном диапазоне концентраций в течение по крайней мере части всего периода культивирования.
(2) Способ по п.(1), в котором определенный диапазон концентраций общего аммиака находится в пределах, удовлетворяющих следующим условиям:
(А) концентрация ионов аммония в среде находится на таком уровне, при котором сумма ионных эквивалентов ионов бикарбоната и/или карбоната и других анионов, растворенных в среде, больше ионного эквивалента основного вещества, ионизированного из основного вещества, аккумулированного в среде; и
(В) концентрация общего аммиака в среде находится на уровне, не ингибирующем продуцирование микроорганизмом основного вещества, который определяют заранее следующим образом:
микроорганизм культивируют в среде с разными значениями рН и разными концентрациями общего аммиака, измеряют продуцирование основного вещества при каждом значении рН и каждой концентрации общего аммиака и для каждого значения рН определяют концентрацию общего аммиака, обеспечивающую 50% или более высокое продуцирование основного вещества на основании продуцирования, достигаемого в оптимальных условиях.
(3) Способ по п.(1), в котором определенный диапазон концентраций общего аммиака определяют заранее следующим образом:
(А') культивирование выполняют в среде, содержащей ионы сульфата и/или хлорида в качестве источника противоионов целевого основного вещества, в количестве, достаточном для культивирования при значении рН, равном 7,2 или ниже, при этом значение рН сохраняют в пределах от 6,5 до 7,2, добавляя по крайней мере одно из нижеследующих веществ, включающих газообразный аммиак, водный раствор аммиака и мочевину, и измеряют продуцирование основного вещества;
(B') культивирование начинают в среде, аналогичной применяемой на стадии (А'), за исключением того, что количество ионов сульфата и/или хлорида компонентов среды уменьшают на требуемую величину, и продолжают культивирование при разных концентрациях общего аммиака в течение периода времени, когда становится невозможно сохранять значение рН среды равным 7,2 или ниже вследствие недостатка ионов сульфата и/или хлорида, используемых в качестве противоионов основного вещества, вызываемого аккумулированием целевого основного вещества, определяя таким образом диапазон концентраций общего аммиака, обеспечивающих 50% или более высокое продуцирование на основании продуцирования, измеренной на стадии (А').
(4) Способ по п.(1), в котором по крайней мере часть общего периода времени включает по крайней мере один период, в течение которого значение рН среды увеличивается вследствие недостатка противоионов, вызываемого аккумулированием целевого основного вещества, и период времени, в течение которого значение рН увеличивается в результате добавления катионов в среду.
(5) Способ по п.(1), в котором концентрацию общего аммиака в среде регулируют, добавляя в среду аммиак или мочевину при снижении или отсутствии активности микроорганизма, определяемой на основании таких индикаторов, как концентрация растворенного кислорода в среде, скорость потребления источника углерода в среде, помутнение среды, продуцирование основного вещества и изменение значения рН в среде.
(6) Способ по п.(1), в котором использована среда, имеющая такой же состав, что и среда, содержащая ионы сульфата и/или хлорида в качестве источника противоионов основного вещества в количестве, достаточном для культивирования при значении рН, равном 7,2 или ниже, за исключением того, что количество ионов сульфата и/или хлорида уменьшено на требуемую величину; и
по крайней мере часть общего периода времени является периодом, когда значение рН среды не может быть сохранено равным 7,2 или ниже вследствие недостатка противоионов для основного вещества, аккумулированного в среде.
(7) Способ по п.(2), в котором другие анионы выбирают из ионов сульфата, ионов хлорида, ионов фосфата и ионизированных органических кислот.
(8) Способ по п.(2) или (7), в котором общее количество других анионов равно 900 мэкв/л или меньше.
(9) Способ по п.(1), в котором концентрацию общего аммиака в среде доводят до 200 мМ или меньше.
(10) Способ по п.(1), который включает стадию пролиферации микроорганизма.
(11) Способ по п.(10), в котором концентрацию общего аммиака не регулируют на стадии пролиферации микроорганизма.
(12) Способ по п.(1), в котором основное вещество выбирают из L-лизина, L-аргинина и L-гистидина.
(13) Способ по п.(12), в котором основное вещество является L-лизином.
(14) Способ по п.(12), в котором основное вещество является L-аргинином.
(15) Способ по п.(1), в котором среду или полученный продукт нагревают после ферментации для удаления ионов бикарбоната и карбоната.
(16) Способ по п.(1), в котором микроорганизм является коринеформной бактерией или бактерией Escherichia.
(17) Ферментационный бульон или продукт ферментации, содержащий основное вещество, полученное способом по п.(15).
Краткое описание чертежей
На Фиг.1 показаны результаты культивирования с целью продуцирования L-лизина, выполненного с использованием стандартной питательной среды и способа культивирования.
На Фиг.2 показаны результаты культивирования с целью продуцирования L-лизина, выполненного в среде с ограниченной концентрацией аммония.
На Фиг.3 показаны результаты культивирования с целью продуцирования L-лизина, которое выполняли, контролируя только концентрацию общего аммиака и не регулируя значение рН.
На Фиг.4 показаны изменения концентрации общего аммиака и значения рН с течением времени в стандартной питательной среде и в среде без сульфата аммония и хлорида аммония.
На Фиг.5 показаны изменения роста, концентрации общего аммиака, значения рН и оставшегося количества сахара с течением времени в процессе ферментации L-аргинина в среде с ограниченной концентрацией аммония.
На Фиг.6 показаны результаты культивирования с целью продуцирования L-аргинина в среде с ограниченной концентрацией аммония.
Предпочтительные варианты осуществления изобретения
Ниже приведено подробное описание настоящего изобретения.
Способ по настоящему изобретению представляет собой способ получения основного вещества ферментацией, который включает культивирование микроорганизма, способного продуцировать основное вещество в жидкой среде, находящейся в ферментере, для получения и аккумулирования основного вещества в указанной среде. Способ по настоящему изобретению отличается тем, что количество ионов сульфата и/или хлорида, используемых в качестве противоионов основного вещества, уменьшают путем регулирования концентрации аммиака в среде в определенном диапазоне концентраций в течение по крайней мере части всего процесса культивирования. То есть способ по настоящему изобретению является способом получения основного вещества в среде с меньшим содержанием ионов сульфата и хлорида, достигаемым в результате регулирования концентрации общего аммиака, используемого в качестве источника азота, в пределах, необходимых для роста микроорганизма или продуцирования целевого вещества и не ингибирующих рост микроорганизма или продуцирование целевого вещества.
Примеры конкретного диапазона концентраций общего аммиака включают диапазон, удовлетворяющий нижеследующим условиям:
(А) концентрация ионов аммония в среде находится на таком уровне, при котором сумма ионных эквивалентов ионов бикарбоната и/или карбоната и других анионов, растворенных в среде, больше ионного эквивалента основного вещества, ионизированного из основного вещества, аккумулированного в среде; и
(В) концентрация общего аммиака в среде находится на уровне, не ингибирующем продуцирование микроорганизмом основного вещества, который определяют заранее следующим образом:
микроорганизм культивируют в среде с разными значениями рН и разными концентрациями общего аммиака, измеряют продуцирование основного вещества при каждом значении рН и каждой концентрации общего аммиака и для каждого значения рН определяют концентрацию общего аммиака, обеспечивающую 50% или более высокое продуцирование основного вещества на основании продуцирования, достигаемого в оптимальных условиях.
Кроме того, в другом варианте осуществления настоящего изобретения конкретный диапазон концентраций общего аммиака определяют заранее следующим образом.
(А') (Способ 1. Оценка результатов ферментации в нейтральных условиях).
Культивирование выполняют в среде, содержащей ионы сульфата и/или хлорида в качестве источника противоионов целевого основного вещества, в количестве, достаточном для культивирования при значении рН, равном 7,2 или ниже, при этом значение рН сохраняют в пределах от 6,5 до 7,2, добавляя по крайней мере одно из нижеследующих веществ, включающих газообразный аммиак, водный раствор аммиака и мочевину, и измеряют продуцирование основного вещества.
(B') (Способ 2. Оценка результатов ферментации с меньшим количеством ионов сульфата и хлорида при разных концентрациях аммония).
Культивирование начинают в среде, аналогичной применяемой в вышеописанном способе 1 (стадия А'), за исключением того, что количество ионов сульфата и/или хлорида компонентов среды уменьшают на требуемую величину, и продолжают культивирование при разных концентрациях общего аммиака в течение периода времени, когда становится невозможно сохранять значение рН среды равным 7,2 или ниже вследствие недостатка ионов сульфата и/или хлорида, используемых в качестве противоионов основного вещества, вызываемого аккумулированием целевого основного вещества, определяя таким образом диапазон концентраций общего аммиака, обеспечивающих 50% или более высокое продуцирование на основании продуцирования, измеренного на стадии (А').
Кроме того, в другом варианте осуществления настоящего изобретения, когда конкретный диапазон концентраций общего аммиака не определен заранее, концентрацию общего аммиака можно отрегулировать в пределах предварительно определенного диапазона. В частности, концентрацию общего аммиака в среде регулируют, добавляя аммиак или мочевину в среду при снижении или отсутствии активности микроорганизма, определяемой на основании таких индикаторов, как концентрация растворенного кислорода в среде, скорость потребления источника азота, помутнение среды, продуцирование основного вещества и изменение значения рН. Указанная среда имеет такой же состав, что и среда, содержащая ионы сульфата и/или хлорида в качестве источника противоионов основного вещества в количестве, достаточном для культивирования при рН, равном 7,2 или ниже, за исключением того, что количество ионов сульфата и/или хлорида уменьшено на требуемую величину. Примеры по крайней мере части общего периода времени включают период, когда невозможно сохранить значение рН среды равным 7,2 или ниже вследствие недостатка противоионов для основного вещества, аккумулированного в среде.
Примеры других анионов включают ионы хлорида, ионы сульфата, ионы фосфата, ионы органических кислот (уксусной кислоты, молочной кислоты, янтарной кислоты и т.д.) и тому подобные. Кроме того, ионы бикарбоната и/или карбоната, растворенные в среде, действуют в качестве противоанионов основного вещества.
В настоящем изобретении ионный эквивалент является значением, полученным в результате умножения молярной концентрации каждого иона на валентность иона, которое выражено в единицах экв/л. То есть ионный эквивалент 1 мМ одновалентного иона равен 1 мэкв/л и ионный эквивалент 1 мМ двухвалентного иона равен 2 мэкв/л.
Вышеуказанную концентрацию общего аммиака регулируют с тем, чтобы общее количество аммиака в среде соответствовало количеству, необходимому для роста микроорганизма или продуцирования основного вещества, и не ингибировало продуцирование основного вещества микроорганизмом, поэтому показатель рН среды автоматически доводят до значения, пригодного для растворения ионов бикарбоната и/или карбоната, используемых в качестве противоанионов основного вещества.
В настоящем изобретении термин "общий аммиак" означает сумму недиссоциированного аммиака (NH3) и ионов аммония (NH4 +). При регулировании концентрации общего аммиака можно измерить недиссоциированный аммиак или ионы аммония либо те и другие вместе.
В среду обычно добавляют сульфат аммония и хлорид аммония в качестве источников противоанионов основного вещества и источника азота в целом. Кроме того, так как для регулирования значения рН среды обычно используют аммиак и мочевину, в среде имеет место высокая концентрация аммиака и ионов аммония. При уменьшении количества сульфата аммония или хлорида аммония для сокращения количества ионов сульфата или хлорида, добавляемых в среду, источник азота, такого как аммиак, пополняют в количестве, соответствующем уменьшаемому количеству. Для выполнения данной операции необходим способ введения аммиака, который должен учитывать баланс между катионами, включающими катионы, продуцируемые бактериями, количество которых увеличивается в процессе культивирования с образованием целевого основного вещества, катионы, ионизируемые из добавляемого аммиака, катионы, добавляемые в среду, такие как катионы натрия и калия, и тому подобные, и анионами, количество которых увеличивается в среде в результате дыхания бактерий или добавления в среду. При нарушении указанного баланса ферментация не будет увеличиваться, так как концентрация аммиака или значение рН станут чрезмерно высокими или, наоборот, аммиака окажется слишком мало. Созданный в соответствии с настоящим изобретением способ добавления аммиака для регулирования концентрации общего аммиака в пределах определенного диапазона позволяет эффективно сохранять вышеуказанный баланс между катионами и анионами, поэтому благоприятный рост микроорганизма и эффективное образование основного вещества могут происходить даже в условиях уменьшения количества ионов сульфата и хлорида.
Концентрацию общего аммиака в среде регулируют путем добавления в среду по крайней мере одного нижеследующего вещества, включающего газообразный аммиак, раствор аммиака и мочевину, с таким расчетом, чтобы концентрация общего аммиака в среде находилась на приемлемом уровне. Кроме того, можно также добавлять соль аммония, такую как хлорид аммония или сульфат аммония, если она не ухудшает эффект, достигаемый настоящим изобретением. Можно также использовать соль аммония, содержащую ион бикарбоната или карбоната в качестве противоиона, которую можно легко удалить в виде газа после окончания культивирования. Концентрацию общего аммиака можно регулировать, используя в качестве индикатора измеренные значения концентрации иона аммония или аммиака в среде или выделяемого газа. Кроме того, концентрацию общего аммиака можно отрегулировать путем предварительного определения значения рН, обеспечивающего приемлемую концентрацию общего аммиака, при регулировании рН с помощью аммиака, и добавлять аммиак до достижения такого значения рН. В данном случае значение рН, определенное вышеописанным способом, при необходимости можно изменить во время культивирования.
Концентрацию общего аммиака в среде можно также отрегулировать, добавляя в среду аммиак или мочевину при уменьшении или отсутствии активности микроорганизма, определяемой на основании таких индикаторов, как концентрация растворенного кислорода в среде, скорость потребления источника углерода в среде, помутнение среды, продуцирование основного вещества и изменение значения рН в среде. То есть при сокращении или истощении источника азота в среде уменьшается или прекращается пролиферация микроорганизма или активность микроорганизма, такая как продуцирование целевого вещества. Активность микроорганизма обычно проявляется в потреблении растворенного кислорода и источника углерода в среде, увеличении мутности среды, сокращении продуцирования целевого вещества и уменьшении значения рН среды вследствие потребления аммиака или высвобождения диоксида углерода в результате дыхания. Таким образом, в случае уменьшения или прекращения активности микроорганизма концентрация растворенного кислорода в среде увеличивается при постоянной скорости аэрации и перемешивания в единицу времени, при этом значение рН среды возрастает вследствие меньшего потребления аммиака и секреции диоксида углерода. Кроме того, уменьшается скорость потребления источника углерода, замедляется помутнение среды и продуцирование целевого вещества. Поэтому сокращение активности микроорганизма, определяемой на основании вышеуказанных индикаторов в условиях достаточного количества других компонентов в среде помимо источника азота, свидетельствует об недостаточном источнике азота или его полном истощении. В таком случае в среду добавляют аммиак или мочевину в количестве, необходимом для роста микроорганизма или продуцирования целевого вещества. В результате повторного выполнения данной операции общая концентрация аммиака в среде сохраняется в пределах определенного диапазона. Если культивирование выполняют с добавлением мочевины в среду, при потреблении микроорганизмом мочевины в среду высвобождается аммиак. При повторном добавлении аммиака или мочевины в соответствии с вышеизложенным показатель рН среды постепенно увеличивается. Количество аммиака или мочевины, добавляемое в каждый период времени, может составлять, например, 300 мМ, предпочтительно 200 мМ, более предпочтительно 100 мМ, в виде конечной концентрации общего аммиака в среде. Альтернативно аммиак или мочевину можно добавлять так, чтобы значение рН после добавления аммиака или мочевины увеличивалось на 0,3 или меньше, предпочтительно на 0,15 или меньше, более предпочтительно на 0,1 или меньше.
Концентрацию растворенного кислорода в среде можно измерить, например, при помощи электрода для растворенного кислорода.
То, что сумма ионных эквивалентов ионов бикарбоната и/или карбоната и других анионов, растворенных в среде, выше ионного эквивалента основного вещества, аккумулированного в среде, можно определить путем измерения концентраций ионов бикарбоната, ионов карбоната и других анионов, а также концентрации основного вещества. Кроме того, вышеуказанные условия могут быть также удовлетворены в результате выполнения предварительного эксперимента с целью определения значения рН и/или дополнительного количества аммиака, соответствующего указанным условиям, и осуществления культивирования при заранее определенном значении рН и/или добавлении заранее определенного количества аммиака.
В настоящем изобретении значение рН культуры может быть постоянным или непостоянным. Кроме того, значения рН среды можно регулировать, используя сам показатель рН в качестве индикатора, или косвенным путем, контролируя концентрацию общего аммиака, не прибегая к прямому регулированию значения рН. При добавлении аммиака или мочевины, когда индикатором служит активность микроорганизма в соответствии с приведенным выше описанием, концентрацию общего аммиака в среде регулируют так, чтобы данный показатель находился в пределах приемлемого диапазона концентраций, при этом значение рН постепенно увеличивается по мере аккумулирования основного вещества. Если в процессе культивирования концентрацию общего аммиака регулируют в пределах определенного диапазона, значение рН изменяется в результате изменения баланса аккумулирования разных катионов и анионов в среде. Независимо от выбранного способа концентрация общего аммиака в среде остается в пределах определенного диапазона концентраций, что позволяет сократить количество ионов сульфата и/или хлорида, используемых в качестве противоионов основного вещества.
В настоящем изобретении выражение "не ингибирующий продуцирование основного вещества" означает, что созданы благоприятные условия для роста микроорганизма по настоящему изобретению и продуцирования основного вещества. В том случае, если рост микроорганизма является недостаточным или не достигается эффективное продуцирование основного вещества несмотря на благоприятный рост микроорганизма, считается, что имеет место ингибирование продуцирования основного вещества.
В частности, микроорганизм, используемый в настоящем изобретении, культивируют при разных значениях рН и концентрациях общего аммиака в среде, измеряя продуцирование основного вещества, аккумулируемого в среде, при этом концентрации общего аммиака, которые обеспечивают продуцирование основного вещества на уровне, равном предпочтительно 50% или выше, более предпочтительно 70% или выше, особенно предпочтительно 90% или выше, по сравнению с количеством основного вещества, получаемого в оптимальных условиях, например, в стандартных условиях с нейтральным значением рН, считаются концентрациями, "не ингибирующими продуцирование основного вещества". В настоящем изобретении термин "продуцирование" означает выход продукта, скорость продуцирования или общее продуцированное количество. Термин "выход" означает количество продуцированного основного вещества в расчете на источник углерода, присутствующий в среде, который может потребляться микроорганизмом, и термин "скорость продуцирования" означает количество продукта, продуцируемого в единицу времени. Кроме того, когда термин "количество продукта" или "продуцированное количество" используется отдельно, он означает количество основного вещества, аккумулированного в среде, после полного потребления источника углерода.
Альтернативно микроорганизм, используемый в настоящем изобретении, культивируют в оптимальных условиях, например, в стандартных условиях с нейтральным значением рН, и измеряют продуцирование основного вещества, аккумулированного в среде. Тогда культивирование осуществляют в среде, имеющей такой же состав, за исключением того, что количество ионов сульфата и/или хлорида уменьшают на требуемую величину, и измеряют продуцирование основного вещества. В данном случае имеет место период, когда значение рН среды увеличивается вследствие недостатка ионов сульфата и/или хлорида, используемых в качестве противоионов, по мере аккумулирования целевого основного вещества. В течение указанного периода культивирование выполняют при сохранении концентрации общего аммиака в пределах определенного диапазона концентраций. Что касается диапазона, в пределах которого контролируют концентрацию, то культивирование выполняют при разных концентрациях в диапазоне от 1 до 500 мМ, при этом концентрации, обеспечивающие продуцирование основного вещества на уровне, равном предпочтительно 50% или выше, более предпочтительно 70% или выше, особенно предпочтительно 90% или выше, по сравнению с продуцированием, достигаемым в оптимальных условиях, определяются как концентрации, "не ингибирующие продуцирование основного вещества". Примеры среды, используемой для создания вышеуказанных "стандартных условий с нейтральным значением рН", включают среду, содержащую ионы сульфата и/или хлорида в количестве, достаточном для культивирования при значении рН 7,2 или ниже.
Требуемое уменьшение количества ионов сульфата и/или хлорида не имеет конкретных ограничений, если достигается необходимое продуцирование основного вещества.
Концентрацию общего аммиака, определяемую как "не ингибирующая продуцирование основного вещества", можно также охарактеризовать, например, следующим образом. Микроорганизм, используемый в настоящем изобретении, культивируют при разных значениях рН и концентрациях общего аммиака в среде, измеряя при этом количество основного вещества, аккумулируемого в среде. Аккумулированное количество основного вещества, получаемое в разных условиях, сравнивают с количеством, аккумулированным в оптимальных условиях. Таким образом можно определить концентрацию общего аммиака, которая не ингибирует продуцирование основного вещества. Оптимальные условия определяются как условия культивирования с использованием достаточного количества противоионов при нейтральном значении рН, как это имеет место в стандартных условиях с нейтральным значением рН.
Кроме того, существует другой способ определения концентрации общего аммиака, определяемой как "не ингибирующая продуцирование основного вещества". Микроорганизм, используемый в настоящем изобретении, культивируют в оптимальных условиях, например, в стандартных условиях с нейтральным значением рН, измеряя при этом продуцирование основного вещества, аккумулируемого в среде. Культивирование выполняют в среде, имеющей такой же состав, за исключением того, что количество ионов сульфата и/или хлорида уменьшают на требуемую величину, и контролируют продуцирование. В данном случае имеет место период, когда значение рН среды увеличивается вследствие недостатка ионов сульфата и/или хлорида, используемых в качестве противоионов, по мере аккумулирования целевого основного вещества. В течение указанного периода культивирование выполняют при сохранении концентрации общего аммиака в пределах определенного диапазона концентраций. Что касается диапазона регулирования концентраций, то культивирование выполняют при разных концентрациях в пределах от 1 до 500 мМ и продуцирование основного вещества сравнивают с аналогичным показателем, достигаемым в оптимальных условиях.
Концентрация, определяемая как "не ингибирующая продуцирование основного вещества" включает, например, концентрацию, которая обеспечивает продуцирование основного вещества на уровне, равном предпочтительно 50% или выше, более предпочтительно 70% или выше, особенно предпочтительно 90% или выше, по сравнению с продуцированием основного вещества в оптимальных условиях. В частности, концентрация общего аммиака в среде, например, составляет предпочтительно 300 мМ или меньше, более предпочтительно 200 мМ или меньше, особенно предпочтительно 100 мМ или меньше. Степень диссоциации аммиака уменьшается при увеличении значения рН. Недиссоциированный аммиак является более токсичным для бактерий, чем ионы аммония. Поэтому верхний предел концентрации общего аммиака зависит также от значения рН среды. То есть по мере увеличения значения рН среды приемлемая концентрация общего аммиака становится ниже. Что касается вышеуказанной концентрации общего аммиака, определяемой как "не ингибирующая продуцирование основного вещества", то диапазон концентраций общего аммиака, приемлемый для самого высокого значения рН во время культивирования, можно рассматривать как диапазон концентраций общего аммиака на протяжении всего культивирования.
С другой стороны, общая концентрация аммиака, используемого в качестве источника азота, необходимого для роста микроорганизма и продуцирования основного вещества, не имеет конкретных ограничений до тех пор, пока продуцирование целевого вещества микроорганизмом не уменьшается вследствие недостатка азота в процессе культивирования, и может быть определена соответствующим образом. Например, концентрацию аммиака измеряют в процессе культивирования и при отсутствии аммиака в среде добавляют в среду небольшое количество аммиака. Хотя концентрация аммиака после его добавления не имеет конкретных ограничений, желательно, чтобы указанная концентрация была равна предпочтительно 1 мМ или выше, более предпочтительно 5 мМ или выше, особенно предпочтительно 10 мМ или выше в расчете на концентрацию общего аммиака.
Способ по настоящему изобретению может включать стадию культивирования, предназначенную для пролиферации микроорганизма, обладающего способностью продуцировать основное вещество, и стадию культивирования, предназначенную главным образом для продуцирования микроорганизмом основного вещества. Кроме того, в способе по настоящему изобретению пролиферация микроорганизма и продуцирование основного вещества могут происходить параллельно. Помимо вышеописанного культивирования, которое может быть также названо основной ферментацией, основным культивированием или тому подобным, независимо может быть выполнено предварительное культивирование.
В настоящем изобретении помимо регулирования концентрации общего аммиака в среде вышеописанным способом может быть выполнена операция, облегчающая растворение ионов бикарбоната и/или карбоната в среде. Примеры такой операции включают создание положительного давления в ферментере во время культивирования в результате введения в среду газообразного диоксида углерода или газовой смеси, содержащей газообразный диоксид углерода, ограничение аэрации в ферментере, благодаря чему ионы бикарбоната и/или карбоната растворяются в среде, увеличение значения рН среды путем добавления в среду катионов, отличных от ионов аммония, таких как ионы натрия, ионы калия и тому подобные.
Для создания положительного давления в ферментере, например, можно повысить давление воздуха, подаваемого в ферментер, по сравнению с давлением отходящего газа. В результате повышения давления в ферментере газообразный диоксид углерода, образующийся в процессе ферментации, растворяется в культуральной среде и образует ионы бикарбоната или карбоната. В частности, давление в ферментере может быть равно 0,13-0,3 МПа, предпочтительно 0,15-0,25 МПа.
Кроме того, газообразный диоксид углерода можно растворить в культуральной среде путем введения в среду газообразного диоксида углерода или газовой смеси, содержащей газообразный диоксид углерода. Альтернативно газообразный диоксид углерода, образующийся в процессе ферментации, может также растворяться в среде при ограничении аэрации ферментера. Приемлемую скорость аэрации можно определить, например, измеряя количество ионов бикарбоната или карбоната в среде или измеряя значение рН и концентрацию аммиака в среде. При введении в среду газообразного диоксида углерода, например, чистого газообразного диоксида углерода или газовой смеси, содержащей газообразный диоксид углерода в количестве 5 об.% или больше, газ можно барботировать в среду. Вышеуказанные способы растворения ионов бикарбоната и/или карбоната в среде могут быть использованы независимо или в виде комбинации двух или более способов.
Операцию регулирования концентрации общего аммиака в среде и операцию облегчения растворения ионов бикароната и/или карбоната в среде при необходимости можно выполнять в течение по крайней мере части общего периода времени процесса культивирования.
Хотя время, определяемое выражением "по крайней мере часть общего периода времени", не имеет каких-либо конкретных ограничений, пока достигается требуемое продуцирование, оно может составлять, например, 1/10 или больше, предпочтительно 1/5 или больше от общего времени основного культивирования. В частности, примеры указанного периода времени включают период, когда значение рН среды увеличивается вследствие недостатка противоионов, таких как ионы сульфата и/или хлорида, по мере аккумулирования целевого основного вещества, или период, когда значение рН среды увеличивается в результате добавления катионов, или оба указанных периода.
Среда, используемая в настоящем изобретении, не имеет каких-либо конкретных ограничений, если концентрация общего аммиака может быть отрегулирована в пределах вышеуказанного диапазона и среда, содержащая органические и неорганические питательные вещества, такие как источник углерода, источник азота и другие питательные микроэлементы, остается приемлемой для используемого микроорганизма.
Можно использовать любой источник углерода, пригодный для потребления микроорганизмом, и примеры таких источников включают сахариды, такие как сахароза, глюкоза, фруктоза, моласса и гидролизат крахмала, органические кислоты, такие как уксусная кислота, спирты, такие как этанол, и углеводороды, такие как метан.
Примеры источника азота включают неорганические вещества, такие как аммиак, гидролизаты белка, дрожжевой экстракт и тому подобные. Примеры питательных микроэлементов включают аминокислоты, витамины и микропримеси металлов.
Примеры анионов, отличных от ионов бикарбоната и/или карбоната, которые присутствуют в среде, включают ионы хлорида, ионы сульфата, ионы фосфата, ионизированные органические кислоты, ионы гидроксида и тому подобные. Сумма ионных эквивалентов вышеуказанных других ионов обычно равна 900 мэкв/л или меньше, предпочтительно 700 мэкв/л или меньше, более предпочтительно 500 мэкв/л или меньше, еще предпочтительнее 300 мэкв/л или меньше, особенно предпочтительно 200 мэкв/л или меньше.
Одним объектом настоящего изобретения является уменьшение количества используемых ионов сульфата и/или хлорида и ионного эквивалента ионов сульфата или хлорида, при этом сумма ионных эквивалентов указанных ионов, присутствующих в среде, обычно равна 700 мэкв/л или меньше, предпочтительно 500 мэкв/л или меньше, более предпочтительно 300 мэкв/л или меньше, еще предпочтительнее 200 мэкв/л или меньше, особенно предпочтительно 100 мэкв/л или меньше.
Схема ферментации не имеет каких-либо конкретных ограничений и может представлять собой периодическое культивирование, в соответствии с которым среду не добавляют, культивирование с подпиткой, в соответствии с которым среду вводят после потребления загруженного сахара, непрерывное культивирование, в соответствии с которым среду удаляют, когда объем среды превышает объем, допустимый для ферментера, культивирование с рециркуляцией клеток, в соответствии с которым бактериальные клетки рециркулируют, и тому подобные. Температура культивирования может быть определена в зависимости от выбранного микроорганизма. Указанная температура обычно равна 25-45°С, предпочтительно 30-40°С. Кроме того, желательно перемешивать культуру для поступления в среду достаточного количества кислорода во время ферментации.
Культивирование с целью продуцирования целевого основного вещества выполняют, например, следующим образом. Получают среду, содержащую типичные компоненты, но при этом удаляют большую часть или все соли аммония, такие как сульфат аммония и хлорид аммония. Микроорганизм, который культивировали отдельно, инокулируют в указанную среду и культивируют, регулируя концентрацию общего аммиака в пределах диапазона, приемлемого для выбранного микроорганизма, который определяют вышеописанным способом. Концентрацию аммиака в среде, находящейся в ферментере, или в образце среды можно измерить, например, при помощи коммерчески доступного измерителя ионов или подобного устройства. Используя измеренные значения в качестве индикатора, можно регулировать концентрацию общего аммиака. Для сохранения концентрации общего аммиака в заранее определенном диапазоне концентраций в среду можно добавить газообразный аммиак, водный раствор аммиака или мочевину. Концентрацию общего аммиака в среде можно также измерить непрямым методом путем измерения концентрации аммиака в отходящем газе, удаляемом из ферментера, при помощи стандартного электрода для аммиака.
Кроме того, при осуществлении настоящего изобретения концентрацию общего аммиака в среде можно регулировать нижеследующим методом, используя значение рН среды в качестве вышеуказанного индикатора.
Культивирование выполняют в среде, имеющей такой же состав, что и среда, содержащая ионы сульфата и/или хлорида в количестве, достаточном для сохранения показателя рН равным 7,2 или ниже, за исключением уменьшения количества ионов сульфата и/или хлорида на требуемую величину при разных значениях рН, причем уровень рН изменяют, добавляя по крайней мере одно из нижеследующих веществ, включающих газообразный аммиак, водный раствор аммиака и мочевину, и продолжают культивирование, сохраняя концентрацию общего аммиака в среде в пределах предпочтительного диапазона концентраций путем введения в среду по крайней мере одного из нижеследующих веществ, включающих газообразный аммиак, водный раствор аммиака и мочевину, с учетом таких индикаторов, как изменение концентрации растворенного кислорода в среде, изменение скорости потребления углерода в среде, изменение мутности среды, изменение значения рН в среде и тому подобные, при непрямом измерении в течение периода времени, когда значение рН среды невозможно сохранить равным 7,2 или ниже вследствие недостатка противоионов для основного вещества, аккумулированного в среде.
Примеры основного вещества, продуцируемого способом по настоящему изобретению, включают основные аминокислоты, в частности, L-лизин, L-аргинин и L-гистидин. Из указанных аминокислот L-лизин является наиболее предпочтительным.
Микроорганизм, способный продуцировать основное вещество, не имеет каких-либо конкретных ограничений, и для указанной цели может быть выбран любой микроорганизм, если он способен продуцировать основное вещество путем ферментации. В частности, предпочтительно выбирают микроорганизм, который эффективно продуцирует основное вещество даже при высоком значении рН среды, если концентрация общего аммиака в среде является низкой. Примеры такого микроорганизма включают бактерии, относящиеся к коринеформным бактериям, роду Escherichia, Serratia или Bacillus.
Коринеформные бактерии и бактерии Escherichia будут рассмотрены ниже, однако микроорганизм, используемый в способе по настоящему изобретению, не ограничивается указанными бактериями.
Коринеформные бактерии, используемые в настоящем изобретении, включают бактерии Corynebacterium и бактерии, которые ранее были классифицированы как род Brevibacterium, но затем были переклассифицированы в род Corynebacterium (Int. J. Syst. Bacteriol., 41, 255 (1981)), а также бактерии, относящиеся к роду Brevibacterium, которые чрезвычайно близки к роду Corynebacterium. Конкретные примеры включают нижеследующие бактерии:


В объем настоящего изобретения, в частности, входят нижеследующие штаммы:

Примеры бактерий Escherichia включают Escherichia coli. Для создания штамма Escherichia coli методами рекомбинантных ДНК может быть выбран штамм К12 E.coli и его производные, то есть штамм MG1655 E.coli (ATCC № 47076), штамм W3110 (АТСС № 27325) и тому подобные. Штамм К12 E.coli был выделен в Станфордском университете в 1922 г. и представляет собой лизогенные бактерии λ-фага. Кроме того, указанный штамм является очень гибким штаммом, имеющим F-половой фактор, для которого могут быть созданы генетические рекомбинантны путем конъюгирования или подобными методами. Кроме того, определена геномная последовательность штамма К12 E.coli и генетическая информация является общедоступной. Штамм К12 E.coli и его производные можно получить из Американской коллекции типовых культур (АТСС, адрес: P.O. Box 1549, Manassas, VA 20108, United States of America).
Примеры коринеформных бактерий, способных продуцировать L-лизин, включают мутантные штаммы, устойчивые к S-(2-аминоэтил)цистеину (далее использована аббревиатура "AEC"), мутантные штаммы, которым для роста необходима аминокислота, такая как L-гомосерин (публикации патентов Японии (Kokoku) № 48-28078 и 56-6499), мутантные штаммы, устойчивые к АЕС и требующие присутствия аминокислоты, такой как L-лейцин, L-гомосерин, L-пролин, L-серин, L-аргинин, L-аланин и L-валин (патенты США № 3708395 и 3825472), продуцирующие L-лизин мутантные штаммы, обладающие устойчивостью к DL-α-амино-ε-капролактаму, α-аминолауриллактаму, аналогу аспарагиновой кислоты, сульфат-содержащим лекарственным средствам, хиноиду и N-лауроиллейцину, продуцирующие L-лизин мутантные штаммы, обладающие устойчивостью к оксалоацетат-декарбоксилазе или ингибитору ферментов дыхательных путей (выложенные патенты Японии № 50-53588, 50-31093, 52-102498, 53-9394, 53-86089, 55-9783, 55-9759, 56-32995, 56-39778, публикации патентов Японии №№ 53-43591 и 53-1833), продуцирующие L-лизин мутантные штаммы, требующие присутствия инозита или уксусной кислоты (выложенные патенты Японии № 55-9784 и 56-8692), продуцирующие L-лизин мутантные штаммы, чувствительные к фторпирувиновой кислоте или температуре, равной 34°С или выше (выложенные патенты Японии № 55-9783 и 53-86090), продуцирующие L-лизин мутантные штаммы бактерий Brevibacterium или Corynebacterium, обладающие устойчивостью к этиленгликолю (заявка на патент США № 333455), и тому подобные.
Конкретные примеры включают, например, штаммы ATCC 31269 Brevibacterium lactofermentum, ATCC 21475 Brevibacterium flavum и ATCC 21491 Corynebacterium acetoglutamicum.
Штамм ATCC 13869/pVK-C*, plysE Brevibacterium lactofermentum, описанный в примерах, также является предпочтительным продуцирующим L-лизин штаммом коринеформных бактерий. Указанный штамм был получен путем введения плазмиды pVK-C*, содержащей ген, кодирующий аспартокиназу, десенсибилизированную в отношении ингибирования по типу обратной связи L-лизином и L-треонином (lysC*), и плазмиды plysE (заявка на патент США № 2003/113899), содержащей ген lysE, гомологичный гену, стимулирующему секрецию L-лизина, который известен для бактерий Corynebacterium (международная публикация 9723597А2), в штамм АТСС 13869, который является штаммом Brevibacterium lactofermentum дикого типа.
Ген lysC* может быть выделен, например, из продуцирующего L-лизин мутантного штамма AJ3463 (FERM P-1987) (см. публикацию патента Японии № 51-34477), который был создан путем мутагенеза штамма АТСС 13869. Штамм AJ3463 депонирован в Международный депозитарий патентуемых организмов, Национальный институт передовой промышленной науки и технологии (ранее именовавшийся Национальным институтом биологической науки и технологии изучения человека, Агентство промышленной науки и технологии, адрес: Tsukuba Central 6, 1-1, Higashi 1-Chome, Tsukuba-shi, Ibaraki-ken, 305-8566, Japan) 22 марта 1973 г. под номером доступа FERM P-1987. Кроме того, фрагмент гена lysC* можно также выделить из штамма AJ2691 Brevibacterium lactofermentum, который содержит плазмиду p399AK9B, включающую данный ген. Штамм AJ12691 депонирован в Международный депозитарий патентуемых организмов, Национальный институт передовой промышленной науки и технологии, 10 апреля 1992 г. под номером доступа FERM P-12918. Указанный штамм приобрел статус международного депозита согласно условиям Будапештского соглашения 10 февраля 1995 г. под номером доступа FERM BP-4999. Плазмида р399АК9В (патент США № 5766925) была получена путем введения фрагмента ДНК, обеспечивающего автономную репликацию указанной плазмиды в бактериях Corynebacterium, в плазмиду р399АК9, которая была получена путем введения гена lysC, выделенного из штамма AJ3463, в клонирующий вектор pHSG399 (см. публикацию Takeshita, S. et al., Gene (1987), 61, 63-74).
В вышеуказанной десенсибилизированной аспартокиназе остаток аланина в положении 279 α-субъединицы и остаток аланина в положении 30 β-субъединицы аспартокиназы дикого типа заменены остатками треонина. α-Субъединица и β-субъединица кодированы в одной рамке считывания гена lysC. Нуклеотидная последовательность гена lysC* и аминокислотная последовательность α-субъединицы десенсибилизированной аспартокиназы представлены в списке последовательностей соответственно SEQ ID NO:5 и 6; нуклеотидная последовательность того же гена и аминокислотная последовательность β-субъединицы десенсибилизированной аспартокиназы представлены соответственно SEQ ID NO:7 и 8.
Ген lysE коринеформных бактерий можно получить методом PCR (полимеразная цепная реакция, см. публикацию White, T.J. et al., Trends Genet., 5, 185 (1989)) с использованием праймеров на основе описанной нуклеотидной последовательности (номер доступа в банке генов GenBank X96471), например, праймеров, представленных SEQ ID NO:3 и 4, и хромосомной ДНК коринеформных бактерий в качестве матрицы. Нуклеотидная последовательность фрагмента ДНК, содержащего гены LysG и lysE Corynebacterium glutamicum (номер доступа в банке генов GenBank X96471), представлена SEQ ID NO:10, и аминокислотная последовательность белка LysE, кодированного указанным геном, представлена SEQ ID NO:9. Белок LysG кодирован комплементарной последовательностью, соответствующей нуклеотидам 1723-2352 в SEQ ID NO:8.
ДНК, кодирующие α-субъединицу, β-субъединицу и белок LysE аспартокиназы, включают ДНК, кодирующие белки, которые могут содержать делеции, замены, инсерции или добавления одного или нескольких аминокислотных остатков в одном или нескольких положениях каждого белка при условии сохранения активности указанных белков. Хотя число аминокислотных остатков, определяемое термином "несколько", может изменяться в зависимости от положений в трехмерных структурах белков и типов аминокислотных остатков, число аминокислотных остатков предпочтительно равно 2-30, более предпочтительно 2-20, особенно предпочтительно 2-10 для каждого белка. Подобный вывод сделан на основании следующих факторов. Некоторые аминокислоты являются очень гомологичными, и различия между такими аминокислотами не оказывают существенного влияния на трехмерные структуры и активность белков. Поэтому каждый белок может быть белком, который на 50% или больше, предпочтительно на 70% или больше, более предпочтительно на 90% или больше, особенно предпочтительно на 95% или больше гомологичен аминокислотным остаткам SEQ ID NO:6, 8 или 10 и обладает активностью аспартокиназы или белка LysE.
Вышеописанная модификация белков является консервативной мутацией, сохраняющей активность каждого белка. Замена является изменением, в соответствии с которым удаляют по крайней мере один остаток аминокислотной последовательности и вводят другой остаток. Примеры замены первоначального аминокислотного остатка другим аминокислотным остатком, рассматриваемой в качестве консервативной замены, включают замену остатка ala остатком ser или thr, замену остатка arg остатком gln, his или lys, замену остатка asn остатком glu, gln, lys, his или asp, замену остатка asp остатком asn, glu или gln, замену остатка cys остатком ser или ala, замену остатка gln остатком asn, glu, lys, his, asp или arg, замену остатка glu остатком asn, gln, lys или asp, замену остатка gly остатком pro, замену остатка his остатком asn, lys, gln, arg или tyr, замену остатка ile остатком leu, met, val или phe, замену остатка leu остатком ile, met, val или phe, замену остатка lys остатком asn, glu, gln, his или arg, замену остатка met остатком ile, leu, val или phe, замену остатка phe остатком trp, tyr, met, ile или leu, замену остатка ser остатком thr или ala, замену остатка thr остатком ser или ala, замену остатка trp остатком phe или tyr, замену остатка tyr остатком his, phe или trp и замену остатка val остатком met, ile или leu.
ДНК, кодирующую белок, по существу аналогичный белку, имеющему аминокислотную последовательность, представленную SEQ ID NO:6, 8 или 10, можно получить путем модификации нуклеотидной последовательности, кодирующей аминокислотную последовательность, представленную SEQ ID NO:6, 8 или 10, например, методом сайт-специфического мутагенеза с заменой, делецией, инсерцией или добавлением одного или нескольких аминокислотных остатков. Такую модифицированную ДНК можно получать стандартным методом, включающим обработку реагентом, или в условиях, вызывающих мутацию. Примеры такой обработки включают обработку ДНК, кодирующей белок по настоящему изобретению, гидроксиламином, ультрафиолетовое облучение микроорганизма, содержащего данную ДНК, обработку таким реагентом, как N-метил-N'-нитро-N-нитрозогуанидин или азотистая кислота.
ДНК, кодирующую вышеописанный модифицированный белок, можно также получить, выделяя ДНК, способную гибридизировать с геном lysC, геном lysE или фрагментом указанных генов в строгих условиях и кодирующую белок, обладающий активностью аспартокиназы или активностью белка LysE. Термин "строгие условия" означает условия, в которых образуется так называемый специфический гибрид и не образуется неспецифический гибрид. Строгие условия включают, например, условия, в которых могут гибридизировать ДНК с высокой степенью гомологии, например, ДНК со степенью гомологии не менее 70%, предпочтительно не менее 80%, более предпочтительно не менее 90%, особенно предпочтительно не менее 95%. Строгие условия включают также типичные условия промывки при гибридизации методом саузерн-блоттинга, то есть 1 х SSC, 0,1% SDS, предпочтительно 0,1 х SSC, 0,1% SDS, при 60°С.
Примеры продуцирующих L-лизин бактерий, относящихся к роду Escherichia, включают мутанты, обладающие устойчивостью к аналогам L-лизина. Аналоги L-лизина ингибируют рост бактерий Escherichia, но указанное ингибирование полностью или частично устраняется при наличии в среде L-лизана. Примеры аналогов L-лизина включают оксализин, гидроксамат лизина, (S)-(2-аминоэтил)-L-цистеин (АЕС), γ-метиллизин, α-хлоркапролактам и тому подобные. Мутанты, обладающие устойчивостью к аналогам лизина, можно получить, подвергая микроорганизмы Escherichia стандартной искусственной мутации. Конкретные примеры бактериальных штаммов, используемых для продуцирования L-лизина, включают штамм AJ11442 E.coli (FERM BP-1543, NRRL B-12185; см. выложенный патент Японии № 56-18596 и патент США № 4346170) и штаммы VL611 E.coli. Штамм AJ11442 депонирован в Международный депозитарий патентуемых организмов, Национальный институт передовой промышленной науки и технологии (ранее именовавшийся Национальным институтом биологической науки и технологии изучения человека, Агентство промышленной науки и технологии, адрес: Tsukuba Central 6, 1-1, Higashi 1-Chome, Tsukuba-shi, Ibaraki-ken, 305-8566, Japan) 1 мая 1981 г. под номером доступа FERM P-5084. Указанный штамм приобрел статус международного депозита согласно условиям Будапештского соглашения 29 октября 1987 г. под номером доступа FERM BP-1543. В указанных микроорганизмах десенсибилизировано ингибирование аспартокиназы по типу обратной связи L-лизином.
В качестве предпочтительных бактерий, продуцирующих L-лизин, можно также использовать, например, бактерии с повышенной экспрессией гена, кодирующего фермент, участвующий в биосинтезе L-лизина, отличный от десенсибилизированной аспартокиназы. Примеры такого фермента включают ферменты, участвующие в метаболизме диаминопимелата, такие как дигидродипиколинат-синтаза, дигидродипиколинат-редуктаза, диаминопимелат-декарбоксилаза, диаминопимелат-дегидрогеназа (все вышеуказанные ферменты описаны в международной публикации патента WO 96/40934), фосфоенолпируват-карбоксилаза (выложенный патент Японии № 60-87788), аспартат-аминотрансфераза (публикация Японии № 6-102028), диаминопимелат-эпимераза (выложенный патент Японии № 2003-135066) и дегидрогеназа полуальдегида аспарагиновой кислоты (международная публикация WO 00/61723), ферменты, участвующие в метаболизме аминоадипита, такие как гомоаконитат-гидратаза (выложенный патент Японии № 2000-157276) и тому подобные.
Конкретные примеры штаммов E.coli, способных продуцировать L-лизин, включают штамм W3110(tyrA)/pCABD2 E.coli (международная публикация WO 95/16042) и т.п. Штамм W3110(tyrA)/pCABD2 E.coli был получен путем введения плазмиды рСАВD2, содержащей гены, кодирующие ферменты системы биосинтеза L-лизина, в штамм W3110(tyrA), который является штаммом с отсутствием tyrA E.coli (указанный штамм получил название AJ12604 и был депонирован в Международный депозитарий патентуемых организмов, Национальный институт передовой промышленной науки и технологии (ранее именовавшийся Национальным институтом биологической науки и технологии изучения человека, Агентство промышленной науки и технологии, адрес: Tsukuba Central 6, 1-1, Higashi 1-Chome, Tsukuba-shi, Ibaraki-ken, 305-8566, Japan) 28 января 1991 г. под номером доступа FERM P-11975, затем данный штамм приобрел статус международного депозита согласно условиям Будапештского соглашения 26 сентября 1991 г под номером доступа FERM BP-3579).
Плазмида pCABD2 содержит ген, кодирующий мутантную дигидродипиколинат-синтазу, в которой остаток гистидина в положении 118 мутирован в остаток тирозина и десенсибилизировано ингибирование по типу обратной связи L-лизином, ген, кодирующий мутантную аспартокиназу III, в которой остаток треонина в положении 352 мутирован в остаток изолейцина и десенсибилизировано ингибирование по типу обратной связи L-лизином, и гены, кодирующие дигидродипиколинат-редуктазу и диаминопимелат-дегидрогеназу.
Кроме того, штамм W3110(tyrA) E.coli может быть получен описанным ниже способом. Многие штаммы, полученные путем введения плазмиды в штамм W3110(tyrA), описаны в опубликованном описании европейского патента № 488424/1992. Например, штамм, полученный путем введения плазмиды pHATerm, получил название W3110(tyrA)/pHATerm E.coli и был депонирован в Национальный институт биологической науки и технологии изучения человека, Агентство промышленной науки и технологии под номером доступа FERM BP-3653. Штамм W3110(tyrA) можно получить, например, путем удаления плазмиды pHATerm из штамма W3110(tyrA)/pHATerm E.coli. Указанную плазмиду можно удалить стандартным методом.
В качестве штамма E.coli, продуцирующего L-лизин, можно также использовать штамм WC196 (см. международную публикацию WO 96/17930). Штамм WC196 создавали, сообщая устойчивость к АЕС (S-(2-аминоэтил)цистеину) штамму W3110, выделенному из К-12 E.coli. Указанный штамм получил назначение AJ13069 E.coli и был депонирован в Национальный институт биологической науки и технологии изучения человека, Агентство промышленной науки и технологии (в настоящее время Международный депозитарий патентуемых организмов, Национальный институт передовой промышленной науки и технологии (Tsukuba Central 6, 1-1, Higashi 1-Chome, Tsukuba-shi, Ibaraki-ken, 305-8566, Japan) 6 декабря 1994 г. под номером доступа FERM P-14690. Указанный штамм приобрел статус международного депозита согласно условиям Будапештского соглашения 29 сентября 1995 г. под номером доступа FERM BP-5252.
Микроорганизм, пригодный для использования в настоящем изобретении, может характеризоваться пониженной активностью фермента, катализирующего реакцию образования соединений, метаболизм которых отклоняется от биосинтетического пути метаболизма L-лизина, или фермента, который снижает продуцирование L-лизина, или может не содержать такого фермента. Иллюстративные примеры фермента, участвующего в продуцировании L-лизина, включают гомосериндегидрогеназу, лизиндекарбоксилазу (cadA, ldcC) и фермент яблочной кислоты. Штаммы с пониженной активностью указанных ферментов или их отсутствием описаны в международных публикациях WO 95/23864, WO 96/17930, WO 2005/010175 и тому подобных.
Для снижения или устранения ферментативной активности гены, кодирующие ферменты в хромосоме, могут быть мутированы стандартным методом мутагенеза, в результате чего происходит снижение или устранение внутриклеточной активности ферментов. Например, указанная цель может быть достигнута в результате генетической рекомбинации, направленной на удаление генов, кодирующих такие ферменты в хромосоме, или модификацию экспрессии регуляторной последовательности, такой как промотор или последовательность Шайна-Дальгарно (SD). Указанная цель может быть также достигнута путем замены аминокислоты (миссенс-мутация), введения терминирущего кодона (нонсенс-мутация), введения мутации со сдвигом рамки, добавления или удаления одного или двух нуклеотидов в кодирующих областях ферментов в хромосоме или удаления части генов (Journal of Biological Chemistry, 272:8611-8617 (1997)). Ферментативную активность можно также уменьшить или устранить путем создания гена, кодирующего мутантный фермент с удаленной кодирующей областью, и замены гена дикого типа в хромосоме мутированным геном методом гомологичной рекомбинации или подобным методом или введения в ген транспозона или IS-фактора.
Например, для введения мутации, снижающей или устраняющей активность вышеуказанных ферментов путем генетической рекомбинации, могут быть использованы нижеследующие методы. Целевой ген в хромосоме может быть заменен мутантным геном, не способным продуцировать фермент, для чего неполную последовательность целевого гена модифицируют с образованием мутантного гена и коринеформную бактерию трансформируют ДНК, содержащей мутантный ген, вызывая рекомбинацию между мутантным геном и геном в хромосоме. Такой сайт-специфический мутагенез, основанный на замене генов методом гомологичной рекомбинации, описан в научной литературе, и известны методы с использованием линейной ДНК и методы с использованием плазмид, содержащих чувствительный к температуре ориджин репликации (Proc. Natl. Acad. Sci. USA, 2000, vol.97, No.12, pp.6640-6645; патент США № 6303383; выложенный патент Японии № 05-00791) и тому подобные. Кроме того, вышеописанный сайт-специфический мутагенез, основанный на замене генов методом гомологичной рекомбинации, может быть выполнен с использованием плазмиды, не способной реплицироваться в хозяине.
В настоящем изобретении могут быть также использованы микроорганизмы, модифицированные с увеличением экспрессии генов секреции L-лизина и L-аргинина, ybjE (международная публикация WO 2005/073390).
Примеры продуцирующих L-лизин бактерий, относящихся к роду Serratia, включают бактерии Serratia, трансформированные ДНК, кодирующей дигидродипиколинат-синтазу, которая имеет мутацию, десенсибилизирующую ингибирование по типу обратной связи L-лизином, и бактерии Serratia, содержащие аспартокиназу, десенсибилизированную в отношении ингибирования по типу обратной связи L-лизином (международная публикация WO 96/41871).
Примеры коринеформных бактерий, продуцирующих L-аргинин, включают штаммы коринеформных бактерий дикого типа: коринеформные бактерии, устойчивые к определенным агентам, включающим сульфатсодержащие лекарственные средства, 2-тиазолаланин, α-амино-β-гидроксивалериановую кислоту и тому подобные; коринеформные бактерии, ауксотрофные для L-гистидина, L-пролина, L-треонина, L-изолейцина, L-метионина или L-триптофана и, кроме того, устойчивые к L-тиазолаланину (выложенный патент Японии № 54-44096); коринеформные бактерии, устойчивые к кетомалоновой кислоте, фтормалоновой кислоте или монофторуксусной кислоте (выложенный патент Японии № 57-18989); коринеформные бактерии, устойчивые к аргининолу (выложенный патент Японии № 62-24075); коринеформные бактерии, устойчивые к Х-гуанидину (Х означает производное жирной кислоты или алифатическую цепь; выложенный патент Японии № 2-186995) и тому подобные. Коринеформные бактерии, в которых отсутствует репрессор L-аргинина (заявка на патент США № 2002/0045233), и коринеформные бактерии с повышенной активностью глутамат-дегидрогеназы (публикация европейского патента № 1057893) также являются приемлемыми штаммами для продуцирования L-аргинина.
Такие примеры, в частности, включают штаммы AJ11169 Brevibacterium flavum (FERM BP-6892), AJ12092 Corynebacterium glutamicum (FERM BP-6906), AJ11336 Brevibacterium flavum (FERM BP-6893), AJ11345 Brevibacterium flavum (FERM BP-6894) и AJ12430 Bravibacterium lactofermentum (FERM BP-2228). Штаммы AJ11169 и AJ12092 устойчивы к 2-тиазолаланину (выложенный патент Японии № 54-44096). Штамм AJ11336 устойчив к аргининолу и сульфадиазину (публикация Японии № 62-24075). Штамм AJ11345 устойчив к аргинину, 2-тиазолаланину и сульфагуанидину и является ауксотрофным для гистидина (публикация Японии № 62-24075). Штамм AJ12430 устойчив к октилгуанидину и 2-тиазолаланину (выложенный патент Японии № 2-186995).
Штамм AJ12092 Corynebacterium glutamicum был депонирован в Национальный институт биологической науки и технологии изучения человека, Агентство промышленной науки и технологии (в настоящее время Международный депозитарий патентуемых организмов, Национальный институт передовой промышленной науки и технологии, Tsukuba Central 6, 1-1, Higashi 1-Chome, Tsukuba-shi, Ibaraki-ken, 305-8566, Japan) 6 декабря 1994 г. под номером доступа FERM P-12092. Указанный штамм приобрел статус международного депозита согласно условиям Будапештского соглашения 1 октября 1999 г. под номером доступа FERM BP-6906.
Примеры бактерий Escherichia, способных продуцировать L-аргинин, включают бактерии E.coli, трансформированные геном argA (см. выложенный патент Японии № 57-5693), и штамм 237 E.coli (заявка на патент РФ № 2000117677), который является продуцирующим L-аргинин производным мутантного штамма, способного ассимилировать уксусную кислоту. Штамм 237 был депонирован в Российскую национальную коллекцию промышленных микроорганизмов (VKPM), генетика GNII (адрес: Россия, 117545, Москва, Дорожный проезд, 1) 10 апреля 2000 г. под номером доступа VKPM B-7925. Указанный штамм приобрел статус международного депозита согласно условиям Будапештского соглашения 18 мая 2001 г. Может быть также использован штамм 382 E.coli, который является мутантом, устойчивым к ингибированию по типу обратной связи L-аргинином (выложенный патент Японии № 2002-017342), и производным штамма 237. Штамм 382 E.coli депонирован в Российскую национальную коллекцию промышленных микроорганизмов (VKPM) под номером VKPM B-7926 10 апреля 2000 г. и приобрел статус международного депозита согласно условиям Будапештского соглашения 18 мая 2001 г.
Примеры бактерий Serratia, способных продуцировать L-аргинин, включают бактерии Serratia marcescens, не способные разлагать L-аргинин, устойчивые к антагонисту аргинина и канаванину и ауксотрофные для лизина (см. выложенный патент Японии № 52-8729).
Примеры коринеформных бактерий, способных продуцировать L-гистидин, включают микроорганизмы, относящиеся к роду бактерий Brevibacterium, устойчивых к антагонисту тиамина, в частности, штаммы FERM P-2170, FERM P-2316, FERM P-6478, FERM P-6479, FERM P-6480 и FERM P-6481 Brevibacterium lactofermentum (публикация выложенного патента Японии № 59-63194). Указанные примеры далее включают мутантные штаммы, относящиеся к родам бактерий Brevibacterium или Corynebacterium, устойчивым к поликетидам и способным продуцировать L-гистидин, в частности, штаммы FERM P-4161, FERM P-7273, FERM P-8371, FERM P-8372 и АТСС 14067.
Примеры бактерий Escherichia, способных продуцировать L-гистидин, включают мутантные штаммы, относящиеся к роду бактерий Escherichia, устойчивых к аналогу гистидина, например, штамм R-344 E.coli, и бактерии Escherichia, трансформированные генами ферментов системы синтеза L-гистидина, выделенными из штамма R-344. Указанные примеры, в частности, включают штаммы NRRL-12116, NRRL-12118, NRRL-12119, NRRL-12120 и NRRL-12121 E.coli (выложенный патент Японии № 56-5099).
Примеры бактерий Bacillus, способных продуцировать L-гистидин, включают мутантные штаммы, относящиеся к роду бактерий Bacillus, устойчивых к аналогу гистидина, и бактерии Bacillus, трансформированные геном, полученным из указанных мутантных штаммов, определяющих устойчивость к антагонисту гистидина. Указанные примеры, в частности, включают штаммы FERM BP-218, FERM BP-224 и FERM BP-219 (выложенный патент Японии № 58-107192).
Ферментационный бульон или обработанный продукт, включающий основное вещество, полученное способом по настоящему изобретению, содержит ионы карбоната или бикарбоната в качестве противоанионов для диссоциированного основного вещества. Указанные ионы карбоната или бикарбоната выделяются в виде газообразного диоксида углерода при нагревании или концентрировании культуральной среды и, в случае снижения значения рН среды, при добавлении сильной кислоты, такой как хлористоводородная кислота. Таким образом увеличивается относительное количество основного вещества среди твердых компонентов в ферментационном бульоне.
В соответствии с настоящим изобретением при использовании ионов бикарбоната, ионов карбоната или тому подобных вместо ионов хлорида и ионов сульфата количество ионов хлорида можно уменьшить даже до уровня, не вызывающего коррозию оборудования, или сократить количество ионов сульфата. После ферментации ионы бикарбоната и ионы карбоната можно заменить ионами хлорида путем добавления в среду хлористоводородной кислоты, при этом гидрохлорид лизина может быть получен в результате последующего концентрирования среды без ионного обмена, и, кроме того, можно сразу же отделить кристаллы гидрохлорида лизина.
В настоящем изобретении термин "продукт ферментации" означает концентрат и сухой продукт, полученный из ферментационного бульона, и продукты, полученные в результате обработки ферментационного бульона или сухого продукта.
Примеры
Настоящее изобретение далее будет рассмотрено более конкретно со ссылкой на нижеследующие примеры.
Пример 1
Создание коринеформной бактерии, продуцирующей L-лизин
Ген, кодирующий десенсибилизированную аспартокиназу, и ген, кодирующий фактор секреции лизина, вводили в коринеформную бактерию дикого типа для получения бактерии, продуцирующей L-лизин.
(1) Получение гена, кодирующего десенсибилизированную аспартокиназу
Ген (lysC*), кодирующий аспартокиназу (Ask*), десенсибилизированную в отношении ингибирования по типу обратной связи L-лизином и L-треонином, выделяли методом PCR из мутантного штамма, продуцирующего L-лизин, AJ3463 (FERM P-1987, см. публикацию патента Японии № 51-34477), полученного мутагенезом из штамма АТСС 13869 Corynebacterium glutamicum (Brevibacterium lactofermentum).
Штамм AJ3463 культивировали в среде СМ-Dex и из полученных клеток стандартным методом экстрагировали хромосомную ДНК (Biochem. Biophys. Acta., 72, 619-629 (1963)). Фрагмент ДНК, содержащий ген lysC* в качестве целевого гена, амплифицировали, используя указанную хромосомную ДНК в качестве матрицы с олигонуклеотидом ASK-F (SEQ ID NO:1) для введения сайта рестрикционного фермента BamHI у 5'-конца целевого фрагмента ДНК и с олигонуклеотидом ASK-R (SEQ ID NO:2) для введения сайта рестрикционного фермента KpnI у 3'-конца целевого фрагмента ДНК в качестве праймера для PCR. Для амплификации 25 раз повторяли цикл, включающий стадию денатурации при 98°С в течение 10 секунд, стадию гибридизации при 55°С в течение 30 секунд и стадию удлинения цепи при 72°С в течение 2 минут. Фермент, ДНК-полимеразу Pyrobest (Takara Shuzo) использовали в соответствии с инструкциями изготовителя.
Амплифицированный фрагмент ДНК очищали путем обработки фенолом/хлороформом и осаждения этанолом и расщепляли рестрикционными ферментами BamHI и KpnI. Полученную реакционную смесь разделяли с помощью электрофореза в агарозном геле, полосу, содержащую ген lysC*, вырезали и фрагмент гена очищали стандартными методами.
Шаттл-вектор для E.coli и Corynebacterium glutamicum, pVK7 (см. патент США № 6004773) отдельно обрабатывали рестрикционными ферментами BamHI и KpnI аналогичным образом и лигировали с вышеуказанным фрагментом lysC*. Компетентные клетки штамма JM109 E.coli (Takara Shuzo) трансформировали реакционной смесью для лигирования в соответствии с инструкциями изготовителя и отбирали несколько колоний, устойчивых к канамицину.
Вектор pVK7 был создан путем лигирования криптической плазмиды Brevibacterium lactofermentum, pAM330, с вектором для E.coli, pHSG299 (Kmr, см. публикацию Takeshita, S. et al., Gene, 61,63-74 (1987)) следующим образом (см. выложенный патент Японии № 11-266881, международную публикацию патента WO 99/07853). Плазмида рАМ330 была получена из штамма АТСС 13869 Brevibacterium lactofermentum. Вектор pHSG299 расщепляли AvaII (Takara Shuzo), дефосфолированным ДНК-полимеразой Т4, затем расщепляли HindIII (Takara Shuzo) и лигировали с рАМ330, дефосфолированным ДНК-полимеразой Т4. Таким образом был получен вектор pVK7. Вектор pVK7 автономно реплицируется в клетках E.coli и Brevibacterium lactofermentum и содержит сайт множественного клонирования, выделенный из pHSG299, lacZ', и ген устойчивости к канамицину в качестве маркера.
Плазмидные ДНК экстрагировали из устойчивых к канамицину колоний, полученных вышеописанным способом, при этом плазмида, содержащая целевой ген lysC*, получила название pVK-C*.
(2) Получение гена, кодирующего фактор секреции лизина lysE
Ген lysE выделяли при помощи PCR, используя хромосомную ДНК из штамма АТСС 13869 Brevibacterium lactofermentum в качестве матрицы (см. заявку на патент США № 2003/113899). Как известно, ген lysE стимулирует секрецию L-лизина в бактериях Corynebacterium (международная публикация 0723597А2). Хромосомная ДНК указанного штамма была получена вышеописанным методом.
LysE-F (SEQ ID NO:3) и LysE-R (SEQ ID NO:4) использовали в качестве праймеров. PCR выполняли, используя ДНК-полимеразу Pyrobest (Takara Shuzo), тепловую обработку производили при 94°С в течение 90 секунд и 30 раз повторяли нижеследующий цикл, включающий денатурацию при 94°С в течение 20 секунд, гибридизацию при 55°С в течение 30 секунд и реакцию удлинения цепи при 72°С в течение 60 секунд. Затем реакционную смесь инкубировали при 72°С в течение 10 минут. В результате выполнения указанной реакции был получен фрагмент ДНК требуемой длины. Полученный фрагмент ДНК очищали и клонировали в клонирующем векторе pCR2.1 (Invitrogene) в соответствии с инструкциями изготовителя. Компетентные клетки штамма JM109 E.coli (Takara Shuzo) трансформировали реакционной смесью для лигирования в соответствии с инструкциями изготовителя и отбирали несколько колоний, устойчивых к ампициллину. Из указанных колоний экстрагировали плазмидные ДНК, при этом плазмида, имеющая требуемую структуру, получила название pCRlysE
Плазмиду pCRlysE расщепляли рестрикционными ферментами BamHI и XbaI и разделяли электрофорезом в агарозном геле, получив при этом фрагмент, содержащий ген lysE. Шаттл-вектор для E.coli и Corynebacterium glutamicum, pKC (см. заявку на патент США № 2003/113899) отдельно обрабатывали рестрикционными ферментами BamHI и KpnI аналогичным образом и разделяли электрофорезом в агарозном геле, получив при этом фрагмент гена, содержащий ген устойчивости к хлорамфениколу. Указанный ген очищали и лигировали с вышеуказанным фрагментом lysE. Используя реакционную смесь для лигирования, компетентные клетки штамма JM109 E.coli (Takara Shuzo) трансформировали в соответствии с инструкциями изготовителя и отбирали несколько колоний, устойчивых к хлорамфениколу. Из вышеуказанных колоний были получены плазмиды, которые использовали для создания плазмиды, экспрессирующей LysE, plysE.
Вектор рКС4 был создан следующим образом. Плазмиду рНК4 (см. выложенный патент Японии № 5-7491), имеющую ориджин репликации, выделенный из ранее полученной плазмиды рНМ1519, которая автономно реплицируется в коринеформных бактериях (Agric. Biol. Chem., 48, 2901-2903 (1984)), расщепляли рестрикционными ферментами BamHI и KpnI, получив при этом фрагмент гена, содержащий ориджин репликации. Полученный фрагмент дефосфолировали при помощи набора для дефосфолирования ДНК (Takara Shuzo) и вводили в сайт KpnI вектора pHSG399 (Takara Shuzo) путем лигирования с помощью линкера KpnI (Takara Shuzo). Компетентные клетки штамма JM109 E.coli (Takara Shuzo) трансформировали указанной реакционной смесью для лигирования в соответствии с инструкциями изготовителя и отбирали несколько колоний, устойчивых к хлорамфениколу. Из вышеуказанных колоний были получены плазмиды, которые использовали для создания вектора рКС4.
(3) Создание коринеформной бактерии, продуцирующей L-лизин
Две вышеописанные плазмиды pVK-C* и plysE вводили электропорацией в штамм АТСС 13869 Brevibacterium lactofermentum. Электропорацию выполняли при помощи устройства Gene Pulser (BIO-RAD). Расстояние между электродами в кювете было равно 0,1 см, и создаваемый электрический импульс имел следующие характеристики: 25 мкФ, 200 Ом и 1,8 кВ. Штаммы, содержащие плазмиды, отбирали на агаровой пластинке СМ-Dex (состав среды приведен ниже), содержащей 5 мкг/л хлорамфеникола и 25 мкг/л канамицина. Штамм, содержащий плазмиду, культивировали в течение ночи при 31,5°С, встряхивая в жидкой среде СМ-Dex, содержащей 5 мкг/л хлорамфеникола и 25 мкг/л канамицина. Культивирование выполняли при встряхивании пробирки, содержащей 3 мл культуральной среды.
Среда СМ-Dex была получена следующим образом. Смешивали все компоненты, приведенные в таблице 1, доводили смесь до рН 7,5, добавляя КОН, и стерилизовали в автоклаве при 120°С в течение 20 минут. Агар добавляли в агаровую среду до конечной концентрации, равной 20 г/л.
Состав среды СМ-Dex (в 1 литре)
Как было описано выше, был получен штамм АТСС 13869/pVK-C*, plysE коринеформных бактерий, продуцирующих L-лизин.
Пример 2
Выращивание бактерий, продуцирующих L-лизин, в щелочной среде и влияние концентрации общего аммиака на продуцирование L-лизина
Используя продуцирующую L-лизин бактерию, созданную в примере 1, исследовали концентрацию общего аммиака, не ингибирующую продуцирование L-лизина в щелочной среде.
Сначала выполняли стандартный метод культивирования. То есть использовали среду (среда В), полученную путем добавления сульфата аммония в среду А (состав приведен в таблице 2) в количестве 55% (мас/мас) в расчете на массу глюкозы. Значение рН среды сохраняли на постоянном уровне, используя во время культивирования газообразный аммиак для ферментации L-лизина. Значение рН контролировали на уровне 7,0 или 8,0.
Состав среды А (в 1 литре)
Культивирование, в частности, выполняли следующим образом. Вышеуказанный штамм инокулировали в 3 мл жидкой среды СМ-Dex и культивировали, встряхивая, в течение ночи при 31,5°С, затем 200 мкл указанной среды равномерно распределили по агаровой среде СМ-Dex. Клетки культивировали в течение ночи при 31,5°С в виде стационарной культуры. Затем одну треть бактериальных клеток, продуцирующих L-лизин, которые выращивали на одной пластинке с агаровой средой, инокулировали в 300 мл среды В в ферментере и культивировали. Во время культивирования среду аэрировали стерилизованным фильтрацией воздухом, подаваемым со скоростью 300 мл/мин, и перемешивали со скоростью 700 оборотов/мин, поддерживая температуру среды равной 31,5°С. Результаты показаны на Фиг.1.
В результаты культивирования, выполненного при рН 7,0, было аккумулировано 17,4 г/л L-лизина, при этом скорость продуцирования была равна 0,725 г/л/час. С другой стороны, при рН 8,0 рост клеток почти полностью отсутствовал, и ферментация не прогрессировала (Фиг.1).
Затем ферментацию выполняли, используя бактерии, продуцирующие L-лизин, в среде без сульфата аммония.
Вышеуказанный штамм инокулировали в 3 мл жидкой среды СМ-Dex и культивировали, встряхивая, в течение ночи при 31,5°С, затем 200 мкл указанной среды равномерно распределяли по агаровой среде СМ-Dex и оставляли на ночь при 31,5°С. В ферментер вводили 300 мл среды А (без сульфата аммония) и значение рН доводили до 7,8, 8,2 или 8,9, барботируя в среду газообразный аммиак. Одну треть бактериальных клеток, продуцирующих L-лизин, которые выращивали на одной пластинке с агаровой средой, инокулировали в указанную среду и культивировали. Во время культивирования среду аэрировали стерилизованным фильтрацией воздухом, подаваемым со скоростью 300 мл/мин, и перемешивали со скоростью 700 оборотов/мин, поддерживая температуру среды равной 31,5°С. Во время культивирования сохраняли постоянное значение рН, барботируя в среду газообразный аммиак. Результаты данного эксперимента показали, что при рН 8,9 после того, как концентрация общего аммиака в среде превысила 100 мМ, рост клеток и продуцирование L-лизина, в частности, были сильно ингибированы.
В вышеуказанном методе культивирования газообразный диоксид углерода, образуемый бактериями, продуцирующими L-лизин, растворялся в среде в виде ионов карбоната или бикарбоната, в результате чего значение рН уменьшалось в процессе культивирования. Вследствие этого увеличивалось количество добавляемого аммиака, необходимого для сохранения значения рН на заранее определенном уровне. По мере того, как увеличивалось значение рН среды, возрастали концентрации растворенных ионов карбоната и бикарбоната, и, следовательно, увеличивалась концентрация аммиака, добавляемого для сохранения заранее определенного значения рН.
Недиссоциированный аммиак легко проникает в клетки, вызывая их поражение. Так как при более высоком значении рН происходит меньшая диссоциация аммиака, рост бактерий замедляется по мере увеличения значения рН, даже если концентрация общего аммиака сохраняется на постоянном уровне. Таким образом, был сделан вывод о том, что при значении рН 8,9 или ниже, если концентрация общего аммиака сохраняется на низком уровне, например, равной 100 мМ или меньше, ингибирование роста бактерий и аккумулирования L-лизина является незначительным.
Затем клетки, продуцирующие L-лизин, культивировали, сохраняя концентрацию общего аммиака равной 100 мМ или меньше, при рН 7,8, 8,2 и 8,9.
Вышеуказанный штамм инокулировали в 3 мл жидкой среды СМ-Dex и культивировали, встряхивая, в течение ночи при 31,5°С, затем 200 мкл среды равномерно распределяли по агаровой среде CM-Dex и оставляли на ночь при 31,5°С. В ферментер вводили 300 мл среды А (без сульфата аммония) и значение рН доводили до 7,5, 7,8, 8,2 или 8,9, барботируя в среду газообразный аммиак. Одну треть бактериальных клеток, продуцирующих L-лизин, которые выращивали на одной пластинке с агаровой средой, инокулировали в указанную среду и культивировали. Во время культивирования среду аэрировали стерилизованным фильтрацией воздухом, подаваемым со скоростью 300 мл/мин, и перемешивали со скоростью 700 оборотов/мин, поддерживая температуру среды равной 31,5°С. Во время культивирования значение рН сохраняли на каждом из заранее определенных уровней, добавляя 6 н. раствор гидроксида калия вместо аммиака.
Концентрацию общего аммиака в среде измеряли, используя электрод для аммиака и измеритель ионов (Orion). Из среды периодически отбирали пробы и концентрацию общего аммиака контролировали в пределах 0-100 мМ, добавляя при необходимости 10% водный раствор аммиака. Кроме того, при измерении концентрации растворенного кислорода в среде было обнаружено резкое увеличение концентрации растворенного кислорода при истощении аммиака. При обнаружении данного явления добавляли 10% водный раствор аммиака для предотвращения постоянного истощения аммиака в среде. Результаты показаны на Фиг.2.
Эффективный рост клеток и продуцирование L-лизина наблюдались при всех значениях рН от 7,8 до 8,9. По сравнению с ферментацией, выполненной при рН 7,0 стандартным методом культивирования, скорость продуцирования была равна 115% или выше.
Пример 3
Продуцирование L-лизина
В данном примере ферментацию L-лизина выполняли, контролируя только концентрацию общего аммиака и не регулируя значение рН. Концентрацию общего аммиака сохраняли на уровне 100 мМ или меньше. Данный диапазон был выбран на основании результатов, полученных в примере 2.
Вышеуказанный штамм инокулировали в 3 мл жидкой среды СМ-Dex и культивировали, встряхивая, в течение ночи при 31,5°С, затем 200 мкл среды равномерно распределяли по агаровой среде СМ-Dex и оставляли на ночь при 31,5°С. В ферментер вводили 300 мл среды А (без сульфата аммония) и концентрацию общего аммиака в среде доводили до 23,8 мМ, барботируя в среду газообразный аммиак. Одну треть бактериальных клеток, продуцирующих L-лизин, которые выращивали на одной пластинке с агаровой средой, инокулировали в указанную среду и культивировали. Во время культивирования среду аэрировали стерилизованным фильтрацией воздухом, подаваемым со скоростью 300 мл/мин, и перемешивали со скоростью 700 оборотов/мин, поддерживая температуру среды равной 31,5°С. Периодически измеряли концентрацию общего аммика и добавляли в среду соответствующее количество 10% водного раствора аммиака, необходимое для сохранения концентрации общего аммиака в пределах от 0 до 100 мМ. В результате было аккумулировано 15,9 г/л лизина, при этом ферментация L-лизина прогрессировала (Фиг.3).
Пример 4
Создание бактерии E.coli, продуцирующей L-лизин
<1> Создание штамма с удаленными генами cadA и ldcC, кодирующими лизиндекарбоксилазу
Сначала был создан штамм с отсутствием лизиндекарбоксилазы. Лизиндекарбоксилазы кодированы геном cadA (номер доступа в банке генов Genbank NP_418555, SEQ ID NO:15) и геном ldcC (номер доступа в банке генов Genbank NP_414728, SEQ ID NO:17) (см. международную публикацию WO 96/17930). В данном примере в качестве родительского штамма был использован штамм WC196.
Гены cadA и ldcC, кодирующие лизиндекарбоксилазу, удаляли с помощью метода, разработанного Даценко и Ваннером, который получил название "интеграция, стимулированная восстановлением" (Proc. Natl. Acad. Sci. USA, 2000, vol.97, No.12, pp. 6640-6645), и эксцизионной системы, выделенной из λ-фага (J. Bacteriol., 2002 Sep., 184 (18):5200-3, Interactions between integrase and excisionase in the phage lambda excisive nucleoprotein complex, Cho EH, Gumport RI, Gardner JF). В соответствии с методом "интеграции, стимулированной восстановлением", штамм с удаленным геном можно получить одностадийным методом с использованием продукта PCR, полученного с помощью синтетических олигонуклеотидных праймеров, в которых часть целевого гена создана со стороны 5'-конца и часть гена устойчивости к антибиотикам создана со стороны 3'-конца. Кроме того, ген устойчивости к антибиотикам, введенный в штамм с удаленным геном, может быть удален при помощи совместно используемой эксцизионной системы, выделенной из λ-фага (выложенный патент Японии № 2005-058227).
(1) Удаление гена cadA
Плазмида pMW118-attL-Cm-attR (выложенный патент Японии № 2005-058827) была использована в качестве матрицы при выполнении PCR. Плазмида pMW118-attL-Cm-attR была получена путем введения генов attL и attR, которые являются сайтами присоединения λ-фага, и гена cat, который является геном устойчивости к антибиотикам в pMW118 (Takara Bio). Порядок введения включает attL-cat-attR.
PCR выполняли с использованием синтетических олигонуклеотидных праймеров, представленных SEQ ID NO:11 и 12, которые имеют последовательности, соответствующие обоим концам attL и attR у 3'-концов праймеров, и последовательность, соответствующую части целевого гена cadA у 5'-концов праймеров.
Амплифицированный продукт PCR очищали на агарозном геле и вводили электропорацией штамм WC169 E.coli, содержащий плазмиду pKD46, которая реплицируется в зависимости от температуры. Плазмида pKD46 (Proc. Natl. Acad. Sci. USA, 2000, vol.97, No.12, pp.6640-6645) содержит фрагмент ДНК, состоящий из 2154 нуклеотидов λ-фага, включающего гены, кодирующие рекомбиназу красного системы гомологичной рекомбинации красным λ-фага (λ-, β-, exo-гены), контролируемой арабиноза-индуцибельным параВ-промотором (номер доступа в банке генов GenBank/EMBL J02459, нуклеотиды в положениях 31088-33241). Плазмида pKD46 необходима для введения продукта PCR в хромосому штамма WC196.
Компетентные клетки для выполнения электропорации были получены следующим образом. Штамм WC196 E.coli культивировали в течение ночи при 30°С в среде LB, содержащей 100 мг/л ампициллина, которую 100-кратно разводили 5 мл среды SOB (Molecular Cloning: A Laboratory Manual, 2nd Edition, Sambrook, J. et al., Cold Spring Harbor Laboratory Press(1989)), содержащей ампициллин (20 мг/л) и L-арабинозу (1 мМ). Клетки в разведенной культуре выращивали при 30°С с аэрацией до достижения оптической плотности OD600 около 0,6, затем культуру концентрировали в 100 раз и трижды промывали 10% глицерином, благодаря чему клетки можно было использовать для электропорации. Электропорацию выполняли, используя 70 мкл компетентных клеток и около 100 нг продукта PCR. После электропорации клетки вводили в 1 мл среды SOC (Molecular Cloning: A Laboratory Manual, 2nd Edition, Sambrook, J. et al., Cold Spring Harbor Laboratory Press (1989)), культивировали при 37°С в течение 2,5 часов и затем культивировали при 37°С в виде культуры на твердой L-агаровой среде, содержащей 25 мг/л Cm (хлорамфеникола), после чего отбирали Cm-устойчивые рекомбинанты. Затем клетки дважды субкультивировали при 42°С на L-агаровой среде, содержащей Cm, для удаления плазмиды pKD46 и исследовали устойчивость колоний к ампициллину для получения ампициллин-чувствительного штамма без pKD46.
Удаление гена cadA в мутанте, идентифицированном на основании гена устойчивости к хлорамфениколу, было подтверждено методом PCR. Созданный штамм с отсутствием cadA получил название штамма WC196ΔcadA::att-cat.
Для удаления гена att-cat, который был введен в ген cadA, была использована хелперная плазмида pMW-intxis-ts (выложенный патент Японии № 2005-058827). Плазмида pMW-intxis-ts несет ген, кодирующий интегразу (Int), и ген, кодирующий эксцизионную гидролазу (Xis) λ-фага, и реплицируется в зависимости от температуры.
Компетентные клетки вышеуказанного штамма WC196ΔcadA::att-cat, полученные стандартным методом, трансформировали хелперной плазмидой pMW-intxis-ts и культивировали на L-агаровой среде, содержащей 50 мг/л ампициллина, при 30°С в виде культуры на твердой среде, затем отбирали штаммы, устойчивые к ампициллину.
Для удаления плазмиды pMW-intxis-ts отобранные штаммы дважды субкультивировали на L-агаровой среде при 42°С и исследовали устойчивость полученных колоний к ампициллину и хлорамфениколу для получения чувствительного к хлорамфениколу и ампициллину штамма с удаленным геном cadA без att-cat и pMW-intxis-ts. Данный штамм получил название WC196ΔcadA.
(2) Удаление гена ldcC из штамма WC196ΔcadA
Ген ldcC удаляли из штамма WC196ΔcadA вышеуказанным методом, используя праймеры SEQ ID NO:13 и14 в качестве праймеров для удаления гена ldcC. Таким образом был получен штамм с удаленными генами cadA и ldcC WC196ΔcadAΔldcC.
<2> Введение плазмиды для продуцирования Lys в штамм WC196ΔcadAΔldcC
Штамм WC196ΔcadAΔldcC трансформировали плазмидой рСАВD2 для продуцирования Lys, несущей гены dapA, dapB и lysC (международная публикация WO 01/53459), стандартным методом, получив при этом штамм WC196ΔcadAΔldcC/pCABD2 (WC196LC/pCABD2).
Пример 5
Продуцирование L-лизина с использованием E.coli
В данном примере описано продуцирование L-лизина бактериями E.coli по настоящему изобретению. L-лизин был продуцирован ферментацией без добавления сульфата аммония и хлорида аммония, которые обычно вводят в среду для доставки азота и противоионов для L-лизина при продуцировании L-лизина ферментацией. В частности, культивирование выполняли, не регулируя значение рН, но контролируя концентрацию аммиака в среде. Диапазон, в пределах которого необходимо контролировать концентрацию аммиака в среде, был исследован заранее. В результате было установлено, что концентрация общего аммиака предпочтительно находится в пределах 50-100 мМ. Поэтому в процессе основного культивирования концентрацию общего аммиака контролировали на уровне 100 мМ или ниже, барботируя газообразный аммиак. Когда концентрация общего аммиака уменьшалась до 50 мМ, вводили газообразный аммиак для сохранения требуемой концентрации.
Для продуцирования лизина использовали штамм WC196ΔcadAΔldcC/ pCABD2. В ферментер вводили 300 мл среды для продуцирования L-лизина штаммом E.coli, состав которой приведен в таблице 3. Концентрацию общего аммиака доводили до 95 мМ, барботируя газообразный аммиак. В указанную среду инокулировали клетки, полученные в результате культивирования продуцирущего L-лизин штамма на всей поверхности агаровой среды LB, содержащей 20 мкг/л стрептомицина, при 37°С в течение 24 часов. Число инокулированных клеток соответствовало клеткам, выращенным на трех пластинках с агаровой средой. Культивирование выполняли при температуре среды 37°С, аэрации стерилизованным фильтрацией воздухом, подаваемым со скоростью 50 мл/мин, и перемешивании со скоростью 700 оборотов/мин. Когда концентрация растворенного кислорода в среде снижалась до 20% насыщения, скорость аэрации увеличивали до 100 мл/мин. Питательный раствор для E.coli, состав которого приведен в таблице 4, добавляли в среду по каплям так, чтобы глюкоза постоянно присутствовала в среде в концентрации, не превышающей 30 г/л. И наконец, после потребления 36 г глюкозы культивирование прекращали. Результаты культивирования были весьма благоприятными, при этом вся добавленная глюкоза была потреблена через 33 часа, было аккумулировано 13,4 г L-лизина и скорость продуцирования L-лизина была равна 1,2 г/л/час. Выход продукта составил 37%.
Ниже приведены результаты контрольного эксперимента по продуцированию L-лизина тем же штаммом при добавлении сульфата аммония без осуществления контроля за концентрацией общего аммиака, но с регулированием значения рН аналогично стандартным методам продуцирования основных аминокислот. Тот же штамм инокулировали в среду для продуцирования L-лизина бактериями E.coli, приведенную в таблице 3, в которую добавляли 13 г/л сульфата аммония, и культивировали при постоянном значении рН, равном 6,7, которое регулировали, барботируя газообразный аммиак. Температура культуры, скорость аэрации и скорость перемешивания были аналогичны вышеуказанным показателям. В данном случае вместо питательного раствора для E.coli, представленного в таблице 4, добавляли питательный раствор для E.coli, содержащий 112,5 г/л сульфата аммония (таблица 5), при этом глюкоза постоянно присутствовала в среде в концентрации, не превышающей 30 г/л, в результате чего было потреблено 36 г глюкозы. Вся добавленная глюкоза была потреблена через 33 часа, было аккумулировано 14,7 г L-лизина, и скорость продуцирования L-лизина была равна 1,3 г/л/час. Выход продукта составил 40%.
Все вышеуказанные концентрации лизина показаны в расчете на гидрохлорид лизина. Кроме того, изменения концентрации общего аммиака и значения рН во время культивирования показаны на Фиг.4. Сравнивая полученные результаты, можно сделать вывод о том, что при использовании способа по настоящему изобретению L-лизин можно продуцировать ферментацией без добавления сульфата аммония или хлорида аммония при скорости продуцирования около 92%, выходе продукта около 93% и количестве продуцированного L-лизина около 91% по сравнению с результатами, получаемыми в процессе стандартной ферментации с добавлением сульфата аммония.
Состав среды для продуцирования L-лизина бактериями E.coli
(в 1 литре)
Глюкозу и FeSO4 .7H2O отвешивали в виде порции А, другие компоненты отвешивали в виде порции В, после чего порцию А как есть и порцию В, доведенную до рН 5,0, отдельно стерилизовали в автоклаве при 115°С в течение 10 минут и затем смешивали. Перед использованием в среду добавляли 20 мкг/л стрептомицина.
Состав питательного раствора для E.coli (в 1 литре)
Компоненты стерилизовали в автоклаве при 120°С в течение 20 минут. Перед использованием в среду добавляли 20 мкг/л стрептомицина.
Состав питательного раствора для E.coli, содержащий сульфат аммония (в 1 литре)
Компоненты стерилизовали в автоклаве при 120°С в течение 20 минут. Перед использованием в среду добавляли 20 мкг/л стрептомицина.
Пример 6
Продуцирование L-аргинина
В данном примере описано продуцирование L-аргинина коринеформными бактериями по настоящему изобретению. В качестве штамма, продуцирующего L-аргинин, использовали штамм AJ12092 (FERM BP-6906) Corynebacterium glutamicum.
Сначала приведены результаты контрольного эксперимента по продуцированию L-аргинина тем же штаммом при добавлении сульфата аммония, который выполняли, не контролируя концентрацию аммиака в среде, но регулируя значение рН, аналогично стандартным методам продуцирования основных аминокислот. Для продуцирования L-аргинина использовали среду, состав которой представлен в таблице 6, с добавлением 65 г/л сульфата аммония. Кроме того, концентрация глюкозы была изменена до 40 г/л. В ферментер вводили 300 мл указанной среды и значение рН доводили до 7,0, барботируя газообразный аммиак. В указанную среду инокулировали две пластинки клеток, полученных в результате культивирования штамма AJ12092 Corynebacterium glutamicum на всей поверхности агаровой среды CM-Dex при 31,5°С в течение 24 часов. Культивирование выполняли при температуре среды 31,5°С, аэрации стерилизованным фильтрацией воздухом, подаваемым со скоростью 150 мл/мин, и перемешивании со скоростью 700 оборотов/мин. Кроме того, во время культивирования значение рН доводили до 6,9, добавляя 6 н раствор КОН, который стерилизовали отдельно. В процессе культивирования концентрация глюкозы уменьшалась. Для сохранения концентрации глюкозы, равной 30-40 г/л, добавляли отдельно стерилизованный раствор глюкозы в количестве 692 г/л. Культивирование выполняли в течение 54 часов. В результате было аккумулировано 23,4 г/л L-аргинина, выход L-аргинина был равен 26,7% в расчете на потребленную глюкозу, и скорость продуцирования была равна 0,43 г/л/час. В процессе культивирования глюкоза была потреблена в количестве 29,1 г на одну загрузку.
L-аргинин продуцировали без добавления сульфата аммония в среду, контролируя только концентрацию общего аммиака и не регулируя значения рН. Результаты приведены ниже. В ферментер вводили 300 мл среды для продуцирования L-аргинина, состав которой представлен в таблице 6, но без сульфата аммония, и концентрацию общего аммиака доводили до 12,6 мМ, барботируя газообразный аммиак. В указанную среду инокулировали две пластинки клеток штамма, продуцирующего L-аргинин, который культивировали так же, как в контрольном эксперименте. Культивирование выполняли аналогично контрольному эксперименту при температуре 31,5°С, аэрации стерилизованным фильтрацией воздухом, подаваемым со скоростью 150 мл/мин, и перемешивании со скоростью 700 оборотов/мин. Путем периодического измерения концентрации общего аммиака в среде или использования устройства, контролирующего концентрацию аммиака, общий аммиак в среде контролировали на разных уровнях во время культивирования. Было установлено, что для достижения благоприятных результатов концентрацию общего аммиака в среде необходимо сохранять на уровне, равном примерно 20 мМ, добавляя газообразный аммиак. Культивирование, выполняемое при сохранении концентрации общего аммиака в среде, равной примерно 20 мМ, обеспечивало достижение благоприятных результатов, при этом было аккумулировано 24,2 г/л L-аргинина через 51 час, и таким образом была достигнута ферментация L-аргинина (Фиг.4). Количество глюкозы, потребленной во время культивирования, было равно 35,1 г на одну загрузку, выход L-аргинина был равен 20,6% в расчете на потребленную глюкозу, и скорость продуцирования была равна 0,47 г/л/час. Кроме того, значение рН среды увеличилось с 7,92 в начале культивирования до 8,02 в конце культивирования.
При сравнении приведенных выше результатов с результатами контрольного эксперимента было продемонстрировано, что L-аргинин можно продуцировать ферментацией без добавления сульфата аммония или хлорида аммония с выходом продукта около 77% и при скорости продуцирования, которая более чем примерно на 9% превышает аналогичный показатель, достигаемый в процессе стандартной ферментации с добавлением сульфата аммония.
Состав среды для продуцирования L-аргинина (в 1 литре)
Среду доводили до значения рН 7,0, добавляя водный раствор гидроксида калия до 1 л, и стерилизовали в автоклаве при 115°С в течение 10 минут.
Пояснения к списку последовательностей
SEQ ID NO:1: последовательность праймера для клонирования гена lysC;
SEQ ID NO:2: последовательность праймера для клонирования гена lysC;
SEQ ID NO:3: последовательность праймера для клонирования гена lysE;
SEQ ID NO:4: последовательность праймера для клонирования гена lysE;
SEQ ID NO:5: нуклеотидная последовательность гена lycC* и аминокислотная последовательность α-субъединицы аспартокиназы, десенсибилизированной в отношении ингибирования;
SEQ ID NO:6: аминокислотная последовательность α-субъединицы аспартокиназы, десенсибилизированной в отношении ингибирования;
SEQ ID NO:7: нуклеотидная последовательность гена lycC* и аминокислотная последовательность β-субъединицы аспартокиназы, десенсибилизированной в отношении ингибирования;
SEQ ID NO:8: аминокислотная последовательность β-субъединицы аспартокиназы, десенсибилизированной в отношении ингибирования;
SEQ ID NO:9: нуклеотидная последовательность гена LysE и аминокислотная последовательность белка LysE;
SEQ ID NO:10: аминокислотная последовательность белка LysE;
SEQ ID NO:11: праймер для удаления гена cadA;
SEQ ID NO:12: праймер для удаления гена cadA;
SEQ ID NO:13: праймер для удаления гена ldc;
SEQ ID NO:14: праймер для удаления гена ldc;
SEQ ID NO:15: нуклеотидная последовательность гена cadA и аминокислотная последовательность лизиндекарбоксилазы;
SEQ ID NO:16: аминокислотная последовательность лизиндекарбоксилазы (cadA);
SEQ ID NO:17: нуклеотидная последовательность гена ldc и аминокислотная последовательность лизиндекарбоксилазы;
SEQ ID NO:18: аминокислотная последовательность лизиндекарбоксилазы (ldc).
Промышленная применимость
В соответствии с настоящим изобретением основное вещество может быть получено ферментацией даже при высоком значении рН, что позволяет уменьшить количество промышленного сырья, такого как сульфат аммония, без значительного снижения производительности, достигаемой при осуществлении стандартных методов культивирования.
Несмотря на то что ферментационный бульон, получаемый способом по настоящему изобретению, содержит ионы карбоната и/или бикарбоната, они легко выделяются в воздух при нагревании, поэтому можно получить ферментационный бульон или продукт ферментации с большим количество основного вещества, присутствующего в виде твердого вещества. Кроме того, в случае очистки, когда в ферментационный бульон добавляют более сильную кислоту, чем угольная кислота, карбонат можно легко заменить более сильной кислотой без ионного обмена, который обычно выполняют при осуществлении стандартных методов продуцирования. Кристаллы гидрохлорида лизина могут быть получены в результате прямого концентрирования ферментационного бульона.





















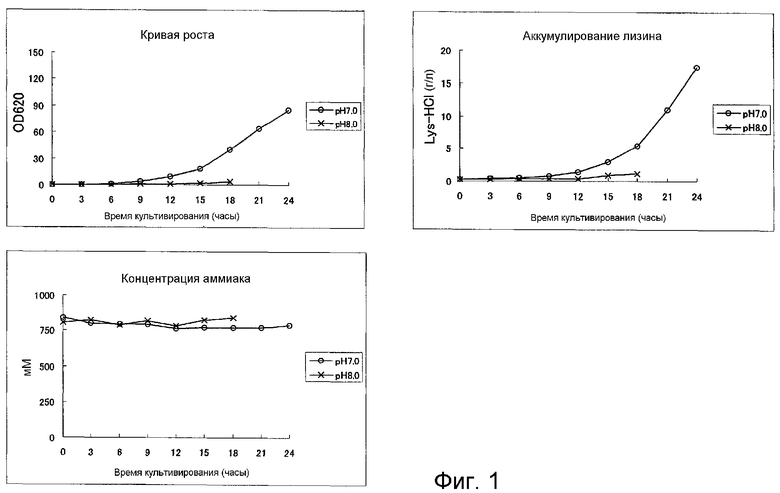
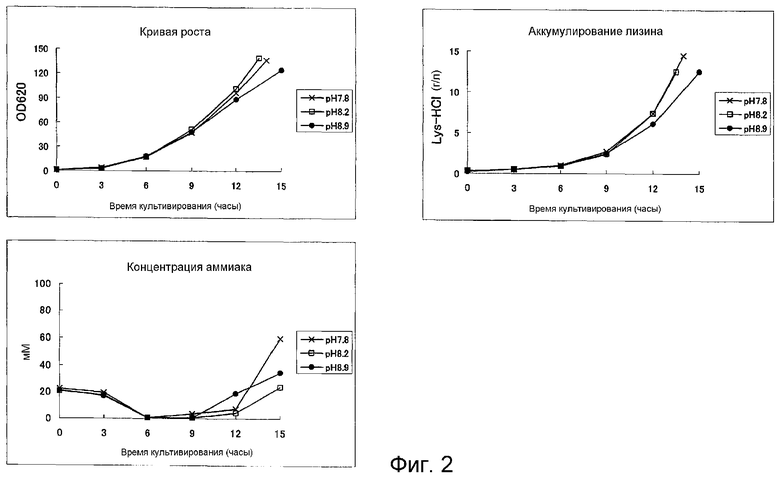
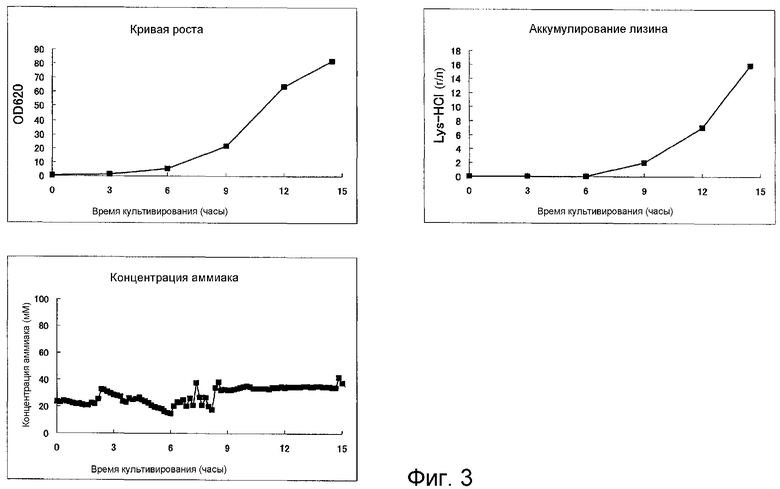
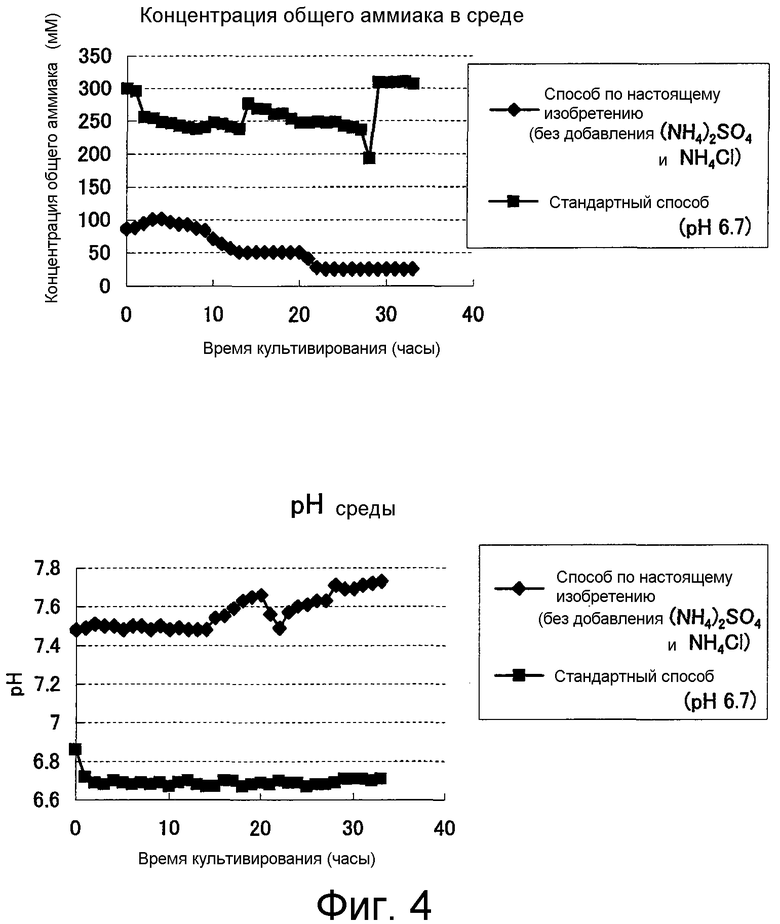
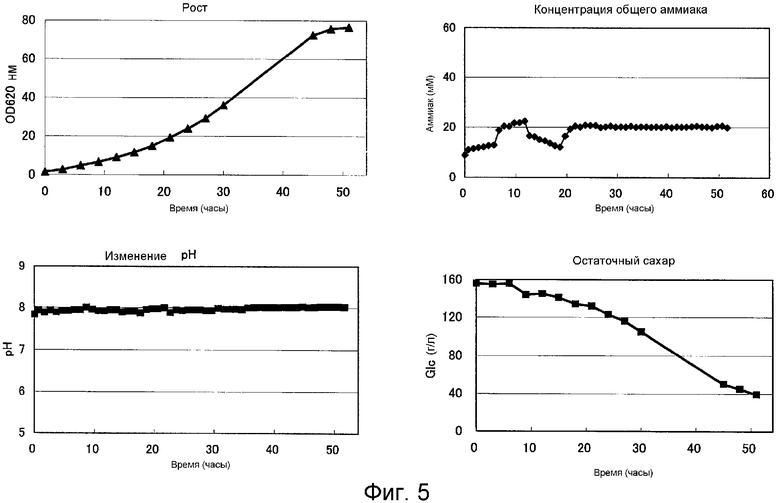
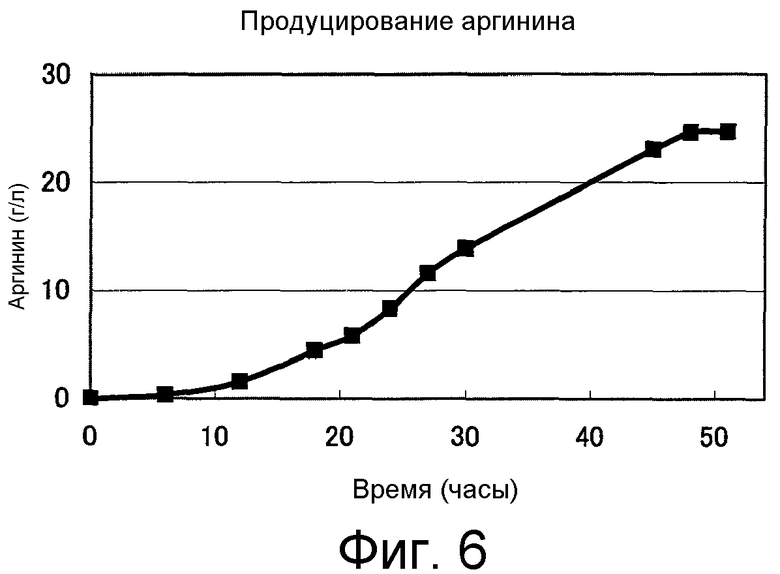
Изобретение относится к биотехнологии и представляет собой способ получения L-лизина или L-аргинина ферментацией, который включает культивирование бактерии, обладающей способностью продуцировать основную аминокислоту в жидкой среде, находящейся в ферментере, для продуцирования и аккумулирования основной аминокислоты в среде, где количество ионов сульфата и/или хлорида, используемых в качестве противоионов основной аминокислоты, уменьшают, регулируя концентрацию общего аммиака в среде в течение периода времени, выбранного из группы, состоящей из периода, в течение которого значение рН среды увеличивается вследствие недостатка противоионов основной аминокислоты, вызываемого аккумулированием основных аминокислот, и периода времени, в течение которого значение рН увеличивается в результате добавления катионов в среду, при этом концентрация ионов аммония в среде находится на таком уровне, при котором сумма ионных эквивалентов ионов бикарбоната и/или карбоната и других анионов, растворенных в среде, больше ионного эквивалента основной аминокислоты, ионизированной из основной аминокислоты, аккумулированной в среде, и где указанная концентрация общего аммиака в среде находится на уровне, не ингибирующем продуцирование основной аминокислоты бактерией, которую определяют заранее. Изобретение позволяет получать L-лизин или L-аргинин с высокой степенью эффективности. 10 з.п. ф-лы, 6 ил., 6 табл.
бактерию культивируют в среде с разными значениями рН и разными концентрациями общего аммиака, измеряют продуцирование основной аминокислоты при каждом значении рН и каждой концентрации общего аммиака, и для каждого значения рН определяют концентрацию общего аммиака, обеспечивающую 50% или более высокое продуцирование основной аминокислоты по отношению к продуцированию, достигаемому в оптимальных условиях.
(А′) культивирование выполняют в среде, содержащей ионы сульфата и/или хлорида в качестве источника противоионов основной аминокислоты в количестве, достаточном для культивирования при значении рН, равном 7,2 или ниже, при этом значение рН сохраняют в пределах от 6,5 до 7,2, добавляя по крайней мере одно из нижеследующих веществ, включающих газообразный аммиак, водный раствор аммиака и мочевину, и измеряют продуцирование основной аминокислоты;
(В′) культивирование начинают в среде, аналогичной применяемой на стадии (А′), за исключением того, что количество ионов сульфата и/или хлорида компонентов среды уменьшают на требуемую величину, и продолжают культивирование при разных концентрациях общего аммиака в течение периода времени, когда становится невозможно сохранять значение рН среды, равным 7,2 или ниже, вследствие недостатка ионов сульфата и/или хлорида, используемых в качестве противоионов основной аминокислоты, вызываемого аккумулированием основной аминокислоты, определяя таким образом диапазон концентраций общего аммиака, обеспечивающих 50% или более высокое продуцирование на основании продуцирования, измеренного на стадии (А′).
по крайней мере часть общего периода времени является периодом, когда значение рН среды не может быть сохранено, равным 7,2 или ниже, вследствие недостатка противоионов для основной аминокислоты, аккумулированной в среде.
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| СПОСОБ ПОЛУЧЕНИЯ ЛИЗИНА | 1992 |
|
RU2107097C1 |
| US 6255086, 03.07.2001. | |||
Авторы
Даты
2009-03-27—Публикация
2005-10-07—Подача