Данное изобретение в основном касается аминирования гетероциклов, содержащих азот, амиды щелочных металлов, и, в частности, усовершенствованного способа аминирования пиридиновых оснований по Чичибабину.
В 1914 году Чичибабин и Сайд (Seide) первыми сообщили, что 2-митилпиридин или в более общем случае альфа-пиколин при обработке амидом натрия в толуоле при повышенных температурах подвергается прямому аминированию по свободному третьему положению кольца. [Chichibabin and Seide, J. Russ. Phys. Chem. Soc., 46, 1216 (1914)]. Позднее Чичибабин и его современники применили эту реакцию для аминирования многих пиридиновых, хинолиновых и изохинолиновых оснований. С тех пор ее считают одной из наиболее важных и влиятельных разработок в химии пиридинов, настолько важной, что сама реакция стала носить имя ее первооткрывателя. Нельзя не принимать во внимание ее коммерческую значимость, например продукт 2-амино-аминирования самого пиридина стал чрезвычайно важным и полезным исходным материалом для дальнейших синтезов во многих областях.
С течением времени реакцию Чичибабина подвергали многочисленным изучениям и обсуждениям как с точки зрения области применения, так и механизма аминирования. Например, хотя впервые реакцию проводили в толуоле, с тех пор ее осуществляют в других апротонных растворителях, среди которых наиболее обычными являются диалкиланилины, жидкий парафин и другие углеводороды, такие как бензол, ксилол, кумол, мезитилен и нефтяные фракции. Аналогично, хотя впервые реакцию провели, используя амид натрия (более общее английское название "sodamide"), с тех пор ее осуществляют с амидами других металлов, такими как амид калия, амид бария и т.д., в особенности, применяя низкие температуры и длительное время реакции, пытаясь замедлить реакцию с целью изучения механизма процесса аминирования. Реакция Чичибабина остается одной из наименее понятных реакций замещения в химии гетероциклов вследствие сложности работы с амидами щелочных металлов и изучения кинетики процесса, происходящего в гетерогенных условиях при высоких температурах. Классически, эти условия включают нагревание смеси при атмосферном давлении и при температуре от 100 до 200oC. Другим отличительным признаком является выделение газообразного водорода и газообразного аммиака, которое обозначает начало реакции и указывает на ее развитие по направлению к завершению. [Новиков, Пожарский и Доронькин, Перевод из Хим. Гетероцикл, Соединений, N 2: 244 (1976); Zevitt & Zevitt, Chem. & Ind, - 1621 (1963)].
Предприняты также многочисленные исследования основных соединений, подвергающихся аминированию. Отчеты подтверждают аминирование моно- и диазинов, таких как пиридины, хинолины, изохинолины, бензохинолины, фенатридины, акридины, бензимидазолы, хиназолины, нафтиридины, пиримидины, пиразины и другие гетероциклические системы. Исследована также реакция, которая относится к аминированию по Чичибабину, но касается не гетероциклов, а соединений с N=CH группой, таких как основания Шиффа. [Пожарский, Симонов и Доронькин, RUSS. Chem. Rev., 47, 1042 (1978), Перевод из Усп. хим., 47, 1933 (1978)]. Результатом этих исследований является то, что полагают, что для данных оснований высока предсказуемость аминирования по Чичибабину, т.е. получают ожидаемый продукт или продукты реакции. Хотя такая определенность полезна, возникают ситуации, когда желательно частичное или полное изменение результата реакции Чичибабина. Например, ожидаемые продукты не нужны или могут потребоваться новые продукты, или может быть предпочтительным обратное соотношение изомеров.
Важным примером этой последней категории является случай 3-замещенных пиридиновых оснований, и в частности 3-алкилпроизводных, которые, как было указано в ранней работе, подвергаются аминированию по Чичибабину, давая предпочтительно 2-амино-3-алкилпиридин ("2,3-изомер") и 2-амино-5-алкилпиридин ("2,5-изомер") в значительно меньшем количестве. Превосходным примером является аминирование 3-метилпиридина, известного также как бета-пиколин, который по данным ранних работ дает в результате 2,3- и 2,5-изомеры в соотношении примерно 10.5: 1 [Abramovitch, Advan, Heterocycl. Chem, 6, 294 (1966); Abramovich, Helmer and Saha, Chem. & Ind., 659 (1964); Abramovich, Helmer and Saha, Can. J. Chem., 43, 727 (1965)].
Патент США N 4386209 описывает существенно усовершенствованную реакцию Чичибабина, которая обеспечивает высокое соотношение 2,5-:2,3-изомеров. Усовершенствованные реакции проводят под сжатой газовой фазой, содержащей аммиак, что, как было показано, меняет нужным образом соотношение изомеров, получаемых по реакции Чичибабина, и делает возможным производство большего количества 2,5-изомера. Однако скорости реакций описанных процессов довольно низки, и обработка реакционной смеси после гидролиза осложнена значительным количеством пены или эмульсионно/разделительным слоем.
В свете приведенных выше предпосылок существуют области, в которых хотелось бы должным образом усовершенствовать аминирование по Чичибабину, например, в том, что касается увеличения скоростей реакций, не рискуя уменьшить подходящий выход продуктов, и облегчения переработки продукта. Настоящее изобретение направлено на обеспечение этих требований.
Краткое содержание изобретения
Согласно сказанному настоящее изобретение обеспечивает усовершенствованное аминирование по Чичибабину пиридиновых оснований, при этом получают увеличение скоростей реакций и другие преимущества. Например, обеспечивают аминирование пиридиновых оснований при увеличенных скоростях реакций без риска уменьшить (а в некоторых случаях с увеличением) выход требуемых продуктов и/или селективность. Предпочтительные способы реакции аминирования по Чичибабину данного изобретения включают реакции реакционной смеси, содержащей органический растворитель, пиридиновое основание, амид натрия и добавку органического соединения, которое повышает скорость указанной реакции и описано формулой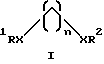
где X - S, O, NR3 или CO2; R1, R2 и R3 - H, алкил, арил, или аралкил и n равно числу от 0 до примерно 12;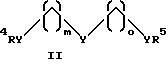
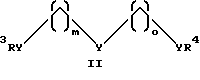
где Y - O, S или NR6; R4, R5 и R6 - H, алкил, арил или аралкил, а m и о равны числу от 1 до примерно 12;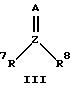
где Z - C или S; A - O или NR9 и R7, R8 и R9 - H, алкил, арил или аралкил;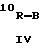
где В - OR11, NR12R13, SR14, CO2R15, NO2 или CN; R10 - алкил, а R11, R12, R13, R14 и R15 - H, алкил, арил или аралкил;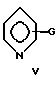
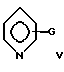
где G - OR16, ROR17 или NR22R23; R16 и R17 - H или алкил, a R, R22 и R23 - алкил;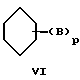
где B определен выше и p равно от 1 до 4;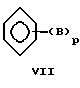
где B такое, как определено выше, и p равно от 1 до 4; или является простым циклическим эфиром или одноэлектронным агентом переноса, с тем, чтобы аминировать указанное основание. Предпочтительно проводить реакции в твердо-жидкой гетерогенной реакционной смеси в присутствии выбранной добавки и под газовой фазой, содержащей аммиак, при давлении выше атмосферного. В особо предпочтительных вариантах данного изобретения добавка (добавки) включает гидроксиалкиламино-соединения формулы (R18)(R19)N-R20, где R18 и R19, которые могут быть одинаковыми или отличаться друг от друга, являются H, низшим алкилом или гидрокси-замещенным низшим алкилом, a R20 является гидрокси-замещенным низшим алкилом.
Таким образом, в одной из своих предпочтительных форм данное изобретение обеспечивает усовершенствованное аминирование по Чичибабину, которое включает реакцию реакционной смеси, содержащей пиридиновое основание, амид натрия, указанную добавку и органический растворитель, причем реакция проходит под газовой фазой при давлении по крайней мере около 3.515 кг/см2 (50 фунтов/дюйм2), газовая фаза содержит аммиак при парциальном давлении по крайней мере около 0.352 кг/см2 (5 фунтов/дюйм2).
В другой предпочтительной форме данное изобретение обеспечивает способ производства аминированного пиридинового основания, в котором получают реакционную смесь, содержащую пиридиновое основание, амид натрия и указанную выше добавку, и проводят реакцию данной реакционной смеси с получением аминированного пиридинового основания. Во время реакции над реакционной смесью сохраняют газовую фазу, содержащую аммиак, при давлении выше атмосферного. Добавка должна присутствовать в таком количестве, которое эффективно увеличивает скорость реакции (то есть скорость выше, чем была бы получена в отсутствие добавки). Затем реакционную смесь подвергают гидролизу, а после этого выделяют полученное таким образом аминированное пиридиновое основание.
В другой предпочтительной форме данное изобретение обеспечивает способ повышения скорости реакции при аминировании по Чичибабину. Способ включает проведение аминирования по Чичибабину в гетерогенной реакционной смеси, содержащей амид натрия, пиридиновое основание, одну или более указанных выше добавок и органический растворитель, причем реакционную смесь во время аминирования выдерживают в газовой фазе, содержащей азот, при давлении выше атмосферного.
Изобретение обеспечивает также предпочтительное аминирование по Чичибабину пиридиновых оснований при использовании амида натрия в присутствии органического растворителя, при этом аминирование проводят в присутствии одной или более указанных выше добавок и под газовой фазой при давлении выше атмосферного и парциальном давлении аммиака, по существу равном или превышающем аутогенное давление аммиака, образующегося в данной реакции.
Реакцию аминирования описанных выше вариантов данного изобретения желательно проводить в атмосфере, по существу инертной, при температуре примерно от 100 до 250oC и без нагревания смеси с обратным холодильником, как обычно делают в классической реакции Чичибабина. Добавленный аммиак можно впускать в реакционную смесь в газообразном виде или наоборот в виде жидкого аммиака, когда амид натрия получают на месте посредством реакции натрия в избытке жидкого аммиака перед проведением аминирования. Температуру и давление в реакционном сосуде предпочтительно поддерживать постоянными в течение периода времени, достаточного для прохождения аминирования в существенной степени, что определяют по выделению при реакции газообразного водорода, хотя и то, и другое может меняться в зависимости от начального значения. Например, температуру предпочтительно поддерживать примерно 130-200oC, при этом предпочтительно реакционное давление, по крайней мере, около 21.09 кг/см2 (300 фунтов/дюйм2), если начальное давление аммиака составляет, по крайней мере, 1.055-7.03 кг/см2 (15-100 фунтов/дюйм2). Аутогенное давление газов, выделяющихся в процессе аминирования, можно использовать для увеличения давления в реакционном сосуде, а избыток газов можно выпускать во избежание слишком высокого давления
Предпочтительные способы данного изобретения включают также присутствие в реакционной смеси аминопиридина, более предпочтительно, одного или более из требуемых продуктов данной реакции, например 2-амино-5-(низший алкил) пиридина.
Дополнительные предпочтительные варианты, отличительные признаки и преимущества настоящего изобретения будут ясны из следующего далее описания.
Описание
Для облегчения понимания принципов данного изобретения будут сделаны ссылки на некоторые его варианты и для их описания будет использован специфический язык. Однако необходимо понимать, что эти варианты не ограничивают области изобретения, обычно при этом специалист, которого данное изобретение касается, рассматривает подобные изменения и дополнительные модификации, а также дополнительные применения принципов данного изобретения.
Отличительным признаком данного изобретения является открытие, что существенные и удивительные результаты достигнуты путем включения в аминирование пиридинового основания по Чичибабину одной или более добавок органических соединений, которые определены формулой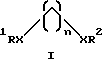
где X - S, O, NR3 или CO2; R1, R2 и R3 - H, алкил, арил или аралкил и n равно числу от 0 до примерно 12;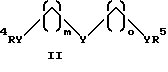
где Y - O, S или NR6; R4, R5 и R6 - H, алкил, арил или аралкил, a m и o равны числу от 0 до примерно 12;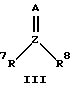
где Z - C или S; A - O или NR9 и R7, R8 и R9 - H, алкил, арил или аралкил;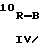
где B - OR11, NR12R13, SR14, CO2R15, NO2 или CN; R10 - алкил, a R11, R12, R13, R14 и R15 - H, алкил, арил или аралкил;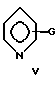
где G - OR16, -ROR17 или NR22R23; R16 и R17 - H или алкил, а R, R22 и R23 - алкил;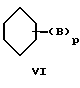
где B определен выше и p равно от 1 до 4;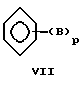
где B такое, как определено выше, и p равно от 1 до 4; или являются простым циклическим эфиром или одноэлектронным агентом переноса, с тем, чтобы аминировать указанное основание.
В приведенных выше формулах термин "алкил" относится к алкильным группам, имеющим от 1 до примерно 12 атомов углерода, и обычно предпочтительными алкильными группами являются низшие алкилы, то есть, имеющие от 1 до примерно 5 атомов углерода. Термин "арил" относится к моно- или полициклическим ароматическим соединениям, предпочтительно имеющим примерно до 30 атомов углерода. Предпочтительные арильные группы включают фенильную и нафтильную группы. Термин "аралкил" относится к группам формулы -алкил-арил, например бензильной группе.
Что касается добавок приведенной выше формулы (I), предпочтительными оказываются соединения, где n составляет от 1 до примерно 6 и в которых присутствующие группы "R" (то есть R1, R2 и т.д.) являются либо H, либо низшим алкилом. Добавки формулы (II) также предпочтительно имеют группы "R", которые являются либо H, либо низшим алкилом, и кроме того, по крайней мере, один параметр m или n предпочтительно равен, по крайней мере, 1. Предпочтительные значения для m или n составляют от 0 до 6. Добавки формулы (III) оказываются предпочтительными, когда Z - C и A - O. Предпочтительны добавки формулы (IV), в которых группы "R" являются H или низшим алкилом, и обычно могут включать низшие алкиламины и низшие спирты. Пиридиновые соединения формулы (V) также являются предпочтительными, когда группы "R" представляют собой H или низший алкил, наряду с гидроксилсодержащими пиридиновыми соединениями, демонстрирующими преимущества, показанные в приведенных ниже Примерах. Добавки формул (VI) и (VII) являются преимущественными, когда p равно 2 и заместители В находятся в кольце непосредственно друг за другом (то есть в ортоконфигурации), хотя подходят также мета- и параконфигурации. Разнообразные простые циклические эфиры, например такие относительно большие эфиры, как 18-краун-эфиры, также являются подходящими добавками для данного изобретения, это так называемые одноэлектронные агенты переноса, такие как кумол, дифенилкетон и подобные. Подходят также различные другие соединения, увеличивающие скорость реакции, которые включают, например, гексаметилфосфорамид (НМРА), ацетат тетраметиламмония (ТМА) и 1-гексин.
В этом смысле предпочтительная группа добавок (из практики на сегодняшний день) включает соединения гидроксиламина формулы (R18)(R19)N-R20, где R18 и R19, которые могут быть одинаковыми или отличаться друг от друга, являются -H, низшим алкилом или гидроксизамещенным низшим алкилом, a R20 является гидроксизамещенным низшим алкилом. Предпочтительно включить добавку в реакционную смесь в молярном соотношении примерно от 0.001 до 0.2 относительно пиридинового основания и более предпочтительно молярное отношение примерно от 0.02 до 0.08. Эти количества эффективно увеличивают скорость аминирования по Чичибабину и, соответственно, снижают время реакции до ее завершения. В этом отношении заявители обнаружили, что в предпочтительных реакциях включение добавки может снижать время реакции на 10% или более по сравнению с соответствующими реакциями, которые не включают добавок. Существенные снижения времени реакции (что достигается благодаря настоящему изобретению) обеспечивают огромное преимущество при коммерческом использовании, например, увеличивая производительность и снижая таким образом стоимость производства. Кроме того, заявители обнаружили, что включение добавки в реакцию аминирования по Чичибабину 3-(низший алкил)пиридинов существенно увеличивает выход 2,5-изомера наряду с увеличением соотношения 2,5-:2,3-изомеров, а в случае таких гидроксиалкиламинов, как моноэтаноламин, также улучшает цвет реакционной смеси после гидролиза и облегчает решение проблем, связанных с образованием пены и эмульсий, с которыми можно столкнуться при выделении продукта после реакции без использования гидроксиалкиламина.
В предпочтительном способе аминирования согласно изобретению после соединения реагентов и гидроксиалкиламина в аппарате высокого давления сначала производят увеличение давления указанной выше газовой фазы до величины, по крайней мере, около 3.515 кг/см2 (50 фунтов/дюйм2) и добавляют в сосуд аммиак в количестве, достаточном для получения начального парциального давления аммиака в этой газовой фазе, по крайней мере, около 0.352 кг/см2 (5 фунтов/дюйм2). Смесь нагревают до температуры, достаточной для начала аминирования, давление во время протекания реакции поддерживают при начальном значении 3.515 кг/см2 (50 фунтов/дюйм2) или выше до тех пор, пока в основном не прекратится выделение водорода. Хотя аутогенное давление выделяющихся в процессе аминирования газов можно использовать для поддержания давления во время реакции, предпочтительно сначала очистить сосуд от воздуха и увеличивать давление, используя инертный газ, такой как азот, аргон и т.п., а затем проводить аминирование в по существу инертной атмосфере азота. В данном случае термин "по существу" обозначает условие, которое развивается в процессе аминирования, когда выделившийся водород и другие возможные газы входят в газовую фазу, давая в результате преобладающе (но не полностью) инертную атмосферу азота.
Более предпочтительно, чтобы начальное давление аммиака в газовой фазе составляло, по крайней мере, около 1.055-7.03 кг/см2 (15-100 фунтов/дюйм2), наиболее предпочтительно - в диапазоне 2.812 - 3.515 кг/см2 (40-50 фунтов/дюйм2). Когда начинается аминирование, некоторое количество аммиака может быть утеряно при отводе избытка давления, образовавшегося вследствие выделения водорода и других газов, что не снижает результаты реакции. Это конечно зависит от размера и эффективности использованного реакционного сосуда и компрессора.
В одном способе изобретения амид натрия получают на месте в реакторе посредством реакции натрия с избытком жидкого аммиака. После образования амида натрия часть жидкого аммиака удаляют и в тот же сосуд добавляют органический растворитель. Затем в сосуде объединяют пиридиновое основание и добавку гидроксилалкиламина. В реакторе оставляют такое количество жидкого аммония, что, когда смесь достигает температуры, достаточно высокой, чтобы вызвать начало аминирования, парциальное давление оставшегося в газовой фазе аммиака является достаточным для достижения требуемого уровня. Реакционную смесь можно снабдить соединениями, которые диссоциируют с образованием свободного аммиака, являясь, таким образом, источником аммиака. Однако более предпочтительно вводить газообразный аммиак прямо в сосуд во время увеличения давления газовой фазы.
Что касается других условий реакции, после доведения смеси до температуры, достаточно высокой, чтобы вызвать начало выделения водорода (и, следовательно, аминирования), температуру реакционной смеси поддерживают достаточно высокой, чтобы вызвать (или разрешить) протекание аминирования в достаточной степени. Предпочтительным является диапазон температур примерно 100-250oC, наиболее предпочтительным - диапазон 130-200oC. Кроме того, доказано преимущество проведения начальных стадий данной реакции при относительно низкой температуре внутри указанного диапазона, а последующих стадий реакции при относительно высокой температуре внутри указанного диапазона. Такой температурный режим во время проведения реакции сохраняет преимущественно высокое соотношение 2,5-:2,3-изомеров при аминировании 3-алкилпиридинов, позволяя быстрее завершить реакцию.
Что касается органического растворителя (бензола, замещенного низшим алкилом), предпочтительными являются, например, толуол и ксилол, хотя можно также использовать другие органические растворители. Многие такие растворители являются обычными для аминирования по Чичибабину.
Аминирование согласно настоящему изобретению можно применять для широкого ряда пиридиновых оснований, которые включают как замещенные, так и незамещенные пиридиновые основания. Кроме того, использованные здесь пиридиновые основания включают также бензо-производные пиридиновых оснований, такие как хинолины и изохинолины. В этом отношении известны разнообразные подходящие замещенные и незамещенные пиридинвоые основания, и их использование в настоящем изобретении будет разумным для специалистов, компетентных в соответствующей области.
Предпочтительным аминированием настоящего изобретения является применение данного способа для 3-(низший алкил) пиридина. В этом случае использованный здесь термин "низший алкил" обозначает разветвленные или неразветвленные алкильные группы, имеющие от 1 до 5 атомов углерода. Таким образом, предпочтительные субстраты для аминирования включают 3-метилпиридин, 3-этилпиридин, 3-пропилпиридин, 3-изопропилпиридин, 3-бутилпиридин (все изомеры бутила) и 3-пентилпиридин (все изомеры пентила). Наиболее предпочтительным на сегодняшний день является 3-метилпиридин.
Преимущественные реакции данного изобретения можно проводить, добавляя определенное количество пиридинового основания и добавку в аппарат высокого давления (такой как автоклав), в котором предварительно получили амид натрия в количестве, по крайней мере, немного превышающем стехиометрическое относительно пиридинового основания. Эту стадию добавления можно проводить при комнатной температуре, добавив предварительно органический растворитель и обычно диспергирующий агент (такой как олеиновая кислота). После этого аппарат закупоривают, очищают от воздуха азотом и увеличивают давление в газовой фазе над гетерогенной твердо-жидкой реакционной смесью примерно до 3.164 кг/см2 (45 фунтов/дюйм2), закачивая газообразный аммиак, и примерно до 21.09 кг/см2 (300 фунтов/дюйм2), закачивая азот. Аппарат и его содержимое быстро нагревают при перемешивании до температуры примерно 130-200oC, в это время начинается выделение газообразного водорода, что означает начало аминирования. Как правило, давление в сосуде увеличивается вследствие роста температуры и выделения газа даже без дополнительной подкачки газообразного азота. Температуру предпочтительно поддерживают в диапазоне 130-200oC, а давление - примерно в диапазоне 21.09-70.3 кг/см2 (300-1000 фунтов/дюйм2) [используемый в коммерческом производстве диапазон; наиболее предпочтительно давление 24.61 кг/см2 (350 фунтов/дюйм2)] до тех пор, пока в основном не завершится выделение водорода, обозначая завершение аминирования. Избыточное давление во время протекания реакции можно спускать через клапан сброса давления или используя другое приспособление. По окончании аминирования аппарату дают охладиться до комнатной температуры и спускают давление до атмосферного. Затем реакционную смесь можно гидролизовать и выгружать, а продукты реакции выделяют, используя стандартные процедуры.
Прежде, чем увеличить давление в реакторе, в реакционную смесь предпочтительно включают аминопиридиновый катализатор, который помогает инициировать данную реакцию и способствует образованию требуемого продукта или продуктов. Предпочтительно, чтобы аминопиридиновый катализатор был одним (или более) из требуемых продуктов реакции, например 2-амино-3-(низший алкил)пиридином или 2-амино-5-(низший алкил)пиридином, или их смесью. Катализатор или смесь катализаторов может быть, например, частью реакционных продуктов предыдущего аминирования, которые не выделяют, а оставляют в реакторе исполнять функцию катализатора в следующем аминировании. Кроме того, можно использовать другие определенные здесь добавки в комбинации друг с другом для достижения еще более выгодных характеристик реакции аминирования.
Для дальнейшей оценки и понимания настоящего изобретения, обеспеченных им преимуществ и предпочтительных способов проведения реакции далее приведены специфические примеры. Должно быть ясно, что эти примеры служат для иллюстрации изобретения и не ограничивают его по существу. В этих примерах, как во всем описании и в формуле изобретения, которая следует далее, температуры приведены в градусах Цельсия (oC), а давление - в фунтах на квадратный дюйм, если не указано отдельно. Кроме того, использованы следующие сокращения: MEA - моноэтаноламин; ГХ (GC) - газовая хроматография; 2A5 - 2-амино-5-метилпиридин; 2A3 - 2-амино-3-метилпиридин.
Примеры 1-2
Аминирование 3-пиколина в присутствии моноэтаноламина (МЕА)
В трехгорлой колбе на один литр, снабженной механической мешалкой, готовят 2.86 моля амида натрия путем медленного добавления 65.78 г натрия к примерно 700 мл жидкого аммиака, содержащего каталитическое количество гексагидрата нитрата трехвалентного железа. Аммиак в основном выпаривают и замещают 300 мл толуола, содержащего 0.1 мл олеиновой кислоты. К NaNH2/толуоловой пасте добавляют при перемешивании моноэтаноламин (0.1 моля). Смесь переносят из колбы в автоклав на один литр, используя 100 мл толуола для ополаскивания колбы.
Автоклав (от Hagard Evaluation Zaboratories, Zimited) снабжен автоматическими регуляторами через интерфейс компьютера температуры, давления и перемешивания, а также автоматической задержкой для температуры, давления, перемешивания и выпуска газа.
Сначала автоклав освобождают от воздуха при помощи азота и нагнетают давление до 3.164 кг/см2 (45 фунтов/дюйм2), закачивая NH3, и затем до 7.03 кг/см2 (100 фунтов/дюйм2), закачивая N2. После этого реактор нагревают до реакционной температуры 150oC и дают достаточное время для того, чтобы температура масла и реактора достигла условия равновесного состояния. В течение этого времени давление в реакторе поднимают до 24.61 кг/см2 (350 фунтов/дюйм2), используя N2.
После этого добавляют 3-метилпиридин со скоростью 20 г/мин до количества 190.2 г (2.04 моля). Затем дают реакции продолжаться, поддерживая температуру в реакторе 150oC и давление 24.61 кг/см2 (350 фунтов/дюйм2). Реакция экзотермична. О завершении реакции узнают, когда скорость выделения газа становится по существу равной нулю. Затем реактор охлаждают и спускают давление до 10.55 кг/см2 (150 фунтов/дюйм2).
Реакционную смесь осторожно гидролизуют, используя 320 г воды при 25-30oC при 10.55 кг/см2 (150 фунтов/дюйм2). После этого давление в реакторе спускают до атмосферного.
Потом разделяют два слоя. Водный слой экстрагируют добавкой 25-40 мл толуола и объединяют органические слои. Органический слой перегоняют для удаления толуола и всех низкокипящих органический веществ. Полученный растворитель отделяют, а концентрированные аминопиридины подвергают газохроматографическому анализу (GC). Концентрат, который остается после удаления растворителя, можно снова перегонять для получения отделенной смеси 2-амино-5-(низший алкил) пиридина и 2-амино-3-(низший алкил) пиридина и остатка.
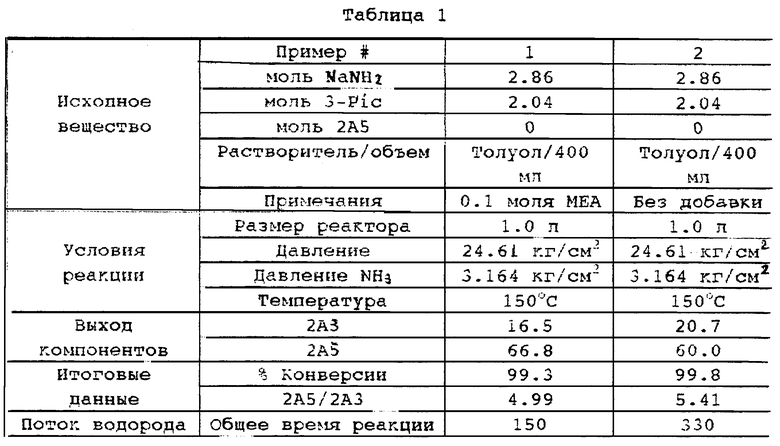
Результаты реакции представлены в таблице 1 и демонстрируют, что добавка МЕА дает более высокий выход 2-амино-5-метилпиридина и реакция доходит до конца значительно быстрее, чем реакция, проводимая аналогичным образом в отсутствие добавки (пример 2). Обнаружено, что МЕА снижает общее время реакции примерно на 55% по сравнению с реакцией в отсутствие катализатора. Обнаружено также, что МЕА увеличивает соотношение 2,5-:2,3-изомеров от 2.90 до 4.04. Снижение времени реакции при увеличении выхода 2,5-изомера и соотношения 2,5-: 2,3-изомеров обеспечивает существенные преимущества данного способа аминирования и иллюстрирует важность открытия заявителей.
Примеры 3-10
Аминирование 3-пиколина в различных условиях
Для характеристики влияния МЕА при варьировании условий реакции провели серию экспериментов. Область исследования включала присутствие 2-амино-5-метилпиридина (2А5), влияние температуры, парциального давления NH3 и концентрации МЕА.
1. Влияние МЕА и 2А5 в качестве одновременных добавок (примеры 3-4).
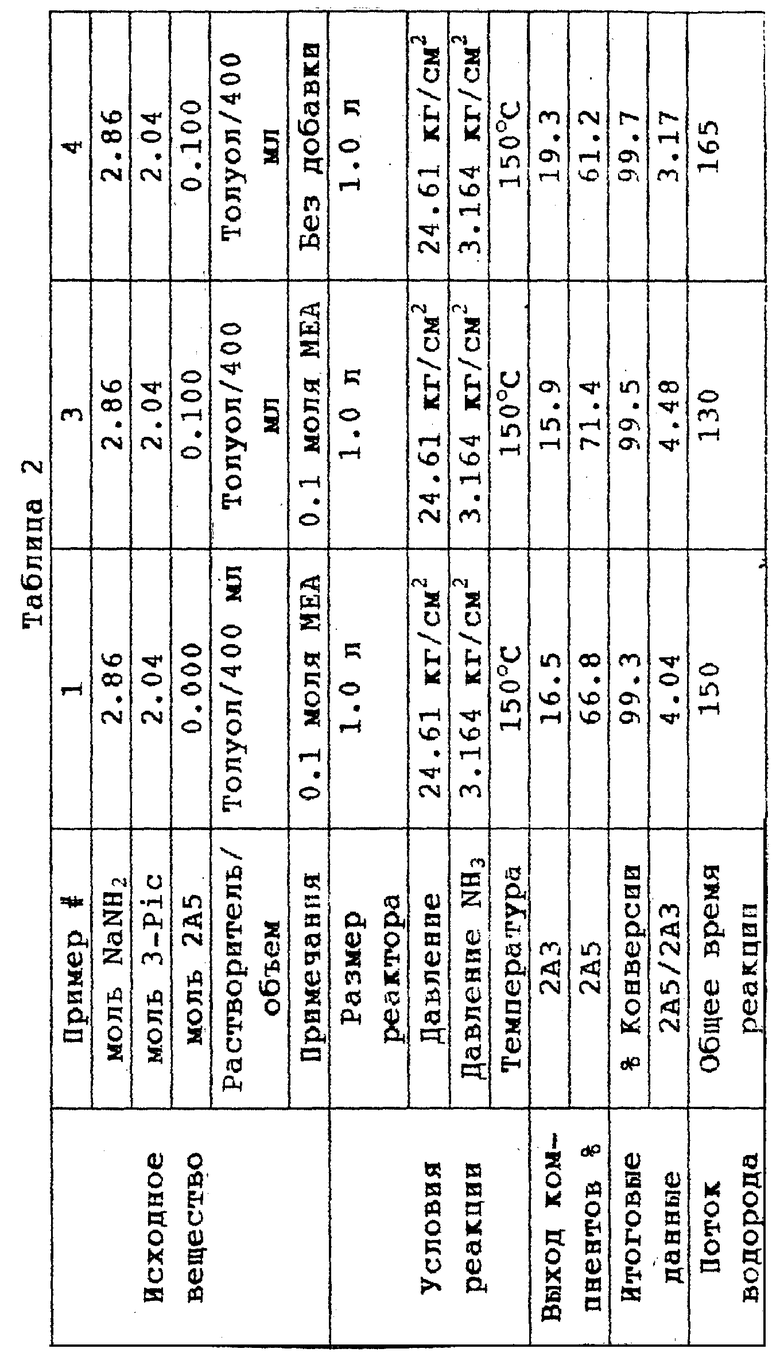
Проводили эксперименты с целью проверки влияния объединенных 2А5 и МЕА по сравнению со случаями использования каждого из них отдельно. Реакции примеров 3 и 4 (таблица 2) проводят так, как описано в примере 1, за исключением того, что 0.1 моля 2-амино-5-метилпиридина добавляют как сопутствующую добавку к системе (пример 3) или саму по себе (пример 4).
Результаты, представленные в таблице 2, показывают, что экзотерма в реакции с использованием обеих добавок (2А5 и МЕА) завершается значительно быстрее, чем в реакциях с использованием только МЕА, только 2А5 или вообще без катализатора. Общее время реакции уменьшается на 13% по сравнению с использованием только МЕА. Обнаружено, что реакция с применением 2А5/МЕА увеличивает выход 2А5 от 66.8% до 71.4%, а также увеличивает соотношение изомеров от 4.04. до 4.48.
Дополнительным открытием является то, что применение МЕА вызывает значительно меньшее окрашивание реакционной смеси после гидролиза. Кроме того, отделение слоя после гидролиза происходит значительно быстрее и легче, так как образуется меньший эмульсионно/разделительный слой.
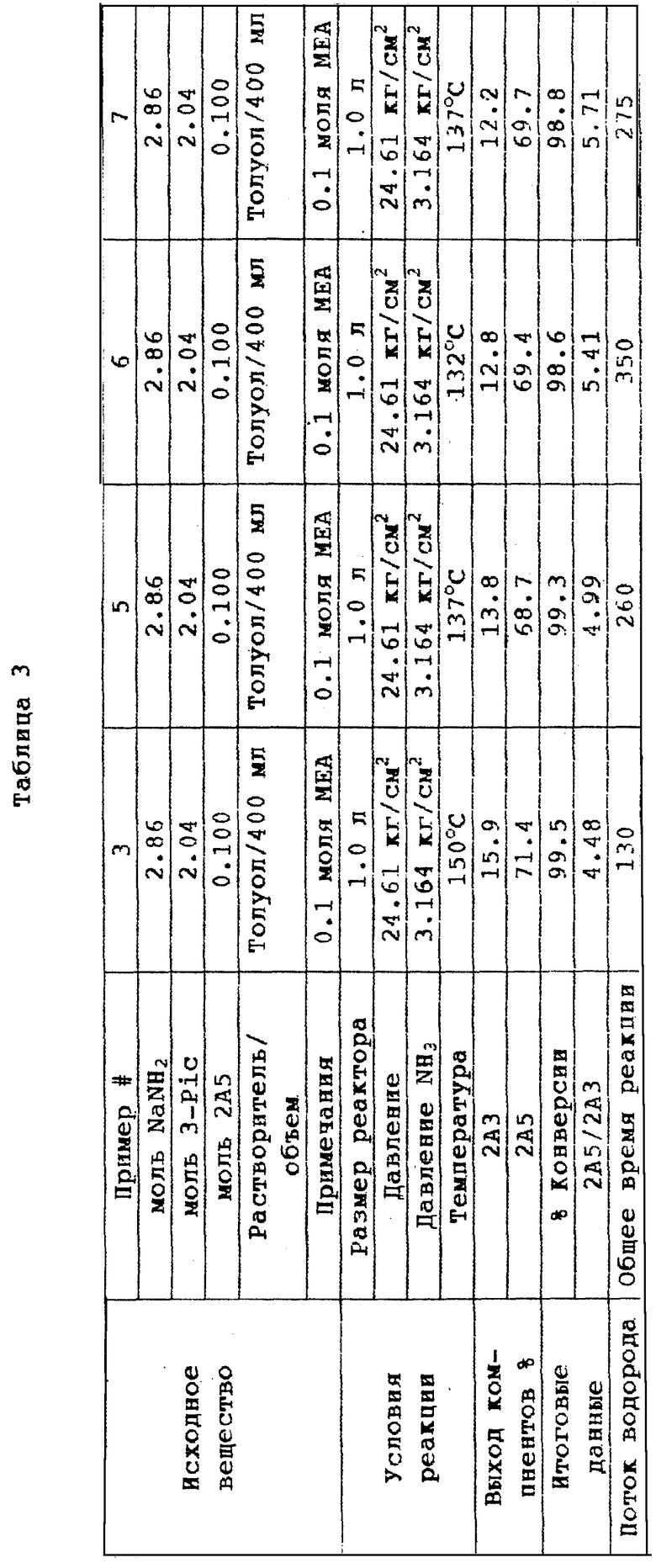
2. Исследование влияния температуры/давления аммиака (примеры 5-7).
Проводили эксперименты с целью проверки влияния на реакцию температуры и парциального давления NH3. Все реакции осуществляют как в примере 1, используя в качестве сопутствующей добавки 0.1 моля 2А5. Результаты представлены в таблице 3. Результаты показывают, что время реакции увеличивается с увеличением давления аммиака или с понижением температуры. Таким образом, наблюдаемое время реакции эквивалентно или улучшено по сравнению с реакцией, проводимой в отсутствие какой-либо добавки. Соотношение 2,5-:2,3-изомеров улучшают, увеличивая концентрацию аммиака или снижая температуру. Выходы продуктов для различных исследованных условий сравнимы по величине. Эти примеры иллюстрируют, что можно варьировать температуру и давление аммиака, сохраняя описанные преимущества.
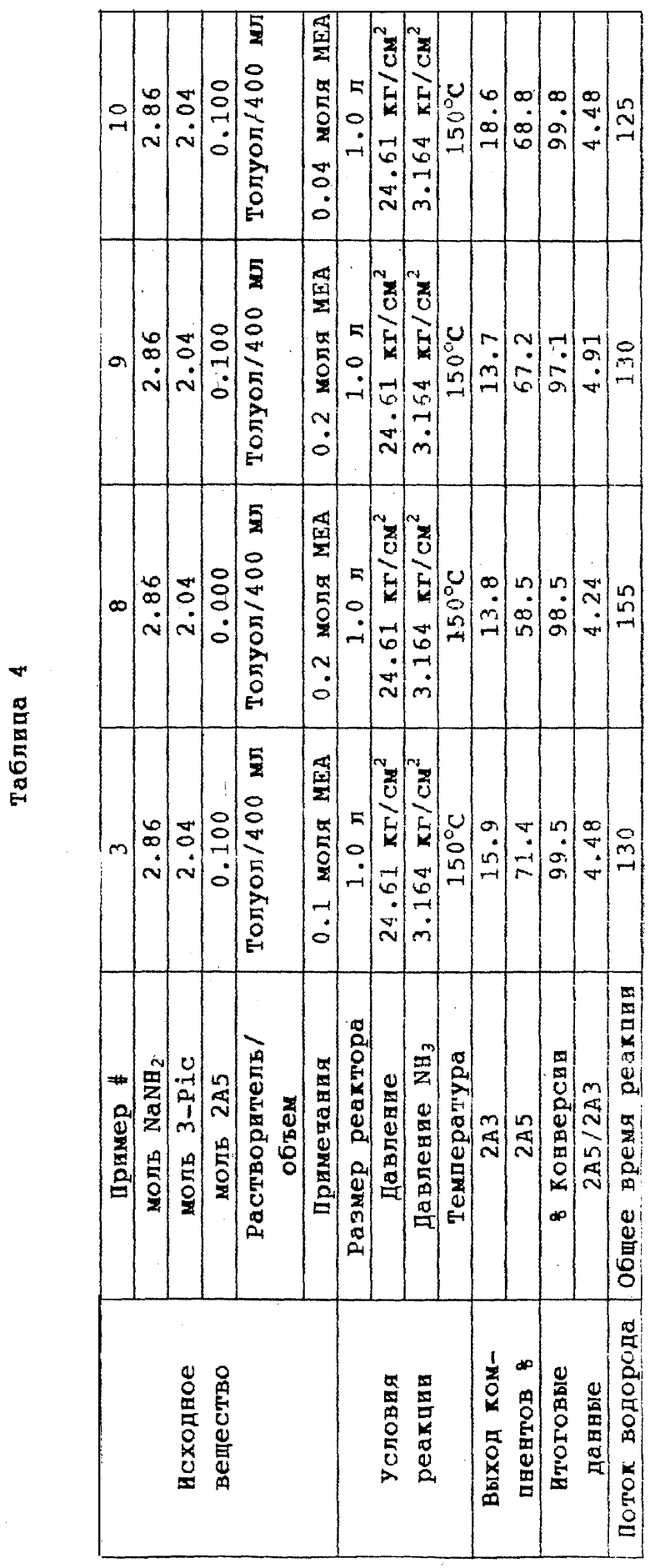
3. Концентрация МЕА (примеры 8-10).
Ряд экспериментов провели с целью проверки влияния на реакцию концентрации МЕА. Реакции проводят как в примере 1, при наличии и в отсутствие в системе 2А5. Результаты представлены в таблице 4. Проверка результатов примера 8, в котором не используют 2А5 в качестве сопутствующей добавки, показывает, что двойная концентрация МЕА не улучшает время реакции. В то время как соотношение 2,5-:2,3-изомеров улучшается, наблюдают снижение выхода 2А5. Проверка результатов примеров 3, 9 и 10, в которых используют 2А5 в качестве сопутствующей добавки, показывает, что улучшенное время реакции сохраняется при использовании увеличенной или уменьшенной концентрации МЕА. Наблюдают изменение соотношения 2,5-:2,3- изомеров, при том что улучшенное соотношение получают при двойной концентрации МЕА. Выходы 2А5 сравнимы по величине внутри диапазона исследованных концентраций. Таким образом, можно варьировать количество использованного МЕА, сохраняя описанные преимущества.
Пример 11
Аминирование ниацина
120 мл толуола, содержащего 0.06 мл олеиновой кислоты, 18.45 г (примерно 0.15 моля) ниацина марки USP и 15.2 г (0.350 моля) 90% NaNH2 (Aldrich Chemical), загружают в реактор автоклава PARR на 300 мл. Для реакций, катализируемых МЕА, перед загрузкой в автоклав к смеси толуол/олеиновая кислота добавляют 0.46 г МЕА (5 молярных% относительно ниацина). Затем автоклав три (3) раза продувают N2, откачивают и вводят NH3, поддерживая давление в автоклаве примерно 2.250 кг/см2 (32 фунтов/дюйм2). Добавляют N2, увеличивая общее давление до 14.06 кг/см2 (200 фунтов/дюйм2). Автоклав при перемешивании нагревают до реакционной температуры, в это время еще добавляют азот, получая давление 24.61 кг/см2 (350 фунтов/дюйм2). Во время протекания реакции аминирования водород выпускают через регулятор и определяют его количество. По окончании реакции выделение газа прекращается, температуру поднимают до 165oC, при повышенной температуре для обоих способов наблюдают выделение дополнительного небольшого количества газа (или газ больше не выделяется). Реакционную смесь охлаждают до 25oC, снижают давление газа и осторожно гидролизуют, используя 45 г воды, поддерживая температуру гидролиза ниже 50oC. Затем разделяют два слоя. После анализа водного слоя титрованием pH доводят до 8.2, 6.0 и 3.85, а осаждающееся твердое вещество отфильтровывают, промывают минимальным количество H2O и сушат. Твердые вещества анализируют по точке плавления, методом ИК-спектроскопии и ЯМР. В обоих случаях аминирования (в присутствии МЕА и без МЕА) образуются аналогичные продукты. В отсутствие МЕА выход 6-аминоникотиновой кислоты (6.4 г) и 2,6-диаминоникотиновой кислоты (2.6 г) составляет 13.3% и 4.8% соответственно. Для аминирования, катализируемого МЕА, выход 6-аминоникотиновой кислоты (7.5 г) и 2,6-диаминоникотиновой кислоты (1.7 г) составляют 15.6% и 3,1% соответственно. Процесс, катализируемый МЕА, по существу заканчивается за 30 минут, в то время как процесс в отсутствие МЕА требует для своего завершения 95 минут. МЕА улучшает выход 6-аминоникотиновой кислоты и значительно улучшает скорость реакции.
Пример 12
Аминирование 4-(5-нонил) пиридина
В трехгорлой колбе на один литр, снабженной механической мешалкой, готовят 0.41 моля амида натрия путем добавления натрия (0,41 моля) к жидкому NH3, катализируемому нитратом трехвалентного железа. К указанной смеси добавляют 250 мл смеси ксилолов, содержащей 0.25 мл олеиновой кислоты, для замещения NH3. Полученную пасту амида натрия нагревают с обратным холодильником под слоем азота до кипения. Через 10 минут добавляют нонилпиридин. Реакционную смесь выдерживают при кипении с обратным холодильником до тех пор, пока практически не прекратится выделение газа. За выделением газа следят по пузырькам газа, выходящим через ловушку с минеральным маслом. Для аминирования, катализируемого МЕА, к нагреваемой с обратным холодильником пасте NaNH2/толуол до внесения нонилпиридина добавляют МЕА (1,49 г, 5 молярных % относительно нонилпиридина). Реакционную смесь гидролизуют, используя 45 мл воды, добавляемой при кипячении с обратным холодильником. Гидролизованную реакционную смесь охлаждают и разделяют два слоя. Органический слой делят на ректификационной колонке (Vigerous) максимально до 295oC/1.5 мм рт.ст. Дистиллят уходит, а остаток анализируют способом газовой хроматографии. Для аминирования, катализируемого не МЕА, получен выход 2-амино-4-(5-нонил) пиридина 14.3% относительно 4-(5-нонил) пиридина. Процесс, катализируемый МЕА, дает улучшенный выход 2- амино-4-(5-нонил)пиридина 28.5% относительно 4-(5-нонил) пиридина. Кроме того, процесс, катализируемый МЕА, завершается за 1/2 времени реакции, катализируемой не МЕА (примерно 1 1/2 часа по сравнению с 3 часами в отсутствие МЕА).
Пример 13
Аминировавие хинолина
В автоклав PARR на 300 мл загружают 19.5 г 90% твердого NaNH2 (0.45 моля). К нему добавляют 100 мл толуола и 6 капель олеиновой кислоты. Затем сосуд закупоривают и продувают азотом. После этого увеличивают давление в реакторе до 10.55 кг/см2 (150 фунтов/дюйм2) и одновременно нагревают до 140oC. Затем загружают в реактор хинолин (0.25 моля), сначала со скоростью 3 мл/мин, а затем, через несколько минут добавления, со скоростью 2 мл/мин. Реактор выдерживают при 140oC в течение 3.5 часов (10.55 кг/см2 = 150 фунтов/дюйм2). Реактор охлаждают до комнатной температуры для гидролиза. После промывания подающего трубопровода толуолом, метанолом и водой его заполняют водой и подают 50 г воды в реактор со скоростью 5.0 мл/мин для гидролиза реакционной смеси. После удаления водного слоя твердые вещества отфильтровывают от органического слоя гидролизной смеси. Эти твердые продукты промывают толуолом, который добавляют в маточник. Затем их сушат в вакуумной печи в течение ночи. Водный слой экстрагируют толуолом. Объединенные органические слои и твердые вещества анализируют способом газовой хроматографии (GC) и масс-спектрометрии с газохроматографическим вводом (GC/MS). Для аминирования, катализируемого МЕА и в отсутствии МЕА, получают аналогичные продукты. Для реакции, катализируемой не МЕА, выход 2-аминохинолина (10,7 г) и 2-амино-3,4-дигидрохинолина (14.7 г) составляет 29.8% и 40.4% соответственно. Для реакции, катализируемой МЕА, выход 2-аминохинолина (12.7 г) и 2-амино-3,4- дигидрохинолина (16,6 г) составляет 35.3% и 45.4% соответственно. Для реакции, катализируемой МЕА, наблюдают улучшенные выходы обоих этих соединений.
Пример 14
Аминирование пиридина
В трехгорлой колбе на 1.0 л получают амид натрия, используя 25.30 г (1.10 моля) твердого Na и 1.25 г катализатора - нитрата трехвалентного железа в жидком NH3, получая 1.10 моля NaNH2. Жидкий аммиак заменяют на 300 мл растворителя толуола, который содержит 1.0 мл олеиновой кислоты и который затем нагревают с обратным холодильником до кипения в течение одного часа. После охлаждения пасту NaNH2 переносят в автоклав, как указано выше в примере 1, промывая колбу дополнительным количеством (100 мл) толуола. После этого автоклав закупоривают, продувают азотом и увеличивают давление, закачивая азот. Для реакции, катализируемой МЕА, к холодному NaNH2 до переноса в автоклав добавляют пипеткой 3.06 г (0.05 моля) МЕА. Затем спускают давление в реакторе, закачивают N2 до давления 10.55 кг/см2 (150 фунтов/дюйм2) и нагревают до 125oC, поддерживая давление 10.55 кг/см2 (150 фунтов/дюйм2). Добавляют 79.1 г (1.0 моль) пиридина со скоростью 10 г/мин и дают реакции протекать изотермически при 125oC и давлении примерно 10.55 кг/см2 (150 фунтов/дюйм2). О завершении реакции узнают, когда прекращается выделение газа. После этого реактор охлаждают для гидролиза. Охлажденную реакционную смесь гидролизуют, используя 123 г H2O. Во время этой операции температура гидролиза никогда не превышает 80oC (давление 10.55 кг/см2 = 150 фунтов/дюйм2). Гидролизованную реакционную смесь охлаждают и удаляют из реактора. Слои делят и дважды экстрагируют водную фазу толуолом по 30 - 40 мл. Слои разделяют после каждой экстракции и органические части объединяют. Затем органическую часть перегоняют при атмосферных условиях, концентрируя 2-аминопиридин и анализируя способом газовой хроматографии. Стандартные реакции (без МЕА) протекают аналогично при реакционной температуре 125oC и давлении 10.55 кг/см2 (150 фунтов/дюйм2). Полученное при использовании МЕА в качестве добавки время реакции значительно снижено, примерно от 500 минут (без МЕА) до 220 минут (при использовании МЕА).
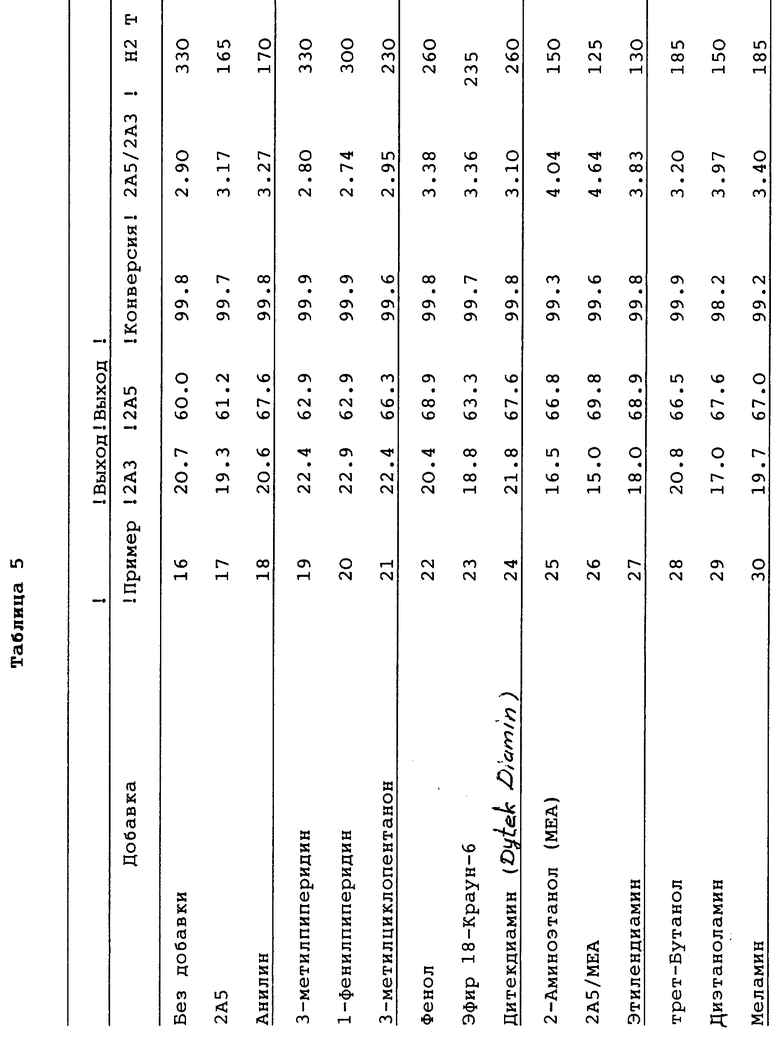
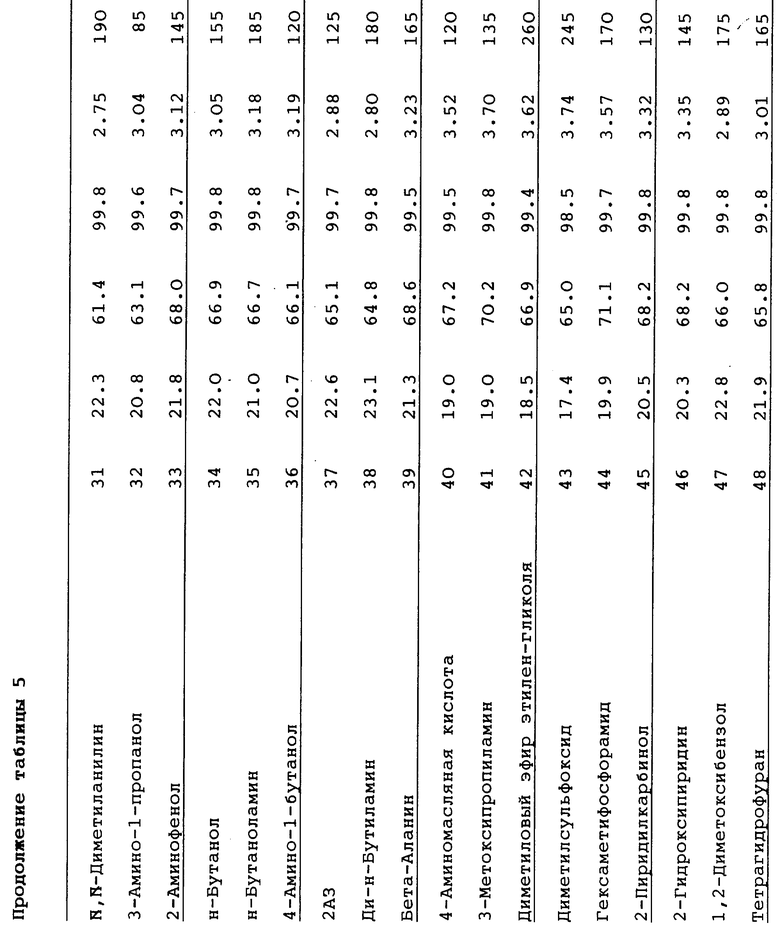
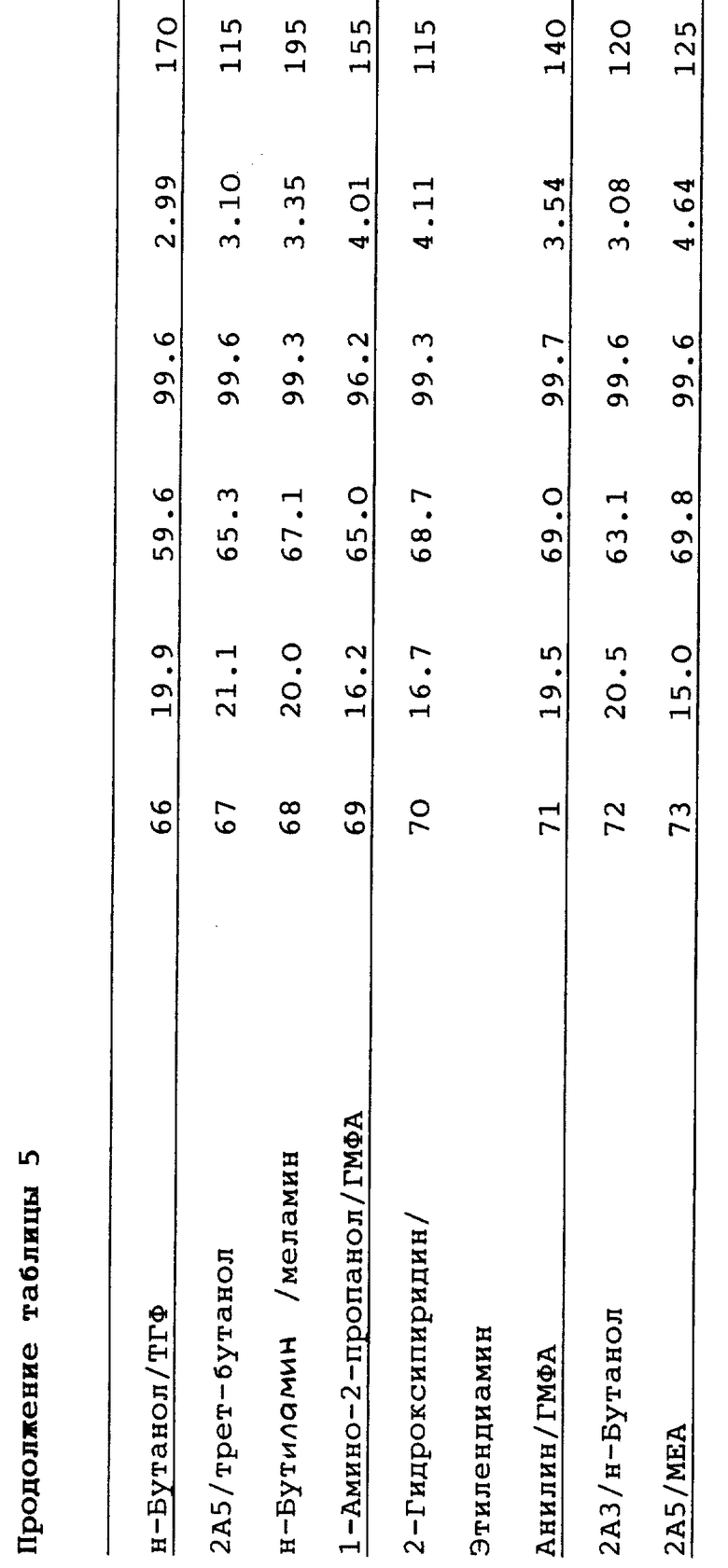
Примеры 16-73
В этих примерах оценивают разнообразные добавки по их способности благоприятно влиять на аминирование по Чичибабину. Процедура проведения реакций повторяет способы, описанные в примере 1, за исключением того, что в каждом случае используют добавку, указанную в таблице 5. Как показывают результаты, заявители открыли широкий класс добавок для совершенствования аминирования пиридиновых оснований, в частности, например, добавок, значительно снижающих продолжительность реакции до завершения.
Все цитированные здесь работы являются иллюстрациями уровня техники и включены в описание в виде ссылок.
Несмотря на то, что данное изобретение достаточно подробно описано, оно служит лишь для иллюстрации и не носит ограничительный характер. Очевидно, что описан только предпочтительный вариант и что патентная защита желательна для всех изменений и модификаций в рамках настоящего изобретения.

Описывается усовершенствованный способ аминирования по Чичибабину, включающий проведение аминирования в условиях воздействия содержащей аммиак газовой фазы и повышенного давления. Отличие способа заключается в том, что проводится взаимодействие в реакционной смеси, содержащей органический растворитель, пиридиновое основание, амид натрия и добавку органического соединения, которое повышает скорость указанной реакции и имеет формулу I, где Х представляет собой О, NH или CO2; R1 и R2 каждый независимо представляют собой Н или низший алкил и n равно числу от 1 до 6; формулу II, где Y - О или NH; R3 и R4 - Н, a m и о равны числу от 1 до 6; формулу III, где Z - С или S; A - О и R5 и R6 - низший алкил или фенил; формулу IV 7R - В, где В - ОR8 или NR9 R10; R7 - низший алкил; R8 - Н, R9 - Н и R10 - низший алкил; формулу V, где G - ОН или - R11ОН; R11 - низший алкил; формулу VI, где В - аминогруппа и р равно 2; формулу VII, где В представляет собой группу NO2, OR8, NR12R13; R12 и R13 - Н, низший алкил или метоксигруппа, а p равно числу от 1 до 3; или является простым циклическим эфиром, или представляет собой гексаметилфосфорамид или ацетат тетраметиламмония, или гексин, с тем, чтобы аминировать указанное основание. Технический результат - увеличение скорости реакции без уменьшения выхода целевого продукта. 3 с. и 23 з.п. ф-лы, 5 табл.
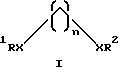

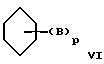
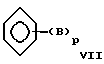
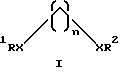
где Х представляет собой О, NН или СО2;
R1 и R2 каждый независимо представляют собой Н или низший алкил;
n равно числу от 1 до 6;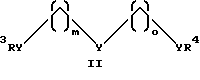
где Y - О или NН;
R3 и R4 - Н;
m и о равны числу от 1 до 6,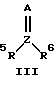
где Z - С или S;
А - О;
R5 и R6 - низший алкил или фенил,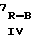
где В - ОR8 или NR9R10;
R7 - низший алкил;
R8 - Н;
R9 - Н;
R10 - низший алкил;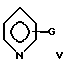
где G - -ОН или -R11ОН;
R11 - низший алкил;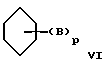
где В - аминогруппа;
р равно 2;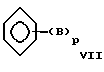
где В представляет собой группу NО2, низший алкил, NR12R13, где R12 и R13 представляют Н или низший алкил, или ОR8, где R8 представляет собой Н или метил;
р равно числу от 1 до 3;
или является простым циклическим эфиром, или представляет собой гексаметилфосфорамид, или ацетат тетраметиламмония, или гексин, с тем, чтобы аминировать указанное основание.
| US 4386209 А, 31.05.1983 | |||
| US 4405790 А, 20.09.1983 | |||
| Способ получения 2-аминопиридинов | 1985 |
|
SU1250565A1 |
| 2-Октиламинопиридин в качестве реагента для экстракционного извлечения иридия и родия | 1977 |
|
SU687073A1 |
| Способ получения амино-анабазина | 1934 |
|
SU39108A1 |
Авторы
Даты
2001-04-20—Публикация
1995-06-26—Подача