Изобретение относится к биотехнологии и физиологии и может быть использовано в экспериментальной медицине, биологии и биотехнологии для тестирования ангиогенной активности, преимущественно рекомбинантного ангиогенина.
Ангиогенин представляет собой катионный полипептид, состоящий из единственной цепи; он стимулирует ангиогенез, особенно демонстративно, на хориоаллантоисной оболочке куриных эмбрионов (ХАО) и роговице глаза кролика. Впервые ангиогенин был изолирован из среды роста клеточной культуры аденокарциномы человека. Показано, что ангиогенин является фактором ангиогенеза, он стимулирует функции эндотелиальных клеток, важных для развития кровеносных сосудов. Этим объясняется интерес к ангиогенину, как к перспективному средству для лечения ран, ожогов, язв, сердечно-сосудистой и сосудистой патологии; всех патологий, при которых необходима васкуляризация.
Препаративные количества ангиогенина для использования в медико-биологических и клинических исследованиях получают методами генной инженерии (рекомбинантный ангиогенин человека). Экспрессия синтетического гена ангиогенина позволяет нарабатывать рекомбинантный белок в количестве 2% и более суммарного клеточного белка. Для практического использования требуется препарат со стандартной ангиогенной активностью, оцененной количественно. Только в этом случае возможно сравнение результатов его действия в экспериментах и клинике.
Известен способ тестирования активности ангиогенина при имплантации диска, импрегнированного ангиогенином, в переднюю камеру глаза кролика (Cancer Research, 1974, 34, N 8, 2109-2113). Через 15 дней наблюдений учитывают факт повышенной инфильтрации сосудами, направленными к имплантированному диску, роговицы глаза подопытного кролика. Реакция на тестируемый ангиогенин учитывается в зависимости от степени инфильтрации как слабая, сильная, отрицательная, то есть производится качественная оценка активности.
Недостатком известного способа является трудоемкость и нестандартность условий тестирования; само введение имплантанта в переднюю камеру глаза может вызвать воспалительную реакцию, что затруднит учет результатов, а необходимость статистически достоверной оценки требует использования значительного количества животных. Последнее увеличивает финансовые и трудозатраты. Однако самый большой недостаток способа заключается в том, что он (тест) является качественным, нет количественной оценки активности ангиогенина.
Наиболее ближайшим к заявляемому способу - прототипом является способ тестирования активности ангиогенина, заключающийся в аппликации импрегнированного ангиогенином диска (Termanox Flow Laba) на хориоаллантоисную оболочку (ХАО) 4-9-суточных коммерческих куриных эмбрионов (Biochemistry, 1985, 24, N 20, 5480-5486) с последующим инкубированием эмбрионов в течение 72-96 часов. Активность ангиогенина учитывают как отрицательную, слабую, среднюю, сильную в зависимости от степени инфильтрации ХАО сосудами в зоне (под и вокруг) апплицированного диска.
Недостатками известного способа являются следующие:
известный способ не обеспечивает количественной оценки активности ангиогенина;
условия тестирования активности ангиогенина нестандартны, так как генетически неоднородные коммерческие куриные эмбрионы не обеспечивают воспроизводимость результатов.
Технической задачей предлагаемого изобретения является повышение функциональных возможностей способа.
Поставленная задача достигается предлагаемым способом, заключающимся в следующем.
На обнаженную ХАО 6-7-суточных куриных эмбрионов чистой генетической линии апплицируют диски стерильного лигнина, импрегнированного контрольными растворами и растворами ангиогенина. Диаметр диска - 6 мм. Через 96 часов инкубации эмбрионов ХАО в зоне диска (под ним и вокруг него) извлекают, фиксируют в формалине и помещают на предметное стекло, на предварительно очерченный круг с диаметром 10 мм и расчерченный на 4 сектора (что облегчает подсчет сосудов). Под лупой с 10-кратным увеличением проводят прямой подсчет сосудов в каждом секторе круга, строго ограничиваясь площадью круга. Сумма числа сосудов во всех секторах и представляет собой плотность сосудов на ограниченном участке ХАО и является показателем активности ангиогенина в количественном выражении.
Существенными определяющими отличиями предлагаемого способа от прототипа являются следующие:
использование 6-7-дневных эмбрионов генетически чистых линий кур, что позволяет стандартизировать условия тестирования активности ангиогенина; 7 дней - это оптимальные сроки, в которые хорошо выражен ангиогенез и еще не затруднен учет результатов;
использование параллельно для контроля дисков, импрегнированных компонентами, содержащимися в препарате, но без ангиогенина, что позволяет исключить неспецифическую ангиогенстимулирующую реакцию на компоненты среды и хирургическое вмешательство;
определение плотности сосудов на строго определенной площади ХАО в количественном выражении, что позволяет перевести оценку активности ангиогенина из качественной в количественную и способствует стандартизации тестируемого препарата.
Преимущественно для аппликации используют диски из лигнина, что дополнительно делает способ более дешевым и доступным.
В результате поиска по источникам патентной и научно-технической информации не выявлено сведений о способе тестирования активности ангиогенина, аналогичном заявляемому.
Изобретение иллюстрируется следующим примером конкретного выполнения.
Пример.
В стерильных условиях на обнаженную ХАО 6-7-суточных линейных куриных эмбрионов апплицируют диски лигнина диаметром 6 мм, импрегнированные 10 мкл исследуемого препарата, контрольными растворами и тест-образцом. Предварительно в ХАО с помощью стерильной инъекционной иглы делают микроотверстия, чтобы облегчить диффузию препаратов через эктодермальный слой ХАО.
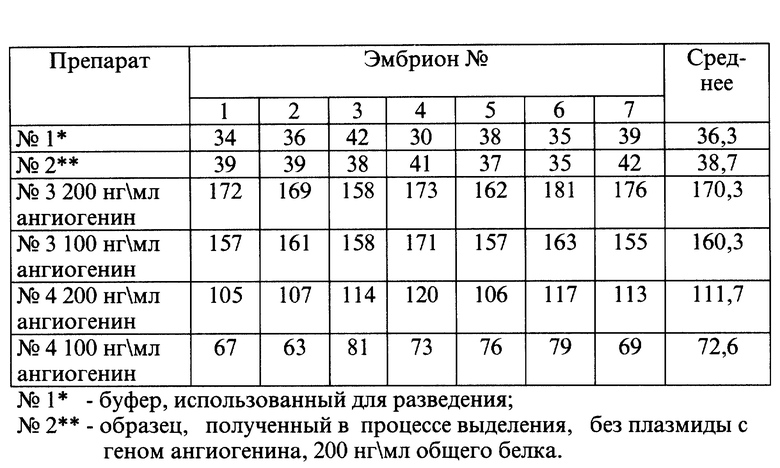
На каждый исследуемый образец препарата берут не менее 7 эмбрионов. После 96-часовой инкубации эмбрионы вскрывают, участок ХАО под диском (диаметром примерно 10 мм) и прилегающий к границам диска извлекают, фиксируют в формалине, переносят на предварительно расчерченное предметное стекло, строго на площадь очерченного круга (диаметр 10 мм). Круг для удобства счета сосудов разделен на 4 сектора. Сумма сосудов четырех секторов каждого круга представляет количественное выражение плотности сосудов для каждого эмбриона. Средняя величина плотности сосудов, использованных для тестируемого образца ангиогенина, является величиной ангиогенной активности. Данные вносят в таблицу.
Из таблицы видно, что предлагаемый способ позволяет получить количественную оценку активности ангиогенина, а также отличается более высокой точностью за счет исключения неспецифической реакции.
Использование предлагаемого способа позволит по сравнению с прототипом:
обеспечить количественное тестирование активности ангиогенина;
упростить и обеспечить экономичность способа за счет использования отечественных дисков из лигнина для аппликации;
стандартизовать условия тестирования активности ангиогенина за счет использования эмбрионов генетических линий кур;
повысить точность тестирования за счет исключения неспецифической ангиогенстимулирующей реакции на балластные компоненты препарата путем проведения параллельного контроля с дисками, импрегнированными компонентами, но без ангиогенина.
Изобретение относится к биотехнологии и медицине. На обнаженную хориоаллантоисную оболочку (ХАО) 6-7-дневных куриных эмбрионов чистых генетических линий апплицируют диски из лигнина, импрегнированные контрольными растворами и растворами исследуемого препарата, содержащими ангиогенин. После 96 ч инкубации эмбрионов ХАО в зоне диска извлекают, фиксируют в формалине и помещают на строго ограниченную площадь, представляющую собой круг с диаметром 10 мм, разделенный на четыре сектора. Под лупой проводят прямой подсчет сосудов в каждом секторе. Сумма числа сосудов в четырех секторах представляет собой плотность сосудов на ограниченном участке ХАО и является показателем активности ангиогенина. Способ обеспечивает количественную оценку ангиогенной активности в стандартных условиях, что делает возможным стандартизацию различных серий препарата и сопоставимости результатов экспериментальных и клинических исследований его действия. 2 з.п. ф-лы,1 табл.
| JAMES W.FETT et all | |||
| Jsolation characterization of angiogenin | |||
| An angiogenic protein from haman carcinoma cells, Biochemistry, v.24, № 20, 1985, p.5480-5485 | |||
| КОМОЛОВА Г.С | |||
| Количественная оценка биологической активности ангиогенина | |||
| - Известия РАН, Серия биологическая, 1992, № 5, с.684-689 | |||
| WO 9213874 А2, 02.01.1992. |
Авторы
Даты
2001-05-10—Публикация
1999-10-13—Подача