Изобретение относится к соединениям триазола и к применению таких соединений. Указанные соединения обладают ценными терапевтическими свойствами и могут быть использованы для лечения заболеваний, связанных с допамин-D3-рецепторными лигандами.
Описаны соединения обсуждаемого здесь типа и имеющие физиологическую активность. Патенты США-А-4338453, 4408049 и 4577020 описывают соединения триазола, обладающие противоаллергической активностью.
FR-А 2551439 описывает соединения формулы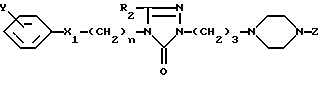
где n равно 2-4;
R2 обозначает водород или низший алкил;
X1 обозначает кислород или связь, Y обозначает водород, галоген, низший алкокси или CF3 , и
Z обозначает фенил, замещенный галогеном, или обозначает незамещенный или замещенный радикал 2-пиридина, 2-пиримидина, 3-пиримидина, 3-пиридазина, 2-хинолина или 3-бензотиазола.
Эти соединения обладают антидепрессивной активностью. J. Med. Chem. 37 (1994) 1060-1062 описывает соединение формулы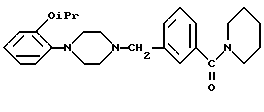
Оно обладает высоким сродством к D2, D3, 5-HT1A и α1A- aдренергическим рецепторам и проявляет высокую и селективную активность в моделях животных, приводящую к мысли о противопсихотическом воздействии на человека.
Нервные волокна получают свою информацию, помимо прочего, через G-протеинсвязанные рецепторы. Существует множество соединений, которые проявляют свое воздействие через эти рецепторы. Одним из них является допамин.
Опубликованы данные, подтверждающие наличие допамина и его физиологического воздействия в качестве нейромедиатора. Реагирующие на допамин клетки связаны с этиологией шизофрении и болезни Паркинсона. Эти и другие расстройства лечат лекарственными препаратами, взаимодействующими с допаминовыми рецепторами.
К 1990 г. отчетливо были распознаны два подкласса допаминовых рецепторов, а именно D1- и D2-рецепторы.
Соколов и др., Nature 1990, 347: 146-151, установили третий подкласс, а именно D3-рецепторы. В основном они выражены в лимбической системе. D3-рецепторы отличаются структурно от D1- и D2-рецепторов приблизительно половиной аминокислотных остатков.
Действие нейролептиков обычно приписывают их сродству к D2-рецепторам. Это подтверждают последние исследования рецепторного связывания. Согласно им большинство допаминовых антагонистов, таких как нейролептики, обладают высоким сродством к D2-рецепторам, но исключительно низким сродством к D3-рецепторам.
Неожиданно найдено, что соединения по данному изобретению обладают высоким сродством к допамин-D3-рецепторам, и исключительно низким сродством к D2-рецептору. Таким образом, они являются селективными D3-лигандами.
Поэтому данное изобретение относится к соединениям триазола формулы 1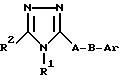
где А обозначает линейную или разветвленную C1-C18- алкиленовую группу, которая может включать по крайней мере одну группу, которую выбирают из О, S, NR3, CONR3, NR3CO, COO, OCO, C3-C6-циклоалкилена или двойной или тройной связи,
В обозначает радикал формулы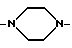
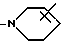
или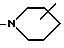
R1 обозначает H, СО2R3, NR3R4, OR4, C3-C6-циклоалкил или C1-C8-алкил, который незамещен или замещен ОН, OC1-C8-алкилом или галогеном;
R2 имеет значения, указанные для R1, или обозначает CF3, SR3, галоген или CN;
R3 обозначает H или C1-C8-алкил, незамещенный или замещенный ОН, ОС1-С8-алкилом, фенилом или галогеном;
R4 имеет значения, приведенные для R3, или обозначает COR3 или CO2R3;
Ar обозначает фенил, пиридил, пиримидил или триазинил, где Ar может иметь от одного до четырех заместителей, которые выбирают, независимо друг от друга, их OR4, С1-С8-алкила, С2-С6-алкенила, С2-С6-алкинила, галогена, CN, СО2R3, NO2, SO2R3, SO3R3, NR3R4, SO2NR3R4, SR3, CF3, CHF2, 5- или 6-членного ароматического или неароматического карбоцикла и 5- или 6-членного ароматического или неароматического гетероцикла с 1-4 гетероатомами, которые выбирают из О, S и N, где карбоцикл или гетероцикл может быть незамещенным или замещенным С1-С8-алкилом, галогеном, ОС1-С8-алкилом, ОН, NO2 или CF3 и где Ar может также быть конденсирован до карбоцикла или гетероцикла указанного выше типа, за исключением соединения формулы: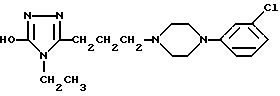
и их солям с физиологически приемлемыми кислотами.
Соединения по данному изобретению являются селективными лигандами допамин-D3-рецептора, которые региоселективно вмешиваются в лимбическую систему, и вследствие их низкого сродства к D2-рецептору они обладают меньшими побочными эффектами, чем классические нейролептики, являющиеся D2-антагонистами. Поэтому соединения могут быть использованы для лечения заболеваний, связанных с допамин-D3-рецепторными антагонистами или веществами, обладающими сродством к D3-рецепторам, например, для лечения нарушений центральной нервной системы, в частности, шизофрении, депрессии, неврозов и психозов. Кроме того, они могут быть использованы для лечения расстройств сна, тошноты и в качестве антигистаминов.
В рамках объема данного изобретения и пунктов формулы изобретения следующие термины имеют приведенные ниже значения:
Алкил (также и в радикалах, таких как алкокси, алкиламино и т.д.) обозначает линейную или разветвленную алкильную группу с 1-8 углеродными атомами, предпочтительно с 1-6 углеродными атомами и в особенности с 1-4 углеродными атомами. Алкильная группа может иметь один или более заместителей, которые выбирают независимо друг от друга из OH и OC1-C8-алкила.
Примерами алкильных групп служат метил, этил, н-пропил, изопропил, н-бутил, изобутил, трет-бутил и т.д.
Алкилен обозначает линейные или разветвленные радикалы, имеющие предпочтительно 2-15 углеродных атомов, особенно желательно 3-10 углеродных атомов.
Алкиленовые группы могут содержать по крайней мере одну из вышеупомянутых групп. Она может быть так же, как вышеупомянутая двойная или тройная связь, расположена в любой точке или в конце цепи, таким образом, что она соединяет цепь с радикалом триазола. Последнее предпочтительно. Когда алкиленовая группа включает двойную или тройную связь, она содержит по крайней мере три углеродных атома в цепи.
Галогенами служат F, Cl, Br, I и, в частности, Cl, Br, I.
R1 и R2 предпочтительно обозначают, независимо друг от друга, H, C1-C8-алкил, NR3R4 или OR4.
Ar может иметь один, два, три или четыре заместителя. Заместители предпочтительно выбирают, независимо друг от друга, из галогена, CF3, CHF2, NR3R4, OR4, NO2, C1-C8-алкила, OC1-C8-алкила, SR3 и CN, где R3 и R4 имеют вышеуказанные значения.
Если один из заместителей Ar обозначает C1-C8-алкил, предпочтителен разветвленный радикал, в частности, изопропил или трет-бутил.
Ar предпочтительно имеет по крайней мере один заместитель и обозначает, в частности,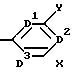
где D1, D2 и D3 обозначают, независимо друг от друга, CR или N, a R, X и Y обозначают H или обозначают заместители радикала Ar, приведенные выше или ниже.
Ar предпочтительно обозначает незамещенный или замещенный фенил, 2-, 3- или 4-пиридинил или 2-, 4(6)- или 5-пиримидил.
Когда один из заместителей радикала обозначает 5- или 6- членный гетероцикл, примерами таких циклов служат пирролидин, пиперидин, морфолин, пиперазин, пиридин, пиримидин, триазин, пиррол, тиофен, тиазол, имидазол, оксазол, изоксазол, пиразол или тиадиазол.
Когда один из заместителей радикала Ar представляет карбоциклический радикал, то это, в частности, фенил, циклопентил или циклогексил.
Когда Ar обозначает конденсированный до карбоцикла или гетероцикла радикал, Ar, в частности, представляет нафталин, ди- или тетранафталин, хинолин, ди- или тетрагидрохинолин, индол, дигидроиндол, бензимидазол, бензотиазол, бензотиадиазол, бензопиррол или бензотриазол.
В предпочтительно обозначает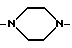
или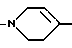
Предпочтительный вариант воплощения включает соединения формулы 1, где А обозначает C3-C10-алкилен, который включает по крайней мере одну группу, которую выбирают из О, S, NR3, циклогексилена, в частности, 1,4-циклогексилен, и двойную или тройную связь, где R3 имеет вышеуказанные значения.
Другой предпочтительный вариант воплощения включает соединения формулы 1, где
R1 обозначает H, OR4, где R4 представляет H или С1-С8-алкил, или С3-С6-циклоалкил или C1-C8-алкил, незамещенный или замещенный ОН, OC1-C8-алкилом или галогеном;
R2 обозначает H, C1-C8-алкил, незамещенный или замещенный ОН, OC1-C8-алкилом или галогеном, или NR3R4, где R3 и R4 обозначают, независимо друг от друга, H, фенил-C1-C8-алкил или C1-C8-алкил, или OR4, где R4 обозначает H или C1-C8-алкил, или CF3;
А имеет значения по п.3; и
Ar обозначает фенил, пиридил или пиримидил, который может иметь один, два, три или четыре заместителя, которые выбирают из H, C1-C8-алкила, который незамещен или замещен ОН, OC1-C8-алкилом или галогеном, или OR4, где R4 обозначает H, C1-C8-алкил, незамещенный или замещенный ОН, OC1-C8-алкилом или галогеном, или из CHF2, CF3, CN, галогена, C2-C6-алкенила, C2-C6-алкинила, фенила, нафтила и 5- или 6-членного гетероциклического ароматического радикала с 1-3 гетероатомами, которые выбирают из О, N и S.
Другой предпочтительный вариант воплощения включает соединения формулы 1, где
R1 обозначает водород или C1-C8-алкил, незамещенный или замещенный ОН, OC1-C8-алкилом или галогеном;
R2 обозначает H, C1-C8-алкил, незамещенный или замещенный ОН, OC1-C8-алкилом или галогеном, или NR3R4, где R3 и R4 независимо друг от друга обозначают H или C1-C8-алкил, или OR4, где R4 обозначает H или C1-C8-алкил, или CF3;
A обозначает С1-С10-алкилен, который может включать кислород или атом серы, или группу NR3, где R3 - такой, как определено выше;
Ar обозначает фенил, который может иметь от одного до четырех заместителей, которые выбирают независимо друг от друга из H, CN, SR3, галогена, С1-С8-алкила, незамещенного или замещенного ОН, OC1-С8-алкилом или галогеном, или из фенила, нафтила, OR4, NO2, NR3R4, CHF2 и CF3, где R3 и R4 имеют приведенные значения.
Особенно предпочтительны в этом отношении соединения формулы 1, где
А обозначает SC3-С10-алкилен, ОС3-С10-алкилен или NR3-С3-С10-алкилен, где R3 обозначает H или C1-C8-алкил;
R1 обозначает H или C1-C8-алкил;
R2 обозначает вышеуказанные радикалы;
B обозначает: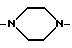
или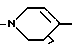
Ar обозначает фенил, который имеет от одного до четырех заместителей, независимо друг от друга обозначающих H, C1-C8-алкил, OC1-C8-алкил, CHF2, CF3 или CN.
В частности, Ar имеет два заместителя, которые локализованы в положениях 3 и 5, один из заместителей является CF3, CHF2 или C1-C8-алкилом, а другой заместитель обозначает H или C1-C8-алкил.
Другой предпочтительный вариант воплощения включает соединения формулы 1, где
Ar обозначает пиримидинил с 1-3 заместителями, которые выбирают независимо друг от друга из H, C1-C8-алкила, фенила, нафтила, С5-С6-циклоалкила, ОН, OC1-C8-алкила, галогена, CN, CF3, CHF2 и 5- или 6-членного гетероциклического ароматического радикала с 1-3 гетероатомами, которые выбирают из О, N и S;
R1 обозначает H или C1-C8-алкил, незамещенный или замещенный ОН, OC1-C8-алкилом или галогеном;
R2 обозначает H, NR3R4 или OR4, где R3 и R4 обозначают независимо друг от друга, H, C1-C8-алкил или фенил-C1-C8-алкил;
A обозначает С1-C10-алкилен, который может включать по крайней мере одну группу, которую выбирают из О, S, NR3, где R3 обозначает H или C1-C8-алкил, и двойную или тройную связь; и
B - как определено выше.
Другой предпочтительный вариант воплощения включает соединения формулы 1, где
Ar обозначает пиридинил, который имеет от одного до четырех заместителей, заместители независимо друг от друга выбирают из H, C1-C8-алкила, фенила, нафтила, ОН, OC1-C8-алкила, галогена, CF3, CN, C2-C6-алкенила, C2-C6-алкинила и 5- или 6-членного ароматического гетероциклического радикала с 1-3 гетероатомами, которые выбирают из О, N и S;
R1 обозначает H, C1-C8-алкил, С3-С6-циклоалкил или OR4, где R4 обозначает H, или C1-C8-алкил, замещенный или незамещенный ОН, OC1-C8-алкилом или галогеном; и
R2, А и В - такие, как определено выше.
Изобретение включает также соли кислотного присоединения соединений формулы 1 с физиологически приемлемыми кислотами. Примеры подходящих физиологически приемлемых органических и неорганических кислот включают хлористоводородную кислоту, бромистоводородную кислоту, фосфорную кислоту, серную кислоту, щавелевую кислоту, малеиновую кислоту, фумаровую кислоту, молочную кислоту, винную кислоту, адипиновую кислоту и бензойную кислоту. Другие кислоты, которые могут быть использованы, описаны в Fortschritte der Arzneimittelforschung. Vol. 10, р. 224 и последующие, Birkhаuser Verlag, Basle and Stuttgart, 1966.
Соединения формулы 1 могут иметь один или более центров асимметрии. Поэтому изобретение включает не только рацематы, но также соответствующие энантиомеры и диастереомеры. Изобретение также включает в каждом случае таутомерные формы.
Соединения формулы 1 могут быть получены способами, аналогичными общепринятым способам, описанным, например, в Houben Weyl "Handbuch der Organishen Chemie", 4th Ed., Thieme Verlag, Stuttgart 1994. Vol. E8/d, р. 479 и последующие; and A.R. Katritzky, C.W. Rees (ed.) "Comprehensive Heterocyclic Chemistry", 1st Ed. Pergamon Press 1984, в частности vol. 5, part 4a, р. 733 и последующие, и в приведенной здесь в качестве ссылок литературе.
Способы получения соединений включают:
i) взаимодействие соединения общей формулы II: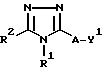
где Y1 обозначает стандартную отщепляемую группу, с соединением общей формулы III:
H-B-Ar;
ii) с целью получения соединения формулы 1, где А обозначает атом кислорода или серы или NR3:
а) взаимодействие соединения общей формулы IV: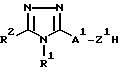
где Z1 обозначает О, S или NR3, и А1 обозначает C1-C18-алкилен, с соединением общей формулы VI:
Y1-А2-B-Ar
где Y1 имеет вышеуказанные значения, и А2 обозначает C1-C18-алкилен, где А1 и А2 вместе содержат от 1 до 18 углеродных атомов;
iii) с целью получения соединения формулы 1, где А включает группу COO или CONR3:
а) взаимодействие соединения общей формулы VII: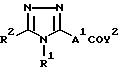
где Y2 обозначает ОН, OC1-С4-алкил, Cl или вместе с CO обозначает активированную карбоксильную группу, и А1 имеет вышеуказанные значения, с соединением формулы VIII:
Z1-A2-B-Ar,
где A2 имеет вышеуказанные значения, и Z1 обозначает ОН или NHR3;
iv) с целью получения соединения формулы l, где А включает группу OCO или NR3CO:
а) взаимодействие соединения формулы IV: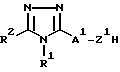
где Z1 обозначает O или NR3, с соединением формулы X:
Y2CO-А2-B-Ar,
где В и Y2 имеют указанные выше значения, и где R1, R2, A, B и Ar имеют вышеуказанные значения.
Описанные здесь реакции обычно протекают в растворителе при температуре от комнатной до температуры кипения используемого растворителя. Примеры растворителей, которые могут быть использованы, включают этилацетат, тетрагидрофуран, диметилформамид, диметоксиэтан, толуол, ксилол или кетон, такой, как ацетон или метилэтилкетон.
В случае необходимости присутствует кислотный акцептор. Подходящие кислотные акцепторы включают неорганические основания, такие, как карбонат натрия или калия, метилат натрия, этилат натрия, гидрид натрия или органические основания такие, как триэтиламин или пиридин. Последний может также служить растворителем.
Сырой продукт выделяют стандартным способом, например, фильтрацией, удаляют растворитель из реакционной смеси перегонкой или экстракцией. Полученное соединение может быть очищено стандартным способом, например, перекристаллизацией из растворителя, хроматографией или превращением в соединение кислотного присоединения.
Соли кислотного присоединения получают общепринятым способом, смешивая свободное основание с подходящей кислотой, возможно, в растворе в органическом растворителе, например, в низшем спирте, таком, как метанол, этанол или пропанол, в простом эфире, таком, как метиловый трет-бутиловый эфир, в кетоне, таком как ацетон или метилэтилкетон, или в сложном эфире, таком как этилацетат.
Вышеуказанные исходные вещества описаны в литературе или могут быть получены известными способами.
Для лечения вышеупомянутых нарушений, соединения по данному изобретению вводят общепринятым способом перорально или парентерально (подкожно, внутривенно, внутримышечно, внутрибрюшинно). Возможно также введение с парами или путeм распыления через носоглотку.
Доза зависит от возраста, состояния и веса пациента и от способа введения. Как правило, суточная доза активного соединения составляет приблизительно от 10 до 1000 мг в день при пероральном введении и приблизительно от 1 до 500 мг в день при парентеральном введении.
Изобретение относится также к фармацевтическим композициям, содержащим соединения по данному изобретению. Эти композиции существуют обычно в твeрдых или жидких фармацевтических лечебных формах, например, в виде таблеток, покрытых плeнкой таблеток, капсул, порошков, гранул, покрытых сахаром таблеток, суппозиториев, растворов или в распылeнных формах. В этих случаях активные соединения могут быть переработаны с общепринятыми фармацевтическими добавками, такими как связывающие вещества, наполнители, консерванты, дисинтеграторы, регуляторы текучести, пластификаторы, смачивающие агенты, диспергаторы, эмульгаторы, растворители, агенты, замедляющие высвобождение, антиоксиданты и/или движущие газы (cf. Н. Sucker et al., Pharmazeutische Technologie, Thieme-Verlag, Stuttgart, 1978). Полученные таким путем лекарственные формы содержат от 1 до 99% по весу активного соединения.
Следующие далее примеры служат для разъяснения изобретения, но не ограничивают его.
Пример 1
4-Метил-3-[3-(4-{ 3-трифторметилфенил} пиперазинил) пропилмеркапто]-4H-1,2,4-триазол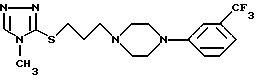
а) 1-(3-Хлорпропил)-4-(3-трифторметилфенил)пиперазин
30 г (0,13 моль) м-трифторметилфенилпиперазина, 23 г (0,146 моль) 1,3-бромхлорпропана и 15 г (0,148 моль) триэтиламина в 200 мл ТГФ кипятят с обратным холодильником 4 ч. Охлаждают, затем фильтруют с отсасыванием и концентрируют. Вязкий остаток растворяют в этилацетате, промывают водой, сушат над MgSO4 и затем концентрируют. Образовавшийся остаток содержит 39 г продукта в виде желтоватого масла (количественный выход).
b) 4-Метил-3-[3-(4-{ 3-трифторметилфенил}пиперазинил) - пропилмеркапто] -4H-1,2,4-триазол
1,15 г (10 ммоль) 3-меркапто-4-метил-4H-1,2,4-триазола, 3,1 г (10,1 ммоль) 1-(3-хлорпропил)-4-(3-трифторметилфенил)-пиперазина и 1,5 г (15 ммоль) триэтиламина в 5 мл ДМФ перемешивают при 100oC 1 ч. Затем смесь выливают в 5%-ную соляную кислоту и экстрагируют этилацетатом. Водную фазу подщелачивают раствором гидроокиси натрия и затем снова экстрагируют этилацетатом и органическую фазу сушат над MgSO4 и концентрируют. Остаток чистят хроматографически (подвижная фаза: CH2Cl2/CH3ОН = 95/5). Получают 2,1 г продукта в виде желтоватого масла (= 55% выход).
ПМР [δ, м. д.]: 2,02 (2H); 2,55 (2H); 2,61 (4H); 3,23 (6H); 3,33 (2H); 3,61 (3H); 7,06 (3H); 7,33 (1H);
Пример 2
4-Метил-3-[5-(4-{ 3-трифторметилфенил} пиперазинил) пентилмеркапто]-4H-1,2,4-триазол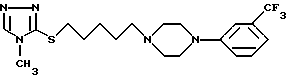
a) 3-(5-Хлорпентилмеркапто)-4-метил-4H-1,2,4-триазол
2,88 г (25 ммоль) 3-меркапто-4-метил-4H-1,2,4-триазола, 4,64 г (25 ммоль) 1,5-бромхлорпентана и 5.58 г (25,5 ммоль) триэтиламина в 100 мл ТГФ кипятят с обратным холодильником 4 ч. Охлаждают с последующей фильтрацией при отсасывании, концентрируют и очищают остаток хроматографически (подвижная фаза: CH2Cl2/CH3ОН = 95/5), получают 1,9 г продукта (= 35% выход).
b) 4-Метил-3-[5-(4-{ 3-трифторметилфенил}пиперазинил) - пентилмеркапто] -4H-1,2,4-триазол
1,9 г (8,66 ммоль) продукта из 2а), 2,19 г (9,52 ммоль) м-трифторметилфенилпиперазина и 0,96 г (9.52 ммоль) триэтиламина в 5 мл ДМФ перемешивают при 90oC 5 ч. Затем смесь выливают в воду и экстрагируют трижды CH2Cl2, и органическую фазу сушат над MgSO4 и концентрируют. Остаток смешивают с метиловым трет-бутиловым эфиром и фильтруют с отсасыванием, маточник концентрируют. Очистка хроматографией (подвижная фаза: CH2Cl2/CH3ОН = 95/5) приводит к 2,1 г продукта (= 59% выход).
Температура плавления 70-76oC.
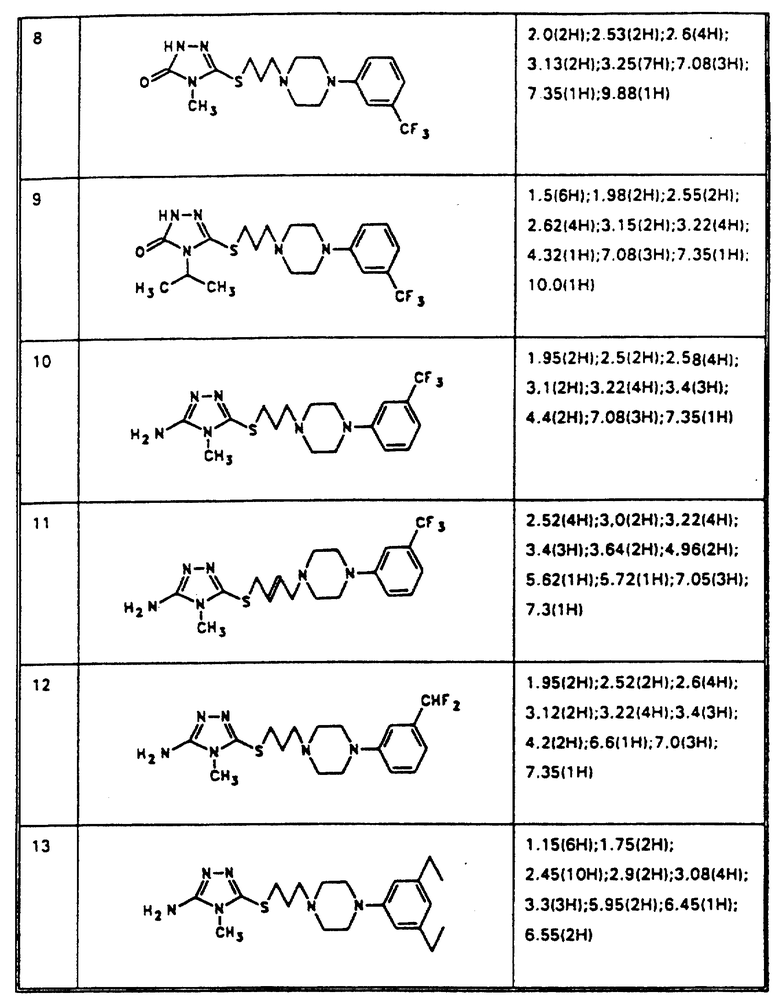
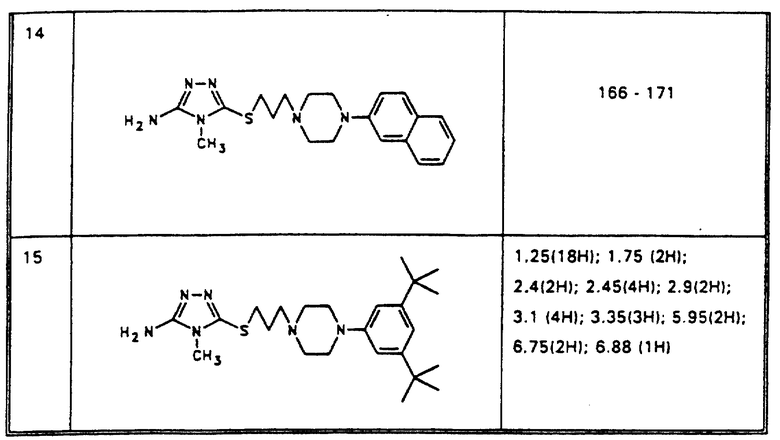
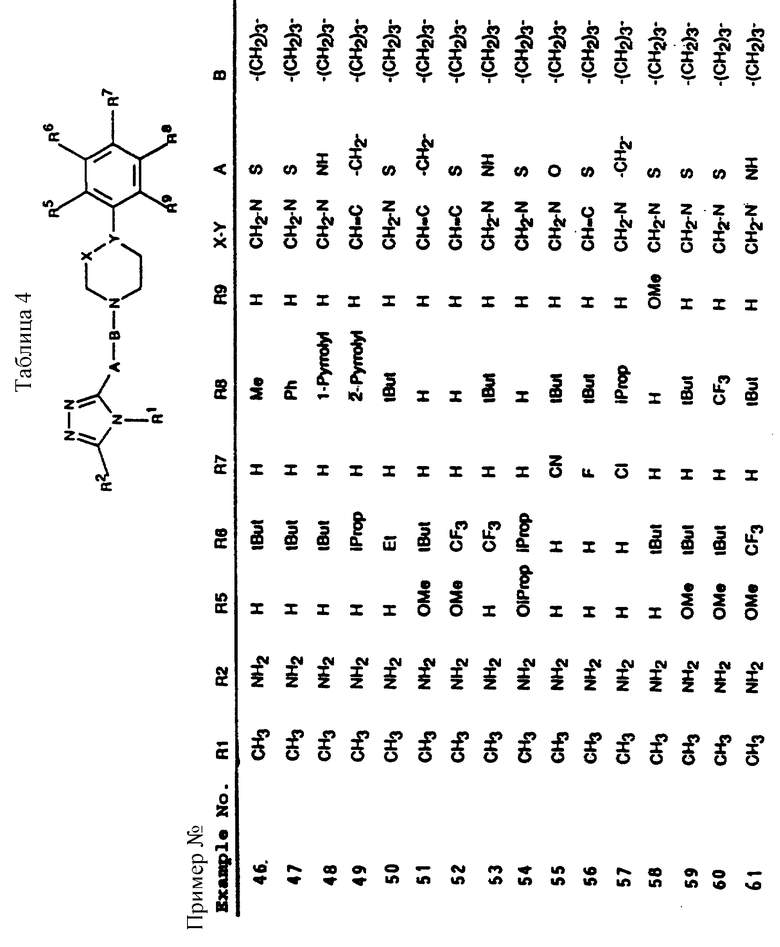
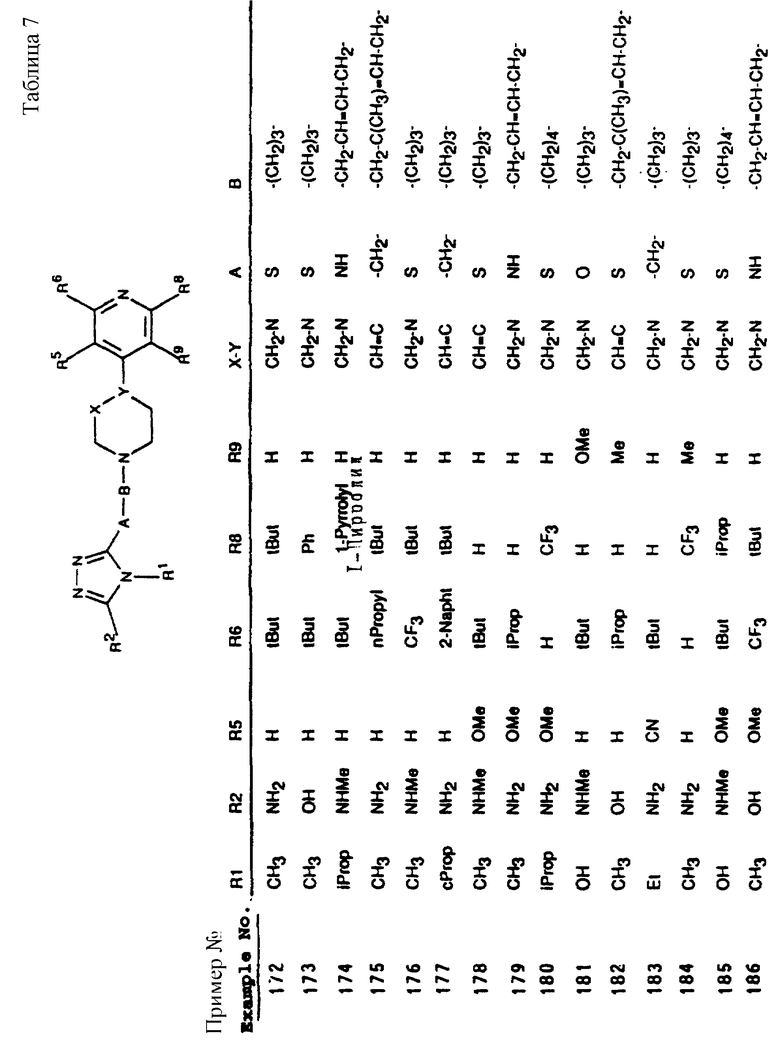
Аналогичным способом получены соединения, приведенные в табл. 1а.
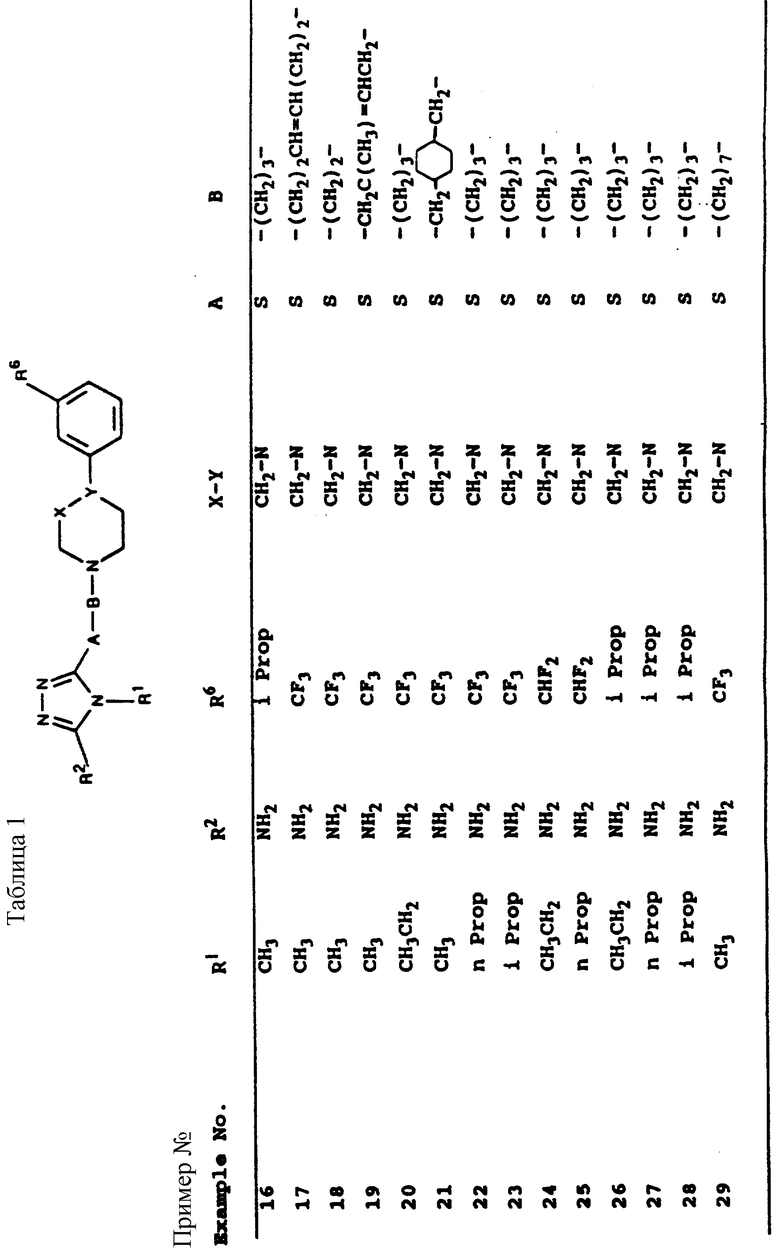
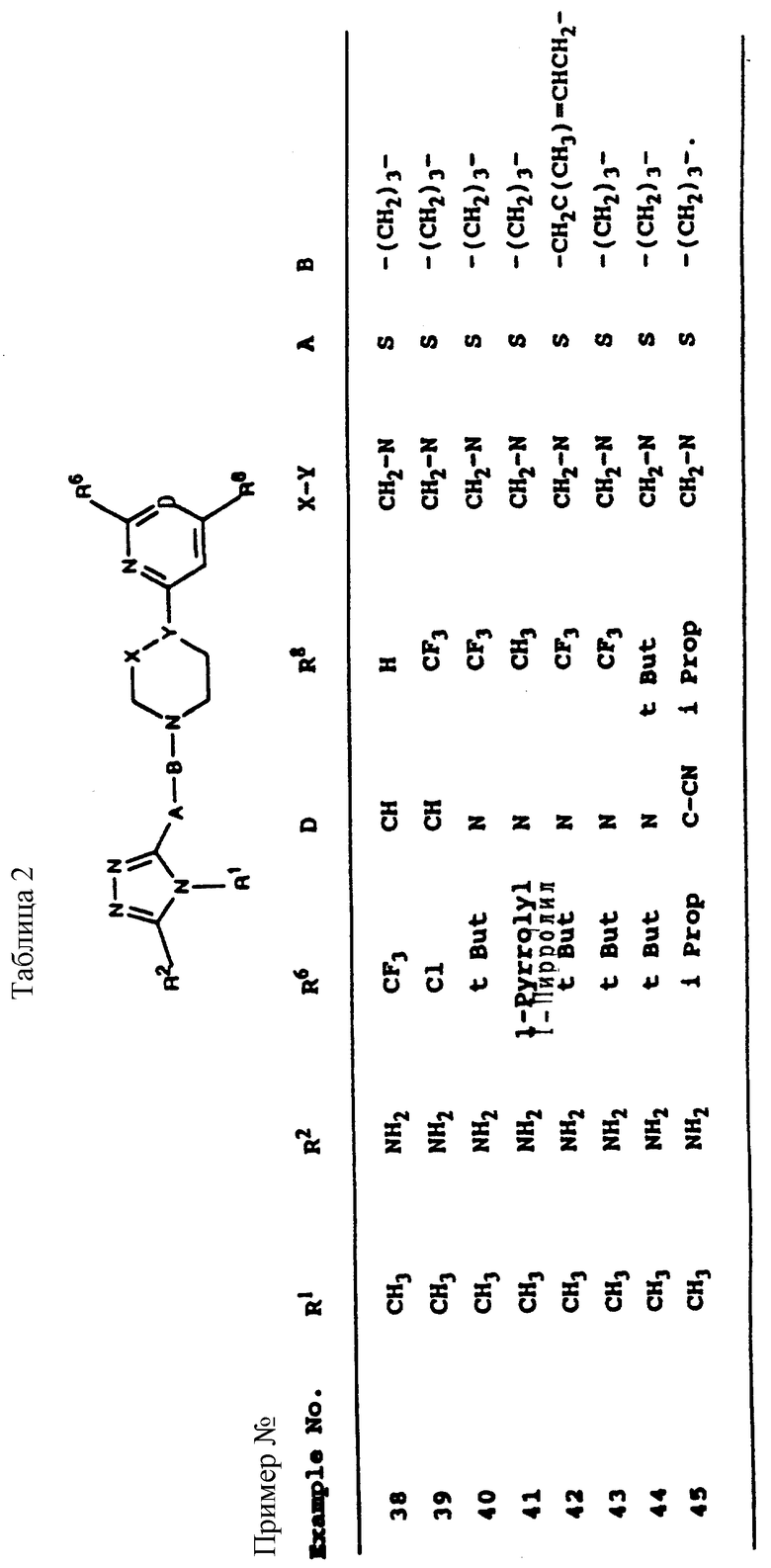
Аналогичным способом получены соединения по изобретению, входящие в таблицы 1-3.
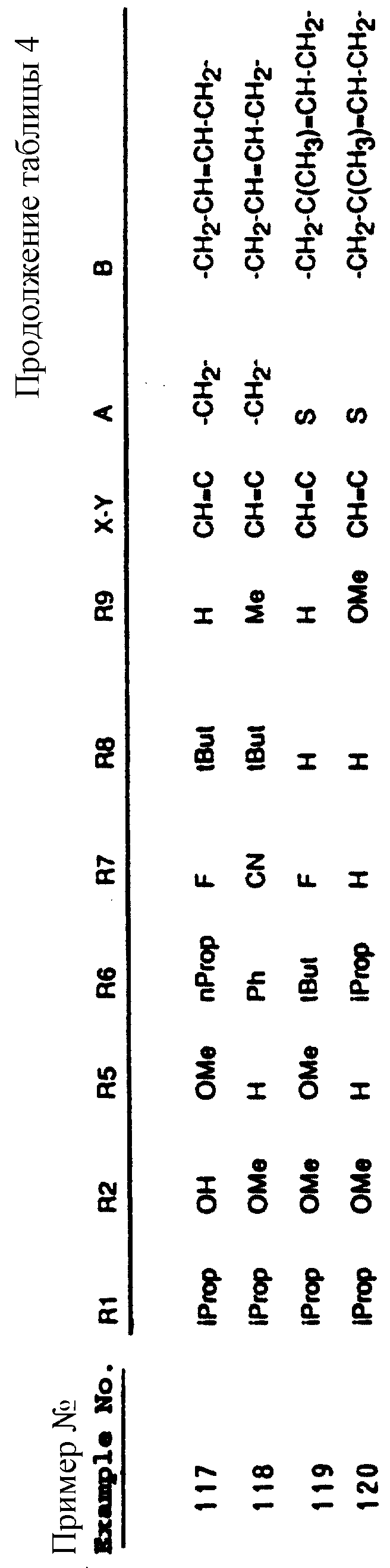
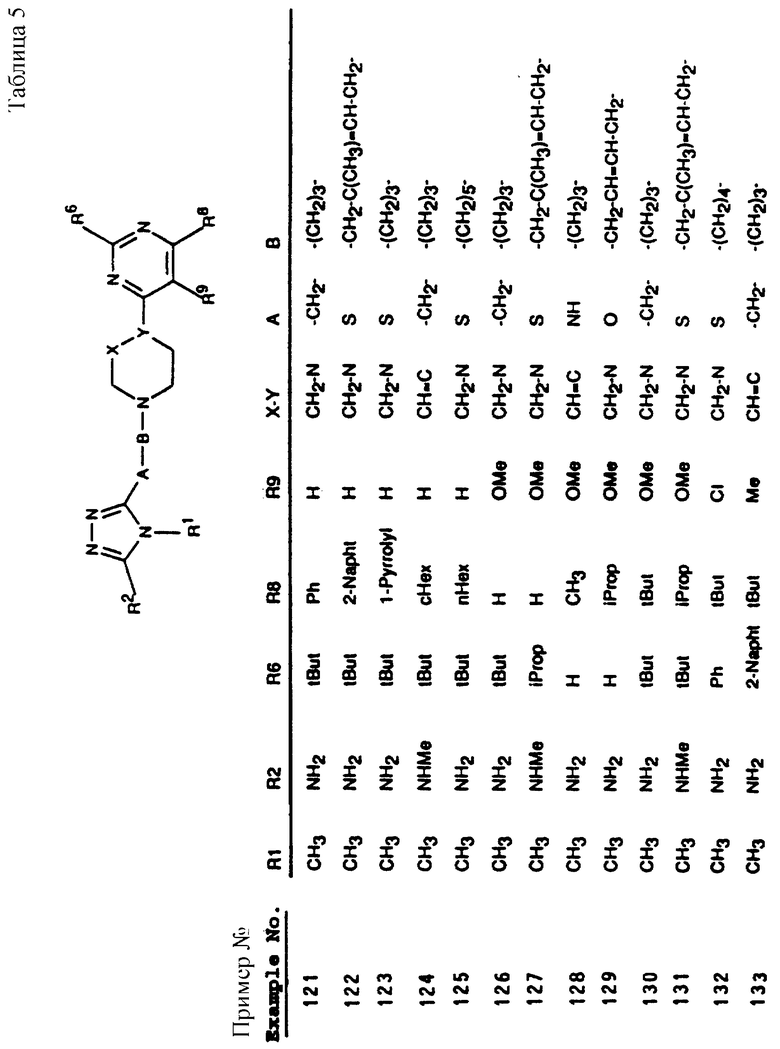
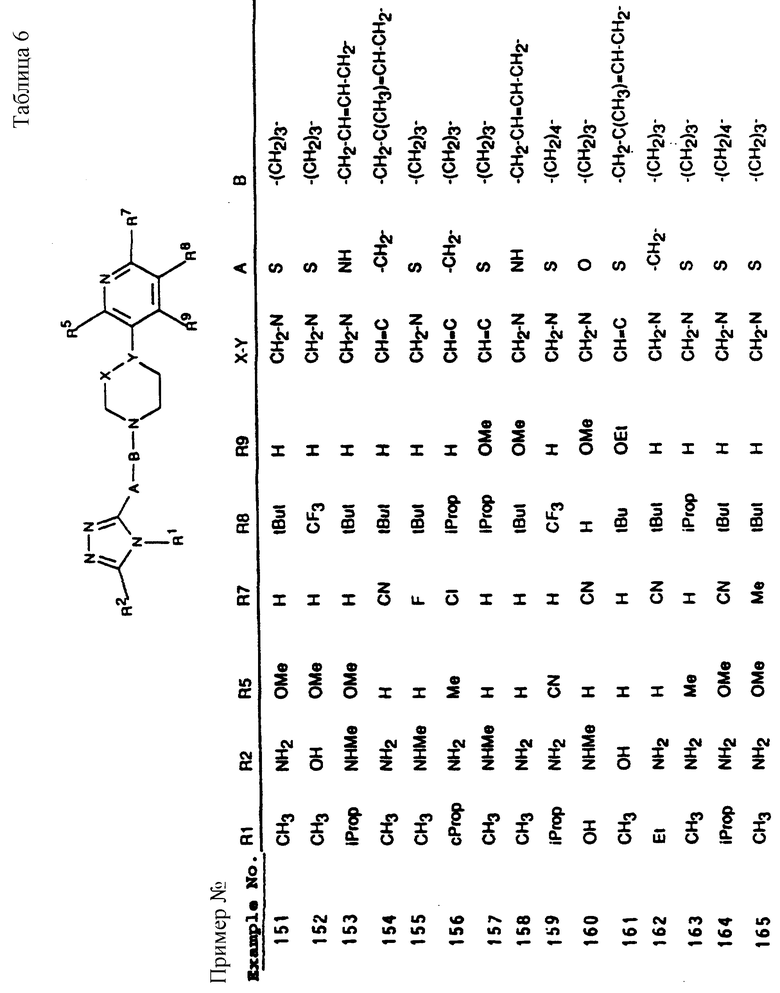
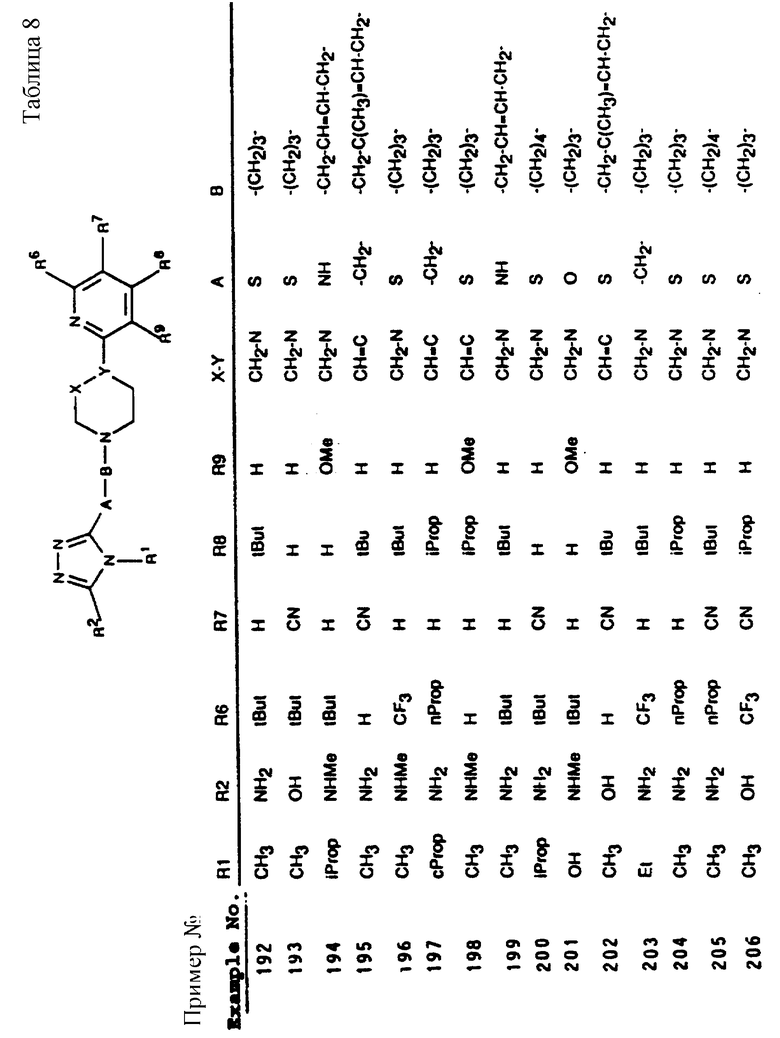
Также аналогичным способом могут быть получены соединения, входящие в таблицы 4-8.
Примеры фармацевтических форм
А) Таблетки
Таблетки следующей композиции прессуют в таблетирующей машине общепринятым способом:
40 мг вещества из примера 1
120 мг кукурузного крахмала
13,5 мг желатина
45 мг лактозы
2,25 мг Аэросила (Aerosil®) (химически чистая двуокись кремния в субмикроскопически тонкой дисперсии)
6,75 мг картофельного крахмала (паста 6%-ной концентрации)
В) Таблетки с сахарным покрытием
20 мг соединения из примера 4
60 мг композиции ядра
70 мг композиции сахарного покрытия
Композиция ядра включает 9 частей кукурузного крахмала, 3 части лактозы и 1 часть винилпирролидон/винилацетатного сополимера при соотношении (60: 40). Композиция сахарного покрытия включает 5 частей сахарозы, 2 части кукурузного крахмала, 2 части карбоната кальция и 1 часть талька. Полученные таким путем покрытые сахаром таблетки снабжают впоследствии энтеросолюбильной оболочкой.
Биологические исследования - изучение рецепторного связывания
1) Испытания по D3-связыванию.
Клонированные мышиные фибропласты CCL 1,3, экспрессирующие человеческий D3-рецептор, получают от Res. Biochemicals Internat. Для изучения связывания используют соответствующие фибропласты Strathmore Rd., Natick, MA 01760-2148 USA.
Приготовление клеток
D3-экспрессирующие клетки выращивают в RPMI-1640, содержащей 10%-ную сыворотку плода коровы (GIBCO N 041-32400N), 100 ед/мл пенициллина и 0.2% стрептомицин (GIBCO BRL, Gaithersburg, MD, USA). Через 48 ч клетки промывают PBS (фосфатно-солевым буферным раствором) и инкубируют с 0.05% трипсинсодержащим PBS в течение 5 мин. Затем среду нейтрализуют и клетки собирают центрифугированием при 300 об/мин. Для лизирования клеток осадок после центрифугирования промывают кратковременно лизирующим буфером (5 мМ трис-HCl, pH 7,4 с 10% глицерина) и затем инкубируют при концентрации лизирующего буфера 107 клетки/мл при 4oC в течение 30 мин. Клетки центрифугируют при 200 об/мин в течение 10 мин, и осадок после центрифугирования хранят в жидком азоте.
Испытания по связыванию
Для испытания по D3-рецепторному связыванию мембраны суспендируют в инкубационном буфере (50 мМ трис-HCl, pH 7,4 со 120 мМ NaCl, 5 мМ KCl, 2 мМ CaCl2, 2 мМ MgCl2, 10 мкМ хинолина, 0,1% аскорбиновой кислотой и 0,1% BSA (альбумина бычьей сыворотки)) при концентрации около 106 клетки/250 мкл испытуемой смеси и инкубируют при 30oC с 0,1 нМ 125иодсульпиридом в присутствии или отсутствии испытуемого соединения. Неспецифическое связывание измеряют, используя 10-6 М спиперон.
Через 60 мин свободный и связанный радиолиганд разделяют фильтрацией через GF/B фильтры из стекловолокна (Whatman, England) на сборнике клеток Skatron'a (Skatron, Lier, Norway), и фильтры промывают охлажденным льдом трис-HCl-буферным раствором, pH 7,4. Собранную на фильтрах радиоактивность измеряют, используя жидкий сцинтилляционный счетчик Packard'a 2200 CA.
Значения Кi определяют путем анализа по методу нелинейной регрессии, используя LIGAND-программу.
2) Испытание по D2-связыванию.
Приготовление мембран
а) Каудатус ядер (бычьи)
Каудатус ядер выделяют из головного мозга быка и промывают охлаждаемым льдом 0,32 М раствором сахарозы. После взвешивания материал растирают в порошок и гомогенизируют в 5-10 объемах раствора сахарозы, используя гомогенизатор Potter-Elvehjem'a (500 об/мин). Гомогенат центрифугируют при 3000 об/мин в течение 15 мин (4oC) и полученный супернатант снова центрифугируют 15 мин при 40000 об/мин. Затем остаток промывают дважды, ресуспендируя и центрифугируя, с 50 мМ трис-HCl, pH 7,4. Мембраны до использования хранят в жидком азоте.
b) Стриатум (крыс)
Стриатумы Spragne-Dawley крыс промывают охлаждаемым льдом 0,32 М раствором сахарозы. После взвешивания участки головного мозга гомогенизируют в 5-10 объемах раствора сахарозы, используя гомогенизатор Potter-Elvehjem'a (500 об/мин). Гомогенат центрифугируют при 40000 об/мин в течение 10 мин (4oC), и затем остаток промывают несколько раз, ресуспендируя и центрифугируя, с 50 мМ трис-HCl, 0,1 мМ EDTA (этилендиаминтетрауксусной кислотой) и 0.01%-ной аскорбиновой кислотой (pH 7,4). Промытый остаток ресуспендируют в вышеупомянутом буфере и инкубируют при 37oC 20 мин (чтобы разрушить эндогенный допамин). Затем мембраны дважды промывают буфером и порции замораживают в жидком азоте. Мембранный препарат хранится максимум одну неделю.
Испытание по связыванию
а) 3H-Спиперон (D2низк.)
Мембраны ядерных каудатусов растворяют в инкубационном буфере (мМ: трис- HCl 50, NaCl 120, KCl 5, MgCl2 1, CaCl2 2, pH 7,4). Готовят различные смеси, по 1 мл каждой:
- Общее связывание: 400 мкг мембран + 0,2 нмоль/л 3H- спиперона (Du Pont de Nemours, NET-565).
- Неспецифическое связывание: те же смеси, что для общего связывания + 10 мкМ (+)-бутакламола.
- Испытуемое соединение: те же смеси, что для общего связывания + возрастающие концентрации испытуемого соединения.
После инкубации при 25oC в течение 60 мин смеси фильтруют через GF/B фильтры из стекловолокна (Whatman, England) на сборнике клеток Skatron (от Zinsser, Frankfurt) и фильтры промывают охлажденным льдом 50 мМ трис-HCl буфером, pH 7,4. Собранную на фильтрах радиоактивность измеряют, используя жидкий сцинтилляционный счeтчик Packard'а 2200 CA.
Значения Ki определяют путeм анализа по методу нелинейной регрессии, используя LIGAND-программу или преобразованием IC50 значений, используя формулу Cheng'a и Prusoff'a.
b) 3H-ADTN (D2выс.)
Мембраны стриатумов растворяют в инкубационном буфере (50 мМ трис-HCl, pH 7,4, 1 мМ MnCl и 0,1%-ная аскорбиновая кислота).
Готовят различные смеси, каждой по 1 мл.
- Общее связывание: 300 мкг влажного веса + 1 мМ 3H-ADTN (Du Рont de Nemours, синтез на заказ) + 100 нМ SCH 23390 (содержащего D1-рецепторы).
- Неспецифическое связывание: те же смеси, что для общего связывания + 50 нМ спиперона.
- Испытуемое соединение: те же смеси, что для общего связывания + возрастающие концентрации испытуемого соединения.
После инкубации при 25oC в течение 60 мин, смеси фильтруют через GF/B фильтры из стекловолокна (Whatman, England) на сборнике клеток Skatron'a (от Zinsser, Frankfurt), и фильтры промывают охлажденным льдом 50 нМ трис-HCl буфером, pH 7,4. Собранную на фильтрах радиоактивность измеряют, используя жидкий сцинтилляционный счетчик Packard'а 2200 CA.
Оценку производят аналогично пункту а), приведенному выше.
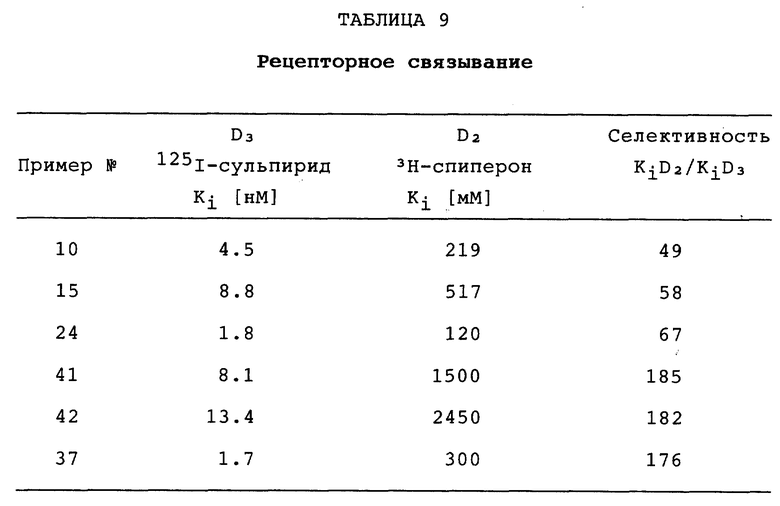
В этих испытаниях соединения по данному изобретению проявляют очень хорошее сродство и высокую селективность в отношении D3-рецептора. Полученные для представленных соединений результаты собраны в таблицу 9.
Для сравнения соединение формулы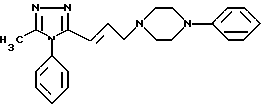
(патент США 4577020; пример 3) подвергают приведенному выше испытанию на D3-связывание. Получена Ki 4100 [нМ]; т.е. соединение действительно не обладает сродством к D3-рецептору.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОЕДИНЕНИЕ ПИРИМИДИНА(ВАРИАНТЫ) И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ СРОДСТВОМ К ДОПАМИН D3-РЕЦЕПТОРАМ | 1995 |
|
RU2172736C2 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ОСНОВЕ ПРОИЗВОДНЫХ ТИАЗОЛА ИЛИ ТИАДИАЗОЛА, ПРОИЗВОДНЫЕ ТИАЗОЛА ИЛИ ТИАДИАЗОЛА И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1995 |
|
RU2173687C2 |
| ПРОИЗВОДНЫЕ ПИРАЗИН-2-КАРБОКСАМИДА В КАЧЕСТВЕ АНТАГОНИСТОВ mGluR5 | 2006 |
|
RU2407739C2 |
| ПРОИЗВОДНЫЕ АЗЕТИДИНА В КАЧЕСТВЕ АНТАГОНИСТОВ CCR-3 РЕЦЕПТОРА | 2003 |
|
RU2314292C2 |
| ПРОИЗВОДНЫЕ ТИАЗОЛА В КАЧЕСТВЕ АНТАГОНИСТОВ А2В | 2005 |
|
RU2374242C2 |
| СПОСОБ ПОЛУЧЕНИЯ ОКСАЗОЛОВ КОНДЕНСАЦИЕЙ АРОМАТИЧЕСКИХ АЛЬДЕГИДОВ С АЛЬФА-КЕТОКСИМАМИ С ОБРАЗОВАНИЕМ N-ОКСИДОВ И ПОСЛЕДУЮЩИМ ВЗАИМОДЕЙСТВИЕМ С АКТИВИРОВАННЫМИ ПРОИЗВОДНЫМИ КИСЛОТ | 2005 |
|
RU2402537C2 |
| НОВЫЕ ФЛУОРЕСЦИРУЮЩИЕ СОЕДИНЕНИЯ | 2012 |
|
RU2587082C2 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ЦИКЛОГЕКСИЛМЕТИЛА | 2006 |
|
RU2451009C2 |
| ПРОДУКТ, ВКЛЮЧАЮЩИЙ ПО МЕНЬШЕЙ МЕРЕ ОДНО ВЕЩЕСТВО, ИНГИБИРУЮЩЕЕ NO-СИНТАЗЫ, В КОМБИНАЦИИ ПО МЕНЬШЕЙ МЕРЕ С ОДНИМ ВЕЩЕСТВОМ, ИНГИБИРУЮЩИМ ФОСФОЛИПАЗЫ А2 | 2000 |
|
RU2256465C2 |
| ПУРИНОВЫЕ ПРОИЗВОДНЫЕ ДЛЯ ПРИМЕНЕНИЯ В КАЧЕСТВЕ АГОНИСТОВ АДЕНОЗИНОВОГО РЕЦЕПТОРА А-2А | 2005 |
|
RU2403253C2 |
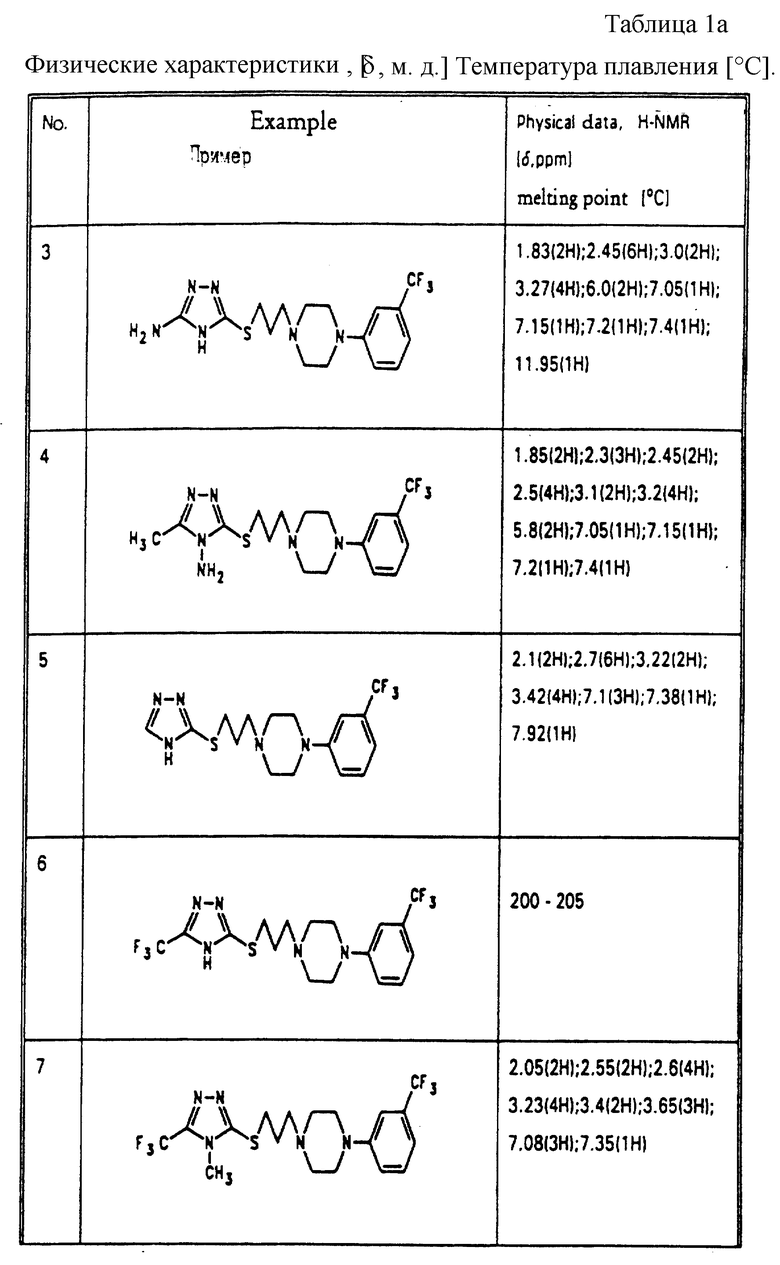











Изобретение относится к новым соединениям триазола общей формулы (1), где А обозначает линейную или разветвленную С1-С18-алкиленовую группу, которая может включать по крайней мере одну группу, которую выбирают из О, S, CONH, COO, С3-С6-циклоалкилена или двойную или тройную связь; В обозначает радикал формулы (а), (в) или (с); R1 обозначает Н, NH2, С3-С6-циклоалкил или С1-С8-алкил, который не замещен или замещен OС1-С8-алкилом; R2 обозначает Н, ОН, С1-С8-алкил, С3-6-циклоалкил, CF3, CN, NR3R4, SR3 или CO2R3, где R3 обозначает Н или С1-С8-алкил, a R4 обозначает Н, С1-С8-алкил или COR3, где R3 обозначает С1-С8-алкил; Ar обозначает нафтил, фенил, имеющий 1-2 заместителя, выбранных из С1-С8-алкила, CF3, CHF2, NO2, SR3, SO2R3, где R3 означает С1-С8-алкил; а также пиридил, пиримидил или триазинил, которые имеют от 1 до 3 заместителей, выбранных из С1-С8-алкила, С2-С6-алкенила, C2-C6-алкинила, галогена, CN, CF3, OR4, где R4 означает водород или С1-С8-алкил, CO2R3, где R3 означает С1-С8-алкил, фенил, который может быть замещен галогеном, алкокси- или феноксигруппой, C3-C6-циалоалкила, возможно конденсированного, фенилалкиламина или 5-членного ароматического гетероцикла с 1-2 атомами азота, который может быть сконденсирован с бензольным кольцом. Соединения по данному изобретению обладают высоким сродством к допамин-D3-рецепторам и поэтому могут быть использованы для лечения нарушений, реагирующих на допамин-D3-лиганды. Описывается также фармацевтическая композиция на основе соединений формулы (1). 2 с. и 9 з.п. ф-лы, 10 табл.

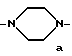
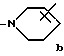
или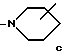

где А обозначает линейную или разветвленную C1-C18-алкиленовую группу, которая может включать по крайней мере одну группу, которую выбирают из О, S, CONH, СОО, C3-C6-циклоалкилена, или двойную или тройную связь;
В обозначает радикал формулы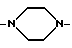
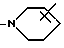
или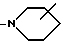
R1 обозначает Н, NH2, C3-C6-циклоалкил или C1-C8-алкил, который не замещен или замещен ОC1-C8-алкилом;
R2 обозначает Н, ОН, C1-C8-алкил, C3-C6 циклоалкил, СF3, CN, NR3R4, SR3 или CO2R3,
где R3 обозначает Н или C1-C8-алкил, a R4 обозначает Н, C1-C8-алкил или COR3, где R3 в данном случае означает только C1-C8-алкил;
Аr обозначает нафтил, фенил, имеющий 1-2 заместителя, выбранных из C1-C8-алкила, СF3, CHF2, NO2, SR3, SO2R3, CO2R3, где R3 в данном случае означает только C1-C8-алкил, OR4, где R4 в данном случае означает только C1-C8-алкил, а также пиридил, пиримидил или триазинил, которые имеют от 1 до 3 заместителей, выбранных из C1-C8-алкила, C2-C6-алкенила, C2-C6-алкинила, галогена, CN, СF3, OR4, где R4 означает водород или C1-C8-алкил, CO2 R3, где R3 в данном случае означает только C1-C8-алкил, фенила, который может быть замещен галогеном, алкокси- или феноксигруппой, C3-C6-циклоалкила, возможно конденсированного, фенилалкиламина или 5-членного ароматического гетероцикла с 1-2 атомами азота, который может быть сконденсирован с бензольным кольцом,
или его соль с физиологически активными кислотами.
А, В, R2 имеют значения по п.1.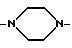
или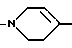
Аr обозначает фенил, который имеет от одного до двух заместителей, которые независимо друг от друга обозначают C1-C8-алкил, OC1-C8-алкил, CHF2, СF3.
| ГОРЕЛОЧНОЕ УСТРОЙСТВО ДЛЯ СЖИГАНИЯ ГАЗООБРАЗНОГО И ЖИДКОГО ТОПЛИВА | 2014 |
|
RU2551439C1 |
| ПРОМЕЖУТОЧНЫЙ ПРИВОД ЛЕНТОЧНОГО КОНВЕЙЕРА И СПОСОБ УПРАВЛЕНИЯ ИМ | 2014 |
|
RU2552759C1 |
| US 4577020, 1986 | |||
| Хонинговальная головка | 1975 |
|
SU649539A1 |
| УСТРОЙСТВО ДЛЯ КАЛИБРОВКИ ПЛОДОВ И ИМ ПОДОБНЫХ ПРЕДМЕТОВ | 0 |
|
SU261804A1 |
| EP 0225718, 1987 | |||
| Способ получения производных 1,2,4-триазолокарбамата или их кислотно-аддитивных солей | 1985 |
|
SU1436873A3 |
Авторы
Даты
2001-05-27—Публикация
1995-07-14—Подача