Настоящее изобретение относится к способу получения спиртов с использованием (3-алкоксифенил) хлоридов магния.
Многие фармацевтические и агрохимические действующие вещества содержат в своем составе м-анизильную группу. Эту группу предпочтительно с помощью металлоорганического м-анизильного соединения, прежде всего м-анизильного соединения Гриньяра, вводят в синтезируемое соединение. В качестве соединения Гриньяра используют при этом м-анизилбромид магния, который получают взаимодействием м-анизилбромида с металлическим магнием в соответствующем растворителе (см. Arzn. Forsch. /Drug Res. 28(I), 107 (1978)).
При получении соединений Гриньяра обычно используют реакционноспособные бромиды. Однако по экономическим и экологическим причинам при получении соединений Гриньяра замещению бромидов предпочитают обладающие меньшей реакционной активностью хлориды, поскольку последние являются, во-первых, более дешевыми продуктами и, во-вторых, благодаря своей более низкой молекулярной массе обусловливают образование меньших количеств солей. Кроме того, при использовании хлоридов образуется меньше побочных продуктов.
Из патента США 2959596 и публикации в Journ. Chem. Soc. 1968, 1265 известно получение и применение о- и п-анизилхлорида магния. В патенте Японии 60/72833, сущность которого опубликована в Derwent WPI Асе 85-137805/23, описывается (4-этоксифенил) хлорид магния без указания способа его получения. В отличие от этого получение и применение (3-метоксифенил)- и (3-этоксифенил)хлорида магния до настоящего времени не было описано. Это объясняется электронной дезактивацией ароматических углеводородов алкоксигруппой в мета-положении.
Из ЕР 0073569 известен способ получения спиртов с использованием соединений Гриньяра путем непрерывной подачи части необходимого количества органического галогенида и необходимого количества магния в среде инертного растворителя в первую реакционную зону для получения реактива Гриньяра с последующей непрерывной подачей полученной реакционной смеси, включающей реактив Гриньяра, во вторую реакционную зону, куда непрерывно подают оставшуюся часть органического галогенида и необходимое количество карбонильного соединения необязательно в среде инертного органического растворителя. Полученную таким образом реакционную смесь, включающую продукт реакции Гриньяра, гидролизуют с получением спирта.
Положенная в основу настоящего изобретения задача состояла в разработке способа получения (3-алкоксифенил) хлоридов магния.
Неожиданным образом было установлено, что (3-алкоксифенил) хлориды магния с одним до пяти атомов углерода в алкоксильном остатке могут быть получены взаимодействием соответствующих 3-алкоксифенилхлоридов с активированным магнием с высоким выходом.
Предметом изобретения в соответствии с этим является способ получения спиртов с использованием (3-алкоксифенил) хлоридов магния с одним до пяти атомов углерода в алкоксильном остатке, которые получают взаимодействием 3-алкоксифенилхлорида с активированным магнием, получаемым путем восстановления галогенидов магния с помощью щелочного металла.
Для осуществления способа согласно изобретению пригоден прежде всего активированный магний, получаемый путем восстановления галогенидов магния, прежде всего хлорида магния с помощью лития, натрия или калия (см. Journ. Org. Chem. 52, 3674 (1987); Journ. Am. Chem. Soc. 96, 1775 (1974)). Реакцию восстановления проводят обычно с 1-5%-ным молярным избытком галогенида магния в инертном растворителе либо в смеси растворителей, например, в простых алифатических эфирах, таких как тетрагидрофуран, замещенные тетрагидрофураны, диметоксиэтан и/или диметилдигликоль, при температурах в интервале от 65oС до 162oС. Для успешного осуществления реакции может оказаться целесообразным проводить восстановление в присутствии солей щелочных и щелочноземельных металлов, например, иодидов щелочных металлов, сульфатов щелочных металлов и/или сульфатов щелочноземельных металлов. Получаемый путем восстановления активированный магний предпочтительно без выделения взаимодействием с 3-алкоксифенилхлоридом, содержащим от одного до пяти атомов углерода в алкоксильном остатке, трансформируют в соответствующее соединение Гриньяра. С1-С5-алкоксильный остаток в фенилхлоридном соединении может быть прямоцепочечным, разветвленным либо циклическим. Предпочтительны фенилхлоридные соединения с алкоксильным остатком в мета-положении, выбранным из группы, включающей метокси, этокси, пропокси, изопропокси, н-бутокси и циклопентокси. Наиболее предпочтительными для проведения взаимодействия с активированным магнием являются 3-метоксифенилхлорид и 3-этоксифенилхлорид.
С помощью предлагаемого согласно изобретению способа магниевохлоридные соединения можно получать без образования побочных продуктов и с высоким выходом. Если в отличие от этого 3-алкоксифенилхлориды подвергают взаимодействию с неактивированным магнием в присутствии небольших количеств дибромэтана или же если эту реакцию осуществляют по описанному в европейской заявке ЕР 307106 способу для 3-трет-бутоксифенилхлорида с использованием неактивированного магния в присутствии этилбромида, то соответствующие соединения Гриньяра получают лишь с неудовлетворительным выходом. Кроме того, в этой реакции в значительных количествах образуются побочные продукты.
Взаимодействием с получаемыми согласно изобретению (3-алкоксифенил) хлоридами магния альдегиды и кетоны можно трансформировать в соответствующие спирты с хорошим выходом.
Еще одним предметом изобретения в соответствии с этим является применение (3-алкоксифенил) хлорида магния с одним до пяти атомов углерода в алкоксильном остатке для осуществления взаимодействия с β-аминоальдегидом или с β-аминокетоном формулы I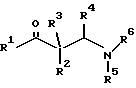 ,
,
в которой R1 означает Н или С1-С4алкил, R2 означает Н или C1-С4алкил либо R2 вместе с R1 представляет собой -(СH2)4-, либо R2 вместе с R3 представляет собой С4-С7циклоалкил, либо R2 вместе с R4 представляет собой С5-С8циклоалкил, либо R2 вместе с R5 представляет собой пяти-восьмичленный гетероцикл, R3 означает Н или прямоцепочечный С1-С4алкил, R4 является Н и R5 означает С1-С3алкил и R6 означает С1-С3алкил или же для осуществления взаимодействия с альдегидом или кетоном формулы II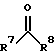 ,
,
в которой R7 и R8 являются идентичными либо различными и означают соответственно Н, С1-С6алкил или С3-С6циклоалкил.
Для осуществления вышеуказанного взаимодействия с β-аминоальдегидом или β-аминокетоном предпочтительно используют (3-алкоксифенил)хлорид магния, где алкоксильный остаток представляет собой метокси, этокси, пропокси, изопропокси, н-бутокси или пиклопентокси, наиболее предпочтительны (3-метоксифенил) хлорид магния или (3-этоксифенил) хлорид магния. К особенно пригодным β-аминоальдегидам или β-аминокетонам относятся таковые формулы I, в которой R1 является С1-С4алкилом, R2 означает Н или С1-С4алкил или R2 вместе с R1 представляет собой -(СН2)4-, R3 представляет собой Н или прямоцепочечный С1-С4алкил, а R4 означает Н, R5 означает СН3 и R6 означает СН3.
Конверсию полученного согласно изобретению магниевохлоридного соединения осуществляют по известной методике, подвергая соединение Гриньяра в растворителе либо в смеси растворителей, например, в простых алифатических эфирах, таких как тетрагидрофуран, замещенные тетрагидрофураны, простые диалкиловые эфиры и/или диоксан, и/или в ароматическихуглеводородах, таких как бензол, толуол и/или ксилол, при температурах в интервале от -78oС до 120oС взаимодействию с соединением формулы I или II.
Примеры
Все реакции проводили с использованием безводных растворителей и реагентов в атмосфере защитного газа.
Пример 1
Получение (3-метоксифенил) хлорида магния
2,04 г (21,4 ммоля) хлорида магния помещали в трехгорлую колбу объемом 100 мл, снабженную обратным холодильником, термометром и капельной воронкой, и покрывали слоем из 50 мл тетрагидрофурана (ТГФ). Затем порциями добавляли 0,82 г (21,0 ммоль) свеженарезанного калия и при перемешивании нагревали в течение 90 мин с обратным холодильником. Далее в течение 30 мин с использованием обратного холодильника по каплям добавляли 3,05 г (21,4 ммоля) 3-хлоранизола, растворенного в 20 мл ТГФ. После добавления перемешивали в течение 20 ч при комнатной температуре и полученное соединение Гриньяра использовали в последующей реакции.
Пример 2
Получение 2-((диметиламино) метил)-1-(3-метоксифенил) циклогексанола
К раствору полученного согласно примеру 1 (3-метоксифенил) хлорида магния при охлаждении ледяной баней по каплям добавляли в течение 40 мин 3,32 г (21,4 ммоля) 2-(диметиламино) метилциклогексанона, растворенного в 10 мл ТГФ. После 24-часового перемешивания при комнатной температуре при охлаждении ледяной баней гидролизовали 20 мл 20%-ного раствора хлорида аммония. Органическую фазу отделяли, а водную фазу еще дважды экстрагировали этиловым эфиром уксусной кислоты. Объединенные органические фазы сушили над сульфатом магния и фильтровали. После удаления перегонкой растворителя получали 3,4 г (60% от теории) циклогексанолового соединения.
| название | год | авторы | номер документа |
|---|---|---|---|
| 6-ДИМЕТИЛАМИНОМЕТИЛ-1-ФЕНИЛЦИКЛОГЕКСАНОВЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ФАРМАЦЕВТИЧЕСКИ ДЕЙСТВУЮЩИХ ВЕЩЕСТВ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ) | 1996 |
|
RU2178409C2 |
| ЗАМЕЩЕННЫЕ АМИНОСОЕДИНЕНИЯ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1998 |
|
RU2197474C2 |
| ЗАМЕЩЕННЫЕ ЦИКЛОГЕПТЕНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1999 |
|
RU2233268C2 |
| ПРОИЗВОДНЫЕ ГЕТЕРОЦИКЛИЧЕСКИХ БЕНЗОЦИКЛОАЛКЕНОВ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1998 |
|
RU2197484C2 |
| ДИМЕТИЛ(3-АРИЛБУТ-3-ЕНИЛ)АМИНОСОЕДИНЕНИЯ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 1997 |
|
RU2167146C2 |
| НОВЫЕ ПРОИЗВОДНЫЕ БЕНЗОКСАЗИНДИОНА И ЛЕКАРСТВЕННЫЙ ПРЕПАРАТ НА ИХ ОСНОВЕ | 1998 |
|
RU2184114C2 |
| ЗАМЕЩЕННЫЕ ИМИДАЗОЛИДИН-2,4-ДИОНОВЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ФАРМАЦЕВТИЧЕСКИХ ДЕЙСТВУЮЩИХ ВЕЩЕСТВ | 1996 |
|
RU2163603C2 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ 1-АМИНОБУТАН-3-ОЛА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2001 |
|
RU2288219C2 |
| 1-ФЕНИЛ-2-ДИМЕТИЛАМИНОМЕТИЛЦИКЛОГЕКСАН-1-ОЛОВЫЕ СОЕДИНЕНИЯ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ИХ ОСНОВЕ | 1996 |
|
RU2167148C2 |
| СОЛИ БИЦИКЛИЧЕСКИХ N-АЦИЛИРОВАННЫХ ИМИДАЗО-3-АМИНОВ ИЛИ ИМИДАЗО-5-АМИНОВ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2001 |
|
RU2268888C2 |
Изобретение относится к способу получения спиртов взаимодействием карбонильного соединения с органическим производным галогенида магния, полученного взаимодействием соответствующего органического галогенида с активированным магнием. В качестве карбонильного соединения используют β-аминоальдегид или β-аминокетон формулы (I)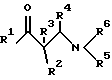 ,
,
в которой R1 означает Н или C1-C4 алкил, R2 означает Н или C1-C4 алкил, либо R2 вместе с R1 представляет собой -(СН2)4-, либо R2 вместе с R3 представляет собой С4-С7 циклоалкил, либо R2 вместе с R4 представляет собой C5-C8 циклоалкил, либо R2 вместе с R5 представляет собой пяти-восьмичленный гетероцикл, R3 означает Н или прямоцепочный C1-C4 алкил, R4 является Н и R5 означает C1-С3 алкил и R6 означает C1-С3 алкил либо альдегид или кетон формулы (II)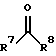 ,
,
в которой R7 и R8 являются идентичными либо различными и означают соответственно Н, C1-C6 алкил или С3-С6 циклоалкил. В качестве органического производного галогенида магния используют (3-алкоксифенил)магнийхлорид, содержащий от одного до пяти атомов углерода в алкоксильном остатке. В качестве органического галогенида используют (3-алкоксифенил)хлорид, при этом активированный магний получают восстановлением галогенидов магния щелочным металлом. В результате повышается выход спиртов. 7 з. п. ф-лы.
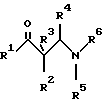
в которой R1 означает Н или С1-С4алкил, R2 означает Н или С1-С4алкил либо R2 вместе с R1 представляет собой -(СН2)4-, либо R2 вместе с R3 представляет собой С4-С7циклоалкил, либо R2 вместе с R4 представляет собой С5-С8циклоалкил, либо R2 вместе с R5 представляет собой пяти-восьмичленный гетероцикл, R3 означает Н или прямоцепочечный С1-С4алкил, R4 является Н и R5 означает С1-С3алкил и R6 означает С1-С3алкил, либо альдегид или кетон формулы (II)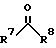
в которой R7 и R8 являются идентичными либо различными и означают соответственно Н, C1-C6алкил или С3-С6циклоалкил, в качестве органического производного галогенида магния используют (3-алкоксифенил)магнийхлорид, содержащий от одного до пяти атомов углерода в алкоксильном остатке, и в качестве органического галогенида используют (3-алкоксифенил) хлорид, при этом активированный магний получают восстановлением галогенидов магния щелочным металлом.
| Отрывной табель-календарь | 1947 |
|
SU73569A1 |
| Способ получения @ 2-метил(1,1 @ -бифенил)-3-ил @ -метанола | 1986 |
|
SU1424728A3 |
| 0 |
|
SU156949A1 |
Авторы
Даты
2002-01-10—Публикация
1997-02-14—Подача