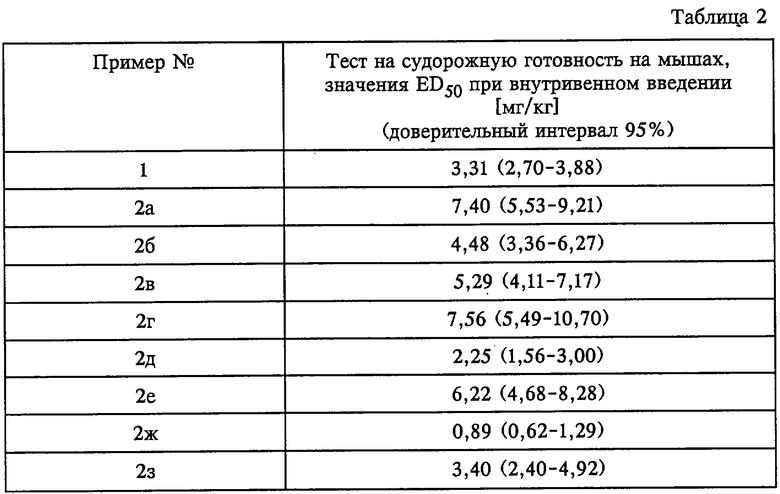
Настоящее изобретение относится к замещенным циклогептенам общей формулы I
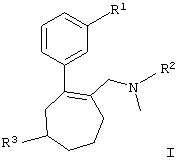
в которой
R1 обозначает ОН, O-C1-С6алкил, O-С3-С7циклоалкил, O-арил, С1-С6алкил-СОО-, арил-СОО-,
R2 обозначает С1-С6алкил, (СН2)(1-2)-арил, С2-С6алкениленарил и
R3 обозначает (СН2)(0-1)-С5-С7циклоалкил, (CH2)(0-2)-арил, гетероциклил, С1-С6алкилгетероциклил,
или к представленным в форме их энантиомеров, диастереомеров, рацематов, оснований или в виде солей физиологических приемлемых кислот, а также к способу их получения и к их применению в качестве лекарственных средств.
Классические опиоиды, такие как морфин, высоко эффективны при лечении сильных и очень сильных болей. Однако возможности их применения ограничены из-за обусловленных ими известных побочных действий, как, например, депрессия дыхания, рвота, необходимость успокоения седативными средствами и запоры, а также по причине развития привыкания. Кроме того, их эффективность снижается при невропатических или инцидентальных болях, от которых в первую очередь страдают онкологические больные.
Опиоиды проявляют свое анальгетическое действие благодаря связыванию с присутствующими на мембране рецепторами, относящимися к семейству так называемых связанных с G-протеином рецепторов. Биохимические и фармакологические характеристики подтипов этих рецепторов позволяют надеяться, что специфические по отношению к этим подтипам опиоиды обладают другим механизмом действия, включая побочные эффекты, по сравнению, например, с морфином. Если морфин связывается избирательно с так называемыми μ-рецепторами, то эндогенные энкефалины характеризуются как δ-селективные пептиды. Дальнейшие фармакологические исследования дают основание предположить, что существует целый ряд подтипов этих опиоидных рецепторов (μ1, μ2, к1, к2, к3, δ1 и δ2).
Сведения о физиологическом значении субстанций, селективных по отношению к δ-рецепторам, были существенно расширены благодаря открытию непептидного антагониста налтриндол. На сегодняшний день очевидно, что δ-агонисты обладают собственным, независимым антиноцицептивным потенциалом. Наряду с данными, полученными при проведении многочисленных экспериментов на животных, имеются также результаты исследований, проводившихся с пептидным агонистом D-аланин2-D-лейцин5-энкефалином (DADL) на онкологических больных, у которых морфин более не проявлял анальгетической эффективности. При интратекальном введении DADL обеспечивал продолжительный анальгетический эффект. Ярко выраженное отличие δ-агонистов от μ-агонистов проявляется в их взаимодействии с "эндогенным антагонистом опиоидов" холецистокинином (ХЦК). Наряду с этим различием в механизме действия δ-агонисты, как полагают, могут отличаться от μ-агонистов также и в той его части, которая касается побочных эффектов, что проявляется, в частности, в снижении депрессии дыхания и запоров.
Вполне допустима возможность применения этих соединений в терапии в качестве анальгетических средств и, в принципе, при всех патологических состояниях, для лечения которых обычно используют агонисты опиатных δ-рецепторов.
С учетом вышеизложенного в основу изобретения была положена задача разработать обладающие анальгетическим действием субстанции, биологическая эффективность которых частично либо преимущественно опосредуется агонистами опиатных δ-рецепторов.
Как было установлено, указанным требованиям отвечают замещенные циклогептеновые соединения общей формулы I. В соответствии с этим объектом настоящего изобретения являются новые замещенные циклогептены общей формулы I
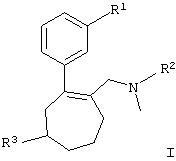
в которой
R1 обозначает ОН, O-C1-С6алкил, O-С3-С7циклоалкил, O-арил, С1-С6алкил-СОО-, арил-СОО-,
R2 обозначает С1-С6алкил, (СН2)(1-2)арил, С2-С6алкениленарил и
R3 обозначает (СН2)(0-1)-С5-С7циклоалкил, (CH2)(0-2)-арил, гетероциклил, С1-С6алкилгетероциклил,
или представленные в форме их энантиомеров, диастереомеров, рацематов, оснований или в виде солей физиологических приемлемых кислот.
Предпочтительными являются соединения общей формулы I, в которых R1 обозначает ОН, O-С1-С6алкил, О-С3-C7циклоалкил, O-арил, С1-С6алкил-СОО-или арил-СОО-, а R2 и R3 имеют значения, указанные для общей формулы I, или
R1 обозначает ОН, О-С1-С6алкил или О-С3-С7циклоалкил, R2 обозначает С1-С6алкил или (СН2)(1-2)-арил, а R3 имеет значения, указанные для общей формулы I, или
R1 обозначает ОН, R2 обозначает С1-С6алкил или (СН2)(1-2)-арил, а R3 имеет значения, указанные для общей формулы I, или
R1 обозначает ОН, R2 обозначает С1-С6алкил, а R3 имеет значения, указанные для общей формулы I.
К предпочтительным относятся далее следующие соединения:
3-[6-(4-хлорфенил) -2-диметиламинометилциклогепт-1-енил]фенол, гидрохлорид,
3 -(2-диметиламинометил-6-фенилциклогепт-1-енил)фенол, гидрохлорид,
3-(2-диметиламинометил-6-нафт-1-илциклогепт-1-енил)фенол, гидрохлорид,
3-(2-диметиламинометил-6-нафт-2-илциклогепт-1-енил)фенол, гидрохлорид,
3-[2-диметиламинометил-6-(4-гидроксифенил)циклогепт-1-енил]фенол, гидрохлорид,
3-(2-диметиламинометил-6-м-толилциклогепт-1-енил)фенол, гидрохлорид,
3-[6-(3-трет-бутилфенил)-2-диметиламинометилциклогепт-1-енил]фенол, гидрохлорид,
6-[4-диметиламинометил-3-(3-гидроксифенил)циклогепт-3-енил]нафт-2-ол, гидрохлорид,
3-[2-диметиламинометил-6-(3-фтор-4-гидроксифенил)циклогепт-1-енил]фенол, гидрохлорид,
3-[2-диметиламинометил-6-(2-гидроксифенил)циклогепт-1-енил]фенол, гидрохлорид,
3-(6-циклогексил-2-диметиламинометилциклогепт-1-енил)фенол, гидрохлорид,
3-(6-циклогексилметил-2-диметиламинометилциклогепт-1-енил)фенол, гидрохлорид,
3 -(6-бензил-2-диметиламинометилциклогепт-1-енил)фенол, гидрохлорид,
3-[2-диметиламинометил-6-(3-гидроксибензил)циклогепт-1-енил)фенол, гидрохлорид,
3-(2-диметиламинометил-6-фенетилциклогепт-1-енил)фенол, гидрохлорид
3-[2-диметиламинометил-6-(3,5-диметил-4-гидроксифенил)циклогепт-1-енил]фенол, гидрохлорид,
3-[2-диметиламинометил-6-(3-гидроксифенил)циклогепт-1-енил]фенол, гидрохлорид,
3-{2-[(метилфенетиламино)метил]-6-фенилциклогепт-1-енил}фенол, гидрохлорид и
[2-(3-метоксифенил)-4-нафт-1-илциклогепт-1-енилметил]диметиламин, гидрохлорид.
Понятие "С1-С6алкил" в контексте настоящего изобретения обозначает прямоцепочечные либо разветвленные углеводороды с 1-6 атомами углерода. В качестве примеров можно назвать метил, этил, пропил, изопропил, н-бутил, втор-бутил, трет-бутил, н-пентил, неопентил и н-гексил.
Понятие "С2-С6алкенилен" в контексте настоящего описания включает прямоцепочечные либо разветвленные углеводородные остатки с 2-6 атомами углерода, которые могут содержать одну или несколько двойных связей. В качестве примеров можно назвать 2-пропенил, 2-бутенил, 1-метил-2-пропенил, 2-метил-2-пропенил, 2-пентенил, 3-пентенил, 4-пентенил, 1-метил-2-бутенил, 2-метил-2-бутенил, 3-метил-2-бутенил, 1-метил-3-бутенил, 2-метил-3-бутенил, 3-метил-3-бутенил, 1,1-диметил-2-пропенил, 1,2-диметил-2-пропенил, 2-гексенил, 3-гексенил, 4-гексенил, 5-гексенил, 1-метил-2-пентенил или 1,3-диметил-3-бутенил.
Понятие "арил" в контексте настоящего описания обозначает незамещенные либо одно- или многократно замещенные ОН, F, Cl, CF3, C1-С6алкилом, С1-С6алкоксигруппой, С1-С7циклоалкоксигруппой, С3-С7циклоалкилом, С2-С6алкениленом, гетероциклилом или фенилом фенилы. Гетероциклильные или фенильные остатки при необходимости могут присоединяться по реакции конденсации. Под указанным понятием при определенных условиях может иметься в виду также нафтил.
Под понятием "гетероциклил" в контексте настоящего изобретения имеются в виду 5- или 6-членные насыщенные либо ненасыщенные, при необходимости с присоединенной путем конденсации арильной системой, гетероциклические соединения, содержащие 1 или 2 гетероатома из группы, включающей азот, кислород и/или серу.
В качестве примеров насыщенных гетероциклилов можно привести 1,4-диоксан, тетрагидрофуран и 1,4-тиоксан.
В качестве примеров из группы ненасыщенных гетероциклилов в контексте настоящего изобретения можно назвать фуран, тиофен, пиридин, пиримидин, тиазол, оксазол, изоксазол, пирадазин, пиразин, хинолин, изохинолин, фталазин и хиназолин.
Под понятием "C1-С6алкилгетероциклил" в контексте настоящего описания имеется в виду, что указанные выше гетероциклилы связаны через C2-С6алкильную группу.
Понятие "С2-С6алкениленарил" в контексте настоящего описания означает, что указанные выше арилы связаны через С2-С6алкениленовую группу.
Под понятием "силанильное соединение" в контексте настоящего изобретения имеются в виду триалкил-либо триарилсилилы, диалкиларилсилилы либо диарилалкилсилилы, которые используются в качестве защитной группы для гидроксильной функции. Примерами таких соединений могут служить триэтил-силил, трипропилсилил, диметилфенилсилил, ди-трет-бутилфенилсилил, триизопропилсилил, диметилизопропилсилил, диэтилизопропилсилил, диметилгексилсилил, трет-бутилдиметилсилил, трет-бутилдифенилсилил, трибензилсилил, три-п-ксилилсилил, трифенилсилил, дифенилметилсилил или пропилдифенилсилил.
Объектом изобретения является также способ получения соединений общей формулы I, который отличается тем, что осуществляют взаимодействие между третичным спиртом общей формулы II
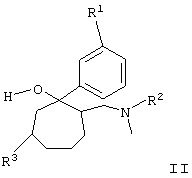
в которой R1-R3 имеют то же значение, что и в формуле I, и полуконцентрированными либо концентрированными органическими либо неорганическими кислотами, такими, например, как соляная кислота, бромистоводородная кислота, муравьиная кислота, или растворами бромистого водорода в уксусной кислоте при температурах в интервале от 20 до 110°С, причем третичные спирты общей формулы II получают благодаря тому, что аминокетоны общей формулы III
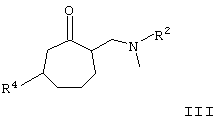
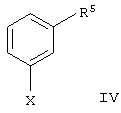
где R2 имеет указанное выше значение, a R4 идентичен R3, за исключением тех случаев, когда необязательно имеющаяся в наличии гидроксильная функция представлена в защищенной форме в виде бензилокси- или силанилоксигруппы, подвергают взаимодействию с металлоорганическим соединением формулы IV
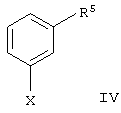
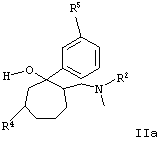
в которой Х представляет собой MgCl, MgBr, MgI или Li, a R5 имеет значение, идентичное R1, за исключением тех случаев, когда необязательно имеющаяся в наличии, как в R4, гидроксильная функция представлена в защищенной форме в виде бензилокси- или силанилоксигруппы, с получением соединения общей формулы IIа
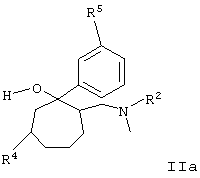
которое затем переводят в соединение общей формулы II.
Соединения общей формулы III получают из циклогептанонов общей формулы V
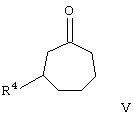
в которой R4 имеет значения, указанные выше, взаимодействием с аминами общей формулы HN(CH3)R2 (необязательно в виде их солей) и параформальдегидом, соответственно водным раствором формальдегида в растворителях, таких как вода, спирты или уксусная кислота, при температурах в интервале от 20°С до температуры кипения растворителя. Предпочтительно, однако, получать соединения общей формулы III взаимодействием циклогептанонов V с галогенидами метилениммония общей формулы H2C=N(CH3)R2X, где R2 имеет значения, указанные выше, а Х обозначает атом хлора либо иода, в растворителях, таких как ацетонитрил или тетрагидрофуран, при температурах в интервале от 20 до 50°С.
Взаимодействие соединений формул III и IV проводят в простом алифатическом эфире, например в диэтиловом эфире и/или тетрагидрофуране, при температурах в интервале от -70 до +60°С. Соединения формулы IV, в которых Х представляет собой атом лития, получают при этом из соединений формулы IV, в которых Х обозначает Вr или I, за счет обмена галоген-литий, осуществляемого с помощью, например, раствора н-бутиллития/н-гексана.
Для получения из соединения формулы IIа соединения формулы II имеется в зависимости от значений R5, соответственно от защитной группы в R4 целый ряд методов.
Так, если R5 представляет собой бензилоксигруппу и/или если такая группа содержится в R4, то целесообразно применять метод восстановительного дебензилирования с использованием каталитически активированного водорода, причем в качестве катализатора служит платина либо палладий, абсорбированные на носителе, таком как активированный уголь. Реакцию проводят в растворителе, таком как уксусная кислота, или в С1-С4алкиловом спирте при давлении в диапазоне от 1 до 100 бар и при температурах в интервале от 20 до 100°С, причем соединение IIа применяют предпочтительно в виде одной из его солей.
Если R5 представляет собой силанилоксигруппу и/или если такая группа содержится в R4, то отщепление защитной группы осуществляют благодаря тому, что соответствующее соединение формулы IIа при температуре 20°С подвергают в инертном растворителе, таком как тетрагидрофуран, диоксан либо диэтиловый эфир, взаимодействию с фторидом тетра-н-бутиламмония или же обрабатывают метанольным раствором хлористого водорода.
Если же R5 в соединении формулы IIа представляет собой метоксильный радикал и/или если таковой содержится в R4, то взаимодействием с гидридом диизобутилалюминия, осуществляемом в ароматическеом углеводороде, таком как толуол, при температуре в интервале от 60 до 130°С, можно получить соединение формулы II, в котором R1 представляет собой гидроксильную группу и/или такую группу содержит R3. В этом случае существует также возможность непосредственного получения аналогичного соединения формулы I, состоящая в том, что соединение IIа нагревают либо с раствором бромистого водорода в ледяной уксусной кислоте, либо с концентрированной бромистоводородной кислотой. Такая возможность может быть реализована и взаимодействием соединения IIа с метансульфокислотой/метионином при температурах в интервале от 20 до 50°С.
В соединениях формулы I, в которых R1 представляет собой метоксильную группу и/или если такая группа содержится в R3, то эту группу можно также описанным выше путем, т.е. взаимодействием с гидридом диизобутилалюминия преобразовать в гидроксильную функцию.
Соединения общей формулы I, в которых R1 представляет собой гидроксильную функцию, можно переводить по известной технологии в сложноэфирную функцию.
Соединения формулы I с помощью физиологически приемлемых кислот, таких как соляная кислота, бромистоводородная кислота, серная кислота, метансульфоновая кислота, муравьиная кислота, уксусная кислота, щавелевая кислота, янтарная кислота, винная кислота, миндальная кислота, фумаровая кислота, молочная кислота, лимонная кислота, глутаминовая кислота и/или аспарагиновая кислота, могут переводиться по известной методике в их соли. Предпочтительно процесс солеобразования проводить в растворителе, таком как диэтиловый эфир, диизопропиловый эфир, алкиловый эфир уксусной кислоты, ацетон и/или 2-бутанон. Для получения гидрохлоридов особенно предпочтительным является триметилхлорсилан в водосодержащем растворе.
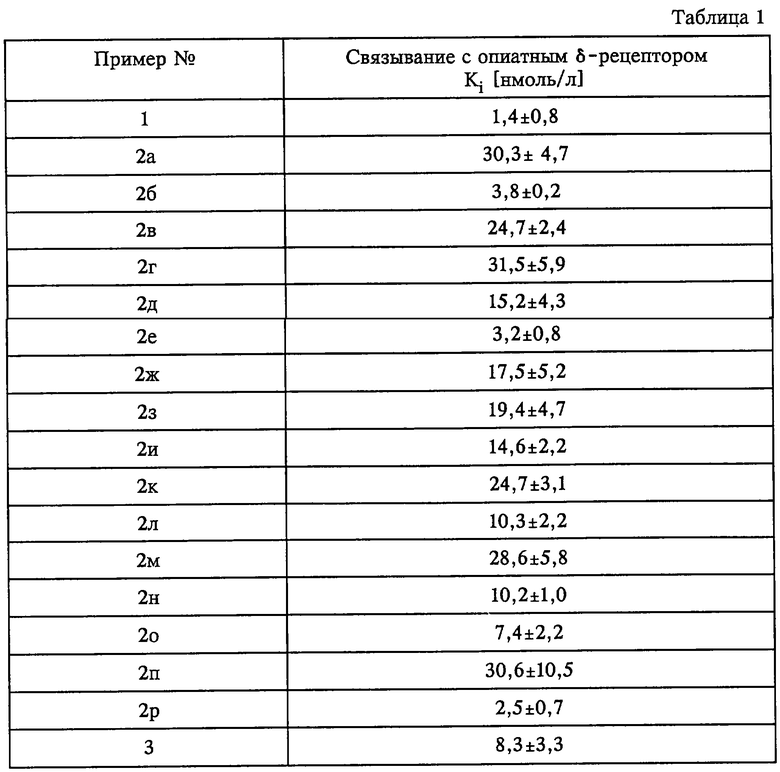
Исследования по связыванию с опиатным δ-рецептором
Исследования по определению сродства предлагаемых согласно изобретению соединений формулы I к опиатному δ-рецептору, которое является решающим условием для наличия анальгетических свойств, проводили на гомогенатах мембран головного мозга (гомогенат головного мозга мужских особей крыс линии Wistar без мозжечка, моста и продолговатого мозга).
С этой целью свежепрепарированный для каждого эксперимента мозг крыс при охлаждении льдом гомогенизировали в 50 ммолях/л трис-НСl [трис(гидроксиметил)аминометангидрохлорид] (рН 7,4) и в течение 10 минут центрифугировали при 5000g и 4°С. После декантирования и отбрасывания надосадочной жидкости, повторного растворения и гомогенизации мембранного осадка в 50 ммолях/л трис-НСl (рН 7,4) гомогенат в течение 20 минут центрифугировали при 20000 g и 4°С. Эту операцию по промывке повторяли еще раз. Затем надосадочную жидкость декантировали, а мембранный осадок гомогенизировали в холодном 50 ммолей/л трис-HCl, 20% глицерина (мас./об.), 0,01% бацитрацина (мас./об.) (рН 7,4) и в аликвотных количествах замораживали до начала тестирования. Для проведения исследований по связыванию с рецептором аликвоты оттаивали и разбавляли соответствующим буфером в соотношении 1:10.
В качестве буфера в исследованиях на связывание применяли 50 ммолей/л трис-HCl, 5 ммолей/л MgCl2 (рН 7,4), дополненные 0,1% (мас./об.) бычьего сывороточного альбумина, а в качестве радиоактивного лиганда использовали 1 нмоль/л (3Н)-2-D-Аlа-дельторфина II. Долю неспецифического связывания определяли в присутствии 10 ммолей/л налоксона.
В других смесях соединения по изобретению добавляли в последовательно варьируемых концентрациях и определяли вытеснение радиоактивного лиганда из его специфически связанного состояния. Соответствующие смеси, которые применяли в трех параллельных опытах, инкубировали в течение 90 минут при 37°С, после чего для выявления связанного с гомогенатом мембран радиоактивного лиганда последний собирали путем фильтрации через фильтр из стекловолокна (GF/B). Радиоактивность дисков этого стекловолоконного фильтра измеряли после добавления сцинциллятора с помощью счетчика β-излучения.
Сродство соединений по изобретению к опиатному δ-рецептору рассчитывали в виде показателя IC50 согласно закону действующих масс методом нелинейной регрессии. Ki-значения в таблице 1 указаны в качестве средних значений ± стандартные отклонения по 3 проведенным независимо друг от друга опытам.
 Испытание на антиноцицептивную активность на мышах в тесте на судорожную готовность
Испытание на антиноцицептивную активность на мышах в тесте на судорожную готовность
Антиноцицептивную эффективность исследовали на мышах в тесте на судорожную готовность, индуцированную фенилхиноном (модифицированный метод I.C. Hendershot, J. Forsaith, Journ. Pharmacol. Exp. Ther. 125, стр. 237-240 (1959)). В этих целях использовали мужских особей мышей линии NMRI весом 25-30 г. Группам по 10 животных в каждой, предназначенным для испытания одной дозы субстанции, по истечении 10 мин после внутривенной инъекции соединения по изобретению в дозе 0,3 мл/мышь внутрибрюшинно вводили 0,02%-ный водный раствор фенилхинона (фенилбензохинон, фирма Sigma, Дейзенхофен; приготовление раствора с добавлением 5% этанола и выдержкой в водяной бане при 45°С). Подопытных животных помещали поодиночке в специальные клетки для наблюдения за ними. С помощью кнопочного счетчика в течение 5-20 мин после введения фенилхинона подсчитывали число индуцированных болью разгибательных движений (так называемые реакции судорожной готовности, заключающиеся в прогибании тела с вытягиванием задних конечностей). Исходя из зависимого от дозировки уменьшения числа реакций судорожной готовности в сравнении с таковыми у тестируемых одновременно контрольных групп, которым не вводили соединение по изобретению, методом регрессионного анализа (программа обработки фирмы Martens EDV Service, Эккенталь) рассчитывали значения ED50 реакции судорожной готовности. Результаты представлены в таблице 2.
Примеры
Ниже изобретение более подробно поясняется на следующих примерах, которые никоим образом не ограничивают его объем.
В качестве неподвижной фазы в хроматографии на колонках использовали силикагель 60 (0,040-0,063 мм) фирмы Е.Меrск, Дармштадт.
Хроматографические исследования проводили с помощью готовых пластин для тонкослойной хроматографии высокого разрешения (ТСХВР), силикагель 60 F 254 фирмы E.Merck, Дармштадт.
Соотношения в смесях элюентов для всех хроматографических исследований указаны в отношении объем/объем.
Понятие TRIS-HCl обозначает трис(гидроксиметил)аминометангидрохлорид.
Сокращение (мас./об.) обозначает масса/объем.
Пример 1
3-[2-диметиламинометил-6-(3-гидроксифенил)циклогепт-1-енил] фенол, гидрохлорид
Стадия 1
(3 -метоксифенил)циклогептанон
К свежеприготовленному раствору Гриньяра из 5,83 г магниевой стружки и 28,7 мл 1-бром-3-метоксибензола в 675 мл безводного диэтилового эфира при 20°С при перемешивании добавляли сначала 20,95 г иодида меди(I), а затем по каплям - раствор из 15,2 г циклогепт-2-енона (80%-ного) в 175 мл безводного диэтилового эфира. После добавления в течение 45 мин нагревали с обратным холодильником. После этого разлагали, добавляя по каплям 85 мл насыщенного раствора хлорида аммония. После разбавления 200 мл воды органическую фазу отделяли, а водную фазу еще дважды экстрагировали порциями по 100 мл диэтилового эфира. Объединенные органические фазы промывали по одному разу насыщенными растворами гидрокарбоната натрия, соответственно хлорида натрия, сушили над сульфатом натрия и упаривали под вакуумом. Остаток очищали посредством колоночной хроматографии, используя в качестве элюентов диэтиловый эфир/н-гексан сначала в соотношении 1:4, а затем 1:1. Таким путем получили 16,5 г (68,6% от теории) указанного в заголовке соединения в виде масла, слегка окрашенного в желтый цвет.
Стадия 2
2-диметиламинометил-6-(3-метоксифенил)циклогептанон, гидрохлорид
Раствор из 16,4 г продукта из стадии 1 в 150 мл ацетонитрила смешивали с 7,2 г хлорида N,N-диметилметилениммония и тремя каплями ацетилхлорида и смесь перемешивали в течение 48 ч при 20°С. Затем разбавляли 100 мл диэтилового эфира, кристаллический продукт выделяли, промывали диэтиловым эфиром и сушили под вакуумом при 40°С. В результате получили 21,9 г (93,6% от теории) указанного в заголовке соединения в виде белых кристаллов, tпл 130-134,5°С.
Стадия 3
2-диметиламинометил-1,6-бис(3-метоксифенил)циклогептанол
К свежеприготовленному раствору Гриньяра из 4,42 мл 1-бром-3-метоксибензола и 0,90 г магниевой стружки в 35 мл безводного тетрагидрофурана при 20°С при перемешивании добавляли по каплям раствор из 9,1 г свободного основания продукта из стадии 2 в 52 мл безводного тетрагидрофурана, после чего нагревали с обратным холодильником. По завершении обменной реакции проводили переработку аналогично описанной на стадии 1. После хроматографической очистки на колонке, используя в качестве элюентов этиловый эфир уксусной кислоты/метанол (5:1), получили 10,44 г (82,4% от теории) указанного в заголовке соединения в виде практически бесцветного масла.
Стадия 4
3-[2-диметиламинометил-6-(3-гидроксифенил)циклогепт-1-енил]фенол, гидрохлорид
10,35 г продукта из стадии 3 при перемешивании нагревали в течение 5 ч со 120 мл раствора бромистого водорода в ледяной уксусной кислоте (33% НВr) до 100-110°С, после чего упаривали под вакуумом, остаток растворяли в 150 мл воды и подщелачивали разбавленным едким натром (приблизительно 5%-ным) (рН 9-10). Затем трижды экстрагировали порциями по 100 мл этилового эфира уксусной кислоты, объединенные экстракты промывали один раз насыщенным раствором хлорида натрия, сушили над сульфатом натрия и упаривали под вакуумом. Остаток очищали посредством колоночной хроматографии, используя в качестве элюента этиловый эфир уксусной кислоты. Таким путем получили 3,71 г (40,7% от теории) свободного основания указанного в заголовке соединения, которое с помощью триметилхлорсилана/воды в 2-бутаноне переводили в гидрохлорид, tпл: разложение выше 110°С.
Пример 2
Используя соответствующие исходные соединения, по технологии аналогично описанной в примере 1, стадии 1-4, варьируя при необходимости условия реакции (растворители, температуру), удалось получить следующие соединения:
2а: 3-[6-(4-хлорфенил)-2-диметиламинометилциклогепт-1-енил]фенол, гидрохлорид, tпл: разложение выше 134°С,
2б: 3-(2-диметиламинометил-6-фенилциклогепт-1-енил)фенол, гидрохлорид, tпл: 162-166°С,
2в: 3-(2-диметиламинометил-6-нафт-1-илциклогепт-1-енил)фенол, гидрохлорид,
2г: 3-(2-диметиламинометил-6-нафт-2-илциклогепт-1-енил)фенол, гидрохлорид, tпл: 183°С,
2д: 3-[2-диметиламинометил-6-(4-гидроксифенил)циклогепт-1-енил] фенол, гидрохлорид, tпл: 240-242°С,
2е: 3-(2-диметиламинометил-6-м-толилциклогепт-1-енил)фенол, гидрохлорид, tпл: 231-233°С,
2ж: 3-[6-(3-трет-бутилфенил)-2-диметиламинометилциклогепт-1-енил] фенол, гидрохлорид, tпл: 215-218°С,
2з: 6-[4-диметиламинометил-3-(3-гидроксифенил)-циклогепт-3-енил]нафт-2-ол, гидрохлорид, tпл: разложение вьппе 190°С,
2и: 3-[2-диметиламинометил-6-(3-фтор-4-гидроксифенил)циклогепт-1-енил] фенол, гидрохлорид, tпл: 227-230°С,
2к: 3-[2-диметиламинометил-6-(2-гидроксифенил)циклогепт-1-енил] фенол, гидрохлорид, tпл: разложение выше 125°С,
2л: 3-(6-циклогексил-2-диметиламинометилциклогепт-1-енил)фенол, гидрохлорид, tпл: 224-225,5°С,
2м: 3-(6-циклогексилметил-2-диметиламинометилциклогепт-1-енил)фенол, гидрохлорид, tпл: 203-206°С,
2н: 3-(6-бензил-2-диметиламинометилциклогепт-1-енил)фенол, гидрохлорид, tпл: 208-212°С,
2о: 3-[2-диметиламинометил-6-(3-гидроксибензил)циклогепт-1-енил)фенол, гидрохлорид, tпл: 88°С,
2п: 3-(2-диметиламинометил-6-фенетилциклогепт-1-енил)фенол, гидрохлорид, tпл: 188-190°С,
2р: 3-[2-диметиламинометил-6-(3,5-диметил-4-гидроксифенил)циклогепт-1-енил]фенол, гидрохлорид, tпл: разложение выше 156°С.
Пример 3
3-{2-[(метилфенетиламино)метил]-6-фенилциклогепт-1-енил} фенол, гидрохлорид
Стадия 1
2-[(метилфенетиламино) метил] -6-фенилциклогептанон, гидрохлорид
Смесь из 2,77 г 3-фенилциклогептанона, 2,52 г метилфенетиламина, гидрохлорида, и 1,23 мл водного раствора формальдегида (36%-ного) при интенсивном перемешивании и подаче азота нагревали в течение 2 ч на водной бане. Затем упаривали под вакуумом, остаток трижды экстрагировали диэтиловым эфиром/н-гексаном (1:1) и сушили под вакуумом. В результате получили 5,4 г сырого соединения, указанного в заголовке.
Стадия 2
1-(3-метоксифенил)-2-[(метилфенетиламино)метил]-6-фенилциклогептанол
4,7 г свободного основания продукта из стадии 1, 2,76 г 1-бром-3-метоксибензола и 0,4 г магниевой стружки подвергали взаимодействию друг с другом аналогично тому, как это описано в примере 1, стадия 3. После аналогичной переработки и хроматографической очистки на колонке с использованием в качестве элюентов этилового эфира уксусной кислоты/н-гексана (1:1) получили 3,1 г (49,9% от теории) указанного в заголовке соединения в виде желтого масла.
Стадия 3
3-{2-[(метилфенетиламино) метил]-6-фенилциклогепт-1-енил} фенол, гидрохлорид
2,67 г продукта из стадии 2 аналогично тому, как это описано в примере 1, стадия 4, подвергали взаимодействию с 27 мл раствора бромистого водорода в ледяной уксусной кислоте (33% НВr). После аналогичной переработки получили 1,24 г (50,2% от теории) свободного основания указанного в заголовке соединения, которое с помощью триметилхлорсилана в 2-бутаноне переводили в гидрохлорид, tпл: разложение выше 105°С.
Пример 4
[2-(3-метоксифенил) -4-нафт-1-илциклогепт-1-енилметил]диметиламин. гидрохлорид
4,04 г 2-диметиламинометил-1-(3-метоксифенил)-6-нафт-1-илциклогептанола (продукт из примера 2в, стадия 3) перемешивали в течение 24 ч при 50°С с 50 мл 6н. соляной кислоты. Затем подщелачивали едким натром и трижды экстрагировали порциями по 50 мл этилового эфира уксусной кислоты соответственно. Экстракты промывали насыщенным раствором хлорида натрия, сушили над сульфатом натрия и упаривали под вакуумом. Остаток очищали посредством хроматографии на колонке с использованием в качестве элюентов этилового эфира/метанола (4:1), получая в результате 2,94 г (76,3% от теории) свободного основания указанного в заголовке соединения, которое с помощью триметилхлорсилана/воды в 2-бутаноне переводили в гидрохлорид.
Ki полученного соединения имеет значение 36,50 нмоль/л. В опытах in vivo (мыши, тест на судорожную активность, табл.2) показывает ED50=4,00 мг/кг.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ ГЕТЕРОЦИКЛИЧЕСКИХ БЕНЗОЦИКЛОАЛКЕНОВ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1998 |
|
RU2197484C2 |
| ПРОИЗВОДНЫЕ АКРИДИНА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1999 |
|
RU2225399C2 |
| ЗАМЕЩЕННЫЕ АМИНОСОЕДИНЕНИЯ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1998 |
|
RU2197474C2 |
| 6-ДИМЕТИЛАМИНОМЕТИЛ-1-ФЕНИЛЦИКЛОГЕКСАНОВЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ФАРМАЦЕВТИЧЕСКИ ДЕЙСТВУЮЩИХ ВЕЩЕСТВ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ) | 1996 |
|
RU2178409C2 |
| ДИМЕТИЛ(3-АРИЛБУТ-3-ЕНИЛ)АМИНОСОЕДИНЕНИЯ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 1997 |
|
RU2167146C2 |
| АРИЛПИРИМИДИНОВЫЕ ПРОИЗВОДНЫЕ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1997 |
|
RU2189976C2 |
| СУЛЬФИРОВАННЫЕ АМИНОКИСЛОТНЫЕ ПРОИЗВОДНЫЕ И СОДЕРЖАЩИЕ ИХ ИНГИБИТОРЫ МЕТАЛЛОПРОТЕИНАЗ | 1997 |
|
RU2198656C2 |
| 1-ФЕНИЛ-2-ДИМЕТИЛАМИНОМЕТИЛЦИКЛОГЕКСАН-1-ОЛОВЫЕ СОЕДИНЕНИЯ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ИХ ОСНОВЕ | 1996 |
|
RU2167148C2 |
| НОВЫЕ ПРОИЗВОДНЫЕ ПРОСТОГО ПРОПАРГИЛОВОГО ЭФИРА | 2000 |
|
RU2237058C2 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ОКСАЗОЛА С АНАЛГЕТИЧЕСКИМ ДЕЙСТВИЕМ | 2006 |
|
RU2424236C2 |
Изобретение относится к обладающим анальгетическим действием новым замещенным циклогептенам общей формулы I
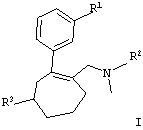
в которой R1 обозначает ОН, O-C1-С6алкил, R2 обозначает C1-С6алкил, (СН2)(1-2)-арил, и R3 обозначает (СН2)(0-1)-С5-С7циклоалкил, (CH2)(0-2)-арил, причем остаток арила может быть однократно или многократно замещен ОН, F, Cl, CF3, C1-С6алкилом, в виде их рацемата или энантиомеров, как в виде оснований, так и в виде солей физиологических приемлемых кислот. Способ получения соединения формулы I заключается в том, что третичный спирт общей формулы II
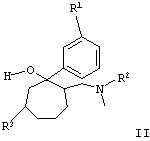
в которой R1-R3 имеют те же значения, что и в формуле I, взаимодействует с кислотой в интервале температуры от 20 до 110°С. Ипользуемый при этом третичный спирт общей формулы II получают взаимодействием аминокетона общей формулы III
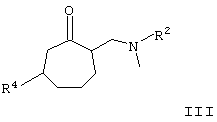
в которой R2 имеет значения, что и в формуле I, R4 идентичен R3 и в случае, если R4 имеет гидроксильную группу, за исключением тех случаев, когда имеющаяся в наличии гидроксильная группа представлена в защищенной форме в виде бензилокси- или силанилоксигруппы, с металлоорганическим соединением формулы IV, где Х обозначает MgCl, MgBr, MgI или Li, R5 имеет значения, идентичные R1, за исключением тех случаев, когда имеющаяся в наличии гидроксильная группа представлена в защищенной форме в виде бензилокси- или силанилоксигруппы, и полученное промежуточное соединение формулы IIа
где R4 и R5 имеют вышеуказанные значения, переводят в соединение формулы II. 2 с. и 3 з.п. ф-лы, 2 табл.
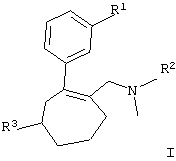
в которой R1 обозначает ОН, O-C1-С6алкил;
R2 обозначает C1-С6алкил, (СН2)(1-2)-арил;
R3 обозначает (СН2)(0-1)-С5-С7циклоалкил, (CH2)(0-2)-арил, причем остаток арила может быть однократно или многократно замещен ОН, F, Сl, СF3, C1-С6алкилом,
в виде их рацемата или энантиомеров, как в виде оснований или так и в виде солей физиологических приемлемых кислот.
3-[6-(4-хлорфенил)-2-диметиламинометилциклогепт-1-енил]фенол, гидрохлорид,
3-(2-диметиламинометил-6-фенилциклогепт-1-енил)фенол, гидрохлорид,
3-(2-диметиламинометил-6-нафт-1-илциклогепт-1-енил)фенол, гидрохлорид,
3-(2-диметиламинометил-6-нафт-2-илциклогепт-1-енил)фенол, гидрохлорид,
3-[2-диметиламинометил-6-(4-гидроксифенил)циклогепт-1-енил]фенол, гидрохлорид,
3-(2-диметиламинометил-6-м-толилциклогепт-1-енил)фенол, гидрохлорид,
3-[6-(3-трет-бутилфенил)-2-диметиламинометилциклогепт-1-енил]фенол, гидрохлорид,
6-[4-диметиламинометил-3-(3-гидроксифенил)циклогепт-3-енил]нафт-2-ол, гидрохлорид,
3-[2-диметиламинометил-6-(3-фтор-4-гидроксифенил)циклогепт-1-енил]фенол, гидрохлорид,
3-[2-диметиламинометил-6-(2-гидроксифенил)циклогепт-1-енил]фенол, гидрохлорид,
3-(6-циклогексил-2-диметиламинометилциклогепт-1-енил)фенол, гидрохлорид,
3-(6-циклогексилметил-2-диметиламинометилциклогепт-1-енил)фенол, гидрохлорид,
3-(6-бензил-2-диметиламинометилциклогепт-1-енил)фенол, гидрохлорид,
3-[2-диметиламинометил-6-(3-гидроксибензил)циклогепт-1-енил]фенол, гидрохлорид,
3-(2-диметиламинометил-6-фенетилциклогепт-1-енил)фенол, гидрохлорид,
3-[2-диметиламинометил-6-(3,5-диметил-4-гидроксифенил)циклогепт-1-енил]фенол, гидрохлорид,
3-[2-диметиламинометил-6-(3-гидроксифенил)циклогепт-1-енил]фенол, гидрохлорид,
3-{2-[(метилфенетиламино)метил]-6-фенилциклогепт-1-енил}фенол, гидрохлорид и
[2-(3-метоксифенил)-4-нафт-1-илциклогепт-1-енилметил]диметиламин, гидрохлорид.
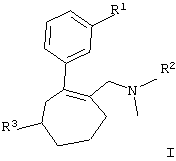
в которой R1-R3 имеют значения, указанные в п.1,
отличающийся тем, что третичный спирт общей формулы II
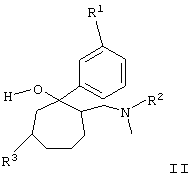
в которой R1-R3 имеют те же значения, что и в формуле I,
взаимодействует с кислотой в интервале температуры от 20 до 110°С, при этом используемый третичный спирт общей формулы II получают взаимодействием аминокетона общей формулы III
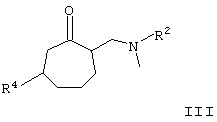
в которой R2 имеет значения, что и в формуле I;
R4 идентичен R3 и, в случае если R4 имеет гидроксильную группу, за исключением тех случаев, когда имеющаяся в наличии гидроксильная группа представлена в защищенной форме в виде бензилокси- или силанилоксигруппы,
с металлоорганическим соединением формулы IV
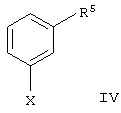
где Х обозначает MgCl, MgBr, Mgl или Li;
R5 имеет значения, идентичные R1 за исключением тех случаев, когда имеющаяся в наличии гидроксильная группа представлена в защищенной форме в виде бензилокси- или силанилоксигруппы,
и полученное промежуточное соединение формулы IIа
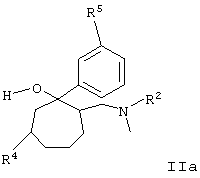
где R4 и R5 имеет вышеуказанные значения,
переводят в соединение формулы II.
| Способ получения бета-циклогексен-1-илэтиламина из циклогексен- 1 -илацетонитрила | 1959 |
|
SU130517A1 |
| US 3470249 A, 30.09.1969 | |||
| US 3830934 A, 20.08.1974 | |||
| GB 2005266 A, 19.04.1979. | |||
Авторы
Даты
2004-07-27—Публикация
1999-12-14—Подача