Изобретете относится к области органической химии и может найти применение в биохимии и в медицине.
Современные методы исследования физиологически активных соединении требует их наличия в виде высокомеченных производных. Одним из таких соединений является высокомеченный тритием N-[3-(3-цианопиразоло[1,5-а]пиримидин-7-ил)фенил]-N-этилацетамид общей формулы I: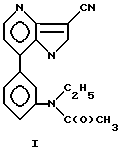
(Jhе Merck Jndex an encyclopedia af chemicals, drugs, and biologicals, Eleventth Editon, 12th, 1989-1996, Susan Budavari, Editor Maryadele JO'. Neil, Associate Editor Ann Smith, Assistant Editor Patricia E. Heckelman, Editorial Assistant; Published by Merck and CO., Jnc. Rahway N.J. U.S.A.)
Данное соединение, известное также под названием залеплон, обладает седативной активностью, является агонистом бензодиазепиновых рецепторов (патент (XI 4626538, 1986). Однако его высокомеченное тритием производное не описано.
Задачей, решаемой настоящим изобретением явилось расширение ассортимента высокомеченных тритием органических соединений.
Задача решается тем, что впервые получен высокомеченный тритием N-[3-(3-анопиразоло [1,5-а]пиримидин-7-ил) фенил]-N-этилацетамид.
Ниже приведены примеры, иллюстрирующие изобретение.
Пример 1. В реакционную ампулу помещали 10 мг N-[3-(3-циaнoпиpaзoлo[1,5-a] пиpимидин-7-ил)фeнил] -N-этилaцeтaмидa, 30 мг 5% PdO/Al2O3, 20 мг РdO, соотношение окись палладия-гетерогенный катализатор-N-[3-(3-цианопиразоло [1,5-а] пиримидин-7-ил) фенил]-N-этилацетамид (2:3:1). Напускали газообразный тритий до давления 400 гПа, и при охлаждении жидким азотом средней части ампулы смесь нагревали при 80oС в течение 10 мин. При этом образующаяся при восстановлении окиси палладия стопроентная тритиевая вода конденсировалась в средней части ампулы. Затем реакцию вели следующим образом. Снимали охлаждение со средней части ампулы и охлаждали жидким азотом нижнею часть ампулы. При этом тритиевая вода перегонялась в смесь катализатора и вещества, затем, продолжая охлаждение, реакционную смесь вакуумировали для удаления избыточного трития, ампулу снимали с установки, в реакционную ампулу впрыскивали 100 мкл смеси диоксана с триэтиламином (9:1), ампулу запаивали и реакцию вели при 180oС 40 мин. Затем содержимое ампулы замораживали жидким азотом, ампулу вскрывали, катализатор отфильтровывали и промывали метанолом (5х0,5 мл). Тритиевую воду удаляли многократным увариванием вещества с метанолом (5х3 мл). Полученный N-[3-(3-цианопиразоло[1,5-а]пиримидин-7-ил)фенил]-N-этилацетамид первоначально очищали методом ТСХ, система (Б). Зону, содержащую целевой продукт, вырезали, экстрагировали метанолом (3х10 мл), фильтровали и упаривали. Остаток хроматографировали в системе (Д). Радиохимическая чистота меченого препарата выше 97%. Выход - 30-35%, молярная радиоактивность -18,5 Ки/ммоль.
Меченый препарат очищали хроматографическими методами: TCХ: Силикагельные пластинки Silufol (Чехия), система (А): хлористый метилен-метанол (95: 5) Rf : 0,79; система (Б): этилацетат-гексан-уксусная кислота (75:25:1) Rf : 0,63. ВЭХХ: LiChrosphere. С18, 5 мкм (2 мм х 60 мм), многоволновая детекция, V- 0,1 мл, система (В): ацетонитрил-25 мМ дигидрофосфат аммония (рН 3) (1:1), время удерживания - 2,57 мин; система (Г): ацетонитрил-25 мМ дигидрофосфат аммония (рН 3) (2:3), время удерживания - 4,17 мин. Silasorb C18, 13 мкм (10 мм x 250 мм), детекция -UY-220, V - 2,0 мл/мин, система (Д): ацетонитрил-25 мМ дигидрофосфат аммония (рН 3) (45:65), время удерживания - 13,68 мин.
Пример 2. В реакционную ампулу помещали N-[3-(3-цианопиразоло [1,5-а] пиримидин-7-ил) фенил)-N-этилацетамид, 5% PdО/Al2O3, PdO соотношение окись палладия-гетерогенный катализатор-N-[3-(3-цианопиразоло[1,5-а]пиримидин-7-ил)фенил]-N-этилацетамид (2:10:1). Напускали газообразный тритий до давления 450 ГПа, и при охлаждении жидким азотом средней части ампулы смесь нагревали при 70oС в течение 15 мин. При этом образующаяся при восстановлении окиси палладия стопроцентная тритиевая вода конденсировалась в средней части ампулы. Затем реакцию вели следующим образом. Снимали охлаждение со средней части ампулы и охлаждали жидким азотом нижнюю часть ампулы. При этом тритиевая вода перегонялась к смеси катализатора и вещества. Затем, продолжая охлаждение, реакционную смесь вакуумировали для удаления избыточного трития, ампулу снимали с установки, в реакционную ампулу впрыскивали 100 мкл смеси диоксана с триэтиламином (9:1), ампулу запаивали и реакцию вели при 180oС 40 мин. Затем содержимое ампулы замораживали жидким азотом, ампулу вскрывали, катализатор отфильтровывали и промывали метанолом (5х0,5 мл).Тритиевую воду удаляли многократным упаривахнем вещества с метанолом (5х3 мл). Меченый препарат первоначально очищали методом ТСХ, система (Б). Зону, содержащую целевой продукт, вырезали, экстрагировали метанолом (3х10 мл), фильтровали и упаривали. Остаток хроматографировали в системе (Д). Радиохимическая чистота полученного меченого N-[3-(3-цианопиразоло [1,5-a]пиримидин-7-ил)-фенил]-N-этилацетамида выше 97%. Выход - 33-38%, молярная радиоактивность - 15,3 Ки/ммоль.
Пример 3. В реакционную ампулу помещали 5 мг N-(3-(3-цианопиразоло[1,5-a] пиримидин-7-ил)фенил] -N-этилацетамида, 15 мг 5% РdO/Al2O3, 10 мг PdО, соотношение окись палладия-гетерогенный катализатор- N-[3-(3-цианопиразоло[1,5-а] пиримидин-7-ил)-фенил] -N-этилацетамид (2: 3:1). Напускали газообразный тритий до давления 450 ГПa и при охлаждении жидким азотом средней части ампулы смесь нагревали при 80oС в течение 10 мин. При этом образующаяся при восстановлении окиси палладия стопроцентная тритиевая вода конденсировалась в средней части ампулы. Затем реакцию вели следующим образом. Снимали охлаждение со средней части ампулы и охлаждали жидким азотом нижнюю часть ампулы. При этом тритиевая вода перегонялась в смесь катализатора и вещества, затем, продолжая охлаждение, реакционную смесь вакуумировали для удаления избыточного трития, ампулу снимали с установки, в реакционную ампулу впрыскивали 100 мкл смеси диоксана с триэтиламном (9:1), ампулу запаивали я реакцию вели при 150oС 120 мин. Затем содержимое ампулы замораживали жидким азотом, ампулу вскрывали, катализатор отфильтровывали и промывали метанолом (5х0,5 мл). Тритиевую воду удаляли многократным увариванием вещества с метанолом (5х3 мл). Меченый N-[3-(3-цианопиразоло [1,5-а] пиримидин-7-ил)-фенил] -N-этилацетамид первоначально очищали методом ТСХ, система (Б). Зону, содержащую целевой продукт, вырезали, экстрагировали метанолом (3х10 мл), фильтровали, упаривали. Остаток хроматографировали в системе (Д). Радиохимическая чистота меченого N-[3-(3-цианопиразоло [1,5-а]пиримидин-7-ил)-фенил] -N-этилацетамида выше 97%. Выход - 40-45%, молярная радиоактивность - 8,1 Ки/ммоль.
Таким образом, впервые получен высокомеченный тритием N-[3-(3-цианопиразоло[1,5-а] пиримидин-7-ил)-фенил]-N-этилацетамид.
Изобретение относится к новому высокомеченному третием N-[3-(3-цианопиразоло [1,5-а] примидин-7ил-)фенил] -N-этилацетамиду формулы I, которое обладает седативным действием и является агонистом бенздиазепиновых рецептов. Указанное соединение может быть использовано при исследованиях в медицине. 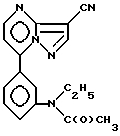
Высокомеченный тритием N-[3-(3-цианопиразоло[1,5-a] пиримидин-7-ил)фенил] -N-этилацетамид формулы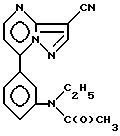
| US 4626538 A, 02.12.1986 | |||
| US 4236005 A, 25.11.1980 | |||
| US 4576943 A, 18.03.1986 | |||
| US 4281000 A, 27.08.1981 | |||
| ПИРАЗОЛОПИРИМИДИНИЛ- И ПИРИМИДИНИЛАЛКИЛИДЕНБИСФОСФОНОВЫЕ КИСЛОТЫ, ИХ ЭФИРЫ ИЛИ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ | 1992 |
|
RU2079506C1 |
Авторы
Даты
2002-06-20—Публикация
2000-11-15—Подача