Изобретение относится к молочной, биотехнологической, медицинской и фармацевтической промышленности, а именно к способам получения биологически активных веществ, которые могут использоваться в качестве биологически активных добавок (БАД).
При производстве детских молочных продуктов известны способы получения БАД на основе лизоцима, а также лизоцима и молочнокислых бактерий ацидофильной палочки. Этими способами получают БАД, предназначенные для использования в детском, диетическом и лечебно-профилактическом питании. При получении БАД используют препарат куриного лизоцима и бактериальный концентрат ацидофильной палочки. Данный способ включает использование только одного фермента - лизоцима, обладающего бактерицидным действием, при этом не из молочного источника. Поэтому данный способ является менее совершенным и экономически менее эффективным [Детские молочные продукты, обогащенные лизоцимом: Обзорная инф. / Щербакова Э.Г., Растунова Г.А., Журавлева Т.П., Шаманова Г.П., Недайвозова Н.Н. - М.: АгроНИИТЭИММП, 1986, - 40 с.].
Известны способы переработки молока и получения белкового полисахаридного концентрата, которые заключаются в том, что с целью повышения биологической ценности и создания безотходной технологии обезжиренное молоко в количестве 5-100% с кислотностью 15-23oТ обрабатывают при 2-40oС полисахаридом с молекулярной массой 20000-80000 до разделения на казеиновую и полисахаридную фазу [Патент 1725803 (Россия). Способ переработки молока. / Молочников В. В. , Толстогузов В.Б.]. И получают концентрат натурального казеина (КНК), содержащий около 97% казеина и безказеиновую фракцию, содержащую всю водорастворимую часть молока и полисахарид. В дальнейшем безказеиновую фазу сгущают, получая при этом концентрат структурирующий пищевой (КСП) [Патент 181876 (Россия). Способ получения белкового полисахаридного концентрата./ Молочников В.В., Щанов В.Ю., Анисимов С.В., Храмцов А.А.]. КСП рекомендован для использования в качестве добавки к молочным и кондитерским изделиям как сруктурообразующий компонент, а также для регулирования содержания в продуктах растворимых биологически активных компонентов, повышающих устойчивость организма к вредным воздействиям окружающей среды [ТУ 49 1171-85 Концентрат структурирующий пищевой КСП]. Недостатком данных способов является содержание в готовом продукте (КСП) биологически активных веществ в неконцентрированном состоянии, а также содержание наряду с белковыми компонентами минеральных веществ, лактозы и пектина, а кроме того, КСП подвергается технологической обработке, в результате которой нативные свойства биологически активных веществ молока снижаются.
Японскими учеными запатентован в России способ получения продукта, содержащего "активные молочно-белковые компоненты", и продукт, полученный этим способом (варианты) [Патент 21-6785 (Россия). Способ получения продукта, содержащего активные молочно-белковые компоненты, и продукт, полученный этим способом (варианты)./ Йосиказу Юки (JP), Кумико Теразава (JP), Томойо Накагава (JP), Казуо Кате (JP)]. Целью разработанного способа является получение для недоношенных детей продуктов, получаемых из грудного или коровьего молока и содержащих активные молочные белковые компоненты, а именно иммуноглобулины, лактоферрин и лизоцим. Эти продукты также могут быть использованы в качестве добавки к грудному молоку и как фармацевтические продукты, например, при терапии неподдающегося поноса. Авторы патента термин "активные белковые компоненты" используют для обозначения любого белка, который в минимальных количествах проявляет физиологические и фармакологические свойства. Продукты получают по способу, состоящему из стадий добавления к молочной плазме или сыворотке сахарного спирта, или дисахарида, или стабилизатора, состоящего из дисахарида и аминокислоты (глицин), и проведения термообработки полученной смеси при рН 6-8, при примерно 60oС в течение около 10 ч; продукты, содержащие активные компоненты молочного белка, представляют собой осадок, образовавшийся при добавлении сульфата аммония в концентрации 30-60% (мас./объем) к термообработанной смеси. Термообработанную смесь охлаждают, а осажденную фракцию собирают центрифугированием и растворяют в изотоническом солевом растворе, подвергают адекватному диализу и стерилизации с помощью мембранной фильтрации. Недостатком данного способа является использование длительной (10 ч) термообработки, в результате которой уничтожаются не только вирусы, но и нативные вещества молока.
Корейскими учеными (Department of Biochemistry, Anatomy, Chemistry Korea) проведены исследования по использованию иммуноферментного анализа (ИФА) для определения и очистки ангиогенина из коровьего молока [Soo-lk Chang, Goo-Bo Jeong, et.al. Detection, Quantitation, and Localization of Bovine Angiogenin by Immunological Assays // Biochemical and biophysical research cjvvunications. 1997, v. 232. N 2. Pp. 323-327].
В Японии запатентован способ выделения из молока препарата ангиогенина, обладающего физиологической активностью [Патент 2-296000 (Япония)]. Благодаря наиважнейшей функции ангиогенина - способности индуцировать рост кровеносных сосудов предлагается использовать его для обработки поврежденных тканей, язв, при имплантации органов.
Однако в Японии запатентован способ использования ангиогенина в качестве препарата, стимулирующего рост волос [Патент 4-210618 (Япония)], а в США способ использования ангиогенина, выделенного из молозива или молока млекопитающих, например коровы, овцы, козы, в качестве биологически активного компонента косметического средства (в виде крема, эмульсии, лосьона) для удаления прыщей, веснушек и пятен с кожи [Патент 5698185 (США). Whitening cosmetic preparation and method of using same / Yasuharu Itagaki, Hidetoshi Ishikawa, Seiji Kurosawa].
Известен способ выделения ангиогенина, который представляет собой трехэтапный метод хроматографической очистки ангиогенина от белков молока с помощью ионообменной хроматографии на СМ-целлюлозе и гидрофобной хроматографии на CM Toyopearl 650S и Butyl Toyopearl 650 S [Патент 2109748 (РФ). Способ выделения ангиогенина / Рогов И.А., Шалыгина А.М., Комолова Г.С., Михайлов А. М. , Тихомирова Н.А.]. Данный способ является прототипом. Его недостатком является использование в качестве сорбентов дорогостоящих препаратов импортного производства, таких как CM Toyopearl 650 S и Butyl Toyopearl 650 S, а также использование трех этапов хроматографической очистки.
Таким образом, в результате патентного и литературного поиска установлено, что получение биологически активных веществ из молока является актуальной задачей, а использование нового белка ангиогенина в виде биологически активного препарата находит широкое распространение не только в медицине, фармакологии, но и в косметических целях.
Задачей, на решение которой направлено настоящее изобретение, является разработка способа получения БАД из различных видов молочного сырья, в том числе не используемого рационально, а именно: молозива, стародойного молока и вторичного сырья молочной промышленности, и полученная этим способом БАД "Милканг", содержащая в концентрированном виде низкомолекулярные катионные белковые вещества (ангиогенин, лизоцим, панкреатическую РНКазу и полипептиды), обладающие парафармацевтическими свойствами.
Это достигается тем, что для получения БАД "Милканга" низкомолекулярные катионные белки молочного происхождения отделяют от жировой фракции, подвергая центрифугированию молочное сырье, далее проводят их сорбцию и хроматографическое разделение, элюирование, определение фракций с оптической плотностью при длине волны 280 нм более 0,1 ед., подвергают диализу и согласно изобретению сорбцию и хроматографическое разделение проводят на СМ-целлюлозе, а диализ полученной белковой фракции проводят против физиологического раствора, при этом ее стабилизацию осуществляют микрофильтрацией через полупроницаемую мембрану с селективностью более 50 кДа, после чего полученную БАД, включающую ангиогенин, панкреатическую РНКазу, лизоцим и полипептиды, направляют на расфасовку.
Возможно полученную БАД "Милканг" подвергнуть сушке перед фасовкой.
Кроме того, следует указать, что для получения БАД "Милканг" возможно использовать в качестве источника нативных низкомолекулярных катионных белковых веществ: молоко, молозиво, стародойное молоко и вторичное сырье молочной промышленности: обезжиренное молоко; подсырную и творожную сыворотку; ультрафильтрат цельного и обезжиренного молока; ультрафильтрат подсырной или творожной сыворотки.
Технический результат, полученный согласно данному способу производства, заключается в том, что БАД содержит в нативном виде ангиогенин, лицозим, панкреатическую РНКазу и полипептиды, которые обладают ранозаживляющим и общеукрепляющим действием.
Разработан простой современный способ получения БАД на основе низкомолекулярных белков молока, обладающих биологической активностью. Впервые получена фракция низкомолекулярных катионных белков, обогащенных ангиогенином, панкреатической РНКазой, лизоцимом и полипептидами в очищенном виде. Благодаря получению белков в нативном состоянии данную фракцию целесообразно использовать в качестве БАД к пище или в терапевтических целях. Для ее получения применена ионообменная хроматография на СМ-целлюлозе. Впервые для стерилизации (микробиологической очистки) БАД использована микрофильтрация через полупроницаемые мембраны. В качестве источника низкомолекулярных катионных белковых веществ молока, обладающих общеукрепляющим и ранозаживляющим свойством, использовано сырое молоко, молозиво, стародойное молоко, а также вторичное сырье молочной промышленности. Молоко млекопитающих и вторичное молочное сырье является ценным источником биологически активных веществ [Биологически активные вещества молока / А.М. Шалыгина, Н.А. Тихомирова, И. И. Ионова, А. А. Петухов, Г.С. Комолова. М.: АгроНИИТЭИПП. 1997, 16 с.] и может быть использовано для получения БАД. В частности, представляют интерес практически не используемые в традиционных технологиях низкомолекулярные катионные белки, обладающие полифункциональными свойствами: панкреатическая РНКаза (12 кДа, противовирусное действие), ангиогенин (14,5 кДа, полифункциональный белок: фактор роста кровеносных сосудов, иммунорегулятор, бактерицидное действие), лизоцим (около 14 кДа, бактерицидное действие), а также полипептиды (с молекулярным весом менее 8 кДа, обладающие иммунорегуляторным действием). Разработанный способ позволяет получать БАД, содержащую в концентрированном и при этом в нативном виде вышеперечисленные белки и полипептиды. Благодаря сохраненным их нативным свойствам она обладает бактерицидным, иммунорегулирующим, а также ангиогенным свойствами, что позволяет ее использовать как непосредственно, так и в виде добавки к молочным и другим продуктам питания, которые могут быть рекомендованы в качестве диетического и лечебно-профилактического питания в общеукрепляющей и ранозаживляющей терапии.
Белковый состав БАД проверяют электрофорезом в ПААГ, а нативность белков - по ферментативной активности (лизоцим и РНКаза) и по взаимодействию с плацентарным ингибитором (ангиогенин).
Для получения БАД "Милканг" берут молочное сырье с нативными низкомолекулярными катионными белковыми веществами, обезжиривают, подвергая центрифугированию, далее обезжиренную белковую фракцию наносят на колонку с сорбентом СМ-целлюлозой и проводят ионообменную хроматографию, элюируют, собирая фракции с А280>0,1. Фракции объединяют и проводят диализ против физиологического раствора. Полученный диализат подвергают микрофильтрации через полупроницаемые мембраны селективностью более 50 кДа. В результате получают БАД в жидкой форме. Для получения сухой формы ее подвергают сушке.
Пример 1.
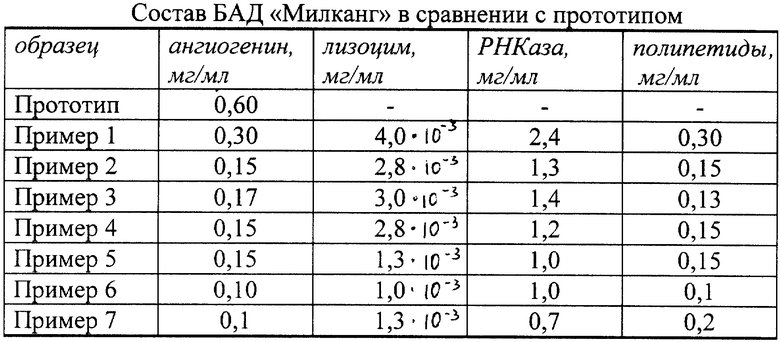
Молозиво в количестве 1 л обезжиривают центрифугированием, далее обезжиренную фракцию наносят на колонку с сорбентом СМ-целлюлозой и проводят ионообменную хроматографию, элюируют, собирая фракции с А280>0,1. Фракции объединяют и проводят диализ против физиологического раствора. Полученный диализат подвергают микрофильтрации через полупроницаемые мембраны селективностью более 50 кДа. В результате получают 25 мл БАД, состав которой в сравнении с прототипом представлен в таблице. Для получения сухой формы ее высушивают и получают 1 г БАД.
Пример 2.
Пример 2 осуществляют по примеру 1, при этом в качестве сырья используют молоко и получают БАД, состав которой представлен в таблице.
Пример 3.
Пример 3 осуществляют по примеру 1, при этом в качестве сырья используют стародойное молоко и получают БАД, состав которой представлен в таблице.
Пример 4.
Пример 4 осуществляют по примеру 1, при этом в качестве сырья используют обезжиренное молоко и получают БАД, состав которой представлен в таблице.
Пример 5.
Пример 5 осуществляют по примеру 1, при этом в качестве сырья используют подсырную сыворотку и получают БАД, состав которой представлен в таблице.
Пример 6.
Пример 6 осуществляют по примеру 1, при этом в качестве сырья используют творожную сыворотку и получают БАД, состав которой представлен в таблице.
Пример 7.
Пример 7 осуществляют по примеру 1, при этом в качестве сырья используют ультрафильтрат молочного сырья (цельное молоко, или обезжиренное молоко, или подсырная сыворотка, или творожная сыворотка) и получают БАД, состав которой представлен в таблице.
Таким образом, в сравнении с прототипом в состав БАД "Милканг" входят лизоцим, панкреатическая РНКаза и полипептиды, обладающие парафармацевтическими свойствами. В связи с чем БАД обладает не только ранозаживляющим, но и общеукрепляющим свойством.
| название | год | авторы | номер документа |
|---|---|---|---|
| СТЕРИЛИЗОВАННОЕ МОЛОКО, ОБОГАЩЕННОЕ АНГИОГЕНИНОМ | 2000 |
|
RU2182791C2 |
| СПОСОБ ПОЛУЧЕНИЯ БАД ИЗ НИЗКОМОЛЕКУЛЯРНЫХ КАТИОННЫХ БЕЛКОВ МОЛОКА И ПОЛУЧЕННАЯ ЭТИМ СПОСОБОМ БАД | 2006 |
|
RU2318406C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОЛОГИЧЕСКИ АКТИВНОЙ ДОБАВКИ "МОБЕЛИЗ" И ПОЛУЧЕННАЯ ЭТИМ СПОСОБОМ БАД "МОБЕЛИЗ" | 2008 |
|
RU2366294C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОЛОГИЧЕСКИ АКТИВНОГО БЕЛКОВОГО КОНЦЕНТРАТА, ОБОГАЩЕННОГО ПАНКРЕАТИЧЕСКОЙ РИБОНУКЛЕАЗОЙ А, АНГИОГЕНИНОМ И ЛИЗОЦИМОМ, ИЗ МОЛОЧНОГО УЛЬТРАФИЛЬТРАТА | 2001 |
|
RU2204262C2 |
| СПОСОБ ПОЛУЧЕНИЯ БАД "Л-ПФИ" ИЗ ВТОРИЧНОГО МОЛОЧНОГО СЫРЬЯ И ПОЛУЧЕННАЯ ЭТИМ СПОСОБОМ БАД "Л-ПФИ" | 2009 |
|
RU2400106C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ АНГИОГЕНИНА В БИОЛОГИЧЕСКОМ СЫРЬЕ | 1996 |
|
RU2110066C1 |
| СПОСОБ ПРОИЗВОДСТВА ФУНКЦИОНАЛЬНОГО ПРОДУКТА | 2013 |
|
RU2536952C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ АНГИОГЕНИНА В МОЛОЧНОМ СЫРЬЕ | 1998 |
|
RU2133464C1 |
| СПОСОБ ВЫДЕЛЕНИЯ БЕЛКОВОЙ ФРАКЦИИ, ОБОГАЩЕННОЙ АНГИОГЕНИНОМ | 2000 |
|
RU2175195C1 |
| СПОСОБ ПЕРЕРАБОТКИ МОЛОКА И ПРОДУКТ, ПОЛУЧЕННЫЙ ЭТИМ СПОСОБОМ | 2012 |
|
RU2535876C2 |
Изобретение относится к молочной, биотехнологической, медицинской и фармацевтической промышленности, а именно к способам получения биологически активных веществ, которые могут использоваться в качестве биологически активных добавок (БАД). Способ включает очистку сырья центрифугированием, сорбцию белков на ионообменнике, хроматографическое их разделение, элюирование, определение фракции с оптической плотностью при длине волны 280 нм более 0,1 ед., диализ и стабилизацию. В качестве сырья используют нативные низкомолекулярные катионные белковые вещества молочного происхождения. Хроматографическое разделение проводят на СМ-целлюлозе, а диализ - против физиологического раствора, при этом стабилизацию осуществляют микрофильтрацией через полупроницаемые мембраны с селективностью более 50 кДа. Полученную БАД фасуют. Перед фасовкой БАД подвергают сушке. В качестве нативных низкомолекулярных катионных белковых веществ молочного происхождения используют молоко, или молозиво, или стародойное молоко, или обезжиренное молоко, или подсырную сыворотку, или творожную сыворотку, или ультрафильтрат обезжиренного или цельного молока, а также ультрафильтрат подсырной или творожной сыворотки. Биологически активная добавка может дополнительно содержать лизоцим, панкреатическую РНКазу и полипептиды. Данный способ позволяет получить БАД, содержащую в нативном виде ангиогенин, лизоцим, панкреатическую РНКазу и полипептиды, которая обладает ранозаживляющим и общеукрепляющим действием. 2 с. и 9 з.п. ф-лы, 1 табл.
Ангиогенин - 0,1-0,3
Лизоцим - 1,0•10-3-4,0•10-3
Панкреатическая РНКаза - 0,7-2,4
Полипептиды - 0,1-0,3
| СПОСОБ ВЫДЕЛЕНИЯ АНГИОГЕНИНА | 1996 |
|
RU2109748C1 |
| US 5698185 A, 16.12.1997 | |||
| СПОСОБ ПРИГОТОВЛЕНИЯ ВОДНО-ЦЕМЕНТНОЙ СМЕСИ И УСТАНОВКА ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2009 |
|
RU2410237C1 |
Авторы
Даты
2002-06-27—Публикация
2000-04-06—Подача