Изобретение относится к медицине, более точно к фармации, и может быть использовано при изготовлении препарата для лечения и профилактики гриппа, ОРЗ и энцефалитов, а также др. вирусных заболеваний у детей и взрослых.
Проблема лечения вирусной патологии чрезвычайно актуальна ввиду увеличения количества таких больных. Средства для профилактики и лечения вирусных заболеваний активно разрабатываются фармацевтической промышленностью.
В патентном фонде России и СССР широко представлены изобретения, посвященные этой проблеме.
Так, в патенте RU 2135187 C1, A 61 K 31/765, 27.08.99 описано использование сополимера стирола с ангидридом для лечения герпетического кератита. Лечение герпеса губ с помощью полиметакриловой кислоты описано в патенте RU 2111751 Cl, A 61 K 31/78, 27.05.98. Лечение герпетического поражения глаз с помощью полиакриламида описано в патенте SU 628924, A 61 K 31/78, 25.10.78. Лечение опоясывающего лишая путем применения 0,1% смеси гликозаминогликанов, выделенных из плаценты человека, изложено в патенте RU 2140786 Cl, A 61 K 31/725, 10.11.99.
Средства для лечения ОРЗ известны из патентов RU 2127116 C1, A 61 K 35/80, 10.03.99, SU 1336301 Al, A 61 K 35/78, 22.03.74. Усиление свойств известного противовирусного препарата ацикловира описано в авторском свидетельстве SU 1375113 A3, A 61 K 9/107, 18.07.80. Распространенность и тяжесть заболеваний требует необходимости создания и профилактики, в первую очередь, таких заболеваний, как ОРЗ, грипп, герпес, клещевой энцефалит.
Известны противовирусные препараты, содержащие в качестве активного начала ремантадин.
Ремантадин - аминоэтиладамантан, представляет собой каркасное соединение, имеющее трехмерную структуру в виде гидрофобного ядра адамантат. Фармакологическая активность ремантадина в значительной степени определяется наличием положительно заряженной при α-1C аминогруппы: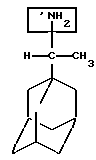
Механизм действия препарата в настоящее время хорошо изучен. В институте Гриппа детально исследованы все стадии фармакологического действия препарата. Ремантадин эффективно взаимодействует с клеточными мембранами и, в частности, с отрицательно заряженными на поверхности клеточных мембран фосфолипидами. Гидрофобное ядро адамантана интеркалирует внутрь мембран между остатками жирных кислот. Поэтому ремантадин относится к мембранотропным препаратам. Высокая атрактивность к мембранам позволяет ремантадину быстро достигнуть белка-мишени. Таким белком является белок М2 вируса гриппа. Вирус гриппа кодирует в 7 фрагменте два мембранных белка: Ml и М2. Белок М2 организован в вирусной и клеточной мембране в виде тетрамера, который выполняет функции ионного канала - протонной помпы. Именно поэтому вирус гриппа является зависимым от рН, то есть кислотности окружающей среды. Ремантадин, связываясь с мембранами инфицированных, увлекается потоком протонов внутрь полого канала тетрамера белка М2. Положительно заряженная аминогруппа ремантадина взаимодействует с гидроксилом Серина в 31 положении белка М2, что приводит к практически полной блокаде протонного насоса и, следовательно, блокирует инфекционную активность вируса на уровне лизосомального этапа декапсидации вирусных частиц. Фактически это блокирует развитие инфекции. К этому следует добавить, что ремантадин адамантановым ядром прочно связывается с так называемым адамантан-связывающим сайтом белка М2, составляющим часть трансмембранного домена: 25-Про-Лей-Вал-Вал-Але-Але-Сер-31. Эта связь необратимая, потому ремантадин можно отнести к суицидным для белка М2 ингибиторам.
Именно этим и объясняется высокая специфичность ремантадина в отношении вирусов гриппа А и его высочайшая эффективность при лечении гриппозной инфекции. Ремантадин не действует на грипп В и другие респираторные вирусы. Но при этом следует учитывать, что в период эпидемии только 15% заболеваемости гриппом приходится на долю вирусов гриппа В и парагриппа. Этим и оправдывается широкое применение ремантадина в эпидемический период (Ершов Ф.И., Чижов Е.П., Тазулахова Э.Б. Противовирусные средства. СПб., 1993, c. l9; Amer. J.Med. - 1987, Y. 82, 6А, Р. 35-41; Перший Г.Н., Богданова Н.С. Химиотерапия вирусных инфекций. М.: Медицина, 1973, с. 73).
Следует отметить, что ремантадин в общепринятой лекарственной форме имеет ряд существенных недостатков, ограничивающих его применение в высоких дозировках для взрослых и детей дошкольного возраста. К этим недостаткам относятся:
- появление побочных результатов при длительном приеме (более 5 дней) тошноты, головных болей (в 10% случаев);
- быстрое появление штаммов, резистентных к препарату;
- быстрое выведение из организма в течение 1,5-4,5 часов;
- отсутствие влияния на нейротоксикоз при осложненном гриппе и ОРЗ, в случае развития неврологической симптоматики;
- недостаточная активность при лечении энцефалитов;
- изменение кислотности желудка при пониженной кислотности в силу основных свойств ремантадина.
Было синтезировано соединение ремантадина с сополимером винилового спирта и N-винилимидоянтарной кислотой за счет формирования связи С-О под названием "Полирем" (см. патент RU 2071323, А 61 К 31/785, 10.01.97). Это средство обладает рядом преимуществ перед нативным ремантадином, т.к. обладает более выраженным противовирусным действием, имеет интерфероногенный эффект, безвреден.
Этот объект был выбран в качестве наиболее близкого аналога заявленного изобретения. Однако известный препарат обладает побочными эффектами (в т.ч. изменение кислотности желудка), недостаточными иммуномодулирующими свойствами и коротким периодом выведения из крови.
Техническим результатом изобретения является снижение токсичности, обеспечение оказания лечебного воздействия на частоту выделения резистентных к ремантадину вирусов гриппа, на вирусы клещевого энцефалита при одновременном повышении биодоступности его и обеспечении пролонгированного действия.
Технический результат достигается тем, что в препарате для лечения и профилактики вирусных заболеваний, содержащем ремантадин, фиксированный к полимеру, в качестве полимера используют альгинат натрия, а препарат дополнительно содержит сахарный сироп или сироп сорбитола 20-60%-ный, причем препарат получен путем смешения ремантадина, альгината натрия и указанного сиропа, взятых в количествах, соответствующих следующему соотношению исходных компонентов, мас.%:
Ремантадин - 0,05-5,0
Альгинат натрия - 0,05-5,0
Сахарный сироп или сироп сорбитола 20-60%-ный - Остальное
причем предпочтительно брать ремантадин и альгинат натрия в соотношении 1:1.
Растворимая форма ремантадина в сочетании с альгинатом натрия позволяет использовать форму сахарного сиропа для приготовления препарата, что позволяет использовать его для лечения детей. Могут использоваться и твердые формы препарата, например, в виде таблеток или капсул.
Получение препарата
Альгинат является кислым мукополисахаридом водорослей. При взаомодействии с основанием аминоэтиладамантаном (ремантадином) альгинат-Na образует прочный солевой комплекс. Комплексообразование проверяли гельхроматографией на колонках с сефарозой - 2В. О насыщении альгината ремантадином судили по количеству ремантадина, выявляемому во втором пике элюции. Первым пиком элюировался высокополимерный альгинат.
Таким образом, комплекс ремантадина/альгината является полимерной формой ремантадина.
В ранее разработанном препарате "Полирем" (RU 2071323) α-1-метил-α(1-адамантил)метиламин (ремантадин) связан с полимерным носителем на основе сополимера винилового спирта с N-виниламиноянтарной кислотой. Полимеризация ремантадина в такой системе существенно улучшает свойства препарата.
При выборе альгината преследовалась цель замены синтетического полимера со слабой активностью в индукции интерферона на природный носитель, обладающий выраженными иммуномодулирующими свойствами, каким и является природный мукополисахарид - альгинат.
Для получения целевого продукта готовят сироп, например, 60%-ный сахарный сироп, и одновременно готовят смесь ремантадина с альгинатом натрия в расчетных количествах. После трехчасовой инкубации смесь добавляют в сироп при медленном перемешивании. Полученный сироп перемешивают и фасуют.
В таблице 1 приведены примеры рецептуры для приготовления препарата.
Полученный препарат исследовали на биодоступность и фармакокинетику.
Биодоступность и фармакокинетика альгината иремантадина
Биодоступность исследовали путем определения концентрации ремантадина в крови после внутрижелудочного введения через зонд альгината ремантадина у мышей. Через 1,5 часа ремантадин появляется в крови и достигает максимума через 5,5 часа. Концентрация ремантадина остается стабильной в течение 12 часов и затем к концу суток снижается до следовых концентраций. Ремантадин-мономер имеет более короткий период полужизни в периферической крови. Достигая максимума через 1,5-2 часа, ремантадин-мономер полностью элиминируется из крови через 6 часов.
Таким образом, альгинат ремантадина имеет высокую биодоступность и длительный период выведения из крови, что позволяет рекомендовать прием 2 раза в день.
Анализировали также токсичность полученного средства.
Токсичность ремантадина в комплексе с альгинатом натрия
Для оценки токсичности препарата использовали концентрацию ремантадина, равную 5,7 мг/кг массы тела подопытных мышей, которая соответствует десятикратной эквитерапевтической дозе.
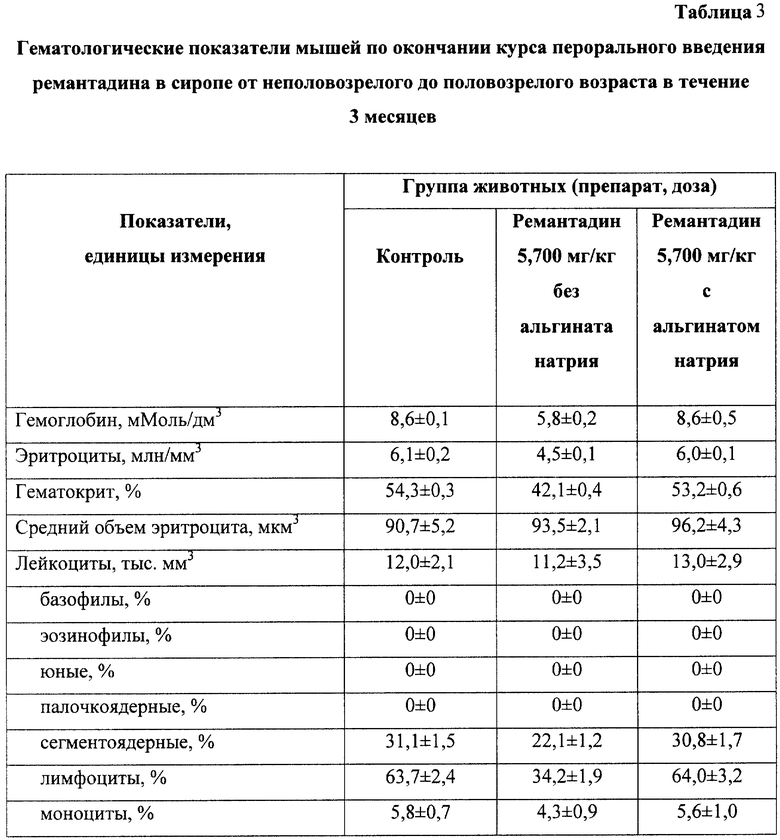
Эксперименты проводили на двух группах мышей неполовозрелого возраста, одна из которых получала суточную дозу ремантадина в сиропе без альгината натрия, другая - равную дозу с альгинатом натрия. На протяжении трех месяцев оценивалась динамика изменения массы тела и гематологические показатели.
Как следует из данных, приведенных в табл. 1 и 2, прием ремантадина в дозе 5,7 мг/кг веса без альгината натрия существенно ухудшает динамику нарастания массы тела у подопытных животных и снижает гематологические показатели. Тогда как в параллельных экспериментах у мышей, получавших ремантадин в той же дозе, но в комплексе с альгинатом натрия, упомянутые показатели практически не отличаются от контроля, что убедительно свидетельствует о существенном снижении токсичности ремантадина в случае его приема в комплексе с альгинатом натрия.
Результаты изучения действия альгината-Na и ремантадина на частоту выделения резистентных к ремантадину вирусов гриппа от больных гриппозной инфекцией
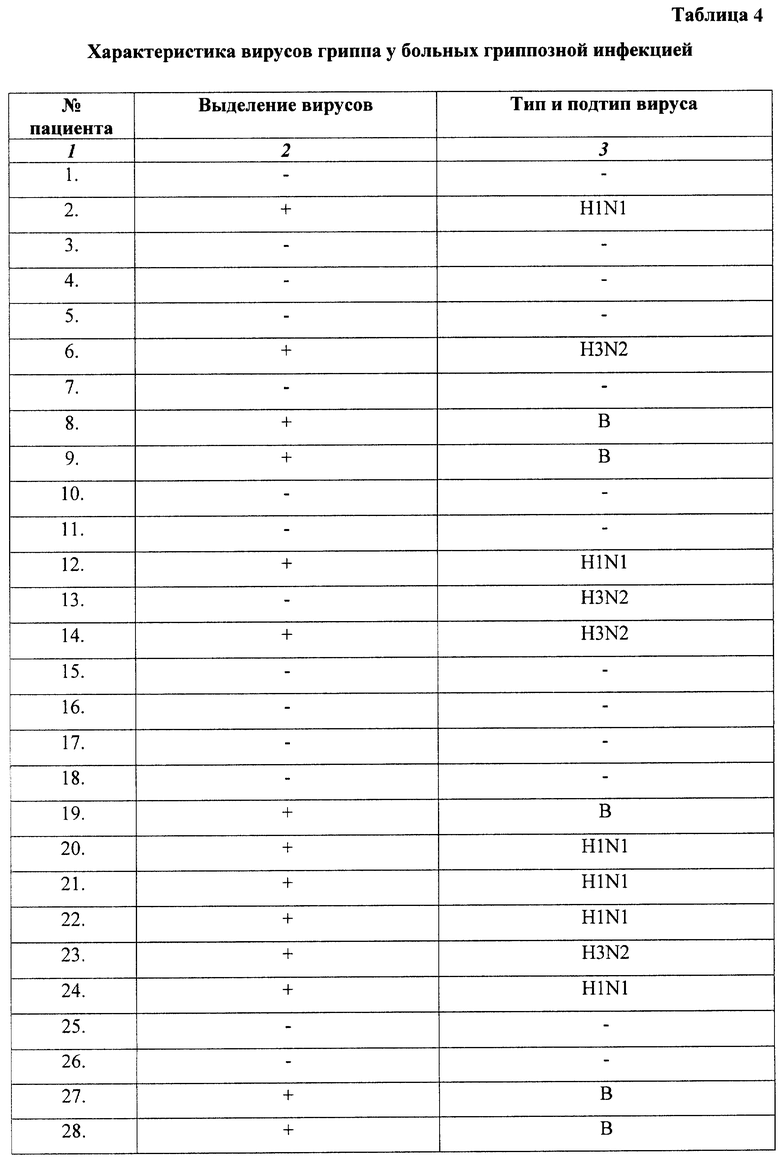
Наблюдение проводили на 56 больных гриппом в эпидемический период 1998/1999 гг. , в январе-феврале, когда наблюдался в Санкт-Петербурге пик заболеваемости гриппом. В группу наблюдения отбирались дети в возрасте от 10 до 16 лет. Прием ремантадина половине пациентов назначали немедленно по 1 чайной ложке 4 раза в день. У больных через 2 дня после начала приема ремантадина в сиропе отбирали носоглоточные смывы и заражали клеточную культуру MDCK, высокочувствительную к вирусам гриппа.
Данные по выделению вирусов гриппа представлены в таблице 3. Как видно из таблицы 3, максимальная частота выделения характерна для вирусов H1N1 (21,4%). Вирусы гриппа H3N2 выделялись с частотой около 14%, а грипп В - около 18%. Совпадающие данные с превышением эффектности выделяемости вирусов на 32% получены в контрольной группе детей, не получавших ремантадин в сиропе, а принимавших антигриппин и другие симптоматические средства. Выделяемые вирусы исследовали после двух пассажей на устойчивость к ремантадину. Для выделения ремантадин-резистентных вирусов использовали клетки MDCK и ремантадин в концентрации 10 мкг/мл. В результате установлено, что у детей, получавших ремантадин в сиропе, выделен только один штамм вируса гриппа, резистентный к ремантадину. В контрольной группе также выделен один штамм вируса гриппа H3N2, резистентный к ремантадину. Из этих данных следует, что ремантадин с альгинатом не вызывает при рекомендованном режиме применения повышения частоты выделяемости вирусов, резистентных к ремантадину.
По данным Хайдена частота выделения резистентных к ремантадину вирусов гриппа при применении в режиме по 1 таблетке (50 мг) 4 раза в день в его эпидемических исследованиях достигала 26-32% (для разных возрастных групп).
Полученные результаты свидетельствуют о том, что сочетание альгината и ремантадина в сиропе, благоприятно изменяющее фармакокинетику ремантадина, приводит к снижению частоты появления ремантадин-резистентных вирусов.
Пример 1 использования полученного средства.
Для подтверждения лечебного эффекта предлагаемого препарата было взято две группы больных детей от 6 до 10 лет полностью по 20 человек с признаками заболевания гриппом, подтвержденного лабораторными анализами смывов из носоглотки. 1-ая группа получала сироп альгирем по 4 ч. л. в день в течение 10 дней. 2-ая группа не получала специального противовирусного лечения.
В процессе наблюдения установлено, что в первой группе больных на 4-5-ый день после начала приема препарата значительно уменьшились клинические проявления гриппозной инфекции, нормализовалась температура, отсутствовали осложнения.
Во второй группе наблюдалось значительно более тяжелое течение заболевания, продолжительная гипертермия, у некоторых больных появились признаки пневмонии и неврологическая симптоматика. В ряде случаев потребовались интенсивные лечебные мероприятия.
Полученные результаты подтверждают высокую эффективность препарата при лечении гриппа.
Пример 2
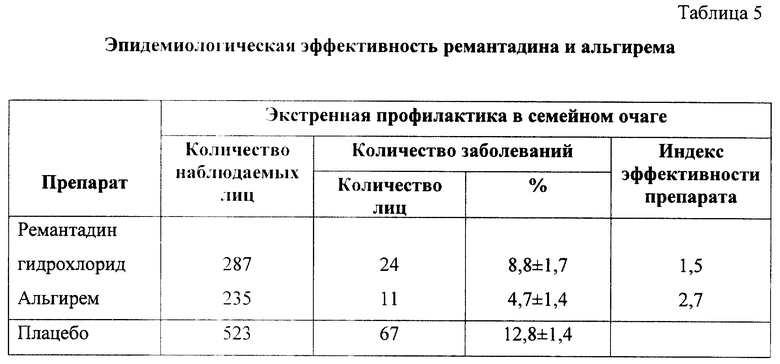
Результаты, полученные при изучении предлагаемого препарата в условиях эпидемической ситуации, подтвердили его высокую эффективность. В семейных очагах контактирующие с больными окружающие в профилактических целях принимали по 2 чайных ложки ремантадина с альгинатом (альгирем) (по 20 мг в пересчете на ремантадин - основание). Эффективность профилактики гриппа в условиях эпидемии в результате приема альгирема более чем в 2 раза превосходила эффективность при применении ремантадина гидрохлорида (табл. 4). Индекс эффективности предлагаемого препарата с высокой степенью достоверности (р<0,01) в 2,1 раза выше индекса ремантадина гидрохлорида.
Пример 3
Эффективность альгирема в отношении вируса клещевого энцефалита была определена на модели инфекции мышей при введении вируса клещевого энцефалита, штамма Абсеттаров, выделенного из крови больного. Для воспроизведения летальной инфекции использовали периферический (подкожный) путь введения вируса, культивированного в мозговой ткани мышей. Заражение проводили при введении 0,2 мл/мышь взвеси мозговой ткани в физиологическом растворе (водный раствор NaC1 массовой доли 0,85%), содержащей 1-10 ЛД50 вируса.
В экспериментальных группах животных вводили альгирем перорально в дозе на каждый прием в пересчете на содержание 0,5 мкг/кг веса.
Введение препарата осуществляли по различным схемам. Альгирем вводили однократно за 24 ч до инфицирования (схема 1) или за 1 ч до инфицирования (схема 2). Альгирем вводили трехкратно за 1 ч до инфицирования и через 48 и 96 ч после инфицирования (схема 3). Введение препарата осуществляли за 24 ч до инфицирования и через 4 ч и далее через 24 ч после (схема 4).
Эффективность препарата оценивали по уровню гибели животных по сравнению с контрольной группой мышей, которым давали плацебо (физиологический раствор) по схеме опытной группы.
При всех использованных схемах введения альгирема наблюдалось выраженное снижение гибели зараженных мышей (табл. 5). Эффект достигался уже при однократном введении препарата. Более высокая эффективность при введении по лечебно-профилактическим схемам (3 и 4) обусловлена особенностью патогенеза инфекции клещевого энцефалита, который характеризуется двухволновым течением. Наблюдаемые различия в показателях защиты препарата при разных схемах его введения зависят от некоторых колебаний гибели животных в контрольных группах.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОТИВОВИРУСНЫЙ ПРЕПАРАТ "ПОЛИРЕМ" | 1994 |
|
RU2071323C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ГРИППА | 2003 |
|
RU2229877C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ ДЫХАТЕЛЬНОГО ТРАКТА "ГЛЮКАФЕРОН" | 2011 |
|
RU2450812C1 |
| ПРОТИВОВИРУСНОЕ СРЕДСТВО ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ КЛЕЩЕВОГО ЭНЦЕФАЛИТА | 2010 |
|
RU2444363C2 |
| СПОСОБ И СРЕДСТВО АКТИВАЦИИ IRF-3 ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ЗАБОЛЕВАНИЙ, ВЫЗЫВАЕМЫХ (+) PHK-СОДЕРЖАЩИМИ ВИРУСАМИ | 2012 |
|
RU2518314C2 |
| ТВЕРДАЯ ДОЗИРОВАННАЯ ФОРМА ДЛЯ ПЕРОРАЛЬНОГО ПРИМЕНЕНИЯ, ОБЛАДАЮЩАЯ ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ (ВАРИАНТЫ) | 1995 |
|
RU2115415C1 |
| СРЕДСТВО ДЛЯ ПОВЫШЕНИЯ УСТОЙЧИВОСТИ ОРГАНИЗМА К ВИРУСНЫМ И ВИРУС ИНДУЦИРОВАННЫМ ЗАБОЛЕВАНИЯМ | 2005 |
|
RU2319497C2 |
| НОВЫЕ СОСТАВЫ 2-(ИМИДАЗОЛ-4-ИЛ)-ЭТАНАМИДА ПЕНТАНДИОВОЙ-1,5 КИСЛОТЫ ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ВИРУСНЫХ ЗАБОЛЕВАНИЙ | 2020 |
|
RU2782532C2 |
| НОВЫЕ СОСТАВЫ 2-(ИМИДАЗОЛ-4-ИЛ)-ЭТАНАМИДА ПЕНТАНДИОВОЙ-1,5 КИСЛОТЫ ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ВИРУСНЫХ ЗАБОЛЕВАНИЙ | 2020 |
|
RU2746692C1 |
| НОВЫЕ СОСТАВЫ 2-(ИМИДАЗОЛ-4-ИЛ)-ЭТАНАМИДА ПЕНТАНДИОВОЙ-1,5 КИСЛОТЫ ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ВИРУСНЫХ ЗАБОЛЕВАНИЙ | 2020 |
|
RU2791902C2 |


Изобретение относится к медицине, а именно к фармацевтической промышленности. Препарат содержит ремантадин, фиксированный к полимеру, и сахарный сироп или сироп сорбитола 20-60%-ный, причем препарат получают путем смешения ремантадина, альгината натрия и указанного сиропа при следующем соотношении исходных компонентов, мас. %: ремантадин 0,05-5,0, альгинат натрия 0,05-5,0, сахарный сироп или сироп сорбитола 20-60%-ный - остальное. Предпочтительным является соотношение ремантадина и альгината натрия 1:1. Препарат обладает высокой биодоступностью и эффективностью. 1 з.п.ф-лы, 5 табл.
Ремантадин - 0,05-5,0
Альгинат натрия - 0,05-5,0
Сахарный сироп или сироп сорбитола 20-60%-ный - Остальное
2. Препарат по п. 1, отличающийся тем, что он получен путем смешения указанных компонентов при соотношении ремантадина и альгината натрия, равном 1: 1.
| ПРОТИВОВИРУСНЫЙ ПРЕПАРАТ "ПОЛИРЕМ" | 1994 |
|
RU2071323C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ ПРОТИВОВИРУСНЫМ ДЕЙСТВИЕМ | 1999 |
|
RU2145218C1 |
| СПОСОБ УСИЛЕНИЯ ЛЕЧЕБНОГО ЭФФЕКТА ЛЕКАРСТВЕННЫХ СРЕДСТВ | 1997 |
|
RU2104032C1 |
| СПОСОБ СНИЖЕНИЯ ТОКСИЧНОСТИ ЛЕКАРСТВЕННЫХ СРЕДСТВ, МЕТАЛЛОВ, ОРГАНИЧЕСКИХ И НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ И ДРУГИХ ТОКСИНОВ | 1997 |
|
RU2104033C1 |
| Устройство для определения момента резки спиралей с тире | 1979 |
|
SU773791A1 |
| ПЛАТОНОВ В.Г | |||
| и др | |||
| Поиск эффективных средств профилактики и лечения гриппа в ряду полимерных соединений аминопроизводных адамантана | |||
| - Химиотерапия и химиопрофилактика гриппа и ОРЗ, Л., 1990, с.24-29. | |||
Авторы
Даты
2002-07-27—Публикация
2000-08-01—Подача