Область изобретения
Областью изобретения является иммунология.
Предпосылки изобретения
Лимфокины - это группа полипептидов, принадлежащих к семейству цитокинов, то есть гормоноподобных молекул, которые способны влиять на различные функции клеток и осуществлять коммуникацию между различными клетками. Недавние исследования помогли прояснить роль лимфокинов в иммунном ответе. Продуцирование лимфокинов хелперными Т клетками CD4+ (а также CD8+) часто приводит к одному из двух фенотипов. Th1 и Th2, как в иммунной системе мыши, так и человека (Romagnani. 1991, Immunol Today 12: 256-257, Mosmann, 1989, Annu Rev Immunol, 7:145-173). Th1 клетки продуцируют интерлейкин 2 (IL-2), фактор некроза опухоли (TNFα) и интерферон гамма (IFNγ), и они отвечают прежде всего за клеточно-опосредованный иммунитет, такой как гиперчувствительность замедленного типа. Th2 клетки производят интерлейкины, IL-4, IL-5, IL-6, IL-9, IL-10 и IL-13 и прежде всего участвуют в обеспечении оптимальной помощи гуморальным иммунным ответам, таким как переключение изотипов IgE и IgG4 антител. (Mosmann, 1989, Annu Rev Immunol, 7:145-173).
Сильно поляризованные Th1 и Th2 ответы не только играют различные роли в защите, они также могут усиливать различные иммунопатологические реакции. Ответы Th1-типа участвуют в органно-специфическом аутоиммунитете, таком как экспериментальный аутоиммунный увеоретинит (Dubey et al, 1991, Eur Cytokine Network, 2:147-152), экспериментальный аутоиммунный энцефалит (ЕАЕ) (Beraud et al, 1991. Cell Immunol, 133:379-389) и инсулинзависимый сахарный диабет (Hahn et al, 1987, Eur J Immunol, 18:2037-2042), в контактном дерматите (Kapsenberg et al, Immunol Today, 12: 392-395) и некоторых хронических воспалительных заболеваниях. Напротив, ответы Тh2-типа ответственны за запуск аллергических атонических заболеваний (против обычных аллергенов окружающей среды), таких как аллергическая астма (Walker et al, 1992, Am Rev Resp Dis 148:109-115) и атопический дерматит (van der Heijden et al, 1991, J Invest Derm 97:389-394), считается, что они обостряют инфекцию живущими в тканях протозоа, такими как гельминты (Finkelman et al, 1991, Immunoparasitol Today 12:A62-66) и Leishmania major (Caceres-Dittmar et al., 1993, Clin Exp Immunol, 91:500-505); преимущественно вовлечены в некоторые первичные иммунодефициты, такие как гипер-IgE синдром (Del Prete et al, 1989. J. Clin Invest, 84: 1830-1835) и синдром OmennOs (Schandene et al, 1993, Eur J. Immunol, 23, 56-60), и связаны с пониженным гипер-IgG синдромом (Del prete et al, 1989, J. Clin Invest, 84:1830-1835) и синдромом OmennOs (Schandene et al, 1993, Eur J. Immunol 23:56-60) и связаны с пониженной способностью подавлять репликацию ВИЧ (Barker et al, 1995, Proc Soc Nat Acad Sci USA 92: 11135-11139).
Таким образом, ясно, что модуляция профилей лимфокинов ранее упомянутых заболеваний была бы терапевтически выгодна. Усиление Тh1 ответа вероятнее всего приведет к реверсии Th2 фенотипа и наоборот. Было показано, что моноклональные антитела к лимфокинам, сами лимфокины и другие агенты, такие как тиоловые антиоксиданты (Jeannin et al, 1995, J Exp. Med, 182:1785-1792) изменяют патогенез некоторых болезней путем ингибирования стимулирующего заболевание типа цитокинов, либо Тh1 или Th2. Например, внутриклеточные протозойные инфекции ограничиваются IFNγ, но усиливаются IL-4, в то время как нематодные инфекции контролируются IL-4 и усиливаются IFNγ (Heinzel et al, 1989, J Exp Med 162:59-72, Else et al, 1994, J Exp Med 179:347-351). Инсулинзависимый сахарный диабет у NOD мышей и ЕАЕ у мышей и крыс может быть улучшен лечением IL-4 или анти-IFNγ моноклональными антителами до развития указанной болезни (Rapoport et al, 1993, J Exp Med 178:87-99, Racke et al, 1994, J Exp Med 180:1961-1966, Campbell et al, 1991, J Clin Invest 87:739-742). В дополнение к этому аутоиммунная реакция "трансплантат против хозяина" (GVHD), характеризующаяся эритрематозноподобным синдромом - системной волчанкой, ассоциирована с продуцированном Th2 лимфокинов и ингибируется aнти-IL-4 антителами (Umland el al, 1992, Clin Immunol Immunopathol 63:66-73). С другой стороны, Тh1 цитокины продуцируются при остром GVHD, при котором донорские CD8+ Т клетки развиваются в CTL и разрушают иммунную систему хозяина. Лечение анти-EFNγ или анти-TNFα моноклональными антителами облегчает заболевание, а лечение анти-IL-2 моноклональными антителами превращает острый GVHD в аутоиммунный GVHD (Via and Finkelman, 1993, Int Immunol 5: 565-572).
Клинические испытания нативного и рекомбинантного IL-2 при лечении ВИЧ-инфицированных пациентов проводятся с 1983 г. (Volberding et al, 1987, AIDS Res Hum Retroviruses, 3:115-124). При этом причиной послужил тот факт, что было показано, что развитие СПИДа (AIDS) ассоциировано с переключением типа производимых лимфокинов (Clerici and Shearer, 1994, Immunol Today, 15: 575-581). Со временем у инфицированного индивидуума с развитием болезни обнаруживается пониженная экспрессия Тh1 лимфокинов, таких как IL-2 (Maggi et al, 1987, Eur J. Immunol, 17:1685-1690, Grutes et al, 1990, Eur J. Immunol, 20: 1039-1044, Clerici et al, 1993, J/ Clin Invest, 91:759-765), чему сопутствует повышенное продуцирование Th2 лимфокинов, таких как IL-4 и IL-10 (Clerici et al, 1994, J Clin Invest 93:768-775, Hoffman et al, 1985, Virology. 147:326-335). Т-клетки от асимптоматических или длительно живущих больных, обработанные IL-2, усиливали свою анти-ВИЧ активность, в то время как экспозиция с IL-4 или IL-10 уменьшала их способность подавлять репликацию ВИЧ и продуцировать IL-2 (Barker et al, 1995. Proc Soc Nat Acad Sci USA, 92: 11135-11139).
Эти современные иммуномодуляторные терапевтические средства (моноклональные антитела и рекомбинантные цитокины) имеют, однако, ограничения. Например, при постоянном лечении моноклональными антителами животное-хозяин производит антитела против моноклональных антител, ограничивая таким образом их полезное действие. Получены "гуманизированные" моноклональные антитела, что заметно снизило риск индуцированного иммунного ответа на эти моноклональные антитела. Однако это еще находится на стадии разработки, и к тому же эти новые моноклональные антитела остаются большими белками и поэтому могут иметь трудности в достижении сайтов-мишеней. Терапевтические средства, основанные на цитокинах, также имеют ограничения. Например, лечение аутоиммунного GVHD с помощью IL-2 ведет к развитию острого GVHD у мышей.
Рибавирин (1-b-D-рибофуранозил-1,2,4-триазол-3-карбоксамид) представляет собой синтетический нуклеозид, способный ингибировать репликацию РНК и ДНК вируса (Huffman et al, 1973, Antimicrob Agents Chemother, 3:235, Sidwell et al, 1972, Science, 177:705). Авторы подтвердили наблюдения тех, кто предположил, что рибавирин в дополнение к своей антивирусной активности влияет на некоторые иммунные ответы (см. обзор Jolley and Suchil, 1984, Clinical Applications of Ribavirin: p.93-96). Авторы также подтвердили наблюдения других. что рибавирин влияет на пролиферацию митоген- и антиген-активированных Т и В лимфоцитов (Tam et al, 1995 (данные не показаны), Peavy et al, 1980, Infection and Immunity, 29:583-589), а затем, при комбинировании с циклоспорином, рибавирин проявил эффективность при долгосрочном выживании аллотрансплантата (Jolley et al, 1988, Transplantation Proc, 20:703-706).
В дополнение, авторы значительно продвинули первоначальные исследования, показав, что рибавирин модулирует тип цитокина при иммунном ответе, по меньшей мере частично стимулируя Th1 ответ и подавляя Th2 ответ. При сопоставлении с ранее полученными данными это открытие не является несовместимым с предыдущими исследованиями. Во-первых, известно, что рибавирин ингибирует как функциональный гуморальный иммунный ответ (Peavy et al, 1981, J Immunol, 126: 861-864, Powers et al, 1982, Antimicrob Agents Chemother 22:108-114), так и IgE-опосредованную модуляцию секреции стволовых клеток (Marquardt et al, 1987, J Pharmacol Exp Therapeutics 240:145-149, (оба случая опосредованы Th2 лимфокинами)). Во-вторых, рибавирин антагонизирует антивирусный эффект азидотимидина (AZT) в лимфоцитах периферической крови ВИЧ пациентов (Vogt et al, 1987, Science 235:1376-1379). Это значительное открытие, потому что AZT уменьшает экспрессию IL-2 рецептора (IL-2R), но не экспрессию IL-2 (Viora and Camponeschi, 1995, Cell Immunol 163:289-295). Таким образом, возможно, что рибавирин является антагонистом AZT, модулируя экспрессию IL-2 и повышая сниженные уровни IL-2R. В-третьих, лечение рибавирином иммунодефицитного пациента с хроническим GVHD (Th-2 -опосредованное заболевание) привело к резкому прекращению заболевания, исходу, который не происходит при общепринятой иммуноподавляющей терапии, например при лечении циклоспорином и глюкокортикоидами (Cassano, 1991, Bone Marrow Transplantation, 7:247-248). Наконец, лечение рибавирином (один год) пациентов с гепатитом С (HCV) выявило меньшее агрегирование лимфоцитов и гораздо меньшее поражение печени, чем при плацебо контроле (Dusheiko et al, 1994, Hepatology, 20:206A). Это наблюдение может отражать тот факт, что хотя доминирующий иммунный ответ на гепатит С опосредуется Th1 лимфокинами, Т клетки фенотипа Th0/Th2 могут быть инфицированы HCV (Zignego et al, 1994, неопубликованные данные) и эта инфекция может привести к дальнейшему опосредованному антителами разрушению гепатоцитов.
Краткое описание чертежей
Таблица 1 представляет уровень покоя и РМА/иономицин-активированный уровень лимфокинов, IL-2, IL-4, TNFα и IFNγ (пг/мл), через 48 и 72 часа, измеренные во внеклеточных супернатантах, и экспрессию на клеточной поверхности IL-2 (IL-2R) и IL-4 (IL-4R) рецепторов (средняя интенсивность канала флюоресценции) в Т клетках человека.
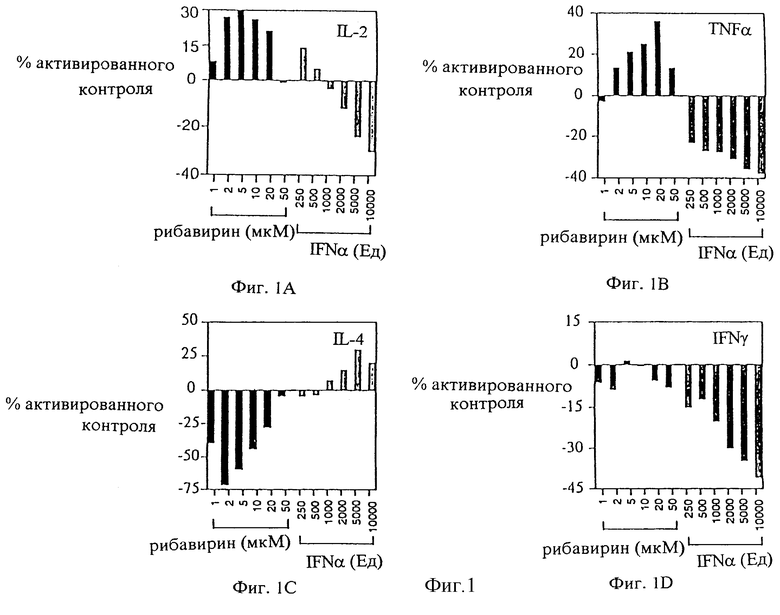
Фиг.1 является графическим представлением влияния рибавирина и интерферона альфа на внеклеточную экспрессию IL-2, IL-4, TNFα и IFNγ в лимфоцитах, активированных РМА/иономицином. Результаты выражены как процент повышенной экспрессии лимфокина, полученной после обработки только РМА/иономицином.
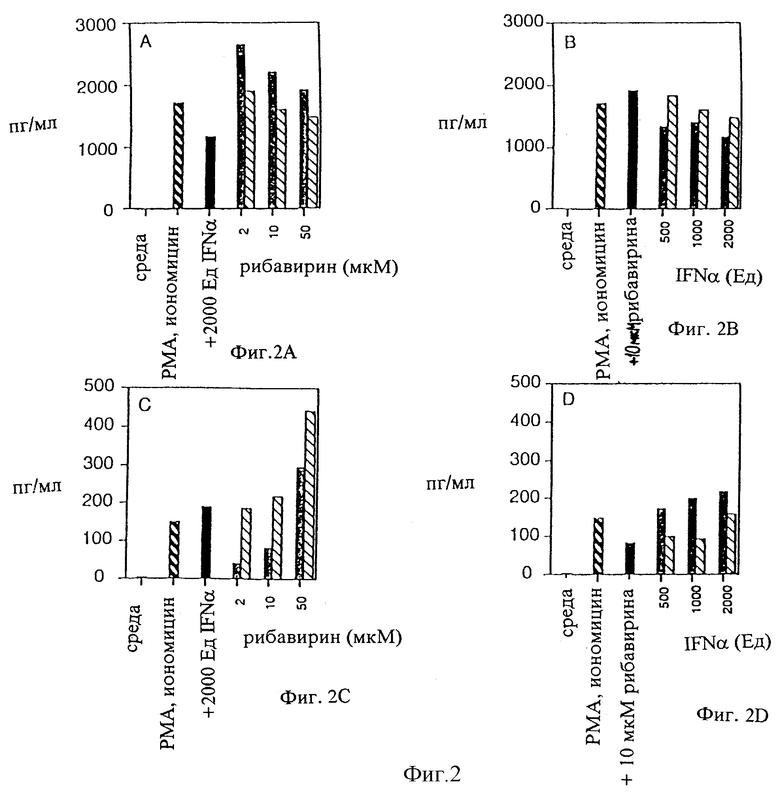
Фиг. 2 является графическим представлением влияния 2, 10 или 50 мкМ рибавирина в присутствии 2000 ЕД/мл интерферона альфа (левая панель) и влияния 500, 1000 или 2000 ЕД/мл интерферона альфа (правая панель) в присутствии 10 мкМ рибавирина на внеклеточную экспрессию IL-2 (А и С) и IL-4 (В и D) Т лимфоцитами, активированными РМА/иономицином.
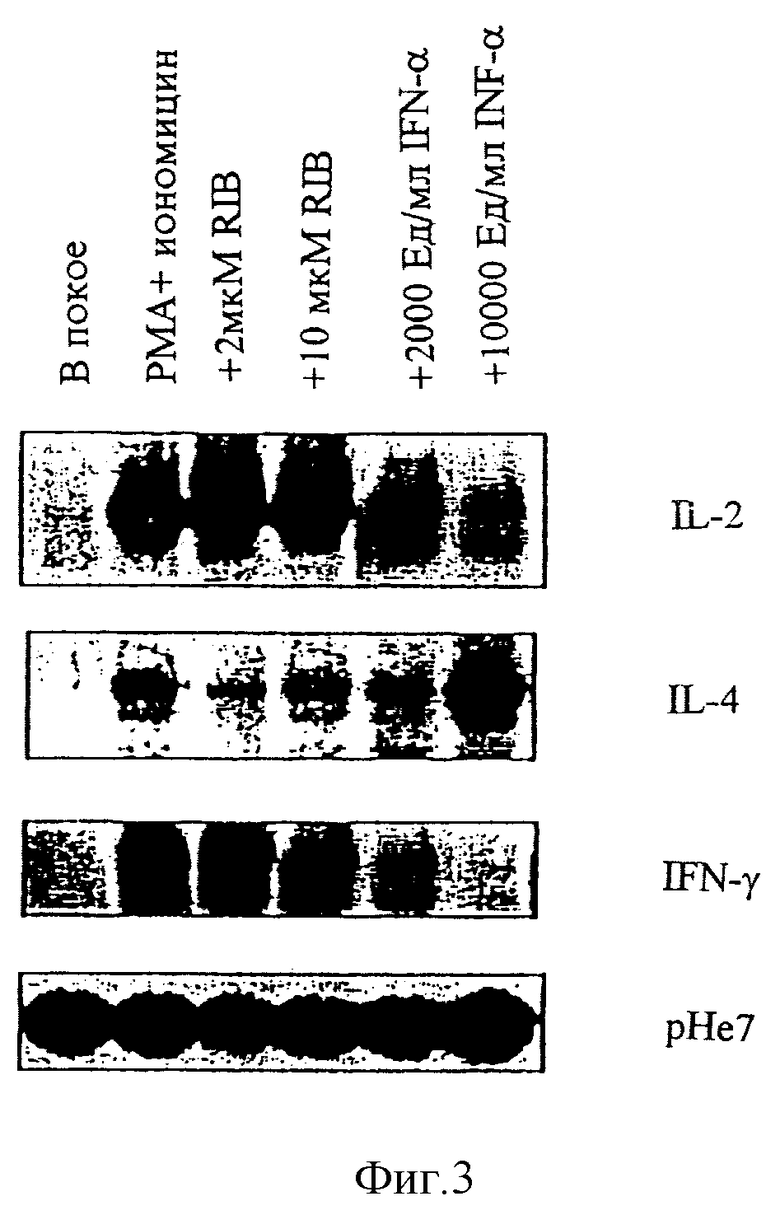
Фиг.3 является графическим представлением влияния рибавирина и интерферона альфа на экспрессию мРНК IL-2, IL-4 и IFNγ Т лимфоцитами, активированными РМ/иономицином.
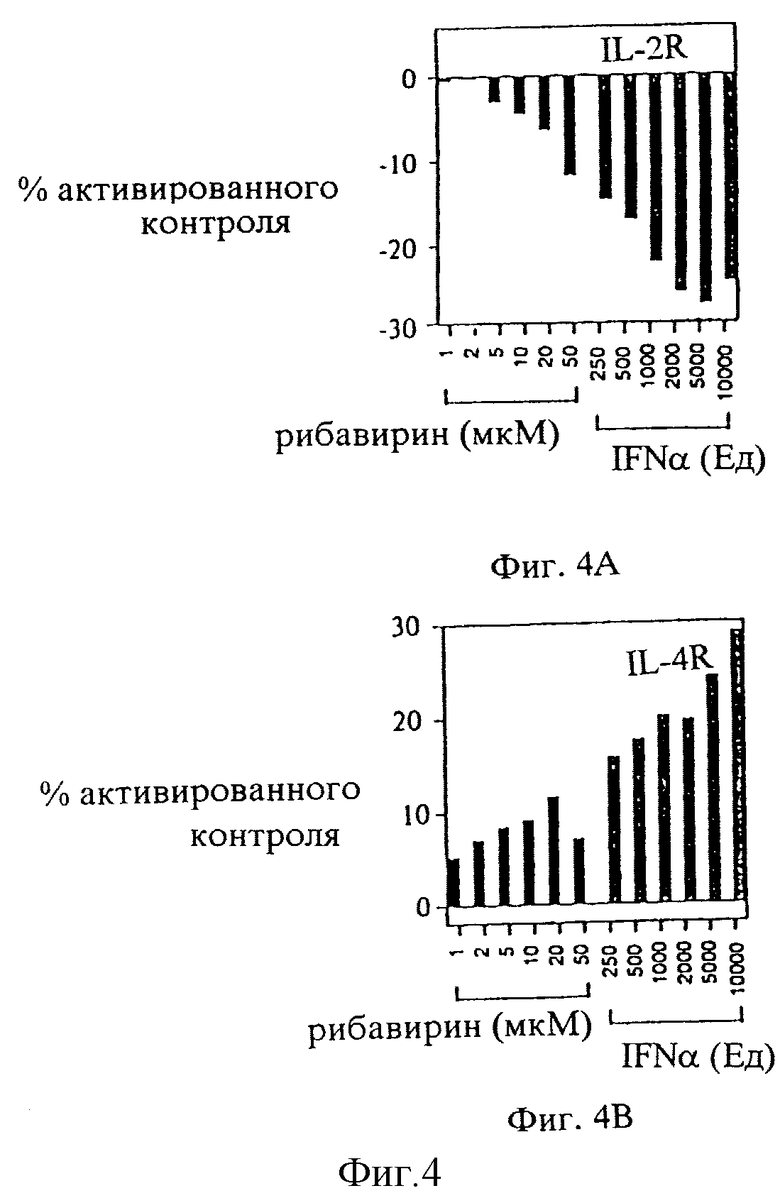
Фиг.4 является графическим представлением влияния рибавирина и интерферона α на экспрессию на клеточной поверхности IL-2 и IL-4 рецепторов Т лимфоцитами, активированными РМА/иономицином. Результаты представлены как процент увеличения экспрессии рецептора лимфокина, полученной после обработки только РМА/иономицином.
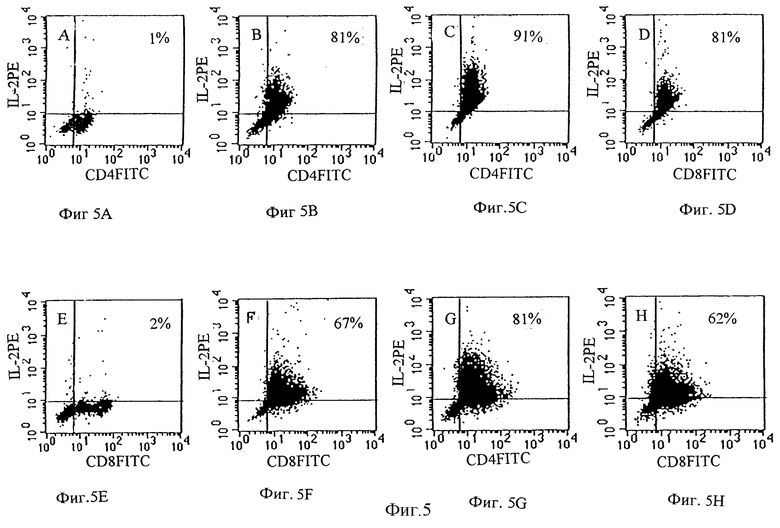
Фиг.5 является графическим представлением выражения внутриклеточной экспрессии IL-2 в покоящихся (А и Е) или активированных CD4+ (верхняя панель) или CD8+ (нижняя панель) Т клетках, обработанных только РМА/иономицином (В и F) или в присутствии 10 мкМ рибавирина (С и G) или 5000 ЕД/мл интерферона альфа (D и Н). Показаны данные одного эксперимента и представлены как процент клеток, демонстрирующих двойное положительное окрашивание на IL-2 и CD4 или CD8.
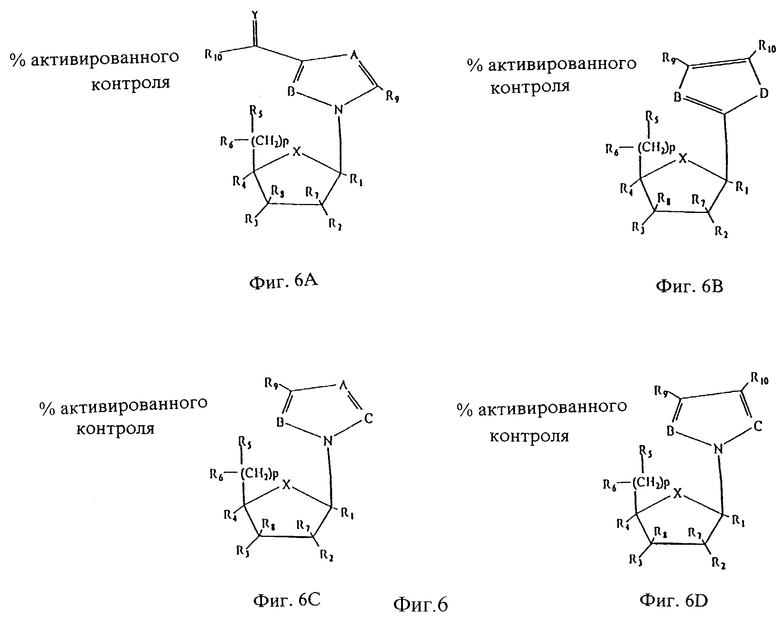
Фиг. 6 является графическим представлением рассматриваемых аналогов рибавирина.
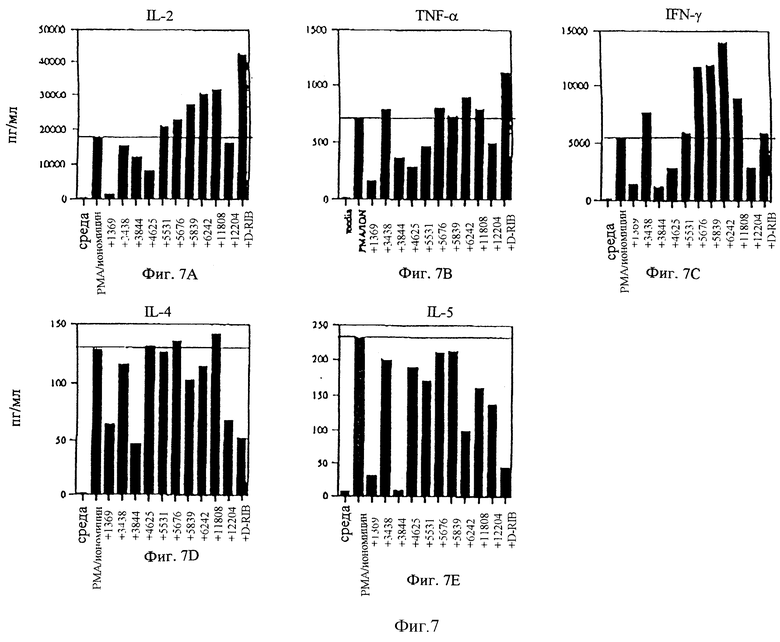
Фиг. 7 является совокупностью графиков, показывающих результаты влияния различных концентраций аналогов рибавирина на IL-2, TNF-α, IFN-γ, IL-4 и IL-5.
Резюме
В соответствии с одним аспектом настоящего изобретения указанный нуклеозид рибавирин вводится пациенту в интервале дозировки, которая является эффективной для модуляции экспрессии лимфокинов в активированных Т клетках. В частности, рибавирин используется для подавления Th-2 опосредованных ответов Т клеток и стимуляции Th-1 опосредованного ответа Т клеток.
Таким образом, вместо введения рибавирина как хорошо признанного антивирусного агента рибавирин здесь используется для лечения дисбалансов экспрессии лимфокинов. Такие дисбалансы могут быть спутниками аллергических атопических нарушений, таких как аллергическая астма и атопический дерматит, гельминтная инфекция и лейшманиоз, и различные первичные и вторичные иммунодефициты, которые могут быть связаны и также не связаны с вирусной инфекцией.
В соответствии с другими аспектами настоящего изобретения, один или более аналогов рибавирина вводится пациенту в интервале дозировки, которая эффективна для модулирования экспрессии лимфокинов в активированных Т клетках. Аналог(и) рибавирина могут быть использованы для подавления или усиления Th1 или Тh2-опосредованных ответов Т клеток.
Подробное описание конкретных воплощений
В предпочтительном воплощении рибавирин вводится орально человеку в дозировке, которая достигает уровня содержания в сыворотке крови в среднем 0,25-12,5 мкМ, а наиболее предпочтительно 2,5 мкМ. У типичных индивидуумов этот оптимальный уровень в сыворотке выражается приблизительно в 4,5 мг/кг/день веса тела, что может быть введено в дозах от 200-1200 мг. Предпочтительно дозировки разделяются на некоторое количество меньших доз, которые затем вводятся в течение всего дня.
Так как рибавирин существует в продаже несколько лет, известно много форм дозировки и путей введения, и все приемлемые формы дозировки и пути введения могут быть использованы. Например, в дополнение к оральному введению рибавирин можно давать внутривенно, внутримышечно, внутрибрюшинно, местно и подобным образом, все эти способы известны. Фармацевтические составы, содержащие рибавирин, могут также содержать один или более фармацевтически, приемлемых носителей, которые могут включать эксципиенты такие как стабилизаторы (для долгосрочного хранения), эмульгаторы, связывающие агенты, загущающие агенты, соли, консерванты, растворители, дисперсионные среды, покрывающие, антибактериальные и антигрибковые агенты, изотонические и замедляющие абсорбцию агенты и подобные. Использование таких сред и агентов для фармацевтически активных составов хорошо известно в мире. За исключением того случая, когда какая-либо общепринятая среда или агент несовместимы с рибавирином, можно предполагать его/ее использование в терапевтических составах и препаратах. Дополнительные активные ингредиенты могут также быть введены в композиции и препараты.
В дополнение к терапевтическим использованиям рибавирина, рассмотренным здесь, рибавирин может также быть использован как лабораторное средство для исследования абсорбции, распределения, клеточного поглощения и эффективности.
Было также открыто, что некоторые аналоги Виразола (ранее известные и неизвестные), которые ранее были отвергнуты как имеющие минимальную активность, также имеют значительную цитокинную активность. Наши исследования показали, что существуют несколько классов аналогов виразола, имеющих такую активность, и примеры даны ниже под заголовком "Аналоги рибавирина". Эти примеры предназначены для характеристики позиций, в которых Виразол может быть модифицирован для получения активных составов, и это описание, таким образом, не должно быть ограничено показанными специфическими модификациями. Далее предполагается, что эти модификации могут быть применены к стандартной D форме Виразола, так же как и к L форме Виразола.
Примеры.
Клеточные линии и очистка Т клеток
Мононуклеарные клетки периферической крови (PBMCs) были выделены из лейкоцитной пленки путем центрифугирования в градиенте плотности Ficoll-Hypaque 60 мл крови от здоровых доноров. Т клетки были затем выделены из PBMCs с применением Lymphokwik реагента выделения лимфоцитов, специфичного для Т клеток (LK-25T, One Lambda, Canoga Park CA). 40-60•106 Т клеток, что составляет средний выход, были затем инкубированы в течение ночи при 37oС в 20-30 мл RPMI-AP5 (RPMI-1640 среда (ICN, Costa Mesa, CA), содержащая 20 мМ HEPES буфера, рН 7,4, 5% исходной плазмы, 1% L-глютамина, 1% пенициллина/стрептомицина и 0,05% 2-меркаптоэтанола) для удаления всех загрязняющих прикрепившихся клеток. Во всех экспериментах Т клетки промывались RPMI-AP5 и затем наносились на 96-луночные микротитрационные планшеты при концентрации клеток 1•106 клеток/мл.
Активирование Т клеток и обработка рибавирином
Т клетки активировались добавлением 500 нг иономицина и 10 нг форбол 12-миристат 13-ацетата (РМА) (Calbiochem, La Jolla, CA) и инкубировались в течение 48-72 часов при 37oС. РМА/иономицин-активированные Т клетки обрабатывались 0,5-5,0 мкМ рибавирина или 250-10000 ЕД/мл контрольного антивирусного интерферона-альфа (Accurate, Westbury, NY) сразу же после активирования и обработка повторялась через 24 часа. Т клетки с каждой чашки использовались для иммунофлюоресцентного анализа и супернатанты использовались для измерений внеклеточных цитокинов. Следом за активацией 900 мкл клеточного супернатанта из каждой микроплаты переносили в другую микроплату для анализа на продукцию цитокинов из клеток. Клетки затем использовались для иммунофлюоресцентного анализа уровней внутриклеточных цитокинов и экспрессии рецепторов цитокинов.
Анализ внеклеточных цитокинов
Концентрации цитокинов из клеток человека определялись в клеточных супернатантах для каждой микроплаты. Вызванные активацией изменения уровней интерлейкина-2 (IL-2) определялись с использованием коммерчески доступного набора ELISA (R& D systems Quantikine kit, Minneapolis, MN) или биотеста с использованием IL-2-зависимой клеточной линии CTLL-2 (АТСС, Rockville, MD). Вызванные активацией изменения уровней интерлейкина-4 (IL-4), фактора некроза опухоли (TNFα), интерлейкина-8 (IL-8) (R & D systems (Quantikine kit, Minneapolis, MN) и интерферона-гамма (IFNγ) (Endogen (Cambrige, MA) определялись с использованием наборов ELISA. Все результаты ELISA выражены в пг/мл, а результаты CTLL-2 биотеста - как подсчет импульсов в минуту, представляющих IL-2 - зависимое клеточное включение 3Н-тимидина (ICN, Costa Mesa, CA) клетками CTLL-2.
Исследование прямой иммунофлюоресценции (рецепторы цитокинов)
Для прямого окрашивания антителами к антигенам клеточной поверхности, связанными с флюоресцентной меткой, клетки дважды промывались изотоническим солевым раствором, рН 7,4 (Becton Dickinson, Mansfield, MA) и ресуспендировались в 50 мл изотонического солевого раствора и разделялись на две пробы. Одна аликвота пробы соокрашивалась либо РЕ-анти СD25/FIТС-анти CD4 или РЕ-крыса анти-мышиными IgG + анти-CDw124/FIТС-анти CD4 моноклональными антителами, и неспецифическая флюоресценция определялась окрашиванием второй аликвоты РЕ/FIТС-меченными подходящими по изотипу контрольными моноклональными антителами. Все меченные флюоресцентной меткой моноклональные антитела были получены от Becton Dickinson (San Jose, CA), кроме aнти-CDwl24, которые были получены от Pharmingen, San Diego, CA. Инкубации проводились при 4oС в темноте в течение 45 минут при насыщающих концентрациях моноклональных антител. Невключенная метка удалялась промыванием PBS перед анализом на FACScan проточном цитометре (Becton Dickinson).
Плотность антигена определялась непрямым методом в пропускаемых живых CD4+T клетках и выражалась как среднее значение канала флюоресценции (MCF). Поверхностная экспрессия специфического антигена (Cdwl24, CD25) выражалась как средний сдвиг канала (MCS), полученный вычитанием MCF клеток, окрашенных контрольными FITC- или РЕ-меченными подходящими по изотипу (IgG1) моноклональными антителами из MCF клеток, окрашенных FITC-или РЕ-меченными антиген-специфичными моноклональными антителами. Альтернативно поверхностная экспрессия СD4+-подгруппы клеток, окрашенных CD28 моноклональными антителами, определялась вычитанием MCF клеток СD28+ CD4+ из MCF клеток CD28- CD4-.
Жизнеспособность контрольных не обработанных и обработанных рибавирином и интерфероном-α клеток определялась в каждой партии всех олигонуклеотидов у многих доноров путем окрашивания прижизненным красителем, пропидиум иодидом (5 мг/мл конечная концентрация). Процент живых клеток, которые не включали пропидиум иодид, определялся проточной цитометрией и составлял > 90% (порядка 90-99%) после обработки всеми используемыми концентрациями.
Иммунофлюоресцентный анализ внутриклеточной экспрессии цитокинов
Для анализа внутриклеточной экспрессии IL-2 в CD4+ и CD8+ подгруппах Т клеток Т клетки были сначала обработаны в течение последних 4 часов из 48-72 часового активирования 10 мг Brefeldin A (Gibco BRL, Gaithersburg, MD) для минимизирования секреции вновь синтезированного IL-2 во внеклеточное пространство. После активирования 900 мл клеточного супернатанта из каждой микроплаты были перенесены в другую микроплату для анализа продукции цитокинов из клеток. Перед прямым окрашиванием (30 мин, 4oС, в темноте) связанными с FITS антителами к антигенам клеточной поверхности, CD4 и CD8, клетки дважды промывали изотоническим солевым раствором, рН 7,4, и ресуспендировали в 100-150 мл окрашивающего буфера (фосфатный солевой буфер, рН 7,4, содержащий 1% фетальной сыворотки теленка (FCS) (Hyclone, Logan, UT) и 0,1% азида натрия) и разделили на две пробы. Окрашенные клетки промывали 1 мл окрашивающего буфера и клеточный осадок ресуспендирован в 100 мл фиксирующего буфера (4% параформальдегида в PBS), за чем следовало удаление супернатанта. Фиксированные клетки выдерживали при 4oС в течение 20 минут, затем промывали в 1 мл окрашивающего буфера и клеточный осадок ресуспендировали перемешиванием в 50 мл пермеабилизирующего буфера (0,1% сапонина (ICN, Costa Mesa, CA) в PBS). Пермеабилизированные клетки окрашивались РЕ-меченными антителами к IL-2 в течение 30 минут при 4oС в темноте и затем промывались в 1 мл пермеабилизирующего буфера, ресуспендировались в 250 мл окрашивающего буфера перед FACS анализом.
Анализ мРНК цитокинов
Общая РНК экстрагировалась из находящихся в покое Т клеток и из обработанных рибавирином и интерфероном-α и необработанных активированных Т клеток с использованием коммерческой разновидности гуанидил тиоцианат/фенол экстрагирующего метода (Trizol reagent (GIBCO/BRL). РНК промывалась 70% этанолом и в конце ресуспендировалась в 10 мкл обработанной DEPC воды.
Реакция синтеза кДНК проводилась, как указано в инструкции производителя (Promega, Madion, WI). Вкратце, 1 мкг общей РНК нагревали при 65oС 10 минут и охлаждали на льду перед смешиванием с 2 мкл 10 кратного буфера обратной транскрипции (100 мМ Трис НС1 (рН 8,8), 500 мМ КС1, 1% Triton X-100), 5 мМ MgCl, 2 мкл 10 мМ dNTPs (1 мМ каждого dNTP), 0,5 мкл ингибитора РНКазы, 1 мкл олиго (dT)15 праймера (0,5 мкг/мкг РНК) и 0,65 мкл AMV обратной транскриптазы (Н.С.) Реакция инкубировалась при 42oС в течение 1 часа, а затем 10 минут при 95oС и 5 мин на льду.
Реакция PCR проводилась с использованием GeneAmp PCR набора (Perkin-Elmer Cetus, Foster City, CA). В новой пробирке RT реакционная смесь (3 мкл) смешивалась с 5 мкл 10 кратного PCR буфера (500 мМ КС1, 100 мМ Трис-HCl, рН 8,3, 15 мМ MgCl2 и 0,01% (вес./об.) желатина), 1 мкл 10 мМ dNTPs и 1 ЕД Taq DNA полимеразы. Использовались следующие праймеры: праймеры интерлейкина-2, интерлейкина-4, интерферона-γ (человека) (Stratagene, La Jolla, CA) и рНЕ7 рибосомальный ген. Условиями амплификации были 45 с при 94oС, 1 мин при 57oС и 2 мин при 72oС для 35 циклов, за чем следовали 8 мин при 72oС. Продукты PCR анализировались на 2% агарозном геле, содержащем этидиум бромид. После электрофореза продукты PCR переносили на Hybond N+ мембрану (Amersham, Arlington Heights, GL) в 20 кратном SSC в течение ночи и иммобилизовывали с помощью 0,4 М NaOH. Блоты гибридизовали с 32P-gATP - меченными пробами нуклеотидов в Rapid-hyb буфере (Amersham) в течение 1 часа при 42oС. Каждая смесь праймеров цитокинов использовалась как проба с радиоактивной меткой (по инструкции). Эквивалентная нагрузка определялась после гибридизации с пробой, образованной рНЕ7 смысловым праймером. Промытые блоты затем анализировались с помощью Phosphorlmager.
Влияние рибавирина на уровни внеклеточных цитокинов в активированных Т клетках
Обработка РМА/иономицином (48-72 часа) Т клеток человека существенно повышает уровни всех анализированных цитокинов т.е. IL-2, IL-4, TNFα, IFNγ (таблица 1) Первая цифра в каждой ячейке указывает арифметическое значение, а числа в скобках обозначают соответствующие диапазоны. N=4. В показательном эксперименте, показанном на фиг. 1, добавление рибавирина в дозовом интервале 0,5-5,0 мкМ увеличивает активированные уровни Тh1 цитокинов, IL-2 и TNFα максимально при 5 мкМ (30%) и 20 мкМ (36%) соответственно. Напротив, интерферон-α ингибирует экспрессию IL-2 и TNFα в зависимости от дозы (интервал 250-10000 ЕД/мл, максимальное ингибирование 33 и 38% соответственно) при сравнении с уровнями в необработанных активированных Т клетках. В дополнение к этому рибавирин опосредует сопутствующее снижение активированных уровней Th2 цитокина, IL-4 (пик ингибирования 74% при 2 мкМ), в то время как интерферон-α максимально увеличивает внеклеточный IL-4 на 26% (10000 ЕД/мл). При использовании комбинаций рибавирина и интерферона альфа, как показано на фиг.2, постоянная концентрация 2000 ЕД/мл интерферона альфа подавляет зависимое от дозы рибавирина увеличение уровней активированного IL-2 (А) и обращает ингибирование уровней активированного IL-4 (С). Сходным образом, постоянная величина 10 мкМ рибавирина обращает опосредованное интерфероном альфа зависимое от дозы ингибирование уровней активированного IL-2 (В) и подавляет увеличение уровней активированного IL-4 (D).
Влияние рибавирина на уровни мРНК цитокинов в активированных Т клетках.
Эти противоположные влияния рибавирина и интерферона-α на уровни активированных внеклеточных цитокинов наблюдались также на уровне транскрипции. На фиг. 3 показано, что обработка РМА/иономицином Т клеток человека значительно увеличивает уровни мРНК IL-2, IL-4 и IFNγ. Обработка рибавирином (2, 5 и 10 мкМ), следующая за активацией Т клеток, повышает IL-2, снижает IL-4 и не влияет на IFNγ мРНК. Напротив, интерферон-α, при 1000, 2000 и 5000 ЕД/мл снижает IL-2, повышает IL-4 и снижает мРНК IFNγ. Таким образом, соответственные зависимые от дозы влияния рибавирина и интерферона-α на экспрессию мРНК IL-2, TNFα и IL-4 соответствовали анализам ELISA. Эти данные предполагают, что рибавирин усиливает синтез Тh1 цитокинов, IL-2 и TNFa ингибирует экспрессию Th2 цитокина, IL-4 в активированных Т клетках человека.
Влияние рибавирина на уровни рецепторов IL-2 и IL-4 в активированных Т клетках.
Используя FACS анализ, авторы сравнили влияния рибавирина и интерферона-α на экспрессию IL-2 (CD25) и экспрессию IL-4 (CDwl24) рецептора в активированных Т клетках. Обработка РМА/иономицином увеличивает экспрессию CD25 и CDwl24 от уровня покоя 50,16±0,45 и 62,31±1,46 до активированных уровней 162,48±2,89 и 87,53±3,98 соответственно (n=4). В представленных трех экспериментах на фиг.4 показано, что рибавирин (1-50 мкМ) слабо влияет на активированные уровни IL-2 и IL-4 рецепторов, в то время как интерферон-α, в дозовом интервале 250-10000 ЕД/мл, уменьшает экспрессию IL-2 рецептора и повышает экспрессию GL-4 рецептора в зависимости от дозы при сравнении с уровнями рецептора в контрольных активированных Т клетках. Таким образом, эти данные показывают, что влияние рибавирина на синтез цитокина существует независимо от экспрессии рецептора цитокина. Напротив, влияние обработки интерфероном-α на IL-2 и IL-4 рецептор коррелирует с тем, что наблюдается при его влиянии на экспрессию активированных IL-2 и IL-4.
Влияние рибавирина на внутриклеточные уровни IL-2 в CD4 и CD8+ подгруппах активированных Т клеток.
Авторы исследовали, является ли влияние рибавирина на экспрессию IL-2 специфичным для CD4- или СD8+ Т клеток. Экспрессия внутриклеточного IL-2 в фиксированных и пермеабилизированных активированных Т клетках определялась с помощью двухцветной проточной флюориметрии с использованием антител к CD4 или CD8 и к IL-2, меченных флюоресцентной меткой. На фиг. 5 показано, что после обработки рибавирином при 10 мкМ процент CD4+ Т клеток, экспрессирующих IL-2, растет с 82 до 91% и процент CD8+, экспрессирующих IL-2, увеличивается с 81 до 91%. Напротив, процент экспрессирующих IL-2 CD4+ и CD8+ клеток после обработки интерфероном-α (5000 ЕД/мл) был 81 и 71% соответственно. Эти данные предполагают, что рибавирин влияет на экспрессию внутриклеточного IL-2, которая не различается между CD4+ и СD8+ подгруппами Т клеток. Напротив, обработка интерфероном-α слабо влияет на CD4+ Т клетки и даже понижает экспрессию IL-2 в CD8+ подгруппе Т клеток.
Аналоги рибавирина.
Существует несколько классов аналогов рибавирина, которые считаются клинически эффективными для модуляции Тh1 или Тh2-опосредованных ответов Т клеток. Они включают молекулы, отвечающие общей формуле фиг.6, где Х представляет собой О, S, CH2, СНОН или N-CO-R11; А, В и С представляют собой независимо N, Р, СН, С-ОН, С-СН3, С-алкил, С-алкенил, C-CH2, -CN, С-галоген, С-CN, С-СООСН3, C-NH2, C-SNH2, C-SO2-NH2, C-CONH2, C-CS-NH2, C-C(NH)NH2, СРО2-NH2, или С-гетероциклическое кольцо; D представляет собой S, Se, Те, РН, NH или NR12; R1 представляет собой Н, (СН2)р(ОН), галоген, CN, (CH2)pONH2, (CH2)pNH2, СН3, CH2SPH или (СН2)-гетероциклическое кольцо; R2 представляет собой Н, ОН, ОСН3, SH, SCH3, галоген, CN, NH2, ONH2, NHСН3, (СН2)ОН, (CH2)pNH2, СН3, СООМе; R3, R4, R5, R6, R7 и R8 являются независимо Н, ОН, ОСН3, SH, SCH, галоген, CN, NН2, ONH2, NHCH3, (СН2)ОН, (CH2)pNH2, СН3, СООМе или фенил; R9 представляет собой Н, галоген, NH2, СН3, CONH, CSNH2, СООМе, SNH2, SONH2, PО2NH2, (СН2)р, (СН2)р-гетероциклическое кольцо или (СН2)р-глюкоза; R10 представляет собой Н, галоген, NH2, СН3, CONH, CSNH2, СООМе, SNH2, SО2NH2, PО2NH2, (СН2)р, (СН2)р-гетероциклическое кольцо,
(СН2)р-глюкоза, О-СН3, О-СН2СН3 или аминокислота; Y представляет собой О, S, NH•HC1, NOH, NOCH3 или NOCH2PH; R10 & Y в комбинации являются гетероциклическими системами, такими как тиазол, имидазол и т.д.; R11 представляет собой СН3(СН2)pNH2, (СН2)р-гетероцикл, (СН2)р-аминокислота или (СН2)р-сахар (глюкоза и т. п.); р представляет собой целое между О и 8; и все вышеизложенное включает как L, так и D нуклеозиды.
Такие молекулы могут быть созданы в соответствии с одной или более чем одной из приведенных ниже примерных схем.
1. Синтез ICN1369 (Пиразомицин): методика синтеза для этого соединения описана в следующих ссылках: (a) J. Farkas, Z. Flegelova and F. Sorm, Tetrahedron Letts, 22, 2279 (1972); (b)S. De Bernardo and M. Weigele, J. Org. Chem. , 41, 287 (1976); (с) J. G. Buchanan, A. Stobie and R.H, Wightrnan, J. Chem. Soc. Chem Commun, 916 (1980); N. Karagiri, К. Takashima, Т. Haneda and T. Kato, J. Chem. Soc. Perkin Trans., 553 (1984).
2. Синтез ICN3438 (1-β-D-ксилофуранозил-1,2,4-триазол-3-карбоксамид): синтез этого соединения выполняют, следуя процедуре, описанной в J.Т. Witkowski, M. Fuertes, P.D. Cook and R.K. Robins. J. Carbohydr. Nucleosides, Nucleotides 2(1), 1 (1975).
3. Синтез ICN3844 (1 (5-О-сульфамоил-β-D-рибофуранозил)-1,2,4-триазол-3-карбоксамид): Данное соединение было приготовлено, следуя процедуре, описанной в G.D. Kini, B.M. Henry, R.K. Robins, S.B. Larson, J.J Marr, R.L. Berens, C.J. Bacchi, H.C. Nathan and S.Keithly, J. Med. Chem., 33, 44 (1990)/
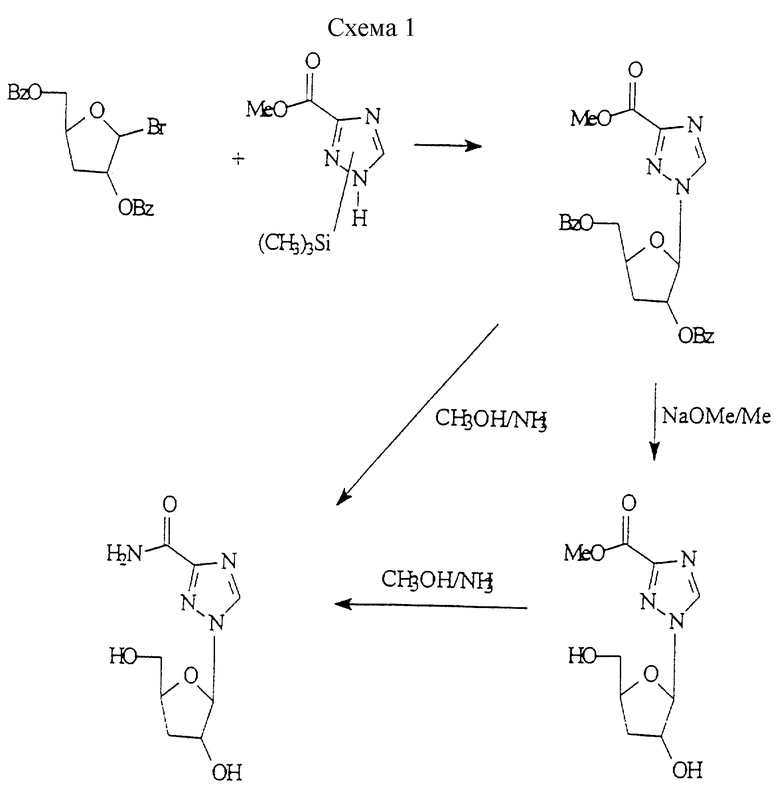
4. Синтез ICN4625 (1 (3-деокси-β-D-эритропентофуранозил)-1,2,4-триазол-3-карбоксамид): Данное соединение приготовлено с использованием метода синтеза, показанного на схеме 1 (см. в конце описания).
См.: J/Med. Chem., 8, 659 (1965)
5. Синтез ICN5531 (5-амино-1-β-D-рибофуранозилпиразол-4-карбоксамид): для получения указанного соединения следовали методологии синтеза, доложенной в B.K.Bhattacharaya, R.K.Robins and G.R. Revankar. J. Heterocyclic Chem. , 21, 795 (1990)
6. Синтез ICN5676 (1-β-D-арабинофуранозил-1,2,4-триазол-3-карбоксамид): синтез этого соединения проводился, следуя процедуре, описанной в J.T. Witkowski, М. Fuefles, P. D. Cook and R.K. Robins. J. Carbohydr. Nucleosides, Nucleotides, 2(1), 1 (1975).
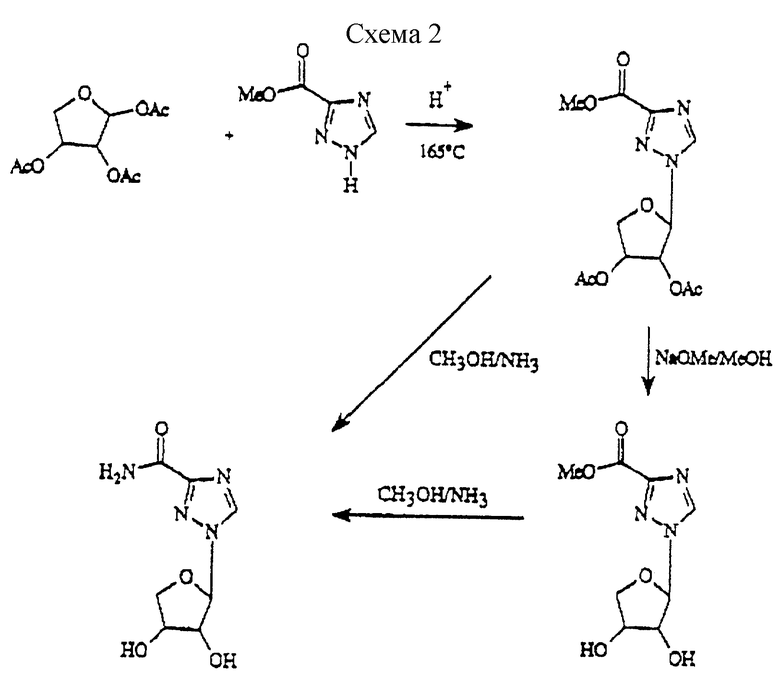
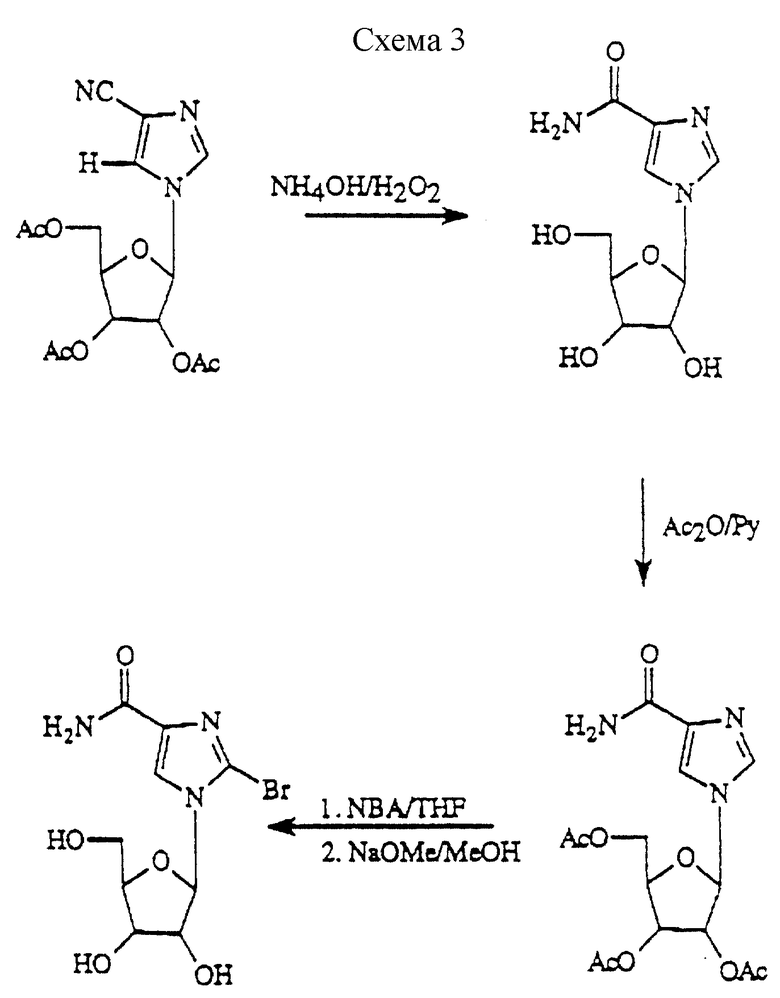
7. Синтез ICN5839 (1-β-D-эритрофуранозил-1,2,4-3-карбоксамид): это соединение было приготовлено с использованием последовательности синтеза, показанной на схеме 2 (см. в конце описания) 8. Синтез ICN6242 (2-бромо-1-β-D-рибофуранозилимидазол-4 карбоксамид): ICN6242 был приготовлен согласно методу, показанному на схеме 3 (см. в конце описания).
См. : Р. С. Srivastava, G.A. Ivanovics, R.J.Rousseau and R.K.Robins, J. Org. Chem., 40, 2920 (1975).
9. Синтез ICN11808 (1-β-D-рибофуранозил-пиразол-3,4-дикарбоксамид): синтез этого соединения описан в Y.S.Sanghvi, В.К. Bhattacharaya, G.D. Kini, S.S. Matsumoto, S.B. Larson, W.J. Jolley, R.K. Robins and G. R. Revankar, J. Med. Chem., 33, 336 (1990), и соединение было приготовлено в соответствии с этим.
10. Синтез ICN 12204 (2-β-D-рибофуранозил)имидазол-5-карбоксамид): синтез этого соединения был проведен, следуя процедуре, описанной в J. Igoleo, Т.Н. Dinh, A. Keib and С. Perreur, Chimie Therapeutique, 207 (1972).
Для карбоциклических производных 4'-тиосахара и 4'-азасахара аналогов рибавирина следующие сахара могли бы быть конденсированы с подходящими гетероциклическими соединениями и получены производные, как описано в вышеприведенных схемах и ссылках.

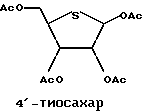

1. Карбоциклические сахара могут быть получены, следуя описанной в литературе процедуре: М. Yoshikawa, Y. Yoshikawa, Y. Inoue, S. Yamaguchi and N. Murakami, Tetrahedron, 50, 9961(1994); L. Agrofoglio, E. Suhas, A. Parese, R. Condom, S.R. Challand, R. A. Earl and R. Guedj, Tetrahedron, 50, 10611 (1994).
2. Указанный 4'-азасахар был получен по описанной в литературе процедуре: E. J. Reist, D.E. Gueffroy and L.Goodman, J.Am. Chem. Soc., 87, 677 (1965).
3. Указанная 4'-тио-D-рибофураноза была получена, следуя описанной в литературе процедуре: М. Hobek and R.L. Whistler в "Methods in Carbohydrate Chemistry", Vol. 1.292 (1962).
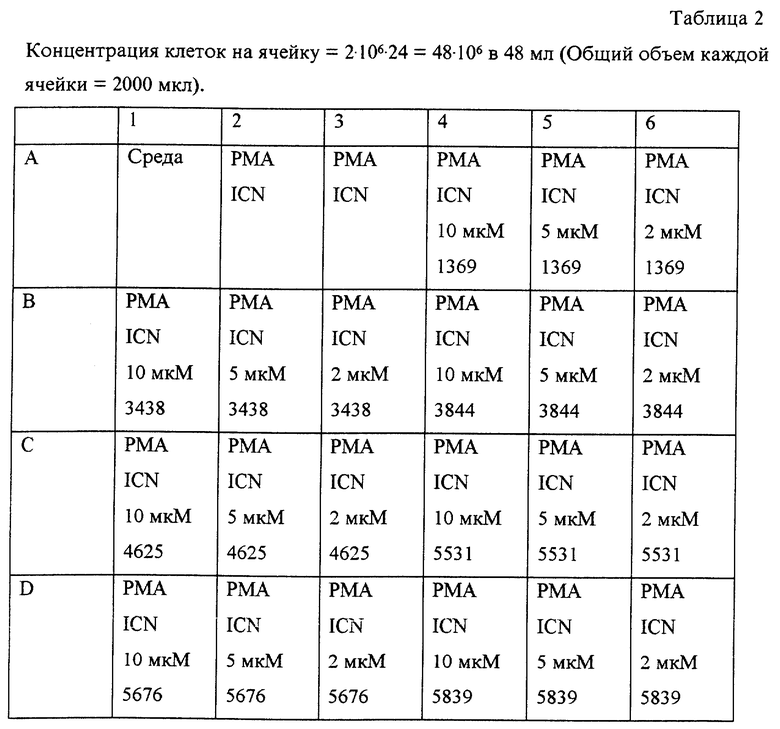
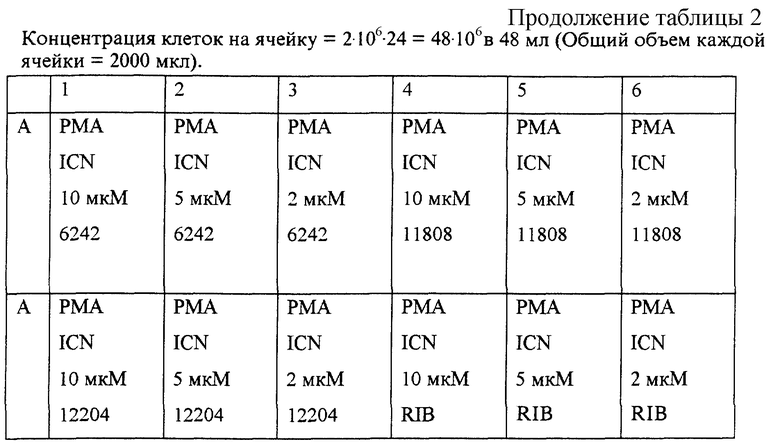
Доказательство эффективности аналогов рибавирина в модулировании Th1 и Th2 цитокинов изложено на фиг. 7 и в таблице 2. Испытания, приведенные здесь, включают короткий список из 35 аналогов тестированных аналогов рибавирина и все испытания проводились три раза. В общем, можно видеть, что тестированные соединения разделяются на три больших категории: (I) соединения, такие как ICN1369 и ICN3844, подавляющие IFNγ, IL-2, IL-4, IL-S и TNFα; (2) соединения, такие как рибавирин, который повышает IL-2 и TNFα и подавляет ILA и IL-5; и (3) соединения, такие как ICN6242, ICN3839 и ICN3531, которые повышают IL-2 IFNγ и подавляют IL-4 и IL-5. Такие активности, перечисленные выше, были бы потенциально пригодны для определения, в котором модуляция цитокинов оказывала бы соответствующий иммунный ответ.
Таким образом, было показано, что рибавирин и аналоги рибавирина эффективны для модифицирования экспрессии лимфокинов в активированных Т клетках. В то время как специфические воплощения и приложения были приведены, должно быть очевидно для квалифицированных специалистов, что гораздо больше модификаций возможно без отрыва от приведенных здесь концепций изобретения. Изобретение, таким образом, не должно быть ограничено только сущностью прилагаемой формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| МОДУЛЯЦИЯ ИММУННОГО ОТВЕТА С ПОМОЩЬЮ РИБАВИРИНА | 1999 |
|
RU2211698C2 |
| ПУРИНОВЫЕ L-НУКЛЕОЗИДЫ, ИХ АНАЛОГИ И ПРИМЕНЕНИЕ | 1997 |
|
RU2183639C2 |
| МОНОЦИКЛИЧЕСКИЕ L-НУКЛЕОЗИДЫ, ИХ АНАЛОГИ И ПРИМЕНЕНИЯ | 1997 |
|
RU2188828C2 |
| СПОСОБ ДИАГНОСТИКИ АЛЛЕРГИЧЕСКИХ РЕАКЦИЙ | 2009 |
|
RU2536291C2 |
| ЛЕЧЕНИЕ АУТОИММУННОГО ЗАБОЛЕВАНИЯ ПУТЕМ МОДУЛИРОВАНИЯ АКТИВНОСТИ АННЕКСИНА-1 (ЛИПОКОРТИНА-1) | 2009 |
|
RU2554801C2 |
| РЕКОМБИНАНТНЫЙ ХИМЕРНЫЙ БЕЛОК ANTH1, КОДИРУЮЩАЯ ЕГО НУКЛЕИНОВАЯ КИСЛОТА И ИХ ПРИМЕНЕНИЕ | 2003 |
|
RU2322455C2 |
| НУКЛЕИНОВЫЕ КИСЛОТЫ, МОДИФИЦИРОВАННЫЕ АМИНОКИСЛОТАМИ | 1995 |
|
RU2154638C2 |
| СПОСОБ ДИАГНОСТИКИ, ЛЕЧЕНИЯ И ПРОГНОЗА ДЛЯ СОЛИДНЫХ НЕЛИМФОИДНЫХ ОПУХОЛЕЙ И ИХ МЕТАСТАЗОВ | 1994 |
|
RU2144675C1 |
| СПОСОБ УСИЛЕНИЯ ИММУННОГО ОТВЕТА НА АНТИГЕН У МЛЕКОПИТАЮЩИХ | 2004 |
|
RU2341289C2 |
| ЭКСПРЕСС-АНАЛИЗЫ АКТИВАЦИИ Т-КЛЕТОК, ОСНОВАННЫЕ НА ИЗМЕРЕНИИ РНК С ИСПОЛЬЗОВАНИЕМ ПРОТОЧНОЙ ЦИТОМЕТРИИ | 2013 |
|
RU2671707C2 |

Изобретение относится к иммунологии и касается модуляции экспрессии TH1/TH2 цитокинов рибавирином и аналогами рибавирина в активированных Т-лимфоцитах. Сущность изобретения включает экспрессию Th1/Th2 лимфокинов в Т клетках пациента человека рибавирином, добавляемых к клеткам в дозировке, которая стимулирует экспрессию одного из лимфокинов TNFα, IL2 и IFNγ и подавляет экспрессию Th2 лимфокина IL-4. Преимущество изобретения заключается в разработке способа модуляции лимфокином, т.е. к усилению Th1 ответа при одновременной реверсии Th2 фенотина и наоборот. 7 з.п.ф-лы, 7 ил., 2 табл.
Приоритет по пунктам:
23.01.1996 - по пп.1-7;
14.01.1997 - по п.8.
| УСТАНОВКА ДЛЯ ПРИГОТОВЛЕНИЯ СУХОГО ПОРОШКА ИЗ ГЛИНЯНОЙ МАССЫ | 0 |
|
SU346132A1 |
| EP 0623348 A1, 09.11.1994 | |||
| US 5290540 A, 01.03.1994 | |||
| Дыхательный клапан | 1978 |
|
SU707855A1 |
| МАШКОВСКИЙ М.Д | |||
| Лекарственные средства | |||
| - М.: Медицина, 1993, ч.11, с.393-394 | |||
| БОГДАНОВИЧ Л.Н., МАТВЕЕВ В.А., МАРТОВА Т.В | |||
| Лечение виролексом тяжелой формы ветряной оспы у детей с иммунодефицитным состоянием | |||
| - Здравоохранение Белоруссии, 1991, № 8, с.38-39 | |||
| PAWLOTSKY J.M., MARCELLIN, P.TREPO C., DHUMEAUX D., Treatment of viral hepatis C., Gastroenterol | |||
| Clin | |||
| Biol., 1994, v | |||
| Способ использования делительного аппарата ровничных (чесальных) машин, предназначенных для мериносовой шерсти, с целью переработки на них грубых шерстей | 1921 |
|
SU18A1 |
Авторы
Даты
2002-08-10—Публикация
1997-01-21—Подача