Изобретение относится к области химической технологии, в частности извлечению йода из буровых вод. Йод находит широкое применение в медицине, сельском хозяйстве, в качестве промежуточного продукта в органическом синтезе.
Содержание йодида в гидроминеральном сырье Российской Федерации (подземные буровые воды, попутные воды нефтедобычи) составляет 10-60 мг/дм3. При извлечении йодида из указанного сырья последний, как правило, окисляют до свободного состояния.
Известен способ извлечения йода из рассола путем окисления йодида хлором с последующей отдувкой йода воздухом [1]. Хлор берут с избытком от стехиометрии.
Недостатком способа является невозможность избежать побочной реакции, что снижает степень извлечения йода (85-87%) из-за переокисления йодида до йодата в присутствии избыточного количества хлора. Кроме того, применение токсичного хлора представляет экологическую опасность.
Известен способ извлечения йода из кислых промышленных растворов окислением пероксидом водорода и экстракцией трибу -тилфосфатом [2]. Извлечение йода составляет ~99%.
Недостатком способа является взрывоопасность пероксида водорода, его высокая стоимость, способность разлагаться при хранении.
Известно применение озона в качестве окислителя для выделения элементарного йода из буровых вод [3, 4]. В слабокислой среде (кислотность 1-3 мг-экв/л) и при насыщении буровой воды СО2 удается окислять 79-84% содержащегося в ней йодида. При этом для получения йода из щелочных вод через определенный объем йодсодержащей буровой воды пропускают озон в таком количестве, чтобы все йодид-ионы окислились до йодат-ионов (IcO3 -). После этого раствор подкисляют серной кислотой и к нему добавляют 4-5 таких же объемов неокисленной исходной буровой воды. Йод выделяется вследствие реакции йодида с йодатом. Выход свободного йода составляет 96%.
Недостатком способа является побочное окисление бромида, особенно в буровых водах, в которых содержание бромида значительно превосходит содержание йодида [5]
2Вr-+О3+Н2О-->Вr2+ОН-+О2/
Это приводит к загрязнению йодсодержащих концентратов элементарным бромом и переокислению йодида до йодата.
Проведенное нами окисление по описанному выше способу природной буровой воды озоновоздушной смесью (пример 7) подтвердили невысокую селективность процесса, так как в окисленной воде обнаружен элементарный бром, что крайне нежелательно.
Наиболее близким техническим решением является способ получения йода путем окисления раствора йодида аммония кислородом или кислородсодержащим газом в присутствии соединений металлов переменной валентности (Fе, Со, Ni, Cr, Мо, W, Cu, Ag, V) и слабой кислоты [6]. Количество применяемого соединения переходного металла 3•10-4-0,3 мол. на 100 г воды. Реакцию проводят при 20-100oС и парциальном давлении кислорода 0,2-10 кг/см2. Концентрация NН4I в реакционной смеси составляет 10-200 г на 100 г воды. Выход йода 70%.
Недостатком прототипа является невозможность извлечения данным способом йода из природного гидроминерального сырья, где содержание йодида значительно ниже (10-60 мг/дм3)(пример 8).
Задачей изобретения является разработка способа извлечения йода из йодбромсодержащих буровых вод с низкими концентрациями йодида.
Поставленная задача достигается путем обработки предварительно подкисленного гидроминерального сырья воздухом с инициатором озоном в присутствии соли железа (II), как стабилизатора йода, в жидкой фазе.
Используемый для окисления воздух содержит озон в количестве 0,5-1,1 мг/л. Уменьшение концентрации озона ниже 0,5 мг/л заметно понижает степень окисления йодида, в то время как повышение его концентрации выше 1,1 мг/л экономически нецелесообразно.
Окисление ведут в присутствии соли железа (II), которую добавляют в гидроминеральное сырье в виде 10-15%-ного водного раствора, соль железа добавляют в количестве 0,4-0,6 вес.ч. на 1 вес.ч. йодида. При величине добавки Fе2+ менее 0,4 вес. ч. степень окисления йодида понижается и одновременно ухудшается селективность процесса. Увеличение количества добавки Fе2+ более 0,6 вес.ч. экономически нецелесообразно.
Продолжительность процесса окисления составляет 2-5 мин в зависимости от требуемой степени окисления йодида.
В работе использовали природную буровую воду Оверятского участка Краснокамского месторождения, содержащую (мг/л): йодида - 10, бромида - 750; общая минерализация до 270 г/л. Также использовали искусственно приготовленную воду, аналогичную по солевому составу некоторым попутным водам газо- и нефтедобычи, содержащую (мг/л): йодида - 50, бромида - 150 при обшей минерализации до 50 г/л.
Окисление гидроминерального сырья проводили в стеклянном цилиндрическом реакторе диаметром 55 мм с насадкой из стеклянных капилляров высотой 100 см. Реактор имеет днище с отверстиями для подачи воздуха с инициатором и отвода окисленной воды, а также крышку с отверстиями для подачи буровой воды и вывода газа.
Отбор проб окисленной буровой воды для анализе на содержание йода и брома производили по истечении 10-15 мин от начала опыта, что является достаточным для установления равновесия в системе при изменении режима питания колонны. Йод и бром в буровых водах анализировали путем извлечения их хлороформом и титрования хлороформенной вытяжки раствором тиосульфата натрия в присутствии муравьиной кислоты, которая восстанавливает бром и не реагирует с йодом, что позволяет провести раздельное определение йода и брома при их совместном присутствии [7]. Для определения йодида и йодата пробу перед экстракцией хлороформом обрабатывают соответствующими реагентами (азотистокислым или сернистокислым натрием) для перевода связанных форм йода в свободное состояние [8].
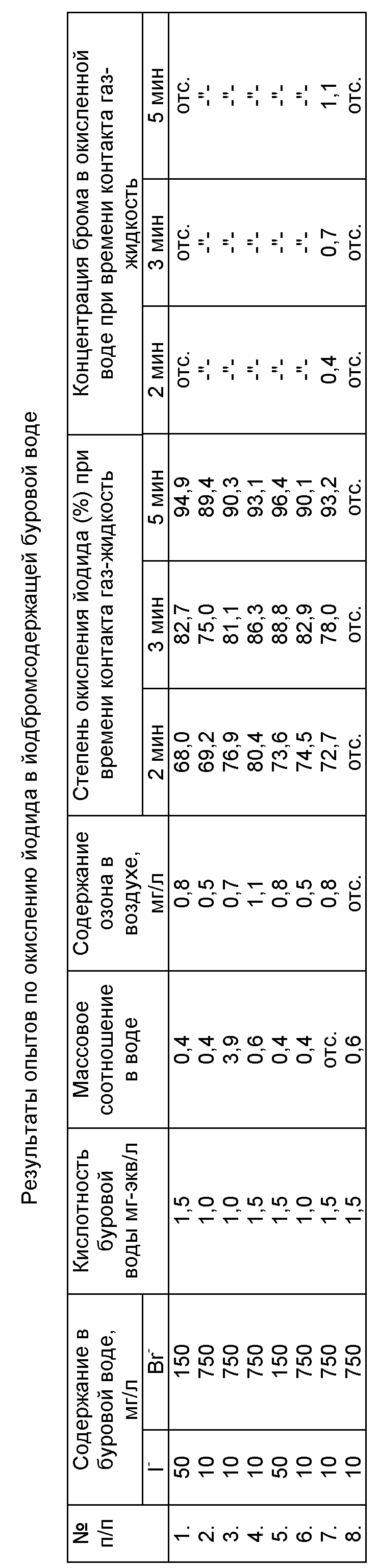
Результаты опытов представлены в таблице, из которой следует, что степень извлечения йода из буровых вод составляет 70-95%, при этом бром в окисленной воде отсутствует. В разработанном способе используется экологически безопасный окислитель - воздух с незначительным содержанием озона, что позволяет вести выделение элементарного йода с минимальными затратами.
Таким образом, способ характеризуется высокой эффективностью и селективностью окисления йодида в природном гидроминеральном сырье с широким диапазоном содержания йодида и бромида и позволяет организовать промышленное производство йода по экологически безопасной технологии.
Отличительным признаком предлагаемого способа является использование озона в качестве инициатора окисления йодида в буровой воде воздухом. Данный признак, отличающий заявленный способ от прототипа, не выявлен в других технических решениях, касающихся окисления галогенидов в жидких средах.
Следующие примеры иллюстрируют сущность изобретения.
Пример 1. Реактор заполняют на высоту насадки предварительно подкисленной до свободной кислотности 1,0 мг-экв/л буровой водой, содержащей 50 мг/л йодида и 150 мг/л бромида, а также добавку хлористого железа в количестве 1 г FеСl2 на 1 г I-(0,4 г Fе2+ на 1 г I-).
С помощью вакуума через реактор снизу вверх начинают пропускать со скоростью 0,1 л/л•мин воздух, содержащий 0,3 мг/л озона. Затем начинают подачу подкисленной буровой воды вышеуказанного состава и вывод окисленной воды из реактора.
По результатам химанализа образцов окисленной воды вычислили значения степени окисления йодида при времени контакта фаз 2, 3 и 5 мин, соответственно составившие (%): 68,0; 82,7 и 94,9. Элементарного брома в окисленной воде не обнаружено.
Последующие опыты по окислению йодида (примеры 2-6) выполнены аналогично примеру 1. Условия окисления йодида и полученные результаты приведены в таблице.
Источники информации
1. Ксензенко В.И., Стасиневич Д.С. // Химия и технология брома, йода и их соединений. М.: Химия, 1995, с.300-304.
2. Авт. свид. 1161459, C 01 B 7/13, опубл. 15.06.85, БИ 22.
3. Ксензенко В.И., Стасиневич Д.С. // Химия и технология брома, йода и их соединений. М.: Химия, 1995, с.300.
4. Авт. свид. РФ 66684, 12i9, заявл. 18.05.45.
5. Каут В. М. , Гобов С.Л., Чусова Л.Л. // Вопросы химии и химической технологии. 1983, 70, с.88-91.
6. Патент США 4487752, C 01 B 7/14, опубл. 11.12.84, РЖХ 1985, 18Л29П (прототип).
7. Шарло Г. // Методы аналитической химии. М.: Химия, 1965, с.890.
8. Методика 339-01-90. Определение массовой концентрации йода в буровой воде. Пермь, Йодобром. 1990.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ВЫДЕЛЕНИЯ ЙОДА ИЗ ПРИРОДНОГО ЙОДСОДЕРЖАЩЕГО РАСТВОРА И ЙОДНЫЙ ПРЕПАРАТ | 2001 |
|
RU2194021C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ЙОДА ИЗ МИНЕРАЛЬНЫХ ИСТОЧНИКОВ | 2012 |
|
RU2481266C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЙОДА ИЗ МИНЕРАЛИЗОВАННЫХ ПРИРОДНЫХ ВОД | 2021 |
|
RU2782603C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЙОДАТА КАЛИЯ (ВАРИАНТЫ) | 2002 |
|
RU2210533C1 |
| СПОСОБ ВЫДЕЛЕНИЯ ЙОДА РЕАКТИВНОЙ КВАЛИФИКАЦИИ ИЗ ПРИРОДНОГО ЙОДСОДЕРЖАЩЕГО РАСТВОРА И ЙОДНЫЙ КРИСТАЛЛИЧЕСКИЙ ПРЕПАРАТ НА ОСНОВЕ ЭТОГО ЙОДА | 2002 |
|
RU2210548C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ 1,5-ДИАЗОБИЦИКЛО-(3.1.0)-ГЕКСАНА В ВОДНЫХ РАСТВОРАХ | 1996 |
|
RU2102727C1 |
| СПОСОБ КОМПЛЕКСНОЙ ПЕРЕРАБОТКИ ГИДРОМИНЕРАЛЬНОГО СЫРЬЯ | 1997 |
|
RU2132819C1 |
| Способ получения иодата калия из иодида калия | 2022 |
|
RU2780562C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ 1,5-ДИАЗОБИЦИКЛО-(3.1.0)-ГЕКСАНА В ПОЧВАХ | 1996 |
|
RU2102728C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ЙОДА | 1995 |
|
RU2112080C1 |
Изобретение относится к области технологии получения йода из буровых вод. Йод извлекают путем обработки предварительно подкисленного гидроминерального сырья воздухом, содержащим инициатор окисления озон, в присутствии соли железа (II). Концентрация озона в воздухе 0,5-1,1 мг/л. Способ характеризуется степенью окисления йодида 70-95% при высокой селективности процесса и позволяет извлекать йод из йодсодержащих буровых вод с низкими концентрациями йодида. 1 табл.
Способ извлечения йода, заключающийся в окислении водных растворов йодидов воздухом в кислой среде, содержащей соли железа (II), отличающийся тем, что окисление проводят в присутствии озона в количестве 0,5-1,1 мг/л воздуха.
| US 4487752 A, 11.12.1984 | |||
| КСЕНЗЕНКО В.И | |||
| и др | |||
| Химия и технология брома и йода и их соединений | |||
| - М.: Химия, 1995, с | |||
| Машина для добывания торфа и т.п. | 1922 |
|
SU22A1 |
| Способ получения закиси азота | 1983 |
|
SU1097556A1 |
| Способ получения закиси азота | 1989 |
|
SU1675202A1 |
| СПОСОБ КОМПЛЕКСНОЙ ПЕРЕРАБОТКИ ГИДРОМИНЕРАЛЬНОГО СЫРЬЯ | 1997 |
|
RU2132819C1 |
| GB 1591952 A, 01.07.1981 | |||
| АВТОМАТИЧЕСКИЙ МОСТ ПЕРЕМЕННОГО ТОКА С ЭКСТРЕМАЛЬНЫМ УРАВНОВЕШИВАНИЕМ | 0 |
|
SU218998A1 |
Авторы
Даты
2002-08-10—Публикация
1999-12-20—Подача