Изобретение относится к способу получения коллагена, включающему стадию стерилизации указанного коллагена, к полученному таким образом стерильному коллагену, к композициям и применению, в частности к фармацевтическим и/или парафармацевтическим, и/или медико-хирургическим, и/или офтальмологическим, и/или косметическим композициям и к применению последних.
Коллаген и его применения в целом были описаны в работах, приводимых в качестве ссылок, таких как, например, Collagen, Vol. 1,2,3 Marcel E. Nimni., CRC Press Inc., 1988, и Methods in Enzymology, Vol. 144, 1987, and Vol. 82, 1982, Ed. Leon W. Gunningham.
Хорошо известно, что коллаген представляет собой молекулу с трехмерной структурой, которая присутствует в большинстве тканей человека и животных и обнаруживается, в частности, в коже, сухожилиях и плаценте.
Среди его различных известных свойств имеются, между прочих, свойства увлажнения, свертывания крови и заживления ран.
Для сохранения кровоостанавливающего действия коллагена в целом желательно сохранить его нативную форму перед введением в организм человека, как указывается, например, в документе US-A-4515637.
Кроме того, ввиду сфер применения коллагена, в частности в медицине и/или в косметике, он должен быть лишен каких-либо загрязнений (вирусов, бактерий, прионов и т.д.). Стерилизация коллагена разнообразно исследовалась в предшествующем уровне техники, которая, вследствие естественного происхождения коллагена, в течение нескольких лет столкнулась с новыми проблемами (риск передачи СПИДа, болезни Крейцфельда - Якоба и т.д.).
Методики стерилизации коллагена в твердой форме включают применение этиленоксида в соответствии, в частности, с документом FR-A-2393581, или облучения (использование бета- или гамма- ионизирующей радиации), как описано, например, в документе ЕР-А-0224453. В последнем из указанных документов, в котором описаны косметическая и фармацевтическая сферы применения типа губки на основе коллагена, рекомендуется стерилизация в сухой форме ввиду невозможности, в соответствии с этим документом, стерилизации растворимого естественного коллагена, включенного в эмульсии или растворы.
В документе ЕР-А-0664132 описывается клеевая композиция для применения в хирургии, основанная на коллагене без поперечной сшивки, модифицированном окислительным расщеплением. Один предпочтительный вариант реализации композиции, описанной в этом документе, состоит в получении с помощью окислительного расщепления стерильного порошка коллагена I типа без поперечной сшивки (лакуна) и в растворении этого порошка в стерильной, подвергнутой ультрафильтрации воде путем нагревания приблизительно до 60oС при перемешивании. Указано, что ввиду проводимого контролируемого нагревания, коллаген теряет свою спиральную структуру и трансформируется в желатин. Кроме того, объясняется, что с клеевыми композициями, представляющими предшествующий уровень техники в этом документе, которые основаны на поперечно сшитом коллагене, нелегко обращаться, и это связано с проблемами их нанесения на склеиваемые поверхности и механической прочности.
В документе ЕР-А-0667352 описана щелочная обработка, используемая по отношению к коллагену в растворе, с целью устранения возможных прионов. Для того, чтобы избежать весь риск остаточного загрязнения указанными прионами, в этом документе, в частности, приводится способ, состоящий в солюбилизации экстрагированного из ткани коллагена или с помощью ферментативной обработки, или с помощью щелочного расщепления ковалентных связей, которые обеспечивают взаимосвязь между цепями коллагена, а затем в удалении фрагментов ткани с помощью фильтрации и воздействия на солюбилизированный таким образом коллаген щелочной обработки.
В документе FR-A-2586703 приводится способ получения прозрачных и физиологичных гелей или растворов коллагена, основанных на коллагене IV типа. Однако указывается, что поскольку коллагены I, II или III типа практически нерастворимы при нейтральном рН, они позволяют получать лишь непрозрачные суспензии, и что невозможно их применять для получения прозрачных и физиологичных гелей без того, чтобы не прибегнуть к химической модификации молекул коллагена, что может вероятно сделать их антигенными и/или токсичными.
Знание предшествующего уровня техники и исследование в ходе научно-исследовательской работы позволило автору настоящего изобретения продемонстрировать следующие трудности и проблемы, которые еще остаются до настоящего времени в получении стерильного нативного коллагена, в частности, I типа:
* Обращение
- Высокая вязкость нативного коллагена, которая вносит технические ограничения в проведение процедур фильтрации, в частности в процедуры прямой фильтрации обычного нативного коллагена в жидкой среде.
* Денатурация
- Частичная или полная тепловая денатурация нативного коллагена во время различных обычно применяемых способов стерилизующей обработки, которая вызывает потерю всей или части его структуры и/или его благоприятных свойств, таких как, например, резорбция, механическая прочность или увлажнение.
- Стерилизация облучением (ионизирующим излучением) или этиленоксидом, которая вызывает разрушение благоприятных активных составных частей, которые предстоит комбинировать в растворе с коллагеном, таких как, например, антибиотики, и/или которая приводит к разделению обычного геля, основанного на нативном коллагене, на две фазы, делая его непригодным для коммерческого применения.
- Денатурация под воздействием длительной щелочной обработки.
* Токсичность и/или загрязнение (вирусы, прионы)
- Присутствие следовых количество остаточного этиленоксида в продуктах, стерилизованных с помощью этих средств, присутствие примесей в необработанном исходном коллагене.
* Несовместимость
- Несовместимость между рН благоприятных активных составных частей, которые растворимы при нейтральном рН, таких как, например, противоинфекционные средства, и рН коллагена, который растворим в кислой среде.
* Галеновая композиция
- Неудовлетворительная форма, в которой представлены препараты, основанные на нативном коллагене, которые имеют волокнистый и неоднородный внешний вид.
- Форма, в которой представлены обычные препараты биологического клея, неприемлемая для предполагаемых видов их применения (например, такие как препараты, которые не готовы для применения и которые требуют слишком длительного времени подготовки).
Таким образом, целью настоящего изобретения является преодоление указанных выше трудностей и разрешение упомянутых выше проблем, в частности стерилизации коллагена в жидкой среде, сохраняя в то же самое время его нативную форму, и другие проблемы, которые будут изложены ниже.
Таким образом, предметом настоящего изобретения является способ получения коллагена в нативной форме, включающий этап предварительной обработки коллагена в смесителе с двойными поперечными резцами, который оборудован устройством регулирования скорости перемешивания и скорости сдвига, и термостатом, и последующий этап стерилизации коллагена в жидкой среде.
Предметом настоящего изобретения является также стерильный коллаген, в частности коллаген преимущественно I типа, в нативной форме и композиции для применения у людей и/или в ветеринарии, которые содержат его в качестве единственной активной составной части или в которых он комбинируется с другими веществами, которые предпочтительно приемлемы с фармацевтической, парафармацевтической, медико-хирургической и/или офтальмологической, и/или косметической точки зрения.
Предметом изобретения является также применение коллагена в соответствии с изобретением в производстве композиции, предназначенной для фармацевтического и/или парафармацевтического, и/или медико-хирургического, и/или офтальмологического, и/или косметического лечения организма человека или животного.
Эти и другие предметы станут очевидными для специалистов по прочтении нижеследующего подробного описания.
Имеющиеся способы получения стерильного коллагена создают уже упомянутые выше проблемы осуществления, и до настоящего времени не позволили на практике осуществить прямую стерилизацию в жидкой среде одного коллагена или коллагена в присутствии других активных веществ. Проведение этой стерилизации отличается простотой, и она особенно эффективно гарантирует стерильность и нативную природу полученного коллагена, сохраняя таким образом его благоприятные свойства.
Таким образом, настоящее изобретение достигло эту цель и относится к способу получения коллагена, включающему перед стерилизацией стадию механической предварительной обработки в смесителе, таком как "режущий смеситель", имеющийся в продаже под товарным названием DITO-SAMA 175 (LA BOVIDA), и, например, модифицированный компанией "J.F.I., Graulhet France", который оборудован системой регулировки температуры экстракта нестерильного нативного коллагена, который солюбилизируется и очищается и, необязательно, подвергается действию пепсина. Самое удивительное и неожиданное, что этот этап предварительной обработки обеспечивает возможность стерилизации коллагена в жидкой форме и сохранения его нативной формы, когда он не был подвергнут воздействию пепсина.
Предпочтительно полученный таким образом коллаген представляет собой в основном коллаген I типа.
В основном коллаген I типа, полученный таким образом, является стерильным и имеет ненативную форму, т.е. с неизмененными вторичными и третичными структурами, и даже после стерилизации сохраняет все свои благоприятные свойства.
Коллаген в соответствии с настоящим изобретением может использоваться в очень многих сферах применения, которые подробно описаны ниже, в частности:
различные виды применения в медицине и ветеринарии;
различные виды фармацевтического применения;
различные виды парафармацевтического применения;
различные виды применения в офтальмологии;
различные виды медико-хирургического применения;
различные виды косметического применения.
Он может применяться сам по себе, т.е. без каких-либо других активных составляющих веществ, например, в форме стерильного прозрачного раствора, для инъекционных препаратов или альтернативно в качестве биологического клея и в других формах, которые подробно описаны ниже.
Он может применяться в композициях в комбинации при низком рН в качестве носителя для других активных составных частей с целью немедленного высвобождения последних. Эти другие активные составные части преимущественно выбраны из группы, состоящей из факторов свертывания, например тромбина, противоинфекционных средств, например метронидазола, антибиотиков, в частности макролидов, таких как гентамицин, фторхинолонов, таких как пефлоксацин, противовоспалительных средств, например ацилкарбоксильных или оксикамовых производных стероидных или нестероидных противовоспалительных средств, антимикотических средств и факторов роста, в частности факторов роста кости, таких как соматотропин, и эпидермальные факторы роста, такие как EGF.
Однако при определенных специфических сферах применения, например в офтальмологии или в случае применения лекарственных комбинаций, включающих активные составные части, которые несовместимы с кислым рН, таких как гликопептидный антибиотик ванкомицин, именно в приведенных этих двух примерах очевидно, что предпочтительно иметь коллаген при нейтральном рН.
Может также быть предпочтительным иметь коллаген при нейтральном рН в качестве носителя для активных составных частей пролонгированного высвобождения, таких как, например, факторы свертывания, или, альтернативно, когда предусматривается комбинация активности последних и механического действия. Таким образом, особенно предпочтительно также применять коллаген в соответствии с настоящим изобретением или путем комбинирования двух предшествующих комбинаций в стратифицированных твердых формах при кислом рН и при нейтральном рН при специфических способах применения, которые будут описаны ниже.
В качестве примеров очень многих форм представления коллагена в соответствии с изобретением можно упомянуть:
- жидкие формы: гель, в частности, гель для инъекций, капли, пену, аэрозоль;
- псевдотвердые формы: пленки, листки, мембраны, ленты или накладки и т. д.;
- твердые формы: порошки, ламинированные/стратифицированные губки, пленки, мембраны, нити, шовный материал и т.д.
Можно также использовать свойства кислотности и растворимости стерильного коллагена в соответствии с изобретением в фармацевтических или косметических композициях, в частности в увлажняющих композициях.
Можно, например, использовать коллаген при низком рН и в псевдотвердой форме, полученной в соответствии со способом изобретения, отдельно или в комбинации с другими активными составными частями, такими как витамин Е или витамин С, в частности, в качестве увлажнителя ткани на эпидермисе и в качестве носителя для активной составной части (частей) в маске для лица.
Эти и некоторые другие формы представления будут проиллюстрированы в остальной части настоящего описания.
В контексте настоящего изобретения термин "нативный коллаген" предназначен для обозначения коллагена, который не был подвергнут модификации его первоначальной структуры, причем сохраняется целостность его полипептидных цепей (включая телопептиды) и спиральная структура молекулы остается нетронутой.
Термин "ателопептидный коллаген" предназначен для обозначения коллагена, который был подвергнут ограниченному протеолизу с помощью ферментативной обработки с использованием протеолитического фермента, отличного от коллагеназы, такого, например, как трипсин, папаин и т.д., или еще лучше пепсин, приводящий к удалению его телопептидов. Конечно, если коллаген был в нативной форме, то он сохраняет свою трехспиральную структуру.
Термин "стерильный коллаген" предназначен для обозначения коллагена, который стерилен в соответствии со стандартами Всемирной Организации Здравоохранения, Европейской Фармакопеи и Фармакопеи США (USP 22), т.е. который сертифицирован как стерильный после микробиологического анализа в соответствии с критериями, признанными соответствующими администрациями.
Термин "жидкий коллаген" предназначен для обозначения коллагена в растворе или в форме суспензии, дисперсии или геля.
Термин "псевдотвердый коллаген" предназначен для обозначения коллагена в форме геля, который не текуч и который образует компактную и однородную массу, содержащую более чем 75% воды.
Термин "твердый коллаген" предназначен для обозначения коллагена, который содержит не более чем 10 - 25% воды и который может быть в твердой форме, например в виде порошка, пленки, губки, мембраны и т.д.
Фраза "нативный коллаген со способностью к полимеризации" предназначена для обозначения нативного коллагена, полученного в соответствии с вариантом способа в соответствии с настоящим изобретением, который в жидкой форме или будучи однажды солюбилизированным из твердой формы, имеет жидкую природу при температуре выше чем 37oС. Он трансформируется в однородную массу и находится в "псевдотвердой" форме при температуре, меньшей 37oС или приблизительно равной ей. Ателопептидный коллаген также может иметь указанную способность полимеризоваться.
Фраза "солюбилизированный и очищенный экстракт" предназначена для обозначения нестерильного экстракта коллагена при низком рН (от 1,5 до 6,5, обычно от 3 до 6, еще лучше от 4 до 5), в котором содержание серосодержащей золы в целом менее чем 2% и содержание липидов в целом менее чем 1% и который содержит от 12 до 13,9% гидроксипролина и от 17 до 18,7% общего азота, и который не содержит следовых количеств триптофана или полипептидных цепей менее чем 95000 Да.
Такой экстракт может быть получен из высушенных обработанных известью свежих шкур, таких как шкура ягненка или кролика, и/или из соединительных тканей, в частности, от крупного рогатого скота, коз, свиней, овец, лошадей, кроликов, молодых жеребцов, страусов, рыб и т.д., или из высушенных или свежих костей, роговиц или даже сухожилий животных (например, ахилловых сухожилий страусов), или альтернативно из очищенных коллагеновых волокон или порошков. Он может также экстрагироваться из плаценты человеческого происхождения.
Экстракт, который может использоваться в контексте настоящего изобретения, получают с помощью серии обработок, включающих в итоге этапы: обработки известью / удаления волос / промывания / удаления извести / удаления эпидермиса и подкожных тканей / разрезания / центрифужной сушки / погружения в 1 н. NaOH на 12 ч при 25oС / промывания для полного устранения NaOH / размалывания / разрезания на пленки / обезжиривания в бане Triton X100 при 0,01% / необязательного удаления аминогликанов в бане K2HPO4 / промывания / центрифужной сушки / промывания очищенной водой / центрифужной сушки / подкисления в 10-2 М уксусной кислоте, монохлоруксусной кислоте или лимонной кислоте / необязательного разведения экстракта коллагена.
Способ настоящего изобретения может применяться к различным коллагенам типа I, II, III, IV и т.д. Однако далее и исключительно в качестве не ограничивающей иллюстрации термины "экстракт коллагена" и "коллаген" при отсутствии других указаний относятся к экстракту коллагена преимущественно типа I.
Таким образом, в контексте настоящего изобретения экстракт коллагена состоит преимущественно из коллагена I типа, т.е. содержащего более чем 90% коллагена I типа. Экстракт может также состоять полностью из коллагена I типа, например, с помощью продолжения удаления коллагена III типа в соответствии с известными методиками диализа, центрифугирования и дифференциального осаждения с хлоридом натрия.
Коллаген I типа представляет собой полимер с высокой молекулярной массой, составляющей 285000 Да, и состоящий из ассоциации трех спиральных из двух идентичных полипептидных цепей, называемых α1(I)2 и из полипептидных цепей, называемых α2(I)1. Он относится к семейству фибриллярных коллагенов (типа I, II, III и V).
Коллаген имеет пик денатурации, который зависит от его происхождения, от способа экстракции, приводящего к нему, и от его поперечно сшитой или не поперечно сшитой формы. У не поперечно сшитой формы пик денатурации находится при 35-45oС.
Коллаген преимущественно I типа имеет соотношение α2(I)1/α1(I)2 от 0,48 до 0,52, по данным измерения с помощью денситометрии, проводимой на полиакриламидном геле после миграции цепей с помощью электрофореза.
Вирусная инактивация этого экстракта и необязательно присутствующего пепсина может проводиться с помощью химической обработки путем попеременного пропускания через буферные растворы при рН, превышающем или равном 13, и при рН ниже 2,5 или равном ему. В целом проводятся такие известные сами по себе способы обработки, как вымачивание в бане гидроксида кальция при концентрации 4% в комбинации с сульфидом натрия при концентрации 3% с последующей второй баней метабисульфита натрия при концентрации 0,5% в комбинации с аммония хлоридом при концентрации 2%.
Необязательная нейтрализация пепсина проводится с помощью обработки натрием, которая возвращает рН к уровню от 6,8 до 7,4, как изложено, например, в документе FR 2586703.
Аналогичным известным образом, как описано, например, в распоряжениях ВОЗ (WHO/COS/VHP/92.104) и Европейского Сообщества от 11 декабря 1991 г., может также проводиться устранение возможных агентов, которые ответственны за бычьи губчатообразные энцефалопатии и которые называются "прионами". Это устранение может таким образом состоять из обработки раствором 1 н. гидроксида натрия в течение 1-48 ч при 25oС или, альтернативно, из обработки гипохлоритом натрия в течение, по меньшей мере, 1 ч при 25oС.
В соответствии с первым аспектом, предметом настоящего изобретения является таким образом более точно способ получения коллагена из солюбилизированного и очищенного, необязательно пепсинизированного экстракта нестерильного нативного коллагена. Обычно этапы состоят из смешивания и сдвигания указанного экстракта в смесителе с двойными поперечными резцами в течение периода от 1 до 60 мин, преимущественно от 15 до 40 мин, а предпочтительно от 10 до 20 мин, при скорости перемешивания от 100 до 10000 об/мин, в целом от 500 до 7000 об/мин, а предпочтительно от 1000 до 5000 об/мин, с контролем в то же самое время температуры, а затем в стерилизации указанного экстракта.
Преимущественно в соответствии с первым вариантом реализации и когда экстракт обычно не пепсинизируется (для простоты именуемый далее "вариант 1" - вариант реализации способа изобретения, при котором при отсутствии других указаний экстракт не пепсинизируется), температура, которая всегда контролируется, в целом не превышает 40-50oС или даже 60 - 80oС в присутствии поперечно сшивающего агента (в соответствии с другим вариантом реализации, который представляет собой альтернативу этому варианту и подробно описан ниже).
Предпочтительно в соответствии с первым вариантом способа настоящего изобретения, поскольку экстракт не пепсинизируется, его температура постепенно увеличивается от комнатной температуры до тех пор, пока в указанном смесителе не будет достигнута температура от 40 до 50oС, в то же самое время поэтапно повышая первоначальную скорость перемешивания с 500 об/мин с тем, чтобы достичь скорости от 5000 до 7000 об/мин, и на каждой фазе увеличения вязкости проводится разведение экстракта. Таким образом, поддерживается выбранная высокая вязкость коллагена, и в то же самое время уменьшается его концентрация. Преимущественно указанная высокая вязкость составляет от 15000 до 20000 сП (от 15 до 20 Па•с). Например, если указанная максимальная температура составляет от 42 до 44oС, указанный экстракт оставляют стоять перед указанным этапом стерилизации.
После стерилизации наблюдают, что полученный таким образом коллаген из непепсинизированного экстракта сохранил свою нативную форму и приобрел улучшенные свойства, в частности эластичность и механическую прочность. Он обладает сцепляющей и полимеризующей способностью.
Предпочтительно, температура указанного экстракта в указанном смесителе ступенчато повышается от комнатной температуры до температуры максимум от 40 до 50oС на 2-10oС, предпочтительно на 3-5oС, при одновременном также ступенчатом увеличении скорости перемешивания на 500-1000 об/мин с тем, чтобы достичь скорости от 1500 до 7000 об/мин, предпочтительно 5000 об/мин.
Действительно важно ступенчатое повышение температуры, поскольку резкое увеличение температуры вызывает временную денатурацию коллагена без достаточного увеличения его эластичных свойств. Эта температура доводится до, по меньшей мере, 40oС, поскольку ниже этой температуры последующая фильтрация затрудняется или даже становится невозможной.
Важно также ступенчато увеличивать скорость перемешивания с тем, чтобы лучше контролировать выбранную высокую вязкость, в то же самое время уменьшая концентрацию коллагена, как уже упоминалось.
Концентрация коллагена в экстракте составляет от 0,001 до 15%, в целом от 0,1 до 10%, а предпочтительно от 3 до 6%.
Как описано выше, температура в указанном смесителе может, однако, достигать более высоких величин, которые могут достигать 80oС, в присутствии поперечно сшивающих агентов, таких как глутаральдегид и азиловые кислоты, таких как гидразин, или любого другого поперечно сшивающего агента, который совместим с коллагеном. При их присутствии эти агенты имеют конечную концентрацию в экстракте от 0,00075 до 0,1%, предпочтительно от 0,0075 до 0,01% в случае глутаральдегида и от 0,1 до 2%, предпочтительно от 0,5 до 1,5% для гидразина. "Поперечно сшитый" таким образом коллаген имеет более высокую температуру отверждения, которая может составлять около 40-50oС, и имеет время резорбции in vivo, которое длиннее, в сравнении с коллагеном без поперечной сшивки, и которое может достигать от 8 до 12 нед.
В соответствии с особым вариантом реализации этого варианта способа в соответствии с изобретением, который состоит в получении стерильного нативного коллагена в форме вязкой жидкости, проводятся следующие процедуры:
- Нестерильный нативный коллаген, который экстрагируется из кроличьих шкур или из ахилловых сухожилий страусов, получают в достаточно высокой концентрации, составляющей около 10-15%.
- Затем экстракт нестерильного нативного коллагена подвергается перемешиванию и сдвигу в уже упоминавшемся смесителе с двойными поперечными резцами с умеренной скоростью от 500 до 1000 об/мин и при комнатной температуре около 20oС.
- Скорость вращения и скорость сдвига ступенчато увеличиваются, что оказывает эффект в виде значительного увеличения вязкости экстракта. Вязкость может иметь величины от 7000 до 20000 сП. Начиная от 1500 сП, экстракт имеет по существу эластичный вид, что крайне затрудняет его перемешивание и его сдвиг в смесителе.
- На каждой фазе увеличения вязкости осуществляют разведение экстракта с помощью добавления воды для инъекций (ВДИ) или 10-2 М лимонной кислоты и ступенчато увеличивают скорость перемешивания и температуру в смесителе до тех пор, пока не будет получена очень высокая вязкость, составляющая около 20000 сП (20 Па•с).
- Эту операцию повторяют несколько раз, предпочтительно 4-5 раз до тех пор, пока не будут достигнуты температура 35oС, скорость от 3000 до 5000 об/мин и концентрация коллагена около 3-6%.
- Продукт держат при этой температуре 35o С и при этой скорости от 3000 до 5000 об/мин в течение нескольких минут, предпочтительно от 3 до 5 мин.
- Температуру в смесителе увеличивают до тех пор, пока не будет достигнут ее уровень от 40 до 50oС, предпочтительно, в случае коллагена без поперечной сшивки, от 40 до 45oС. При этой температуре наблюдается наиболее удивительное разжижение экстракта с падением вязкости до уровня приблизительно от 40 до 100 сП.
- Экстракт коллагена, полученный с помощью изложенного выше способа, немедленно тщательно фильтруют через мембраны с размером пор от 0,45 мкм до 0,22 мкм при контролируемой рабочей температуре от 40 до 50oС.
- Затем его подвергают стерилизации предпочтительно с помощью абсолютной фильтрации через мембрану с размером пор 0,22 мкм, такую как мембрана Millidisck®, продаваемая компанией Millipore, при контролируемой рабочей температуре от 40 до 50oС. Время фильтрации при температуре от 40 до 50oС выбирают так, чтобы оно не превышало 1 ч, еще лучше, чтобы оно составляло от 10 до 20 мин. Можно также проводить стерилизацию предпочтительно также с помощью добавления надуксусной кислоты, производимой, в частности, компанией "Air Liquide" под названием Soproper®, в конечной концентрации в тщательно профильтрованном экстракте от 0,5 до 50%, а предпочтительно от 5 до 15 мас.% по отношению к сухой массе коллагена. Нейтрализацию этого стерилизующего агента проводят с помощью добавления тиосульфата натрия в пропорции от 2 до 20 г на 1 г надуксусной кислоты, предпочтительно от 4 до 12 г/г надуксусной кислоты. Время контакта, требуемое для стерилизации надуксусной кислотой, составляет от 1 ч до 24 ч при комнатной температуре предпочтительно от 2 до 4 ч.
В соответствии с другим определенным вариантом реализации этого первого варианта способа в соответствии с настоящим изобретением, который состоит в получении нативного коллагена в форме псевдотвердого геля, ввиду того, что концентрация коллагена составляет от 0,5 до 10%, предпочтительно также стерилизовать его прямо облучением в дозе 2,5 Мрад (2,5•10-5 Грэй) (бета- или гамма-ионизирующее излучение). Неожиданно наблюдается, что псевдотвердый гель остается компактным и однородным и что, в отличие от обычных гелей, поэтому не происходит разделения на две фазы, и он сохраняет свои физико-химические свойства и его полимеризующую способность. Этот псевдотвердый гель, стерилизованный с помощью этого способа, может преимущественно разжижаться с тем, чтобы комбинироваться со стерильными активными составными частями, которые чувствительны к ионизирующему излучению, такими как факторы свертывания, антибиотики, антимикотические средства и т.д., для производства жидких или твердых препаратов, в частности препаратов, приведенных ниже в качестве примеров: губок, порошков, пленок, мембран, накладок и т.д.
При использовании этого способа стерилизации применительно к твердым препаратам коллагена, который получен в соответствии с этим первым вариантом способа, и который используется сам по себе или в комбинации с активными составными частями, которые устойчивы к ионизирующему излучению и которые выбраны из терапевтических классов, приведенных в настоящем документе, не происходят изменения физико-химических свойств или полимеризующей или сцепляющей способности этой формы коллагена.
В соответствии с этим 1 вариантом способ в соответствии с изобретением может также включать этап нейтрализации. Эту нейтрализацию можно проводить до и после этапа стерилизации. Нейтрализацию можно проводить, например, гидроксидом натрия для доведения рН в диапазоне от 6,8 до 8,2, а предпочтительно от 7,0 до 7,4. Наиболее неожиданно то, что, как было отмечено, эта нейтрализация коллагена в вязкой жидкости и форме при температуре от 40 до 50o С не вызывает никакого осаждения коллагена. Экстракт остается в светлой и прозрачной вязкой жидкой форме и быстро отвердевает при тех же условиях, что и коллаген при низком рН. Это имеет большие преимущества, поскольку до настоящего времени препятствием производству определенных препаратов, таких как гель на основе коллагена или комбинация коллагена с ванкомицином, было осаждение коллагена при нейтральном рН.
Анализы молекулы коллагена изобретения с помощью уже упомянутых обычных методик подтверждают целостность первичных, вторичных и третичных структур нейтрализованного таким образом коллагена.
Характеристики коллагена, полученного в соответствии с вариантом 1.
Самым неожиданным было то, что, как отмечено, коллаген, стерилизованный в соответствии с первым вариантом способа настоящего изобретения, сохранял свою нативную форму.
При температуре от 40 до 50oС он представляет собой вязкую прозрачную жидкость.
Вязкость в целом варьирует от 20 до 300 сП (от 20•10-3 до 300 •10-3 Па•с), а предпочтительно от 30 до 200 сП (от 30•10-3 до 200•10-3 Па•с), а еще даже лучше от 40 до 100 сП (от 40•10-3 до 100•10-3 Па•с).
Его рН в целом составляет от 1,5 до 6,5, предпочтительно от 2 до 5 и даже еще лучше от 3 до 4.
Его концентрация в целом составляет от 0,001 до 15%, предпочтительно от 0,1 до 10% и даже еще лучше от 3 до 6%.
Он очень быстро отвердевает при температуре ниже или равной 38oС. Он принимает псевдотвердую форму, которая обладает заметными сцепляющими свойствами кровоостанавливающего клея. Время его отвердения при температуре около 38o С составляет менее 1 мин при концентрации, превышающей или равной 5%, от 1 до 2 мин при концентрации от 3 до 4% и около 3 мин при концентрации ниже 2%.
Полученный нативный стерильный коллаген имеет также следующие другие важные характеристики или свойства:
- коллаген преимущественно представляет собой коллаген I типа, т.е. содержит его в количестве 90% или более, т.е. имеет соотношение α2(I)1/α1(I)2 от 0,48 до 0,52;
- содержание воды: более 80%;
- внешний вид: жидкость при температуре выше чем приблизительно 38oС и липкая на ощупь; псевдотвердая плотная и однородная желеобразная масса при температуре ниже чем приблизительно 38oС;
- общее содержание азота: от 17,0 до 18,7%;
- гидроксипролин: от 12 до 13,9%;
- не содержит триптофан, аминогликаны и полипептиды с молекулярной массой <95000 Да;
- липиды <1%;
- серосодержащая зола <2%;
- пик денатурации: от 38 до 45oС, по данным измерения с помощью дифференциальной термографии (DSC);
- обладает способностью склеивания;
- обладает способностью полимеризоваться;
- хранится при комнатной температуре;
- готов к немедленному применению.
Таким образом, предметом настоящего изобретения является также такой коллаген, который имеет упомянутые выше характеристики.
Препараты на основе коллагена, полученного в соответствии с этим первым вариантом способа в соответствии с настоящим изобретением, и способы их применения.
Как уже упоминалось, коллаген в соответствии с изобретением обладает способностью полимеризоваться и склеиваться при кислом или нейтральном рН. Последнее из упомянутых свойств в комбинации с его кровоостанавливающими и резорбционными свойствами придают ему качество рассасываемого гемостатического клея.
Коллаген изобретения может предпочтительно распределяться в шприцы или флакончики емкостью от 2 до 5 мл, которые предпочтительно изготовлены из стекла и которые хранятся при температуре, позволяющей ему полимеризоваться или отвердеть при температуре от 0 до 38 oС, даже еще лучше при комнатной температуре.
Другой преимущественной формой этого рассасываемого гемостатического клея в соответствии с изобретением является сухая, порошкообразная или губчатая форма. Эта форма не требует предварительной подготовки перед ее применением.
Для получения такой формы коллаген изобретения, полученный в вязкой форме, подвергается, например, лиофилизации.
Коллаген изобретения в жидкой форме равномерно распределяется в контейнеры (лиофилизационные лотки) в асептических условиях, обеспечивая получение лиофилизатов с толщиной от 1 до 20 мм, предпочтительно от 2 до 10 мм и даже еще лучше от 3 до 5 мм. Полученный лиофилизат имеет кремовый цвет и имеет слегка эластичный образующий пленку вид. Он имеет содержание воды от 1 до 25%, а предпочтительно от 5 до 15%. Лиофилизаты могут подвергаться размалыванию с тем, чтобы получить порошок с выбранным маленьким размером частиц.
Для порошкообразных препаратов предпочтительно иметь перед лиофилизацией концентрацию коллагена приблизительно от 3 до 6% или более, с тем чтобы обеспечить лучшее распыление.
Порошок после размалывания может распределяться в стерильные полиэтиленовые флаконы с двойным колпачком или в другой контейнер, который обеспечивает возможность поддержания стерильности и который облегчает распыление по кровоточащей поверхности.
В случае губок концентрация коллагена должна быть относительно низкой, предпочтительно от 1 до 2%.
Образующие пленку губки могут после лиофилизации упаковываться отдельно в двойные мешочки или в блистерные упаковки, которые закрываются термической пайкой. Они имеют, например, квадратную, треугольную или круглую форму и, в зависимости от способов применения, имеют длину стороны или диаметр от 1 до 30 см.
Действие упомянутых выше двух сухих форм одинаково с действием уже описанной жидкой формы. Однако образующая пленку губка оказывает также механическое действие, которое часто жизненно важно в случае кровоизлияния или кровотечения в полости, в частности в брюшную полость.
Клей, независимо от его формы, в частности, в виде вязкой жидкости, псевдотвердого вещества, образующей пленку губки или порошка может комбинироваться с активными составными частями, в частности с фармацевтическими активными составными частями, таким как, например, факторы свертывания, которые участвуют в ускорении гемостаза (такие как, например, тромбин, фибриноген, фактор XII и т.д.) или, альтернативно, антибиотики, в частности, в случае хирургических операций на костях.
В случае содержания факторов свертывания этот клей может преимущественно комбинироваться со стабилизаторами, такими как, например, полиолы (например, глицерин или полиалкиленгликоль, в котором алкиленовый радикал имеет от 1 до 4 атомов углерода, таком как, в частности, полиэтиленгликоль или полипропиленгликоль) или моно-, ди- или полисахариды (такие как глюкоза или сахароза).
В качестве других препаратов, полученных из вязкой жидкой формы коллагена в соответствии с вариантом 1 способа изобретения, можно упомянуть: псевдотвердую накладку в качестве носителя для активных составных частей для экстраэпидермального местного применения, или, альтернативно, аэрозоль, способствующий рубцеванию, который пригоден, в частности, для пациентов с ожогами третьей степени, а также в качестве увлажняющей маски для косметического применения.
Накладка может включать один или более антибиотиков, противовоспалительные средства, антисептики, антибактериальные средства, противогрибковые средства и антимикотические средства и другие физиологически и фармацевтически активные вещества, в частности салициловую кислоту или никотин. Эти активные составные части добавляются при температуре выше 40oС до получения гомогенизации. Смесь дегазируют и приводят в действие с помощью компрессорного устройства, например, такого как дозировочный насос, и распределяют в герметично запаянные упаковки (например, блистеры или полиэтиленовые пленки или им подобные). После охлаждения жидкости до комнатной температуры упаковку закрывают с помощью термической пайки.
Концентрации коллагена, используемые в накладке, находятся в диапазоне от 1 до 8%, а предпочтительно от 2 до 5%.
Антибиотики в случае их присутствия имеют следующую концентрацию в мг антибиотика на 1 мг коллагена.
Гентамицин: от 0,01 до 2 мг/мг, еще даже лучше от 0,1 до 0,7 мг/мг, а предпочтительно от 0,15 до 0,5 мг/мг.
Ванкомицин: от 0,01 до 2 мг/мг, еще даже лучше от 0,1 до 0,7 мг/мг, а предпочтительно от 0,15 мг/мг до 0,5 мг/мг.
Пефлоксацин: от 0,01 до 2 мг/мг, еще даже лучше от 0,05 до 0,5 мг/мг, а предпочтительно от 0,075 мг/мг до 0,25 мг/мг.
Толщина накладки может быть в диапазоне от 1 до 5 мм или толще. Однако предпочтительны накладки толщиной от 1,5 до 2,5 мм.
Длина и ширина подбираются в зависимости от предусмотренного применения.
Накладка, полученная в соответствии с настоящим изобретением, имеет псевдотвердую форму, является гибкой, прочной и высоко гидратированной (содержание воды выше 80%), а также имеет прозрачный внешний вид.
Она легко накладывается на внутренние или наружные тканевые поверхности независимо от того, повреждены они или здоровы. В случаях наружного эпидермального применения накладка может фиксироваться на непроницаемый гипоаллергенный клей, который обеспечивает возможность ее приклеивания и удерживания на поверхности ткани.
Маску получают с помощью выливания самого коллагена или в комбинации с активными составными частями, такими как, например, витамины (С, Е и т.д.), поверхностно-активным веществом, таким как бензалконийхлорид, или увлажняющими веществами, такими как глицерин, например, на ленту медленно движущегося конвейера, что обеспечивает возможность получения однородной пленки равномерной толщины. После охлаждения ее разрезают на куски подходящих размеров в псевдотвердой форме и упаковывают в герметичные мешочки (например, изготовленные из алюминия с внутренними полиэтиленовыми слоями).
Концентрации коллагена, которые могут использоваться при приготовлении такой маски, составляют в целом от 0,2 до 3%, даже еще лучше от 0,5 до 2%, а предпочтительно от 1 до 1,5%.
Формы и размеры маски ни в коей мере не ограничены.
Маска для лица в целях удобства имеет форму и размеры листа типа А4 (21 х 29,7 см). Толщина в целом составляет от 0,5 до 3 мм, а предпочтительно от 1 до 1,5 мм.
Маска имеет псевдотвердую форму, очень гибка, мягка на ощупь, прозрачна и высоко гидратирована (содержание воды более 97%). Она очень легко накладывается на кожу. К ней могут добавляться один или более красителей и других активных составных частей, которые совместимы с коллагеном.
Аэрозоль содержит коллаген и активные составные части в тех же концентрациях и в тех же комбинациях, как те, которые описаны для накладки. Он преимущественно упакован во флакончики, содержащие одну дозу, или аэрозольные баллончики емкостью от 5 до 25 мл, которые предпочтительно изготовлены из стекла или полиэтилена.
Коллаген, который при комнатной температуре находится в полимеризованной форме, перед применением разжижают с помощью нагревания в течение 2-3 мин в водной бане или в инкубаторе в его первоначальной упаковке. Коллаген непосредственно перед его затвердением распыляют в виде аэрозоля на тканевую поверхность.
Распыленный таким образом аэрозоль коллагена прилипает к поверхности ткани и очень быстро полимеризуется на этой поверхности, образуя таким образом кровоостанавливающую и способствующую рубцеванию однородную пленку. Такой аэрозоль, в частности, пригоден с целью обеспечения действия, способствующего рубцеванию повреждений ткани, и/или длительного высвобождения активных веществ, таких как антибиотики, антисептики, антимикотические средства, противовоспалительные средства и т.д.).
Это устройство для аэрозольного распыления с расстояния имеет преимущество в том, что позволяет избежать какого-либо контакта оператора с поврежденной тканевой поверхностью, а следовательно, какой-либо риск возможной местной инфекции.
Одно из применений этого аэрозоля, которое имеет особые преимущества и возможность которого обеспечивается благодаря специфическим свойствам коллагена в соответствии с настоящим изобретением, касается, в частности, пациентов с ожогами третьей степени, у которых необходимы гарантия стерильности и быстроты наступления лечебного эффекта.
В качестве других препаратов, полученных из вязкой жидкой формы коллагена в соответствии с вариантом 1 способа изобретения, можно упомянуть: пленки или мембраны, полученные, например, с помощью выливания на полиэтиленовую ленту с последующей сушкой на воздухе в вентилируемом инкубаторе или в вакууме. Рабочая температура составляет от 10 до 35oС, а предпочтительно от 20 до 25oС.
Для получения, например, пленок толщиной менее 1 мм, предпочтительно от 25 до 250 мкм, обычно используются растворы коллагена, в которых его концентрация находится в диапазоне от 2 до 5%, предпочтительно от 2,5 до 3,5%. Длительность сушки может быть в диапазоне от 1 до 120 ч. Преимущественно длительность сушки составляет около 24 ч. В частности наблюдается, что лучшие результаты получаются
при относительно медленной сушке и относительно низкой скорости воздушного потока.
Полученные таким образом пленки или мембраны имеют содержание воды от 1 до 15%, а предпочтительно от 5 до 10%. Их разрезают в асептических условиях (или вручную, или автоматически) и упаковывают в герметичные и непроницаемые пакеты.
Аналогичным образом, подобно упомянутым выше формам, пленки или мембраны могут содержать активные составные части, такие как антибиотики, антисептики или также противовоспалительные средства и т.д. Они могут производиться из кислотного (с низким рН) или нейтрального коллагена.
Они используются для наружных и внутренних целей для ускорения заживления и/или высвобождения активных составных частей, например, лекарственного препарата. Ввиду их эластичности при контакте с кровоточащей влажной поверхностью они могут преимущественно образовывать оболочку, которая прилипает к области поврежденной ткани.
При способах применения в офтальмологии они изготавливаются из коллагена при рН предпочтительно от 6,8 до 7,2. В этом случае пленки или мембраны могут принимать форму цилиндрического резервуара или прозрачных контактных линз для длительной местной доставки активных составных частей, например, в глаза. Если желательно использовать эти изделия из коллагена в жидкой форме (капли/жидкость для промывания глаз), коллаген сохраняют в капсулах или других упаковках, содержащих одну дозу, которые перед использованием должны повторно нагреваться.
В случае использования в офтальмологии концентрация коллагена при нейтральном рН для мембран и линз составляет от 1 до 2,5%, а предпочтительно, от 0,5 до 2%, а для глазных капель при нейтральном рН концентрация коллагена составляет от 0,1 до 1,5%, предпочтительно от 0,2 до 0,5%.
Таким образом, предметом настоящего изобретения являются также описанные выше композиции, для которых только в качестве иллюстрации могут быть приведены некоторые возможные фармацевтические формы.
В соответствии со вторым вариантом способа в соответствии с настоящим изобретением перед механической обработкой в указанном смесителе с температурным контролем экстракт подвергают ограниченному протеолизу подходящим ферментом, за исключением коллагеназы, таким как, например, трипсин, папаин или пепсин, предпочтительно пепсин, как будет изложено ниже. В целом, концентрация коллагена в экстракте составляет от 0,1 до 2%, еще даже лучше от 0,2 до 1%, и наиболее предпочтительно от 0,3 до 0,5%.
Затем указанный пепсинизированный экстракт (очищенный и солюбилизированный) обрабатывают следующим образом:
- Проводят осветляющую фильтрацию через серию мембран с различным размером пор, например от 100 до 50, а затем 20 мкм, 1 мкм до 0,45 мкм.
- Затем проводят новый этап очистки с помощью дифференциального осаждения с солями щелочноземельных металлов, например хлоридом калия или натрия, предпочтительно хлоридом натрия, необязательно с последующим диализом против фосфатных буферов K2HPO4 и Na2HPO4 и, наконец, с помощью центрифугирования для выделения осажденного коллагена.
- Полученный таким образом шарик гомогенизируют с помощью осторожного перемешивания в очищенной воде, причем концентрация коллагена составляет от 1 до 30%, а затем ее промывают 2-3 раза перед повторным суспендированием в очищенной воде и оставлением для осторожного перемешивания на 48 ч при температуре от 0 до 20oС, а предпочтительно при температуре от 0 до 10oС.
- Эту суспензию центрифугируют или сцеживают с помощью центрифужной сушки. Коллаген собирают в раствор 10-2 М лимонной кислоты при низком рН, от 2 до 5, предпочтительно от 2,5 до 3,5, объем которой рассчитывают как функцию выбранной конечной концентрации коллагена.
- Шарик оставляют в этом кислом растворе без какого-либо перемешивания при низкой температуре от 0 до 10oС на время от 2 до 48 ч, а предпочтительно от 12 до 24 ч. Шарик коллагена набухает и теряет свою белую окраску, становясь прозрачным.
- Шарик переносят в смеситель с двойными поперечными резцами, такой как, например, уже упомянутый резец/смеситель DITO-SAMA, и затем скорость перемешивания и сдвига постепенно увеличивают, не превышая скорость 10000 об/мин с тем, чтобы достичь скорость перемешивания предпочтительно от 1000 до 5000 об/мин, а еще лучше от 2000 до 3000 об/мин, еще более предпочтительно 2500 об/мин, в то же самое время контролируя ступенчатое увеличение температуры от 2 до 10oС, предпочтительно, от 3 до 5oС, с тем чтобы до получения солюбилизации не превысить температуру 35oС, предпочтительно 25oС. Полученный раствор прозрачен.
И в этом случае снова коллаген получают из экстракта коллагена, который предпочтительно представляет собой в основном коллаген I типа.
В соответствии с этим вариантом 2 полученный и очищенный таким образом раствор ателопептидного коллагена может затем подвергаться преимущественно стерилизации с помощью абсолютной фильтрации через мембрану с размером пор 0,22 мкм при рабочей температуре, т.е. в соответствии с этим вариантом, предпочтительно при температуре от 20 до 25o С, или, альтернативно, с помощью добавления надуксусной кислоты в условиях, которые идентичны условиям, уже описанным выше, или, альтернативно, с помощью ионизирующего излучения (2,5 Мрад - 2,5•10-5 Грэй) на предварительно высушенной форме, которую необязательно предполагается солюбилизировать в стерильной жидкой среде для комбинирования со стерильным препаратом активных составных частей, которые чувствительны к ионизирующему излучению и которые выбраны из классов терапевтических средств, на которые имеются ссылки в настоящем документе.
Необязательную нейтрализацию проводят при комнатной температуре, предпочтительно после этапа стерилизации. Наблюдается, что при комнатной температуре со второго часа нейтрализации и далее начинает образовываться осадок. Таким образом, имеет особое преимущество хранение коллагена при температуре от 0 до 8oС и приготовление комбинаций или смесей коллагена с другими активными составными частями, которые несовместимы при низком рН (от 1 до 6,5) в течение первых двух часов после нейтрализации, предпочтительно в пределах первого часа, а даже еще лучше в пределах 30 мин, а затем начало проведения, в частности, необязательных операций замораживания, лиофилизации или сушки на воздухе или в вакууме.
Характеристики коллагена, полученного в соответствии с вариантом 2:
Полученный таким образом ателопептидный коллаген является стерильным и сохраняет свою трехспиральную структуру. Он представлен в форме прозрачного раствора, который имеет низкую вязкость от 2 до 40 сП (от 2•10-3 до 40•10-3 Па•с), и который, если требуется, имеет кислый или нейтральный рН.
Полученный таким образом коллаген имеет следующие другие характеристики:
- коллаген, содержащий 90% или более коллагена I типа, т.е. соотношение α2(I)1/α1(I)2 от 0,48 до 0,52;
- пик денатурации: от 38 до 45oС, по данным дифференциальной термографии (DSC);
- общее содержание азота: от 17,0 до 18,7%;
- гидроксипролин: от 12 до 13,9%;
- не содержит триптофан, аминогликаны и полипептиды с молекулярной массой <95 000 Да;
- липиды <1%;
- серосодержащая зола <2%.
Таким образом, предметом настоящего изобретения является также такой ателопептидный стерильный нативный коллаген.
Препараты на основе коллагена, полученного в соответствии с вариантом 2, и способы их применения. В качестве примеров можно упомянуть:
- Применение без модификации в жидкой форме при кислом рН в качестве увлажнителя ткани или в комбинации с препаратами, например с косметическими активными составными частями в концентрации от 0,1 до 3%; в комбинации с ускоряющими рубцевание терапевтическими препаратами, например в присутствии активной составной части, применяемой в дерматологии, такой как противовоспалительные средства, местные антисептики, антибактериальные средства, противогрибковые средства, салициловая кислота и т.д. Эти композиции представлены в форме крема, геля, пены или мази для наружного применения, причем коллаген включен в них в концентрации от 1 до 3%. Они могут также быть в форме жидкости или аэрозоля для наружного применения, причем концентрация коллагена составляет от 0,1 до 1%. Упомянутые активные составные части применяются в известных лечебных дозах.
- Применение при нейтральном рН в форме пасты или геля в комбинации с фосфатами и щелочными солями (например, хлоридом натрия), причем концентрация коллагена в них составляет от 2 до 7%, для коррекции углублений на коже, таких как морщины или тонкие линии, или, альтернативно, для укрепления гладких мышц, как в случае недержания мочи, или, наконец, для производства заменителей ткани, такой как, например, сердечные клапаны или заместители костей, причем затем коллаген комбинируется, в частности, с гидроксиапатитом или с кораллом.
- Применение при нейтральном или кислом рН при получении пены, которая содержит коллаген в низкой концентрации и которая может, в частности, применяться в хирургии и микрохирургии для восстановления поврежденной ткани и для обеспечения сохранения межтканевого и паренхиматозного пространства и во избежание анатомо-патологических спаек между поврежденными или пораженными тканями (предпочтительно, при операциях на паренхиматозных органах, в сердечно-сосудистой, торакальной, пластической хирургии или в оториноларингологической хирургии). Эта пена может включать активные составные части, в частности антибиотики, антисептики и противовоспалительные средства в тех же концентрациях, как упомянуто выше для препаратов в соответствии с вариантом 1. Такая пена будет подробнее описана ниже.
Используя стерильный коллаген в соответствии с вариантом 2, можно также получить, в частности, с помощью сушки путем лиофилизации, рассасываемые гемостатические губки, которые имеют особое преимущество вследствие их кровоостанавливающего действия и ввиду функции местного носителя одного или более активных составных частей, таких как, в частности, противоинфекционные средства и/или факторы свертывания.
Такие губки, полученные из коллагена при кислом рН в соответствии с вариантом 2, имеют большое преимущество, поскольку они мгновенно растворимы при контакте с жидкой средой, что обеспечивает возможность немедленного высвобождения одного или более активных составных частей, являющихся действующим началом. Такие же губки, полученные из коллагена при нейтральном рН в соответствии с вариантом 2 и имеющие микроволокнистый вид, обеспечивают возможность длительного высвобождения действующего начала, а также оказывают преимущественное механическое действие на кровоточащую поверхность, к которой они прилипают.
Коллаген при кислом или нейтральном рН в концентрации от 0,1 до 3%, предпочтительно от 0,2 до 2% и даже еще лучше от 0,5 до 1%, может применяться при изготовлении таких губок.
Для препаратов варианта 1 в случае присутствия в них антибиотиков используются следующие антибиотики в концентрациях, уже упомянутых для препаратов варианта 1: гентамицин, пефлоксацин и ванкомицин.
Могут также присутствовать другие действующие начала, такие как тромбин, в концентрации в Международных Единицах на 1 мг коллагена от 0,1 до 20 МЕ/мг, предпочтительно от 0,5 до 10 МЕ/мг и еще даже лучше от 1 до 5 МЕ/мг, или фибриноген (в мг фибриногена на мг коллагена) в пропорции от 0,1 до 20 мг/мг, предпочтительно от 0,1 до 10 мг/мг и еще даже лучше от 0,5 до 5 мг/мг. С ними могут также комбинироваться другие активные составные части, такие как другие производные крови, в частности протромбин, фактор Ха, фактор IХа, фактор XIII и любой другой активатор или проактиватор внутренних и внешних механизмов свертывания, необязательно в комбинации с другими физиологически и фармакологически активными веществами, такими как, например, активаторы и ингибиторы плазминогена или антифибринолитические средства. С ними могут также комбинироваться другие вещества, например, специфические ферменты, которые регулируют резорбцию коллагена, или, альтернативно, поперечно сшивающие средства.
Смеси коллагена в соответствии с изобретением и указанных выше активных составных частей готовят в контейнерах, которые изготовлены из нержавеющей стали, стекла или полиэтилена и при температуре от 5 до 35oС, предпочтительно от 10 до 30oС и даже еще лучше от 15 до 20oС.
Как уже указывалось, при нейтральном рН коллаген должен использоваться в пределах 2 ч после его нейтрализации. Затем смесь распределяют в лиофилизационные контейнеры, которые обеспечивают возможность получения слоев, имеющих толщину от 1 до 20 мм, предпочтительно, от 3 до 15 мм и еще даже лучше от 5 до 8 мм. Эти препараты могут таким образом лиофилизироваться в качестве монослоя в соответствии со следующими функциональными параметрами: температура замораживания от -5 до -60oС, температура резорбции от 20 до 50oС, в целом от 25 до 40oС, предпочтительно от 30 до 35oС.
Лиофилизированные таким образом препараты губок имеют белый цвет и имеют однородный, плетеный, "пушистый" вид. Содержание воды в них составляет от 1 до 25%.
Губки в соответствии с изобретением могут применяться без изменения или могут подвергаться ламинированию in situ (в камере лиофилизатора) с помощью воздействия на них или снаружи индивидуального давления в асептических условиях с помощью пропускания через валки. Эта операция обеспечивает возможность увеличить прочность этого типа губки.
Указанные препараты могут быть преимущественно лиофилизированы в один или более слоев. В этом случае сцепление между слоями предпочтительно происходит во время фазы замораживания при выбранных температурах от -11 до -20oС, предпочтительно от -11 до -13oС. Затем получают ламинат, в котором два нижних слоя, например, могут содержать коллаген при кислом рН в комбинации, например, с тромбином и с фибриногеном (обеспечивая возможность высвобождения этих продуктов и образования биологического клея), и в котором верхний слой состоит, например, из коллагена при нейтральном рН (обеспечивая возможность оказывать, как уже упоминалось, механическое действие на кровоточащую поверхность). Указанная выше форма, в отличие от известных клеевых препаратов, обеспечивает возможность служить связующей основой биологического клея без какой-либо предшествующей подготовки, что дает большое преимущество. Слой при нейтральном рН преимущественно содержит антибиотики, что обеспечивает возможность их продолжительного высвобождения, которое имеет особые преимущества в случае костных инфекций. Выбор порядка и количества слоев несуществен; это является предметом компетенции специалистов, которые подберут эти показатели в зависимости от предусматриваемого применения.
В эти комбинации в соответствии с настоящим изобретением могут также включаться стабилизаторы, такие как полиолы, полиалкиленгликоли или полисахариды, или, альтернативно, аминокислоты или другие активные средства, которые совместимы с коллагеном, такие как, например, противовоспалительные средства или, альтернативно, как уже упоминалось, поперечно сшивающие средства, для вновь преимущественного увеличения времени их резорбции. С ними можно также комбинировать другие рассасываемые средства, которые оказывают механическое действие и которые обеспечивают возможность наложения швов, такие как ткани из целлюлозы или окисленной целлюлозы, или викрил® (продаваемый компанией "Ethnor").
Кроме того, коллаген при кислом или нейтральном рН, полученный в соответствии с вариантом 2 способа изобретения, возможно, в комбинации с другими активными составными частями, может после лиофилизации или сушки обеспечить возможность получения гемостатического порошка. Используемый затем коллаген имеет концентрацию от 1 до 3%.
Таким образом, предметом настоящего изобретения являются также описанные выше композиции, для которых были проиллюстрированы некоторые из возможных фармацевтических форм, которые представляют препараты неполимеризованного коллагена, полученного в соответствии с вариантом 2.
Далее здесь будут приведены не ограничивающие примеры некоторых предметов настоящего изобретения со ссылкой на чертежи, в которых:
- фиг. 1 и 2 представляют собой диаграммы электрофореза на полиакриламидном геле, показывающие разделение полипептидных цепей коллагена I типа, соответственно до и после механической и тепловой обработки в соответствии с изобретением (вариант 1);
- фиг.3 и 4 представляют собой диаграммы тепловой денатурации коллагена, демонстрирующие нативную (не денатурированную) природу коллагена соответственно до и после механической и тепловой обработки в соответствии с изобретением (вариант 1).
ПРИМЕРЫ
Пример 1. Способ получения коллагена с полимеризующей способностью (вариант 1: непепсинизированный экстракт).
Экстракт коллагена в концентрации 10%, полученный из ахилловых сухожилий страуса, как описано выше, переносят в уже упомянутый смеситель с двойными поперечными резцами. Затем в течение 7 мин проводят перемешивание и сдвиг при скорости и частоте 1500 об/мин при комнатной температуре (20oС). Отмечается возрастание вязкости до 15000 сП. Экстракт приобретает беловатый цвет и имеет эластичный вид. Затем проводят последовательные разведения с тем, чтобы получить концентрацию коллагена 6%. После каждого разведения температуру постепенно повышают на 4oС и скорость перемешивания постепенно повышают на 500 об/мин через 3-4- минутные интервалы. По достижении скорости перемешивания 3500 об/мин и температуры 35-36oС эти условия поддерживают приблизительно в течение 3 мин, а затем перемешивание прекращают и экстракт оставляют на 30 мин стоять при той же температуре 35-36oС. Затем проводят новое разведение (пятикратное) и скорость увеличивают так, чтобы достичь уровня 5000 об/мин, а температуру повышают так, чтобы через 3-4 мин достичь 42oС. Коллаген приобретает пастообразный вид и имеет вязкость 17000-20000 сП (17-20 Па•с). Температуру повышают с тем, чтобы достичь 44oС. Затем эти условия поддерживают в течение 30 сек - 1 мин; пастообразный коллаген быстро разжижается, приобретая вид жидкости, причем ее вязкость снижена до 30-50 сП (от 30•10-3 до 50•10-3 Па•с).
Разжиженный экстракт немедленно переносят в устройство для фильтрации под давлением, которое предварительно было подвергнуто термической стерилизации, и которое оборудовано двойной оболочкой с циркуляцией воды, позволяющей поддерживать температуру на уровне от 42 до 45oС. Затем экстракт тщательно фильтруют через две мембраны для стерилизующей фильтрации с размером пор первой мембраны 0,45 мкм, а второй 0,22 мкм. Фильтрат собирают в контейнер под давлением, оборудованный двойной оболочкой, причем температуру поддерживают на уровне от 42 до 45oС. Затем этот фильтрат подвергают абсолютной фильтрации через мембрану с размером пор 0,22 мкм.
Полученный коллаген стерилен, что подтверждается бактериологическими исследованиями в соответствии с Европейской Фармакопеей.
Кроме того, анализы полученного таким образом коллагена, проведенные до, во время и после механической и термической обработки коллагена, показывают, что аминокислотный состав коллагена остается неизменным. Более того, с помощью электрофореза на полиакриламидном геле не выявляются полипептиды с молекулярной массой ниже чем 95000 Да (фиг.1 и 2). Отмечается также, что соотношение α2(I)1/α1(I)2 составляет 0,49, т.е. коллаген содержит более 95% коллагена I типа.
Термографический анализ с помощью дифференциальной термографии (DSC), проведенный с помощью устройства модели Delta-Series DSC 7 компании "Perkin-Elmer" и выполненный во время термической и механической обработки при 40-50oС, подтверждает исчезновение пика денатурации коллагена, который соответствует потере трехспиральной структуры молекулы. Однако это исчезновение является лишь временным, поскольку после охлаждения экстракта коллагена и его отверждения отмечается повторное появление пика денатурации (фиг. 3 и 4). Это является доказательством того, что потеря трехспиральной структуры коллагена во время термической и механической обработки в соответствии с настоящим изобретением обратима по природе.
Этот набор данных доказывает, что сохраняются полученные таким образом вторичные и третичные структуры коллагена.
Другие основные характеристики и свойства полученного таким образом коллагена представлены ниже:
- содержание воды: 95%;
- вид: вязкая жидкость при температуре выше чем приблизительно 38oС и липкая на ощупь; псевдотвердая компактная и однородная желеобразная масса при температуре ниже, чем приблизительно 38oС;
- вязкость: 45 сП (45•10-3 Па•с) в жидкой форме
- общее содержание азота: 17,9%;
- гидроксипролин:12,8%;
- не содержит триптофан, аминогликаны и полипептидные цепи с молекулярной массой <95000 Да;
- рН 5,5;
- липиды <1%;
- серосодержащая зола <2%.
Стерильный коллаген, полученный как было только что описано, хранят при температуре 42-45oС в течение ограниченного периода времени для быстрого распределения без изменения в подходящие контейнеры или упаковки, такие как флаконы, шприцы, блистеры и т.д., или после смешивания с другими активными составными частями, такими как факторы свертывания, которые, если требуется, заранее были простерилизованы.
При изолированном применении полученный таким образом коллаген образует клей, который имеет отличные кровоостанавливающие свойства, делающие его пригодным для применения в общей хирургии, при операциях на паренхиматозных органах, в сердечно-сосудистой, торакальной, ортопедической хирургии, оториноларингологической, урологической, печеночной, висцеральной и акушерско-гинекологической хирургии, а также в трансплантологии и хирургии костного мозга; в микрохирургии и любых других областях медицины, требующих действия этой лекарственной формы, возможно, в комбинации с другими активными составными частями.
Его держат при комнатной температуре, при которой он отвердевает.
Это отчетливо отличает его от других имеющихся в настоящее время на рынке так называемых биологических клеев, таких как Tissucol® от компании "Immuno-AG", Austria, или Biocolle® из "Laboratoires des Fractionnements et des Biotechnologies", France, сухую форму которого необходимо хранить при низкой температуре, около +4oС.
Клей на основе коллагена в соответствии с настоящим изобретением перед применением должен восстанавливаться в жидкую форму. Для этого достаточно простое нагревание в течение 2-3 мин, например, в инкубаторе или в водяной бане при 40-45oС с последующим медленным ручным перемешиванием.
Таким образом, в сравнении с указанными выше известными клеями, клей на основе коллагена в соответствии с изобретением, кроме своих преимущественных свойств, имеет время приготовления, которое приблизительно в 10 раз короче.
При присутствии факторов свертывания их готовят заранее, перед их добавлением в коллаген, следующим образом.
В раствор 40 мМ хлорида кальция в воде для инъекций (ВДИ) помещают количество порошка тромбина или фибриногена, эквивалентное соответственно 2 МЕ/мг и 1 МЕ/мг коллагена (т.е. 1 мл коллагена на 50 ME тромбина). Затем отдельно проводят фильтрацию через мембрану для абсолютной фильтрации, имеющей размер пор 0,22 мкм.
Затем в стерильный коллаген, который заранее был нейтрализован (рН 7,0), как уже упоминалось, добавляют тромбин или фибриноген. Смесь гомогенизируют и распределяют в емкости.
Распределение в подходящие контейнеры производят под давлением, используя, например, дозировочный насос, в частности в стеклянные флаконы или шприцы, например, в случае приготовления биологического клея, в блистерные упаковки или мешочки, герметизируемые термической пайкой, как в случае, например, накладок, пленок или увлажняющих масок, или, альтернативно, в лотки лиофилизатора для получения порошка или губки и т.д., как описано выше.
Пример 2. Стерильный жидкий биологический клей, содержащий коллаген + тромбин.
Используя продукт в стерильной жидкой форме, полученный в примере 1, в стеклянном флаконе готовят композицию, содержащую 2 мл 5% коллагена и количество тромбина, соответствующее 200 ME.
Во время его нанесения на кровоточащую поверхность он отвердевает и прилипает к тканевой поверхности, обеспечивая возможность закрытия поражения или разреза, и он действует в качестве контактного кровоостанавливающего средства, которое прекращает кровотечение.
Пример 3. Порошок, содержащий стерильный коллаген + фибриноген.
Используют продукт, полученный в примере 1, и после лиофилизации и размалывания коллагена в комбинации с фибриногеном в стерильную порошкообразную форму, в стерильные полиэтиленовые флаконы распределяют по 360 мг коллагена, содержащего 700 ME фибриногена на флакон.
Порошок при нанесении с помощью распыления на кровоточащую поверхность, в частности, при микрохирургических операциях в областях, где затруднен доступ, обеспечивает возможность прекратить кровотечение посредством своего кровоостанавливающего действия через внутренние и внешние механизмы свертывания, и прилипает к кровоточащей поверхности.
Пример 4. Губка, содержащая стерильный коллаген + тромбин.
Начиная с 35 мл стерильного жидкого коллагена, который имеет концентрацию 1% и который соответствует коллагену, полученному в примере 1 с последующей нейтрализацией, его распределяют по лоткам или блистерным упаковкам размером 5 х 7 см. Затем проводят лиофилизацию и после этого лотки или блистерные упаковки закрывают в асептических условиях, причем эти лотки или блистерные упаковки затем упаковывают в стерильные двойные мешочки.
Полученная таким образом губка обеспечивает возможность покрыть область площадью 35 см2 и соответствует количеству коллагена 350 мг, включающему 700 ME тромбина.
Эта губка оказывает быстрое кровоостанавливающее действие, которое сочетает действие коллагена с действием тромбина на механизмы свертывания, и прилипает к кровоточащей поверхности, обеспечивая значительное механическое воздействие. Его образующий пленку вид обеспечивает возможность покрытия больших кровоточащих площадей.
Пример 5. Накладка, содержащая коллаген (псевдотвердый) + метронидазол.
Противоинфекционное средство метронидазол в жидкой форме и после предварительной стерилизующей фильтрации добавляют в 2% коллаген, полученный в примере 1, в жидкой форме при 42-45oС и нейтрализованный, как указано выше, в пропорции 0,05 мг/мг сухого коллагена.
После охлаждения коллаген, который имеет вид прозрачного и однородного псевдотвердого геля толщиной 1 мм, подвергают стерилизации с помощью облучения бета-лучами при 2,5 Мрад (25•10-5 Грэй), Laboratoires Caric Orsay, France.
Неожиданно отмечено, что, гель, полученный из коллагена в соответствии с настоящим изобретением "не ломается", т.е. не разделяется на две фазы, в отличие от обычного геля, подвергающегося такой же обработке стерилизации облучением.
Прокладка при наложении на инфицированную рану оказывает местное и защитное действие в качестве дезинфицирующего средства вследствие присутствия и высвобождения метронидазола.
Пример 6. Ателопептидный коллаген со способностью к полимеризации (вариант 1).
Используя 10% экстракт очищенного коллагена, полученного из свежего ахиллова сухожилия страуса, проводят следующие процедуры:
- коллаген разводят с помощью добавления раствора 10-2 М лимонной кислоты при рН 2,5 до тех пор, пока не будет получена концентрация коллагена 1%,
- добавляют пепсин; 1/10 мас./мас. сухого коллагена,
- его оставляют для действия при комнатной температуре (20oС) в течение 7 ч,
- на 7-ой день коллаген нейтрализуют гидроксидом натрия (30%) для получения рН 7,2. Коллаген выпадает в осадок, неколлагеновые белки и остатки пепсина, которые остаются в растворе, удаляют с помощью центрифугирования устройством для сушки при вращении/декантации, такого как, например, устройство, продаваемое компанией "Rousselet" под маркой RC40,
- шарик промывают деминерализованной водой с последующей центрифужной сушкой, причем масса воды соответствует 10 массам шарика, а затем получают коллагеновый шарик в виде влажных волокон,
- эту операцию повторяют 3 раза в тех же условиях, причем при этом получают волокна коллагена с содержанием воды 70%,
- шарик солюбилизируют в 10-2 М лимонной кислоте при рН 2,5,
- смесь гомогенизируют до тех пор, пока не произойдет полная солюбилизация, и получают экстракт коллагена с концентрацией 10%, который прозрачен и имеет вязкость 6000 сП (6 Па•с),
- экстракт переносят в уже упомянутый смеситель с двойными поперечными резцами и процедуру продолжают в соответствии с положениями примера 1 до получения приблизительно 5% коллагена.
Этот стерильный ателопептидный нативный коллаген со способностью полимеризоваться имеет особые преимущества при применении в офтальмологии и может быть в виде хрусталика, гибких мембран или уже описанных выше капель/жидкости для промывания глаз. Кроме того, отсутствие потенциально иммуногенных телопептидов делает его особенно привлекательным.
Пример 7. Коллагеновая пена (вариант 2).
Пену получают из шарика из влажных волокон коллагена с содержанием воды 70%, который обрабатывают в соответствии с уже описанным вариантом 2. Этот шарик гомогенизируют и держат в течение 48 ч при осторожном перемешивании в очищенной воде при +4oС. После центрифугирования шарик помещают в раствор 10-2 М лимонной кислоты (рН 2,5), концентрация коллагена 2,5%. После отстаивания в течение 24 часов при 4oС шарик переносят в смеситель с двойными поперечными резцами. Скорость перемешивания, частоту сдвига и температуру постепенно увеличивают, достигая уровень 2000 об/мин и температуру 25 oС. Затем экстракт фильтруют через абсолютную мембрану с размером пор 0,22 мкм при рабочей температуре 25oС.
В полученный таким образом стерильный коллаген в концентрации 2,5% добавляют бензалконийхлорид в концентрации 1,5 г/л. Смесь подвергают перемешиванию в атмосферных условиях, увеличивая скорость с 500 до 2500 об/мин, экстракт густеет и приобретает белый цвет, и таким образом получают пену в соответствии с настоящим изобретением.
Пену распределяют в дозирующие насосы емкостью 10 мл или более, необязательно оборудованные катетером, который обеспечивает возможность ее введения в области, к которым затруднен доступ, как часто бывает в микрохирургии.
Пена, консервированная таким образом, устойчива при хранении при комнатной температуре в течение, по меньшей мере, 24 мес. В случае присутствия термочувствительной активной составной части предпочтительно поддерживать температуру при хранении полученной таким образом пены на уровне от 4 до 10oС.
Эта пена преимущественно используется, в частности, при операциях на паренхиматозных органах и на органах грудной клетки. Она может, в частности, использоваться при поддержании межтканевых и паренхиматозных пространств и обеспечивает возможность избежать образования анатомо-патологических спаек между поврежденными или пораженными тканями.
Пример 8. Стратифицированные или однослойные гемостатические губки (вариант 2).
Губки производят из коллагена, полученного в соответствии с вариантом 2, как в примере 1, который стерилизуют с помощью абсолютной фильтрации через мембрану с размером пор 0,22 мкм.
Для получения однослойной губки, которая также включает, например, фактор свертывания, проводят следующую процедуру:
- 35 мл жидкого коллагена в концентрации 1%, который был предварительно смешан со стерильным тромбином (700 ME) или со стерильным фибриногеном (350 ME) и затем нейтрализован, распределяют по блистерным упаковкам размером 5х7 см.
- каждую из указанных выше комбинаций коллагена (при температуре замораживания и резорбции соответственно -25oС и 35oС) подвергают обычной и раздельной лиофилизации.
Полученная таким образом губка, содержащая коллаген при нейтральном рН имеет "пушистый", слегка волокнистый вид, и в присутствии фибриногена и тромбина имеет соответственно белый и кремовый цвет.
Эта губка обладает кровоостанавливающим действием, которое связано с внутренним и внешним действием коллагена на механизмы свертывания, которое дополнительно усиливается гемостатическим действием факторов свертывания, а именно тромбином и фибриногеном.
Кроме того, коллаген при нейтральном рН, полученный в соответствии с вариантом 2, ввиду своей нерастворимости, оказывает механическое действие на кровоточащую поверхность ткани, которое не могут оказать факторы свертывания в лиофилизированной форме при изолированном их применении.
Кроме того, и как уже упоминалось выше, в такой форме предоставления в соответствии с настоящим изобретением полностью сохраняется активность факторов свертывания, в отличие от обычных форм предоставления (таких, например, как Tachocomb®, Hafslund Nycomed, описанный в документе ЕР-А-59265), причем последние стерилизуются с помощью ионизирующего излучения и поэтому являются частично денатурированными.
Для получения стратифицированной губки проводятся следующие процедуры:
- 18 мл жидкого коллагена при рН 5, который содержится в концентрации 0,5% и который был заранее смешан с тромбином (700 ME) и с 1 мл 40 мМ хлорида кальция, распределяют по блистерам размером 5 x 7 см, а затем
- проводят легкое замораживание при -10oС и затем в этот первый слой добавляют 18 мл 0,5% жидкого коллагена при рН 5, который предварительно был смешан с фибриногеном (350 ME), а затем
- снова проводят легкое замораживание в тех же условиях и во второй полученный таким образом слой добавляют окончательный слой 1% жидкого коллагена, который в это время имеет нейтральный рН,
- проводят лиофилизацию, как описано выше в случае однослойной губки.
Таким образом, получают трехслойную стратифицированную губку, которая имеет следующие отличительные свойства:
- при нанесении коллаген при кислом рН немедленно солюбилизируется, высвобождая таким образом факторы свертывания, которые на кровоточащей поверхности образуют кровоостанавливающий клей,
- наружный слой при нейтральном рН также оказывает механическое действие, усиливая таким образом действие кровоостанавливающего клея, особенно в случае большой площади кровотечения.
Кроме того, эта губка в соответствии с изобретением имеет преимущество в том, что она не требует приготовления перед ее применением.
Эта форма предоставления кровоостанавливающего средства особенно пригодна для применения в общей, паренхиматозной, сердечно-сосудистой, торакальной, пластической, ортопедической, оториноларингологической, урологической, печеночной, висцеральной и акушерско-гинекологической хирургии, при операциях трансплантации и в хирургии костного мозга, микрохирургии и в целом в любой области, требующей такого кровоостанавливающего действия.
Пример 9. Губка + ванкомицин (вариант 2).
Проводят следующую процедуру:
- 6 л 1,4% раствора коллагена, полученного в соответствии с вариантом 2 способа в соответствии с настоящим изобретением помещают в стерильный контейнер и нейтрализуют с помощью добавления гидроксида натрия, затем
- в раствор коллагена, который хранят при комнатной температуре в течение 1 ч после нейтрализации, добавляют 1 л раствора ванкомицина гидрохлорида при концентрации 42 г/л, затем
- раствор гомогенизируют, а затем с помощью дозирующего насоса полученную в результате смесь переносят через фильтрующую мембрану с размером пор 0,22 мкм в контейнеры для лиофилизации в пропорции по 70 мл на контейнер с размером сторон 10 см, а после этого
- начинают цикл замораживания до -25oС с последующим циклом сублимации и десорбции до +35oС,
- стерильные губки, которые имеют толщину 7 мм и которые содержат коллаген в пропорции 8,4 мг коллагена/см2 и 4,2 мг ванкомицина гидрохлорида/см2, или в конечном счете с помощью воздействия автоматического давления на поверхность слоев внутри лиофилизатора для получения слоистой губки получают губки, которые имеют толщину от 1 до 2 мм, а затем
- проводят термическую пайку для герметизации блистеров и последние упаковывают в стерильные полиэтиленовые двойные мешочки.
Идентичные губки в соответствии с изобретением получают с включением гентамицина, пефлоксацина или других антибиотиков или противоинфекционных средств, вместо ванкомицина.
Эти губки, которые локально и постепенно высвобождают свои активные составные части, могут, в частности, применяться при лечении многих патологических состояний, в частности при поражении костей, внутренних органов, в травматологии и при хирургической патологии, в частности, для профилактики и лечения возможных микробных заражений.
Эти губки, содержащие коллаген в соответствии с настоящим изобретением, кроме их отличной переносимости и способности подвергаться биологическому разложению, имеют большое преимущество ввиду содержания в них ванкомицина, который был подвергнут стерилизации фильтрацией, как описано выше, и который, таким образом, сохранил всю свою активность, в отличие от обычных препаратов, в которых этот антибиотик частично денатурирован в результате стерилизации ионизирующим излучением.
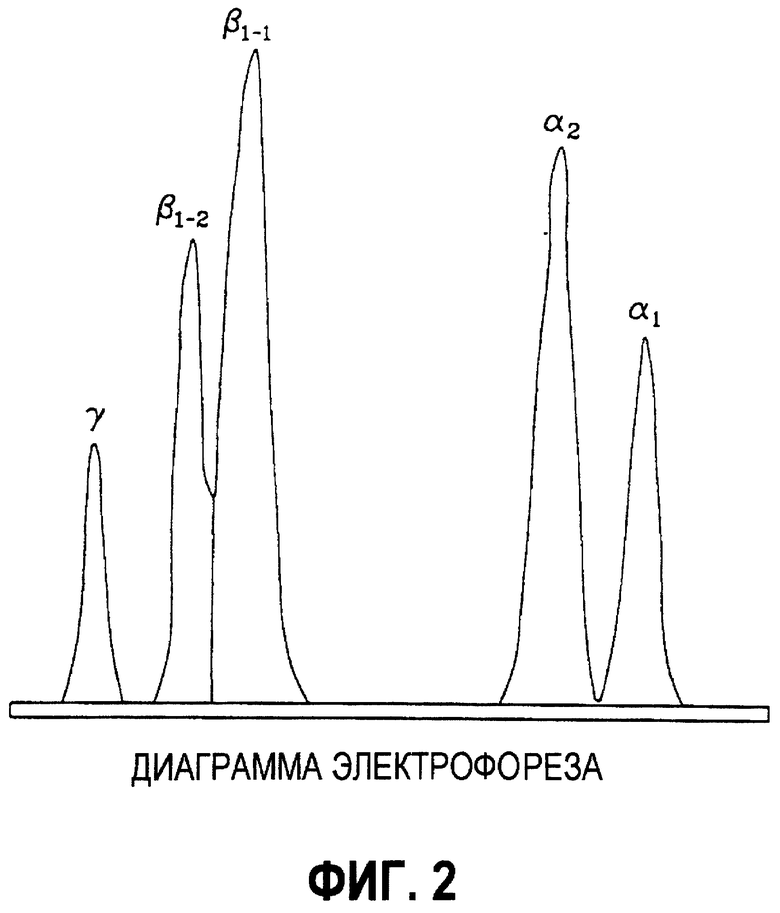
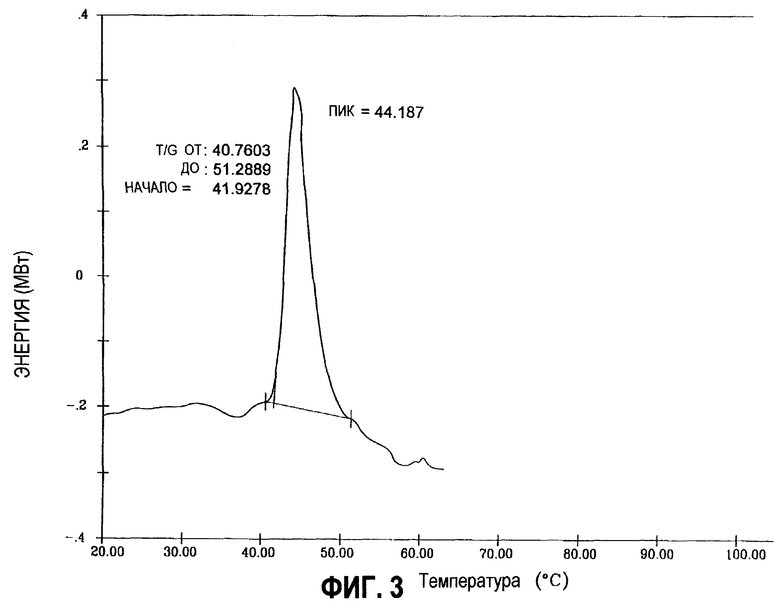
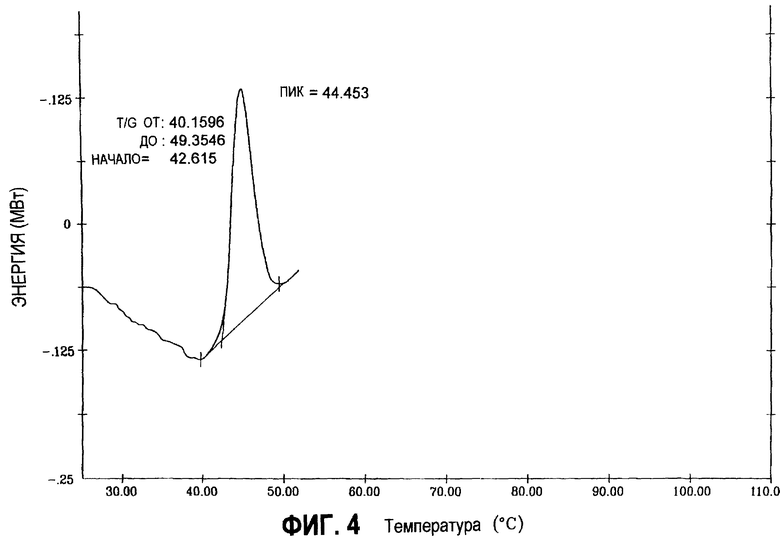
Изобретение относится к усовершенствованному способу получения коллагена из солюбилизированного и очищенного, возможно, пепсинизированного экстракта нестерильного нативного или ателопептидного коллагена, включающему: i) стадию перемешивания и сдвига указанного экстракта в смесителе с двойными поперечными резцами при поэтапном повышении первоначальной скорости перемешивания на 500-1000 об/мин без превышения скорости 10000 об/мин и при поэтапном повышении температуры на 2-10oС, предпочтительно на 3-5oС, таким образом, чтобы увеличить исходную окружающую температуру экстракта до максимально контролируемой температуры, составляющей не выше 50oС, а затем ii) стадию стерилизации в жидкой среде указанного экстракта с получением стерильного коллагена в нативной или ателопептидной форме, к нативному или ателопептидному коллагену типа I, полученному в условиях вышеуказанного способа, имеющему следующие характеристики или свойства: соотношение α2(I)1/α1(I)2 от 0,48 до 0,52; стерильность в соответствии со стандартом Европейской Фармакопеи; общее содержание азота от 17,0 до 18,7%; гидроксипролин от 12 до 13,9%; не содержит триптофан, аминогликаны и полипептиды с мол.м. <95000 Да; липиды <1%; серосодержащая зола <2%, к фармацевтической и/или парафармацевтической, и/или медико-хирургической, и/или офтальмологической, и/или косметической композиции. 4 с. и 9 з.п.ф-лы, 4 ил.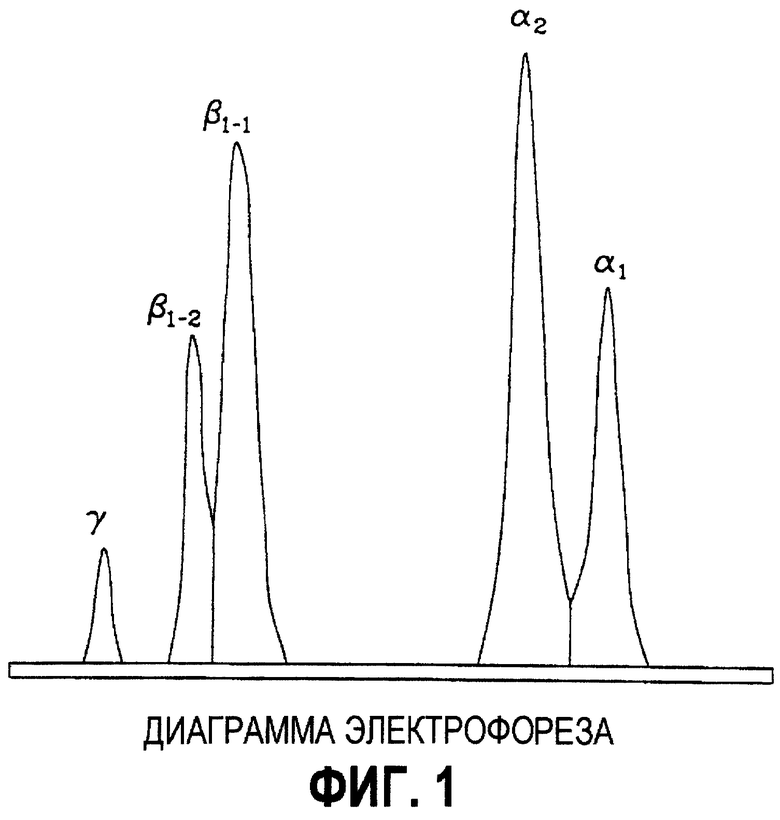
| СПОСОБ ПОЛУЧЕНИЯ ПОРИСТОГО КОЛЛАГЕНСОДЕРЖАЩЕГО МАТЕРИАЛА | 1995 |
|
RU2116801C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОЛЛАГЕНА | 1993 |
|
RU2076718C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОЛЛАГЕНОВЫХ ВОЛОКОН ИЗ КОЛЛАГЕНСОДЕРЖАЩИХ ТКАНЕЙ ЖИВОТНЫХ | 1990 |
|
RU2007926C1 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ АРТЕРИАЛЬНОЙ ГИПЕРТОНИЕЙ С МЕТАБОЛИЧЕСКИМИ НАРУШЕНИЯМИ | 2011 |
|
RU2462222C1 |
| ОКСИГЕНАТОР КРОВИ ПУЗЫРЬКОВОГО ТИПА | 1967 |
|
SU214035A1 |
| УСТРОЙСТВО ДЛЯ ГИДРОСТАТИЧЕСКИХ ИССЛЕДОВАНИЙ ПРЕДОХРАНИТЕЛЬНЫХ КЛАПАНОВ ВЫСОКОГО ДАВЛЕНИЯ | 1966 |
|
SU224453A1 |
| Магниточувствительное устройство | 1977 |
|
SU664132A1 |
| ЕР 0681863 А, 15.11.1995 | |||
| US 5670369 A, 23.09.1997. | |||
Авторы
Даты
2002-08-27—Публикация
1999-04-09—Подача