Изобретение относится к медицинским токсикологическим исследованиям, в частности к санитарной токсикологии, и может быть использовано для количественного определения фенола в биологических жидкостях, в частности в крови.
Известен колориметрический метод определения фенола в плазме крови [1]. Согласно известному способу в колбе для перегонки вместимостью 75-100 см3 смешивают 1 см3 плазмы с 5 см3 0,22 н. Н2SO4 (кислота используется для разрушения комплексов фенола с белками). Смесь нагревают до температуры кипения и перегоняют водяным паром в градуированную емкость, собирая 4 см3 конденсата. К 3,5 см3 отогнанного раствора добавляют 0,2 см3 аммиачного буфера, 0,02 см3 7%-го раствора пирамидона в этаноле и 0,2 см3 25%-го водяного раствора феррицианата калия. Пробирку встряхивают и раствор фотометрируют через 15 мин. При 490 нм (зеленый фильтр). Концентрацию фенола в пробе определяют по калибровочному графику. Диапазон определяемых концентраций фенола составляет 0,15-24 мкг/см3.
Недостатком указанного известного способа является его недостаточная точность и чувствительность.
Также известен способ определения фенола в крови путем отгонки свободного фенола с водяным паром и его спектрофотометрического определения в дистилляте [2].
Сущность указанного известного метода заключается в следующем. В дистилляционную колбу помещают 10 см3 анализируемой крови с 5 см3 раствора лимоннокислого натрия. Подкисляют 10 см3 винной кислоты и добавляют 3 см3 раствора сульфата кадмия. Присоединяют колбу с пробкой к установке, закрывают среднюю трубку парообразователя, доводят воду в нем до сильного кипения и производят дистилляцию с водяным паром со скоростью 8-10 см3 дистиллята в минуту. Отбор дистиллята ведут в 100-миллилитровый мерный цилиндр. Собирают 2 порции дистиллята, каждая по 86 см3. Вторая порция должна содержать не более 25% фенола от количества его в первой.
В полученных дистиллятах могут присутствовать липоидные вещества, мешающие дальнейшему анализу из-за образующейся мути. Для их удаления каждую порцию дистиллята тщательно взбалтывают с 4 г окиси алюминия. К образовавшейся суспензии добавляют по 10 см3 боратного буфера, перемешивают, вносят по 4 см3 хромогенного реактива и после встряхивания оставляют на час. Через час центрифугируют дистиллят, а затем фотометрируют относительно воды в области 620 нм.
Обнаруживаемая концентрация фенола в крови указанным способом составляет 3,5 мкг/см3, что является низким показателем чувствительности.
Наиболее близким к предлагаемому техническому решению является газохроматографический способ количественного определения фенола в сыворотке крови [3]. Известный способ по очистке сыворотки включает перегонку, экстракцию фенолов из дистиллятов хлороформом и последующий газохроматографический анализ концентрированных растворов фенола в хлороформе.
Газохроматографический анализ по указанному известному способу проводят на хроматографе "Цвет-102", снабженном пламенно-ионизационным детектором, стеклянными колонками длиной 1 м. В качестве сорбента используют хроматон N-AW-DMCS с нанесенным на него динонилфталатом в жидкой фазе.
Точность указанного известного способа составляет ±8%. Диапазон измеряемых концентраций фенола в сыворотке крови составил 0,5-2,3 мкг/см3.
К недостаткам известного способа относится его недостаточная чувствительность.
Изобретением решается задача повышения чувствительности способа при одновременном сохранении высокой точности.
Для достижения названного технического результата в предлагаемом способе, включающем экстракцию фенола органическим экстрагентом и определение фенола в полученном экстракте газохроматографическим анализом, перед экстракцией в пробу крови добавляют последовательно карбонат натрия и йодистый метил, далее при экстракции в качестве органического экстрагента используют диэтиловый эфир при соотношении экстрагент : йодистый метил : карбонат натрия как (2,0-10,0) об. ч. : (0,25-0,3) об.ч. : (1,5-2,0) мас.ч. соответственно, а перед газохроматографическим анализом полученного экстракта последний нагревают до температуры +35÷40oС, выдерживают при этой температуре 9-12 с и центрифугируют.
Отличительными признаками заявляемого способа является применение экстракционного концентрирования деривата фенола - метилфенилового эфира из крови из щелочной среды с использованием дополнительных факторов (нагревание до температуры +35÷40oС, выдержка и центрифугирование), повышающих эффективность экстракционной системы, с последующим газохроматографическим анализом концентрата. При этом количественное определение фенола проводят методом внутреннего стандарта.
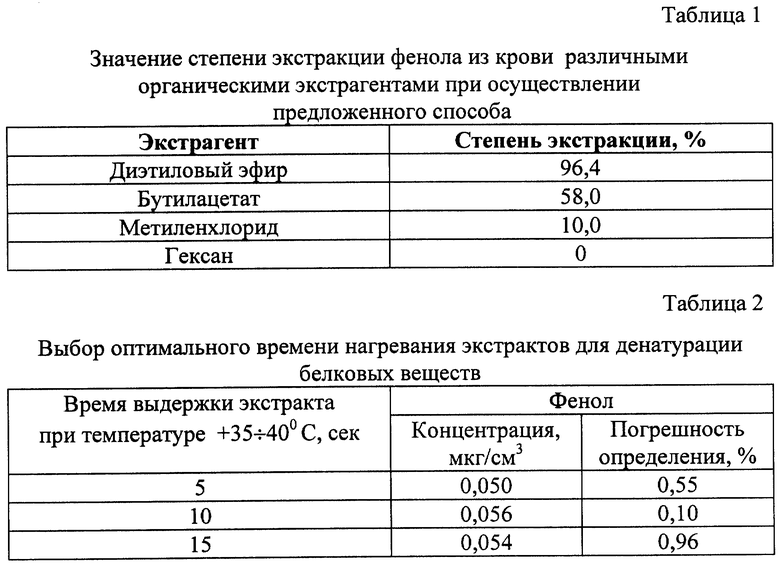
Экспериментальным путем было обнаружено, что применение в качестве экстрагента диэтилового эфира позволяет более полно извлечь фенол из пробы крови, что повышает чувствительность способа. Результаты этих исследований приведены в таблице 1.
Оптимальный эффект извлечения фенола из крови наблюдается при использовании в качестве экстрагента диэтилового эфира и нагревании экстракта при температуре +35÷40oС в течение 9-12 с.
Данные об этих исследованиях приведены в таблице 2.
Превращение фенола в простые и стойкие эфиры путем метилирования представляет собой один из простейших способов перевода с помощью йодистого метила в производные для газохроматографического анализа.
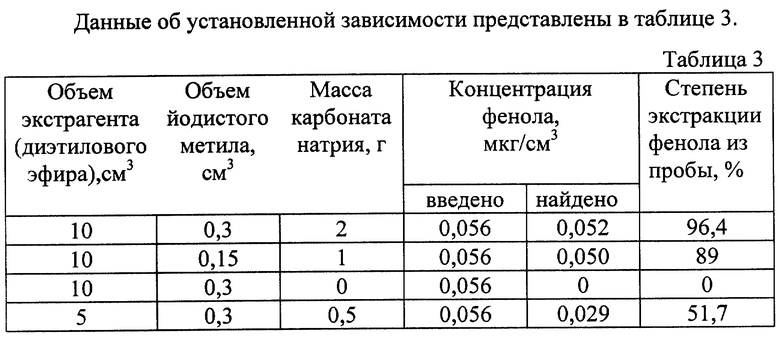
Изучена зависимость степени экстракции фенола из крови в предлагаемом способе от различных объемных соотношений экстрагента, метилирующего агента (йодистого метила) и количества карбоната натрия.
Данные об установленной зависимости представлены в таблице 3.
Экспериментальным путем было установлено, что в предлагаемом способе более полно извлекать фенол из крови (до 96%) возможно лишь при следующем соотношении используемых реагентов, а именно экстрагент : йодистый метил : карбонат натрия как (2,0-10,0) об.ч. : (0,25-0,3) об.ч. : (1,5-2) мас.ч соответственно.
Предлагаемый способ осуществляется в следующей последовательности:
- берут пробу крови объемом 2 см3;
- доводят ее бидистиллированной водой до 50 см3;
- добавляют в пробу карбонат натрия;
- далее вводят йодистый метил и встряхивают для перевода фенола в метилфениловый эфир;
- осуществляют экстракцию диэтиловым эфиром при следующем соотношении реагентов: экстрагент (2,0-10,0 об.ч.) : йодистый метил (0,25-0,3 об.ч.) : карбонат натрия (1,5-2 мас.ч.);
- выделенный экстракт нагревают до температуры +35÷40oС;
- выдерживают при этой температуре в течение 9-12 с;
- затем экстракт центрифугируют со скоростью 7000 об/мин;
- проводят газохроматографический анализ и расчет количественного содержания фенола осуществляют по площадям пиков на гематограмме с использованием внутреннего стандарта.
Пример конкретного выполнения.
Анализируют пробы крови (контрольная группа детей) с различным содержанием в них фенола. Анализ проводят по следующей схеме: 2 см3 пробы крови, содержащей заданную концентрацию фенола, доводят до 50 см3 бидистиллированной водой, переносят в делительную воронку объемом 250 см3 и добавляют 2 г кристаллического карбоната натрия (для создания щелочной среды рН 8). Плавным покачиванием перемешивают содержимое воронки, затем вводят 0,3 см3 йодистого метила и перемешивают в течение 5 мин для перевода фенола в метилфениловый эфир. Продукт метилирования экстрагируют диэтиловым эфиром в течение 5 мин при следующих соотношениях: экстрагент (2,0-10,0), метилирующий агент (0,25-0,3), карбонат натрия (1,5-2 г). Для денатурации белковых веществ полученные экстракты нагревают при температуре +35÷40oС в течение 10 с, а затем центрифугируют при 7000 об/мин в течение 5 мин. Полученные экстракты хроматографируют 5 раз на хроматографе ЛХМ-8МД с детектором ионизации в пламени. Анализ осуществляют на стальной колонке длинной 3 м, диаметром 3 мм, заполненной хроматоном N-AW-DMCS с нанесенной неподвижной жидкой фазой 5% OV-1. Режим работы прибора: температура термостата колонок - 110oС, температура детектора - 170oС, испарителя - 170oС, скорость газа-носителя (гелий) - 33 см3/мин. Расчет количественного содержания фенола осуществляют по площадям пиков на гематограмме с использованием внутреннего стандарта в биопробах 1-5.
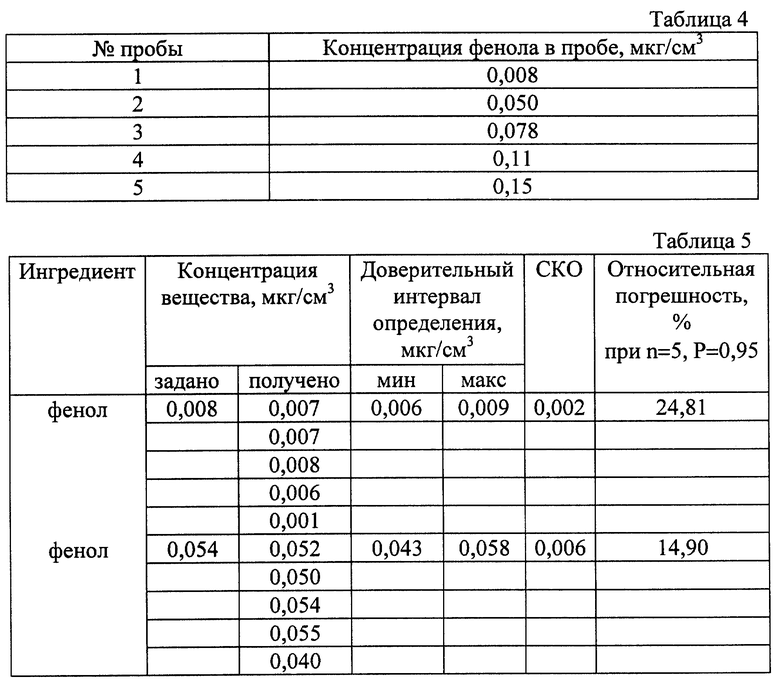
Полученные результаты приведены в таблице 4.
Чувствительность определения фенола в крови предложенным способом составила 0,008 мкг/см3. Возможно также определение фенола 0,00008 мкг в анализе объема пробы.
Погрешность определения по предложенному способу составляет 14,9-24,81%. Данные об этом приведены в таблице 5.
Таким образом, предлагаемым способом можно с высокой степенью точности и чувствительности определить фенол в крови. Применение предлагаемого способа позволяет повысить чувствительность определения по фенолу в 100 раз.
Источники информации
1. Захарченко В.Н., Погочанский В.А. Колориметрическое определение фенола в плазме крови. Ж. "Лабораторное дело", 9, 1983.
2. Гадаскина И.Д. и др. Превращение и определение промышленных органических ядов в организме. Л.: Медицина, 1971.
3. Кочетова Н.Н., Лурье Б.Л., Агнохов Х.Б. Некоторые аспекты лечения гемосорбцией первичного билиарного цирроза (удаление фенолов). Труды института им. М.Ф.Владимирского, XXXI, Москва, 1981 (прототип).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ФЕНОЛА В МОЧЕ | 2001 |
|
RU2200958C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ХЛОРОФОРМА И ТЕТРАХЛОРМЕТАНА В КРОВИ | 2000 |
|
RU2163379C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ 2-ХЛОРФЕНОЛА В МОЧЕ | 2001 |
|
RU2190854C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ХЛОРОФОРМА И 1,2-ДИХЛОРЭТАНА В МОЧЕ | 1999 |
|
RU2151395C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ФОРМАЛЬДЕГИДА, АЦЕТАЛЬДЕГИДА, ПРОПИОНОВОГО И МАСЛЯНОГО АЛЬДЕГИДОВ В МОЧЕ МЕТОДОМ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ | 2001 |
|
RU2189596C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ХЛОРБЕНЗОЛА В МОЧЕ | 2002 |
|
RU2226692C1 |
| Способ определения массовых концентраций фенола и пирокатехина в крови методом высокоэффективной жидкостной хроматографии | 2022 |
|
RU2786509C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ ТЯЖЕЛЫХ МЕТАЛЛОВ В ЦЕЛЬНОЙ КРОВИ | 2001 |
|
RU2184973C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ФТАЛЕВОЙ КИСЛОТЫ В СЫВОРОТКЕ КРОВИ | 2006 |
|
RU2324185C1 |
| СПОСОБ ОЦЕНКИ ВЛИЯНИЯ ЭКОЛОГИЧЕСКОЙ ОБСТАНОВКИ НА СОСТОЯНИЕ ИММУННОГО СТАТУСА НАСЕЛЕНИЯ | 2000 |
|
RU2180116C1 |
Использование: изобретение относится к области медицинских, токсикологических исследований, в частности к санитарной токсикологии. Сущность: согласно предлагаемому способу в пробу крови добавляют последовательно карбонат натрия и йодистый метил, далее производят экстракцию диэтиловым эфиром при соотношении экстрагент : йодистый метил : карбонат натрия как (2,0-10,0) об.ч. : (0,25-0,3) об.ч. : (1,5-2,0) мас.ч. соответственно, затем полученный экстракт нагревают до температуры 35-40oС, выдерживают при этой температуре 9-12 с, центрифугируют и осуществляют определение фенола газохроматографическим методом. Технический результат: повышение чувствительности при сохранении высокой точности определения. 5 табл.
Способ количественного определения фенола в крови, включающий экстракцию фенола органическим экстрагентом и определение фенола в полученном экстракте газохроматографическим анализом, отличающийся тем, что перед экстракцией в пробу крови добавляют последовательно карбонат натрия и йодистый метил, далее при экстракции в качестве органического экстрагента используют диэтиловый эфир при соотношении экстрагент : йодистый метил : карбонат натрия как (2,0-10,0) об.ч. : (0,25-0,3) об.ч. : (1,5-2,0) мас.ч. соответственно, а перед газохроматографическим анализом полученного экстракта последний нагревают до температуры +35-40oС, выдерживают при этой температуре 9-12 с и центрифугируют.
| КОЧЕТОВА Н.Н., ЛУРЬЕ Б.Л., АГНОХОВ Х.Б | |||
| Некоторые аспекты лечения гемосорбцией первичного билиарного цирроза (удаление фенолов) | |||
| Труды института им | |||
| М.Ф | |||
| Владимирского, XXXI, М., 1981 | |||
| СПОСОБ ОПРЕДЕЛЕНИЯ ФЕНОЛОВ | 1991 |
|
RU2030743C1 |
| RU 94034405 А1, 27.06.1996 | |||
| RU 94012872 А1, 27.01.1996. | |||
Авторы
Даты
2002-08-27—Публикация
2001-10-04—Подача