Изобретение относится к области аналитической химии и может быть использовано в санитарно-гигиенических, экологических, лечебных и научных организациях, осуществляющих деятельность в области профпатологии и экологии человека.
Актуальность определения фенола и его первичного метаболита пирокатехина в биологических средах связана с профессиональной деятельностью работников предприятий органического синтеза, производства бисфенолов, красителей, лака, синтетических смол, пластификаторов, стабилизаторов, пестицидов и других продуктов промышленного и бытового назначения, условия труда которых характеризуются воздействием фенола и пирокатехина на состояние здоровья.
Фенол является промежуточным продуктом обмена белков и ароматических аминокислот в организме человека. Являясь естественным продуктом метаболизма фенол в микроколичествах циркулирует в крови и удаляется в виде конъюгатов с мочой.
Пирокатехин является первичным метаболитом фенола. Экзогенное поступление фенола в организм человека происходит через вдыхание загрязненного воздуха, при контакте с кожей.
Для оценки риска воздействия производственных факторов среды на состояние здоровья работников актуальным является разработка и совершенствование методического обеспечения по определению массовых концентраций фенола и пирокатехина в крови на уровне фоновых значений и выше с использованием высокочувствительного и селективного метода высокоэффективной жидкостной хроматографии.
Из уровня техники известен ряд способов количественного определения фенола в крови методом газовой хроматографии:
- (Метод 1) в плазме крови с использованием химической дериватизации и анализе методом газовой хроматографии на капиллярных колонках в сочетании с масс-спектрометрией. Пробу крови центрифугировали для отделения плазмы. К аликвоте плазмы объемом 500 мкл добавляли 500 мкл дистиллированной воды, содержащей 50 мкл бензола и 5 мкл п-крезола в качестве внутреннего стандарта. В смесь добавляли 3 мл изооктана и диэтилового эфира (80/20 по объему) и перемешивали содержимое в течение 1 ч в орбитальном шейкере. Отбирали 2 мл экстракта и проводили дериватизацию фенола с целью повышения летучести производного фенола. К экстракту добавляли 100 мкл триэтиламина в бензоле с концентрацией 1 моль/л в качестве катализатора процедуры дериватизации, 20 мкл гептафтормасляного ангидрида (дериватизирующий агент), перемешивали и инкубировали при комнатной температуре в течение 30 мин. Смесь промывали 2 мл 1М раствора фосфатного буфера (рН 6,0) и удаляли остаток воды безводным сульфатом натрия. После проведения реакции дериватизации 500 мкл экстракта переносили в виалы для анализа. Температура инжектора и термостата колонок 250°С, детектора 300°С. Анализировали 2 мкл экстракта трижды, после каждого анализа промывали колонку ацетонитрилом. Идентификацию фенола проводили по фрагменту гептафтормасляного производного с массовым зарядом 69 m/z. Количественное определение проводили по молекулярному иону дериватизированного фенола с массовым зарядом 290 m/z. Чувствительность определения 0,4 мг/дм3 (Harrison L., Morrison J., Fennessey P. Microtechnique for quantifying phenol in plasma by gas chromatography-mass spectrometry // Clin. Chem. - 1991. - Vol. 37. - P. 1739-1742.).
- (Метод 2) известен способ определения в сыворотке крови свободного фенола и о,м,п - крезола методом газовой хроматографии с детектированием на пламенно-ионизационном детекторе. Согласно способу извлечение фенола и крезолов из сыворотки крови проводили перегонкой с водяным паром и последующей экстракцией хлороформом. Разделение аналитов проводилось на стеклянной набивной колонке (2 м х 4 мм), заполненной сорбентом Chromaton-N-AW- DMCS (0,20-0,25) мм с нанесенной на него неподвижной жидкой фазой динонилфталатом (10%) и Chromaton-N-AW-DMCS (0,16-0,20) мм с нанесенным на него OV-17 (фенил (50%) метил силиконовое масло). В качестве газа-носителя использовали особо чистый азот со скоростью потока 50 мл/мин. Температура колонки 140°С, температура испарителя 180°С. Анализ проб проводили в изотермическом режиме. Объем вводимой пробы составлял от 2 до 5 мкл. Идентификацию фенола проводили по относительному времени удерживания. Количественное определение фенола проводили методом внутреннего стандарта, в качестве которого использовали о-крезол. Чувствительность определения 2,0 мг/дм3 (Кочетова М.М., Лурье Б.Л. Определение свободного фенола в сыворотке крови методом газожидкостной хроматографии при гемосорбции // Вопросы медицинской химию. - 1985. - Т. 31, №1. - С. 72-74).
- (Метод 3) известен способ определения фенола и крезола в крови методом газовой хроматографии с масс-спектрометрическим детектированием. Извлечение фенола и крезола проводили с предварительной депротеинизацией путем добавления к 1 мл крови 2 мл ацетонитрила, полученную суспензию перемешивали и центрифугировали при 1000 об./мин 10 минут. Органическую фазу выпаривали под струей азота при температуре 40°С. К остатку добавляли внутренний стандарт (анилин) и растворяли в 1 мл дихлорметана. Пробу объемом 1 мкл анализировали на газовом хроматографе. Нижний предел количественного определения составил 0,069 мг/дм3 для о-крезола и 0,26 мг/дм3 для фенола (Boatto G., Nieddu М., Carta A., A. Pau A., Lorenzoni S., Manconi P., Serra D. Determination of phenol and o-cresol by GC/MS in a fatal poisoning case // J. Forensic Science International. - 2004. - Vol. 139. - P. 191-194.).
- (Метод 4) Известен способ определения в крови свободного фенола методом газовой хроматографии с пламенно-ионизационным детектором. Определение основано на предварительном переводе фенола в метилфениловый эфир при взаимодействии с йодистым метилом в щелочной среде, извлечении продукта дериватизации из крови экстракцией диэтиловым эфиром и последующем газохроматографическом анализе экстракта. Градуировочную характеристику устанавливают методом внутреннего стандарта (нафталина) на градуировочных смесях фенола на основе цельной крови. Определению не мешают ксиленолы и о-,м-,п-крезолы. Чувствительность определения массовой концентрации фенола в крови 0,04 мг/дм3 с погрешностью не более 25% (Определение вредных веществ в биологических средах: Сборник методических указаний. / МУК 4.1.2108-06 «Определение массовой концентрации фенола в биосредах (кровь) газохроматографическим методом». - М.: Федеральный центр гигиены и эпидемиологии Роспотребнадзора, 2008. - 183 с.).
Недостатками указанных известных методов являются:
- использование в пробоподготовке высокотоксичных органических растворителей бензола, диэтилового эфира, хлороформа, дихлорметана. (методы 1-4),
- низкая чувствительность определения (методы 1-4),
- невозможность применения известного способа для анализа именно смеси фенола и пирокатехина в пробах крови при их совместном присутствии (методы 1-4),
- сложная пробоподготовка (дериватизация, перегонка с водяным паром) (методы 1, 2, 4).
Из патента РФ №2188416 известен способ количественного определения фенола в крови, согласно которому в пробу крови добавляют последовательно карбонат натрия и йодистый метил, далее производят экстракцию диэтиловым эфиром при соотношении экстрагент: йодистый метил: карбонат натрия как (2,0-10,0) об.ч. : (0,25-0,3) об.ч. : (1,5-2,0) мас.ч. соответственно, затем полученный экстракт нагревают до температуры 35-40°С, выдерживают при этой температуре 9-12 с, центрифугируют и осуществляют определение фенола газохроматографическим методом.
Однако, этот известный способ характеризуется сложной пробоподготовкой, включающей проведение реакции дериватизации, использованием высокотоксичных йодистого метила в реакции дериватизации (2 класс опасности, канцероген) и высоколетучего диэтилового эфира для экстракции, недостаточной чувствительностью определения фенола (0,008 мг/л), невозможностью определения в крови пирокатехина при совместном присутствии с фенолом.
Из патента РФ №2205398 известен способ определения гидрохинона или пирокатехина в водных растворах физико-химическим методом с предварительной стадией экстракционного концентрирования при рН 2-3 гидрофобными растворителями в присутствии органических оксидов. При этом в качестве гидрофобного растворителя применяют гексановый раствор триоктилфосфиноксида с концентрацией 0,5 моль/дм3 и раздельное определение гидрохинона и пирокатехина проводят в выделившейся органической фазе методом микроколоночной высокоэффективной жидкостной хроматографии.
Недостатком этого способа является то, что способ предназначен для определения гидрохинона и пирокатехина в сточной воде и не может быть использован для анализа фенола и пирокатехина в биологической матрице (крови).
Также известны способы определения содержания фенола и его производных в биологических средах (кровь, моча) методом высокоэффективной жидкостной хроматографии (ВЭЖХ):
- (Метод 5) определение фенола, п-крезола и 4-хлорфенола в плазме крови с использованием жидкостной мембранной экстракции и колоночной жидкостной хроматографии с амперометрическим биосенсором модифицированным ферментом тирозиназой в качестве блока селективного детектирования. Фенолы селективно экстрагируются в пористую мембрану из ПТФЭ (политетрафторэтилена), пропитанную органическим растворителем, не смешивающимся с водой, и далее в щелочную акцепторную фазу. Через ионообменный интерфейс аналиты переносятся в колонку жидкостного хроматографа с обращенной фазой, где они разделяются и обнаруживаются с помощью биосенсора. Никакой предварительной обработки образца перед экстракцией, за исключением центрифугирования, не производится. Разделение аналитов осуществляется методом обращенно-фазовой жидкостной хроматографии с использованием подвижной фазы, состоящей из метанола (градиент 0-10%) и 10 мМ натрий-фосфатного буфера (рН 6,0) в 0,9% растворе хлорида натрия при скорости потока 0,1 мл/мин на колонке длиной 20 мм и внутренним диаметром 1 мм. Нижний предел определения фенола, п-крезола и 4-хлорфенола в плазме крови составил 0,05 м/дм3 (Norberg J., Emnrus J., Jonsson J.A., Mathiasson L., Burestedt E., Knutsson M., Marko-Varga G. On-line supported liquid membrane-liquid chromatography with a phenol oxidase-based biosensor as a selective detection unit for the determination of phenols in blood plasma // Journal of Chromatography B. - 1997. - Vol. 701. - P. 39-46.).
- (Метод 6) известен способ определение фенола и п-крезола в моче методом высокоэффективной жидкостной хроматографии с флуориметрическим детектированием. Образцы мочи центрифугировали в течение 15 мин при 1000 g, чтобы обеспечить осаждение эритроцитов или других клеток крови, если они присутствовали в моче. Анализировали супернатант в количестве 20 мкл на жидкостном хроматографе с флуориметрическим детектором при длине волны возбуждения 284 нм и длине волны излучения 310 нм. Градуировка детектора проводилась на стандартных растворах фенолов в моче методом внешнего стандарта в диапазоне 0,002-0,040 и 0,00075-0,045 мг/дм3 для фенола и п-крезола соответственно. Разделение аналитов проводили на колонке длиной 250 мм и внутренним диаметром 4,6 мм с обращенной фазой С18 GL Sciences (Япония), размер частиц 5 мкм, с использованием подвижной фазы метанол-вода (65:35) со скоростью потока 1,4 мл/мин при температуре термостата колонки 35°С. Нижний предел определения 0,0005 мг/дм3 для фенола и 0,00025 мг/дм3 для п-крезола (Tekkeli S.E., Kiziltas M.V., Dincel D., Erkoc R., Topcu G. Simultaneous Determination of Phenol and p-Cresol in Human Urine by an HPLC Method // Acta Chromatographica, 2016. - 28(2): p. 255-262).
Недостатками указанных известных методов являются:
- низкая чувствительность (метод 5),
- применение токсичного растворителя метанола для приготовления подвижной фазы (метод 5),
- невозможность применения описанного способа пробоподготовки для анализа смеси фенола и пирокатехина в крови из-за загрязнения аналитической колонки компонентами матрицы (метод 6).
Также известен способ, описанный в работе Niwa Т. Phenol and p-cresol accumulated in uremic serum measured by HPLC with fluorescence detection // Clin. Chem. - 1993. - Vol. 39, No. 1. - P. 108-111. Согласно известному способу отбирают пробу венозной крови объемом не менее 1 см3 в чистую пробирку. Далее производят ее пробопод готовку путем переноса 1 см3 крови в центрифужную пробирку и центрифугирования со скоростью 1500 об/мин в течение 5 мин. Отбирают 0,1 мл сыворотки, 1 мкг добавляют внутреннего стандарта п-этилфенола и 10 мл дистиллированной воды. Пробу подкисляют 1 М раствором соляной кислоты до рН 1, добавляют 0,1 г NaCl и экстрагируют 0,3 мл этилацетата встряхиванием в течение 10 мин. Центрифугируют пробу со скоростью 1500 об/мин в течение 5 мин, отбирают экстракт (верхний слой этилацетата) для анализа методом ВЭЖХ. Далее производят введение подготовленной пробы в пробоотборное устройство жидкостного хроматографа, проводят анализ экстракта в количестве 10 мм3 на обращено-фазной колонке Finepak Sil C18S длиной 150 мм и внутренним диаметром 4,6 мм. Подвижная фаза: смесь дистиллированной воды и ацетонитрила в объемном соотношении 70:30, скорость движения подвижной фазы 1 мл/мин, длина волны возбуждения флуориметрического детектора 260 нм, длина волны эмиссии 305 нм, температура термостата колонки соответствовала температуре окружающей среды (воздух лаборатории), время удерживания фенола 6,2 мин. Определяют содержание фенола с использованием ранее построенного градуировочного графика. Диапазон измеряемых концентраций фенола в крови 0,1-10 мг/дм3, погрешность определения 10%.
Недостатки известного способа: невозможность совместного определения фенола и пирокатехина при использовании в качестве подвижной фазы смеси ацетонитрила и дистиллированной воды в соотношении 70:30 без подкисления дистиллированной воды уксусной кислотой до получения концентрации 0,1% раствора, т.к. в данных условиях пирокатехин не удерживается на обращено-фазной колонке Finepak Sil C18S, что затрудняет проведение количественного анализа пирокатехина.
Кроме того, данный метод не позволяет определять содержание фенола и пирокатехина в крови на уровне концентраций ниже 0,1 мг/дм3, реально присутствующих в крови.
При этом из уровня техники не были выявлены известные способы количественного определения фенола и пирокатехина в цельной крови, поэтому сделать выбор ближайшего аналога к заявляемому изобретению не представляется возможным.
Технический результат, достигаемый предлагаемым способом, заключается в возможности определения фенола и пирокатехина из одной пробы крови при их совместном присутствии, при одновременном обеспечении высокой чувствительности за счет увеличения степени экстракции фенола и пирокатехина до 87-100% и достижения селективности определения содержания фенола и пирокатехина в крови на уровне от 0,004 мг/дм3.
Кроме того применение предлагаемого способа упрощает процедуру построения градуировочной кривой и расчета концентраций аналитов в крови.
Указанный технический результат достигается предлагаемым способом определения массовых концентраций фенола и пирокатехина в крови методом высокоэффективной жидкостной хроматографии, согласно которому осуществляют отбор пробы крови, проводят ее подкисление 0,1%-ным раствором ортофосфорной кислотой в объемном соотношении проба : раствор кислоты как 20:1, выполняют извлечения аналитов жидкостной экстракцией, для чего добавляют к подкисленной пробе ацетонитрил в объемном соотношении проба: ацетонитрил как 1:1 соответственно, смесь центрифугируют 10 мин со скоростью 5000 об/мин, производят отбор верхнего слоя экстракта, добавляют в него 0,1 г смеси сорбента марки С18 и соли сульфата магния в массовом соотношении 1:6 соответственно, для очистки экстракта, перемешивают 1 мин и вновь центрифугируют 10 мин со скоростью 5000 об/мин, очищенный экстракт фильтруют и вводят в хроматограф 10 мм3 отфильтрованного экстракта, проводят измерение и определяют концентрацию фенола и пирокатехина с использованием градуировочного графика.
Достижение указанного технического результата обеспечивается за счет следующего.
Благодаря тому, что пробу крови подкисляют ортофосфорной кислотой, обеспечивается повышение эффективности извлечения фенола и пирокатехина из крови, например, по сравнению с применением для подкисления раствора соляной кислоты.
Применение при экстракции в качестве экстрагента ацетонитрила, позволяет получить чистый экстракт, в то время как при использовании, например, этилацетата наблюдается разрушение клеток крови, выделенный экстракт мутный и окрашен в красный цвет. И даже при последующей очистке экстракта сорбентом он остается мутным и слабоокрашенным, что отрицательно влияет на точность измерения.
При выполнении центрифугирования со скоростью 5000 об./мин в течение 10 минут достигается более полное выделение ацетонитрильного слоя.
Проведение очистки ацетонитрильного экстракта от компонентов матрицы методом твердофазной экстракции путем добавления к экстракту смеси насыпного сорбента С18 и сульфата магния в массовом соотношении 1:6 соответственно, позволяет получать чистый, прозрачный экстракт, что положительно влияет на достоверность определения. Например, указанную смесь можно использовать из набора vetexQ Тох - набор для анализа наркотических и лекарственных веществ в тканях и органах, производство компании «Интерлаб». Но можно приготовить смесь и из указанных компонентов.
Благодаря тому, что подготовленную пробу фильтруют через мембранный фильтр с размером пор не более 0,45 мкм, обеспечивается дополнительная очистка анализируемой пробы.
При лабораторном исследовании хроматографическое разделение фенола и пирокатехина выполняли на обращенно-фазной колонке Eclipse XDB С18 длиной 150 мм и внутренним диаметром 4,6 мм зернением 5 мкм. Элюирование проводить смесью ацетонитрила и 0,1% водного раствора уксусной кислоты в соотношении 40:60 (объемные доли). При этом скорость элюирования 0,8 мл/мин. Температура колонки 30°С, объем анализируемой пробы 10 мкл, длина волны возбуждения флуориметрического детектора 275 нм, длина волны эмиссии 315 нм. В данных условиях время выхода пирокатехина составляет 3,0 мин, фенола - 4,7 мин.
Предлагаемый способ был опробован в лабораторных условиях. Для его реализации были использованы следующие химреактивы, оборудование и расходные материалы: - государственный стандартный образец (ГСО) фенола в этаноле массовой концентрации 1 мг/см3 с чистотой реактива не менее 99,0%;
- аналитический стандарт пирокатехина, чистота реактива 99,9%;
- ацетонитрил для хроматографии, сорт «0», ТУ 2634-002-54260861-2013;
- кислота ортофосфорная, химически чистая, ГОСТ 6552-80;
- кислота уксусная, химически чистая, ледяная ГОСТ 61-75;
- дистиллированная вода, ГОСТ 58144-2018;
- смесь для твердофазной очистки экстракта, состоящая из 6 мас.ч магния сульфата и из 1 мас.ч сорбента С18);
- жидкостный хроматограф, оснащенный флуориметрическим детектором, насосом для смешивания двух растворителей;
- весы лабораторные электронные аналитические 2 класса точности, погрешность взвешивания ± 0,5 мг, ГОСТ Р 53228;
- центрифуга с охлаждением, обеспечивающая рабочую температуру 4°С, допустимая скорость центрифугирования не менее 4000 об/мин;
- Eclipse XDB С18 длиной 150 мм и внутренним диаметром 4,6 мм зернением 5 мкм;
- мембранные фильтры из политетрафторэтилена (ПТФЭ) с размером пор 0,45 мкм.
Приготовление растворов и подготовку проб к анализу проводят в условиях:
- температура воздуха (20±5)°С;
- атмосферное давление от 84,0 до 106,7 кПа (630-800 мм рт.ст.);
- влажность воздуха от 30 до 80%.
Приготовление растворов:
1. Подвижная фаза для элюирования
Состав подвижной фазы - смесь ацетонитрила и 0,1%-го водного раствора уксусной кислоты в соотношении 35:65 (объемные доли) задают на двух каналах насоса жидкостного хроматографа.
2. Исходный раствор пирокатехина с концентрацией 1 г/дм3
Взвешивают 0,1 г пирокатехина, переносят в мерную колбу вместимостью 100 см3, доводят дистиллированной водой до метки, закрывают пробкой и перемешивают. Массовая концентрация пирокатехина в исходном растворе составляет 1 г/дм3. Срок хранения раствора 3 дня.
3. Рабочий раствор фенола и пирокатехина в ацетонитриле с концентрацией 5 мг/дм3
В колбу на 100 см3 переносили с помощью дозатора 0,5 см3 исходного раствора пирокатехина с концентрацией 1 г/дм3, 0,5 см3 стандартного образца фенола в этаноле массовой концентрацией 5 мг/см3, доводили дистиллированной водой до метки и перемешивали. Используют свежеприготовленный раствор.
4. Приготовление 0,1%-го водного раствора уксусной кислоты
В мерную колбу вместимостью 500 см3, приливают 100 см3 дистиллированной воды и 0,5 см3 уксусной кислоты, перемешивают, доводят дистиллированной водой до метки, закрывают пробкой и перемешивают. Используют свежеприготовленный раствор.
5. Приготовление 0,1%-го водного раствора ортофосфорной кислоты
В мерную колбу вместимостью 50 см3, приливают 10 см3 дистиллированной воды и 0,05 см3 ортофосфорной кислоты, перемешивают, доводят дистиллированной водой до метки, закрывают пробкой и перемешивают. Используют свежеприготовленный раствор.
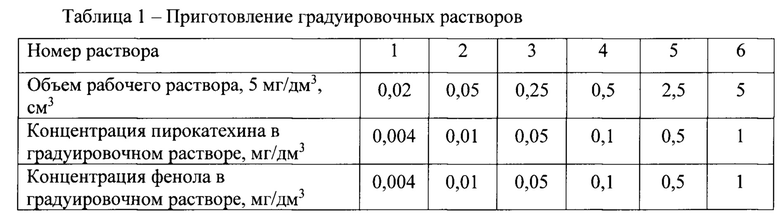
6. Построение градуировочной характеристики проводят в мерных колбах вместимостью 25 см3, в которые вносят рабочий раствор фенола и пирокатехина с концентрацией аналитов 5 мг/дм3 в количестве, указанном в таблице 1. Доводят содержимое колб до метки дистиллированной водой и перемешивают. Используют свежеприготовленные градуировочные растворы. Растворы фильтруют через тефлоновые фильтры с диаметром пор 0,45 мкм в стеклянную виалу и аликвотную часть (10 мм3) анализируют на жидкостном хроматографе в рабочем режиме работы хроматографа.
Рассчитывают градуировочный коэффициент по формуле:
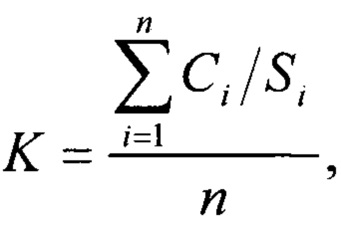 где
где
Ci - концентрация фенола и пирокатехина в градуировочном растворе i-й концентрации, мг/дм3;
Si - среднее значение измерений площади пика фенола и пирокатехина i-й концентрации, единицы оптической плотности (е.о.п.);
n - количество градуировочных смесей (n=5).
Градуировку проверяют 1 раз в квартал и при смене партии реактивов.
Предлагаемый способ осуществляют следующим образом.
Производят отбор проб крови в количестве 2 мл в химически чистые полипропиленовые пробирки с добавлением антикоагулянта (гепарин) или в вакуумные пробирки с внесенным антикоагулянтом.
Далее проводят подготовку проб крови способом жидкостной экстракции. В полипропиленовую пробирку вместимостью 15 см3 помещают 1 см3 цельной крови, вносят 50 мм3 0,1% раствора ортофосфорной кислоты, перемешивают 1 минуту, добавляют 1 см3 ацетонитрила, перемешивают 1 минуту и центрифугируют 10 мин со скоростью 5000 об/мин при температуре +4°С. Отбирают 1 см3 верхнего (ацетонитрильного) слоя, добавляют в него 0,1 г смеси магния сульфата и сорбента С18 для очистки экстракта, перемешивают 1 мин и центрифугируют 10 мин в тех же условиях. Очищенный экстракт фильтруют через фильтр ПТФЭ с размером пор 0,45 мкм. Вводят в хроматограф 10 мм3 экстракта и дважды анализируют в рабочем режиме хроматографа.
Концентрацию фенола и пирокатехина в крови определяют с использованием градуировочных графиков.
Результат определения представляется как среднее арифметическое двух измерений пробы.
Массовую концентрацию фенола и пирокатехина в крови рассчитывают по формуле:
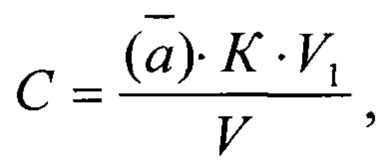 где
где
С - массовая концентрация определяемого соединения в крови, мг/дм3;
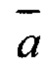 - среднее значение двух измерений площади хроматографического пика определяемого соединения в экстракте, у.е.;
- среднее значение двух измерений площади хроматографического пика определяемого соединения в экстракте, у.е.;
К - градуировочный коэффициент;
V1 - объем экстракта, см3;
V - объем крови, взятой на анализ, см3.
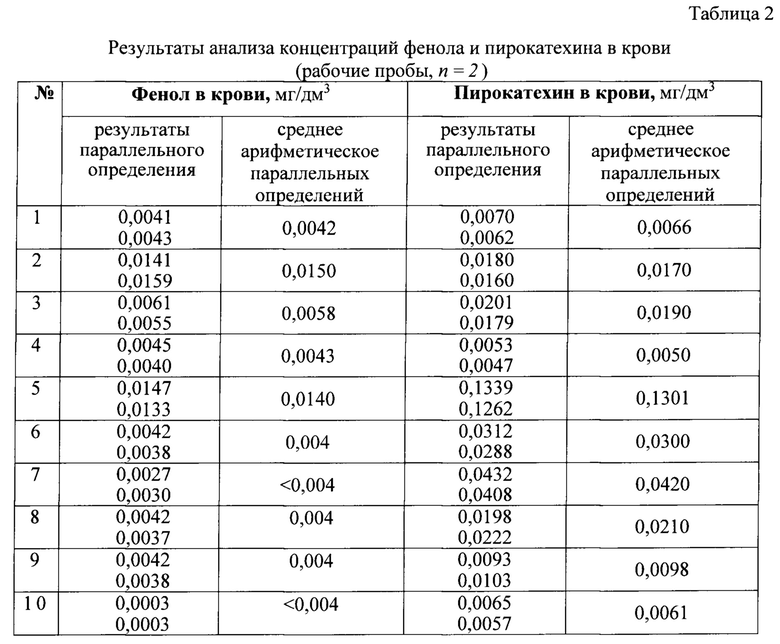
Полученные результаты измерения фенола и пирокатехина в крови (рабочие пробы) предлагаемым способом приведены в таблице 2.
Для расчета относительной погрешности предлагаемого способа использовали способ «введено-найдено».
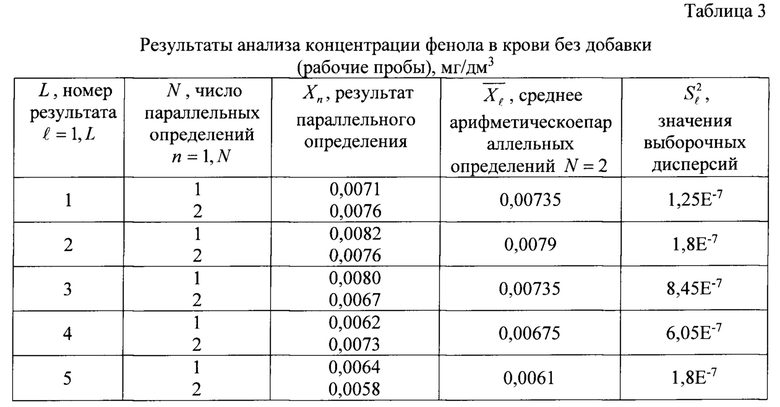
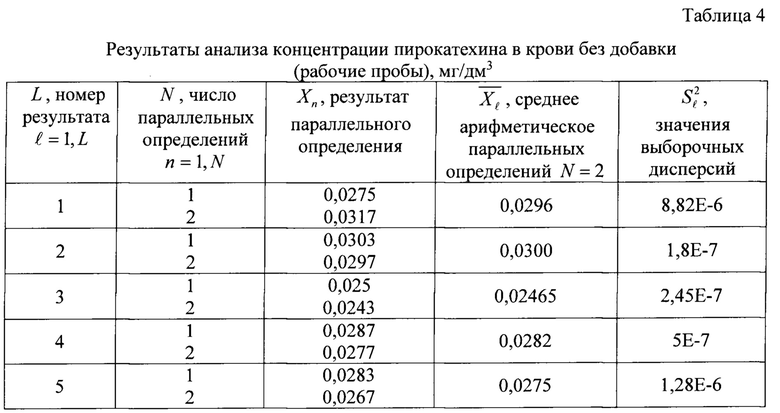
Для этого проводят анализ проб крови без добавления и с добавлением в них определенного количества анализируемого компонента (добавка составляет 50-150% от найденной концентрации фенола и пирокатехина в рабочей пробе) для выяснения правильности и точности заявляемого способа (относительная погрешность). Полученные результаты измерений фенола и пирокатехина в рабочей пробе крови без добавки приведены в таблицах 3 и 4 соответственно.
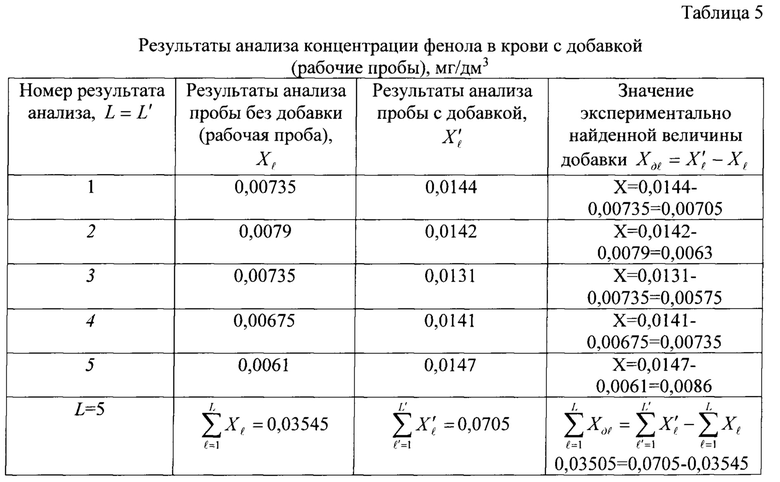
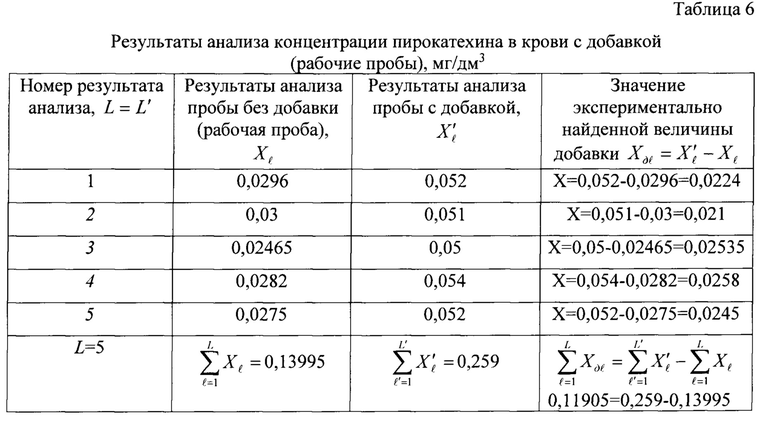
Результаты измерений фенола и пирокатехина в подготовленной пробе с добавкой аналитов в пробу крови приведены в таблицах 5 и 6 соответственно. В данном примере величина добавки фенола в пробу крови была равна 0,007 мг/дм3, добавка пирокатехина 0,026 мг/дм3. Среднее обнаруженное значение внесенной добавки фенола составило 0,0705 мг/дм3, добавки пирокатехина - 0,024 мг/дм3.
Данные, приведенные в таблицах 5 и 6, показывают, что предлагаемый способ характеризуется высокой точностью и правильностью анализа.
Также в ходе лабораторных испытаний предлагаемого способа были установлены следующие его характеристики: диапазоны измерений фенола и пирокатехина в крови, значения показателей точности, правильности, повторяемости и внутрилабораторной прецизионности. Полученные данные приведены в таблицах 7 и 8.
Приведенные в таблицах 7 и 8 данные показывают, что предлагаемый способ позволяет с высокой точностью определять в цельной крови фенол и пирокатехин в диапазоне концентраций 0,004-1,0 мг/дм3.
Чувствительность заявляемого способа позволяет обнаружить низкие концентрации, в том числе на уровне фоновых значений (как продуктов метаболизма), а также высокие концентрации, связанные с контаминацией биологических сред в условиях производства.


| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ ФУМАРОВОЙ И МАЛЕИНОВОЙ КИСЛОТ В ПЛАЗМЕ КРОВИ МЕТОДОМ ВЫСОКОЭФФЕКТИВНОЙ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ | 2018 |
|
RU2677341C1 |
| Способ количественного определения содержания 4-гидрокси-2,2,6,6-тетраметилпиперидин-1-оксила в воздухе рабочей зоны методом высокоэффективной жидкостной хроматографии | 2021 |
|
RU2756549C1 |
| Способ количественного определения N-нитрозаминов в детских кашах | 2015 |
|
RU2613303C1 |
| Способ определения концентрации стирола в атмосферном воздухе методом высокоэффективной жидкостной хроматографии | 2017 |
|
RU2648018C1 |
| Способ количественного определения гексахлорбензола в крови методом газохроматографического анализа | 2016 |
|
RU2613306C1 |
| Способ подготовки пробы мочи для определения монометилфталата, моноэтилфталата, монобутилфталата, монобензилфталата, моноэтилгексилфталата методом высокоэффективной жидкостной хроматографии/масс-спектрометрии | 2019 |
|
RU2687738C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ БЕНЗ(А)ПИРЕНА В КРОВИ МЕТОДОМ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ | 2014 |
|
RU2546530C1 |
| Способ количественного определения N-нитрозоаминов: N-диметилнитрозоамин, N-метилэтилнитрозоамин, N-диэтилнитрозоамин, N-дибутилнитрозоамин, N-дипропилнитрозоамин, N-пиперидиннитрозоамин, N-пирролидиннитрозоамин, N-морфолиннитрозоамин, N-дифенилнитрозоамин, в пробах копченых мясопродуктов методом хромато-масс-спектрометрии | 2017 |
|
RU2657822C1 |
| Способ количественного определения N-дифенилнитрозамина в мясных пробах пищевой продукции методом хромато-масс-спектрометрии | 2017 |
|
RU2626601C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ БЕНЗ(А)ПИРЕНА В МОЧЕ МЕТОДОМ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ | 2011 |
|
RU2466406C1 |
Изобретение относится к области аналитической химии. Способ определения массовых концентраций фенола и пирокатехина в крови методом высокоэффективной жидкостной хроматографии характеризуется тем, что осуществляют отбор пробы крови, проводят ее подкисление 0,1%-ным раствором ортофосфорной кислоты в объемном соотношении проба/раствор кислоты как 20:1, выполняют извлечения аналитов жидкостной экстракцией, для чего добавляют к подкисленной пробе ацетонитрил в объемном соотношении проба/цетонитрил как 1:1 соответственно, смесь центрифугируют 10 мин со скоростью 5000 об/мин, производят отбор верхнего слоя экстракта, добавляют в него 0,1 г смеси сорбента марки С18 и соли сульфата магния в массовом соотношении 1:6 соответственно, для очистки экстракта, перемешивают 1 мин и вновь центрифугируют 10 мин со скоростью 5000 об/мин, очищенный экстракт фильтруют и вводят в хроматограф 10 мм3 отфильтрованного экстракта, проводят измерение и определяют концентрацию фенола и пирокатехина с использованием градуировочного графика. Техническим результатом является возможность определения фенола и пирокатехина из одной пробы крови при их совместном присутствии, при обеспечении высокой чувствительности метода. 8 табл.
Способ определения массовых концентраций фенола и пирокатехина в крови методом высокоэффективной жидкостной хроматографии, характеризующийся тем, что осуществляют отбор пробы крови, проводят ее подкисление 0,1%-ным раствором ортофосфорной кислоты в объемном соотношении проба/раствор кислоты как 20:1, выполняют извлечения аналитов жидкостной экстракцией, для чего добавляют к подкисленной пробе ацетонитрил в объемном соотношении проба/ацетонитрил как 1:1 соответственно, смесь центрифугируют 10 мин со скоростью 5000 об/мин, производят отбор верхнего слоя экстракта, добавляют в него 0,1 г смеси сорбента марки С18 и соли сульфата магния в массовом соотношении 1:6 соответственно, для очистки экстракта, перемешивают 1 мин и вновь центрифугируют 10 мин со скоростью 5000 об/мин, очищенный экстракт фильтруют и вводят в хроматограф 10 мм3 отфильтрованного экстракта, проводят измерение и определяют концентрацию фенола и пирокатехина с использованием градуировочного графика.
| NIWA T | |||
| "PHENOL AND P-CRESOL ACCUMULATED IN UREMIC SERUM MEASURED BY HPLC WITH FLUORESCENCE DETECTION", CLINICAL CHEMISTRY, V | |||
| Машина для изготовления проволочных гвоздей | 1922 |
|
SU39A1 |
| Приспособление для останова мюля Dobson аnd Barlow при отработке съема | 1919 |
|
SU108A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ГИДРОХИНОНА И ПИРОКАТЕХИНА В ВОДНЫХ РАСТВОРАХ | 2001 |
|
RU2205398C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ФЕНОЛА В КРОВИ | 2001 |
|
RU2188416C1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
Авторы
Даты
2022-12-21—Публикация
2022-03-29—Подача